BAB 2
TINJAUAN PUSTAKA
1.5 Hepatitis C
Hepatitis C adalah penyakit hati yang disebabkan oleh virus hepatitis C
(HCV). Terdiri dari hepatitis C akut dan kronik, dari tingkat keparahan yang
ringan yang berlangsung beberapa minggu menjadi kronik dan menyebabkan
komplikasi yang serius (WHO, 2014).
Infeksi akut HCV adalah terdeteksinya anti-HCV dan HCV RNA yang
kurang dari 6 bulan pasca paparan HCV. Sebagian besar penderita akan
menyebabkan infeksi kronik, yaitu bila anti-HCV dan HCV RNA terdeteksi
didalam darah selama ≥ 6 bulan. Hepatitis C kronik dapat menyebabkan sirosis
hati dan kanker hati primer (hepatocellular carcinoma) (CDC, 2014).
Prevalensi hepatitis C di Indonesia berdasarkan data Riset Kesehatan
Dasar (Riskesdas) 2007 didapatkan anti-HCV positif sebesar 1,7% dari 12.715
laki-laki dan 2,4% dari 14.821 perempuan (Mihardja, 2012; PPHI, 2014).
Sebelum ditemukannya HCV, dunia medis mengenal 2 jenis virus
penyebab hepatitis, yaitu : virus hepatitis A (HAV) dan virus hepatitis B (HBV).
Ditemukan peradangan hati yang tidak disebabkan oleh kedua virus tersebut dan
tidak dikenal pada saat itu sehingga dinamakan hepatitis Non-A Non-B (NANB).
Hepatitis NANB tersebut, pada dekade tahun 1970-an dikenal sebagai kasus
hepatitis yang sebagian besar atau lebih dari 90% kejadian hepatitis paska
transfusi, yang sekarang disebut virus hepatitis C (HCV). Sejak ditemukannya
HCV pada tahun 1989, virus ini telah menjadi salah satu penyebab utama
penyakit hati kronik di seluruh dunia. (Gani, 2009; Arief, 2011)
Hanya 20-30% penderita hepatitis C akut yang sembuh setelah fase akut.
Sebagian besar (80%) akan menetap menjadi hepatitis C kronik, yang ditandai
dengan gejala klinis minimal atau ringan dan tidak spesifik seperti rasa lelah,
lemah, mual, nafsu makan turun, dan mialgia. (Arief, 2011; PPHI 2014).
HCV adalah virus RNA dari keluarga Flaviviridae. Memiliki partikel
Genom HCV terdiri dari protein struktural (C, E1 dan E2) dan protein
non-struktural (NS1, NS2, NS3, NS4A, NS4B, NS5A, dan NS5B) yang terletak di
dalam poliprotein 5’NTR dan 3’NTR. Protein non-struktural dan RNA virus
hepatitis C telah terbukti ditemukan pada hati pasien yang terinfeksi HCV sehinga
membuktikan bahwa hati adalah tempat replikasi virus HCV (Bartensclager dan
Lohmann, 2000; PPHI, 2014)
Pemeriksaan genotip dan subtipe HCV penting dilakukan untuk
epidemiologi, menentukan jenis dan durasi terapi, respons terapi, termasuk
memperkirakan risiko terjadinya resistensi terapi antiviral.
Ada 7 genotip virus hepatitis C dari nomor 1 sampai 7 dengan 67 subtipe,
akan tetapi belum ada kesepakatan secara internasional sehingga tetap
menggunakan pembagian 6 genotipe dan 50 subtipe.
Genotip 1a dan 1b paling sering dijumpai, meliputi hampir 60% infeksi
HCV, predominan di wilayah Eropa (genotip 1b), Amerika Utara (genotip 1a di
Amerika Serikat) dan Jepang. Genotip 2 ditemukan di gugusan wilayah
Mediterania, lebih jarang dijumpai dan umumnya berhubungan dengan faktor
risiko infeksi HCV dari transfusi darah. Genotip 3 banyak dijumpai di wilayah
Asia Tenggara. Genotip 3a mempunyai prevalensi yang tinggi di Eropa,
khususnya pada populasi orang yang menyuntikkan narkoba. Kelompok ini (saat
ini) mengalami peningkatan insidensi dan penyebarluasan infeksi dengan HCV
genotip 4. Genotip 4 banyak dijumpai di Timur Tengah, Mesir, Afrika Utara dan
Afrika Tengah.
Genotip 5 dan 6 jarang ditemukan di Eropa. Genotip 5 hanya dijumpai di
wilayah Afrika Selatan sedangkan genotip 6 tersebar merata di seluruh wilayah
Asia. Genotip 7 yang tidak diketahui, teridentifikasi pada pasien-pasien dari
Kanada dan Belgia, yang kemungkinan terjangkit dari wilayah Afrika Tengah.
(Sievert, et. al., 2011; EASL, 2014; PPHI, 2014).
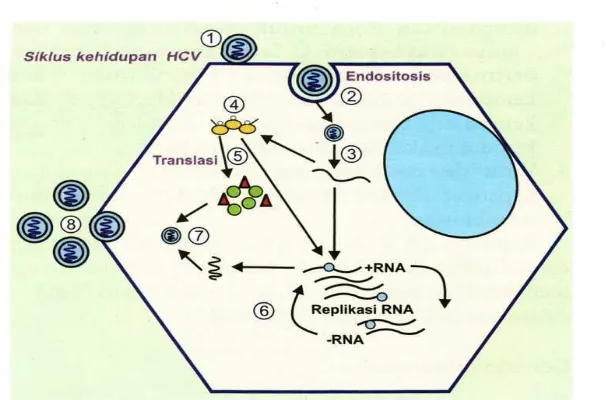
1.6 Patogenesis
Gambar 2.1. Patogenesis Hepatitis C
HCV yang masuk kedalam darah akan mencari hepatosit (HCV hanya bisa
berkembang biak di dalam sel hati) dan kemungkinan sel limfosit B. Virus masuk
kedalam hepatosit dengan mengikat suatu reseptor permukaan sel yang spesifik.
Reseptor ini belum teridentifikasi secara jelas, namun protein permukaan sel
CD81 adalah suatu HCV binding protein yang memainkan peranan khusus yang
dikenal sebagai protein E2 menempel pada reseptor site dibagian luar hepatosit.
Protein inti virus ini menembus dinding sel dimana selaput lemak bergabung
dengan dinding sel dan selanjutnya akan melingkupi dan menelan virus serta
membawanya kedalam hepatosit. Di dalam hepatosit, selaput virus (nukleokapsid)
melarut dalam sitoplasma dan keluarlah RNA virus (virus uncoating) yang
selanjutnya mengambil alih peran bagian dari ribosom hepatosit dalam membuat
bahan-bahan untuk proses reproduksi.
Virus menyebabkan sel hati memperlakukan RNA virus seperti miliknya
sendiri, lalu menutup fungsi normal hepatosit atau menginfeksi hepatosit yang
lain. Virus kemudian membajak mekanisme sintesis protein hepatosit dalam
memproduksi protein yang dibutuhkannya untuk berfungsi dan berkembang biak.
RNA virus dipergunakan sebagai cetakan (template) untuk produksi masal
poliprotein (proses translasi). Poliprotein dipecah menjadi unit-unit protein.
memulai sintesis kopi virus RNA asli. RNA virus mengopi dirinya sendiri dalam
jumlah besar (miliaran) untuk menghasilkan virus baru.
Proses ini berlangsung terus dan dapat membuat terjadinya mutasi genetik
yang menghasilkan RNA untuk strain baru virus dan subtipe virus hepatitis C.
Virus dewasa kemudian dikeluarkan dari dalam hepatosit menuju
pembuluh darah menembus membran sel. Dalam sehari replikasi HCV sangat
banyak. Seorang penderita dapat menghasilkan hingga 10 triliun virion per hari
(bahkan dalam fase infeksi kronik sekalipun) (Sulaiman, 2007).
Reaksi inflamasi yang dilibatkan melalui sitokin-sitokin pro-inflamasi
seperti TNF-α, TGF-β1, akan menyebabkan rekrutmen sel-sel inflamasi lainnya
dan menyebabkan aktivasi sel-sel stelata diruang disse hati. Sel-sel yang khas ini
sebelumnya dalam keadaan tenang (quiscent) kemudian berproliferasi dan
menjadi aktif menjadi sel-sel miofibroblas yang dapat menghasilkan matriks
kolagen sehingga terjadi fibrosis dan berperan aktif dalam menghasilkan
sitokin-sitokin pro-inflamasi. Mekanisme ini dapat timbul terus menerus karena reaksi
inflamasi yang terjadi tidak berhenti sehingga fibrosis semakin lama semakin
banyak dan sel-sel hati yang ada semakin sedikit. Proses ini dapat menimbulkan
kerusakan hati lanjut dan sirosis hati (Gani, 2009).
1.7 Hubungan faktor risiko terhadap terjadinya Hepatitis C
Virus hepatitis C merupakan blood-borne virus yang cara penularannya
terutama melalui paparan media darah atau cairan tubuh yang terkontaminasi
HCV. Angka infeksi hepatitis C meningkat pada beberapa populasi tertentu
seperti narapidana, pengguna narkoba suntik, para gelandangan, pasien
hemodialisis dan pasien yang mendapatkan transfusi produk darah rutin sebelum
tahun 1992 (Arief, 2011).
Sejak tahun 1989, semua darah telah dites untuk pemeriksaan anti-HCV,
sehingga suplai darah dianggap aman. Risiko infeksi melalui transfusi darah
sekarang hanya sekitar 0,001% per unit transfusi, atau sekitar 0,075% per
penerima (ALF, 2012). Di negara berkembang, transfusi darah atau produk darah
Safety diperkirakan 43% produk darah di negara berkembang tidak mendapatkan
skrining HCV yang adekuat (PPHI, 2014; WHO, 2014).
Faktor risiko lainnya adalah peralatan medis yang terpapar HCV seperti
jarum suntik pada pengguna narkoba suntikan (penasun). Secara global,
prevalensi infeksi HCV adalah 67% di antara para pengguna narkoba. Kalangan
tenaga medis juga perlu hati-hati agar tidak tertusuk jarum yang terpapar. Risiko
akibat tertusuk jarum berkisar 3-10%. Risiko infeksi HCV tergantung pada
frekuensi prosedur medis (jumlah suntikan per orang per tahun) dan tingkat
praktek pengendalian infeksi (WHO, 2014).
Infeksi HCV dapat menyebar melalui kontak seksual, meskipun risikonya
diyakini rendah. Risiko meningkat bagi mereka yang memiliki banyak pasangan
seks, memiliki penyakit menular seksual, terlibat dalam seks yang bebas, dan
laki-laki yang terinfeksi HIV yang berhubungan seks dengan laki-laki-laki-laki (LSL) maupun
orang lain yang terinfeksi HIV. Wabah HCV telah dilaporkan pada LSL penderita
HIV di Amerika Utara, Eropa dan Asia. Bukti transmisi diyakini disebabkan oleh
hasil dari pajanan terhadap darah selama kontak seksual. Pada mereka yang
terinfeksi HIV, infeksi HCV akut lebih mungkin untuk menjadi kronik (CDC,
2014; WHO, 2014).
Penularan vertikal HCV dapat terjadi pada proses kelahiran, baik
pervaginam maupun operasi. Transmisi perinatal dari ibu yang tertular hepatitis C
ke bayi mempunyai prevalensi sekitar 5%. Sekitar 4 dari setiap 100 bayi yang
lahir dari ibu dengan hepatitis C terinfeksi dengan virus. Namun, risiko menjadi
lebih besar jika ibu memiliki infeksi HIV dan hepatitis. Dihipotesiskan bahwa ibu
yang mengidap infeksi HIV mengalami penurunan daya imunitas sehingga
mengalami viral load dari HCV yang lebih tinggi menyebabkan mudahnya
penularan secara vertikal (Arief, 2011; CDC, 2014).
Salah satu faktor risiko yang dapat memperberat kerusakan hati adalah
kebiasaan mengkonsumsi alkohol. Kecanduan alkohol (Alkoholisme) adalah
masalah umum di Amerika dengan perkiraan 17-20 juta orang. Dalam hal ini pria
lebih sering mengkonsumsi daripada wanita. Konsumsi alkohol yang lama dan
(fatty liver), hepatitis alkoholik (peradangan pada hati) dan sirosis (jaringan parut
permanen hati). (ACG, 2014).
Pembuatan tato dan body piercing (tindik) juga dapat menjadi metode
transmisi HCV meskipun dengan angka kejadian yang lebih rendah, terutama di
kalangan pemuda, namun belum ditemukan cukup bukti dan ada temuan yang
bertentangan dalam literatur. Hal ini diakibatkan oleh penggunaan instrumen yang
tidak steril. Di Amerika Serikat, pemakaian tato dan tindik yang tidak steril sering
terjadi di penjara dan situasi informal lainnya. Studi menunjukkan tidak ada bukti
definitif untuk peningkatan risiko infeksi HCV bila tato dan tindikan dikerjakan
pada fasilitas tato/tindik komersial yang berlisensi profesional. (Tohme, 2012;
CDC, 2014; WHO, 2014).
Faktor-faktor lainnya juga berpengaruh seperti transplantasi organ dari
donor terinfeksi / pengidap HCV kronik, asupan alkohol, koinfeksi dengan virus
hepatitis B (HBV) atau virus Human Immunodeficiency Virus (HIV), jenis
kelamin laki-laki, dan usia tua saat terjadinya infeksi (Gani, 2009).
Jika seseorang pernah diuji positif terinfeksi HCV, direkomendasikan
untuk tidak pernah menyumbangkan darah, organ, atau air mani (hubungan
seksual) karena dapat menularkan kepada penerima atau pasangan seksual.
Seseorang juga bisa terinfeksi HCV melalui berbagi barang-barang perawatan
pribadi yang mungkin berkontak dengan darah, seperti pisau cukur atau sikat gigi,
tapi penularan ini kurang umum (CDC, 2014).
Hepatitis C tidak dapat ditularkan melalui ASI, makanan atau air atau
melalui kontak biasa seperti memeluk, mencium dan berbagi makanan atau
minuman dengan orang yang terinfeksi. (WHO, 2014).
1.8 Gejala Klinis 2.4.1 Infeksi HCV akut
Umumnya infeksi akut HCV tidak memberi gejala atau hanya bergejala
minimal. Masa inkubasi hepatitis C adalah 2 minggu sampai 6 bulan. Setelah
infeksi awal, sekitar 70-80% penderita HCV tidak menunjukkan gejala. Sebagian
demam, kelelahan, nafsu makan menurun, mual, muntah, sakit perut (biasanya
pada perut kanan atas), urin gelap, kotoran berwarna abu-abu, nyeri sendi dan
jaundice (WHO, 2014).
2.4.2 Infeksi HCV kronik
Infeksi akan menjadi kronik pada 70-90% kasus dan sering kali tidak
menimbulkan gejala walaupun proses kerusakan hati berjalan terus. Dalam
banyak kasus, tidak ditemukan gejala penyakit sampai timbulnya masalah pada
hati pasien. Beberapa penderita menunjukkan gejala-gejala ekstrahepatik
seolah-olah tidak berhubungan dengan penyakit hati. Gejala ekstrahepatik bisa meliputi
gejala hematologis, autoimun, mata, persendian, kulit, ginjal, paru, dan sistem
saraf. Sekitar 30% penderita menunjukkan kadar ALT serum yang normal
sedangkan yang lainnya meningkat sekitar 3 kali nilai normal. Kadar bilirubin dan
fosfatase alkali serum biasanya normal kecuali pada fase lanjut. HCV sering
terdeteksi selama tes darah rutin untuk mengukur fungsi hati dan tingkat enzim
hati. Hilangnya HCV setelah terjadinya hepatitis kronik sangat jarang terjadi.
Diperlukan waktu 20-30 tahun untuk terjadinya sirosis hati yang akan terjadi pada
15-20% pasien infeksi HCV. Dari setiap 100 orang yang terinfeksi,, sekitar 75-85
orang akan mengembangkan infeksi HCV, 60-70 orang mengembangkan penyakit
hati kronik, 5-20 orang akan berlanjut menjadi sirosis selama periode 20-30
tahun, 1-5 orang akan meninggal akibat sirosis atau kanker hati (Gani, 2009;
Arief, 2011; CDC, 2014).
2.5 Diagnosis
Anamnesis dan pemeriksaan fisik sangat penting dalam menegakkan
diagnosis dan menyingkirkan diagnosis banding. Pemeriksaan anti-HCV
merupakan pilihan utama alat diagnostik untuk mendeteksi infeksi hepatitis C.
Apabila pemeriksaan awal terdeteksi anti-HCV positif harus dilanjutkan
dengan pemeriksaan HCV RNA. Diagnosis hepatitis C kronik harus dibuktikan
dengan keberadaan anti-HCV dan HCV RNA positif > 6 bulan dan atau disertai
Infeksi HCV akut dapat dicurigai jika tanda-tanda klinis dan gejala yang
kompatibel dengan hepatitis C akut (alanine aminotransferase [ALT] >10x diatas
normal, adanya jaundice) tanpa adanya riwayat penyakit hati kronik atau
penyebab lain dari hepatitis akut, dan/atau jika dalam sumber sekarang
kemungkinan penularan dapat diidentifikasi. Dalam semua kasus, HCV RNA
dapat terdeteksi selama fase akut meskipun kebanyakan jarang terjadi (EASL,
2014).
2.5.1 Pemeriksaan laboratorium
Untuk pemeriksaan anti-HCV, tes enzyme immunoassay (EIA) merupakan
pemeriksaan yang mudah dikerjakan dan relatif tidak mahal, dan merupakan tes
skrining awal terbaik. Pemeriksaan serologi untuk mendeteksi anti-HCV dengan
menggunakan teknik enzyme-linked immunosorbent assay (ELISA) atau
chemiluminescent immunoassay (CLIA). Bila didapatkan hasil anti-HCV positif
maka dapat dinyatakan orang tersebut terinfeksi virus hepatitis C dan pemeriksaan
selanjutnya yaitu HCV RNA (EASL, 2014).
Anti-HCV mempunyai masa serokonversi sekitar 5-10 minggu pasca
paparan HCV, ada juga yang baru terdeteksi setelah 3 bulan sehingga
pemeriksaan anti-HCV saja dapat menimbulkan kesalahan diagnosis sebesar 30%
kasus hepatitis C akut. Selain itu pada pasien HIV, pasien hemodialisis, dan
pengguna obat imunosupresan, pemeriksaan anti HCV dapat menghasilkan
negatif palsu. Pada keadaan tersebut ataupun bila ada kecurigaan infeksi hepatitis
C maka diperlukan pemeriksaan lanjutan yaitu HCV RNA.
Pemeriksaan HCV RNA dengan real time-PCR dapat mendeteksi
keberadaan jumlah virus HCV sampai muatan virus minimal <50 IU/mL atau
<15 IU/mL. Pemeriksaan tersebut penting untuk menegakkan diagnosis serta
pemantauan terapi antivirus.
Pada infeksi akut serum ALT meninggi, dan jarang lebih dari 1000 IU/L,
alkaline phospatase (ALP) 2x batas atas nilai normal, kecuali pada kasus dengan
komplikasi kolestasis. Prothrombin time jarang melebihi 5 detik dari nilai normal.
peningkatan ringan serum ALT, (biasanya <dari 100 IU/L) dan pada sepertiga
kasus pemeriksaan tes faal hati bisa normal. (Ghany, 2009; Brook, 2010; PPHI,
2014).
Tabel 2.1. Interpretasi Hasil Anti-HCV dan HCV RNA Anti-HCV HCV RNA Interpretasi
Positif Positif Infeksi HCV akut atau kronik bergantung pada gejala klinis
Positif Negatif Resolusi HCV, Status infeksi tidak dapat ditentukan (mungkin dalam status intermittent viremia)
Negatif Positif Infeksi HCV akut awal; HCV kronik pada pasien dengan status imunosupresi; pemeriksaan HCV RNA positif palsu
Negatif Negatif Tidak adanya infeksi HCV Sumber : EASL, 2014
2.5.2 Biopsi hati dan fibroscan
Biopsi hati secara umum direkomendasikan untuk penilaian awal seorang
pasien dengan infeksi HCV kronik. Biopsi berguna untuk menentukan derajat
beratnya penyakit (tingkat fibrosis) dan menentukan derajat nekrosis dan
inflamasi. Pemeriksaan ini juga bermanfaat untuk menyingkirkan kemungkinan
adanya penyebab penyakit hati yang lain, seperti fitur alkoholik, non-alcoholic
steatohepatitis (NASH), hepatitis autoimun, penyakit hati drug-induced atau
overload besi (Sulaiman, 2007). Saat ini dengan fibroscan dapat dilakukan
pemeriksaan untuk menilai fibrosis hati sehingga dapat dipakai pada
pasien-pasien yang menolak untuk dilakukannya biopsi hati.
2.6 Penatalaksanaan
Tujuan pengobatan adalah untuk mengeliminasi atau eradikasi virus HCV
dan mencegah progresifitas penyakit menjadi sirosis maupun karsinoma
hepatoselular dan sebagai endpoint therapy adalah mencapai sustained virologic
response (SVR).
- Tatalaksana hepatitis C akut:
Dari saat identifikasi infeksi HCV akut, pasien harus dipantau tiap 4
minggu, sekitar 15-30% akan sembuh disertai pembersihan HCV tanpa
pengobatan. Mereka yang tidak sembuh harus segera mendapat pegylated
interferon selama 24 minggu. Oleh karena itu, tatalaksana dapat ditunda selama
12-16 minggu menunggu terjadinya resolusi spontan terutama pada yang
simptomatik. Pada pasien genotip IL28B non-CC pemberian antivirus dapat lebih
awal yaitu 12 minggu karena kemungkinan terjadinya resolusi spontan lebih
rendah. Pemberian monoterapi dengan Peg-IFN dapat diberikan pada tatalaksana
hepatitis C akut. Lama terapi hepatitis C akut pada genotip 1 dilanjutkan selama
24 minggu dan pada genotip 2 dan 3 selama 12 minggu. Ini akan mencegah
terjadinya infeksi HCV kronik pada kebanyakan pasien (Muslu, 2010; PPHI,
2014).
- Tatalaksana hepatitis C kronik :
Penatalaksanaan hepatitis C lebih tertuju pada hepatitis C kronik.
Umumnya pasien hepatitis C datang berobat sudah dalam fase kronik. Target
terapi antivirus adalah pencapaian SVR, yaitu muatan virus HCV RNA <50
IU/mL atau tetap tidak terdeteksi setelah 24 minggu setelah pemberian terapi
antivirus selesai. Untuk mengetahuinya, dilakukan pemeriksaan HCV RNA secara
berkala. Bila rapid virological response (RVR) tercapai, yaitu muatan virus HCV
RNA <50 IU/mL atau tidak terdeteksi setelah pemberian terapi antivirus selama 4
minggu, dapat diperkirakan 72,5-100% akan tercapai (Poordad, 2009).
Pilihan terapi standar untuk hepatitis C kronik adalah kombinasi antara
Pegylated Interferon-α (Peg-INFα) dan ribavirin (RBV). Pada genotip 1
memberikan respon 40-50% mencapai SVR, pada genotip 2 dan 3 sekitar 80%
mencapai SVR. Telah ditemukan agen direct acting antivirus (DAA) yaitu
boceprevir (BOC), telaprevir (TVR), simeprevir, sofosbuvir, dll. Di Indonesia
yang baru tersedia adalah boceprevir (PPHI, 2014).
- Pilihan terapi hepatitis C kronik genotip 1 & 4 Naive :
Pada genotip 1, dengan kombinasi dual therapy Peg-IFN dan RBV atau
kombinasi triple therapy dengan penambahan BOC. Pemberian triple therapy
pada pasien genotip 1 naive dapat dipertimbangkan pada pasien dengan IL28B
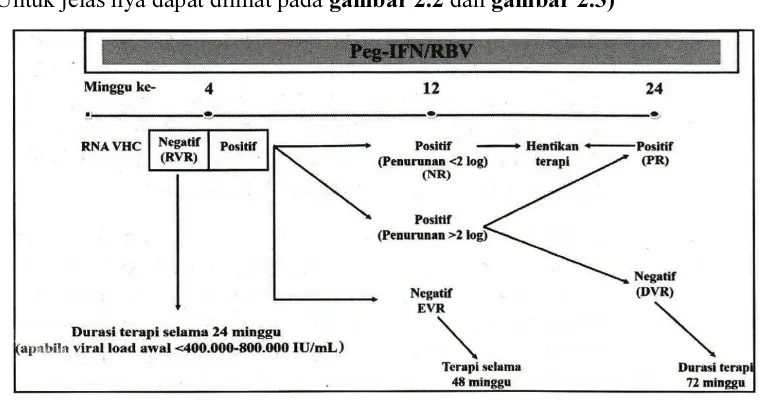
(Untuk jelas nya dapat dilihat pada gambar 2.2 dan gambar 2.3)
Gambar 2.2. Algoritme dual therapy pada genotip 1 dan 4 Ket: DVR (Delayed Virological Response); EVR (Early Virological Response);
NR (Null Response); PR (Partial Response) Sumber : PPHI, 2014
Gambar 2.3. Algoritme triple therapy dengan boceprevir menggunakan response guided therapy (RGT)
Ket: ER (Early Response); LR (Late Response), ***(Stop Terapi)
Dual therapy adalah standard of care (SOC) untuk hepatitis C naive
genotip 1 di Indonesia. Pemberian SOC pada naive genotip 1, bila tercapai RVR,
lama pengobatan dilanjutkan 48 minggu pada pasien dengan viral load tinggi dan
dipertimbangkan triple therapy, pengobatan diperpanjang 72 minggu atau
dihentikan dengan memperhatikan berbagai faktor (IL28B, ketaatan pasien,
obesitas, resistensi insulin, dll). Pada triple therapy, pemberian terapi harus
dihentikan bila didapatkan kondisi dimana muatan virus HCV RNA >100 IU/mL
pada terapi minggu ke-12 atau masih tetap terdeteksi pada minggu ke-24.
- Pilihan terapi hepatitis C genotip 1 yang sudah pernah mendapat terapi :
Dapat dikelompokkan dalam 3 kategori yaitu :
(a) Null responders : pasien dengan muatan virus tidak mencapai penurunan
minimal 2log IU/mL setelah pemberian antivirus 12 minggu
(b) Partial responders : berhasil mencapai penurunan HCV RNA minimal 2log
IU/mL setelah terapi 12 minggu, akan tetapi HCV RNA masih terdeteksi pada
minggu ke 24 terapi
(c) Relapser : berhasil mencapai muatan virus HCV RNA yang tidak terdeteksi
pada saat akhir terapi, tetapi virus kembali terdeteksi setelah terapi dihentikan.
Berdasarkan studi ini maka keputusan untuk memberikan terapi kembali
pada pasien yang pernah mendapatkan terapi sebelumnya sangat ditentukan oleh
respons pada terapi sebelumnya. Pasien dengan kriteria relapse atau partial
responders merupakan kandidat terbaik untuk kembali mendapatkan terapi
antivirus kombinasi triple therapy. Untuk kembali memberikan terapi pada
kelompok null responders bersifat individual mengingat hanya sedikit sekali yang
berhasil mencapai SVR (28-38%) dan cenderung menimbulkan resistensi
terhadap antivirus. Pemberian kembali antivirus pada pasien sirosis hati
kompensata sebaiknya dengan durasi 48 minggu.
- Pilihan terapi pada genotip 2, 3, 5 dan 6
Untuk kelompok ini, pilihan terapi adalah Peg-IFN/RBV. Kedua jenis
Peg-IFN dapat dijadikan pilihan terapi. Genotip 2 dan 3 dapat mencapai SVR
76% dan 82%. Algoritme dual therapy pada genotip 2, 3, 5, dan 6 dapat dilihat
Gambar 2.4. Algoritme dual therapy pada genotip 2, 3, 5, dan 6 Ket: * : Kurang efektif karena tingkat menjadi relapser tinggi, khususnya pada
genotip 3 dengan muatan virus HCV RNA tinggi.
--- : Bila ada faktor risiko dianjurkan untuk diterapi selama 48 minggu Sumber : PPHI, 2014
- Pilihan terapi pada sirosis hati :
Pada sirosis hati kompensata, terapi antivirus dapat diberi selama tidak ada
kontra indikasi. Ini bertujuan untuk mencapai SVR serta menurunkan insiden
terjadinya komplikasi sirosis hati. Pada sirosis hati dekompensata Child Pugh C,
CTP skor ≥10 atau MELD skor 18 adalah kontraindikasi pemberian antivirus, dan
sebaiknya segera dirujuk untuk transplantasi hati. Pemberian pada Child Pugh B
bersifat individual dengan mempertimbangkan risiko dan manfaatnya.
Efek samping penggunaan interferon adalah demam dan gejala-gejala
menyerupai flu (nyeri otot, malaise, tidak nafsu makan, dan sejenisnya), depresi
dan gangguan emosi, kerontokan rambut lebih dari normal, depresi sumsum
tulang, hiperurisemia, kadang-kadang timbul tiroiditis. Ribavirin dapat
menyebabkan penurunan Hb. Maka dari itu, pemantauan pasien mutlak perlu
dilakukan. Pada awal pemberian interferon dan ribavirin dilakukan pemantauan
klinis, laboratoris (Hb, lekosit, trombosit, asam urat, dan ALT) setiap 2 minggu
bila Hb 8 g/dL, lekosit 1500/uL atau kadar netrofil<500/uL, trombosit
<50.000/uL, depresi berat yang tidak teratasi dengan pengobatan anti-depresi,
atau timbul gejala-gejala tiroiditias yang tidak teratasi (Gani, 2009).
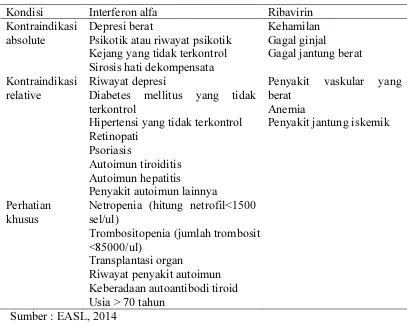
Kontraindikasi pemberian terapi interferon pada pasien hepatitis C dapat
dilihat di tabel 2.
Tabel 2.2 Kontraindikasi Peg-interferon-α dan Ribavirin
Kondisi Interferon alfa Ribavirin
Diabetes mellitus yang tidak terkontrol
Sekitar 75-85% penderita hepatitis C akut berkembang menjadi kronik.
Dari hepatitis C kronik 10-20% akan berlanjut menjadi sirosis hati dalam 15-20
tahun, dan setelah menjadi sirosis hati sebanyak 1-5% per tahun berkembang
2.7.1 Sirosis hati
Sirosis adalah suatu keadaan patologis yang menggambarkan stadium
akhir fibrosis hepatik yang berlangsung progresif yang ditandai dengan distorsi
dari arsitektur hepar dan pembentukan nodulus regeneratif (Gani, 2009).
Gejala-gejala sirosis hati dapat serius dan mengancam jiwa, tapi banyak dari mereka
berhasil ditangani. Keluhan dapat berupa berkurangnya nafsu makan, mual,
penurunan berat badan, nyeri perut, gatal-gatal, dan perut membesar. Gejala yang
dijumpai yaitu asites, edema pretibial, ginekomastia, hepatomegali, jaundice,
malnutrisi, adanya Spider Naevi, palmar eritem, dan haid yang tidak teratur
(ALF, 2012).
2.7.2 Karsinoma hati
Perkiraan insidens karsinoma hati sekitar 0,25-1,2 juta kasus baru setiap
tahunnya, sebagian besar berasal dari penderita dengan sirosis hati. Risiko
terjadinya karsinoma hati pada penderita sirosis akibat hepatitis C kronik
diperkirakan sekitar 1-4%. Perkembangan sejak terjadinya infeksi HCV sampai
timbulnya karsinoma hati berkisar antara 10-50 tahun. DiBisceglie
memperkirakan bahwa antara 1,9–6,7% penderita sirosis HCV berkembang
menjadi karsinoma setelah 10 tahun (Arief, 2011).
Manifestasi klinisnya bervariasi. Gejala yang paling sering dikeluhkan
adalah nyeri atau perasaan tak nyaman di kuadran kanan-atas; atau teraba
pembengkakan lokal dihepar. Terjadinya karsinoma hati perlu diduga bila tidak
terjadi perbaikan pada asites, perdarahan varises atau pre-koma setelah diberi
terapi yang adekuat; atau pasien penyakit hati kronik dengan HbsAg atau
anti-HCV positif yang mengalami perburukan kondisi secara mendadak. Juga harus
diwaspadai bila ada keluhan rasa penuh di abdomen disertai penurunan berat
2.8 Pencegahan
2.8.1 Pencegahan primer
Tidak ada vaksin untuk hepatitis C, oleh karena itu pencegahan infeksi
HCV ditujukan pada mengurangi risiko terpaparnya dengan HCV. Daftar berikut
memberikan contoh terbatas intervensi pencegahan primer yang
direkomendasikan oleh WHO:
• kebersihan tangan: persiapan bedah, mencuci tangan dan penggunaan sarung
tangan
• penanganan yang aman dan pembuangan benda tajam dan limbah
• pembersihan yang aman dari peralatan
• pengujian darah yang disumbangkan
• edukasi kepada masyarakat
• meningkatkan akses terhadap darah yang aman, dan
• pelatihan tenaga kesehatan.
2.8.2 Pencegahan sekunder
Bagi orang-orang yang terinfeksi dengan virus hepatitis C, WHO
merekomendasikan:
• pendidikan dan konseling tentang pilihan untuk perawatan dan pengobatan
• imunisasi dengan vaksin hepatitis A dan B untuk mencegah koinfeksi dari
virus hepatitis ini untuk melindungi hati mereka
• manajemen medis awal dan tepat termasuk terapi antiviral jika sesuai, dan
• pemantauan rutin untuk diagnosis awal penyakit hati kronik