i
EFEK ANTI INFLAMASI ASETIL EUGENOL SECARA ORAL PADA EDEMA KAKI MENCIT GALUR SWISS YANG DIINDUKSI FORMALIN
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Yosephine Dian Hendrawati NIM : 078114110
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
iii
iv
Karya ini kupersembahkan kepada: Tuhan Yesus Kristus dan Bunda Maria, sebagai
ungkapan rasa syukur dan pujianku, Untuk mama dan papa tersayang, sebagai ungkapan kasih dan sayangku, Untuk seseorang yang aku kasihi, teman-temanku,
Dan untuk Almamater kebanggaanku..
Learning is the beginning of wealth..
Learning is the beginning of health..
Learning is the beginning of spirituality..
Searching and learning is where the miracle
process all begins...
v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH
vi
PRAKATA
Puji syukur dan terima kasih kepada Allah Bapa di surga atas berkat, penyertaan, dan kasih-Nya yang begitu besar sehingga penulis dapat menyelesaikan skripsi yang berjudul “Efek Anti Inflamasi Asetil Eugenol Secara Oral pada Edema Kaki Mencit Galur Swiss yang Diinduksi Formalin” sebagai
salah satu syarat untuk mendapatkan gelar Sarjana Farmasi (S.Farm).
Dalam proses penelitian dan penyusunan skripsi ini, penulis telah mendapatkan banyak bantuan serta dukungan baik moril maupun materiil dari berbagai pihak, berupa bimbingan, dorongan, pengarahan, saran, serta sarana. Maka dari itu penulis bermaksud untuk mengucapkan banyak terima kasih kepada:
1. Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta, atas segala dukungan dalam penyelesaian skripsi ini.
2. Ipang Djunarko, M.Sc., Apt. selaku dosen pembimbing atas bimbingan, saran, pengarahan, serta dukungannya dalam penelitian dan penyusunan skripsi ini.
3. Drs. Mulyono, Apt. selaku dosen penguji yang telah memberikan pendampingan, dukungan, saran, serta kritik yang membangun.
4. Jeffry Julianus, M.Si. selaku dosen penguji yang telah memberikan pendampingan, dukungan, saran, serta kritik yang membangun.
vii
telah mendampingi, mendukung, serta memberi semangat kepada penulis selama melakukan studi di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
6. Papa Yohanes Cahyadi, Mama Cesilia Widhi Prih Yunianti, dan Albertus Gatot Hendrasto, untuk doa, kasih sayang, serta dukungan yang tiada henti untuk penulis.
7. Teman-teman seperjuangan dalam penelitian ini, Paulina Maya Octasari dan Devi Nathania, atas kebersamaan, kerja keras, dan keceriaan selama melakukan penelitian.
8. Florentinus Dika Octa Riswanto dan Albertus Eka Yudistira Sarwono, atas kerjasama yang baik dan menyenangkan dalam sintesis senyawa yang digunakan dalam penelitian ini.
9. Emmanuel Vialliresa Susilo, untuk dukungan, kasih, semangat, dan motivasi yang selalu diberikan kepada penulis.
10. Yuma Pinandita Lingga Dewi, Maria Elleonora Winengku Asih, Martha Hesty Susilowati, Paulus Febrianto Silor, Ridho Prayogie, serta seluruh teman-teman untuk dukungan dan perhatian yang diberikan kepada penulis. 11. Mas Kayatno dan Yohanes Ratijo, beserta segenap staf laboran atas
kerjasama, masukan, dan bantuan yang diberikan selama penelitian. 12. Semua orang atas dukungan yang tidak dapat disebutkan satu persatu.
viii
masukan serta kritik yang membangun. Harapan penulis, semoga karya ini dapat bermanfaat bagi masyarakat dan bagi perkembangan ilmu pengetahuan.
Yogyakarta, Januari 2011
ix
x
HALAMAN PERNYATAAN PERSETUJUAN PUBLIKASI ... v
xi
B. Anti Inflamasi... 8
C. Asetil Eugenol ... 8
D. Cataflam® D-50 (Kalium Diklofenak) ... 10
E. Virgin Coconut Oil ... 11
F. Metode Uji Efek Anti Inflamasi ... 12
G. Uji Statistik One Way ANOVA dan General Linear Model... 13
H. Landasan Teori ... 14
I. Hipotesis ... 15
BAB III METODE PENELITIAN... 16
A. Jenis dan Rancangan Penelitian ... 16
B. Variabel Penelitian ... 16
1. Variabel utama ... 16
2. Variabel pengacau ... 16
C. Definisi Operasional... 17
D. Bahan atau Materi Penelitian ... 17
E. Alat atau Instrumen Penelitian ... 18
F. Tata Cara Penelitian ... 19
1. Pembuatan larutan formalin 0,5%... 19
2. Penentuan volume injeksi subplantar dengan formalin 0,5% ... 19
3. Penentuan dosis kalium diklofenak ... 19
4. Penentuan waktu pemberian asetil eugenol ... 20
5. Pemilihan kontrol negatif ... 20
6. Pembuatan larutan stok asetil eugenol ... 20
7. Penentuan dosis asetil eugenol... 20
xii
9. Perlakuan pada hewan uji ... 21
10. Skema perlakuan pada hewan uji ... 22
11. Penentuan % penghambatan inflamasi ... 23
G. Analisis Hasil ... 24
BAB IV HASIL DAN PEMBAHASAN ... 25
A. Hasil Uji Efek Penghambatan Inflamasi dan Besar Penghambatan Inflamasi Asetil Eugenol secara Oral ... 25
B. Hasil Uji Hubungan Linearitas Antara Dosis Asetil Eugenol terhadap Penghambatan Inflamasi ... 36
BAB V KESIMPULAN DAN SARAN ... 40
A. Kesimpulan ... 40
B. Saran ... 40
DAFTAR PUSTAKA ... 41
LAMPIRAN ... 45
xiii
DAFTAR TABEL
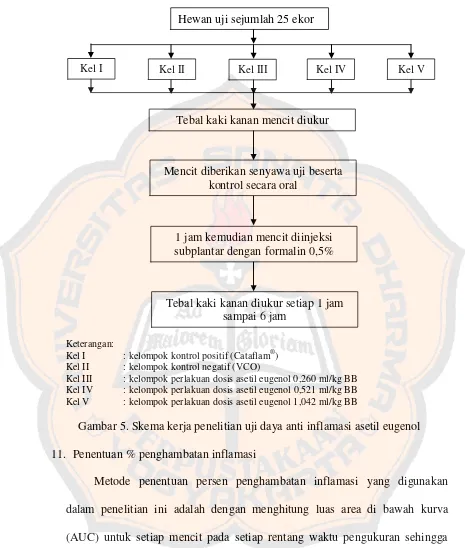
Tabel I. Komposisi asam lemak dalam Virgin Coconut Oil menurut
standar APCC ... 12 Tabel II. Hasil uji presisi terhadap jangka sorong merk Mitutoyo ... 26 Tabel III. Hasil rata-rata AUC, % penghambatan inflamasi dan hasil uji
Scheffe pada perlakuan asetil eugenol secara oral beserta
xiv
DAFTAR GAMBAR
Gambar 1. Jalur metabolisme asam arakidonat ... 7
Gambar 2. Struktur asetil eugenol ... 9
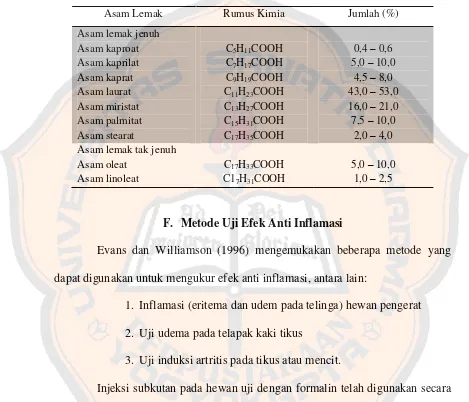
Gambar 3. Mekanisme reaksi sintesis asetil eugenol (Riswanto, 2011) ... 10
Gambar 4. Struktur kalium diklofenak ... 11
Gambar 5. Skema kerja penelitian uji daya anti inflamasi asetil eugenol ... 23
Gambar 6. Grafik tebal edema kaki mencit selama enam jam akibat pemberian asetil eugenol dengan tiga peringkat dosis beserta kontrol... 30
Gambar 7. Diagram batang AUC untuk masing-masing kelompok perlakuan beserta kontrol ... 31
Gambar 8. Reaksi asetilasi serin oleh asetil eugenol... 34
Gambar 9. Interaksi hidrofobik antara asam amino valin dengan asetil eugenol ... 34
Gambar 10. Kerangka struktur diaril atau aril/heteroaril-eter dan turunan tioeter ... 35
Gambar 11. Struktur asetil eugenol ... 35
Gambar 12. Pembentukan radikal alil dari asetil eugenol ... 36
xv
DAFTAR LAMPIRAN
Lampiran 1. Sertifikat kalibrasi vernier caliper merk Mitutoyo ... 45
Lampiran 2. Data beserta hasil uji presisi vernier caliper merk Mitutoyo ... 47
Lampiran 3. Hasil elusidasi struktur asetil eugenol (Riswanto, 2011) ... 48
Lampiran 4. Foto asetil eugenol hasil sintesis di Laboratorium Kimia Organik Universitas Sanata Dharma Yogyakarta ... 53
Lampiran 5. Foto dokumentasi injeksi subplantar pada hewan uji ... 54
Lampiran 6. Perhitungan dosis formalin 0,5% untuk injeksi subplantar ... 55
Lampiran 7. Perhitungan dosis Cataflam® D-50 sebagai kontrol positif ... 56
Lampiran 8. Perhitungan dosis Virgin Coconut Oil (VCO) sebagai kontrol negatif ... 57
Lampiran 9. Perhitungan dosis asetil eugenol ... 58
Lampiran 10. Tabel perhitungan AUC masing-masing kelompok perlakuan asetil eugenol beserta kontrol ... 60
Lampiran 11. Tabel perhitungan % penghambatan inflamasi kelompok perlakuan asetil eugenol secara oral beserta kontrol positif kalium diklofenak (Cataflam® D-50) ... 62
Lampiran 12. Hasil ANOVA pola satu arah dengan taraf kepercayaan 95% % penghambatan inflamasi dengan pemberian asetil eugenol dosis 0,260 ml/kg BB; 0,521 ml/kg BB ; dan 1,042 ml/kg BB beserta kontrol... 63 Lampiran 13. Hasil General Linear Model (GLM) repeated measures
xvi
0,521 ml/kg BB ; dan 1,042 ml/kg BB beserta kontrol ... 67 Lampiran 14. Tabel r ... 75 Lampiran 15. Tabel konversi perhitungan dosis Laurence and Bacharach,
xvii
INTISARI
Asetil eugenol telah terbukti secara in vitro dapat menghambat agregasi platelet diduga akibat terhambatnya metabolisme asam arakidonat (Srivastava dan Malholtra, 1991). Penelitian ini bertujuan untuk menguji efek anti inflamasi senyawa asetil eugenol yang diberikan secara oral terhadap edema kaki mencit galur Swiss yang diinduksi formalin.
Hewan uji dikelompokkan menjadi 5 kelompok, kelompok kontrol negatif menerima Virgin Coconut Oil (VCO), kelompok kontrol positif menerima kalium diklofenak, dan kelompok lainnya menerima asetil eugenol dengan dosis masing-masing 0,260; 0,521; dan 1,042 ml/kg BB. Asetil eugenol diadministrasikan dalam dosis tunggal 1 jam sebelum injeksi subplantar dengan larutan formalin 0,5% dan diukur tebal edema yang terjadi menggunakan jangka sorong setiap satu jam sampai enam jam. Analisis hasil dilakukan dengan menghitung AUC total setiap mencit selama rentang waktu pengukuran untuk menghitung persen penghambatan inflamasi. Hasilnya dianalisis secara statistik dengan uji Kolmogorov-Smirnov dilanjutkan dengan uji ANOVA satu arah serta GLM repeated measures dengan taraf kepercayaan 95%.
Hasil daya anti inflamasi berturut-turut untuk asetil eugenol dosis 0,260; 0,521; dan 1,042 ml/kg BB adalah 39,38%; 52,98%; dan 69,82%. Nilai ED50 dari
xviii
ABSTRACT
Acetyl eugenol had been proven inhibit human platelet agregation in vitro, as a result of arachidonic acid metabolism inhibition (Srivastava and Malholtra, 1991). The study aims to evaluate the anti-inflammatory effect of acetyl eugenol given orally on male mice.
Formalin test was used to evaluate the anti-inflammatory effect, by injecting 0,5% formalin to induce paw edema. In this study, mice were divided into 5 groups, the first was negative control received Virgin Coconut Oil (VCO), the second group was positive control received diclofenac potassium, and the 3 other groups received different doses of acetyl eugenol at 0,260; 0,521; and 1,042 ml/kg BW. All drugs were administered orally in a single dose, 1 hour before the subplantar injection of formalin. The paw thickness was measured using a vernier caliper before injection of formalin and every hour for a period of 6 hour. Analysis of the result was carried out by calculating the AUC for every mouse in the period of measurement to calculate the percentage of inflammatory inhibiton. The result then analyzed statistically using the one way ANOVA and GLM repeated measures (p<0,05).
The result of this research indicated that acetyl eugenol at doses of 0,260; 0,521; and 1,042 ml/kg BW significantly inhibited inflammation with each value of inflammatory inhibition percentage were 39,38%; 52,98%; and 69,82%. The value of ED50 of acetyl eugenol for oral administration in mice was 0,400 ml/kg
BW.
1
BAB I
PENGANTAR
A. Latar Belakang
Inflamasi merupakan respon terlokalisasi yang dihasilkan oleh adanya kerusakan pada jaringan tervaskularisasi, yang berperan untuk menghancurkan, memperkecil, atau menyingkirkan baik agen penyebab kerusakan tersebut serta jaringan yang rusak itu sendiri. Inflamasi dicirikan dengan respon akut berupa tanda-tanda yang meliputi rasa nyeri (dolor), panas (calor), kemerahan (rubor), pembengkakan (tumor), dan hilangnya fungsi jaringan (functiolessa). Inflamasi dapat disebabkan oleh berbagai sebab, antara lain agen biologis (bakteri), agen fisik (panas dan trauma mekanik), serta agen kimiawi (molekul toksik yang kecil dan makromolekul imunogenik). Peran inflamasi adalah untuk menahan meluasnya kerusakan serta memfasilitasi proses penyembuhan (Anonim, 2009).
Karena banyaknya hal yang dapat menyebabkan inflamasi, maka inflamasi menjadi suatu gangguan yang seringkali dihadapi. Sekalipun berperan dalam proses penyembuhan jaringan yang rusak, inflamasi seringkali menimbulkan rasa tidak nyaman seperti rasa nyeri serta panas pada penderitanya. Oleh karena itu, dibutuhkan obat-obatan yang mampu menangani inflamasi.
Eugenol, suatu senyawa yang merupakan komponen utama dari atsiri cengkeh (Syzygium aromaticum L.) adalah salah satu senyawa alam yang tergolong OAINS (Rubin, Pan, dan Volpe, 2001). Sebagai suatu agen anti inflamasi, eugenol bekerja dengan melakukan penghambatan biosintesis prostaglandin dengan menghambat kerja enzim siklooksigenase 2 (Okada, dkk., 2005). Dalam suatu uji anti inflamasi, eugenol dapat diadministrasikan secara per oral dan terbukti efektif sebagai agen anti inflamasi (Daniel, dkk., 2009).
Dalam perkembangannya, pada senyawa eugenol dapat ditambahkan gugus tertentu sehingga terbentuk beberapa senyawa turunan eugenol. Contoh dari senyawa turunan eugenol antara lain metil eugenol, asetil eugenol, serta benzoil eugenol. Telah dilakukan beberapa penelitian yang menunjukkan bahwa beberapa senyawa turunan eugenol hasil sintesis berpotensi dikembangkan sebagai obat anti inflamasi (Sadeghian, Seyedi, Saberi, Arghiani, dan Riazi, 2007).
Asetil eugenol merupakan salah satu senyawa turunan eugenol selain juga terkandung dalam jumlah kecil di dalam atsiri cengkeh yang diduga memiliki aktivitas anti inflamasi. Srivastava dan Maholtra (1991) melakukan penelitian in vitro terhadap asetil eugenol dan menemukan bahwa asetil eugenol dapat menghambat agregasi platelet. Hal ini berarti asetil eugenol sendiri memiliki aktivitas dalam penghambatan metabolisme asam arakidonat.
didominasi neutrofil. Beberapa studi membuktikan bahwa setelah injeksi formalin, edema pada kaki hewan uji terjadi dengan cepat (Lee dan Jeong, 2001).
Dalam penelitian ini, peneliti bermaksud membuktikan adanya efek anti inflamasi dari asetil eugenol bila diberikan secara oral dengan subjek uji yang digunakan adalah mencit jantan galur Swiss dan sebagai model inflamasi digunakan edema kaki terinduksi formalin.
1. Permasalahan
Berdasarkan uraian yang dikemukakan di atas, maka permasalahan yang diteliti adalah:
a. apakah pemberian asetil eugenol secara oral pada mencit dapat mengurangi tebal edema kaki mencit jantan galur Swiss yang diinduksi formalin 0,5%? b. berapa persen penghambatan inflamasi asetil eugenol yang diberikan secara
oral pada edema kaki mencit jantan galur Swiss yang diinduksi formalin 0,5%? c. berapa dosis efektif asetil eugenol secara oral sebagai agen anti inflamasi terhadap edema kaki mencit jantan galur Swiss yang diinduksi formalin 0,5%?
2. Keaslian penelitian
a. Acetyl Eugenol, a Component of Oil of Cloves (Syzygium aromaticum L.) Inhibits Aggregation and Alters Arachidonic Acid Metabolism in Human Blood
Platelets (Srivastava dan Malhotra, 1991).
b. Antinociceptive Effect of Methyl Eugenol on Formalin-Induced Hyperalgesia in Mice (Yano, dkk.,2006).
3. Manfaat penelitian
a. Manfaat teoritis. Penelitian ini diharapkan dapat memperkaya pengetahuan dalam penggunaan senyawa hasil sintesis sebagai anti inflamasi
b. Manfaat praktis. Penelitian ini diharapkan mampu memberikan informasi kepada masyarakat dalam penggunaan asetil eugenol dalam menangani penyakit.
B. Tujuan Penelitian
1. Tujuan umum
Secara umum penelitian ini bertujuan untuk menambah informasi mengenai senyawa turunan bahan alam yang memiliki efek anti inflamasi.
2. Tujuan khusus
Berdasarkan permasalahan yang dikemukakan di atas, maka tujuan dari penelitian ini adalah:
a. mengetahui ada tidaknya penurunan edema kaki mencit jantan galur Swiss yang diinduksi formalin 0,5% dengan pemberian asetil eugenol secara oral b. mengetahui persen penghambatan inflamasi asetil eugenol secara oral pada
6
BAB II
PENELAAHAN PUSTAKA
A. Inflamasi
Inflamasi merupakan suatu reaksi general, non-spesifik, terhadap partikel asing atau stimulus noksius lainnya seperti toksin dan patogen. Inflamasi adalah bentuk usaha dari tubuh untuk menginaktivasi atau menghancurkan organisme penginvasi, menyingkirkan iritan, serta memulai tahap perbaikan jaringan (Madigan, Martinko, dan Parter, 2000). Karakteristik respon inflamasi mencakup kemerahan, pembengkakan, rasa nyeri, serta panas yang sifatnya terlokalisasi pada tempat rusaknya jaringan (Furr, 1992).
Umaru, dkk. (2009) menjelaskan bahwa inflamasi dipacu oleh pelepasan beberapa jenis mediator kimiawi dari jaringan yang rusak dan sel yang bermigrasi. Mediator kimiawi yang dilepaskan bergantung pada tipe inflamasi yang terjadi dan mencakup senyawa amin seperti histamin dan 5-hidroksitriptamin seperti prostaglandin, peptida kecil seperti bradikinin, dan peptida yang lebih besar seperti interleukin-1 yang merupakan sitokin.
Proses terjadinya inflamasi melalui pembentukan prostaglandin dari asam arakidonat terjadi sebagai berikut:
Gambar 1. Jalur metabolisme asam arakidonat (Sakakibara, 2010)
Dalam gambar di atas dijelaskan bagaimana mediator inflamasi disintesis dari asam arakidonat. Asam arakidonat berasal dari fosfolipid, bagian dari membran sel. Enzim fosfolipase akan mengubah fosfolipid menjadi asam arakidonat. Asam arakidonat kemudian menjalani dua jalur metabolisme, yaitu jalur siklooksigenase serta jalur lipooksigenase. Pada jalur lipooksigenase akan dihasilkan leukotrien, suatu mediator inflamasi. Sementara pada jalur siklooksigenase, akan dihasilkan beberapa senyawa eicosanoid, antara lain protaglandin (melalui jalur COX-2) serta prostasiklin dan tromboksan (melalui jalur COX-1) (Sakakibara, 2010). Senyawa eicosanoid yang dihasilkan melalui jalur siklooksigenase ini memiliki karakteristik yang berbeda, prostasiklin (PGI2)
dan tromboksan (TXA2) merupakan senyawa konstitutif yang berfungsi
melandasi terjadinya beberapa efek samping dari OAINS yang tidak selektif terhadap COX-2 (Kawai, 1998).
B. Anti Inflamasi
Obat anti radang bukan steroid atau yang lazim dinamakan non steroidal antiinflammatory drugs (NSAIDs) adalah golongan obat yang terutama bekerja perifer, memiliki aktivitas penghambat radang dengan mekanisme kerja menghambat biosintesis prostaglandin melalui penghambatan aktivitas enzim siklooksigenase (Kartasasmita, 2002).
Menurut Dannhardt dan Laufer (2000), pendekatan untuk menentukan apakah suatu senyawa dapat memiliki aksi sebagai inhibitor COX-2 yang selektif dapat dilakukan secara struktural. Terdapat 5 macam golongan struktural yang berpotensi selektif dalam menghambat enzim COX-2, yaitu (1) karboksil dan heterosiklik yang memiliki moietas aril yang berikatan visinal, (2) diaril atau aril/heteroaril-eter dan turunan tioeter, (3) turunan cis-stillben, (4) diaril dan aril/heteroaril keton, dan (5) komponen dengan moietas antioksidatif.
C. Asetil Eugenol
Asetil eugenol merupakan senyawa yang memiliki nama kimia 4-allyl -2-methoxyphenyl acetate dengan bobot molekul 206.24 dan rumus molekul C12H14O3. Senyawa ini merupakan senyawa yang tidak larut dalam air, akan tetapi
Gambar 2. Struktur asetil eugenol (Anonim, 2000)
Asetil eugenol merupakan komponen dari minyak atsiri cengkeh (Syzygium aromaticum L.) (Srivastava dan Maholtra, 1991). Asetil eugenol dapat juga disintesis dengan mereaksikan eugenol dan anhidrida asam asetat sebagai agen pengasilasi (Bulan, 2004).
Srivastava dan Maholtra (1991) melakukan penelitian in vitro asetil eugenol terhadap platetet manusia. Hasilnya terjadi penghambatan agregasi platelet yang diduga akibat aktivitas asetil eugenol mengganggu metabolisme asam arakidonat di jalur siklooksigenase.
Asetil eugenol dapat disintesis melalui reaksi esterifikasi antara eugenol dengan anhidrida asam asetat dengan berbagai katalis. Bulan (2004) mensintesis asetil eugenol dengan menggunakan asam sulfat sebagai katalis, sementara Riswanto (2011) menggunakan natrium hidroksida sebagai katalis. Penggunaan NaOH sebagai katalis bertujuan untuk meningkatkan nukleofilisitas OH fenolik pada eugenol sehingga lebih optimal menyerang C karbonil pada anhidrida asam asetat. Hal ini terbukti dengan dihasilkannya kemurnia asetil eugenol sebesar 95,88% dengan katalis NaOH sementara sintesis asetil eugenol dengan katalis H2SO4 menghasilkan asetil eugenol dengan kemurnian 69%. Asetil eugenol hasil
berbau cengkeh. Mekanisme reaksi sintesis asetil eugenol dengan katalis natrium hidroksida dapat digambarkan sebagai berikut:
OH
Gambar 3. Mekanisme reaksi sintesis asetil eugenol (Riswanto, 2011)
D. Cataflam® D-50 (Kalium Diklofenak)
Gambar 4. Struktur kalium diklofenak (Novartis, 2009)
Tablet Cataflam® D-50 merupakan sediaan tablet tanpa salut sehingga bersifat dispersible atau dapat digerus dan memungkinkan digunakan dalam peracikan obat untuk resep. Selain kalium diklofenak, bahan inaktif yang terkandung dalam tablet Cataflam® D-50 antara lain kalsium fosfat, silikon dioksida koloidal, besi oksida, magnesium stearat, mikrokristalin selulosa, polietilen glikol, povidone, natrium glikolat, pati jagung, talk, serta titanium dioksida (Novartis, 2009).
E. Virgin Coconut Oil
Virgin Coconut Oil (VCO) atau minyak kelapa murni merupakan minyak yang diperoleh dari pengolahan kopra atau daging kelapa segar dari tanaman kelapa (Cocos nucifera L.) secara mekanik atau natural yang berarti tanpa penggunaan panas, yang hasilnya tidak terjadi perubahan terhadap minyak itu sendiri. VCO sesuai untuk konsumsi manusia dalam bentuk alaminya (APCC, 2004).
Pasific Coconut Community (APCC) sendiri juga telah menetapkan standar kandungan dalam VCO yang dapat dilihat dalam tabel 1.
Tabel I. Komposisi asam lemak dalam Virgin Coconut Oil menurut standar APCC (APPC, 2004)
Asam Lemak Rumus Kimia Jumlah (%)
Asam lemak jenuh
F. Metode Uji Efek Anti Inflamasi
Evans dan Williamson (1996) mengemukakan beberapa metode yang dapat digunakan untuk mengukur efek anti inflamasi, antara lain:
1. Inflamasi (eritema dan udem pada telinga) hewan pengerat 2. Uji udema pada telapak kaki tikus
3. Uji induksi artritis pada tikus atau mencit.
merupakan fase inflamasi yang dimulai 25 menit setelah injeksi (Bruera dan Purtenoy, 2003).
Suatu metode penentuan persen penghambatan inflamasi dengan menggunakan data luas area di bawah kurva memiliki rumus sebagai berikut:
Keterangan :
(AUC0-x)0 = AUC0-x rata-rata kelompok kontrol negatif
(AUC0-x)n = AUC0-x masing-masing hewan uji yang diberi senyawa uji
dengan dosis sebesar n (Ikawati, Suparjan, dan Asmara, 2007).
G. Uji Statistik One Way ANOVA dan General Linear Model
Uji statistik One Way Analysis of Variance (ANOVA) digunakan dalam analisis data numerik dari lebih dari dua kelompok tidak berpasangan. Disebut tidak berpasangan karena subjek uji pada setiap kelompok uji adalah subjek yang berbeda (Dahlan, 2009).
ANOVA merupakan teknik general yang dapat digunakan untuk menguji kebenaran suatu hipotesis di antara lebih dari dua kelompok, dengan asumsi bahwa populasi yang disampel memiliki distribusi normal (Anonim, 2008).
Analisis General Linear Model Repeated Measures merupakan teknik yang digunakan untuk menganalisis respon variabel pada subjek yang sama dengan pengukuran di waktu yang berbeda (Shelden danBrown, 2008).
Analisis Post Hoc dilakukan jika hasil analisis ANOVA menunjukkan hasil adanya perbedaan yang signifikan pada kelompok uji, yaitu untuk menemukan letak perbedaan yang bermakna tersebut (Dahlan, 2009).
H. Landasan Teori
Inflamasi merupakan respon jaringan hidup terhadap suatu gangguan dengan cara memobilisasi semua bentuk pertahanan tubuh berupa reaksi vaskuler, neurologik, humoral, dan seluler. Inflamasi seringkali menimbulkan rasa tidak nyaman pada penderitanya sehingga membutuhkan penanganan dengan obat-obatan anti inflamasi.
Eugenol dan asetil eugenol adalah senyawa yang terkandung dalam minyak atsiri cengkeh. Asetil eugenol juga dapat disintesis dari eugenol dengan mereaksikannya dengan asam asetat anhidrida. Eugenol telah terbukti memiliki aktivitas anti inflamasi yang mirip dengan obat-obatan golongan AINS, yaitu menghambat pembentukan prostaglandin yang merupakan mediator inflamasi, dan dapat diadministrasikan melalui jalur administrasi per oral (Daniel, dkk., 2009).
biosintesis prostaglandin. Dengan demikian diharapkan asetil eugenol seperti halnya eugenol mampu menghambat pembentukan prostaglandin pada model inflamasi berupa edema kaki mencit yang diinduksi larutan formalin secara subplantar sehingga terjadi penurunan tebal edema kaki tersebut.
I. Hipotesis
16
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk jenis penelitian eksperimental murni rancangan acak lengkap pola satu arah.
B. Variabel Penelitian
1. Variabel utama
a. Variabel bebas
Variabel bebas dalam penelitian ini adalah dosis asetil eugenol. Dosis asetil eugenol adalah sejumlah volume asetil eugenol tiap satuan kg berat badan (dengan satuan ml/ kg BB).
b. Variabel tergantung
Variabel tergantung dalam penelitian ini adalah tebal edema kaki mencit yang diinduksi larutan formalin 0,5%. Cara mengukur variabel tergantung adalah dengan mengukur tebal telapak kaki mencit dengan menggunakan jangka sorong (vernier caliper) dengan satuan sentimeter.
2. Variabel pengacau
a. Variabel pengacau terkendali
b. Variabel pengacau tak terkendali
a) kondisi patologi hewan uji
C. Definisi Operasional
1. Tebal edema adalah tebal telapak kaki yang diinduksi oleh larutan formalin 0,5% yang diinjeksikan secara subplantar dan diukur dengan jangka sorong (vernier caliper) dalam satuan sentimeter
2. Asetil eugenol adalah senyawa hasil sintesis dari eugenol dengan asam asetat anhidrida yang disintesis oleh Riswanto (2011) di laboratorium Kimia Organik Universitas Sanata Dharma Yogyakarta
3. Formalin adalah larutan 37% formaldehid dalam aquades. Untuk menginduksi edema digunakan larutan formalin 0,5%
4. Inflamasi merupakan respon lokal tubuh terhadap suatu gangguan yang dicirikan dengan rubor, dolor, kalor, tumor, dan functiolessa. Dalam penelitian ini yang digunakan sebagai indikator inflamasi yang akan diukur adalah tumor (bengkak).
D. Bahan atau Materi Penelitian
1. Bahan utama
memiliki karakteristik organoleptis antara lain berwarna merah dan berbau cengkeh (lampiran 4a). Asetil eugenol yang digunakan telah melalui serangkaian uji elusidasi struktur dan dipastikan bahwa senyawa tersebut adalah benar asetil eugenol. Hasil elusidasi struktur dapat dilihat pada lampiran 3.
b. Mencit putih jantan: hewan uji yang digunakan adalah mencit putih jantan galur Swiss dengan berat badan 20-30 gram dengan umur 2-3 bulan. Hewan uji diperoleh dari Laboratorium Hayati Imono Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
2. Bahan kimia
a. Formalin 0,5% merk Bratachem®: digunakan sebagai bahan penginduksi edema pada kaki mencit dengan injeksi subpantar sebagai model inflamasi. Formalin berasal dari Laboratorium Farmakologi dan Toksikologi Universitas Sanata Dharma Yogyakarta
b. Kalium diklofenak: digunakan sebagai kontrol positif. Kalium diklofenak yang digunakan berasal dari tablet Cataflam® (Novartis) D (dispersible) 50 mg yang diperoleh dari Apotek Kimia Farma Yogyakarta
c. Virgin Coconut Oil (VCO): digunakan sebagai pelarut asetil eugenol serta sebagai kontrol negatif. VCO yang digunakan adalah VCO merk HealthyCo® dan diperoleh dari Apotek Sanata Dharma Yogyakarta.
E. Alat atau Instrumen Penelitian
2. Jangka sorong (vernier caliper) merk Mitutoyo 2. Kotak kaca tempat pengamatan
3. Stopwatch merk Baby-G
1. Pembuatan larutan formalin 0,5%
Pembuatan larutan asam formalin 0,5% dari larutan formalin 100% (formaldehid 37%) menggunakan rumus volume1 x konsentrasi1 = volume2 x
konsentrasi2. Dengan menggunakan rumus ini, larutan formalin 0,5% dibuat
dengan mengambil formalin 100% sebanyak 0,5 ml kemudian diencerkan menggunakan aquadest di dalam labu ukur sampai diperoleh volume 100 ml. 2. Penentuan volume injeksi subplantar dengan formalin 0,5%
Injeksi subplantar dengan larutan formalin 0,5% diberikan sejumlah 0,025 ml tiap 20 gram berat badan mencit (Vogel, 2002).
3. Penentuan dosis kalium diklofenak
didispersikan dalam 100 ml aquadest sehingga diperoleh larutan dengan konsentrasi 0,05% (b/v).
4. Penentuan waktu pemberian asetil eugenol
Asetil eugenol sebagai senyawa uji diberikan 1 jam sebelum induksi edema dengan injeksi formalin 0,5% secara subplantar (Ayoola, dkk., 2009). 5. Pemilihan kontrol negatif
Kontrol negatif adalah zat yang tidak memiliki efek anti inflamasi sehingga dapat digunakan sebagai pembanding terhadap zat yang diuji serta dapat menjadi pelarut yang aman untuk asetil eugenol untuk diberikan secara
6. Pembuatan larutan stok asetil eugenol
Larutan stok asetil eugenol dalam VCO dibuat dengan konsentrasi 6,25% v/v. Cara pembuatannya dengan mengambil 0,5 ml asetil eugenol, dimasukkan ke dalam gelas ukur, kemudian ditambahkan VCO sampai 8 ml.
7. Penentuan dosis asetil eugenol
Dosis I = 0,260 ml/kg BB. Dosis II = 0,521 ml/kg BB. Dosis III = (0,0625 ml/ml x 0,5 ml) / 30 g = 1,042 x 10-3 ml/g BB = 1,042 ml/kg BB.
8. Penentuan lama pengamatan
Lama pengamatan pada hewan uji adalah 6 jam dimulai dari penyuntikan formalin subplantar (Ayoola, dkk., 2009).
9. Perlakuan pada hewan uji
Hewan uji dalam penelitian ini dibagi secara acak menjadi 5 kelompok, di mana tiap-tiap kelompok terdiri dari 5 ekor mencit. Sebelum hewan uji digunakan untuk penelitian, terlebih dahulu hewan uji diadaptasikan dengan lingkungan laboratorium selama ± 2 minggu. Hewan uji diperlakukan sama baik dari segi pakan, kandang, maupun minumnya. Sebelum mencit diberi perlakuan, terlebih dahulu mencit dipuasakan selama 24 jam untuk meminimalkan variabel-variabel pengacau. Mencit yang sedang dipuasakan diletakkan pada kandang terpisah dan tetap diberikan minum.
Kemudian mencit dikelompokkan dan diperlakukan sebagai berikut: Kelompok I
Merupakan kontrol positif. Tebal kaki kanan mencit diukur dengan jangka sorong, kemudian mencit diberi kalium diklofenak secara oral, 1 jam kemudian diinjeksi larutan formalin 0,5% secara subplantar. Mencit diamati dan diukur tebal edemanya setiap satu jam sampai 6 jam.
Kelompok II
diinjeksi larutan formalin 0,5% secara subplantar. Mencit diamati dan diukur tebal edemanya setiap satu jam sampai 6 jam.
Kelompok III
Merupakan kelompok perlakuan pertama. Tebal kaki kanan mencit diukur dengan jangka sorong, kemudian mencit diberi asetil eugenol dosis 0,260 ml/kg BB secara oral, 1 jam kemudian diinjeksi larutan formalin 0,5% secara subplantar. Mencit diamati dan diukur tebal edemanya setiap satu jam sampai 6 jam.
Kelompok IV
Merupakan kelompok perlakuan kedua. Tebal kaki kanan mencit diukur dengan jangka sorong, kemudian mencit diberi asetil eugenol dosis 0,521 ml/kg BB secara oral, 1 jam kemudian diinjeksi larutan formalin 0,5% secara subplantar. Mencit diamati dan diukur tebal edemanya setiap satu jam sampai 6 jam.
Kelompok V
Merupakan kelompok perlakuan ketiga. Tebal kaki kanan mencit diukur dengan jangka sorong, kemudian mencit diberi asetil eugenol dosis 1,042 ml/kg BB secara oral, 1 jam kemudian diinjeksi larutan formalin 0,5% secara subplantar. Mencit diamati dan diukur tebal edemanya setiap satu jam sampai 6 jam.
Keterangan:
Kel I : kelompok kontrol positif (Cataflam®)
Kel II : kelompok kontrol negatif (VCO)
Kel III : kelompok perlakuan dosis asetil eugenol 0,260 ml/kg BB
Kel IV : kelompok perlakuan dosis asetil eugenol 0,521 ml/kg BB
Kel V : kelompok perlakuan dosis asetil eugenol 1,042 ml/kg BB
Gambar 5. Skema kerja penelitian uji daya anti inflamasi asetil eugenol 11. Penentuan % penghambatan inflamasi
Metode penentuan persen penghambatan inflamasi yang digunakan dalam penelitian ini adalah dengan menghitung luas area di bawah kurva (AUC) untuk setiap mencit pada setiap rentang waktu pengukuran sehingga dapat dihitung % penghambatan inflamasinya dengan rumus:
Hewan uji sejumlah 25 ekor
Kel I Kel II Kel III Kel IV Kel V
Tebal kaki kanan mencit diukur
Mencit diberikan senyawa uji beserta kontrol secara oral
1 jam kemudian mencit diinjeksi subplantar dengan formalin 0,5%
Keterangan :
(AUC0-x)0 = AUC0-x rata-rata kelompok kontrol negatif
(AUC0-x)n = AUC0-x masing-masing hewan uji yang diberi senyawa uji dengan
dosis sebesar n (Ikawati, dkk., 2007).
Hasil yang diperoleh kemudian dianalisis secara statistik untuk menemukan dosis asetil eugenol yang dapat menurunkan tebal edema kaki mencit secara signifikan.
G. Analisis Hasil
25
BAB IV
HASIL DAN PEMBAHASAN
A. Hasil Uji Efek Penghambatan Inflamasi dan Besar Penghambatan
Inflamasi Asetil Eugenol secara Oral
Penelitian ini bertujuan untuk mengetahui kemampuan sekaligus besarnya kemampuan senyawa asetil eugenol dalam menangani inflamasi. Asetil eugenol yang akan diuji sebelumnya telah melalui serangkaian pengujian elusidasi struktur dan terbukti bahwa senyawa yang digunakan adalah benar asetil eugenol (Riswanto, 2011). Hasil elusidasi struktur senyawa asetil eugenol yang digunakan dapat dilihat dalam lampiran 3. Penghambatan inflamasi ditandai dengan penurunan tebal edema kaki hewan uji yang diinjeksi secara subplantar dengan larutan formalin 0,5% akibat pemberian senyawa asetil eugenol terhadap hewan uji secara oral. Metode yang digunakan dalam uji anti inflamasi ini adalah metode induksi inflamasi dengan formalin 0,5% dan pengukuran tebal edema kaki hewan uji menggunakan jangka sorong (vernier caliper) yang diadopsi dari penelitian Joseph, dkk. (2005) di mana variabel yang diukur adalah ketebalan edema telapak kaki mencit dengan posisi jangka sorong vertikal. Hewan uji yang digunakan dalam penelitian ini adalah mencit jantan galur Swiss.
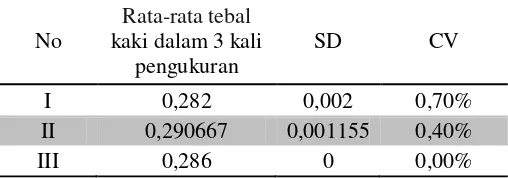
metode ini relatif sederhana dari segi instrumen, serta memungkinkan dihasilkannya data yang lebih akurat karena pengukuran dapat dilakukan secara berulang untuk memastikan data yang terambil sudah tepat. Sebelum memulai rangkaian penelitian, alat jangka sorong yang akan digunakan dikalibrasi terlebih dahulu untuk memastikan kelayakan dan akurasi serta presisi alat tersebut dalam mengukur. Kalibrasi dilakukan dengan membandingkan jangka sorong yang akan digunakan dengan alat lain yang bersertifikat. Berdasarkan hasil kalibrasi, jangka sorong yang digunakan memiliki penyimpangan ± sebesar 10 µm, sedangkan penyimpangan terbesar yang direkomendasikan adalah 20 µm, hal ini berarti jangka sorong tersebut layak untuk digunakan dalam proses pengukuran. Untuk lebih jelas mengenai data kalibrasi alat dapat dilihat pada lampiran 1.
Selain itu, uji keterulangan (presisi) terhadap jangka sorong yang akan digunakan juga dilakukan secara langsung melalui suatu rangkaian pengukuran untuk dapat menentukan Coefficient of Variation (CV) dari hasil pengukuran tersebut. Menurut Mulja dan Hanwar (cit., Wulandari, Friamita, dan Patramurti, 2006) suatu data dikatakan memiliki presisi yang baik bila nilai CV kurang dari 2%. Dari tiga rangkaian uji yang dilakukan, CV yang dihasilkan adalah 0,70%, 0,40%, dan 0,00%. Data uji presisi dapat dilihat pada lampiran 2. Dengan demikian, jangka sorong yang digunakan terbukti memiliki presisi yang baik.
Tabel II. Hasil uji presisi terhadap jangka sorong merk Mitutoyo
Pada pengujian ini dipilih larutan formalin dengan konsentrasi 0,5% sebagai zat penginduksi inflamasi. Larutan formalin disuntikkan secara subplantar pada kaki kanan mencit untuk menimbulkan edema. Larutan formalin dipilih karena inflamasi yang ditimbulkan terjadi dengan cepat dan tampak jelas disertai gejala inflamasi lain seperti merah pada daerah edema. Joseph, dkk. (2005) menyatakan bahwa formalin merupakan zat yang paling cocok untuk menguji kemampuan suatu zat sebagai agen anti inflamasi karena karakter inflamasinya yang mirip dengan artritis pada manusia. Terjadinya edema yang diinduksi formalin merupakan suatu proses bifasik. Fase pertama terjadi karena pelepasan kinin, serotonin, dan histamin. Fase kedua dimulai 25 menit setelah injeksi dan berkaitan dengan pembentukan prostaglandin.
Virgin Coconut Oil (VCO) digunakan sebagai kontrol negatif untuk mengetahui apakah VCO berpengaruh terhadap aktivitas anti inflamasi asetil eugenol. Asetil eugenol merupakan senyawa yang tidak larut dalam air. Secara teoritis asetil eugenol larut dalam etanol dan eter, sementara kedua pelarut tersebut tidak dapat digunakan untuk penghantaran obat secara per oral dikarenakan toksisitasnya. Melalui percobaan yang dilakukan peneliti pada saat orientasi, ternyata VCO mampu melarutkan asetil eugenol dengan baik, selain itu juga relatif aman untuk diberikan secara oral kepada hewan uji.
yang mengandung diklofenak yang beredar merupakan tablet salut enterik yang ditujukan untuk mengurangi resiko iritasi pada lambung (Padmadisastra, Abdassah, dan Wijanarko, 2007). Desain salut enterik bertujuan agar obat baru akan dilepaskan saat sudah mencapai usus halus. Oleh karena itu, pada sediaan tersebut selain kalium diklofenak juga terdapat bahan lain yang menyusun penyalut dari tablet tersebut yang tidak memungkinkan tablet untuk digerus, sedangkan dalam penelitian ini tablet harus digerus agar dapat dilarutkan dalam aquades. Cataflam® D merupakan tablet dispersible tanpa salut sehingga memungkinkan tablet ini untuk digerus dan didispersikan dalam aquades untuk diberikan pada mencit secara per oral. Dosis Cataflam® yang digunakan adalah 9,1 mg/kg BB mencit (Dewi, 2010).
General Linear Model (GLM) repeated measures dengan taraf kepercayaan 95%. Hasilnya dapat dilihat pada lampiran 13.
kelompok II
kelompok III kelompok IV
kelompok I
kelompok V
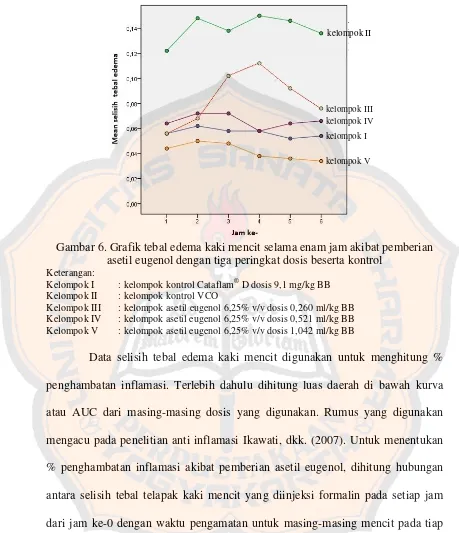
Gambar 6. Grafik tebal edema kaki mencit selama enam jam akibat pemberian asetil eugenol dengan tiga peringkat dosis beserta kontrol
Keterangan:
Kelompok I : kelompok kontrol Cataflam® D dosis 9,1 mg/kg BB
Kelompok II : kelompok kontrol VCO
Kelompok III : kelompok asetil eugenol 6,25% v/v dosis 0,260 ml/kg BB
Kelompok IV : kelompok asetil eugenol 6,25% v/v dosis 0,521 ml/kg BB
Kelompok V : kelompok asetil eugenol 6,25% v/v dosis 1,042 ml/kg BB
inflamasi untuk setiap kelompok perlakuan. Hasil perhitungan % penghambatan inflamasi dianalisis normalitasnya dengan uji Kolmogorov-Smirnov dilanjutkan dengan analisis ANOVA 1 arah dengan taraf kepercayaan 95%.
Gambar 7. Diagram batang AUC untuk masing-masing kelompok perlakuan beserta kontrol
Tabel III. Hasil rata-rata AUC, % penghambatan inflamasi dan hasil uji Scheffe pada perlakuan asetil eugenol secara oral beserta kontrolnya
Kel Rata-rata AUC
Kelompok I : kelompok kontrol positif Cataflam® dosis 9,1 mg/kg BB
Kelompok II : kelompok kontrol negatif VCO
Kelompok III : kelompok asetil eugenol 6,25% v/v dosis 0,260 ml/kg BB
Kelompok IV : kelompok asetil eugenol 6,25% v/v dosis 0,521 ml/kg BB
Kelompok V : kelompok asetil eugenol 6,25% v/v dosis 1,042 ml/kg BB
b : berbeda bermakna (p < 0,05)
tb : berbeda tidak bermakna (p > 0,05)
X : mean (rata-rata)
SE : standard error
Dari tabel di atas terlihat bahwa masing-masing dosis asetil eugenol memiliki efek anti inflamasi yang dinilai dari % penghambatan inflamasi yang diperoleh dengan membandingkan AUC total tiap kelompok perlakuan dengan AUC rata-rata kelompok kontrol negatif. Analisis ANOVA serta uji Scheffe yang dilakukan menunjukkan bahwa efek anti inflamasi asetil eugenol dosis 0,260; 0,521; dan 1,042 ml/kg BB tidak berbeda bermakna (p>0,05) dengan efek anti inflamasi kontrol positif, yaitu Cataflam® yang berisi kalium diklofenak. Hal ini berarti pada dosis terendah, yaitu 0,260 ml/kg BB mencit, senyawa asetil eugenol telah dapat bekerja sebagai anti inflamasi dengan % penghambatan inflamasi yang sebanding dengan kerja kalium diklofenak dalam Cataflam® sebagai senyawa yang diketahui secara pasti sebagai agen anti inflamasi. Pada kelompok perlakuan dengan asetil eugenol, perbedaan yang bermakna terletak pada kelompok yang menerima dosis 0,260 ml/kg BB dengan kelompok yang menerima dosis 1,042 ml/kg BB. Persen penghambatan inflamasi pada kelompok yang menerima dosis 0,521 ml/kg BB tidak berbeda bermakna dengan kedua dosis lainnya.
Mekanisme kerja OAINS meliputi reduksi sintesis prostaglandin dengan menghambatan enzim siklooksigenase melalui antagonisme dengan asam arakidonat untuk berikatan dengan enzim siklooksigenase (COX). Agar suatu obat dapat menjadi inhibitor kompetitif terhadap asam arakidonat untuk dapat berikatan dengan enzim COX, obat tersebut harus memiliki lipofilisitas yang tinggi serta properti asam untuk menyerupai substrat alami dari COX itu sendiri (Mehanna, 2003). Diklofenak sendiri yang dalam penelitian ini digunakan sebagai kontrol positif merupakan golongan OAINS turunan asam asetat yang memiliki fungsionalitas asam sehingga dapat berikatan dengan enzim COX untuk menghambat biosintesis prostaglandin. Asetil eugenol seperti halnya eugenol, merupakan senyawa derivat fenol, yang artinya juga memiliki properti asam. Selain itu, asetil eugenol juga merupakan senyawa penyusun minyak atsiri tanaman cengkeh yang bersifat lipofil (Pauli, 2006). Sifat dasar ini mendukung aksi dari asetil eugenol untuk berkompetisi dengan asam arakidonat dalam berikatan dengan enzim siklooksigenase.
+
Gambar 8. Reaksi asetilasi serin oleh asetil eugenol
Perbedaan antara siklooksigenase 1 dan siklooksigenase 2 terletak pada asam amino yang berada di posisi 523 (Gierse, dkk., 1996). Pada COX-1 posisi 523 adalah isoleusin, sementara pada COX-2 adalah valin. Untuk mampu menjadi suatu inhibitor selektif COX-2, asetil eugenol harus mampu berinteraksi dengan valin. Secara struktural, interaksi yang mungkin terjadi antara asetil eugenol adalah interaksi hidrofobik antara asetil eugenol dengan residu asam amino valin pada COX-2.
Gambar 9. Interaksi hidrofobik antara asam amino valin dengan asetil eugenol Dengan pendekatan struktural yang dikemukakan oleh Dannhardt dan Laufer (2000), asetil eugenol termasuk ke dalam golongan diaril atau aril/heteroaril-eter dan turunan tioeter. Hal tersebut dapat dilihat dalam gambar 10 dan 11.
serin asetil eugenol
valin
Gambar 10. Kerangka struktur diaril atau aril/heteroaril-eter dan turunan tioeter (Dannhardt dan Laufer, 2000)
Dalam gambar tersebut, bagian X dapat berupa molekul O maupun S, yang terikat dengan sebuah cincin aromatis yang mengikat 2 rantai aril, serta sebuah gugus karboksil. Hal ini sesuai dengan struktur asetil eugenol seperti tampak pada gambar 9.
Gambar 11. Struktur asetil eugenol (Anonim, 2000)
Sebuah substituen penarik elektron pada cincin aromatis diduga memegang peranan penting dalam aktivitas fisiologis pada golongan senyawa dengan struktur semacam ini, dengan aktivitas maksimal untuk gugus asetil dan siano (Dannhardt dan Laufer, 2000).
tersebut. Radikal terbentuk pada bagian alil karena atom H pada bagian tersebut tidak terikat kuat dibandingkan H pada cincin benzen maupun H pada ikatan rangkap sehingga mudah lepas.
Gambar 12. Pembentukan radikal alil dari asetil eugenol (Hidalgo, dkk., 2009) Salah satu peristiwa yang terjadi dalam proses inflamasi adalah oksidasi asam arakidonat oleh spesies oksigen reaktif (McIntyre dan Hazen, 2010). Dengan adanya aktivitas penangkapan senyawa radikal oleh asetil eugenol, maka oksidasi asam arakidonat menjadi senyawa HETE (hydroxyeicosatraenoic acid atau asam hidroksieikosatetraenoat) juga akan dihambat dan dengan demikian akan menurunkan reaksi inflamasi yang terjadi.
B. Hasil Uji Hubungan Linearitas antara Dosis Asetil Eugenol terhadap
Penghambatan Inflamasi
Analisis regresi dilakukan terhadap log dosis asetil eugenol serta % penghambatan inflamasi yang dihasilkan oleh masing-masing dosis tersebut. Hasilnya, pengujian daya anti inflamasi asetil eugenol secara oral terhadap mencit jantan galur Swiss yang diinduksi formalin 0,5% memiliki persamaan Y = 50,73x + 69,93 dengan nilai r = 0,9918. Melalui persamaan tersebut dapat diketahui nilai ED50 untuk asetil eugenol secara oral adalah 0,400 ml/kg BB mencit. Dosis ini nantinya apabila dikonversikan untuk manusia dengan menggunakan tabel konversi dosis Laurence dan Bacharach (1964), di mana faktor konversi dosis dari mencit 20 g ke manusia 70 kg adalah 387,9, akan menghasilkan nilai dosis 0,044 ml/kg BB manusia. Tabel konversi Laurence dan Bacharach dapat dilihat pada lampiran 14. Gambar 13 merupakan grafik kurva kekerabatan antara log dosis asetil eugenol dengan % penghambatan inflamasi.
Gambar 13.Grafik hubungan linearitas dosis 0,260; 0,521; dan 1,042 ml/kg BB mencit dengan peningkatan % penghambatan inflamasi
Berdasarkan tabel r, suatu data dikatakan memiliki hubungan kekerabatan yang nyata bila r hitungnya lebih besar atau sama dengan r tabel.
y = 50,73x + 69,93 R2
Untuk hubungan % penghambatan inflamasi asetil eugenol dengan dosisnya digunakan 3 peringkat dosis (N=3) dengan taraf kepercayaan 95%. R tabel untuk N=3 dengan taraf kepercayaan 95% adalah 0,997; sementara pada hasil yang diperoleh dari penelitian ini r hitung adalah 0,9918. Hasil statistik untuk % penghambatan inflamasi ini menunjukkan bahwa adanya peningkatan dosis akan menghasilkan peningkatan nilai % penghambatan inflamasinya, terutama pada dosis I dan III. Oleh karena itu, untuk memperoleh nilai r hitung yang lebih besar atau sama dengan r tabel dapat dilakukan dengan menambah peringkat dosis asetil eugenol. Tabel r dapat dilihat pada lampiran 14.
40
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Berdasarkan hasil dari penelitian ini, dapat disimpulkan bahwa:
1. asetil eugenol yang diberikan secara oral dapat menurunkan tebal edema kaki mencit jantan galur Swiss yang diinduksi formalin 0,5%
2. persentase penghambatan inflamasi yang ditimbulkan oleh asetil eugenol yang diberikan secara oral pada edema kaki mencit jantan galur Swiss yang diinduksi formalin 0,5% dengan dosis 0,260; 0,521; 1,042 ml/kg BB mencit berturut-turut sebesar 39,38%; 52,98%, dan 69,82%
3. dosis efektif asetil eugenol secara oral terhadap edema kaki mencit galur Swiss yang diinduksi formalin 0,5% adalah 0,400 ml/kg BB mencit.
B. Saran
Berdasarkan penelitian yag telah dilakukan, disarankan untuk melakukan penelitian mengenai:
1. identifikasi mekanisme asetil eugenol dalam menghambat proses metabolisme asam arakidonat secara in vitro
DAFTAR PUSTAKA
Anonim, 2000, Acetyl Eugenol, http://www.chemikalienlexikon. de/aroinfo/aceteuge.htm, diakses tanggal 3 November 2010.
Anonim, 2006, The Kruskal-Wallis Test, www.statistics.its.ac.id/ downloads/tugas/Kruskal%20Wallis.pdf, diakses tanggal 23 November 2010.
Anonim, 2008, The Analysis of Variance (ANOVA), http://www.itl. nist.gov/div898/handbook/prc/section4/prc43.htm, diakses tanggal 3 November 2010.
Anonim, 2009, Biomaterials-Tissue Interactions, MIT OpenCourseWare http://ocw.mit.edu/terms, diakses tanggal 29 Oktober 2010.
Anonim, 2010, Introduction to the Eicosanoids, http://themedical biochemistrypage.org/eicosanoids.html, diakses tanggal 2 November 2010.
APPC, 2004, Asian Pasific Coconut Community Standard for Virgin Coconut Oil, www.apccsec.org/document/VCNO.PDF, diakses tanggal 2 September 2010.
Ayoola, G. A., Akpanika, G. A., Awobajo, F. O., Sofidiya, M. O., Osunkalu, V. O., Coker, H. A. B., et al., 2009, Anti-Inflammatory Properties of the Fruits of Allanblanckia Floribunda Oliv. (Guttiferae), Botany Research International, 2(1): 21-26.
Bulan, R., 2004, Reaksi Asetilasi Eugenol dan Oksidasi Metil Iso Eugenol, Skripsi, 2-3, Universitas Sumatera Utara, Medan.
Bruera, E. R., and Portenoy, R. K., 2003, Cancer Pain: Assessment and Management, 15, Cambridge University Press, UK.
Daniel, A. N., Sartoretto, S. M., Schmidt, G., Caparroz-Assef, S. M., Bersani-Amado, C. A., and Cuman, R. K. N., 2009, Anti-inflammatory and Antinociceptive Activities of Eugenol Essential Oil in Experimental Animal Models, Revista Brasileira de Farmacognosia, 19: 1-5.
Dannhardt, G., and Laufer, S., 2000, Structural Approaches to Explain the Selectivity of COX-2 Inhibitors: Is There a Common Pharmacophore?, Current Medicinal Chemistry, 7:1101-1112.
Evans, F. J., and Williamson, E. M., 1996, Selection, Preparation, and Pharmacologicaly Evaluation of Plant Material, John Willey, New York, pp.131-137.
FAO, 2010, Eugenyl Acetate, http://www.fao.org/ag/agn/jecfa-flav/details.html?flavId=4820, diakses tanggal 2 Desember 2010.
Furr, J. R., 1992, Fundamentals of Immunology, in: Hugo, W.B., Russell, A.D. (Ed.), Pharmaceutical Microbiology, 5th ed., Blackwell Scientific Publications, London, pp. 305-331.
Gierse, J.K., McDonald, J. J., Hauser, S. D., Rangwala, S. H., Koboldt, C. M., and Seibert, K., 1996, A Single Amino Acid Difference between Cyclooxygenase-1 (COX-1) and -2 (COX-2) Reverses the Selectivity of COX-2 Specific Inhibitors, The Journal of Biological Chemistry,
271(26):15810-15814.
Hidalgo, M. E., Rosa, C. D. L., Carrasco, H., Cardona, W., Gallardo, C., Espinoza, L., 2009, Antioxidant Capacity of Eugenol Derivatives, Química Nova, 32(6).
Ikawati, Z., Suparjan, A. M., dan Asmara, L. S., 2007, Pengaruh Senyawa Heksagamavunon-1 (HGV-1) Terhadap Inflamasi Akut Akibat Reaksi Anafilaksis Kutaneus Aktif Pada Tikus Wistar Jantan Terinduksi Ovalbumin, Kemajuan Terkini Riset Universitas Gadjah Mada, 36-46. Joseph, S. M., George, M. C., Nair, J. R., Senan, V. P., Pillai, D., and Sherief, P.
M., 2005, Effect of Feeding Cuttlefish Liver Oil On Immune Function, Inflammatory Response And Platelet Aggregation in Rats, Current Science, 88:507-510.
Kartasasmita, R.E., Perkembangan Obat Antiradang Bukan Steroid, Kajian Pustaka, 27(4):75-91.
Kawai, S., 1998, Cyclooxygenase Selectivity and The Risk of Gastro-Intestinal Complications of Various Non-Steroidal Anti-Inflammatory Drugs: A Clinical Consideration, Inflammation Research, 47(2): 1023-3830.
Lee, I. O., and Jeong, Y. S., 2001, Effects of Different Concentrations of Formalin on Paw Edema and Pain Behaviors in Rats, Journal of Korean Medical Sciences, 17: 81-85.
Madigan, M. T., Martinko, J. M., andParter, J., 2000, Microbial Growth Control, in: Brock, T.D. (Ed.), Brock Biology of Microorganisms, 9th ed., Prentice Hill Inc., USA, 347-388.
McIntyre, T. M., Hazen, S. L., 2010, Lipid Oxidation and Cardiovascular Disease: Introduction to a Review Series, Circulation Research, 107:1167-1169. Mehanna, A. S., 2003, NSAIDs: Chemistry and Pharmacological Actions,
American Journal of Pharmaceutical Education, 67(2):1-5.
Mulja, M., dan Hanwar, D., 2003, Prinsip-Prinsip Cara Berlaboratorium yang Baik (Good Laboratory Practice), Majalah Farmasi Airlangga, Vol. III, No.2, 71-76.
Novartis, 2009, Cataflam® (Diclofenac Potassium Immediate-Release Tablet), www.pharma.us.novartis.com/product/pi/pdf/Cataflam.pdf, diakses tanggal 2 September 2010.
Okada, N., Hirata, A., Murakami, Y., Shoji, M., Sakagami, H., and Fujisawa, S., 2005, Induction of Cytotoxicity and Apoptosis and Inhibition of Cyclooxygenase-2 Gene Expression by Eugenol-Related Compounds, Pubmed Anticancer Research,25(5):3263-9.
Padmadisastra, Y., Abdassah, M., and Wijanarko, P., 2007, Formulation of Enteric Coated Tablets of Sodium Diclofenac, International Seminar on Pharmaceutics, 1-6.
Pauli, A., 2006, Essential Oils, Review Science, 13:1-7.
Rang, H. P., Dale, M. M., and Ritter, J. M., 1999, Anti-inflammatory and Immunosuppresant Drugs, in Pharmacology, 4th ed., Churchill Livingstone, London, pp. 229-247.
Sakakibara, H., 2010, Anti-inflammatory and Bronchoprotective Roles of Endogenous Prostaglandin E2, http://ai.jsaweb.jp/fulltext/048020103 /fig01.html, diakses tanggal 3 November 2010.
Shelden, B., and Brown, A., 2008, General Linear Model, http://www.cst.cmich.edu/users/lee1c/spss/StaProcGLM.htm, diakses tanggal 3 November 2010.
Srivastava, K. C., and Malhotra N., 1991, Acetyl Eugenol, a Component of Oil of Cloves (Syzygium aromaticum L.) Inhibits Aggregation and Alters Arachidonic Acid Metabolism in Human Blood Platelets, Pubmed Prostaglandins Leukot Essent Fatty Acids, 42(1):73-81.
Umaru, Titilayo, Nwamba, Charles, Kolo, Ibrahim, et al., 2009, Antimicrobial Activity of Non-Steroidal Anti-Inflammatory Drugs with Respect to Immunological Response: Diclofenac Sodium as a Case Study , African Journal of Biotechnology, 8(25):7332-7339.
Vogel, H. G., 2002, Drug Discovery and Evaluation: Pharmacological Assays, 2nd ed., Springer-Verlag Berlin Heidelberg, Germany, pp. 702-703. Wulandari, M. G. D., Friamita, R. D., dan Patramurti, C., 2006, Penetapan Kadar
Kafein Dalam Campuran Parasetamol, Salisilamida, dan Kafein secara Spektrofotometri Derivatif, www.usd.ac.id/06/publ_dosen/far/devi.pdf, diakses tanggal 25 November 2010.
Lampiran
Lampiran 2. Data beserta hasil uji presisi vernier caliper merk Mitutoyo
Kel tebal kaki rata-rata SD CV
rep. 1 rep. 2 rep. 3
I 0,282 0,284 0,28 0,282 0,002 0,007092
II 0,292 0,29 0,29 0,290667 0,001155 0,003973
III 0,286 0,286 0,286 0,286 0 0
Lampiran 3. Hasil Elusidasi Struktur Asetil Eugenol (Riswanto, 2011)
(b)
(c)
(a) Spektra infra merah senyawa asetil eugenol
(b) Spektra resonansi magnetik inti senyawa asetil eugenol
Lampiran 4. Foto asetil eugenol hasil sintesis di Laboratorium Kimia Organik Universitas Sanata Dharma Yogyakarta
(a) (b)
(c) (d)
Lampiran 5. Foto dokumentasi injeksi subplantar pada hewan uji
(a) (b)
(c) (c)
Lampiran 6. Perhitungan dosis formalin 0,5% untuk injeksi subplantar
a. Pembuatan formalin 0,5%
Formalin 100% = formaldehide 37% (v/v) dalam aquades merk Bratachem®, diperoleh dari Laboratorium Farmakologi dan Toksikologi Universitas Sanata Dharma Yogyakarta.
Pengenceran formalin
volume1 x konsentrasi1 = volume2 x konsentrasi2
volume1 x 100% = 100 ml x 0,5%
volume1 = = 0,5 ml
Jadi, diambil 0,5 ml formalin 100% kemudian diencerkan dengan aquades di dalam labu ukur sampai volume 100 ml.
b. Perhitungan dosis formalin 0,5%
Formalin 0,5% untuk menginduksi inflamasi diberikan 0,025 ml tiap 20 g BB mencit (Vogel, 2002).
Contoh perhitungan volume injeksi subplantar dengan formalin 0,5% pada hewan uji:
BB mencit = 25 g
Lampiran 7. Perhitungan dosis Cataflam® D-50 sebagai kontrol positif
a. Pembuatan larutan Cataflam® D-50
1 tablet Cataflam® D-50 digerus dan dilarutan dengan 100 ml aquades sehingga diperoleh larutan Cataflam 0,05% atau 0,5 mg/ml.
b. Perhitungan dosis Cataflam® D-50
Dosis untuk manusia 50 kg = 50 mg Dosis untuk manusia 70 kg =
Konversi dari manusia 70 kg ke mencit 20 g = 0,0026 (menurut tabel konversi Laurence dan Bacharach, 1964).
Dosis untuk mencit 20 g = 0,0026 x 70 mg = 0,182 mg
Dosis pada mencit = 9,1 x 10-3 mg/g BB mencit = 9,1 mg/kg BB mencit
c. Contoh perhitungan pemberian larutan Cataflam® D-50 pada hewan
uji
BB mencit = 25 g = 0,025 kg
Dosis Cataflam® D-50 = 9,1 mg/kg BB x 0,025 kg = 0,23 mg Volume pemberian larutan Cataflam® D-50 pada mencit
Lampiran 8. Perhitungan dosis Virgin Coconut Oil (VCO) sebagai kontrol negatif
a. Perhitungan dosis VCO
Dosis VCO untuk manusia 50 kg = 15 ml Dosis untuk manusia 70 kg =
Konversi dari manusia 70 kg ke mencit 20 g = 0,0026 (menurut tabel konversi Laurence dan Bacharach, 1964).
Dosis untuk mencit 20 g = 0,0026 x 21 ml = 0,0546 ml
Dosis pada mencit = 2,7 x 10-3 ml/g BB mencit = 2,7 ml/kg BB mencit
b. Contoh perhitungan pemberian VCO pada hewan uji
BB mencit = 25 g = 0,025 kg
Lampiran 9. Perhitungan dosis asetil eugenol
a. Pembuatan larutan asetil eugenol 6,25%
Konsentrasi tertinggi asetil eugenol dalam VCO yang dapat diberikan kepada mencit secara oral adalah 6,25% (v/v).
Pengenceran asetil eugenol:
volume1 x konsentrasi1 = volume2 x konsentrasi2
volume1 x 100% = 8 ml x 6,25%
volume1 = = 0,5 ml
Jadi, diambil 0,5 ml asetil eugenol 100% kemudian diencerkan dengan aquades di dalam tabung ukur sampai volume 8 ml.
b. Perhitungan dosis asetil eugenol secara oral
Range bobot mencit yang digunakan dalam penelitian = 20-30 gram. Digunakan bobot 30 gram dan volume pemberian setengah dari volume maksimal pemberian obat secara oral pada mencit untuk mencari dosis asetil eugenol secara oral pada mencit.
Perhitungan dosis asetil eugenol:
dosis x berat badan = konsentrasi x volume pemberian dosis x 30 g = 0,0625 ml/ml x 0,5 ml
dosis asetil eugenol = = 1,042 x 10-3 ml/g BB mencit = 1,042 ml/kg BB mencit, ditetapkan sebagai dosis III
dosis I = 0,260 ml/kg BB mencit Rumus umum volume pemberian =
Contoh perhitungan volume pemberian pada hewan uji dengan bobot 25 g: dosis I (0,260 ml/kg BB mencit)
= 0,10 ml dosis II (0,521 ml/kg BB mencit)
= 0,21 ml dosis III (1,042 ml/kg BB mencit)
60
61 eugenol
dosis 1,042 ml/kg BB
0,06 0,07 0,06 0,03 0,06 0,06 0,03 0,065 0,065 0,045 0,045 0,06 0,31 0,01 0,01 0,02 0,01 0 0 0,005 0,01 0,015 0,015 0,005 0 0,05 0,03 0,05 0,03 0,04 0,04 0,03 0,015 0,04 0,04 0,035 0,04 0,035 0,205 0,07 0,08 0,09 0,08 0,05 0,06 0,035 0,075 0,085 0,085 0,065 0,055 0,4
62
positif kalium diklofenak (Cataflam® D-50)
Mencit Kelompok
X = rata-rata AUC kontrol negatif
Contoh cara perhitungan % penghambatan inflamasi: Kelompok asetil eugenol dosis 0,260 ml/kg BB no.1
Lampiran 12. Hasil ANOVA pola satu arah dengan taraf kepercayaan 95% % penghambatan inflamasi dengan pemberian asetil eugenol dosis 0,260 ml/kg BB; 0,521 ml/kg BB ; dan 1,042 ml/kg BB
Normal Parametersa,b Mean 44,3264
Std. Deviation 26,95712
Most Extreme Differences Absolute ,189
Positive ,101
Negative -,189
Kolmogorov-Smirnov Z ,946
Asymp. Sig. (2-tailed) ,332
64
Oneway
Descriptives
PersenPenghambatanInflamasi
N Mean Std. Deviation Std. Error
95% Confidence Interval for Mean
Minimum Maximum
Lower Bound Upper Bound
Cataflam 5 59,4560 6,33921 2,83498 51,5848 67,3271 48,19 63,08
VCO 5 ,0000 13,65951 6,10872 -16,9605 16,9605 -19,17 13,21
Asetil260,5 5 39,3782 9,73228 4,35241 27,2940 51,4625 27,46 52,72
Asetil521 5 52,9793 8,35216 3,73520 42,6087 63,3499 44,95 65,03
Asetil1042 5 69,8187 17,03503 7,61830 48,6669 90,9704 48,19 93,52
Total 25 44,3264 26,95712 5,39142 33,1991 55,4538 -19,17 93,52
ANOVA
PersenPenghambatanInflamasi
Sum of Squares df Mean Square F Sig.
Between Groups 14714,724 4 3678,681 26,992 ,000
Within Groups 2725,744 20 136,287
65
Post Hoc Tests
Multiple Comparisons
PersenPenghambatanInflamasi Scheffe
(I) VAR00001 (J) VAR00001 Mean Difference
(I-J) Std. Error Sig.
95% Confidence Interval
Lower Bound Upper Bound
dime
Asetil260,5 20,07772 7,38342 ,159 -4,9218 45,0772
Asetil521 6,47668 7,38342 ,940 -18,5228 31,4762
Asetil1042 -10,36269 7,38342 ,741 -35,3622 14,6368
VCO
dimension3
Cataflam -59,45596* 7,38342 ,000 -84,4555 -34,4564
Asetil260,5 -39,37824* 7,38342 ,001 -64,3778 -14,3787
Asetil521 -52,97927* 7,38342 ,000 -77,9788 -27,9797
Asetil1042 -69,81865* 7,38342 ,000 -94,8182 -44,8191
Asetil260,5
dimension3
Cataflam -20,07772 7,38342 ,159 -45,0772 4,9218
VCO 39,37824* 7,38342 ,001 14,3787 64,3778
Asetil521 -13,60104 7,38342 ,511 -38,6006 11,3985
Asetil1042 -30,44041* 7,38342 ,012 -55,4399 -5,4409
Asetil521
dimension3
Cataflam -6,47668 7,38342 ,940 -31,4762 18,5228
VCO 52,97927* 7,38342 ,000 27,9797 77,9788
Asetil260,5 13,60104 7,38342 ,511 -11,3985 38,6006
66
Asetil1042
dimension3
Cataflam 10,36269 7,38342 ,741 -14,6368 35,3622
VCO 69,81865* 7,38342 ,000 44,8191 94,8182
Asetil260,5 30,44041* 7,38342 ,012 5,4409 55,4399
Asetil521 16,83938 7,38342 ,304 -8,1601 41,8389
*. The mean difference is significant at the 0.05 level.
Homogeneous Subsets
67
Lampiran 13. Hasil General Linear Model (GLM) repeated measures dengan taraf kepercayaan 95% AUC edema kaki mencit dengan pemberian asetil eugenol dosis 0,260 ml/kg BB; 0,521 ml/kg BB ; dan 1,042 ml/kg BB beserta kontrol
General Linear Model
Mauchly's Test of Sphericityb
Measure:MEASURE_1
Within Subjects Effect
Mauchly's W
Approx.
Chi-Square df Sig.
Epsilona
Greenhouse-Geisser Huynh-Feldt Lower-bound
dimension1 factor1 ,300 21,799 14 ,085 ,729 1,000 ,200
69
b. The statistic is an upper bound on F that yields a lower bound on the significance level. c. Design: Intercept + VAR00001
Within Subjects Design: factor1
70
Tests of Within-Subjects Effects
Measure:MEASURE_1
Source Type III Sum of
Squares df Mean Square F Sig.
factor1 Sphericity Assumed ,004 5 ,001 3,634 ,005
Greenhouse-Geisser ,004 3,645 ,001 3,634 ,011
Huynh-Feldt ,004 5,000 ,001 3,634 ,005
Lower-bound ,004 1,000 ,004 3,634 ,071
factor1 * VAR00001 Sphericity Assumed ,012 20 ,001 2,418 ,002
Greenhouse-Geisser ,012 14,579 ,001 2,418 ,007
Huynh-Feldt ,012 20,000 ,001 2,418 ,002
Lower-bound ,012 4,000 ,003 2,418 ,082
Error(factor1) Sphericity Assumed ,024 100 ,000
Greenhouse-Geisser ,024 72,895 ,000
Huynh-Feldt ,024 100,000 ,000
71
Tests of Within-Subjects Contrasts
Measure:MEASURE_1
Source factor1 Type III Sum of
Squares df Mean Square F Sig.
factor1 Linear ,000 1 ,000 ,343 ,565
Quadratic ,004 1 ,004 14,038 ,001
Cubic ,000 1 ,000 ,988 ,332
Order 4 1,286E-6 1 1,286E-6 ,005 ,942
Order 5 1,157E-5 1 1,157E-5 ,080 ,780
factor1 * VAR00001 Linear ,004 4 ,001 2,776 ,055
Quadratic ,005 4 ,001 4,334 ,011
Cubic ,001 4 ,000 ,988 ,437
Order 4 ,002 4 ,000 1,684 ,193
Order 5 ,001 4 ,000 1,159 ,358
Error(factor1) Linear ,006 20 ,000
Quadratic ,006 20 ,000
Cubic ,004 20 ,000
Order 4 ,005 20 ,000