BAB III
METODE PENELITIAN
A.Jenis Penelitian
Jenis penelitian yang dilakukan adalah penelitian deskriptif. Penelitian deskriptif adalah penelitian yang mendeskripsikan suatu gambaran yang sistematis dengan fakta-fakta yang didapatkan (Nazir, 1988).
B. Populasi dan Sampel
1. Populasi yang digunakan dalam penelitian ini adalah 30 individu ikan Gurame (Osphronemus gouramy) yang diambil dari kota Tasikmalaya dan Sukabumi 2. Sampel yang digunakan adalah DNA genome ikan gurame (Osphronemus
gouramy)
3. Sequence gen MC1R dari Ordo Perciformes yang diperoleh dari GenBank NCBI. Daftar species ikan dari Ordo Perciformes yang digunakan sebagaimana dipaparkan pada Tabel 3.1
C. Waktu dan Lokasi Penelitian
Penelitian ini dimulai pada bulan Januari 2015 sampai dengan September 2015 yang dilaksanakan di Laboratorium Mikrobiologi Gedung JICA FPMIPA A dan Laboratorium Bioteknologi Departemen Pendidikan Biologi Gedung FPMIPA B Universitas Pendidikan Indonesia, Jalan Dr. Setiabudhi No.299 Bandung.
D.Alat dan Bahan
Alat dan bahan yang digunakan dalam penelitian ini terdapat pada Laboratorium Mikrobiologi Departemen Pendidikan Biologi FPMIPA UPI. Daftar alat dan bahan terlampir dalam Lampiran 1.
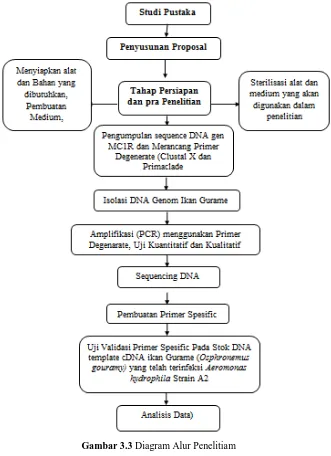
E.Alur Penelitian dan Langkah Kerja
1. Tahap Persiapan
Tahap persiapan meliputi persiapan alat dan bahan yang akan dilakukan dalam proses penelitian. Alat-alat yang bersih dan bahan yang digunakan, dibungkus menggunakan plastik tahan panas dan disterilisasi menggunakan autoclave selama 15-20 menit pada suhu 121ºC dengan tekanan. Alat dan bahan yang digunakan terlampir pada Lampiran 1. Kegiatan penelitian di lakukan Laboratorium Mikrobiologi Departemen Pendidikan Biologi FPMIPA UPI.
2. Tahap Penelitian
a. Mengumpulkan sequence gen MC1R dari berbagai jenis ikan Infraclassis
Teleostei
Primer dibuat dengan menganalisa sequence gen MC1R dari GenBank (http://www.ncbi.nlm.nih.gov/). Sequence gen yang dibuat primernya berasal dari gen MC1R Infraclassis Teleostei, Ordo Perciformes yang tertera pada Tabel 3.1 syarat pembuatan primer dari sequence sekerabat sebanyak minimal lima spesies. Pada penelitian ini total jumlah species yang digunakan sebanyak 11 species. Sequence DNA dikumpulkan dengan format FASTA umtuk multiple alignment
(pensejajaran banyak sequence) dengan menggunakan aplikasi software Clustal X.
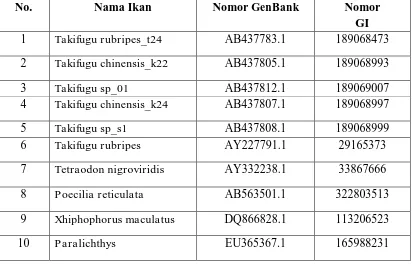
Tabel 3.1 Daftar species ikan Ordo Perciformes untuk desain Primer Degenerate
No. Nama Ikan Nomor GenBank Nomor
GI
1 Takifugu rubripes_t24 AB437783.1 189068473
2 Takifugu chinensis_k22 AB437805.1 189068993
3 Takifugu sp_01 AB437812.1 189069007
4 Takifugu chinensis_k24 AB437807.1 189068997
5 Takifugu sp_s1 AB437808.1 189068999
6 Takifugu rubripes AY227791.1 29165373
7 Tetraodon nigroviridis AY332238.1 33867666
8 Poecilia reticulata AB563501.1 322803513
9 Xhiphophorus maculatus DQ866828.1 113206523
11 Dicentrarchus FN377856.1 270377196
b. Desain Pasanngan Primer Degenerate Gen MC1R
Hasil pensejajaran kemudian dibuat pasangan primer degeneratenya dengan mengakses laman Primaclade (http://primaclade.org/cgi-bin/primaclade.cgi). Hasil amplikon diperkirakan 400-800 bp. Didapatkan beberapa kandidat primer yang terdapat pada Bab 4 Hasil dan Pembahasan (Tabel 4.2).
c. Isolasi DNA Genome Ikan Gurame (Osphronemus gouramy)
1. Isolasi DNA Kromosom
Isolasi DNA genome ikan gurame dari 30 jenis ikan gurame di daerah Sukabumi dan Tasikmalaya menggunakan metode lisis CTAB 2x. Daging atau jaringan ikan gurame dengan ukuran luas 1 cm2 yang sudah dihancurkan dimasukan ke dalam larutan 500 µl buffer lysis CTAB (Buffer (-) CTAB + SDS10% + CTAB perbandingan (0,7:0,3:0,1, pH 8,0) pada tabung eppendorf, ditambahkan 7 µl SDS 20% dan β-mercaptoetanol, dihomogenasi sehingga larut dan merata, lalu tabung diinkubasi pada suhu 60°C selama satu jam, setelah inkubasi ditambahkan 10 µl Proteinase K (10mg/ml) kemudian diinkubasi selama 12-15 jam pada suhu 65°C. Proses sebelumnya dilanjutkan dengan inkubasi lalu Potassium Asetat 5 M sebanyak 1/10 volume awal ditambahkan ke dalam tabung, dihomogenkan dan diinkubasi di dalam freezer pada suhu 20°C selama 20 menit. Tabung yang sudah diinkubasi, disentrifugasi dengan kecepatan 15.000 rpm selama 10 menit, setelah disentrifugasi terbentuk 2 lapisan, lapisan supernatan dan protein.
kloroform. Lapisan pertama dipindahkan pada tabung eppendorf baru, lalu ditambahkan sodium asetat 3M sebanyak 1/10 x volume total pada tabung baru tersebut, lalu dihomogenkan.
Ethanol absolute yang dingin sebanyak 2x volume total ditambahkan,
kemudian dihomogenkan hingga terlihat putih awan, setelah itu diinkubasi pada suhu -20°C selama satu malam. Pada keesokan setelah proses inkubasi, akan dilanjutkan dengan sentrifugasi larutan pada 15000 rpm selama 10 menit, sehingga terdapat pelet berwarna putih yang mengandung DNA, ethanol dibuang secara hati-hati, setelah itu dibilas menggunakan alkohol 70% sebanyak 1 x volume total, lalu alkohol dibuang kembali. Pelet dikeringkan di dalam oven selama kurang lebih 15 menit, setelah kering dilarutkan ke dalam Buffer TE (10 mM Tris/1mM EDTA) larutan tersebut adalah larutan stok DNA simpan pada suhu -20°C. DNA genome yang sudah diisolasi dicampurkan dalam 1 tabung, masing-masing diambil 1µl menjadi 1 tabung mikrotube. DNA bulk atau Mix DNA dan akan menghasilkan konsentrasi yang sesuai diinginkan (Karsinah et al., 2002). Proses ini merupakan tahapan yang dilakukan pada koleksi penelitian sebelumnya (Kusumawaty, Tahun, belum dipublikasikan).
2. Pengukuran Konsentrasi DNA
Pengukuran konsentrasi DNA dengan metode spektrofotometri. DNA murni dapat menyerap cahaya UV karena adanya basa purin dan pirimidin. Pita ganda DNA dapat menyerap UV pada 260 nm, sedangkan kontaminan protein atau fenol akan menyerap cahaya pada 280 nm, sehingga kemurnian dapat diukur dengan dengan menghitung nilai absorbansi 260 nm dibagi dengan nilai absorbansi 280 nm (Å260/Å280). Rumus sebagai berikut (Fatchiyah, 2002) :
[DNA] = Å260 x 50 x faktor pengenceran
d. Amplifikasi dengan Metode PCR dan Elektroforesis
Primer degenerate yang terdapat pada Tabel 4.1, Taq DNA Polymerase, 1 µl DNA template ikan gurame (DNA stok diencerkan 20x dan 200x kemudian (diambil 1µl), dan air deion ditambahkan hingga volume 12,5µl. Bahan tersebut dimasukan ke dalam tabung khusus untuk alat Thermal cycler dengan program Gene Amplyfied PCR System 9700 (Scientific, 2011).
Pembuatan komposisi PCR dilakukan dengan keadaan dingin dengan konposisi terdapat pada Tabel 3.2 Polymerase, dan DNA template, dilakukan dengan cara divorteks (sebelum ditambahkan seluruh bahan), dan menjentik-jentik tabung dengan cepat dan hati-hati, disentrifugasi lalu dimasukan ke dalam mesin PCR, yang sudah diprogram sesuai dengan primer yang sudah dirancang. Setelah itu DNA amplifikasi di elektroforesis pada gel agarosa 1%, dengan tegangan 100 volt selama 40 menit buffer TAE 1 x (larutan buffer TAE 10x diencerkan dalam deion dengan perbandingan 1:19 (v/v) Sampel DNA dicampurkan dengan larutan Loading dye, 5:2 (v/v), sebelum dimasukan ke dalam sumur gel. Disamping sampel DNA, dimasukan marker lambda Hind III/ Eco R1 yang merupakan larutan DNA yang sudah diketahui ukurannya .gel agarosa yang sudah dielektroforesis direndam dengan pewarnaan pada larutan ethidium bromida (10 µg.ml) selama dua menit. Kemudian dibilas menggunakan aquades selama 6 menit, gel agarosa diamati pada UV transiluminator.
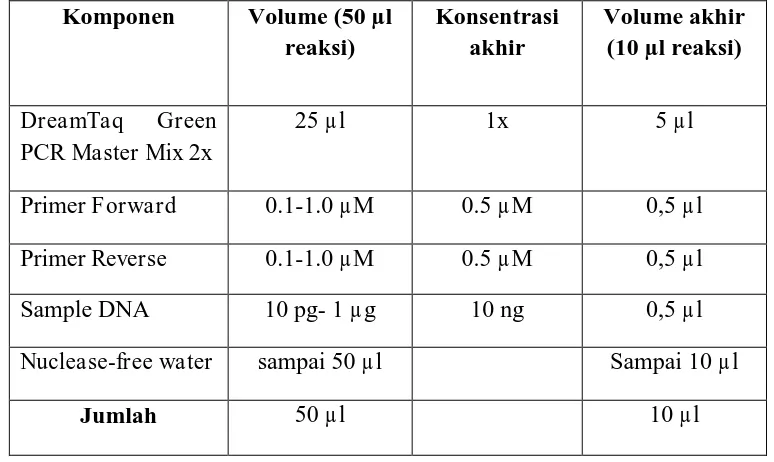
Tabel 3.2. Komposisi reaksi PCR DreamTaq Green PCR Master Mix 2x
Komponen Volume (50 µl
reaksi)
Konsentrasi akhir
Volume akhir (10 µl reaksi)
DreamTaq Green
PCR Master Mix 2x
25 µl 1x 5 µl
Primer Forward 0.1-1.0 µM 0.5 µM 0,5 µl
Primer Reverse 0.1-1.0 µM 0.5 µM 0,5 µl
Sample DNA 10 pg- 1 µg 10 ng 0,5 µl
Nuclease-free water sampai 50 µl Sampai 10 µl
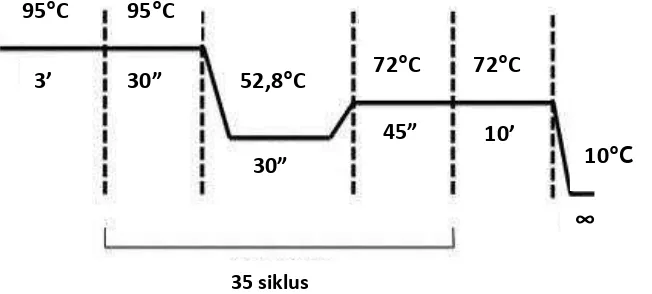
Gambar 3.1 Program PCR Primer Degenerate Non Nested
Gambar 3.2 Program PCR Primer Degenerate Nested
e. Sequencessing DNA dan Analisis Urutan Gen MC1R
Sequencessing (urutan) hasil amplifikasi dengan metode PCR 2 sampel, yaitu
sampel ikan gurame dari primer degenerate non nested dan primer degenerate nested dilakukan dengan reaksi 2 arah pasangan primer menggunakan mesin
sequencer BigDye Applied Biosystem yang tersedia pada Macrogen, Korea
(www.macrogen.com). Analisa urutan merupakan ringkasan dari seluruh metode yang sudah dilakukan untuk mengetahui basa nukleotida dan dibandingkan kesamaannya dengan urutan lainnya.
95ºC 95ºC
51,2ºC
”
’ ” 72ºC 72ºC
” ’
10ºC
∞
35 siklus
95ºC 95ºC
52,8ºC
”
’ ” 72ºC 72ºC
” ’
10ºC
∞
f. Perancangan Primer Spesifik dari Sequence Gen MC1R
Perancangan primer spesifik dilakukan dengan penjajaran hasil sequencessing gen MC1R yang didapatkan dari GenBank (www.ncbi.nih.nlm.gov), untuk mendapatkan daerah sequence yang lestari menggunakan program DNAbaser, dan Clustal X untuk mendapatkan primer forward dan reverse, primer dirancang dengan syarat primer standar.
g. Uji Validasi Primer Spesifik Stok DNA Genome Ikan Gurame
(Osphronemus gouramy) dan Stok Sampel cDNA Ikan Gurame
(Osphronemus gouramy)
Setelah perancangan primer spesifik, uji validasi primer menggunakan amplifikasi dengan metode PCR dan elektroforesis seperti sebelumnya, kepada stok DNA Genome ikan gurame dan stok cDNA ikan gurame (Osphronemus gouramy) yang telah terinfeksi Aeromonas hydrophila Strain A2 (Kusumawaty, 2014) sumber belum dipublikasikan
h. Analisis Data Bioinformatika dan Karakterisasi Pohon Filogenetik
Hasil uji penelitian deksriptif data dan dokumentasi dikumpulkan. Hasil sequencesing berupa basa nukleotida sequence diurutkan dengan cara Alignment
dan Contig menggunakan aplikasi Clustal X dan diurutkan basa nukleotida
sequence gen MC1R menggunakan aplikasi DNABaser. Sequence yang sudah