5 BAB II
TINJAUAN PUSTAKA
2.1Uraian Tumbuhan
Uraian tumbuhan meliputi daerah tumbuh, nama daerah, nama asing, morfologi tumbuhan, sistematika tumbuhan, kandungan kimia dan kegunaan dari tumbuhan. 2.1.1 Habitat
Kitolod (Hippobroma longiflora (L.) G. Don) merupakan tanaman yang berasal dari Hindia Barat tumbuh liar di pinggir saluran air atau sungai, serta tempat yang lembab dan terbuka (Yohana, et. al., 2005).
2.1.2 Nama daerah
Menurut Hariana (2007) kitolod (Hippobroma longiflora (L.) G. Don) memiliki nama daerah:
Sunda : Daun tolod Jawa : Daun kendali Melayu : Lidah payau 2.1.3 Nama asing
Belanda : ster ven bethlehem (Hariana, 2007), Inggris : star of bethelem (Ali, 2003). China : Ma zui cao
Hawaiian : pua hōkū
Prancis : etoile de Bethléem 2.1.4 Morfologi tumbuhan
6
di tempat terbuka dengan tinggi dapat mencapai 50 cm, bercabang dari pangkal batang, batangnya bulat, helaian daun berwarna hijau, bergerigi sampai melekuk, merupakan daun tunggal, lebar daun 2 - 3 cm, panjang 5 - 15 cm, bunga tunggal, tegak, bertangkai panjang, keluar dari ketiak daun, mahkota bunga menyerupai bintang, berwarna putih, buah berbentuk lonceng,berwarna hijau dan merunduk, biji bulat telur, berukuran kecil, berwarna putih, akar tanaman merupakan akar tunggang (Nuraini, 2014).
2.1.5 Sistematika tumbuhan
Menurut Plantamor (2008) kitolod (Hippobroma longiflora (L.) G. Don) diklasifikasikan sebagai berikut:
Kingdom : Plantae
Divisio : Spermatophyta Subdivisio : Angiospermae Kelas : Dicotyledoneae Bangsa : Asterales Suku : Campanulaceae Marga : Hippobroma
Jenis : Hippobroma longiflora (L.) G. Don 2.1.6 Kandungan kimia
Kitolod (Hippobroma longiflora (L.) G. Don) mengandung senyawa kimia seperti alkaloida, saponin, flavonoida dan polifenol (Murtie, 2013).
2.1.7 Kegunaan
7
seperti mata berair, mata plus, minus, katarak, glaukoma (Nuraini, 2014), epilepsi (Ira, et. al., 2009).
2.2 Uraian Kandungan Kimia Tumbuhan 2.2.1 Alkaloida
Alkaloida adalah suatu golongan senyawa sekunder yang terbanyak ditemukan di dalam dunia tumbuhan. Alkaloida tersebar luas dalam berbagai familia tumbuhan. Semua alkaloida mengandung paling sedikit satu atom nitrogen sehingga bersifat basa dan pada sebagian besar alkaloida atom nitrogen ini merupakan bagian dari cincin heterosiklik (Lenny, 2006). Menurut Harborne, alkaloida adalah senyawa bersifat basa yang mengandung satu atau lebih atom nitrogen yang terletak dalam sistem siklik. Di samping itu alkaloida dapat didefinisikan sebagai suatu senyawa yang mengandung nitrogen, dan bersifat basa, terdapat pada tumbuhan dalam jumlah yang relatif kecil dan mempunyai aktivitas farmakologi. Selain unsur nitrogen, alkaloida juga mengandung oksigen dan sulfur (Hanafi, 2012).
Sifat alkaloida yang paling umum adalah bersifat basa, kebasaan dari alkaloida ini bergantung pada ketersediaan pasangan elektron sunyi dari atom N untuk disumbangkan membentuk ikatan kovalen koordinasi (Cordell, 1981). Bila gugus fungsi yang berdekatan dengan nitrogen bersifat sebagai penolak elektron, seperti gugus alkil, maka ketersediaan elektron disekitar nitrogen akan bertambah, mengakibatkan alkaloida bersifat lebih basa, sebaliknya bila gugus fungsi yang melekat pada nitrogen bersifat sebagai penarik elektron, seperti gugus karbonil maka ketersediaan elektron disekitar nitrogen akan berkurang, mengakibatkan alkaloida bersifat netral bahkan sedikit bersifat asam (Lenny, 2006).
8
sehingga alkaloida dapat terurai oleh pengaruh oksigen, panas, cahaya dan terhadap metode yang sesuai dipakai untuk isolasi. Penguraian alkaloida selama atau setelah isolasi dapat menjadi masalah yang serius jika disimpan dalam waktu lama. Pembentukan garam dengan asam organik seperti tartrat, sitrat atau asam anorganik seperti asam klorida, asam sulfat dapat mengurangi penguraian alkaloida (Cordell, 1981). Fungsi alkaloida dalam tumbuhan belum diketahui secara pasti, kemungkinan berfungsi sebagai penarik atau penghalau serangga, ataupun dapat bersifat sebagai zat pengatur tumbuh. (Harborne, 1987). Klasifikassi alkaloida menurut Hegnauer (Farnsworth, 1966) adalah sebagai berikut:
1. Alkaloida Sejati
Alkaloida ini dibentuk atau berasal dari asam amino yang umumnya mempunyai unsur nitrogen yang terikat pada cincin heterosiklik dan kebanyakan bersifat basa seperti vinkristin dan reserpin, kecuali kolkisin yang tidak mempunyai cincin heterosiklik dan tidak bersifat basa.
2. Protoalkaloida
Alkaloida ini dibentuk dari asam amino, tetapi unsur nitrogennya tidak terikat pada cincin heterosiklik dan bersifat basa. Contohnya meskalin dan efedrin.
3. Pseudoalkaloida
Alkaloid ini merupakan alkaloida bukan turunan asam amino, pada umumnya mempunyai unsur nitrogen yang terikat pada cincin heterosiklik dan biasanya bersifat basa. Alkaloida yang penting dari golongan ini adalah alkaloida golongan purina seperti kafein.
9
A. Non heterosiklik atau atipikal alkaloida, disebut juga protoalkaloida atau amin biologis misalnya efedrin yang terdapat dalam Ephedradistachya. B. Heterosiklik atau tipikal alkaloida yang dibagi ke dalam 12 grup berdasarkan struktur cincinnya, yaitu: 1. Alkaloida golongan pirol dan pirolidin:
Contohnya, golongan pirol yaitu stakidrin pada tumbuhan Stachys tuberifera dan golongan pirolidin yaitu higrin pada tumbuhan Erythroxylon coca.
H N
Gambar 2.1 Struktur pirol
H N
Gambar 2.2 Struktur pirolidin
Gambar 2.3 Struktur stakidrin
N CH3
H2
C C CH3
O
10
2. Alkaloida golongan pirolizidin: Contohnya, retronesin pada Crotalaria retus.
N
Gambar 2.5 Struktur pirolizidin
N HO
OH
H
Gambar 2.6 Struktur retronesin 3. Alkaloida golongan piridin dan piperidin:
Contohnya, golongan piridin yaitu nikotin pada tumbuhan Nicotiana tobacum dan golongan piperidin yaitu koniin pada tumbuhan Coninummaculatum.
N
Gambar 2.7 Struktur piridin H
N
11
Gambar 2.9 Struktur nikotin
N
H CH2 H2 C
CH3
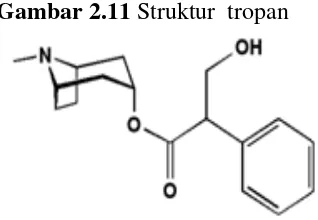
Gambar 2.10 Struktur koniin 4. Alkaloida golongan tropan:
Contohnya, atropin pada tumbuhan Atropabelladonna.
Gambar 2.11 Struktur tropan
Gambar 2.12 Struktur atropin
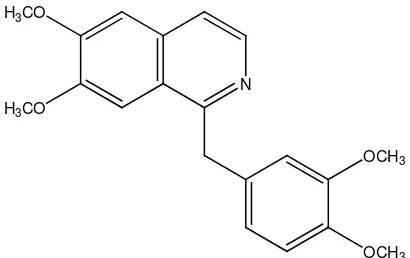
5. Alkaloida isokuinolin:
Contohnya, papaverin pada tumbuhan Papaversomniferum.
N
12
N H3CO
H3CO
OCH3
OCH3
Gambar 2.14 Struktur papaverin 6. Alkaloida golongan kuinolizidin:
Contohnya, sitisin pada tumbuhan Cytisus scoparius.
N
Gambar 2.15 Struktur kuinolizidin
N H
H NH
O
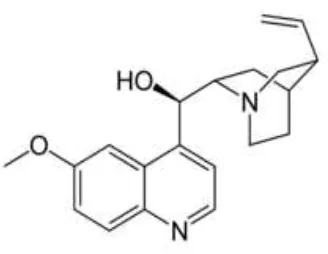
Gambar 2.16 Struktur sitisin 7. Alkaloida golongan kuinolin:
Contohnya, kinin pada tumbuhan Cinchona ledgeriana.
N
13
Gambar 2.18 Struktur kinin 8. Alkaloida golongan aporfin:
Contohnya, morfin pada tumbuhan Papaver somniferum
N
Gambar 2.19 Struktur aporfin
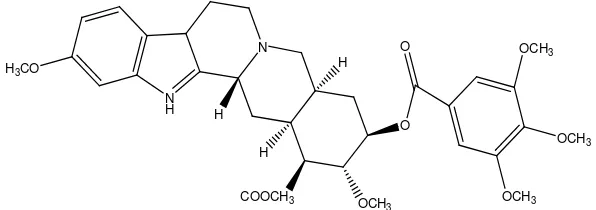
Gambar 2.20 Struktur morfin 9. Alkaloida golongan indol:
Contohnya, reserpin pada tumbuhan Rauwolfia serpentin.
H N
14 10. Alkaloida golongan imidazol:
Contohnya, pilokarpin pada tumbuhan Pilocarpusjaborandi.
11.Alkaloida golongan purin:
15
N
N N
N O
O
Gambar 2.26 Struktur kafein 12.Alkaloida golongan steroid:
Contohnya, solanidin pada tumbuhan Solanum tuberosum.
Gambar 2.27 Struktur steroid
N
HO
CH3
CH3 H3C
CH3
Gambar 2.28 Struktur solanidin 2.3 Ekstraksi
16
atsiri, alkaloida, flavonoida dan lain-lain. Diketahuinya senyawa aktif yang dikandung simplisia akan mempermudah pemilihan dalam pelarut dan cara ekstraksi yang tepat, metode ekstraksi dengan menggunakan pelarut (Depkes RI, 2000).
A. Cara dingin 1. Maserasi
Maserasi adalah proses penyarian simplisia dengan cara perendaman menggunakan pelarut dengan sesekali pengadukan pada temperatur kamar. Maserasi yang dilakukan pengadukan secara terus menerus disebut maserasi kinetik, sedangkan dilakukan pengulangan penambahan pelarut telah dilakukan penyaringan terhadap maserat pertama dan seterusnya disebut remaserasi.
2. Perkolasi
Perkolasi adalah proses penyarian simplisia dengan pelarut yang selalu baru sampai terjadi penyarian sempurna yang umumnya dilakukan pada temperatur kamar. Proses perkolasi terdiri dari tahap pelembaban bahan, tahap perendaman antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak) terus menerus sampai diperoleh perkolat yang jumlahnya 1 - 5 kali jumlah bahan yang diekstraksi. B. Cara panas
1. Refluks
Refluks adalah proses penyarian simplisia dengan menggunakan alat pada temperatur titik didihnya, selama waktu tertentu, jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik.
2. Digesti
17 40-50oC.
3. Sokletasi
Sokletasi adalah proses penyarian dengan menggunakan pelarut yang selalu baru, dilakukan menggunakan alat soklet sehingga terjadi ekstraksi kontinu dengan pelarut relatif konstan dengan adanya pendingin balik.
4. Infundasi
Infundasi adalah proses penyarian dengan menggunakan pelarut air yang padapada temperatur 90oC selama 15 menit. Hasilnya disebut infus (infusum). 5. Dekoktasi
Dekoktasi adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90oC selama 30 menit. Hasilnya disebut dekok (dekoktum).
2.4 Metode Pengocokan Asam Basa
Diketahui bahwa beberapa golongan senyawa tertentu, seperti asam dan basa, yang terdapat di dalam suatu sampel dapat diekstraksi menggunakan cara yang telah disesuaikan. Golongan bahan alam yang diekstraksi dengan cara ini adalah alkaloida, yang banyak terdapat dalam tumbuhan sebagai garam. Uraian mengenai cara ekstraksi senyawa pokok ini adalah sebagai berikut.
a. Alkaloida dapat diperoleh dari garamnya dengan cara membasakan serbuk kering bahan tanaman dengan menggunakan amonia encer. Alkaloida akan terdapat dalam bentuk basa bebas yang tak lagi berupa garam ionik dan lebih larut dalam pelarut organik seperti kloroform.
18
yang tak bercampur (immiscible).
c. Larutan kloroform akan mengandung basa bebas, yang kemudian diekstraksi dengan asam encer, misalnya diekstraksi tiga kali dengan asam klorida 2N dan alkaloida ini akan pindah dari fase organik ke fase berair sebagai garam klorida. Lapisan kloroform yang tersisa dapat diuji dengan reaksi warna khusus untuk alkaloida (reagen Dragendorff) untuk memastikan bahwa semua alkaloida telah ditransfer kelapisan cairan asam.
d. Lapisan asam dibasakan kembali dengan ammonia menghasilkan pengendapan alkaloida, kemudian diekstraksi kembali dengan pelarut organik (Heinrich et al.,2005).
2.5 Cara Umum Isolasi Senyawa Kimia dari Tumbuhan
Isolasi senyawa kimia dari bahan alam adalah suatu usaha untuk memisahkan senyawa yang bercampur sehingga diperoleh senyawa tunggal. Isolasi senyawa kimia ini banyak dilakukan dengan kromatografi (Robinson, 1995).
Kromatografi adalah suatu metode pemisahan berdasarkan proses migrasi dari komponen-komponen senyawa di antara dua fase yaitu fase diam (dapat berupa zat cair atau zat padat) dan fase gerak (dapat berupa gas atau zat cair). Fase gerak membawa zat terlarut melalui media sehingga terpisah dari zat terlarut lainnya yang terelusi lebih awal atau lebih akhir. Umumnya zat terlarut dibawa melewati media pemisah oleh aliran suatu pelarut berbentuk cairan atau gas yang disebut eluen. Fase diam dapat bertindak melarutkan zat terlarut sehingga terjadi partisi antara fase diam dan fase gerak. Proses ini suatu lapisan cairan pada penyangga yang inert berfungsi sebagai fase diam (Depkes RI, 1995).
19
diam yang dapat berupa zat padat atau zat cair. Fase diam berupa zat padat maka cara tersebut dikenal sebagai kromatografi serapan, sedangkan yang berupa zat cair maka dikenal sebagai kromatografi partisi (Depkes RI, 1995; Sastrohamidjojo, 1985).
Pemisahan dan pemurnian kandungan kimia tumbuhan terutama dilakukan dengan menggunakan salah satu dari lima teknik kromatografi atau gabungan teknik tersebut. Kelima teknik kromatografi itu adalah: kromatografi kolom (KK), kromatografi kertas (KKt), kromatografi lapis tipis (KLT), kromatografi gas cair (KGC), dan kromatografi cair kinerja tinggi (KCKT). Pemilihan teknik kromatografi bergantung pada sifat kelarutan senyawa yang akan dipisah (Harborne, 1987).
2.5.1 Kromatografi lapis tipis
Kromatografi lapis tipis merupakan metode pemisahan campuran analit dengan mengembangkan analit melalui suatu lempeng kromatografi lalu melihat komponen atau analit yang terpisah dengan penyemprotan atau pewarnaan (Gandjar dan Rohman, 2012).
Fase diam yang terdiri atas bahan berbutir-butir dilapiskan pada penyangga berupa plat, gelas, logam atau lapisan yang cocok. Campuran yang akan dipisah, berupa larutan ditotolkan berupa bercak ataupun pita, setelah itu plat atau lapisan dimasukkan ke dalam bejana tertutup rapat yang berisi larutan pengembang yang cocok (fase gerak), pemisahan terjadi selama pengembangan, selanjutnya senyawa yang tidak berwarna harus ditampakkan (Stahl, 1985).
20
panjang (366 nm). Senyawa tidak dapat dideteksi maka harus disemprot dengan pereaksi yang membuat bercak tersebut tampak yaitu pertama tanpa pemanasan, kemudian bila perlu dengan pemanasan (Gritter, et al., 1991; Stahl, 1985). Kromatografi lapis tipis dapat dipakai untuk dua tujuan yaitu:
1. Metode untuk mencapai hasil kualitatif (analitik) dan kuantitatif (preparatif). 2. Mencari sistem pelarut yang akan dipakai dalam kromatografi kolom (Gritter, et
al., 1991; Stahl, 1985).
a. Fase diam (lapisan penyerap)
Pada kromatografi lapis tipis pada fase diam berupa lapisan tipis yang terdiri bahan padat yang dilapiskan pada permukaan penyangga datar yang biasanya terbuat dari kaca atau logam. Lapisan fase diam melekat pada permukaan dengan bantuan bahan pengikat. Beberapa contoh fase diam yang digunakan untuk pemisahan dalam kromatografi lapis tipis yaitu silika gel, alumina, kieselguhr dan selulosa. Kromatografi lapis tipis lapisan fase diam harus sesedikit mungkin mengandung air, karena air akan menempati semua titik penyerapan sehingga tidak akan ada senyawa yang melekat, maka sebelum digunakan plat kromatografi lapis tipis perlu diaktifkan dengan pemanasan pada 110oC selama 30 menit (Gritter, et al., 1991).
b. Fase gerak (pelarut pengembang)
Fase gerak ialah medium angkut yang terdiri dari satu atau campuran pelarut, jika diperlukan sistem pelarut multi komponen, harus berupa suatu campuran sesederhana mungkin yang terdiri atas tiga komponen (Stahl, 1985).
21
memperhatikan polaritasnya (Gandjar dan Rohman, 2012).
Hal ini sepasang pelarut atau lebih yang dapat saling melarutkan akan memisah menjadi menjadi dua lapisan. Hal ini lazim terjadi pada dua pelarut yang sangat berbeda kepolarannya dicampur sehingga dapat dilihat berupa bercak berbentuk bulan setengah, bukan bentuk yang bundar atau lonjong ((Gritter, et al., 1991).
c. Harga Rf
Jarak pengembangan senyawa pada kromatogram biasanya dinyatakan dengan harga Rf (Retardation Factor = faktor penghambatan) (Stahl, 1985).
Rf= Jarak titik pusat bercak dari titik awal Jarak garis depan pelarut dari titik awal
Jarak yang ditempuh oleh tiap bercak dari titik penotolan diukur dari pusat bercak. Harga Rf berada antara 0,00 – 1,00. Harga Rf ini sangat berguna untuk mengidentifikasi suatu senyawa (Eaton, 1989).
Faktor-faktor yang mempengaruhi harga Rf adalah sebagai berikut (Sastrohamidjojo, 1985):
a. struktur kimia dari senyawa yang sedang dipisahkan b. bersifat penyerap
c. tebal dan kerataan lapisan penyerap d. jenis pelarut dan derajat kemurniannya
22 g. jumlah cuplikan yang digunakan
h. suhu
i. kesetimbangan
2.5.2 Kromatografi lapis tipis preparatif
Metode pemisahan senyawa bahan alam yang memakai peralatan yang paling dasar merupakan kromatografi lapis tipis (KLT) preparatif. Ketebalan penyerap yang sering dipakai adalah 0,5 - 2 mm, ukuran plat kromatografi biasanya 20 x 20 cm atau 20 x 40 cm. Ketebalan lapisan yang terbatas dan ukuran plat sudah tentu mengurangi jumlah bahan yang dapat dipisahkan dengan KLT preparatif. KLT preparatif dapat memisahkan bahan alam dalam jumlah gram, sebagian besar pemakaian hanya dalam jumlah milligram. Penjerap yang paling umum digunakan adalah silika gel dan dipakai untuk pemisahan senyawa lipofil maupun campuran senyawa hidrofil. Pemilihan pelarut ditentukan berdasarkan pemeriksaan pendahuluan memakai KLT analitik (Hostettmann, et al., 1995).
23 a. menyemprot dengan air (misalnya saponin).
b. menutup plat dengan sepotong kaca,lalu menyemprot salah satu sisi menggunakan pereaksi semprot.
c. menambahkan senyawa pembanding
2.5.3 Kromatografi lapis tipis dua arah (two-dimensional TLC)
KLT dua arah atau KLT dua dimensi ini bertujuan untuk meningkatkan resolusi sampel ketika komponen-komponen solut mempunyai karakteristik kimia yang hampir sama, karena nilai Rf juga hampir sama. Dua sistem fase gerak yang berbeda dapat digunakan secara berurutan pada suatu campuran tertentu sehingga memungkinkan untuk melakukan pemisahan analit yang mempunyai tingkat polaritas yang hampir sama maka KLT dua dimensi dapat dipakai untuk memeriksa kemurnian isolat. KLT dua dimensi dilakukan dengan melakukan penotolan sampel di salah satu sudut lapisan lempeng tipis dan mengembangkannya sebagaimana biasa dengan fase gerak pertama. Lempeng kromatografi selanjutnya dikeluarkan dari
chamber pengembang dan fase gerak dibiarkan menguap dari lempeng. Lempeng
dimasukkan ke dalam chamber yang menggunakan fase gerak kedua sehingga pengembangan dapat terjadi pada arah kedua yang tegak lurus dengan arah pengembangan yang pertama. Pemisahan tergantung pada kemampuan untuk memodifikasi selektifitas eluen pertama (Rohman, 2009).
2.6 Spektrofotometri
2.6.1 Spektrofotometri sinar ultraviolet
24
molekul dalam daerah spektrum ultraviolet sangat tergantung pada struktur elektronik dari molekul yang bersangkutan (Sastrohamidjojo, 1985).
Penyerapan radiasi UV terjadi melalui eksitasi elektron dalam suatu molekul obat ke level energi yang lebih tinggi. Transisi ini terjadi dari tingkat elektronik dasar suatu molekul ke salah satu level dalam keadaan elektronik tereksitasi (Gandjar dan Rohman, 2012). Tipe eksitasi tergantung pada panjang gelombang yang diserap cahaya. Gugus yang dapat mengabsorpsi cahaya sinar ultraviolet disebut gugus kromofor (Dachriyanus, 2004).
Pelarut yang banyak digunakan untuk spektrofotometri sinar UV adalah etanol 95% karena kebanyakan golongan senyawa larut dalam pelarut tersebut dan etanol tidak menyerap sinar UV. Pelarut lain yang digunakan adalah air, metanol, n-heksana, eter minyak bumi dan eter. Konsentrasi dari analit di dalam larutan bisa ditentukan dengan cara mengukur absorbansi pada panjang gelombang tertentu dengan menggunakan hukum Lambert - Beer (Gandjar dan Rohman, 2007; Harborne, 1987).
Spektrofotometer UV pada umumnya digunakan untuk:
1. menentukan jenis kromofor, ikatan rangkap yang terkonjugasi dan ausokrom dari suatu senyawa organik.
2. menjelaskan informasi dari struktur berdasarkan panjang gelombangnya. (Dachriyanus, 2004).
2.6.2 Spektrofotometri sinar inframerah
Spektrofotometri inframerah pada umumnya digunakan untuk: 1. menentukan gugus fungsi suatu senyawa organik.
25
Pengukuran pada spektrum inframerah dilakukan pada daerah cahaya inframerah tengah (mid-infrared) yaitu pada panjang gelombang 2.5 - 50 𝜇𝜇m atau bilangan gelombang 4000 - 200 cm-1. Energi yang dihasilkan oleh radiasi ini akan menyebabkan vibrasi atau getaran pada molekul. Pita absorpsi sinar inframerah sangat khas dan spesifik untuk setiap tipe ikatan kimia atau gugus fungsi (Dachriyanus, 2004).
Hanya frekuensi (energi) dari radiasi inframerah tertentu yang dapat diserap oleh suatu molekul. Agar molekul dapat menyerap radiasi inframerah, maka molekul harus mempunyai gambaran, yakni momen dipol pada molekul harus berubah selama vibrasi (Gandjar dan Rohman, 2012).
Daerah inframerah terletak antara spektrum elektromagnetik cahaya tampak dan spektrum radio, yakni antara bilangan gelombang 4000 - 400 cm-1. Penggunaan spektrofotometri inframerah lebih banyak ditujukan untuk identifikasi suatu senyawa melalui gugus fungsinya. Spektrum inframerah senyawa organik bersifat khas, artinya senyawa yang berbeda akan mempunyai spektrum yang berbeda pula (Noerdin, 1985).
Penafsiran spektrum inframerah dari suatu senyawa yang belum diketahui ditujukan pada penentuan ada atau tidaknya gugus fungsional utama seperti C=O, O-H, N-O-H, C-O, C=C, C≡C, C=N, C≡N, dan NO2. Langkah-langkah yang dilakukan
untuk memeriksa pita - pita yang terpenting pada hasil dari spektrum inframerah (Pavia, et al., 1988):
1. Gugus karbonil
Gugus C=O memberikan puncak yang kuat pada daerah 1820-1660 cm-1.
26 langsung ke nomor 3).
Asam : lihat gugus O-H, merupakan serapan melebar di daerah 3300- 2500 cm-1.
Amida : lihat gugus N-H, merupakan serapan medium di daerah 3500 cm-1, kadang-kadang dengan puncak rangkap.
Ester : lihat gugus C-O, merupakan serapan medium di daerah 1300- 1000 cm-1.
Anhidrida : mempunyai dua serapan C=O di daerah 1810 dan 1760 cm-1. Aldehida : lihat gugus C-H, merupakan dua serapan lemah di daerah 2850
dan 2750 cm-1 yaitu disebelah kanan serapan C-H. Keton : kemungkinan bila kelima senyawa di atas tidak ada. 3. Bila gugus C=O tidak ada
Alkohol atau fenol : lihat gugus O-H, serapan melebar di daerah 3600-3300 cm-1 yang diikuti adanya serapan C- O di daerah 1300-1000 cm-1.
Amina : lihat gugus N-H, yaitu serapan medium di daerah 3500 cm-1.
Eter : lihat gugus C-O (dan tidak adanya O-H), yaitu serapan medium di daerah 1300-1000 cm-1.
4. Ikatan rangkap dua atau cincin aromatik
− Serapan lemah C=C di daerah 1650 cm-1.
27
− cocokkan kemungkinan di atas dengan memperhatikan serapan pada daerah C-H aromatik di sebelah kiri 3000 cm-1, sedangkan C-H alifatis terjadi di sebelah kanan daerah tersebut.
5. Ikatan rangkap tiga
− Serapan medium dan tajam dari C≡N di daerah bilangan gelombang 2250 cm-1.
− Serapan medium dan tajam dari C≡C di daerah bilangan gelombang 2150 cm-1.
6. Gugus nitro
− Dua serapan yang kuat di daerah 1600-1500 cm-1 dan 1390-1300 cm-1. 7. Hidrokarbon
− Apabila keenam serapan di atas tidak ada.
− Serapan C-H alifatis di daerah sebelah kanan 3000 cm-1.