BAB II
TINJAUAN PUSTAKA
2.1 Siklus Adsorpsi
2.1.1 Teori Umum Adsorpsi
Adsorpsi adalah suatu proses yang terjadi ketika suatu fluida
akhirnya membentuk suatu lapisan tipis atau film (zat terserap: adsorbat) pada
permukaannya. Berbeda dengan
fluida lainnya dengan membentuk suat
Adsorpsi secara umum adalah proses penggumpalan substansi terlarut (soluble) yang ada dalam larutan oleh permukaan zat atau benda penyerap dimana terjadi suatu ikatan kimia fisika antara substansi dengan penyerapnya.
Adsorpsi adalah pengumpulan dari adsorbat di atas permukaan adsorben, sedang absorpsi adalah penyerapan dari adsorbat ke dalam adsorben dimana disebut dengan fenomena sorption. Materi atau partikel yang diadsorpsi disebut adsorbat, sedangkan bahan yang berfungsi sebagai pengadsorpsi disebut adsorben.
Adsorpsi dibedakan menjadi dua jenis, yaitu adsorpsi fisika yang disebabkan oleh gaya Van Der dan secara kimia (terjadi reaksi antara zat yang diserap dengan adsorben).
Apabila daya tarik menarik antara zat terlarut dengan adsorben besar maka zat yang terlarut akan diadsorpsi pada permukaan adsorben. Inilah yang disebut dengan gaya Van Der Waals. Pada proses ini gaya yang menahan molekul fluida pada permukaan solid relatif lemah, dan besarnya sama dengan
gayaVan Der Waals) mempunyai derajat
permukaan solid dengan molekul fluida biasanya cepat tercapai dan bersifat reversibel.[12]
Adsorpsi kimia adalah reaksi yang terjadi antara zat padat dengan zat terlarut yang teradsorpsi. Adsorpsi ini bersifat spesifik dan melibatkan gaya yang jauh lebih besar daripada adsorpsi fisika. Karena adanya ikatan kimia maka pada permukaan adsorben akan terbentuk suatu lapisan, di mana terbentuknya lapisan tersebut akan menghambat proses penyerapan selanjutnya oleh bantuan adsorben sehingga efektifitasnya berkurang.[18]
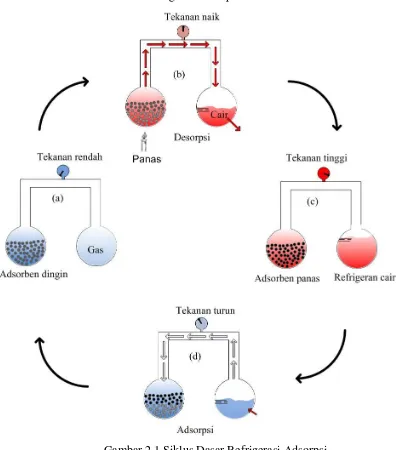
Perhatikan siklus dasar refrigerasi adsorpsi di bawah ini. [16]
Pada kondisi awal sistem berada pada tekanan dan temperatur rendah, adsorben memiliki konsentrasi refrigeran yang tinggi dan vessel lain terdapat refrigeran dalam bentuk gas (gambar a). Vessel yang terdapat adsorben dipanaskan yang mengakibatkan naiknya temperatur dan tekanan sistem sehingga kandungan adsorbat yang ada di dalam adsorben berkurang atau menguap. Proses berkurangnya kandungan adsorbat pada adsorben pada kasus ini disebut desorpsi.
Refrigeran yang terdesorpsi kemudian terkondensasi sebagai cairan di dalam labu kedua dengan dikeluarkannya panas ke lingkungan dimana tekanan dan temperatur sistem masih tinggi (gambar b). Pemanasan pada labu pertama dihentikan, lalu pada botol labu yang pertama terjadi perpindahan panas ke lingkungan sehingga tekanan sistem menjadi rendah. Tekanan sistem yang rendah menyebabkan adsorbat cair pada botol labu yang kedua menguap dan terserap ke botol pertama yang berisi adsorben. Proses terserapnya adsorbat ke adsorben pada kasus ini disebut adsorpsi. Proses adsorpsi menghasilkan efek pendinginan yang terjadi pada botol labu kedua, dimana pada tekanan rendah panas dari lingkungan diserap untuk menguap adsorbat (d) sampai sistem kembali ke kondisi awal.
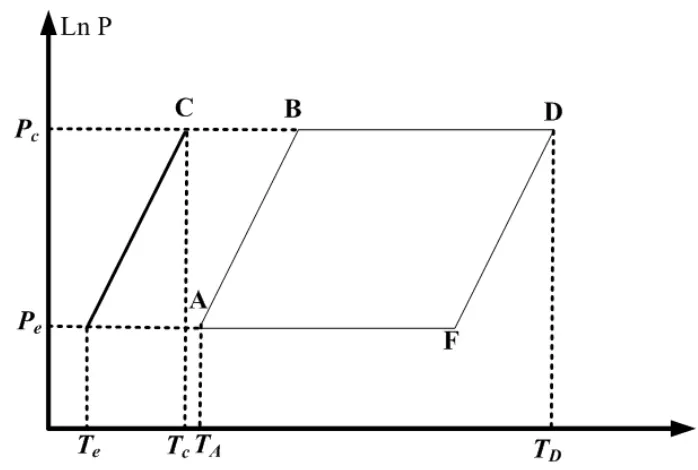
Siklus mesin pendingin adsorpsi dapat digambarkan pada diagram Clayperon berikut ini.
Proses yang terjadi dapat di uraikan sebagai berikut ini. 1. Proses Pemanasan (pemberian tekanan)
Proses pemanasan dimulai dari titik A dimana adsorben berada pada temperatur rendah TA dan tekanan rendah Pe (tekanan evaporator). Adsorber akan
menerima panas sehingga temperatur adsorber meningkat dan diikuti peningkatan tekanan evaporasi menjadi tekanan kondensasi. Selama proses ini tidak ada aliran refrigeran.
2. Proses desorpsi
Proses desorpsi berlangsung pada waktu panas diberikan dari titik B ke D sehingga adsorber mengalami peningkatan temperatur yang menyebabkan timbulnya uap desorpsi. Sehingga, adsorbat yang berada pada adsorben dalam bentuk gas mengalir ke kondensor untuk mengalami proses kondensasi menjadi cair.
3. Proses Pendinginan (penurunan tekanan)
Proses pendinginan berlangsung dari titik D ke F yang berlangsung pada malam hari. Adsorber melepaskan panas dengan cara didinginkan sehingga suhu di adsorber turun dan diikuti oleh penurunan tekanan dari tekanan kondensasi ke tekanan evaporasi.
4. Proses Adsorpsi
Proses adsorpsi berlangsung dari titik F ke A. Adsorber terus melepaskan panas sehingga adsorber mengalami penurunan temperatur dan tekanan yang menyebabkan timbulnya uap adsorpsi.
2.2 Adsorben
2.2.1 Alumina Aktif
kimia yang sama seperti safir dan ruby. Ini memiliki luas permukaan yang sangat tinggi untuk rasio berat, karena banyak "terowongan seperti" pori-pori.
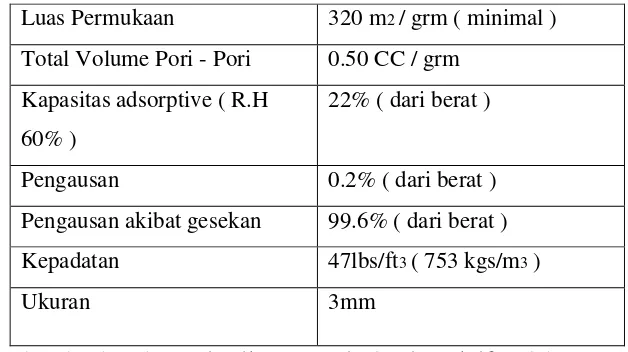
Gambar 2.3 Alumina Aktif Table 2.1 Sifat alumina aktif [18]
Luas Permukaan 320 m2 / grm ( minimal )
Total Volume Pori - Pori 0.50 CC / grm Kapasitas adsorptive ( R.H
60% )
22% ( dari berat )
Pengausan 0.2% ( dari berat ) Pengausan akibat gesekan 99.6% ( dari berat ) Kepadatan 47lbs/ft3 ( 753 kgs/m3 )
Ukuran 3mm
Pada adsorben berpori mikro seperti alumina aktif, salah satu teori yang paling sering digunakan untuk memberi gambaran adsorpsi fisik molekul gas adalah teori pengisian volume pori mikro (TVFM, Theory Of Volume Filling of Micropores) yang dikembangkan oleh M.M Dubinin. Berbeda dengan teori – teori
sebelumnya yang memberikan gambaran fisik berupa pembentukan satu atau lebih lapisan (film) adsorpsi pada permukaan adsorben. Teori pengisian volume mikro menekankan bahwa adsorpsi tidak terjadi melalui pembentukan lapisan (film) adsorpsi tetapi berupa pengisian volume dalam ruang adsorpsi dan zat yang teradsorpsi berada dalam bentuk cair (cal, 1995).
Persamaan adsorpsi dapat dilihat dibawah ini :
W = W0 exp �– (𝐴/(𝐸0))𝑛� ………..(2.1)
W = Volume adsorbat yang terkondensasi pada suhu (T) dan tekanan Relative (P/P0) (cm3/gr)
T = Suhu mutlak (K)
P = Tekanan parsial adsorbat (tekanan kondensasi) atm P = Tekanan uap jenuh adsorbat (tekanan evaporasi) atm
W0 = Volume total pori mikro yang dapat diakses oleh adsorbat (cm3/gr)
A = Kemampuan adsrobsi dari alumina aktif E0 = Energy adsorpsi (KJ/mol)
n = parameter yang bergantung pada jenis adsorbat.
Dalam persamaan ini, parameter n pada persamaan Dubinin – Astakhov ditetapkan memiliki nilai 2 sehingga persamaan Dubinin – Astakhov dinyatakan dalam bentuk :
W = W0 exp �– (𝐴/(𝐸0))2� ……… (2.2)
Persamaan (2.2) selanjutnya dapat diubah ke dalam bentuk : Ln W = LnW0 - (1/(E0))2 A2 ……….. (2.3)
Dimana :
A = R.T Ln (P0/P) ………. (2.4)
Sehingga bentuk persamaan linear model Isoterm adsorpsi DR adalah : Ln W = LnW0 - (1/(E0))2 [R. T Ln (P0/P) ]2 …. (2.5)
2.2.2 Pembuatan Alumina Aktif
Aluminium oksida adalah sebuah senyawa kimia dari aluminium dan oksida, dengan rumus kimia Al2O3. Nama mineralnya adalah alumina, dan dalam bidang pertambangan, kramik dan teknik material senyawa ini lebih banyak disebut dengan nama alumina
Pabrik alumina terbesar di dunia adalah Alcoa, Alcan, dan Rusal. Perusahaan yang memiliki spesialisasi dalam produksi dari aluminium oksida dan aluminium hidroksida misalnya adalah Alcan dan Almatis. Bijih bauksit terdiri dari Al2O3, Fe2O3, and SiO2 yang tidak murni. Campuran ini dimurnikan terlebih dahulu melalui Proses Bayer:
Al2O3 + 3H2O + 2NaOH + panas → 2NaAl(OH)4
Fe2O3 tidak larut dalam basa yang dihasilkan, sehingga bisa dipisahkan melalui penyaringan. SiO2 larut dalam bentuk silikat Si(OH)62-. Ketika cairan yang dihasilkan didinginkan, terjadi endapan Al(OH)3, sedangkan silikat masih larut dalam cairan tersebut. Al(OH)3 yang dihasilkan kemudian dipanaskan
2Al(OH)3 + panas → Al2O3 + 3H2O
Al2O3 yang terbentuk adalah alumina. Pada 1961,perusahaan General Electric mengembangkan Lucalox, alumina transparan yang digunakan dalam lampu natrium. Pada Agustus 2006, ilmuwan Amerika Serikat yang bekerja untuk 3M berhasil mengembangkan teknik untuk membuat alloy dari aluminium oksida dan unsur-unsur lantanida, untuk memproduksi kaca yang kuat, yang disebutalumina transparan. Aloi adalah campuran dua atau lebih unsur pada komposisi tetap tertentu yang mana juzuk utamanya adalah logam.
Gambar 2.4 Diagram proses pembuatan alumina[16]
2.2.3 Kegunaan Alumina Aktif
Alumina aktif digunakan untuk berbagai macam aplikasi adsorben dan katalis termasuk adsorpsi katalis dalam produksi polyethylene , dalam produksi hidrogen peroksida , sebagai adsorben selektif untuk bahan kimia, termasuk arsenik , fluoride , dalam penghapusan belerang dari aliran gas ( Claus proses Catalyst ) .
ideal untuk pengobatan adalah 5.5 yang memungkinkan sampai tingkat penghapusan 95 % .
2.3 Refrigeran
Refrigeran adalah zat yang mengalir dalam mesin pendingin (refrigerasi) atau mesin pengkondisian udara. Zat ini berfungsi untuk menyerap panas dari benda atau udara yang didinginkan dan membawanya kemudian membuangnya ke udara sekeliling di luar benda.
Berdasarkan jenis senyawanya, refrigeran dapat dikelompokan menjadi 7 kelompok yaitu sebagai berikut [19]:
1. Kelompok refrigeran senyawa halokarbon.
Kelompok refrigeran senyawa halokarbon diturunkan dari hidrokarbon (HC) yaitu metana (CH4), etana (C2H6), atau dari propana (C3H8) dengan mengganti
atom-atom hidrogen dengan unsur-unsur halogen seperti khlor (Cl), fluor (F), atau brom (Br). Jika seluruh atom hidrogen tergantikan oleh atom Cl dan F maka refrigeran yang dihasilkan akan terdiri dari atom khlor, fluor dan karbon. Refrigeran ini disebut refrigeran chlorofluorocarbon (CFC). Jika hanya sebagian saja atom hidrogen yang digantikan oleh Cl dan atau F maka refrigeran yang terbentuk disebut hydrochlorofluorocarbon (HCFC). Refrigeran halokarbon yang tidak mengandung atom khlor disebut hydrofluorocarbon (HFC).
2. Kelompok refrigeran senyawa organik cyclic.
Kelompok refrigeran ini diturunkan dari butana. Aturan penulisan nomor refrigeran adalah sama dengan cara penulisan refrigeran halokarbon tetapi ditambahkan huruf C sebelum nomor. Contoh dari kelompok refrigeran ini adalah:
1. R-C316 C4Cl2F6 1,2-dichlorohexafluorocyclobutane
2. R-C317 C4ClF7 chloroheptafluorocyclobutane
3. R-318 C4F8 octafluorocyclobutane
Kelompok refrigeran ini merupakan refrigeran campuran yang bisa terdiri dari campuran refrigeran CFC, HCFC, HFC, dan HC. Refrigeran yang terbentuk merupakan campuran tak bereaksi yang masih dapat dipisahkan dengan cara destilasi.
5. Kelompok refrigeran campuran Azeotropik.
Kelompok refrigeran Azeotropik adalah refrigeran campuran tak bereaksi yang tidak dapat dipisahkan dengan cara destilasi. Refrigeran ini pada konsentrasi, tekanan dan temperatur tertentu bersifat azeotropik, yaitu mengembun dan menguap pada temperatur yang sama, sehingga mirip dengan refrigeran tunggal. Namun demikian pada kondisi (konsentrasi, temperatur atau tekanan) yang lain refrigeran ini bisa saja menjadi bersifat zeotropik.
6. Kelompok refrigeran senyawa organik biasa
Kelompok refrigeran ini sebenarnya terdiri dari unsur C, H dan lainnya. Namun demikian cara penulisan nomornya tidak dapat mengikuti cara penomoran refrigeran halokarbon karena jumlah atom H nya jika ditambah dengan 1 lebih dari 10 sehingga angka kedua pada nomor refrigeran menjadi dua digit. Sebagai contoh butana (C4H10), jika dipaksakan dituliskan sesuai dengan cara penomoran
refrigeran halokarbon, maka refrigeran ini akan bernomor R-3110, sehingga akan menimbulkan kerancuan.
7. Kelompok refrigeran senyawa anorganik.
Kelompok refrigeran ini diberi nomor yang dimulai dengan angka 7 dan digit selanjutnya menyatakan berat molekul dari senyawanya. Contoh dari refrigeran ini adalah:
• R-744 : O2
• R-764 : SO2
8. Kelompok refrigeran senyawa organik tak jenuh.
Kelompok refrigeran ini mempunyai nomor empat digit, dengan menambahkan angka keempat yang menunjukkan jumlah ikatan rangkap di depan ketiga angka yang sudah dibahas dalam sistem penomoran refrigeran halokarbon.[19]
2.3.1 Amonia
Amonia adal
didapati berupa
amonia dapat dilihat seperti tabel di bawah ini. Tabel 2.1 Sifat Amonia[10,18]
Sifat Amonia
Massa jenis
682 kg/m³, cair
Panas Laten Penguapan (Le)
–77,7°C -33,3 °C Kautik, korosif 1357 kJ/kg
Walaupun amonia memiliki sumbangan penting bagi keberadaa
Gambar 2.5 Amonia Cair (NH3)
2.4 Keamanan Lingkungan
Refrigeran dirancang untuk digunakan pada ruangan tertutup atau tidak bercampur dengan udara luar. Jika ada kebocoran karena sesuatu hal yang tidak diinginkan, maka refrigeran ini akan keluar sistem dan bisa saja terhirup oleh manusia. Untuk menghindari hal-hal yang tidak diinginkan maka refrigeran harus dikategorikan aman atau tidak aman. Ada dua faktor yang digunakan untuk mengklasifikasikan refrigeran berdasarkan keamanan, yaitu bersifat racun dan mudah terbakar.
Berdasarkan toxicity, refrigeran dapat dibagi dua kelas, yaitu kelas A bersifat tidak beracun pada konsentrasi yang ditetapkan dan kelas B jika bersifat racun. Batas yang digunakan untuk mendefinisikan sifat racun atau tidak adalah sebagai berikut. Refrigeran dikategorikan tipe A jika pekerja tidak mengalami gejala keracunan meskipun bekerja lebih dari 8 jam/hari (40 jam/minggu) di lingkungan yang mengandung konsentrasi refrigeran sama atau kurang dari 400 ppm (part per million by mass). Sementara kategori B sebaliknya.
temperatur 21,1oC atau kalor pembakarannya kurang dari 19 MJ/kg. Kelas 3 sangat mudah terbakar. Refrigeran ini akan terbakar jika konsentrasinya kurang dari 0,1 kg/m3 ataun kalor pembakarannya lebih dari 19 MJ/kg.
Berdasarkan defenisi ini, sesuai dengan standar 34-1997. Refrigeran diklasifikasikan menjadi 6 kategori.[2]
1. A1 : sifat racun rendah dan tidak terbakar.
2. A2 : Sifat racun rendah dan sifat terbakar rendah. 3. A3 : Sifat racun rendah dan mudah terbakar. 4. B1 : sifat racunlebih tinggi dan tidak terbakar.
5. B2 : sifat racun lebih tinggi dan sifat terbakar rendah. 6. B3 : sifat racun lebih tinggi dan mudah terbakar.
2.5 Kalor (Q)
Kalor adalah salah satu bentuk energi yang dapat mengakibatkan perubahan temperatur. Pada abad ke 19 berkembang teori bahwa kalor merupakan fluida ringan yang dapat mengalir dari suhu tinggi ke suhu rendah, jika suatu benda mengandung banyak kalor, maka suhu benda itu tinggi (panas). Sebaliknya, jika benda itu mengandung sedikit kalor, maka dikatakan benda itu bersuhu rendah (dingin). Kuantitas energi kalor (Q) dihitung dalam satuan joules (J). Laju aliran kalor dihitung dalam satuan joule per detik (J/s) atau watt (W). Laju aliran energi ini juga disebut daya, yaitu laju dalam melakukan usaha
2.5.1 Kalor Laten
Suatu bahan biasanya mengalami perubahan temperatur bila terjadi perpindahan kalor antara bahan dengan lingkungannya. Pada suatu situasi tertentu, aliran kalor ini tidak merubah temperaturnya. Hal ini terjadi bila bahan mengalami perubahan fasa. Misalnya padat menjadi cair, cair menjadi uap dan perubahan struktur kristal (zat padat). Energi yang diperlukan disebut kalor transformasi. Kalor yang diperlukan untuk merubah fasa dari bahan bermassa m adalah
Dimana :
QL = Kalor laten (J)
Le = Kapasitas kalor spesifik laten (J/kg)
M = Massa zat (kg)
2.5.2 Kalor Sensibel
Tingkat panas atau intensitas panas dapat diukur ketika panas tersebut merubah temperatur dari suatu substansi. Perubahan intensitas panas dapat diukur dengan termometer. Ketika perubahan temperatur didapatkan, maka dapat diketahui bahwa intensitas panas telah berubah dan disebut sebagai kalor sensibel. Dengan kata lain, kalor sensibel adalah kalor yang diberikan atau yang dilepaskan oleh suatu jenis fluida sehingga temperaturnya naik atau turun tanpa menyebabkan perubahan fasa fluida tersebut.
Qs = m Cp∆T ... (2.2)
Dimana:
Qs = Kalor sensible (J)
Cp = Kapasitas kalor spesifik sensibel (J/kg.K)
∆T = Beda temperatur (K)
2.5.3 Perpindahan Kalor
Panas hanya akan berpindah jika ada perbedaan temperatur, yaitu dari sistem yang bertemperatur tinggi ke sistem bertemperatur rendah. Perbedaan temperatur ini mutlak diperlukan sebagai syarat terjadinya perpindahan panas. Selama ada perbedaan temperatur antara dua sistem maka akan terjadi perpindahan panas. Mekanisme perpindahan panas yang terjadi dapat dikategorikan atas 3 jenis yaitu: konduksi, konveksi dan radiasi
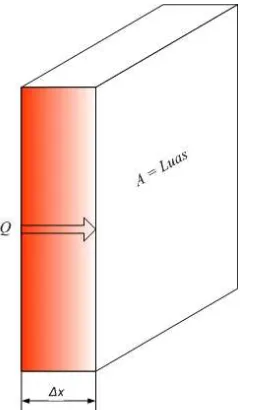
1. Konduksi
cair dan gas. Perpindahan panas di sini terjadi akibat interaksi antara partikel tanpa diikuti perpindahan partikelnya. Perhatikan gambar di bawah ini.
Gambar 2.6 Perpindahan Panas Konduksi Melalui Sebuah Pelat Secara matematik, untuk plat datar seperti gambar di atas ini, laju perpindahan panas konduksi dirumuskan dengan persamaan:
𝑄𝑐 = 𝑘𝐴∆𝑇∆𝑥. . . (2.3)
Atau sering dirumuskan dengan persamaan berikut ini.
𝑄𝑐 =−𝑘𝐴𝑑𝑇
𝑑𝑥 . . . (2.4) [ lit.3]
Dimana:
𝑄𝑐 = Laju aliran energi (W)
A = Luas penampang (m2) ∆T = Beda temperatur (K)
∆x = Panjang (m)
k = Daya hantar (konduktivitas) (W/m.K)
2. Konveksi
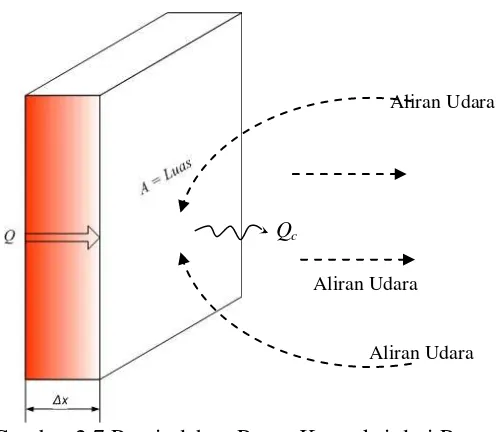
Perpindahan panas konveksi adalah perpindahan panas antara permukaan padat yang berbatasan dengan fluida mengalir. Fluida di sini bisa dalam fasa cair atau fasa gas. Syarat utama
Gambar 2.7 Perpindahan Panas Konveksi dari Permukaan Pelat
Secara matematik perpindahan panas konveksi pada permukaan pelat rata dapat dirumuskan dengan persamaan berikut ini.
Qh = hA(Ts-TL) ... (2.5) [lit.4]
Dimana:
Qh = Laju perpindahan panas konveksi (W)
h = Koefisien konveksi (W/m2K)
A = Lluas penampang perpidahan panas (m2) Ts = Temperatur permukaan
TL = Temperatur fluida
3. Radiasi
Perpindahan panas radiasi adalah panas yang dipindahkan dengan cara memancarkan gelombang elektromagnetik. Berbeda dengan mekanisme konduksi dan konveksi, radiasi tidak membutuhkan medium perpindahan panas. Sampainya sinar matahari ke permukaan bumi adalah contoh yang jelas dari perpindahan panas radiasi.
Persamaan yang dapat digunakan untuk menghitung laju perpindahan panas radiasi antara permukaan pelat (gambar 2.10) dan lingkungannya adalah:
Qc
Aliran Udara
Aliran Udara
Qr= eσAT4 ...(2.6)
Dimana
Qr = Laju perpindahan panas radiasi (W)
σ = Konstanta Boltzman: 5,67 x 10-8 W/m2 K4 e = Emisivitas (0 ≤ e ≤ 1)
T = Temperatur (K)
4. Konveksi Natural
Jika aliran fluida terjadi secara alami, sebagai akibat perpindahan panas yang terjadi. Konveksi ini disebut konveksi natural atau kadang disebut konveksi bebas dalam bahasa Inggris disebut natural convection atau free convection.
Pada kasus konveksi natural pada bidang horizontal panjang yang digunakan menghitung bilangan RaL adalah panjang karakteristik yang didefinisikan dengan
persamaan:
𝐿= 𝐴𝐾. . . (2.7) [lit.4]
Dimana A menyatakan luas bidang horizontal dan K adalah keliling. Dengan menggunakan panjang karakteristik (L) ini bilangan RaL dapat dihitung dengan
menggunakan persamaan berikut (2.8). RaL = 𝑔𝛽
(𝑇𝑠−𝑇𝑙)𝐿3
𝑣2 𝑃𝑟...(2.8)
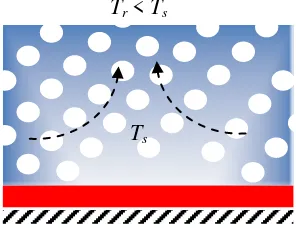
Pola konveksi natural pada permukaan horizontal diperlihatkan seperti gambar berikut ini.
Gambar 2.8 Konveksi Natural pada Bidang Horizontal (tipe a)
Persamaan untuk menghitung Nu seperti gambar di atas (bidang horizontal) dapat digunakan yang diajukan oleh Llyod Moran (1974):
Tr < Ts
Untuk 104 < RaL < 10
7
:
Nu = 0,54R𝑎𝐿0,25...(2.9)
Untuk 107 < RaL < 10
9
Nu = 0,15R𝑎𝐿1/3...(2.10)
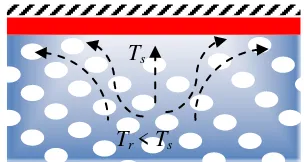
Jika polanya ditunjukkan seperti gambar di bawah ini, yaitu fluida panas akan terdesak dari permukaan yang panas dan mengalir ke sebelah luar. Untuk mengisi kekosongan akibat aliran ini maka fluida dibawahnya akan mengalir ke atas.
Gambar 2.9 Konveksi natural pada bidang horizontal (tipe b)
Persamaan menghitung bilangan Nu untuk kasus ini dapat digunakan persamaan dapat dituliskan:
Nu = 0,27𝑅𝑎𝐿0,25...(2.11)
Persamaan ini berlaku untuk 105 < RaL <1010 Tr < Ts
![Gambar 2.4 Diagram proses pembuatan alumina[16]](https://thumb-ap.123doks.com/thumbv2/123dok/3824917.1835115/8.595.151.507.82.284/gambar-diagram-proses-pembuatan-alumina.webp)
![Tabel 2.1 Sifat Amonia[10,18]](https://thumb-ap.123doks.com/thumbv2/123dok/3824917.1835115/11.595.125.505.360.492/tabel-sifat-amonia.webp)