10
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di PT. Langkat Nusantara Kepong, kampus Sekolah Tinggi Ilmu Pertanian Agrobisnis Pertanian (STIP-AP) Medan dan analisa laboratorium di PT. Socfindo. Waktu penelitian ini berlangsung pada bulan April sampai dengan Juli 2019.
3.2 Rancangan Penelitian
Metode yang dilakukan dalam penelitian ini menggunakan rancangan acak lengkap (RAL) deskriptif kualitatif faktorial dengan 2 faktor, sebagai berikut: 3.2.1 Variabel Bebas
Faktor 1 : Perlakuan Serat (M) dengan 2 taraf,yaitu:
M1 = Tandan Kosong Kelapa Sawit (TKKS) Utuh dan Kotoran Ayam M2 = Empty Fruit Bunch Press Cacah Manual dan Kotoran Ayam Faktor 2 : Waktu Pengomposan (A) dengan 2 taraf, yaitu:
A1 = Pengomposan 1 bulan (5 Liter untuk 1 kali penyiraman LCPKS) A2 = Pengomposan 2 bulan (5 Liter untuk 1 kali penyiraman LCPKS) Diperoleh kombinasi perlakuan sebanyak 4 kombinasi dengan masing-masing 3 ulangan, yaitu:
11
M1A2 M2A2
Sehingga total analisa pada penelitian ini 12 kali ulangan. 3.2.2 variabel terikat
Komposisi kandungan kadar makronutrien pada pupuk organik 3.3 Bahan dan Peralatan
Bahan-bahan yang digunakan dalam penelitian ini adalah serat Tandan Kosong Kelapa Sawit (TKKS) utuh, serat Empty Fruit Bunch Press Cacah manual menggunakan parang atau gunting sehingga mendapatkan ukuran serat yang lebih kecil, dan limbah cair pabrik kelapan sawit (LCPKS) milik PT. Langkat Nusantara Kepong, kotoran unggas (ayam), molase dan EM-4 Adapun alat-alat yang digunakan pada penelitian ini adalah terpal sebagai penutup inkubasi, timbangan sebagai alat menimbang bahan, parang dan gunting sebagai alat pencacah bahan, garukan sampah sebagai pengaduk, dan ember sebagai wadah bahan.
3.4 Tahapan Penelitian
Tahapan penelitian meliputi :
1. Penyediaan Bahan Baku Serat Tandan Kosong Kelapa Sawit (TTKS).
Menyediakan bahan baku serat tandan kosong kelapa sawit utuh, Serat Empty
Fruit Bunch Press, untuk serat Empty Fruit Bunch Press di cacah kembali
memakai parang atau gunting untuk memperkecil ukuran dan memperluas permukaannya.
12
Menyediakan bahan baku limbah Cair Pabrik Kelapa Sawit (LCPKS) hasil pemisahan dari proses mesin ballpress di PT. LNK, Langkat, Sumatera Utara. 3. Pencampuran Bahan Baku.
Setelah bahan baku selesai dikelompokkan sesuai ukuran serat, segera dilakukan penyiraman dengan limbah cair pabrik kelapa sawit (LCPKS) dan kotoran unggas (ayam).
4. Inkubasi Tandan Kosong Kelapa Sawit (TKKS)
Proses inkubasi dikerjakan dengan membungkus kompos memakai plastik terpal sehingga temperatur dan kelembabannya terjaga. Selama proses inkubasi berlangsung, suhu kompos akan meningkat tajam hingga mencapai 70oC selama 1-2 bulan. Hal ini menandakan proses dekomposisi sedang berlangsung secara intensif. Suhu kompos akan kembali normal apabila kompos sudah matang. Ciri-ciri kompos yang sudah matang yaitu warnanya cokelat kehitaman, temperaturnya normal, dan seratnya remah mudah dihancurkan. Kompos yang sudah matang pun bisa diteliti memakai metode kimia, di mana rasio C/N awalnya 50-60 berubah menjadi di bawah 25
5. Analisa Kualitas Kompos
Kompos yang sudah matang akan di uji kualitas kandungan unsur hara.
3.5 Indikator Pengamatan
3.5.1 Nitrogen Total (N) (SNI 2803:2010)
Nitrogen dalam contoh dihidrolisis dengan asam sulfat membentuk senyawa ammonium sulfat. Nitrat dengan asam salisilat membentuk nitrosalisilat, kemudian direduksi dengan natrium tiosulfat membentuk senyawa ammonium. Suling senyawa ammonium dalam suasana alkali, tampung hasil sulingan asam borat. Titrasi dengan larutan asam sulfat sampai warna hijau berubah menjadi merah jambu.
13
1. Timbang teliti 0,5 g contoh yang telah dihaluskan masukkan ke dalam labu kjeldhal.
2. Tambahkan 25 mL larutan asam sulfat-salisilatl goyang hingga merata dan biarkan semalaman.
3. Esoknya tambahkan 4 g Na2S2O2.5H2O kemudian panaskan pada suhu rendah hingga gelembung habis. Naikan suhu secara bertahap maksimum 300oC (sekitar 2 jam) dan biarkan dingin. 4. Encerkan dengan air suling, pindahkan ke dalam labu takar 500
mL kocok dan tepatkan sampai tanda garis.
5. Pipet 25 mL, masukkan ke dalam labu suling tambahkan 150 mL air suling dan batu didih.
6. Suling setelah penambahan 10 mL larutan NaOH 40% dengan penampung hasil sulingan 20 mL larutan asam borat 1 % yang ditambah 3 tetes indikator Conway.
7. Hentikan penyulingan bila hasil sulingan mencapai 100 mL. 8. Titrasi dengan larutan H2SO4 0,05 N sampai titik akhir titrasi
tercapai (warna hijau berubah menjadi merah jambu). 9. Lakukan pengerjaan larutan blanko.
Nitrogen total (𝑁)% =(V1−V2) x N x 14,008 x P x 100
w X
100 100−KA
Keterangan:
V1 adalah larutan H2SO4 yang digunakan untuk titrasi sampel, mL V2 adalah volume H2SO4 yang digunakan untuk titrasi blanko, mL N adalah Normalitas larutan
H2SO4 14,008 adalah berat atom nitrogen
P adalah pengenceran W adalah berat contoh, mg KA adalah kadar air, %
14
3.5.2 Fosfor total (P) sebagai P2O5 (SNI 2803:2010)
Kadar P2O5 ditentukan secara kolorimetri, ortofosfat yang terlarut direaksikan dengan ammonium molibdatvanadat membentuk senyawa kompleks molibdovanadat asam fosfat yang berwarna kuning.
Persiapan larutan contoh
1. Timbang dengan teliti 1 g contoh yang halus, masukkan ke dalam gelas piala 250 mL.
2. Tambahkan dengan 20 – 30 mL HNO3 p.a.
3. Didihkan perlahan-perlahan selama 30 – 45 menit untuk mengoksidasi bahan yang mudah teroksidasi, dinginkan.
4. Tambahkan 10 – 20 mL HClO4 70 – 72 %.
5. Didihkan perlahan-lahan sampai larutan tidak berwarna dan timbul asap putih pada gelas piala, dinginkan.
6. Tambahkan 50 mL air suling dan didihkan beberapa menit, dinginkan. 7. Pindahkan dalam labu ukur 500 mL dan tepatkan dengan air suling
sampai tanda tera dan homogenkan.
8. Saring dengan kertas saring Whatman No. 41. 9. Tampung ke dalam erlenmeyer.
Prosedur
1. Pipet 5 mL larutan contoh dan masing-masing larutan standar fosfat ke dalam labu ukur 100 mL.
2. Tambahkan 45 mL air suling, diamkan selama 5 menit.
3. Tambahkan 20 mL pereaksi molibdovanadat dan encerkan dengan air suling hingga tanda tera dan kocok.
4. Biarkan pengembangan warna selama 10 menit. 5. Lakukan pengerjaan larutan blanko.
15
7. Baca absorbansi larutan contoh dan standar pada spektrofotometer.
8. Buat kurva standar.
9. Hitung kadar P2O5 dalam contoh.
3.5.3 Kalium (K) sebagai K2O (SNI 2803:2010)
Kalium bereaksi dengan natrium tetrafenilborat dalam suasana basa lemah, membentuk endapan kalium tetrafenilborat, kelebihan natium tetrafenilborat dititar dengan benzalkonium klorida.
Standarisasi Larutan
a. Larutan benzalkonium klorida (BAC)
Dalam erlenmeyer 125 mL terdapat 1 mL larutan STPB, tambahkan 20-25 mL air suling, 1 mL NaOH 20 %, 2,5 mL HCHO, 1,5 mL (NH4)2C2O4 4 % dan 6 - 8 tetes indikator titan yellow. Titrasi dengan larutan BAC sampai titik akhir berwarna merah, gunakan buret semimikro 10 mL. (Larutan BAC 2 mL = 1 mL larutan STPB) b. Larutan natrium tetraphenylboron
Larutkan 2,5 g KH2PO4 dengan air suling dalam labu ukur 250 mL, tambahkan 50 mL larutan (NH4)2C2O4 4 %, tepatkan sampai tanda tera dan homogenkan. Ambil 15 mL larutan tersebut masukkan dalam 100 mL labu ukur, tambahkan 2 mL NaOH 20 %, 5 mL HCHO dan 43 mL larutan STPB, tepatkan dengan air suling, homogenkan dan biarkan 5 – 10 menit dan saring. Ambil 50 mL filtrat masukkan dalam erlenmeyer 125 mL, tambahkan 6 – 8 tetes indicator titan yellow dan titrasi kelebihan larutan dengan larutan BAC.
Perhitungan :
16 Prosedur:
1. Timbang teliti 2,5 g contoh yang siap uji dalam 250 mL gelas piala. - Tambahkan 50 mL (NH4)2C2O4 4 %, 125 mL air suling dan didihkan selama 30 menit, dinginkan.
2. Pindahkan ke dalam labu ukur 250 mL, tepatkan sampai tanda tera dengan air suling.
3. Saring atau diamkan hingga jernih. - Ambil 15 mL larutan tersebut, masukkan dalam labu ukur 100 mL. - Tambahkan 2 mL NaOH 20 % , 5 mL HCHO;
4. Tambahkan 1 mL STPB untuk tiap 1% K2O, tambahkan 8 mL untuk berlebihan.
5. Tepatkan sampai tanda tera dengan air suling, aduk dan biarkan 5 – 10 menit, saring dengan kertas saring Whatman No. 12;
6. Ambil 50 mL filtrat masukkan ke dalam erlenmeyer 125 mL, tambahkan 6 – 8 tetes indikator Titan yellow dan titar dengan larutan standar BAC.
% K2O = (mL penambahan STPB – mL BAC) x F 𝑥 = 100
100−KA
3.5.4 C-organik (C : SNI 7763-2018)
C-organik ditetapkan dengan cara pengabuan pada suhu (550 – 600) °C, sehingga bahan organik menjadi CO2 dan logam menjadi oksida logamnya. Bobot bahan yang hilang merupakan bahan organik yang dapat dikonversi menjadi kadar C-organik setelah dikalikan faktor 0,58
Peralatan
a. Neraca analitik dengan ketelitian 0,1 mg; b. Tanur;
17 c. Cawan porselen; d) Desikator
Cara kerja
a. Masukkan contoh setelah penetapan kadar air ke dalam tanur.
b. Abukan mula-mula pada suhu 300 °C selama 1,5 jam dan selanjutnya pada suhu (550 – 600) °C selama 2,5 jam atau lebih.
c. Matikan tanur dan biarkan hingga dingin.
d. Dinginkan contoh dalam desikator kemudian timbang. Perhitungan
Kadar abu = w₂
w₁100%
Kadar bahan organik (%) = 100 % (% kadar air % kadar abu) Kadar C-organik (%) = % kadar bahan organik 0,58 fk Keterangan
w2 adalah berat abu, g w1 adalah berat contoh, g
0,58 adalah faktor konversi bahan organik ke C-organik; fk adalah faktor koreksi kadar air.
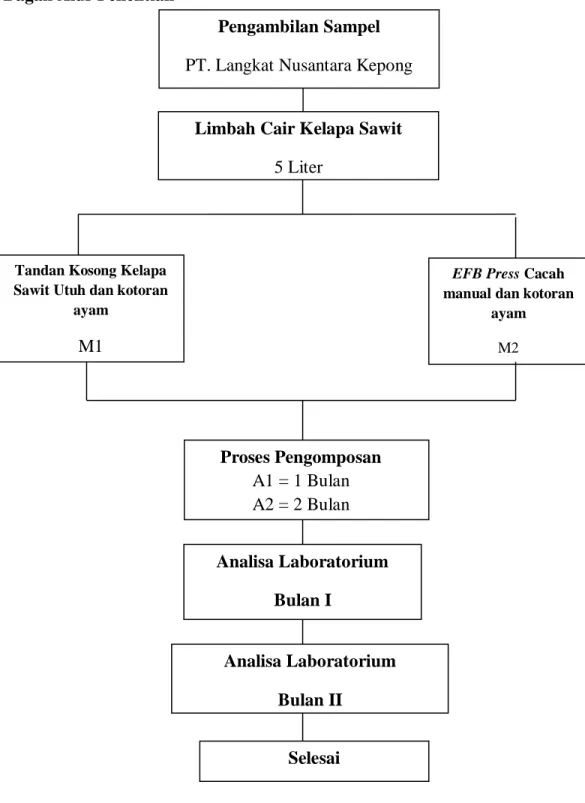
18 3.6 Bagan Alur Penelitian
Gambar 3.1 Bagan Alur Penelitian
EFB Press Cacah manual dan kotoran
ayam M2 Proses Pengomposan A1 = 1 Bulan A2 = 2 Bulan Analisa Laboratorium Bulan I Analisa Laboratorium Bulan II Selesai Pengambilan Sampel PT. Langkat Nusantara Kepong
P
Limbah Cair Kelapa Sawit 5 Liter
Tandan Kosong Kelapa Sawit Utuh dan kotoran
ayam M1
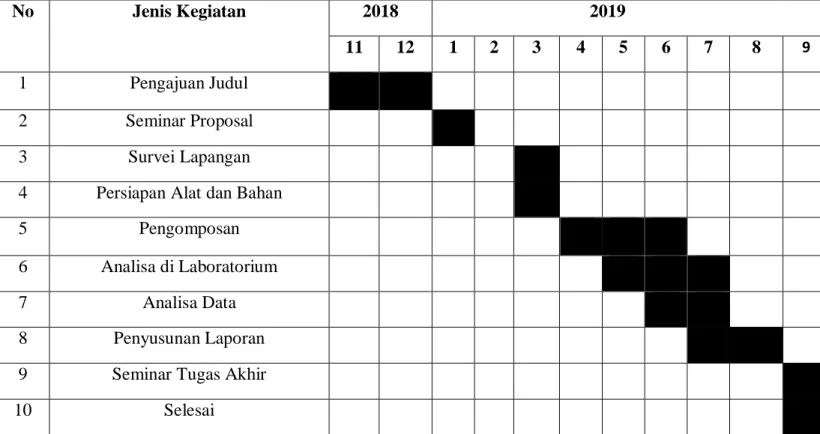
19 3.7 Jadwal Penelitian
Table 3.1. Jadwal Penelitian
No Jenis Kegiatan 2018 2019
11 12 1 2 3 4 5 6 7 8 9
1 Pengajuan Judul
2 Seminar Proposal
3 Survei Lapangan
4 Persiapan Alat dan Bahan
5 Pengomposan
6 Analisa di Laboratorium
7 Analisa Data
8 Penyusunan Laporan
9 Seminar Tugas Akhir