PENGARUH KONSENTRASI H
2SO
4, LAMA WAKTU HIDROLISIS
DAN FERMENTASI TERHADAP KADAR BIOETANOL YANG
DIHASILKAN RUMPUT LAUT
Eucheuma cottonii
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Pendidikan
Program Studi Pendidikan Biologi
Oleh :
Tegar Yudha Restuti NIM : 101434025
PROGRAM STUDI PENDIDIKAN BIOLOGI
JURUSAN PENDIDIKAN MATEMATIKA DAN ILMU PENGETAHUAN ALAM
FAKULTAS KEGURUAN DAN ILMU PENDIDIKAN UNIVERSITAS SANATA DHARMA
i
PENGARUH KONSENTRASI H
2SO
4, LAMA WAKTU HIDROLISIS
DAN FERMENTASI TERHADAP KADAR BIOETANOL YANG
DIHASILKAN RUMPUT LAUT
Eucheuma cottonii
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Pendidikan
Program Studi Pendidikan Biologi
Oleh :
Tegar Yudha Restuti NIM : 101434025
PROGRAM STUDI PENDIDIKAN BIOLOGI
JURUSAN PENDIDIKAN MATEMATIKA DAN ILMU PENGETAHUAN ALAM
FAKULTAS KEGURUAN DAN ILMU PENDIDIKAN UNIVERSITAS SANATA DHARMA
iv
HALAMAN PERSEMBAHAN
“Barang siapa merintis jalan mencari ilmu maka Allah akan memudahkan
baginya jalan ke surga”
(H.R Muslim)
Kupersembahkan karya kecil ini untuk :
Tuhan Yang Maha Esa yang selalu menaungi langkahku
dengan rahmat-Nya
Papa, Mama, Dian dan Anti yang senantiasa mencurahkan
kasih sayang dan do’a mereka untukku
Eugenius Audax .A yang selalu memberi pancaran semangat
dalam penulisan ini
vii ABSTRAK
PENGARUH KONSENTRASI H2SO4, LAMA WAKTU HIDROLISIS DAN
FERMENTASI TERHADAP KADAR BIOETANOL YANG DIHASILKAN RUMPUT LAUT Eucheuma cottonii
Tegar Yudha Restuti
Program Studi Pendidikan Biologi, Universitas Sanata Dharma, Yogyakarta. 2014
Indonesia memiliki beragam sumber daya laut yang dapat dijadikan sebagai sumber energi alternatif. Produksi rumput laut di Indonesia selalu mengalami peningkatan tiap tahun. Rumput laut jenis Eucheuma cottonii mengandung karbohidrat 58% sehingga mampu dijadikan bioetanol melalui proses fermentasi. Tujuan penelitian ini adalah untuk mengetahui pengaruh konsentrasi H2SO4, lama waktu hidrolisis dan fermentasi terhadap kadar bioetanol yang dihasilkan rumput laut Eucheuma cottonii.
Jenis penelitian ini adalah eksperimental laboratoris. Hidrolisis asam dilakukan dengan H2SO4 konsentrasi 0,2M, 0,3M, 0,4M, 0,5M dan variasi waktu 30 menit, 60 menit, 120 menit. Pengujian kadar glukosa dalam rumput laut dilakukan dengan menggunakan metode DNS. Fermentasi dilakukan dengan khamir Saccharomyces cerevisiae dengan waktu inkubasi 1 hari, 3 hari, 6 hari, dan 8 hari. Pengukuran kadar etanol dilakukan menggunakan titrasi iodometri. Analisis data menggunakan metode statistik regresi linier.
Hasil penelitian menunjukkan kondisi terbaik hidrolisis dikonsentrasi H2SO4 0,4M dan waktu 120 menit (7 ppm). Selama proses fermentasi, kadar bioetanol maksimum dicapai pada waktu inkubasi 6 hari yaitu 5,56%. Kesimpulan dari penelitian ini adalah konsentrasi H2SO4, lama waktu hidrolisis dan fermentasi mempengaruhi kadar bioetanol yang dihasilkan rumput laut Eucheuma cottonii.
viii ABSTRACT
EFFECT OF H2SO4 CONCENTRATION, DURATION TIME OF HYDROLYSIS
AND FERMENTATION TO THE LEVEL OF BIOETHANOL PRODUCED BY Eucheuma cottonii SEAWEED
TegarYudhaRestuti
Biology Education Study Program, Sanata Dharma University, Yogyakarta. 2014
Indonesia has various kind of marine resources that can be used as an alternative energy source. Seaweed production in Indonesia always increases each year. Eucheuma cottonii seaweed contains 58% carbohydrates so that they can be used as bioethanol through fermentation process. The purpose of this study was to determine the effect of H2SO4 concentration, duration of hydrolysis and fermentation to bioethanol levels produced by Eucheuma cottonii seaweed.
This research is an experimental laboratory. Acid hydrolysis was conducted with H2SO4 concentration of 0.2 M, 0.3 M, 0,4M, 0.5M and it took 30 minutes, 60 minutes, 120 minutes. The testing of glucose levels in seaweed was done by using the DNS method. Fermentation was carried out with the yeast Saccharomyces cerevisiae with incubation time of 1 day, 3 days, 6 days, and 8 days. The measurement of ethanol level was done byusing iodometric titration. Analysis of the data use the linear regression statistical.
The result of the research showed the best conditions 0,4M hydrolysis of concentrated H2SO4 and time of 120 minutes (7 ppm). During the fermentation process, the maximum of ethanol level was achieved at an incubation time of 6 days, it was 5.56%. The conclusion of this study is the concentration of H2SO4, duration time of hydrolysis and fermentation affect the levels of bioethanol produced by Eucheuma cottonii seaweed.
ix
KATA PENGANTAR
Puji syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas segala
berkat dan karunia-NYA sehingga penulis dapat menyelesaikan skripsi yang berjudul “Pengaruh Konsentrasi H2SO4, Lama Waktu Hidrolisis dan Fermentasi Terhadap Kadar Bioetanol yang Dihasilkan Rumput Laut Eucheuma cottonii”. Skripsi ini disusun guna memenuhi salah satu persyaratan akademik untuk menyelesaikan
Program Sarjana Pendidikan Biologi Universitas Sanata Dharma Yogyakarta.
Dalam proses penyusunan skripsi ini, penulis banyak memperoleh bantuan
dan dorongan semangat dari berbagai pihak. Untuk itu penulis ingin menyampaikan
terimakasih yang sebesar-besarnya kepada berbagai pihak atas bantuan yang telah
diberikan, baik waktu dan tenaga sehingga penulisan skripsi ini dapat diselesaikan
sebagaimana mestinya. Ucapan terimakasih penulis sampaikan kepada:
1. Bapak Rohandi, Ph.D selaku Dekan Fakultas Keguruan dan Ilmu Pendidikan
Universitas Sanata Dharma.
2. Ibu Ch. Retno Herrani Setyati, M.Biotech selaku Dosen Pembimbing skripsi
yang telah begitu sabar dalam mendampingi penulisan skripsi ini dan telah
meluangkan banyak waktu untuk membimbing penulis.
3. Segenap Dosen Pendidikan Biologi Universitas Sanata Dharma yang telah
memberikan ilmu, wawasan dan pengetahuan yang banyak bermanfaat bagi
penulis.
4. Segenap staf sekretariat JPMIPA (Mas Arif, Pak Sugeng, Mbak Tari dan Mas
Agus) yang telah memberikan pelayanan akademik secara prima.
5. Ir. Teguh Rahjudi dan Wahyu Dwi Wadyowati sebagai Ayah dan Ibu yang
selalu mendukung baik berupa materi, semangat dan doa kepada penulis selama
x
6. Dian Wirabuana dan Kurnia Wijayanti sebagai adik yang selalu mendukung
baik berupa semangat dan doa kepada penulis.
7. Eugenius Audax Aditya yang selalu mendukung baik berupa materi, memberi
semangat yang tak henti-hentinya, kasih sayang dan doa kepada penulis.
8. Teman-teman seperjuangan (Ardy, Fery, Yolanda, Nesya, Daus, Mela, Wiwik,
Tri) dan seluruh rekan-rekan Pendidikan Biologi USD angkatan 2010 atas
kerjasama dan bantuannya.
9. Teman-teman kost Aulia tercinta (Mbak Sandhi, Lia, Gita) atas dukungan dan
doanya selama penulis menyusun skripsi.
10.Amung, Ricky, Theo, Gilang, Koido, Alex, Alif, Isnaeni, Lukas, Renny, Ony,
Koh Ben, dan Kak Aski yang memberikan pengiburan selama penulisan skripsi
ini
11.Semua pihak yang telah membatu dan tidak dapat penulis sebutkan satu persatu.
Dukungan kalian berharga untuk penulis hingga dapat menyelesaikan skripsi
ini.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna, oleh sebab itu
penulis terbuka terhadap kritik dan saran dari pembaca. Kritik dan saran yang
membangun menjadi pembelajaran bagi penulis untuk menjadi lebih baik. Semoga
skripsi ini bermanfaat dan dapat menjadi sumbangan ilmu pengetahuan untuk
meningkatkan pengetahuan masyarakat terhadap pembuatan bioetanol dari rumput laut.
xi DAFTAR ISI
HALAMAN JUDUL ……….. i
HALAMAN PERSETUJUAN PEMBIMBING ………... ii
HALAMAN PENGESAHAN ………...iii
HALAMAN PERSEMBAHAN ………. iv
PERNYATAAN KEASLIAN KARYA ……….... v
PERNYATAAN PERSETUJUAN PUBLIKASI ………... vi
ABSTRAK ………...vii
ABSTRACT………...viii
KATA PENGANTAR ……… ix
DAFTAR ISI ……….. xi
DAFTAR TABEL ……….xiv
DAFTAR GAMBAR ……….xv
DAFTAR LAMPIRAN ……….xvi
BAB I. PENDAHULUAN A. Latar Belakang ……… 1
B. Rumusan Masalah ………... 4
C. Tujuan Penelitian ……… 4
D. Batasan Masalah ………. 4
E. Manfaat Penelitian ……….. 5
BAB II. TINJAUAN PUSTAKA A. Tinjauan Umum Rumput Laut ……… 6
1. Alga Hijau (Cholrophyceae) ………. 6
xii
3. Alga Merah (Rhodophyceae) ……… 8
B. Prospek Ekonomi Rumput Laut ……….. 9
C. Kandungan Nutrisi dan Manfaat Rumput Laut ………..11
1. Kandungan Nutrisi Rumput laut ………..11
2. Manfaat Rumput Laut ………...11
D. Eucheuma cottonii………..12
a. Morfologi Eucheuma cotonii………...13
b. Habitat Eucheuma cottonii ………...14
c. Klasifikasi Eucheuma cottonii……….14
d. Komposisi dan Manfaat Kimia Eucheumacottonii………..15
e. Persebaran Eucheuma cottonii di Indonesia ………16
E. Bioetanol ………16
F. Fermentasi ………..………19
G. Khamir (Saccharomyces cerevisiae) ………...………...22
H. Penelitian yang Relevan …………...………..25
I. Kerangka Pemikiran ………...26
J. Hipotesis ……….28
BAB III. METODE PENELITIAN A. Jenis Penelitian ………...29
B. Populasi dan Sampel Penelitian ……….29
1. Populasi ………29
2. Sampel ………..30
C. Tempat dan Waktu Penelitian ………30
D. Desain Penelitian ………30
E. Alat dan Bahan ………...31
F. Prosedur Kerja ………31
xiii
2. Hidrolisis Asam ………32
3. Pengujian Glukosa dengan Metode DNS ……….33
4. Regenerasi Kultur ………34
5. Pembuatan Media dan Fermentasi ………...35
6. Pengukuran Kadar Etanol ………35
G. Teknik Pengumpulan Data ……….36
1. Pengujian Glukosa ………...36
2. Pengukuran Kadar Etanol ………37
3. Pengujian pH ………38
H. Cara Analisis Data ……….38
BAB IV. HASIL DAN PEMBAHASAN A. Data dan Analisis Hasil Penelitian ……….39
1. Uji Glukosa ………..39
2. Uji Kadar Etanol ………..43
B. Pembahasan ………44
1. Uji Kadar Glukosa ………...45
2. Uji Kadar Etanol ………..47
BAB V. IMPLEMENTASI HASIL PENELITIAN UNTUK PEMBELAJARAN ………51
BAB VI. KESIMPULAN DAN SARAN A. Kesimpulan ………53
B. Saran ………..53
DAFTAR PUSTAKA ……… ..55
xiv
DAFTAR TABEL
Tabel 1. Perkembangan Ekspor-Impor Rumput Laut Indonesia ………...10
Tabel 2. Negara Tujuan Ekspor Rumput Laut Indonesia diurutkan berdasarkan Volume
Ekspor Terbesar ………..10
Tabel 3. Hasil Uji Laboratorium Kandungan Nutrisi Rumput Laut Kering …………..15
Tabel 4. Absorbansi pada Larutan Standar ………39
Tabel 5. Kadar Glukosa pada Larutan Sampel ………..41
xv
DAFTAR GAMBAR
Gambar 1. Alga Hijau berbentuk seperti filament ……….. 7
Gambar 2. Ulva lactuta (alga hijau berbentuk lembaran) ...………... 7
Gambar 3. Alga Coklat jenis Fucus ……… 8
Gambar 4. Alga Merah (Rhodophyceae) ……… 8
Gambar 5. Eucheuma cottonii………14
Gambar 6. Saccharomyces cerevisiae dari mikroskop ………..24
Gambar 7. Alur Kerangka Pemikiran ………27
Gambar 8. Diagram Alir Hidrolisis Asam ……….32
Gambar 9. Diagram Alir Pengujian Glukosa dengan Metode DNS ………..33
Gambar 10. Diagram Alir Regenari Kultur ………...34
Gambar 11. Diagram Alir Pembuatan Media dan Fermentasi ………...35
Gambar 12. Kurva Standar Glukosa ………..40
Gambar 13. Grafik Pengaruh Perbedaan Konsentrasi H2SO4 terhadap Kadar Glukosa ………...42
Gambar 14. Grafik Pengaruh Perbedaan Lama Waktu Hidrolisis terhadap Kadar Glukosa ………...42
xvi
DAFTAR LAMPIRAN
Lampiran 1. Perhitungan Kurva Standar Glukosa dengan Regresi Linier ……….59
Lampiran 2. Perhitungan Uji Kadar Etanol Menggunakan Metode Titrasi Iodometri ..61
Lampiran 3. Perhitungan Uji Kadar Etanol pada Fermentasi Hari ke-6 dengan Penambahan Glukosa 150 gram/L ………...63
Lampiran 4. Cara Pembuatan Larutan Reagen untuk Titrasi Iodometri……….64
Lampiran 5. Silabus ….………..65
Lampiran 6. Rencana Pelaksanaan Pembelajaran (RPP) ………...68
1 BAB I
PENDAHULUAN
A. Latar Belakang
Seiring dengan meningkatnya populasi manusia maka terjadi peningkatan
kebutuhan energi untuk kelangsungan hidup manusia dalam melakukan aktivitas
ekonomi dan sosial. Dalam melakukan aktivitasnya dan memenuhi kebutuhan
hidupnya, manusia tidak lepas dari sarana transportasi dan industri. Pertambahan
jumlah penduduk meningkatkan kebutuhan akan transportasi dan aktivitas industri.
Hal ini berakibat pada peningkatan kebutuhan dan konsumsi bahan bakar minyak
(BBM) yang merupakan sumber daya alam yang tidak dapat diperbaharui.
Permasalahan energi bagi kelangsungan hidup manusia merupakan masalah
besar yang dihadapi oleh hampir seluruh negara di dunia. Kebutuhan energi saat ini
pada umumnya didominasi oleh energi fosil yaitu minyak bumi, gas bumi dan
batubara. Energi fosil khususnya minyak bumi, merupakan sumber energi utama
dan merupakan sumber devisa negara. Indonesia mengalami penurunan produksi
minyak nasional akibat menurunnya cadangan minyak pada sumur-sumur produksi
secara alamiah. Krisis Bahan Bakar Minyak (BBM) baru-baru ini menunjukkan
cadangan energi fosil yang dimiliki Indonesia terbatas jumlahnya.
Pemerintah telah mengeluarkan Peraturan Presiden Republik Indonesia
sumber energi alternatif sebagai pengganti BBM. Bahan bakar nabati diharapkan
dapat mengurangi terjadinya kelangkaan BBM.
Indonesia memiliki beragam sumber daya yang dapat dijadikan sebagai
sumber energi. Dua pertiga luas wilayah Indonesia adalah lautan yang mempunyai
potensi sumberdaya alam yang sangat penting bagi kehidupan bangsa. Potensi
tersebut perlu dikelola secara tepat agar dapat dimanfaatkan secara optimal dan
lestari bagi kesejahteraan rakyat.
Pemerintah telah mengupayakan berbagai usaha dalam peningkatan
produksi hasil laut tersebut. Salah satu sumber daya laut yang cukup potensial untuk
dapat dimanfaatkan adalah rumput laut. Saat ini pemerintah tengah menggalakkan
peningkatan produksi rumput laut. Produksi rumput laut di Indonesia dari tahun ke
tahun selalu mengalami peningkatan. Pada dua tahun terakhir yaitu 2012 dan 2013
produksi rumput laut mencapai 5,1 juta ton dan 7,5 juta ton (Ditjen Perikanan
Budidaya Departemen Kelautan dan Perikanan, 2013). Jenis Gracilaria sp.,
Eucheuma sp. (Rodhophyta), Sargassum sp., Turbinaria sp. (Phaeophyta), dan Ulva
sp. (Chlorophyta) merupakan jenis rumput laut yang banyak ditemukan dan cukup
melimpah. Potensi yang sedemikian besar ini belum dimanfaatkan secara optimal
oleh masyarakat.
Wilayah pesisir pantai Kabupaten Jepara memiliki potensi budidaya rumput
laut. Jenis rumput laut yang sudah dibudidayakan adalah Eucheuma cottonii.
ton/Ha. Produk yang dihasilkan tersebut oleh para petani biasa dipasarkan ke pabrik
pengolah rumput laut ataupun ke konsumen secara langsung.. Akan tetapi potensi
daerah untuk pembudidayaan rumput laut Eucheuma cottonii masih sangat besar.
Dari 1.274 Ha lahan yang tersedia, baru 282 Ha lahan yang digunakan. Peluang dan
potensi pembudidayaan rumput laut Eucheuma cottnii di Jepara masih sangat besar
apabila rumput laut tersebut akan dimanfaatkan sebagai penghasil bioetanol (Dinas
Kelautan dan Perikanan Kabupaten Jepara, 2013).
Rumput laut Eucheuma cottonii banyak mengandung karbohidrat, 58%
kandungan rumput laut ini adalah karbohidrat. Bahan yang mengandung
karbohidrat atau glukosa tinggi mampu dijadikan bioetanol melalui proses
fermentasi. Bioetanol merupakan etanol yang berasal dari sumber hayati. Bioetanol
bersumber dari gula sederhana, amilum dan selulosa. Amilum yang berbentuk
polisakarida dapat dihidrolisis menjadi glukosa melalui pemanasan, menggunakan
katalis asam kuat berupa H2SO4. Glukosa selanjutnya difermentasi menghasilkan
etanol.
Fermentasi etanol merupakan aktivitas penguraian gula (karbohidrat)
menjadi etanol dengan mengeluarkan gas CO2, fermentasi ini dilakukan dalam
kondisi anaerob menggunakan Saccharomyces cerevisiae. Oleh karena itu
penelitian ini bertujuan untuk mengetahui pengaruh konsentrasi H2SO4, lama waktu
hidrolisis dan fermentasi terhadap kadar bioetanol yang dihasilkan rumput laut
B. Rumusan Masalah
Apakah konsentrasi H2SO4, lama waktu hidrolisis dan lama waktu fermentasi
berpengaruh terhadap kadar etanol yang dihasilkan dari fermentasi rumput laut
Eucheuma cottonii ?
C. Tujuan Penelitian
Untuk mengetahui pengaruh konsentrasi H2SO4, lama waktu hidrolisis dan lama
waktu fermentasi terhadap kadar etanol yang dihasilkan dari fermentasi rumput laut
Eucheuma cottonii
D. Batasan Masalah
Dalam penulisan skripsi ini, penulis memberikan batasan masalah agar
dalam penjelasannya nanti akan lebih mudah, terarah dan sesuai dengan yang
diharapkan serta terorganisir dengan baik. Pembuatan skripsi ini dibatasi pada
masalah sebagai berikut:
1. Dalam penelitian ini sampel yang digunakan adalah rumput laut Eucheuma
cottonii kering tawar yang diambil dari perairan pantai kabupaten Jepara
2. Dalam penelitian ini hasil fermentasi diuji kadar etanolnya menggunakan
metode titrasi iodometri
E. Manfaat penelitian
Beberapa manfaat yang ingin dicapai dari penelitian ini sebagai berikut:
1. Bagi Masyarakat
Memberikan informasi kepada masyarakat mengenai potensi dan pemanfaatan
rumput laut Eucheuma cottonii sebagai penghasil bioetanol.
2. Bagi Guru/Penulis
a. Melatih kemampuan penulis untuk memecahkan masalah dan menuangkan
ke dalam karya tulis ilmiah.
b. Melatih mengembangkan potensi dan keterampilan proses ilmiah serta
membantu siswa mengenal dan mendekatkan diri pada objek atau persoalan
biologi.
3. Bagi Pengembangan Pengetahuan
Memperluas dan mengembangkan ilmu pengetahuan, khususnya di bidang
6 BAB II
TINJAUAN PUSTAKA
A. Tinjauan Umum Rumput Laut
Rumput laut adalah salah satu sumberdaya hayati dan merupakan ganggang
multiseluler golongan Devisi Thallophyta. Jenis rumput laut sangat beragam, mulai
dari yang berbentuk bulat, pipih, tabung atau seperti ranting dahan
bercabang-cabang. Rumput laut memiliki klorofil atau pigmen warna yang lain. Rumput laut
terdiri dari satu atau banyak sel, berbentuk koloni, hidupnya bersifat bentik di
daerah perairan yang dangkal, berpasir, berlumpur atau berpasir dan berlumpur,
daerah pasut, jernih dan biasanya menempel pada karang mati baik terbentuk secara
alamiah atau buatan (Suparman, 2013).
Komoditas rumput laut yang banyak dimanfaatkan di Indonesia sebagai
bahan mentah industri adalah dari kelas Rhodophyceae dan Phaeophyceae. Alga
yang lebih besar terbagi tiga kelas besar yaitu, Chlorophyceae, Rhodophyta dan
Phaeophyceae (McConnaughey dan Robert, 1983).
1. Alga Hijau (Cholrophyceae)
Alga hijau atau green seaweed banyak dijumpai di lautan dangkal dan
biasanya dalam bentuk lembaran. Warna hijau dari alga hijau ini berasal dari
pigmen pada kloroplas yang berfungsi untuk fotosintesis, yaitu klorofil-a dan
klorofil-b serta karotinoid. Alga hijau menghasilkan dinding sel yang sebagian
bentuk yang beragam, tetapi bentuk yang umum dijumpai adalah bentuk seperti
benang (filament) dengan atau tanpa sekat dan bentuk lembaran (Suparman,
2013).
Gb 1. Alga Hijau berbentuk seperti filament Gb 2. Ulva lactuta (bentuk lembaran)
2. Alga Coklat (Phaeophyceae)
Alga coklat atau brown seaweed ini biasa dijumpai di daerah sub tropis
dan kutub. Tidak semua alga coklat merupakan tumbuhan laut, ada juga
sebagian yang hidup di air tawar meski tidak banyak (Suparman, 2013). Alga
coklat berada di semua samudra dan kerapkali unggul dalam flora alga di
perairan sedang sampai dingin. Bagian terbanyak didapati dekat pantai dalam air
yang tidak lebih dalam dari 20 meter (McConnaughey dan Robert, 1983).
Pada umumnya, alga coklat memiliki ukuran lebih besar bila
dibandingkan dengan kelompok rumput laut lain dan bentuknya sangat beraneka
ragam. Alga coklat terdiri dari klorofil yang ditutupi oleh pigmen-pigmen
Gb 3. Alga Coklat jenis Fucus
3. Alga Merah (Rhodophyceae)
Alga merah atau red seaweed banyak tumbuh di bagian laut yang paling
dalam sekitar 879 kaki di daerah bawah litoral yang kurang cahaya. Warna
merah pada rumput laut ini adalah unsur vital yang menunjang kelangsungan
hidupnya dan mempunyai peranan yang serupa dengan klorofil yaitu menyerap
cahaya biru dan ungu matahari yang menembus air laut (Suparman, 2013). Alga
merah didapati di semua laut termasuk laut di kutub tetapi paling baik
dikembangkan di daerah tropik (McConnaughey dan Robert, 1983).
Gb 4. Alga Merah (Rhodophyceae)
Pada umumnya alga merah berukuran kecil, mempunyai
pigmen-pigmen kromatotrof yang terdiri dari klorofil dan santofil, karotena, fikoeretin
dan fikosianin. Sekelompok tumbuhan ini ada yang disebut koralin yang dapat
koralin dapat dijumpai pada terumbu karang dan membentuk kerak merah muda
pada batu karang. Banyak jenis alga merah yang mempunyai nilai ekonomi
tinggi dan menjadi komoditi dan menjadi komoditi rumput laut yang
diperdagangkan (Suparman, 2013).
B. Prospek Ekonomi Rumput Laut
Perkembangan industri pengolahan rumput laut di Indonesia makin pesat.
Hasil laut Indonesia begitu kaya dan memikat. Karena itu tak heran jika rumput laut
memiliki pasar potensial dan cukup loyal. Tidak hanya pada level dalam negeri
tetapi juga luar negeri. Dengan kata lain rumput laut memiliki peluang ekspor yang
cukup lebar.
Menurut data yang dilansir oleh Fahmi Tri Wendrawan, Indonesia memiliki
peluang dan potensi budidaya komoditi laut yang sangat besar untuk
dikembangkan. Luas potensi budidaya laut diperkirakan mencapai 26 juta Ha.
Kurang lebih dua juta ha di antaranya sangat potensial untuk pengembangan rumput
laut dengan potensi produksi rumput laut kering rata-rata 16 ton per Ha. Potensi
rumput laut Indonesia dapat menjadi salah satu sumber pemasukan bagi devisa
negara, dan juga mampu menjadikan Indonesia sebagai negara pengekspor rumput
laut kering terbesar dunia.
Estimasi kebutuhan bahan baku rumput laut penghasil karagenan pada
tahun 2010 sebesar 322.500 ton yang terdiri dari Euchema sp. sebesar 274.100 ton
pasar rumput laut dunia masih sangat besar, baik untuk pasar bahan baku mentah
(raw seaweeds) ataupun untuk produk olahannya.
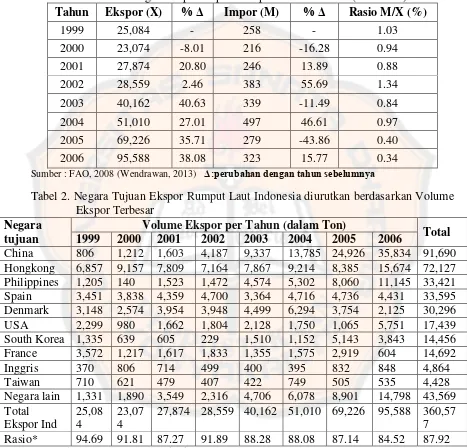
Tabel 1. Perkembangan Ekspor-Impor Rumput Laut Indonesia (dalam ton)
Tahun Ekspor (X) % Δ Impor (M) % Δ Rasio M/X (%) Sumber : FAO, 2008 (Wendrawan, 2013) Δ:perubahan dengan tahun sebelumnya
Tabel 2. Negara Tujuan Ekspor Rumput Laut Indonesia diurutkan berdasarkan Volume Ekspor Terbesar
Negara tujuan
Volume Ekspor per Tahun (dalam Ton)
Total
Sumber : DKP, 2008 (Rajagukguk, 2009)
Saat ini Perancis adalah negara tujuan utama bagi negara-negara produsen
Chili. Sedangkan pemasok lainnya adalah Indonesia, China dan Jepang. Di antara
lima pemasok, Indonesia tercatat mengalami tingkat pertumbuhan tertinggi tahun
2008 lebih dari 500%, hal ini diikuti oleh Filipina dengan 75,3% (Kementrian
Kelautan dan Perikanan, 2010).
C. Kandungan Nutrisi dan Manfaat Rumput Laut
1. Kandungan Nutrisi Rumput laut
Rumput laut mempunyai kandungan nutrisi cukup lengkap. Secara
kimia rumput laut terdiri dari air 27,8%;protein 5,4%;karbohidrat 33,3%;lemak
8,6%;serat kasar 3%;dan abu 22,25%, selain itu juga terdapat enzim, asam
nukleat,asam amino,yodium,vitamin (A,B,C,D,E dan K),dan makro mineral
seperti nitrogen,oksigen,kalsium dan selenium serta mikro mineral seperti zat
besi, magnesium dan natrium. Kandungan asam amino, vitamin dan mineral
dalam rumput laut mencapai 10-20 kali lipat dibandingkan dengan tanaman
darat (Suparman, 2013).
2. Manfaat Rumput Laut
Menurut Suparman(2013) rumput laut memiliki banyak manfaat, antara lain:
a. Aspek Ekologis
Rumput laut merupakan salah satu bagian penting dari ekosistem
pesisir, yang secara ekologis memiliki peranan dan fungsi ekologis yang
sama seperti dengan ekosistem pesisir lainnya seperti mangrove, lamun dan
b. Aspek Biologis
Rumput laut memiliki klorofil yang berperan dalam proses
fotosintesis di dalam perairan, sehingga tumbuhan ini memegang peran
sebagai produsen primer penghasil bahan organik dan oksigen di lingkungan
perairan.
c. Aspek Sosial
Budidaya rumput laut memberikan keuntungan bagi kehidupan
masyarakat di sekitar lokasi budidaya, di antaranya adalah tersedianya
kesempatan kerja dan peningkatan kesejahteraan masyarakat.
d. Segi Kesehatan
Sebagian besar orang hanya mengetahui bahwa rumput laut
digunakan untuk membuat agar-agar dan juga sushi. Lepas dari kedua hal
tersebut, ternyata rumput laut menyimpan banyak manfaat bagi tubuh
manusia. Antara lain adalah untuk diet, kecantikan, mencegah kanker,
mencegah penyakit stroke, mencegah terjadinya penurunan kecerdasan,
mencegah gejala osteoporosis, mencegah penyakit gangguan pencernaan,
meningkatkan daya tahan tubuh, mencegah anemia, mempercepat
penyembuhan luka, meningkatkan gairah seks.
D. Eucheuma cottonii
Indonesia terbukti merupakan penguasa 50 persen pangsa pasar produsen
yang sebagian besar hasilnya digunakan untuk bahan baku industri kosmetik atau
farmasi. Rumput laut jenis Eucheuma cottonii sangat diminati oleh negara-negara
Asia, Eropa dan Amerika. Khususnya Negara Prancis, Denmark, China, Filipina,
Hongkong, Spanyol, Jepang dan Amerika Serikat (Kementrian Kelautan dan
Perikanan, 2010).
Jenis Eucheuma oleh sebagian petani, pedagang diberi nama agar-agar.
Istilah lokal agar-agar bagi Eucheuma ini sedikit mengacaukan karena justru
Eucheuma bukan termasuk jenis rumput laut yang memproduksi agar-agar tetapi
memproduksi karagenan (karagen). Sedangkan jenis yang mengandung agar-agar
adalah dari jenis Gracilaria (Rambukasang) (Itung dan Marthen, 2003). Harga pasar
rumput laut kering Eucheuma cottonii di dunia untuk karagenan mencapai US$ 0,3
per kg. Rumput laut dalam bentuk olahan nilainya 10-20 kali lipat dari harga
karagenan atau sekitar US$ 6-10 per kg. lalu harga rumput laut kering di dalam
negeri berkisar antara Rp 9.000 per kg kering (Kementrian Kelautan dan Perikanan,
2010).
a. Morfologi Eucheuma cotonii
Eucheuma cottonii termasuk kelas dalam Rhodophyceae mempunyai
thallus yang silindris, berduri kecil-kecil dan menutupi thallus, percabangannya
tidak teratur sehingga merupakan lingkaran, ujungnya runcing berwarna coklat
Ada dua cara dalam pengembangbiakan rumput laut Eucheuma
cotonii, yaitu secara kawin (antar gamet-gamet) dan tidak kawin (vegetatif,
konjugatif dan penyebaran spora). Perkembiakan secara vegetatif buatan
dapat dilakukan dengan cara stek (Ditjen Perikanan Budidaya, 2011).
b. Habitat Eucheuma cottonii
Umumnya Eucheuma cottonii tumbuh dengan baik di daerah pantai
terumbu (reef). Habitat khasnya adalah daerah yang memperoleh aliran air laut
yang tetap, variasi suhu harian yang kecil dan menempel pada substrat batu
karang mati, kulit karang, atau benda keras lainnya (Ditjen Perikanan Budidaya,
2011). Rumput laut jenis ini lebih baik hidup diperairan dangkal karena
penetrasi matahari dapat mencapai rumput laut sehingga dapat berguna dalam
proses fotosintesis.
Jenis ini hidup di daerah pasang surut dengan kedalaman 30-50 cm
pada waktu surut terendah. Dengan suhu kisaran 26 – 32 °C, salinitas 28 – 34
mg/l, dan pada pH 7 – 8,5 (Ditjen Perikanan Budidaya, 2012).
c. Klasifikasi Eucheuma cottonii
Secara taksonomi rumput laut jenis Eucheuma dapat diklasifikasikan
sebagai berikut (Ditjen Perikanan dan Budidaya, 2011):
d. Komposisi dan Manfaat Kimia Eucheuma cottonii
1. Komposisi Kimia Eucheuma cottonii
Berikut ini komposisi kimia pada Eucheuma cottonii berdasarkan
hasil penelitian Wisnu dan Rachmawati (2009):
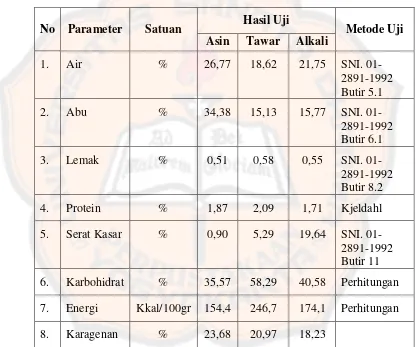
Tabel 3. Hasil Uji Laboratorium Kandungan Nutrisi Rumput Laut Kering
No Parameter Satuan Hasil Uji Metode Uji
Eucheuma sp. mengandung ekstrak karagenan yang bermanfaat
dan kelembaman (kenyal), penetral dan pemadat. Misalnya pembuatan bir,
wine, susu coklat, ice cream, dessert gels, saus, beef daging kaleng, ikan
kaleng, pasta gigi, air freshener, cream, coffe creamer serta dapat berfungsi
sebagai pupuk (Ditjen Perikanan Budidaya, 2011).
e. Persebaran Eucheuma cottonii di Indonesia
Secara alami jenis Eucheuma cottonii banyak dijumpai di perairan laut
Sulawesi, Kepulauan Maluku, Nusa Tenggara, Irian jaya dan Kepulauan Riau
(Ditjen Perikanan Budidaya, 2011). Sentra wilayah budidaya rumput laut jenis
ini terdapat di Sulawesi Tengah, Sulawesi Selatan, NTT, Bali, Jawa Timur,
Sulawesi Tenggara dan NTB (Suparman,2013).
E. Bioetanol
Etanol disebut juga dengan etil alkohol, alkohol murni, alkohol absolut
atau alkohol saja. Etanol merupakan cairan yang mudah menguap, mudah terbakar,
tak berwarna dan merupakan alkohol yang paling sering digunakan dalam
kehidupan sehari-hari. Etanol termasuk dalam alkohol rantai tunggal dengan rumus
kimia C2H5OH dan rumus empiris C2H5O. etanol sering disebut dengan EtOH
dengan Et merupakan singkatan dari gugus etil (C2H5). Etanol dapat diproduksi dari
bahan baku tanaman yang mengandung pati seperti, ubi kayu, ubi jalar, jagung atau
sagu. Etanol ini kemudian disebut dengan bioetanol (Dewi, 2011).
Produksi bioetanol dengan bakan baku seperti di atas dilakukan melalui
dari pati-patian. Proses pembuatannya dapat dibedakan berdasarkan zat pembantu
yang digunakan, yaitu hidrolisa asam (misalnya asama sulfat) dan hidrolisa enzim.
Namun, yang sering digunakan adalah hidrolisa enzim. Dalam proses konversi
karbohidrat menjadi gula (glukosa larut air) dilakukan dengan penambahan air dan
enzim. Kemudian dilakukan proses peragian atau fermentasi gula menjadi etanol
dengan menambahkan yeast atau ragi. Umumnya dalam pembuatan bioetanol
melalui tahapan gelatisasi dan fermentasi .
Gelatisasi adalah proses pengubahan pati menjadi glukosa dengan
bantuan enzim dan beberapa perlakuan seperti kenaikan suhu. Sementara itu,
fermentasi adalah perubahan dari glukosa menjadi alkohol (etanol). Pembuatan
etanol belum selesai pada tahapan ini. Setelah fermentasi alkohol hanya memiliki
kemurnian 30-40% dan belum dikategorikan fuel based etanol. Agar dapat
mencapai kemurnian di atas 95%, maka etanol ini harus melewati proses destilasi
(Dewi, 2011).
Sifat fisika dari etanol adalah bersifat polar disebabkan karena gugus
hidroksilnya (R-OH). Seperti air, etanol dapat membentuk ikatan hidrogen. Karena
adanya ikatan hidrogen ini maka etanol mempunyai titik didih yang lebih tinggi dari
senyawa lain yang mempunyai berat formula yang sama. Etanol juga mempunyai
nilai pH sebagai asam lemah. Mudah menguap meskipun pada suhu rendah, mudah
terbakar dan mendidih pada suhu 78°C. Etanol merupakan produk biokonversi dari
tergantung dari galurnya. Sebanyak 12-14 % alkohol dapat diproduksi secara cepat
jika digunakan galur yang tepat, tetapi semakin tinggi konsentrasi alkohol,
fermentasi semakin lambat, Walaupun laju awal produksi etanol meningkat pada
suhu lebih tinggi (Fardiaz, 1989). Konsentrasi alkohol yang dihasilkan dalam proses
fermentasi tergantung pada jenis khamir yang digunakan, kadar gula, dan efisiensi
fermentasi.
Berdasarkan kadar alkoholnya, etanol terbagi menjadi tiga grade,
diantaranya:
a. Grade industri dengan kadar alkohol 90-94 %.
b. Netral dengan kadar alkohol 96-99,5 %, umumnya digunakan untuk minuman
keras atau bahan baku farmasi.
c. Grade bahan bakar dengan kadar alkohol di atas 993 %.
Hambali et al. (2007) menyatakan bahwa berdasarkan jenis dan
manfaatya, etanol digolongkan menjadi tiga golongan yaitu:
1. Etanol prima
Etanol prima adalah etanol mutu tinggi dengan kadar 96-96,5 % (vlv), disebut
juga etanol murni dengan kadar minyak fusel yang sangat rendah (40 mg/l).
Etanol ini biasanya digunakan untuk minuman keras mutu tinggi, industri
2. Etanol teknis
Etanol teknis adalah etanol dengan kadar 92-94 % (vlv) dan merniliki kadar
minyak fusel antara 15-30 md. Etanol teknis ini digunakan dalam industri untuk
bahan bakar, bahan pelarut organik, bahan baku spirtus, dan bahan produk lain.
3. Etanol absolut
Etanol absolut adalah etanol dengan kadar yang sangat tinggi (795,5 % (vlv))
dan digunakan untuk obat-obatan, bahan pelarut, dan bahan antara produksi
senyawa lain.
F. Fermentasi
Fermentasi adalah suatu kegiatan penguraian gula yang tidak menimbulkan
bau busuk dan menghasilkan gas karbondioksida. Suatu fermentasi yang busuk
merupakan fermentasi yang mengalami kontaminasi. Fermentasi pembentukan
alkohol dari gula dilakukan oleh mikroba seperti bakteri, khamir dan jamur. Khamir
yang biasa digunakan adalah Saccharomyces cerevisiae. Perubahan yang terjadi
biasanya dinyatakan dalam persamaan reaksi berikut (Putra, 2011) :
C6H12O6 + Saccharomyces cerevisiae 2 C2H5OH + 2 CO2
Laju fermentasi dapat diketahui dari kadar kemurnian alkohol yang
dihasilkan dari proses fermentasi per satuan waktu. Kadar kemurnian alkohol yang
dihasilkan dari proses ini adalah kadar alkohol pada bioetanol yang terbentuk
selama proses fermentasi. Berikut ini merupakan persamaan untuk menentukan laju
Rumus Perhitungan Laju Fermentasi
Laju Fermentasi = ( )
( )
Mekanisme fermentasi ini terdiri atas 2 tahap, yaitu (Fardiaz 1989):
a. Pemecahan rantai karbon dari glukosa dan pelepasan paling sedikit 2 pasang
atom hidrogen menghasilkan senyawa karbon lainnya yang lebih mudah
teroksidasi dibandingakan glukosa.
b. Senyawa yang teroksidasi akan direduksi oleh hidrogen yang terlepas pada
tahap pertama dengan membentuk senyawa yang merupakan hasil
fermentasi.
Menurut Saroso (1998) dalam jurnalnya, fermentasi alkohol dipengaruhi
oleh beberapa faktor di antaranya:
a. Media
Media fermentasi harus steril dan mengandung nutrisi, seperti unsur C (faktor
karbohidrat), unsur N dan P (terdapat dalam pupuk), dan mineral-mineral serta
vitamin lainnya. Nutrisi ini nantinya akan digunakan oleh mikroba dalam
melakukan aktivitas, untuk pertumbuhan dan perkembangbiakan.
b. Pada umumnya bahan dasar yang mengandung senyawa organik terutama
glukosa dan pati dapat digunakan sebagai substrat pada proses fermentasi
c. Suhu
Suhu optimum bagi pertumbuban khamir dan aktivitasnya adalah 25-35°C.
d. Jenis mikroba
Mikroorganisme yang mampu menguraikan pati atau senyawa-senyawa
polisakarida menjadi alkohol adalah jenis khamir, dan yang paling banyak
digunakan adalah Saccharomycese cerevisiae.
e. Nutrisi
Selain sumber karbon, khamir juga memerlukan sumber N, vitamin (khususnya
biotin dan thiamin) dan mineral.
f. pH substrat atau media fermentasi merupakan salah satu faktor yang
menentukan kehidupan khamir. pH ideal untuk fermentasi alkoholik adalah pH
4-6.
Fermentasi glukosa menjadi etanol dan CO2 melibatkan enzim Embden
Meyerhof Parnas dan Glikolisis, yang meliputi (Fardiaz 1989):
a. Glukokinase, isomerase, fruktosa fosfokinase
b. Aldolase
c. Gliseroldehide-3-fosfat deidrogenase
d. 3-pospogliserat kinase
e. Pospogliserat mutase
f. Enolase
h. Piruvat dekarboksilase
i. Alkohol dehidrogenase
Enzim-enzim tersebut mengkatalis reaksi perubahan glukosa menjadi
piruvat (EMF') dan piruvat menjadi etanol dalam reaksi (Reed, G. Dan H.J, Peppler,
1973), sebagai berikut:
a. Glukosa + 2ATP Fruktosa 1,6-bifosfat + 2ATP
b. Fruktosa -1,6-bifosfat 2 Gliseroldehide -3-fosfat
c. Gliseroldehide -3-fosfat + 1Pi + NAD+ 1,3 bipospogliserat +
NADH + H+
d. 1,3 bipospogliserat + ADP 3 fosfogliserat + ATP
e. 3 fosfogliserat 2 fosfogliserat + H2O
f. 2 fosfogliserat 2 fosfoenol piruvat + H2O
g. 2 fosfoenol piruvat + ADP Piruvat + ATP
h. Piruvat CO2 + asetaldehid
i. Aselaldehid + NADH + H+ etanol + NAD
G. Khamir (Saccharomyces cerevisiae)
Menurut Oura, 1983 (Putra, 2011), Saccharomyces cerevisiae merupakan
salah satu spesies ragi yang memiliki daya konversi gula menjadi bioetanol dengan
baik. Mikroba ini biasanya dikenal dengan baker’s yeast dan metabolismenya telah
dipelajari dengan baik. Produk metabolik utama adalah bioetanol, CO2, dan air
bersifat fakultatif anaerobik. Saccharomyces cerevisiae memerlukan suhu 30°C dan
pH 4,0-4,6 agar dapat tumbuh dengan baik.
Ragi tumbuh optimum pada suhu 25-30°C dan maksimum pada 35-47°C.
Nilai pH untuk pertumbuhan ragi yang baik antara 3-6. Perubahan pH dapat
mempengaruhi pembentukan hasil samping fermentasi. Pada pH tinggi maka
konsentrasi gliserin akan naik dan juga berkorelasi positif antara pH dan
pembentukan asam piruvat. Pada pH tinggi maka lag phase akan berkurang dan
aktivitas fermentasi akan naik.
Khamir termasuk fungi, tetapi dibedakan dari kapang karena bentuknya
yang terutama uniseluler. Sebagai sel tunggal, khamir lebih cepat berkembang biak
dibanding dengan kapang. Sel khamir mempunyai ukuran yang bervariasi, yaitu
dengan panjang 1-5 pm, dan lebar 1-10 pm. Pada kondisi ideal sel khamir dapat
tumbuh menjadi dua sel dalam waktu 1-2 jam, tetapi setelah membentuk banyak
tunas, waktu generasi menjadi lebih lama sampai kira-kira 6 jam. Kebanyakan
khamir paling baik pada kondisi dengan persedian air cukup. Tetapi khamir dapat
tumbuh pada medium dengan konsentrasi gula atau garam lebih tinggi dari pada
bakteri (Fardiaz, 1989).
Beberapa faktor yang mempengaruhi pertumbuhan mikroorganisme
dalam bahan pangan yang difermentasi :
a. Ketersediaan karbon dan nitrogen, nutrisi khusus yang diperlukan
b. pH substrat, suhu inkubasi dan kelembaban
c. Tahap pertumbuhan mikroorganisme
d. Jumlah mikroorganisme pesaing
Khamir fermentatif dapat melakukan fermentasi alkohol, yaitu memecah
glukosa melalui galur glikolisis dengan total reaksi sebagai berikut:
C6H12O6 2 C2H5OH + 2 CO2
(Glukosa) (etanol) (karbondioksida)
Khamir yang bersifat fermentatif, jika diberi aerasi aktivitas
fermentasinya akan menurun, dan sebagian glukosa akan direspirasi (dioksidasi)
menjadi karbondioksida dan air. Pada khamir yang bersifat fermentif, 70 % dari
glukosa di dalam substrat akan diubah menjadi karbondioksida dan alkohol,
sedangkan sisanya sebanyak 30% tanpa adanya nitrogen akan digunakan kembali
melalui fermentasi endogenous jika glukosa di dalam medium sudah habis (Fardiaz,
1989).
Gb 6. Saccharomyces cerevisiae dari mikroskop
Saccharomyces cerevisiae memproduksi alkohol dalam jumlah besar dan
mempunyai toleransi terhadap kadar alkohol yang tinggi (Elevri, 2006).
fruktosa, galaktosa, maltose dan sedikit terhadap rafinosa. Ragi ini melakukan
reproduksi vegetatif dengan bertunas secara multipolar (tunas dapat berkembang
dari setiap bagian permukaan sel induk). Pertumbuhan ragi memerlukan kondisi
lingkungan yang cocok.
Beberapa kelebihan Saccharomyces dalam proses fermentasi adalah cepat
berkembang biak, tahan terhadap alkohol tinggi, tahan terhadap suhu tinggi, stabil
dan cepat beradaptasi. Beberapa spesies Saccharomyces mampu memproduksi
ethanol hingga 13.01 %. Hasil ini lebih bagus dibanding genus lainnya seperti
Candida dan Trochosporon.
H. Penelitian yang Relevan
Produksi bioetanol dari ubi garut yang memiliki kandungan karbohidrat
sekitar 85,2 gram per 100 gram mampu menghasilkan etanol dengan kadar 11%
(Mustofa, 2012). Dalam penelitian pembuatan bioetanol dari biji durian dengan
kandungan karbohidrat 43,6% mampu menghasilkan etanol dengan kadar 1,61%
(Minarni,dkk, 2013). Penelitian pembuatan bioetanol dari tepung biji nangka
dengan kandungan karbohidrat 36,7 gram per 100 gram mampu menghasilkan
etanol dengan kadar 1,75% (Purwanto, 2012). Penelitian pembuatan bioetanol dari
ubi kayu dengan kandungan karbohidrat 35% mampu menghasilkan etanol dengan
kadar 11% (Wardana, 2012). Penelitian pembuatan bioetanol dari pati garut dengan
kandungan karbohidrat 85,2 gram per 100 gram mampu menghasilkan etanol
bioetanol dari lamun dengan kandungan gula pereduksi sekitar 2% mampu
menghasilkan etanol 0,047 mL/g (Dewi, 2011).
Bahan-bahan yang digunakan dalam pembuatan bioetanol diatas adalah
bahan-bahan yang banyak mengandung karbohidrat. Rumput laut Eucheuma
cottonii juga banyak mengandung karbohidrat, sehingga rumput laut tersebut
mungkin juga mampu menghasilkan bioetanol.
I. Kerangka Pemikiran
Keterbatasan energi merupakan salah satu permasalahn utama dunia karena
konsumsi bahan bakar fosil yang semakin tinggi. Bioetanol adalah salah satu bahan
bakar alternative nonfosil yang diperoleh dari proses fermentasi biomassa yang
mengandung karbohidrat dengan bantuan mikroorganisme. Rumput laut Eucheuma
cottonii merupakan salah satu sumber daya laut Indonesia yang dapat digunakan
sebagai substrat fermentasi penghasil bioetanol karena mengandung karbohidrat
tinggi. Karbohidrat nantinya akan dikonversikan menjadi glukosa. Penggunaan
H2SO4 sebagai katalisator dalam proses hidrolisis dengan berbagai variasi
konsentrasi dan lama waktu pada saat hidrolisis perlu dilakukan agar diketahui pada
konsentrasi dan berapa lama waktu hidrolisis yang mampu menghasilkan glukosa
tinggi. Glukosa yang dihasilkan dari proses hidrolisis nantinya akan digunakan oleh
mikroorganisme dalam proses fermentasi. Kandungan glukosa dalam substrat
fermentasi akan mempengaruhi aktivitas mikroorganisme dalam menghasilkan
fermentasi agar diketahui pada lama waktu fermentasi yang mana dapat dihasilkan
kadar etanol yang tinggi. Alur dari kerangka pemikiran penelitian ini ditunjukkan
pada gambar 7.
J. Hipotesis
Konsentrasi H2SO4, lama waktu hidrolisis dan lama waktu fermentasi
mempengaruhi kadar etanol yang dihasilkan dari fermentasi rumput laut Eucheuma
29
BAB III
METODE PENELITIAN
A. Jenis Penelitian
Jenis penelitian ini berdasarkan keilmiahannya adalah Penelitian Ilmiah,
dimana dalam penelitian ini mengemukakan pokok-pokok pikiran, menyimpulkan
dengan melalui prosedur yang sistematis dengan menggunakan pembuktian
ilmiah/meyakinkan. Berdasarkan teknik yang digunakan penelitian ini termasuk
dalam Experiment Research (Penelitian Percobaan), dimana dilakukan perubahan
(ada perlakuan khusus) terhadap variabel yang diteliti. Dan berdasarkan tempat
penelitian, penelitian ini termasuk dalam Laboratory Research (Penelitian
Laboratorium), di mana penelitian ini dilaksanakan pada tempat tertentu /
laboratorium.
B. Populasi dan Sampel Penelitian
1. Populasi
Populasi merupakan keseluruhan dari subyek penelitian. Populasi dapat
berupa manusia, benda, gejala-gejala, pola hidup, tingkah laku, dan sebagainya.
Ada dua macam populasi dalam penelitian yaitu, populasi terhingga yang terdiri
dari elemen dengan jumlah tertentu dan populasi tak terhingga yang terdiri dari
elemen yang sukar dicari batasannya. Populasi tak terhingga dalam hal ini
populasi terhingga dalam penelitian ini adalah semua jenis rumput laut yang ada
di Pantai Bandengan Jepara.
2. Sampel
Sampel adalah sebagian atau merupakan wakil dari populasi yang
diteliti. Dalam penelitian ini sampel yang dipakai adalah rumput laut Eucheuma
cotonii. Alasan peneliti hanya mengambil Eucheuma cotonii sebagai sampel
yakni Eucheuma cotonii merupakan salah satu jenis rumput laut ekonomis yang
banyak terdapat di Indonesia dan merupakan rumput laut yang dibudidayakan di
Kabupaten Jepara.
C. Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan mulai bulan Desember 2013 – Juli 2014 di
Laboratorium Biologi, Jurusan Pendidikan Matematika dan IPA, dan Laboratorium
Kimia Universitas Kristen Satya Wacana.
D. Desain Penelitian
Variabel-variabel dalam penelitian ini adalah sebagai berikut:
- Variabel bebas : variasi konsentrasi H2SO4, lama waktu hidrolisis dan lama
waktu fermentasi
- Variabel terikat : kadar etanol yang dihasilkan dari fermentasi rumput laut
Eucheuma cottonii
- Variable kontrol : volume Sacchraomyces cerevisiae
Dalam perlakuan ini variasi konsentrasi H2SO4 yang digunakan yaitu
menit, 60 menit dan 120 menit. Variasi lama waktu fermentasi yaitu selama 1 hari,
3 hari, 6 hari dan 8 hari. Pengulangan dilakukan sebanyak 3 kali pada regenerasi
kultur untuk melihat keseragaman mikroorganisme yang tumbuh.
E. Alat dan Bahan
Alat – alat yang digunakan dalam penelitian ini di antaranya beker glass 2
L, ember, kompor listrik, pengaduk, timbangan digital, blender, pH meter, gelas
ukur, saringan, spatula, pipet volume, sarung tangan, jarum ose, labu Erlenmeyer,
thermometer, autoclave, inkubator, tabung reaksi, bioreaktor, oven, cawan porselen,
dan spektrofotometer UV-Vis (Shimadzu 1240).
Bahan – bahan yang digunakan dalam penelitian ini adalah rumput laut
Eucheuma cotonii kering yang diambil dari Pantai Jepara, gula pasir, H2SO4, ragi
Fermipan (Saccharomyces cerevisiae), PDA (Potato Dextrose Agar), PDB (Potato
Dextrose Broth), Asam Dinitrosalisilat (DNS), Aquades, Etanol, NPK, kalium
bikromat, pati, KI, dan Na-thiosulfat.
F. Prosedur Kerja
Penelitian ini terbagi dalam beberapa tahap yaitu preparasi sampel,
hidrolisis dengan asam H2SO4, pengukuran kadar glukosa, fermentasi menggunakan
khamir, dan yang terakhir pengukuran kadar etanol.
1. Preparasi Sampel
Rumput laut diambil dari perairan pantai Bandengan, Jepara pada
sampel rumput laut meliputi kedalaman, pH, suhu, salinitas dan oksigen terlarut
(DO).
Sampel rumput laut kering dicuci dengan air tawar, bertujuan untuk
menghilangkan rasa asin yang terkandung dalam rumput laut dan
menghilangkan kotoran-kotoran yang masih menempel pada rumput laut.
Kemudian dikeringkan di bawah sinar matahari untuk menghilangkan
kandungan air. Karena rumput laut kering tawar lebih banyak mengandung
karbohidrat. Setelah kering sampel dihaluskan dengan blender, dan diayak
sehingga didapatkan tepung ampas rumput laut.
2. Hidrolisis Asam
Hidrolisis asam ini dilakukan untuk mengkonversi karbohidrat yang
terkandung dalam sampel menjadi glukosa.
Gb 8. Diagram alir hidrolisis asam
100 gr sampel
Kemudian dilakukan pengenceran H2SO4 0,2; 0,3; 0,4 dan 0,5 M. masukkan kedalam erlemeyer
Ditambahkan sampel kedalam erlenmeyer berisi H2SO4 dipanaskan dalam waterbath variabel waktu selama 30 menit, 60 menit, dan 120 menit pada suhu
121°C
3. Pengujian Glukosa dengan Metode DNS
metode DNS merupakan salah satu metode yang dapat digunakan
untuk menentukan kadar gula reduksi dalam sampel yang mengandung
karbohidrat menggunakan pereaksi asam dinitro salisilat.
Gb 9. Diagram alir pengujian glukosa dengan metode DNS
Sampel hasil hidrolisis ditambahkan alkohol 70% dengan perbandingan 1 : 1
Sampel disaring menggunakan kertas saring, dan sisa padatan dicuci dengan alkohol hingga netral.
Filtrat dipanaskan pada penangas air 100°C selama 30 menit, lalu disaring
Dimasukkan 3 ml sampel ketabung reaksi dan 3 ml pereaksi DNS
Kemudian sampel dan pereaksi ditempatkan dalam penangas air mendidih selama 5 menit
4. Regenerasi Kultur
Khamir dalam bentuk ragi ini masih dalam keadaan tidak aktif. Oleh
karena itu perlu diaktifkan terlebih dahulu dengan dilakukan regenerasi kultur.
Gb 10. Diagram alir regenerasi kultur
diambil 5 gr ragi fermipan (Saccharomyces cerevisiae)
Ditambahkan 100 ml aquades dengan suhu 30°C difortex sampai larut dan homogen
Masukkan larutan ragi ke dalam agar miring PDA sebanyak 10 ml dengan cara ditebar dipermukaan media
dibiakkan dalam inkubator selama ± 48 jam dengan kondisi aerob pada suhu 30°C
inokulasikan biakan pada PDA sebanyak 5 jarum ose ke dalam PDB (Potato Dextrose Broth) sebanyak 200 ml
diinkubasi selama ± 48 jam dengan kondisi aerob pada suhu 30°C
5. Pembuatan media dan Fermentasi
Gb 11. Diagram alir pembuatan media dan fermentasi
6. Pengukuran Kadar Etanol
Kadar etanol hasil fermentasi di ukur secara kuantitatif menggunakan
metode Titrasi Iodometri. Kadar etanol fermentasi diukur secara kualitatif
dengan melihat adanya gelembung-gelembung pada gelas beker yang berisi air
saat proses fermentasi.
Larutan sampel sebanyak 100 ml ditambah 10 gr NPK dimasukkan kedalam fermentor
Disterilkan menggunakan waterbath dan didinginkan
10% media fermipan (Saccharomyces cerevisiae) dimasukkan ke dalam fermentor
ukur pH awal fermentasi, dan diatur pH menjadi 4–5
G. Teknik Pengumpulan Data
Untuk menentukan data yang diperlukan maka dibutuhkan teknik
pengumpulan data agar bukti-bukti dan fakta-fakta yang diperoleh berfungsi
sebagai data obyektif dan tidak terjadi penyimpangan dari keadaan yang
sebenarnya. Untuk menggali data dari sumber yang telah ditentukan, maka
diperlukan alat kerja untuk mengumpulkan data yang disebut dengan teknik atau
metode pengumpulan data. Adapun metode-metode yang diperlukan tersebut di
antaranya adalah:
1. Pengujian Glukosa
a. Pembuatan Kurva Baku Glukosa
Kurva baku glukosa menyatakan hubungan antara konsentrasi
glukosa dengan kerapatan optik (serapan pada panjang gelombang 540 nm).
Kurva ini dibuat untuk menentukan harga konsentrasi larutan glukosa
dengan pengukuran transmisi cahaya spektrofotometer. Pembuatan kurva
baku glukosa dimulai dengan menimbang glukosa murni dengan timbangan
analitik. Dibuat larutan glukosa standar dengan konsentrasi 5 ppm, 6 ppm, 7
ppm, 8 ppm, 9 ppm. Masing –masing larutan di ukur optical density (OD)
dengan spektrofotometer pada panjang gelombang 540 nm. Setelah
mengetahui nilai OD dan konsentrasi gula maka dapat dibuat kurva standar
b. Pengujian Kadar Glukosa Pereduksi pada Sampel
Penentuan kadar gula pereduksi dilakukan seperti pada pembuatan
kurva standar glukosa dengan mengambil 2 ml sampel. Setelah kadar
glukosa diukur dengan spektrofotometer pada panjang gelombang 540 nm,
kemudian dikalibrasi dengan larutan gula murni. Kadar gula pereduksi
sampel didapatkan dengan menggunakan persamaan regresi linier pada
kurva tersebut.
2. Pengukuran Kadar Etanol
Pengukuran kadar etanol menggunakan metode Iodometri. Adapun caranya
sebagai berikut (Timotius, 1994):
1. Masukkan 10 ml sampel ke dalam erlemeyer, kemudian ditambahkan 10 ml
kalium bikromat (K2Cr2O7) 0,005787 M. Campurkan hingga homogen,
tambahkan 4 ml asam sulfat pekat dengan hati-hati, sambil di goyang.
2. Masukkan erlemeyer tersebut ke dalam penangas air selama 15 menit,
selanjutnya didinginkan.
3. Tambahkan indikator pati-KI dan aduk hingga homogen
4. Kemudian titrasi dengan larutan Na-thiosulfat 0,01 M. volume Na-thiosulfat
yang diperlukan dicatat dan digunakan untuk perhitungan dalam analisis
kadar etanol. Dengan rumus berikut :
Keterangan :
V1 = volume K2Cr2O7
M1 = molaritas K2Cr2O7
V2 = volume titer Na-thiosulfat
M2 = molaritas Na-thiosulfat
BM = berat molekul alkohol
Vs = volume sampel
Untuk cara pembuatan larutan (K2Cr2O7) 0,005787 M, Na-thiosulfat 0,01 M,
larutan pati dan larutan KI, dapat dilihat pada lampiran 4.
3. Pengujian pH
Analisis pH pada sampel menggunakan pH meter.
H. Cara Analisis Data
Data yang diperoleh dari hasil pengamatan, kemudian diolah dengan
39 BAB IV
HASIL DAN PEMBAHASAN
A. Data dan Analisis Hasil Penelitian
1. Uji Glukosa
Dari uji glukosa pada larutan standar dan larutan sampel melalui proses
hidrolisis asam dengan konsentrasi H2SO4 yang berbeda-beda dengan
menggunakan spektrofotometer didapatkan hasil sebagai berikut ini :
Table 4. Absorbansi pada Larutan Standar
Glukosa (ppm) Absorbansi
0 0
5 0,25
6 0,299
7 0,353
8 0,398
9 0,441
Hasil nilai absorbansi larutan standar di atas diolah dengan metode regresi linier
menggunakan SPSS 17.0 sehingga didapatkan persamaan Y = aX + b dan dibuat
grafik perbandingan konsentrasi glukosa dengan absorbansi. Dari perhitungan
regresi linier pada larutan glukosan standar, persamaan yang diperoleh adalah Y
Dari persamaan pada grafik yang didapat, kadar glukosa pada sampel diperoleh
dengan memasukkan nilai absorbansi yang diperoleh dari sampel ke dalam
persamaan Y = 0,049X + 0,002. Sehingga didapatkan hasil sebagai berikut : Gb 12. Kurva Standar Glukosa
Table 5. Kadar Glukosa pada Larutan Sampel
Dari hasil perbedaan konsentrasi H2SO4 dan perbedaan lama waktu hidrolisis
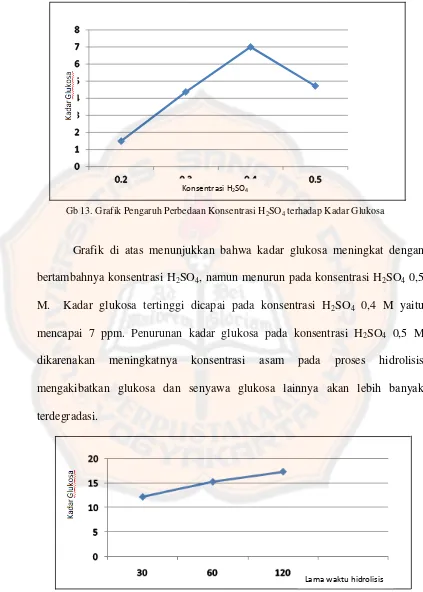
Grafik di atas menunjukkan bahwa kadar glukosa meningkat dengan
bertambahnya konsentrasi H2SO4, namun menurun pada konsentrasi H2SO4 0,5
M. Kadar glukosa tertinggi dicapai pada konsentrasi H2SO4 0,4 M yaitu
mencapai 7 ppm. Penurunan kadar glukosa pada konsentrasi H2SO4 0,5 M
dikarenakan meningkatnya konsentrasi asam pada proses hidrolisis
mengakibatkan glukosa dan senyawa glukosa lainnya akan lebih banyak
terdegradasi.
Gb 13. Grafik Pengaruh Perbedaan Konsentrasi H2SO4 terhadap Kadar Glukosa
Gb 14. Grafik Pengaruh Perbedaan Lama Waktu Hidrolisis terhadap Kadar Glukosa Konsentrasi H2SO4
Grafik di atas menunjukkan bahwa semakin lama waktu hidrolisis
semakin meningkat kadar glukosa. Kadar glukosa tertinggi diperoleh pada lama
waktu hidrolisis 120 menit. Semakin lama waktu hidrolisis, maka kesempatan
untuk merombak karbohidrat yang terkandung dalam rumput laut menjadi
glukosa akan semakin banyak.
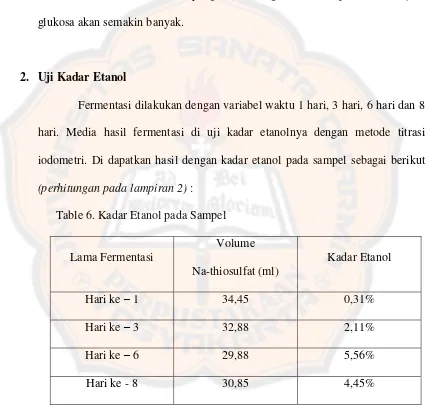
2. Uji Kadar Etanol
Fermentasi dilakukan dengan variabel waktu 1 hari, 3 hari, 6 hari dan 8
hari. Media hasil fermentasi di uji kadar etanolnya dengan metode titrasi
iodometri. Di dapatkan hasil dengan kadar etanol pada sampel sebagai berikut
(perhitungan pada lampiran 2) :
Table 6. Kadar Etanol pada Sampel
Lama Fermentasi
Volume
Na-thiosulfat (ml)
Kadar Etanol
Hari ke – 1 34,45 0,31%
Hari ke – 3 32,88 2,11%
Hari ke – 6 29,88 5,56%
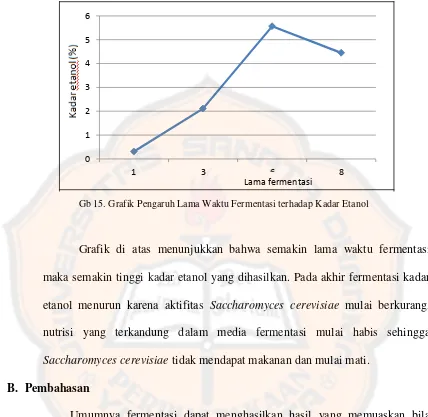
Gb 15. Grafik Pengaruh Lama Waktu Fermentasi terhadap Kadar Etanol
Grafik di atas menunjukkan bahwa semakin lama waktu fermentasi
maka semakin tinggi kadar etanol yang dihasilkan. Pada akhir fermentasi kadar
etanol menurun karena aktifitas Saccharomyces cerevisiae mulai berkurang,
nutrisi yang terkandung dalam media fermentasi mulai habis sehingga
Saccharomyces cerevisiae tidak mendapat makanan dan mulai mati.
B. Pembahasan
Umumnya fermentasi dapat menghasilkan hasil yang memuaskan bila
khamir yang digunakan berasal dari ragi roti. Dalam kenyataannya banyak proses
fermentasi langsung menggunakan ragi roti yang langsung dimasukkan ke
fermentor walaupun hal ini sebenarnya kurang baik. Tidak semua khamir dapat
menghasilkan alkohol secara stabil, oleh karena itu perlu dilakukan regenerasi
kultur dari khamir (Saccharomyces cerevisiae) agar didapatkan strain-strain khamir
yang baik. 0 1 2 3 4 5 6
1 3 6 8
1. Uji Kadar Glukosa
Dalam proses fermentasi yang perlu diperhatikan adalah
komponen-komponen pendukung kegiatan proses tersebut. Pada prinsipnya proses
fermentasi untuk menghasilkan etanol ditentukan secara tidak langsung dari
banyaknya kandungan pati dalam bahan baku. Karena kandungan pati tersebut
akan difermentasikan oleh khamir. Biasanya dalam proses fermentasi alkohol
digunakan khamir (Saccharomyces cerevisiae). Khamir ini dapat mengubah
glukosa menjadi alkohol dan CO2. Khamir tidak dapat langsung
memfermentasikan pati. Oleh karena itu tahap yang penting adalah proses
sakarifikasi, yaitu perubahan pati menjadi maltosa atau glukosa dengan
menggunakan enzim atau asam (Hidayat, dkk. 2006). Dalam penelitian ini
dilakukan hidrolisis asam pada sampel rumput laut dengan tujuan untuk
mengubah karbohidrat yang terkandung dalam rumput laut menjadi glukosa.
Asam yang digunakan dalam proses hidrolisis asam ini adalah asam sulfat
(H2SO4), merupakan asam yang sering digunakan sebagai katalis kimia, sangat
reaktif, dan harganya murah.
Dalam penelitian ini hidrolisis menggunakan H2SO4 dengan
konsentrasi rendah, karena asam sulfat dengan konsentrasi rendah efektif
menghasilkan gula tinggi dan sekaligus mampu menghidrolisis serat. Dibuat
berbagai macam variasi konsentrasi H2SO4 dan variasi waktu untuk hidrolisis,
optimum untuk menghasilkan glukosa paling tinggi. Hasil dari proses ini
digunakan sebagai acuan pada hidrolisis untuk proses fermentasi. Proses
hidrolisis dilakukan pada konsentrasi H2SO4 yaitu 0,2M; 0,3M; 0,4M; dan 0,5M
pada variasi waktu 30, 60 dan 120 menit. Kemudian larutan standar glukosa dan
sampel hasil hidrolisis diukur kadar glukosanya dengan spektrofotometer, dan
hasilnya dihitung menggunakan regresi linier sehingga didapatkan persamaan Y
= 0,049X + 0,002.
Uji pengaruh perbedaan konsentrasi H2SO4 terhadap kadar glukosa
pada sampel rumput laut Eucheuma sp. dapat dilihat pada Gambar 10. Grafik di
atas menjelaskan kadar glukosa meningkat dengan bertambahnya konsentrasi
H2SO4 dari 0,2M; 0,3M; dan 0,4 M, kemudian menurun pada konsentrasi 0,5M.
Meningkatnya kuantitas glukosa pada proses hidrolisis ini dapat dikatakan asam
dengan konsentrasi rendah dapat meningkatkan kuantitas glukosa karena asam
dengan konsentrasi rendah dapat memutuskan ikatan glikosida yang terdapat
pada selulosa, tapi selanjutnya turun pada konsentrasi 0,5M. Penurunan kadar
glukosa ini dikarenakan meningkatnya konsentrasi asam pada proses hidrolisis
mengakibatkan glukosa dan senyawa glukosa lainnya akan lebih banyak
terdegradasi. Sehingga konsentrasi asam sulfat yang optimal menghasilkan
banyak glukosa adalah asam sulfat dengan konsentrasi 0,4M.
Proses uji pengaruh perbedaan waktu hidrolisis dilakukan untuk
mendapatkan kuantitas glukosa terbaik. Hasil proses ini akan digunakan sebagai
acuan lama waktu proses hidrolisis selanjutnya. Proses ini dilakukan dengan
variabel waktu 30 menit, 60 menit, dan 120 menit. Dari Gambar.11 di atas
menjelaskan kadar glukosa terbaik pada waktu 120 menit. Hal ini dapat
dikatakan semakin lama waktu hidrolisis maka semakin tinggi kadar glukosa
yang diperoleh. Selain menggunakan hidrolisis asam, untuk mengubah
karbohidrat menjadi glukosa dapat juga secara enzimatis dengan enzim amylase.
Akan tetapi untuk sekala industri akan lebih murah dan lebih praktis secara
kimiawi dengan hidrolisis asam. Selain itu hidrolisis dengan asam diharapkan
dapat menghidrolisis polisakarida yang tidak mampu dipecah oleh enzim, tetapi
tidak merusak glukosa yang ada.
Dari hasil percobaan memperlihatkan bahwa konsentrasi H2SO4 dan
lama waktu hidrolisis mempengaruhi kadar glukosa yang dihasilkan oleh
sampel. Glukosa tersebut nantinya yang akan digunakan oleh Saccharomyces
cerevisiae untuk menghasilkan bioetanol. Kadar glukosa yang terkandung
dalam media fermentasi itu akan menentukan kadar bioetanol yang dihasilkan
nantinya. Kadar glukosa tertinggi yang diperoleh dari hasil hidrolisis sampel
digunakan sebagai media fermentasi.
2. Uji Kadar Etanol
Kadar etanol adalah parameter yang dapat menunjukkan kualitas dari
khamir yang digunakan, kadar gula, dan efisiensi fermentasi. Proses fermentasi
merupakan proses pembebasan energi tanpa adanya oksigen, sehingga sering
disebut respirasi anaerob. Pada fermentasi, beberapa mikroba peristiwa
pembebasan energi terlaksana karena asam piruvat diubah menjadi asam asetat
dan CO2 kemudian selanjutnya asam asetat diubah menjadi alkohol. Kadar
etanol sebagai hasil dari beberapa perlakuan waktu fermentasi dapat dilihat pada
Tabel 6.
Dari Gambar.12 dapat dijelaskan bahwa dari hari pertama sampai hari
ke-6 kadar etanol semakin meningkat, kemudian kadar etanol turun pada hari
ke-8. Pada lama waktu fermentasi 1 hari Saccharomyces cerevisiae berada pada
fase adaptasi, dimana mikroba tersebut menyesuaikan diri dengan substrat dan
kondisi lingkungan barunya sehingga masih belum banyak beraktivitas dan
menghasilkan etanol. Pada awal proses fermentasi, Saccharomyces cerevisiae
masih beradaptasi dengan lingkungannya dan memanfaatkan glukosa untuk
tumbuh dan memperbanyak diri. Kadar etanol yang rendah juga dihasilkan dari
fermentasi media dengan waktu fermentasi 3 hari. Hal ini diduga pada hari ke-3
Saccharomyces cerevisiae belum bekerja secara optimal karena masih dalam
tahap tumbuh dan memperbanyak diri sehingga kadar etanol yang terbentuk
masih sedikit.
Kadar etanol paling tinggi terdapat pada hasil fermentasi media dengan