PENGARUH WAKTU PEMAPARAN TERHADAP KADAR TIMBAL DALAM BUAH PEPAYA (Carica papayaL.)
YANG DIJUAL DI BEBERAPA PINGGIR JALAN DI YOGYAKARTA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh :
Vivi Elvira
NIM : 078114060
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
PENGARUH WAKTU PEMAPARAN TERHADAP KADAR TIMBAL DALAM BUAH PEPAYA (Carica papayaL.)
YANG DIJUAL DI BEBERAPA PINGGIR JALAN DI YOGYAKARTA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh :
Vivi Elvira
NIM : 078114060
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
Andai aku dapat memohon pada-Nya
agar hidupku sempurna,
kemungkinan ini
sangat menggiurkan,
tapi aku akan merasa hampa,
karena hidup
tak lagi mengajariku apapun..
Kupersembahkan untuk yang tersayang,,,
Seluruh Keluargaku, yang selalu menyayangi
dan memberikan dukungan,,,
vii
PRAKATA
Puji syukur penulis panjatkan kepada Bapa di Surga atas berkat, kasih,
kekuatan, dan penyertaan-Nya maka skripsi berjudul “Pengaruh Waktu
Pemaparan Terhadap Kadar Timbal dalam Buah Pepaya (Carica papaya L.) yang
Dijual di Beberapa Pinggir Jalan di Yogyakarta” dapat terselesaikan dengan baik
oleh penulis. Skripsi ini disusun untuk memenuhi salah satu syarat memperoleh
gelar Sarjana Farmasi (S.Farm) di Fakultas Farmasi Universitas Sanata Dharma
Yogyakarta.
Selama penyusunan skripsi ini, banyak pihak yang telah membantu
penulis dalam mengatasi berbagai permasalahan dan kesulitan. Oleh karena itu,
penulis ingin mengucapkan terima kasih yang sebesar-besarnya kepada:
1. Ipang Djunarko, M.Sc., Apt. selaku Dekan Fakultas Farmasi Unversitas
Sanata Dharma Yogyakarta.
2. Dra. M.M. Yetty Tjandrawati, M.Si. selaku pembimbing utama yang telah
membantu dalam penyelesaian skripsi ini. Terima kasih atas waktu, kritik,
saran dan bantuan yang telah diberikan selama penyusunan skripsi.
3. Prof. Dr. Sudibyo Martono, M. S., Apt. selaku pembimbing pendamping yang
telah membantu dalam penyelesaian skripsi ini. Terima kasih atas waktu,
kritik, saran dan bantuan yang telah diberikan selama penyusunan skripsi.
4. Christine Patramurti, M.Si., Apt. selaku dosen penguji yang telah memberikan
viii
5. Yohanes Dwiatmaka, M.Si. selaku dosen penguji yang telah memberikan
saran dan kritik untuk skripsi ini.
6. Rini Dwiastuti, M.Sc., Apt. yang telah memberikan ijin melakukan penelitian
di laboratorium.
7. Liana Wulan B. sebagai teman seperjuangan dalam skripsi ini, atas
kebersamaan selama penelitian, serta saran dan kritik untuk penulis sehingga
skripsi ini dapat terselesaikan dengan baik.
8. Papa dan Om Indra Boentoro (Papa dari Liana) yang telah membantu selama
survei lokasi perkebunan pepaya dan distribusi buah pepaya dari Magelang ke
Yogyakarta.
9. Mas Bimo, Pak Parlan, Mas Kunto dan Mas Otok yang telah membantu
penulis sejak awal kegiatan penelitian di laboratorium hingga selesai.
10. Mas Narto, Pak Mukminin, dan Mas Dwi atas bantuannya.
11. Teman-teman Kost Dewi I: Eliz, Sasa, Frissa, Venny dan Helen atas
kebersamaan, dukungan, semangat dan doanya.
12. Hadi Setiawan (alm.) atas segala dukungan dan bantuan yang telah diberikan
selama penulis menyelesaikan studi di Fakultas Farmasi USD.
13. Teman-teman di kelas FST 2007 atas kebersamaan dan saat-saat yang
membahagiakan dan tak terlupakan.
14. Pihak Laboratorium Penelitian dan Pengujian Terpadu (LPPT) Universitas
Gadjah Mada Yogyakarta yang telah memberikan ijin untuk melakukan
ix
15. Bu Astuti dan Mbak Pipit sebagai teknisi di LPPT UGM atas bantuan dan
saran selama melakukan penelitian di sana.
16. Semua teman-teman dan pihak-pihak yang tidak dapat disebutkan satu per
satu oleh penulis, terima kasih atas bantuan dan dukungannya selama ini.
Penulis menyadari bahwa skripsi ini masih memiliki banyak kekurangan
mengingat keterbatasan kemampuan dan pengetahuan penulis. Oleh karena itu,
penulis mengharapkan kritik dan saran yang membangun dari semua pihak. Akhir
kata, semoga skripsi ini berguna bagi kemajuan ilmu pengetahuan.
x
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH ... vi
PRAKATA ... vii
DAFTAR ISI ... x
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xvi
DAFTAR LAMPIRAN ... xvii
INTISARI ... xviii
ABSTRACT... xix
BAB I PENGANTAR ... 1
A. Latar Belakang ... 1
1. Permasalahan ... 4
2. Keaslian penelitian ... 4
3. Manfaat penelitian ... 5
B. Tujuan Penelitian ... 5
xi
A. Timbal ... 6
1. Sifat fisika kimia timbal ... 6
2. Pencemaran udara oleh timbal ... 6
3. Metabolisme dan toksisitas timbal ... 7
4. Penelitian timbal dalam buah dan sayur ... 8
B. Pepaya ... 9
1. Morfologi ... 9
2. Kandungan kimia ... 10
3. Manfaat pepaya ... 12
C. Spektrofotometri Serapan Atom ... 13
1. Instrumentasi spektrofotometri serapan atom ... 16
2. Gangguan-gangguan pada spektrofotometri serapan atom ... 18
3. Analisis kuantitatif ... 20
D. Validitas Metode Analisis ... 20
1. Linearitas ... 22
2. Akurasi ... 22
3. Presisi ... 24
4. Spesifisitas ... 24
5. LOD (limit of detection) dan LOQ (limit of quantitation) ... 25
E. Landasan Teori ... 26
F. Hipotesis ... 28
BAB III METODE PENELITIAN ... 29
xii
B. Variabel Penelitian ……….. 29
1. Variabel bebas ………. 29
2. Variabel tergantung ………. 29
3. Variabel terkendali ……….. 29
C. Definisi Operasional ……… 31
D. Bahan Penelitian ……….. 31
E. Alat Penelitian ……….. 31
F. Tata Cara Penelitian ………. 32
1. Teknik pengambilan sampel ……… 32
2. Preparasi sampel ………. 33
3. Pembuatan kurva baku timbal ………... 34
4. Penetapan akurasi dan presisi ……….. 34
5. Penetapan linearitas ... 35
6. Penentuandetection limit... 35
7. Penentuanquantitation limit... 36
8. Analisis sampel secara kuantitatif ………... 36
G. Analisis Hasil ……….. 36
1. Akurasi ……….. ………. 36
2. Presisi ……….. 37
3. Linearitas ………. 37
4.Detection limit….……… 37
5.Quantitation limit….………... 38
xiii
BAB IV HASIL DAN PEMBAHASAN ………... 39
A. Pembuatan Larutan Baku Timbal ……… 39
B. Penetapan Kurva Baku ……… 40
C. Parameter Validitas Metode ……… 42
1.Limit of detection(LOD) danlimit of quantitation(LOQ) .. 42
2. Akurasi ……… 44
3. Presisi ……….. 47
4. Linearitas ………. 48
5. Spesifisitas ... 49
D. Penetapan Kadar Timbal dalam Buah Pepaya ... 49
1. Pengambilan dan perlakuan buah pepaya ... 49
2. Preparasi buah pepaya ……… 50
3. Analisis kadar timbal dalam pepaya ... 52
BAB V KESIMPULAN DAN SARAN……… 60
A. Kesimpulan ……….. 60
B. Saran ……… 60
DAFTAR PUSTAKA ……….. 61
LAMPIRAN ………. 65
xiv
DAFTAR TABEL
Halaman
Tabel I Komponen Kimia dalamCarica papayaL. ... 11
Tabel II Kandungan Nutrisi dalam 100 g Buah Pepaya ... 11
Tabel III Parameter analisis yang harus dipenuhi untuk syarat validasi metode ... 21
Tabel IV Kriteria rata-ratarecoveryyang diijinkan ... 22
Tabel V Kriteria nilai presisi yang diijinkan ... 24
Tabel VI Data Replikasi Seri Kurva Baku Timbal ... 40
Tabel VII Data Replikasi Seri Kurva Baku Timbal dengan Penyesuaian Satuan Kadar Timbal ... 41
Tabel VIII Hasil Pengukuran Absorbansi Blanko (Asam nitrat pH 2), LOD, dan LOQ ... 43
Tabel IX DataRecoveryBaku Timbal ... 44
Tabel X DataRecoveryKadar Timbal dengan Metode Standar Adisi ... 46 Tabel XI Data Nilai KV Baku Timbal ... 47
Tabel XII Hasil KV Kadar Timbal dengan Metode Standar Adisi ... 48
Tabel XIII Hasil Penetapan Kadar Timbal dalam Buah Pepaya
Kontrol ...
53
Tabel XIV Hasil Penetapan Kadar Timbal dalam Buah Pepaya
yang Dititipkan pada Pedagang I selama 4 hari ...
xv
Tabel XV Hasil Penetapan Kadar Timbal dalam Buah Pepaya
yang Dititipkan pada Pedagang I selama 8 hari ...
54
Tabel XVI Hasil Penetapan Kadar Timbal dalam Buah Pepaya
yang Dititipkan pada Pedagang II selama 4 hari ... 55
Tabel XVII Hasil Penetapan Kadar Timbal dalam Buah Pepaya
yang Dititipkan pada Pedagang II selama 8 hari ... 55
Tabel XVIII Hasil Penetapan Kadar Timbal dalam Buah Pepaya
yang Dititipkan pada Pedagang III selama 4 hari ... 56
Tabel XIX Hasil Penetapan Kadar Timbal dalam Buah Pepaya
xvi
DAFTAR GAMBAR
Halaman
Gambar 1. Buah Pepaya ... 10
Gambar 2. Instrumen Spektrofotometer Serapan Atom ... 13
Gambar 3. Bagian-bagian Instrumen Spektrofotometer Serapan
Atom ... 15
Gambar 4. Instrumentasi Spektrofotometer Serapan Atom ... 16
Gambar 5. Absorbansi Logam Pb versus Kadar Timbal (Replikasi
xvii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Data Penimbangan Bahan ... 66
Lampiran 2. Contoh Perhitungan Kadar Seri Larutan Baku Timbal ... 68
Lampiran 3. Persamaan Kurva Baku dan Gambar Kurva Baku Timbal ... 71
Lampiran 4. Perhitungan Penetapan Nilai LOD dan LOQ ... 72
Lampiran 5. Contoh Perhitungan Nilai %RecoveryBaku Timbal 74 Lampiran 6. Contoh Perhitungan Nilai KV ... 78
Lampiran 7. Contoh Perhitungan Penetapan Kadar Timbal dalam Sampel ... 79
Lampiran 8. Data Statistik Kelompok Pedagang I ... 81
Lampiran 9. Data Statistik Kelompok Pedagang II ... 83
Lampiran 10. Data Statistik Kelompok Pedagang III ... 85
Lampiran 11. Gambar Proses Pengambilan Sampel Pepaya ... 87
xviii
INTISARI
Asap kendaraan bermotor yang mengandung timbal dapat mengontaminasi buah yang dijual di pinggir jalan, seperti pepaya. Konsumsi buah yang mengandung timbal dapat mengakibatkan toksisitas kronis. Tujuan penelitian ini untuk mengetahui pengaruh lama waktu pemaparan udara yang terkontaminasi timbal terhadap kadar timbal dalam buah pepaya (Carica papaya
L.) serta mengetahui apakah metode yang digunakan telah memenuhi parameter validitas: LOD, LOQ, akurasi, presisi, spesifisitas dan linearitas.
Penelitian ini merupakan penelitian eksperimental. Sampel diperoleh dengan mengambil daging buah pepaya kemudian didestruksi dan ditetapkan kadar timbalnya dengan spektrofotometer serapan atom.
Berdasarkan hasil penelitian, diperoleh nilai r sebesar 0,9998. Recovery
dan KV baku pada kadar 0,25; 1,5; dan 3,0 ppm adalah 91,66-95,06% dan 1,86%; 100,78-102,38% dan 0,80%; 102,28-105,92% dan 1,76%. Recovery dan KV standar adisi sebesar 97,89-100,95% dan 1,65%. Rata-rata kadar timbal dalam buah pepaya kontrol adalah 0,15187 mg/kg; dalam buah pepaya yang dititipkan di pinggir Jalan Colombo, Jalan A.M. Sangaji dan Jalan Gedong Kuning selama 4 hari adalah 0,15267 mg/kg; 0,15440 mg/kg; 0,15645 mg/kg; dan selama 8 hari adalah 0,15650 mg/kg; 0,14972 mg/kg; 0,15908 mg/kg.
Hasil statistik menunjukkan bahwa perbedaan kadar timbal antara kelompok buah pepaya kontrol, 4 hari dan 8 hari di Jalan Colombo, Jalan A.M Sangaji dan Jalan Gedong Kuning tidak signifikan.
xix
ABSTRACT
Motor vehicle fumes that contain lead can contaminate fruit sold on the roadside, such as papaya. Consumption of fruits that contain lead cause chronic toxicity. The purpose of this study was to determine the effect of exposure duration of lead-contaminated air to the lead content in papaya fruit and determine if the methods used in, compliance with the validity parameters: LOD, LOQ, accuracy, precision, specificity and linearity.
This study is an experimental studies. Samples obtained by taking the papaya fruit flesh, then it’s digested. Lead content determined by atomic absorption spectrophotometer
Based on research results, r value are 0.9998; recovery and CV value at levels 0.25; 1.5; and 3.0 ppm are 91.66-95.06% and 1.86%; 100.78-102.38% and 0.80%; 102.28-105.92% and 1.76%. Recovery and CV value of standard adition are 97.89-100.95% and 1.65%. The lead levels in control group are 0.15187 mg/kg; in papaya fruits which were sold on the Colombo, A.M. Sangaji and Gedong Kuning Roadside for 4 days are 0.15267 mg/kg; 0.15440 mg/kg; 0.15645 mg/kg, and for 8 days are 0.15650 mg/kg; 0.14972 mg/kg; 0.15908 mg/kg.
Statistically, there’s no significant difference in lead levels between controls, 4 days and 8 days groups in Colombo , A.M. Sangaji and Gedong Kuning Street.
BAB I PENGANTAR
A. Latar Belakang
Indonesia merupakan negara yang tingkat kependudukannya tinggi
dengan berbagai aktivitas kehidupan yang pasti menghasilkan suatu limbah. Salah
satu limbah yang tergolong sangat beracun bagi organisme hidup adalah
senyawa-senyawa kimia yang mempunyai bahan aktif logam-logam berat (Palar, 1994).
Timbal, kadmium, tembaga, dan seng merupakan polutan logam yang utama di
lingkungan pinggir jalan (Akbar, Hale, Headley, dan Athar, 2006).
Beberapa logam berat, seperti kadmium, timbal, dan merkuri merupakan
kontaminan utama dalam makanan dan merupakan masalah utama terhadap
lingkungan (Zaidi, Asrar, Mansoor, dan Farooqui, 2005). Kontaminasi logam
berat dalam sayuran dan buah disebabkan oleh kontaminasi pada tanah dan
atmosfer yang dapat mengancam kesehatan manusia (Turkdogan, Kilicel, Kara,
dan Tuncer, 2003).
Namun, menurut Yusuf dan Oluwole (2009), selama proses transportasi
dan penjualan, sayur dan buah yang telah dipanen masih terancam oleh polusi
udara yang dapat menyebabkan peningkatan kadar logam berat dalam sayur dan
buah. Berdasarkan penelitian yang dilakukan oleh Farista (2010), waktu
pemaparan berpengaruh terhadap kadar timbal pada buah jambu biji yang dijual di
pinggir jalan. Semakin lama buah dijajakan secara terbuka di kios di tepi jalan,
kadar cemaran timbalnya akan semakin tinggi (Kristiono, 1999). Oleh karena itu,
perlu dilakukan pemeriksaan kadar timbal dalam buah yang dijual di pinggir jalan
di Yogyakarta, terutama kios-kios buah di pinggir jalan raya dengan kepadatan
lalu lintas tinggi. Pada penelitian ini, kios buah yang dipilih adalah kios buah di
pinggir Jalan Colombo, Jalan Gedong Kuning, dan Jalan A. M. Sangaji,
Yogyakarta.
Buah yang dipilih adalah buah pepaya berusia 2-3 bulan yang diperoleh
langsung dari perkebunan pepaya di Jalan Mayor Unus KM 6, Gentan, Wayuan,
Kabupaten Magelang. Perlakuan yang diberikan adalah lama waktu pemaparan
buah pepaya, yaitu empat hari dan delapan hari setelah dititipkan pada kios-kios
buah. Kontrol yang digunakan adalah pepaya yang baru dipetik sebagai hari ke-0.
Pada penelitian dipilih buah pepaya karena buah pepaya merupakan salah
satu buah yang sering dikonsumsi oleh masyarakat Indonesia karena manfaatnya
yang banyak. Secara ekonomis, pepaya adalah spesies yang penting dalam famili
Caricaceaedan telah dibudidayakan secara luas untuk tujuan konsumsi. Di Asia,
buah pepaya mentah yang diserut sering digunakan sebagai salad. Selain itu, buah
pepaya mentah yang telah dikupas dan dimasak digunakan dalam berbagai menu
makanan di Asia. Di Asia Tenggara, konsumsi pepaya menempati urutan kedua
setelah pisang (Australian Government, 2008). Selama tahun 2008, produksi buah
pepaya di dunia mencapai 9732158 ton dari 20 negara. Indonesia merupakan
negara keempat terbesar produksi pepaya di dunia (FAO, 2011).
Kulit pepaya harus dikupas terlebih dahulu sebelum dikonsumsi. Oleh
karena itu, peneliti ingin memeriksa apakah daging buah pepaya yang dikonsumsi
Pencemaran tersebut dapat ditentukan berdasarkan penambahan kadar timbal
dalam daging buah pepaya.
Penetapan kadar timbal (Pb) dalam buah pepaya ini menggunakan
metode spektrofotometri serapan atom. Menurut Bakkali, Martos, Souhail, dan
Ballesteros (2009), flame atomic absorption spectrometry banyak digunakan
karena selektivitasnya, kecepatannya, dan biaya operasionalnya yang murah.
Selain itu, menurut Khopkar (1990), kelebihan metode spektrofotometri serapan
atom adalah dapat menganalisis logam dalam konsentrasi rendah serta metode
serapan sangat spesifik, dalam hal ini setiap logam yang diukur mempunyai
panjang gelombang tertentu, sehingga serapan yang dihasilkan berasal dari
serapan logam tersebut tanpa ada serapan logam lain.
Validasi adalah proses yang digunakan untuk membuktikan bahwa suatu
metode analisis tertentu dapat digunakan untuk mengukur suatu analit tertentu dan
dapat memberikan hasil pengukuran sesuai dengan tujuan yang telah ditetapkan
(Tanase, Popescu, dan Pana, 2006). Validasi metode perlu dilakukan agar metode
ini valid dan dapat dipertanggungjawabkan. Suatu metode dinyatakan valid
apabila telah memenuhi syarat akurasi, presisi, linearitas serta spesifisitas yang
1. Permasalahan
Berdasarkan latar belakang tersebut, maka dapat disusun permasalahan
sebagai berikut:
a. Apakah metode spektrofotometri serapan atom yang digunakan memiliki nilai
LOD, LOQ, akurasi, presisi, linearitas, dan spesifisitas yang baik untuk
menetapkan kadar timbal dalam buah pepaya?
b. Apakah ada pengaruh antara waktu pemaparan terhadap kadar logam timbal
dalam buah pepaya yang dijual di tepi Jalan Colombo, Jalan A.M. Sangaji,
dan Jalan Gedong Kuning, Yogyakarta?
c. Apakah kadar timbal dalam buah pepaya yang telah mengalami perlakuan
melebihi batas aman kadar timbal dalam buah menurut SNI 7387:2009 yaitu
0,5 mg/kg?
2. Keaslian penelitian
Sepengetahuan penulis, penelitian dengan judul Pengaruh Waktu
Pemaparan terhadap Kadar Timbal dalam Buah Pepaya (Carica papaya L.) yang
Dijual di Beberapa Pinggir Jalan di Yogyakarta belum pernah dilakukan.
Beberapa penelitian yang pernah dilakukan sebelumnya antara lain
Penetapan Kadar Timbal (Pb) dalam Buah Salak, Alpukat, dan Melon dengan
Metode Spektrofotometri Serapan Atom (Kamal, Prayogo, dan Suroso, 2008).
Pengaruh Ketebalan Kulit, Waktu serta Lokasi Penjualan Terhadap Kadar Pb
dalam Buah Jambu Air, Belimbing, Jeruk, dan Pisang (Guntarti dan Kamal,
pada Buah Jambu Biji (Psidium guajava L.) yang Dijual di Pinggir Jalan (Farista,
2010). Kadar Cemaran Pb pada Anggur di Kios Buah : Studi Kasus di Jl. Inspeksi
Saluran Kali Malang, Jakarta Timur (Kristiono,1999).
3. Manfaat penelitian
a. Manfaat metodologis. Hasil penelitian ini diharapkan dapat
memberikan informasi validitas metode spektrofotometri serapan atom pada
penetapan kadar logam timbal (Pb) dalam sampel buah pepaya.
b. Manfaat praktis. Penelitian ini diharapkan dapat menambah khasanah
ilmu kefarmasian.
B. Tujuan Penelitian
Tujuan penelitian ini adalah:
1. Untuk mengetahui apakah metode spektrofotometri serapan atom yang
digunakan memiliki nilai LOD, LOQ, akurasi, presisi, linearitas, dan
spesifisitas yang baik untuk menetapkan kadar timbal dalam buah pepaya.
2. Untuk mengetahui pengaruh antara waktu pemaparan terhadap kadar logam
timbal dalam buah pepaya yang dijual di tepi Jalan Colombo, Jalan A.M.
Sangaji, dan Jalan Gedong Kuning, Yogyakarta.
3. Untuk mengetahui apakah kadar timbal dalam buah pepaya yang telah
mengalami perlakuan melebihi batas aman kadar timbal dalam buah menurut
BAB II
PENELAAHAN PUSTAKA
A. Timbal 1. Sifat fisika kimia timbal
Timbal (plumbum/Pb) atau timah hitam adalah suatu unsur logam berat
yang lebih tersebar luas dibanding kebanyakan logam toksik lainnya. Timbal
dapat masuk ke dalam tubuh manusia melalui pernafasan, ataupun saluran
pencernaan (Darmono, 1995).
Timbal termasuk ke dalam kelompok logam-logam golongan IVA pada
tabel periodik unsur kimia. Logam ini mempunyai nomor atom (NA) 82 dan
bobot atom (BA) 207,2. Timbal merupakan logam berat berwarna kelabu kebiruan
dan lunak dengan titik leleh 327 °C dan titik didih 1620 °C. Pada suhu 550-600
°C Pb menguap dan bereaksi dengan oksigen di udara membentuk timbal oksida.
Walaupun bersifat lunak dan lentur, Pb sangat rapuh dan mengkerut pada
pendinginan, sulit larut dalam air dingin, air panas dan air asam nitrit, asam asetat
dan asam sulfat pekat (Denny, 2005).
2. Pencemaran udara oleh timbal
Selama beberapa dekade terakhir, bensin yang mengandung timbal
(tetraethyllead) merupakan bahan bakar yang banyak digunakan pada kendaraan
bermotor. Partikulat timbal halida diemisikan dalam jumlah yang sangat besar.
Hal ini terjadi karena adanya dikloroetan dan dibromoetan yang ditambahkan
sebagai halogenated scavengers untuk mencegah akumulasi timbal oksida di
dalam mesin. Proses pembentukan timbal halida dapat dilihat pada persamaan 1 di
bawah ini:
Pb(C2H5)4+ O2+halogenated scavengers
CO2+ H2O + PbCl2+ PbClBr + PbBr2(tidak seimbang) (1)
Selama puncak penggunaan bensin yang mengandung timbal mulai awal tahun
1970, sekitar 200000 ton timbal mencemari atmosfer setiap tahun melalui rute ini
(Manahan, 2005).
3. Metabolisme dan toksisitas timbal
Absorpsi timbal di dalam tubuh sangat lambat, sehingga terjadi
akumulasi dan menjadi dasar keracunan yang progresif. Keracunan timbal ini
menyebabkan kadar timbal yang tinggi dalam aorta, hati, ginjal, pankreas, paru,
tulang, limpa, testis, jantung, dan otak (Supriyanto, Samin, dan Kamal, 2007).
Timbal merupakan neurotoksin dan dapat menyebabkan tingkah laku abnormal,
keterbelakangan intelegensi dan mental. Timbal juga dapat mengganggu
metabolisme kalsium dan vitamin D serta mempengaruhi formasi Hb dan
mengakibatkan anemia (Soceanu, 2009).
Sel-sel darah merah merupakan suatu bentuk kompleks khelat yang
dibentuk oleh ion Fe2+dengan gugus haemo dan globin. Efek hematotoksisitas ion
Pb2+ adalah menghambat sebagian besar enzim yang berperan dalam biosintesis
heme. Diantara enzim yang terlibat dalam sintesis heme, enzim δ-aminolevulinic
rentan terhadap efek penghambatan ion Pb2+. Selain itu, toksisitas ion Pb2+ juga
dapat menyebabkan anemia hemolitik akibat destruksi eritrosit. Anemia hemolitik
disebabkan masa hidup eritrosit yang terlalu singkat (Denny, 2005).
4. Penelitian timbal dalam buah dan sayur
Penelitian yang dilakukan Yusuf dan Oluwole (2009) mengenai
Kontaminasi Logam Berat (Cu, Zn, Pb) pada Sayuran di Kota Urban : Studi
Kasus di Lagos menunjukkan bahwa konsentrasi logam berat dalam sayuran dapat
dipengaruhi oleh konsentrasi logam berat dalam tanah, udara, serta air irigasi pada
lokasi penanaman. Selain itu, kadar logam berat tersebut juga dapat bertambah
akibat absorpsi logam berat yang berasal dari deposisi udara pada sayuran selama
proses transportasi dan penjualan.
Penelitian yang dilakukan oleh Kamal dkk. (2008) mengenai Penetapan
Kadar Timbal (Pb) dalam Buah Salak, Alpukat, dan Melon dengan Metode
Spektrofotometri Serapan Atom, menunjukkan bahwa terjadi penyerapan logam
Pb yang ada di udara oleh buah yang dijual di pinggir jalan. Buah alpukat
menunjukkan penyerapan logam Pb yang paling besar. Sebuah penelitian
mengenai Pengaruh Ketebalan Kulit, Waktu serta Lokasi Penjualan Terhadap
Kadar Pb dalam Buah Jambu Air, Belimbing, Jeruk, dan Pisang yang dilakukan
oleh Guntarti dan Kamal (2008), menunjukkan bahwa tidak terdapat perbedaan
nyata pada kadar timbal berdasarkan lama hari diletakkannya sampel di lokasi
Menurut penelitian yang dilakukan oleh Farista (2010) tentang Pengaruh
Waktu Pemaparan dan Pencucian terhadap Kadar Logam Pb pada Buah Jambu
Biji (Psidium guajava L.) yang Dijual di Pinggir Jalan dan Kristiono (1999)
mengenai Kadar Cemaran Pb pada Anggur di Kios Buah : Studi Kasus di Jl.
Inspeksi Saluran Kali Malang, Jakarta Timur diketahui bahwa terdapat pengaruh
semakin meningkatnya lama waktu buah dipaparkan pada udara yang tercemar
asap kendaraan bermotor terhadap peningkatan kadar timbal dalam buah.
Menurut SNI 7387:2009, batas maksimum kadar timbal dalam buah
adalah 0,5 mg/kg. SNI 7387:2009 ini merupakan daftar batas maksimum cemaran
logam berat dalam pangan.
B. Pepaya 1. Morfologi
Pepaya (Carica papaya L.). Pohon berbatang basah, tumbuh tegak,
silindris bercabang atau tidak, dalam rongga seperti sepon dan berongga, luar
dengan bekas-bekas daun. Susunan daun rapat, dengan rumus 3/8 pada
ujung-ujung batang atau cabang, tangkai bulat, berongga 25-100 cm panjang, helaian
daun bulat, berbagi atau bercangap menjadi, pangkal bangun jantung atau
berlekuk, ujung runcing, diameter 25-75 cm. Taju-taju bercangap menyirip tak
beraturan. Bunga berkelamin tunggal berumah dua. Bunga jantan dan beberapa
bunga betina seringkali dalam tandan yang bertangkai panjang. Kelopak kecil,
mahkota bangun terompet, putih kekuning-kuningan dengan tepi bertaju lima dan
Bunga betina kebanyakan terpisah dengan mahkota yang bebas atau hampir
bebas. Bakal buah beruang satu atau dengan sekat-sekat semu nampaknya
beruang lima. Kepala putik lima tak bertangkai putik. Biji banyak diselubungi
oleh selaput, tetapi sebelah dalam selaput kasar seperti duri. Buahnya buah buni
bentuk macam-macam, berdaging lunak berair-air, warna kuning-jingga
(Tjitrosoepomo, 1994). Gambar buah pepaya yang digunakan pada penelitian ini
dapat dilihat pada gambar 1.
Gambar 1. Buah Pepaya
2. Kandungan kimia
Secara biologi, masing-masing bagian dari tanaman pepaya memiliki
komponen kimia dan kandungan nutrisi yang berbeda-beda dan dapat dilihat pada
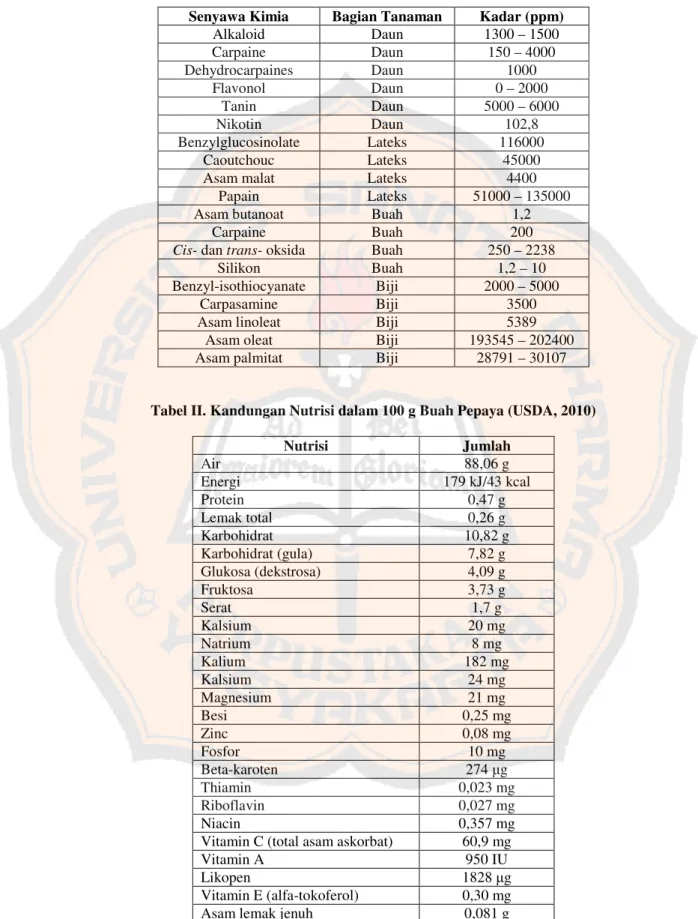
Tabel I. Komponen Kimia dalamCarica papayaL. (Duke, 2007)
Senyawa Kimia Bagian Tanaman Kadar (ppm)
Alkaloid Daun 1300 – 1500
Carpaine Daun 150 – 4000
Dehydrocarpaines Daun 1000
Flavonol Daun 0 – 2000
Tanin Daun 5000 – 6000
Nikotin Daun 102,8
Benzylglucosinolate Lateks 116000
Caoutchouc Lateks 45000
Asam malat Lateks 4400
Papain Lateks 51000 – 135000
Asam butanoat Buah 1,2
Carpaine Buah 200
Cis-dantrans-oksida Buah 250 – 2238
Silikon Buah 1,2 – 10
Benzyl-isothiocyanate Biji 2000 – 5000
Carpasamine Biji 3500
Asam linoleat Biji 5389
Asam oleat Biji 193545 – 202400
Asam palmitat Biji 28791 – 30107
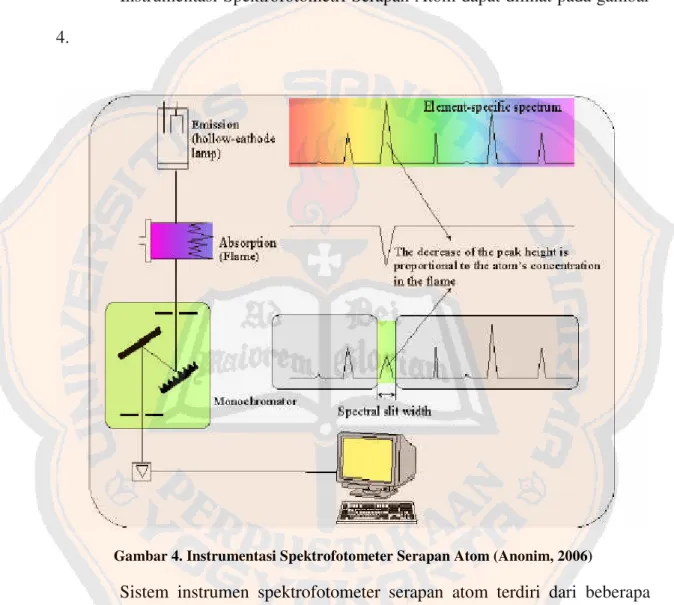
Tabel II. Kandungan Nutrisi dalam 100 g Buah Pepaya (USDA, 2010)
Nutrisi Jumlah
Air 88,06 g
Energi 179 kJ/43 kcal
Protein 0,47 g
Lemak total 0,26 g
Karbohidrat 10,82 g
Karbohidrat (gula) 7,82 g
Glukosa (dekstrosa) 4,09 g
Fruktosa 3,73 g
Beta-karoten 274μg
Thiamin 0,023 mg
Riboflavin 0,027 mg
Niacin 0,357 mg
Vitamin C (total asam askorbat) 60,9 mg
Vitamin A 950 IU
Likopen 1828μg
Vitamin E (alfa-tokoferol) 0,30 mg
3. Manfaat pepaya
Secara ekonomis, pepaya merupakan salah satu spesies terpenting
diantara famili Caricaceae dan telah dibudidayakan secara luas untuk tujuan
konsumsi sebagai buah segar dan diolah menjadi minuman, selai, jeli, es krim dan
dikeringkan (Morton, 1987). Kandungan nutrisi di dalam buah pepaya yang telah
matang menyebabkan pepaya menjadi sumber kalsium, vitamin A dan C yang
sangat baik. Buah pepaya yang belum matang memiliki kandungan lateks yang
tinggi sehingga kurang sesuai untuk dikonsumsi secara langsung. Namun, buah
pepaya mentah yang diserut sering digunakan sebagai salad di Asia. Selain itu,
buah pepaya mentah yang telah dikupas dan dimasak digunakan dalam berbagai
menu makanan di Asia (Australian Government, 2008).
Secara biokimiawi, daun dan buah pepaya memiliki kandungan kompleks
yang memproduksi beberapa protein dan alkaloid untuk kepentingan industri dan
farmasetika. Selain itu, lateks yang dihasilkan oleh seluruh bagian tanaman
pepaya, terutama dalam buah pepaya yang belum matang, memiliki kandungan
kimia berupa papain yang memiliki berbagai manfaat (Australian Government,
2008).
Secara komersial, papain memiliki berbagai kegunaan. Dalam industri
farmasetika atau kosmetik, papain dapat digunakan sebagai komponen sabun,
sampo, lotion, produk-produk perawatan kulit dan pasta gigi. Papain juga banyak
diaplikasikan dalam bidang medis dan kedokteran hewan sebagai sediaan obat
ternak, untuk pengobatan luka yang membusuk, serta untuk mengurangi
pembengkakan, demam dan adesi setelah pembedahan (Morton, 1987).
C. Spektrofotometri Serapan Atom
Spektrofotometri serapan atom digunakan untuk penetapan kadar sekitar
70 elemen secara kualitatif dan kuantitatif. Tingkat sensitivitas metode ini dapat
mencapai satuan ppm dan ppb. Kelebihan lain dari metode ini antara lain cepat,
mudah, memiliki selektivitas yang tinggi, serta biaya yang relatif murah (Skoog,
West and Holler, 1994). Kekurangan dari dari metode ini adalah dibutuhkan
sumber radiasi yang berbeda untuk masing-masing elemen (Christian, 2004).
Spektrofotometer serapan atom yang digunakan pada penelitian ini dapat dilihat
pada gambar 2.
Gambar 2. Instrumen Spektrofotometer Serapan Atom
Prinsip spektrofotometri serapan atom adalah larutan sampel mencapai
nyala tersebut terkandung atom-atom yang diteliti. Beberapa dari atom-atom ini
berada pada excitation state, tetapi sebagian besar berada pada ground state.
Atom-atom pada ground state dapat mengabsorpsi radiasi dari panjang
gelombang tertentu yang dihasilkan oleh sumber tertentu (hollow cathode lamp).
Panjang gelombang radiasi dari sumber yang tidak terserap oleh atom-atom pada
ground stateproporsional dengan jumlah atom-atom yang berada di dalam nyala.
Absorbansi secara langsung proporsional terhadap konsentrasi atom-atom dalam
bentuk gas yang terdapat dalam nyala yang juga proporsional terhadap konsentrasi
analit dalam larutan (Christian, 2004).
Proses pembentukan atom-atom logam dalam bentuk gas di dalam nyala
dapat diringkas sebagai berikut. Bila suatu larutan yang mengandung senyawa
yang cocok dari logam yang akan dianalisis itu dihembus ke dalam nyala,
terjadilah peristiwa berikut secara berurutan dengan cepat:
1. Penguapan pelarut yang meninggalkan residu padat;
2. Penguapan zat padat dengan disosiasi menjadi atom-atom penyusunnya, yang
mula-mula akan berada dalam keadaan dasar;
3. Beberapa atom dapat tereksitasi oleh energi termal (dari) nyala ke
tingkatan-tingkatan energi yang lebih tinggi, dan mencapai kondisi di mana atom-atom
tersebut akan memancarkan energi
(Basset, Martos, Souhail, and Ballesteros, 1991).
Hubungan antara populasi keadaan dasar dan keadaan eksitasi diberikan
N1/N0= (g1/g0) e- ΔE/kT (2)
keterangan : N1 = banyaknya atom dalam keadaan eksitasi N0 = banyaknya atom dalam keadaan dasar
(g1/g0) = angka banding bobot-bobot statistik untuk keadaan dasar dan keadaan eksitasi
ΔE = energi eksitasi = hv k = tetapan Boltzman
T = temperatur Kelvin (Bassetet al., 1991).
Pada gambar 3 dapat dilihat skema instrumen spektrofotometer serapan
atom yang terdiri dari sumber radiasi, nyala, monokromator, detektor, dan
readout.
Gambar 3. Bagian-bagian Instrumen Spektrofotometer Serapan Atom (Harris, 1987)
Penetapan kadar menggunakan metode spektrofotometri serapan atom
terjadi pada medium gas di mana atom-atom logam berada dalam bentuk
bebasnya. Oleh karena itu, tahap pertama dari seluruh tahapan dalam
spektrofotometri serapan atom adalah atomisasi, yaitu suatu proses di mana
sampel diuapkan dan didekomposisi untuk membentuk atom-atom dalam bentuk
presisi dan akurasi metode sehingga dapat dikatakan bahwa atomisasi merupakan
tahap kritis dari metode spektrofotometri serapan atom (Skooget al., 1994).
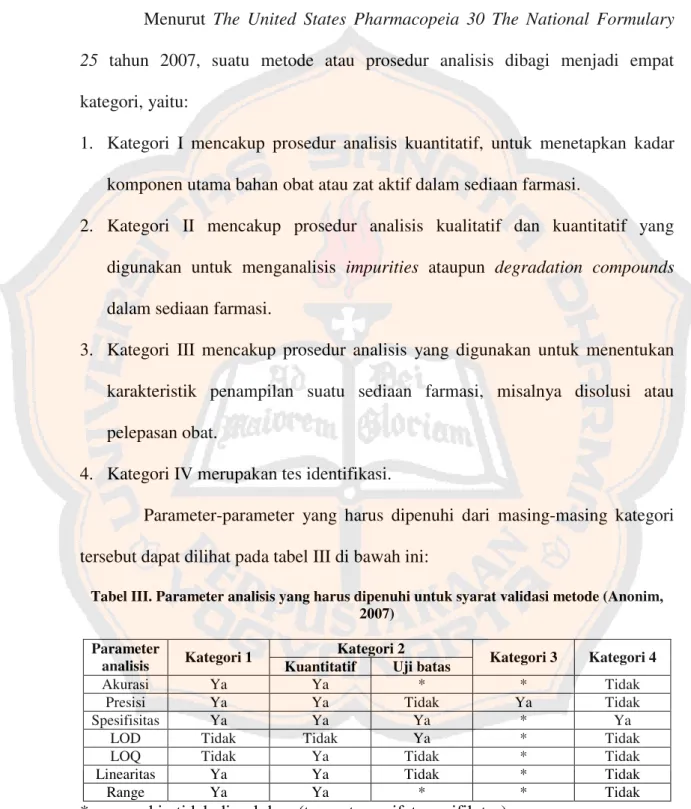
1. Instrumentasi Spektrofotometri Serapan Atom
Instrumentasi Spektrofotometri Serapan Atom dapat dilihat pada gambar
4.
Gambar 4. Instrumentasi Spektrofotometer Serapan Atom (Anonim, 2006)
Sistem instrumen spektrofotometer serapan atom terdiri dari beberapa
bagian yaitu sebagai berikut:
a. Sumber radiasi yang baik digunakan untuk spektrofotometri serapan atom
adalah hollow-cathode lamp yang terdiri dari sebuah anoda tungsten dan
katoda silindris yang terdapat di dalam tabung kaca yang mengandung gas
dilewatkan melalui elektroda, menyebabkan atom-atom dalam bentuk gas
terionisasi pada anoda. Ion-ion positif terakselerasi menuju katoda negatif.
Ketika ion-ion tersebut menyerang katoda, ion-ion tersebut akan
menyebabkan logam dalam sampel bergetar lalu menguap. Logam yang telah
menguap akan tereksitasi menuju tingkat energi yang lebih tinggi melalui
tabrakan terus-menerus dengan ion-ion gas berenergi tinggi. Ketika elektron
kembali ke ground state, spektrum karakteristik dari logam yang diteliti akan
diemisikan (Christian, 2004).
b. Pengabut berfungsi untuk menghasilkan kabut atau aerosol larutan uji. Larutan
yang akan dikabutkan ditarik ke dalam pipa kapiler oleh kerja Venturi dari
semprotan udara yang bertiup melintasi ujung kapiler; diperlukan aliran gas
bertekanan tinggi untuk menghasilkan aerosol yang halus (Bassetet al., 1991).
c. Nyala berfungsi untuk mengubah logam yang terdapat di dalam sampel yang
berupa padatan atau cairan menjadi bentuk atomnya. Sumber nyala yang
paling banyak digunakan adalah campuran asetilen sebagai bahan pembakar
dan udara sebagai pengoksidasi yang dapat menghasilkan temperatur sekitar
2200oC (Rohman, 2007).
d. Monokromator befungsi untuk memilih pita panjang gelombang yang sempit
dari sumber spektra. Monokromator terdiri dari lensa atau cermin untuk
memfokuskan radiasi, katup masuk dan keluar untuk mengurangi radiasi yang
tidak diinginkan, serta kontrol untuk membantu pemurnian spektral dari
radiasi yang diemisikan (Christian, 2004). Dalam kebanyakan instrumen
lebih seragam daripada yang dihasilkan oleh prisma, dan akibatnya instrumen
kisi dapat memelihara daya pisah yang lebih tinggi (Basset et al., 1991). Kisi
difraksi baik digunakan untuk menghasilkan lebar garis puncak serapan atom
yang sangat lebar (> 0,002-0,005 nm) dan kisi difraksi dapat menghalangi
radiasi nyala menuju detektor. Monokromator diletakkan diantara nyala dan
detektor (Mulja dan Suharman, 1995).
e. Detektor berfungsi untuk mengubah intensitas radiasi yang datang menjadi
arus listrik (Mulja dan Suharman, 1995). Pada spektrofotometer serapan atom,
digunakan photomultiplier (Basset et al., 1991). Tabung photomultiplier
terdiri dari katoda photoemissive, di mana terjadi serangan foton, serta
seperangkat elektroda (Christian, 2004).
f. Readout berupa sistem pencatat hasil yang menggunakan suatu alat yang telah
terkalibrasi untuk pembacaan suatu transmisi atau serapan (Rohman, 2007).
2. Gangguan-gangguan pada spektrofotometri serapan atom
Gangguan-gangguan (interferences) pada SSA adalah peristiwa-peristiwa
yang menyebabkan pembacaan serapan unsur yang dianalisis menjadi lebih kecil
atau lebih besar dari kadar yang sebenarnya dalam sampel (Rohman, 2007).
Gangguan-gangguan yang dapat terjadi dalam SSA antara lain:
a. Gangguan Spektral
Pada analisis emisi, baik ketika garis emisi atau pita emisi molekuler dekat
dengan garis emisi elemen yang diuji serta tidak dapat dipisahkan oleh
Gangguan spektral yang disebabkan oleh produk matriks tidak terjadi secara
luas pada atomisasi nyala dan biasanya dapat dihindari dengan variasi
beberapa parameter seperti temperatur dan perbandingan bahan bakar terhadap
senyawa oksidan (Skooget al., 1994).
b. Gangguan Ionisasi
Elemen seperti alkali dan alkali tanah serta beberapa elemen lain dapat
terionisasi dalam nyala pada temperatur yang sangat tinggi. Sinyal emisi
maupun absorpsi dapat menurun karena atom yang diukur adalah
atom-atom yang tidak terionisasi. Selain itu, adanya elemen-elemen yang mudah
terionisasi dalam sampel akan menambah jumlah elektron bebas pada nyala
sehingga menahan ionisasi elemen yang diuji (Christian, 2004).
c. Gangguan Kimia
Pemilihan kondisi operasi yang sesuai dapat meminimalkan gangguan kimia.
Umumnya, gangguan ini disebabkan oleh anion yang dapat membentuk
komponen dengan analit sehingga tingkat volatilitas menurun. Hal ini dapat
menurunkan jumlah analit yang menguap sehingga diperoleh kadar analit
yang rendah (Skooget al., 1994).
d. Gangguan Fisik
Parameter-parameter seperti jumlah sampel pada burner serta efisiensi
atomisasi merupakan gangguan-gangguan fisik. Penyebabnya antara lain,
variasi kecepatan alir gas pembakar, variasi viskositas sampel yang
disebabkan oleh temperatur dan variasi pelarut, kandungan zat padat yang
3. Analisis kuantitatif
Beberapa hal yang perlu diperhatikan dalam analisis kuantitatif antara
lain:
a. Larutan sampel diusahakan seencer mungkin, kadar unsur yang dianalisis
tidak lebih dari 5% dalam pelarut yang sesuai. Larutan yang dianalisis lebih
baik diasamkan atau kalau dilebur dengan alkali tanah, tahap terakhir harus
diasamkan lagi.
b. Hindari pemakaian pelarut aromatik atau halogen. Pelarut organik yang umum
digunakan adalah keton, ester, dan etil asetat. Hendaklah menggunakan
pelarut-pelarut untuk analisis dengan derajat pro-analisis.
c. Dilakukan perhitungan atau kalibrasi dengan zat standar, sama seperti pada
pelaksanaan spektrofotometri UV-Vis (Mulja dan Suharman, 1995).
D. Validitas Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap
parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan
bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita,
2004). Validasi metode analisis diartikan sebagai suatu prosedur yang digunakan
untuk membuktikan bahwa metode analisis tersebut dapat memberikan hasil
seperti yang diharapkan dengan kecermatan dan ketelitian yang memadai. Metode
analisis instrumen merupakan metode yang terpilih dan memadai untuk
dianalisis dan kompleksnya matriks sampel yang dianalisis (Mulja dan Suharman,
1995).
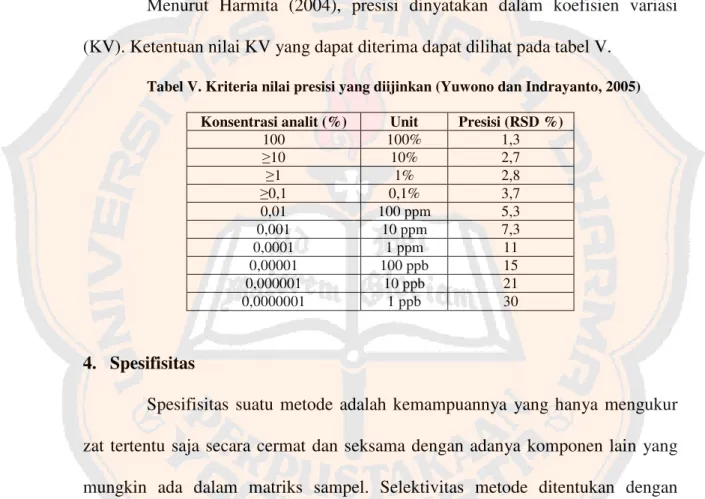
Menurut The United States Pharmacopeia 30 The National Formulary
25 tahun 2007, suatu metode atau prosedur analisis dibagi menjadi empat
kategori, yaitu:
1. Kategori I mencakup prosedur analisis kuantitatif, untuk menetapkan kadar
komponen utama bahan obat atau zat aktif dalam sediaan farmasi.
2. Kategori II mencakup prosedur analisis kualitatif dan kuantitatif yang
digunakan untuk menganalisis impurities ataupun degradation compounds
dalam sediaan farmasi.
3. Kategori III mencakup prosedur analisis yang digunakan untuk menentukan
karakteristik penampilan suatu sediaan farmasi, misalnya disolusi atau
pelepasan obat.
4. Kategori IV merupakan tes identifikasi.
Parameter-parameter yang harus dipenuhi dari masing-masing kategori
tersebut dapat dilihat pada tabel III di bawah ini:
Tabel III. Parameter analisis yang harus dipenuhi untuk syarat validasi metode (Anonim, 2007)
Kategori 2 Parameter
analisis Kategori 1 Kuantitatif Uji batas Kategori 3 Kategori 4
Akurasi Ya Ya * * Tidak
Presisi Ya Ya Tidak Ya Tidak
Spesifisitas Ya Ya Ya * Ya
LOD Tidak Tidak Ya * Tidak
LOQ Tidak Ya Tidak * Tidak
Linearitas Ya Ya Tidak * Tidak
Range Ya Ya * * Tidak
Oleh karena itu, diperlukan suatu pedoman mengenai kesahihan metode
analisis yang didukung oleh parameter-parameter di bawah ini:
1. Linearitas
Linearitas merupakan kemampuan suatu metode (pada rentang tertentu)
untuk mendapatkan hasil uji yang secara langsung proporsional dengan
konsentrasi (jumlah) analit di dalam sampel. Rentang adalah jarak antara level
terbawah dan teratas konsentrasi analit yang telah diuji untuk mendapatkan
presisi, linearitas, dan akurasi yang bisa diterima (Anonim, 2007). Koefisien
korelasi akan mengindikasikan linearitas apabila nilai r > 0,999 (Yuwono dan
Indrayanto, 2005).
2. Akurasi
Akurasi atau kecermatan adalah ukuran yang menunjukkan derajat
kedekatan hasil analisis dengan kadar analit yang sebenarnya. Akurasi dinyatakan
sebagai persen perolehan kembali (recovery) analit yang ditambahkan (Harmita,
2004). Menurut Yuwono dan Indrayanto (2005), rentang kesalahan yang diijinkan
pada setiap konsentrasi analit pada matriks dapat dilihat pada tabel IV.
Tabel IV. Kriteria rata-ratarecoveryyang diijinkan (Yuwono dan Indrayanto, 2005)
Konsentrasi analit (%) Unit Rata-rataRecovery(%)
100 100% 98-102
≥10 10% 98-102
≥1 1% 97-103
≥0,1 0,1% 95-105
0,01 100 ppm 90-107
0,001 10 ppm 80-110
0,0001 1 ppm 80-110
0,00001 100 ppb 80-110
0,000001 10 ppb 60-115
Menurut Snyder, Kirkland dan Glajch (1997), umumnya akurasi
ditentukan melalui penetapan recovery, tetapi ada tiga cara untuk menentukan
akurasi, yaitu:
a. Perbandingan dengan Standar
Penentuan recovery melalui perbandingan langsung terhadap standar (bahan
standar referensi) adalah pilihan teknik yang utama untuk analit dalam matriks
sampel yang tidak kompleks.
b. RecoveryAnalit
Jika analit yang digunakan berada dalam matriks sampel yang kompleks,
dapat digunakan metode spike recovery. Standar referensi analit ditambahkan
dalam matriks kosong (placebo). Misalnya, dalam analisis formulasi obat,
matriks kosong yang digunakan termasuk seluruh komposisi formulasi,
kecuali analit yang diukur.
c. Metode Standar Adisi
Pada metode standar adisi, standar yang telah diketahui jumlahnya
ditambahkan ke dalam matriks sampel yang diketahui telah mengandung
sejumlah analit yang belum diketahui kadarnya. Konsentrasi yang diperoleh
dari larutan tersebut merupakan konsentrasi analit dan standar yang
ditambahkan. Hasil konsentrasi analit dan standar tersebut dibandingkan
dengan konsentrasi analit dalam larutan yang tidak ditambah standar. Hasil
perbandingan tersebut merupakan recovery standar yang ditambahkan.
Metode ini digunakan ketika matriks kosong tanpa analit tidak memungkinkan
3. Presisi
Presisi atau keseksamaan adalah ukuran yang menunjukkan derajat
kesesuaian antara hasil uji individual, diukur melalui penyebaran hasil individual
dari rata-rata jika prosedur diterapkan secara berulang pada sampel-sampel yang
diambil dari campuran yang homogen (Harmita, 2004).
Menurut Harmita (2004), presisi dinyatakan dalam koefisien variasi
(KV). Ketentuan nilai KV yang dapat diterima dapat dilihat pada tabel V.
Tabel V. Kriteria nilai presisi yang diijinkan (Yuwono dan Indrayanto, 2005)
Konsentrasi analit (%) Unit Presisi (RSD %)
100 100% 1,3
0,00001 100 ppb 15
0,000001 10 ppb 21
0,0000001 1 ppb 30
4. Spesifisitas
Spesifisitas suatu metode adalah kemampuannya yang hanya mengukur
zat tertentu saja secara cermat dan seksama dengan adanya komponen lain yang
mungkin ada dalam matriks sampel. Selektivitas metode ditentukan dengan
membandingkan hasil analisis sampel yang mengandung cemaran, hasil urai,
senyawa sejenis, senyawa asing lainnya atau pembawa plasebo dengan hasil
analisis sampel tanpa penambahan bahan-bahan tadi. Penyimpangan hasil
5. LOD (limit of detection) dan LOQ (limit of quantitation)
LOD adalah kuantitas terkecil analit dalam sampel yang dapat dideteksi
dan masih memberikan respon signifikan dibandingkan dengan blanko. LOQ
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi
kriteria akurasi dan presisi. LOD dan LOQ dapat dihitung secara statistik melalui
garis regresi linier dari kurva kalibrasi (Harmita, 2004).
Detection limit dan quantitation limit dapat didefinisikan sebagai rasio
signal-to-noise, dengan nilai 2:1 atau 3:1 untuk detection limit dan nilai 10:1
E. Landasan Teori
Timbal merupakan logam yang terdapat dalam asap kendaraan bermotor.
Walaupun saat ini timbal sebagai bahan aditif bensin tidak digunakan lagi, tetapi
cemaran timbal di atmosfer sudah cukup tinggi. Manusia dapat terpapar oleh
timbal melalui berbagai sumber, diantaranya adalah melalui makanan yang
dikonsumsi. Absorpsi timbal yang berlebih dalam jangka waktu yang lama dapat
mengakibatkan akumulasi timbal di tubuh yang dapat menyebabkan keracunan.
Sampel yang digunakan dalam penelitian ini adalah buah pepaya karena
memiliki banyak manfaat karena banyak mengandung kalsium, vitamin A dan C,
serta kandungan nutrisi yang lain. Selain itu, pepaya merupakan buah yang
banyak dikonsumsi masyarakat Indonesia. Batas kadar timbal dalam buah
menurut SNI 7387:2009 adalah 0,5 mg/kg.
Menurut penelitian yang dilakukan oleh Kristiono (1999) diketahui
bahwa terdapat pengaruh semakin meningkatnya lama waktu buah dipaparkan
pada udara yang tercemar asap kendaraan bermotor terhadap peningkatan kadar
timbal dalam buah. Perlakuan berupa perbedaan lama waktu pemaparan terhadap
udara yang tercemar asap kendaraan bermotor dapat menyebabkan peningkatan
kadar timbal dalam buah pepaya.
Spektrofotometer serapan atom merupakan instrumen yang digunakan
untuk mengukur kadar logam dalam suatu analit. Prinsip metode spektrofotometri
serapan atom adalah atomisasi logam pada temperatur yang sangat tinggi. Logam
akan menjadi atom-atom bebas yang akan mengabsorpsi cahaya dari lampu yang
absorbansi ini proporsional dengan kadar analit logam dalam sampel. Timbal
merupakan logam pada golongan transisi sehingga kadar timbal dalam buah
pepaya akan dapat ditetapkan kadarnya menggunakan spektrofotometri serapan
atom.
Validasi metode analisis untuk membuktikan bahwa metode tersebut
memenuhi persyaratan untuk digunakan serta dapat memberikan hasil seperti
yang diharapkan dengan kecermatan dan ketelitian yang memadai. Parameter
validitas yang akan diukur adalah LOD, LOQ, akurasi, presisi, linearitas, dan
F. Hipotesis
1. Metode spektrofotometri serapan atom pada penetapan kadar timbal (Pb)
dalam buah pepaya memenuhi persyaratan validasi: akurasi, presisi dan
linearitas, LOD, LOQ serta memiliki spesifisitas yang baik.
2. Ho = rata-rata kadar timbal dalam buah pepaya kelompok kontrol, 4 hari, dan
8 hari pada masing-masing pedagang berbeda tidak signifikan.
H1 = rata-rata kadar timbal dalam buah pepaya kelompok kontrol, 4 hari, dan
8 hari pada masing-masing pedagang berbeda signifikan.
3. Rata-rata kadar timbal dalam buah pepaya yang telah mengalami perlakuan
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini merupakan penelitian eksperimental karena adanya
perlakuan berupa perbedaan lama waktu pemaparan di pinggir jalan terhadap
subyek uji, yaitu buah pepaya.
B. Variabel Penelitian 1. Variabel bebas
Variabel bebas adalah variabel yang menyebabkan perubahan pada
variabel tergantung. Variabel bebas pada penelitian ini adalah lama waktu
penitipan buah pepaya pada pedagang di pinggir jalan.
2. Variabel tergantung
Variabel tergantung adalah variabel yang dapat berubah karena
dipengaruhi oleh variabel bebas. Variabel tergantung pada penelitian ini adalah
kadar timbal (Pb) dalam buah pepaya pada tiap kelompok.
3. Variabel terkendali
Variabel terkendali adalah variabel yang keberadaannya tidak diteliti
tetapi dapat menyebabkan perubahan pada variabel tergantung dan dapat
dikendalikan. Variabel terkendali dalam penelitian ini yaitu:
a.
a. Usia buah pepaya
Untuk mengatasinya dilakukan pemilihan usia buah pepaya yang hampir
sama yaitu berkisar 2-3 bulan.
b. Usia pohon pepaya
Untuk mengatasinya, pohon pepaya yang digunakan usianya hampir sama,
yaitu 8 bulan karena ditanam pada waktu yang hampir bersamaan.
c. Instrumen spektrofotometer serapan atom
Untuk mengatasinya, instrumen yang digunakan pada kondisi tinggi burner
dan kecepatan alir yang optimum serta menggunakan panjang gelombang
maksimum.
d. Temperatur
Untuk mengatasinya, digunakan temperatur yang sama pada saat proses
destruksi.
e. Ukuran buah pepaya.
Untuk mengatasinya, buah pepaya yang digunakan ukurannya hampir sama.
f. Perlakuan homogenisasi
Untuk mengatasinya, sampel pada tiap kelompok diberi perlakuan yang
sama yaitu dengan mengelupas kulit buah, memotongnya kecil-kecil
C. Definisi Operasional
1. Metode SSA berprinsip pada absorbansi cahaya oleh atom bebas. Penyerapan
cahaya tersebut pada panjang gelombang tertentu, tergantung pada sifat setiap
unsur. Panjang gelombang penyerapan logam Pb adalah 217 nm.
2. Parameter validasi metode analisis yang digunakan adalah LOD, LOQ,
akurasi, presisi, dan linearitas.
3. Kadar timbal dalam buah pepaya dengan satuan ppm (mg/kg).
D. Bahan Penelitian
Bahan yang digunakan dalam penelitian adalah: larutan standar timbal
1000 ppm (certiPUR®,Merck), HNO3pekatp.a (E. Merck), HClO4 pekatp.a (E.
Merck), larutan asam pengencer (HNO3) dengan pH 2 dan aquabidest (LPPT
UGM), milipore (ukuran 0,45 μm; tipe DURAPORE, MA 01730; Milipore
Corporation, Bedford), bahan bakar untuk spektrofotometer serapan atom berupa
C2H2/udara (Air Product Semarang).
E. Alat penelitian
Alat yang digunakan dalam penelitian ini adalah spektofotometer serapan
atom (merk Analytik Jena; tipe contrAA; nomor seri 300; tahun 2007; teknik
flame; panjang gelombang 217 nm; kecepatan alir bahan bakar 65 L/h; tipeburner
100 mm; tinggi burner 6 mm) dengan hollow cathode lamp untuk timbal, hot
LTD.), alat-alat gelas, dan neraca analitik (OHAUS PAJ 1003; max = 1050 ct;
readability= 0,001 ct; Corp. Pine Brook, NJ, USA).
Pengukuran kadar timbal dengan spektrofotometer serapan atom
dilakukan di LPPT Universitas Gadjah Mada Yogyakarta.
F. Tata Cara Penelitian 1. Teknik pengambilan sampel
Pengambilan sampel buah pepaya dilakukan di perkebunan pepaya
pinggir Jalan Raya Mayor Unus KM 6 Gentan, Wayuhan, Kabupaten Magelang.
Pengambilan sampel dilakukan pada bagian tengah kebun untuk mengurangi
kemungkinan pencemaran timbal yang disebabkan oleh asap kendaraan yang
melintas di sekitar perkebunan. Sampel buah pepaya dengan usia buah yang
hampir sama (2-3 bulan) diambil secara acak sebanyak 35 buah yang dibagi
menjadi beberapa kelompok sesuai dengan tempat penitipan buah sebagai berikut:
a. Kontrol sebanyak 5 buah.
b. Pedagang di Jalan Colombo (I) sebanyak 10 buah.
c. Pedagang di Jalan A.M. Sangaji (II) sebanyak 10 buah.
d. Pedagang di Jalan Gedong Kuning (III) sebanyak 10 buah.
Selanjutnya, perlakuan yang diberikan pada buah pepaya adalah
perbedaan lama waktu penitipan di tiap pedagang. Lama waktu penitipan adalah 4
2. Preparasi sampel
Setelah waktu perlakuan selesai, buah pepaya dipreparasi perkelompok
berdasarkan lokasi penitipan. Buah pepaya dikupas kulitnya, kemudian dipotong
kecil-kecil seukuran dadu. Buah pepaya yang sudah dipotong-potong tersebut
dicuplik untuk dihomogenkan dengan blender sehingga buah pepaya menjadi
halus (seperti bubur).
Pepaya yang sudah dihaluskan lebih kurang 15,0 g ditimbang seksama,
dimasukkan ke dalam Erlenmeyer 250 mL. Kemudian ditambahkan 15 mL HNO3
pekat p.a dan dipanaskan di atas hot plate pada temperatur ± 70-90 oC dengan
keadaan ditutup corong gelas. Proses destruksi dengan HNO3pekat p.adilakukan
hingga larutan tidak mengeluarkan asap coklat lagi dan larutan menjadi jernih
dengan volume < 10 mL. Larutan diturunkan dari hot plate dan ditunggu hingga
dingin. Setelah larutan dingin, ditambahkan HClO4 pekat p.a sebanyak 3 mL
secara hati-hati dan pemanasan dilanjutkan kembali dengan keadaan Erlenmeyer
tidak bertutup hingga volume < 5 mL. Larutan didinginkan pada temperatur
ruangan dan setelah itu dimasukkan dalam labu ukur 5 mL dan ditambah larutan
asam pengencer (larutan HNO3 pH 2) hingga garis batas. Apabila larutan tidak
jernih (ada endapan) maka dilakukan penyaringan denganmilipore.
Proses terakhir larutan sampel diukur absorbansinya dengan
3. Pembuatan kurva baku timbal
Larutan intermediet I dibuat dari larutan baku timbal dengan konsentrasi
1000 ppm yang diencerkan menjadi 100 ppm dalam labu 10 mL. Kemudian dari
larutan intermediet I dibuat larutan intermediet II dengan konsentrasi 50 ppm.
Larutan standar timbal dengan kadar 0,25; 0,5; 1,0; 1,5; 2,0; 2,5; dan 3,0 ppm
diperoleh dengan cara mengencerkan larutan intermediet II. Absorbansi
masing-masing seri kurva baku diukur dengan instrumen spektrofotometer serapan atom
pada panjang gelombang 217 nm.
4. Penetapan akurasi dan presisi
a. Akurasi dan presisi baku. Larutan timbal dibuat dalam tiga konsentrasi
yang berbeda, yaitu konsentrasi tinggi (3,0 ppm), tengah (1,5 ppm) dan rendah
(0,25 ppm). Replikasi dilakukan sebanyak 3 kali dan ripitasi masing-masing
konsentrasi sebanyak 3 kali. Kemudian larutan tersebut diukur absorbansinya
dengan spektrofotometer serapan atom. Kadar`timbal terukur ditentukan dengan
memasukkan nilai absorbansi yang diperoleh dalam persamaan kurva baku lalu
ditentukan nilairecoverydan KV baku timbal.
b. Akurasi dan presisi dengan metode standar adisi. Sampel dipreparasi
dengan destruksi (dengan perlakuan yang sama dengan preparasi sampel yang
akan ditentukan kadarnya). Sampel hasil destruksi diencerkan dengan larutan
asam pengencer hingga volume 5 mL. Replikasi tiga kali dengan ripitasi tiga kali.
Ukur serapan menggunakan instrumen spektrofotometer serapan atom panjang
destruksi (dengan perlakuan yang sama dengan preparasi sampel yang akan
ditentukan kadarnya). Namun, sebelum sampel hasil destruksi diencerkan dengan
larutan asam pengencer pH 2 hingga volume 5 mL, terlebih dahulu ditambahkan
larutan baku timbal dengan konsentrasi 1 ppm. Replikasi tiga kali dengan ripitasi
tiga kali. Ukur serapan menggunakan instrumen spektrofotometer serapan atom
dengan panjang gelombang 217 nm. Presisi baku timbal dengan metode standar
adisi menggunakan data yang diperoleh dari hasil penetapan akurasi dengan
metode standar adisi sebelumnya. Nilai KV diperoleh dengan membagi nilai
standar deviasi (SD) dengan rata-ratarecoverybaku timbal metode standar adisi.
5. Penetapan linearitas
Penetapan linearitas didapat dengan membuat larutan seri kurva baku
dengan konsentrasi 0,25; 0,5; 1,0; 1,5; 2,0; 2,5; dan 3,0 ppm yang masing-masing
direplikasi 3 kali. Mengukur absorbansinya dengan instrumen spektrofotometer
serapan atom pada panjang gelombang 217 nm.
6. Penentuandetection limit
Penentuandetection limit dengan mengukur absorbansi blanko sebanyak
3 kali. Blanko yang digunakan adalah larutan asam pengencer (larutan HNO3pH
2). Berdasarkan data absorbansi blanko yang diperoleh, dapat ditentukan batas
7. Penentuanquantitation limit
Penentuan quantitation limit dengan mengukur absorbansi blanko
sebanyak 3 kali. Blanko yang digunakan adalah larutan asam pengencer (larutan
HNO3 pH 2). Berdasarkan data absorbansi blanko yang diperoleh, dapat
ditentukan batas kuantifikasi yaitu 10 kali rata-rata absorbansi blanko.
8. Analisis sampel secara kuantitatif
Pengukuran secara kuantitatif dilakukan dengan membuat kurva kalibrasi
antara absorbansi dengan konsentrasi larutan standar. Absorbansi sampel yang
dihasilkan diinterpolasikan pada kurva kalibrasi sehingga konsentrasi unsur timbal
dalam larutan sampel dapat ditentukan.
G. Analisis Hasil 1. Akurasi
Berdasarkan persamaan linear kurva baku (y = Bx + A), dapat ditentukan
kadar baku timbal terukur (x) dengan memasukkan nilai absorbansi yang
dihasilkan (y). Perbandingan antara kadar baku timbal terukur (Pb) dengan kadar
baku timbal (Pb) secara teoritis yang diketahui merupakan nilai recovery baku,
yang dapat dihitung dengan cara berikut:
(3)
Syarat akurasi untuk baku timbal menggunakan syarat akurasi untuk
adisi menggunakan syarat untuk konsentrasi analit 1 ppm, yaitu 80-110%
(Yuwono dan Indrayanto, 2005).
2. Presisi
Presisi metode analisis dinyatakan dengan nilai KV (koefisien variansi),
yang dapat dihitung dengan cara berikut :
(4)
Syarat presisi untuk baku timbal menggunakan syarat presisi untuk
konsentrasi analit 100%, yaitu 1,3%. Syarat akurasi dengan metode standar adisi
menggunakan syarat untuk konsentrasi analit 1 ppm, yaitu 11% (Yuwono dan
Indrayanto, 2005).
3. Linearitas
Linearitas dinyatakan dengan nilai koefisien korelasi (r) pada analisis
regresi linear (y = Bx + A). Koefisien korelasi akan mengindikasikan linearitas
apabila nilai r > 0,999 (Yuwono dan Indrayanto, 2005).
4. Detection limit
Detection limit dalam suatu metode analisis dapat ditentukan dengan
5. Quantitation limit
Quantitation limit dalam suatu metode analisis dapat ditentukan dengan
rasiosignal to noisebernilai 10:1 (Yuwono dan Indrayanto, 2005).
6. Penentuan kadar sampel
Berdasarkan hasil pengukuran kadar sampel ditentukan besarnya (x)
dengan memasukkan nilai absorbansi yang dihasilkan (y) pada persamaan linier
kurva baku (y = B x + A) yang dipilih. Satuan kadar dalam (mg/mL) x 10-3
BAB IV
HASIL DAN PEMBAHASAN
A. Pembuatan Larutan Baku Timbal
Larutan baku timbal yang digunakan merupakan larutan stok standar
timbal p.a. yang menggunakan pelarut asam nitrat. Larutan baku timbal ini
kemudian dibuat menjadi beberapa konsentrasi menggunakan pelarut asam nitrat
dengan pH 2. Asam nitrat yang digunakan dalam pembuatan pelarut adalah asam
nitrat p.a.. Penggunaan pelarut asam nitrat pH 2 ini mengacu pada metode SNI
6989.8:2009 yang bertujuan agar ion timbal (Pb2+) dalam larutan menjadi lebih
stabil.
Larutan stok standar timbal p.a. tersedia dalam konsentrasi 1000 ppm.
Kemudian dibuat larutan intermediet 1 dengan kadar 100 ppm dan larutan
intermediet 2 dengan kadar 50 ppm. Selanjutnya dibuat larutan seri baku timbal
dengan tujuh konsentrasi yang berbeda yaitu, 0,25; 0,5; 1; 1,5; 2; 2,5; dan 3 ppm.
Pembuatan kurva baku timbal ini disesuaikan dengan hasil orientasi kadar timbal
dalam sampel yang akan digunakan serta hasil penentuan LOD dan LOQ yang
diperoleh. Selain itu, disesuaikan dengan batas maksimal timbal dalam
buah-buahan menurut SNI 7387:2009 sebesar 0,5 mg/kg. Oleh karena itu, pemilihan
seri konsentrasi kurva baku ini bertujuan agar kadar yang terdapat dalam sampel
dapat diinterpolasikan dalam persamaan kurva baku sehingga persamaan kurva
baku yang diperoleh dapat digunakan untuk menentukan kadar timbal dalam
sampel.
B. Penetapan Kurva Baku
Pembuatan kurva baku timbal untuk penetapan kadar dilakukan replikasi
tiga kali. Hasil pengukuran absorbansi masing-masing konsentrasi kurva baku
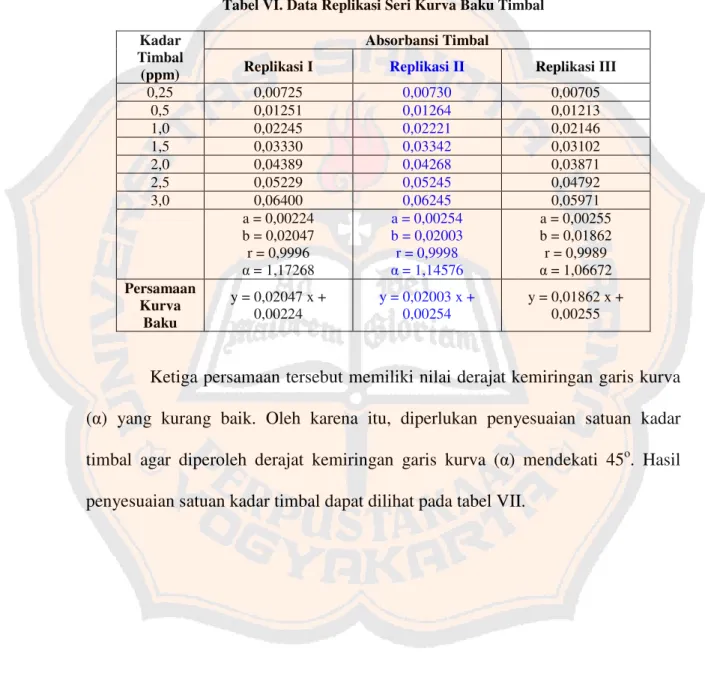
timbal diperoleh data yang dapat dilihat pada tabel VI berikut:
Tabel VI. Data Replikasi Seri Kurva Baku Timbal
Absorbansi Timbal Kadar
Timbal
(ppm) Replikasi I Replikasi II Replikasi III
0,25 0,00725 0,00730 0,00705
0,5 0,01251 0,01264 0,01213
1,0 0,02245 0,02221 0,02146
1,5 0,03330 0,03342 0,03102
2,0 0,04389 0,04268 0,03871
2,5 0,05229 0,05245 0,04792
3,0 0,06400 0,06245 0,05971
a = 0,00224
Ketiga persamaan tersebut memiliki nilai derajat kemiringan garis kurva
(α) yang kurang baik. Oleh karena itu, diperlukan penyesuaian satuan kadar
timbal agar diperoleh derajat kemiringan garis kurva (α) mendekati 45o. Hasil
Tabel VII. Data Replikasi Seri Kurva Baku Timbal dengan Penyesuaian Satuan Kadar Timbal
Absorbansi Timbal Kadar Timbal
(mg/20 mL) x 10-3 Replikasi I Replikasi II Replikasi III
5 0,00725 0,00730 0,00705
10 0,01251 0,01264 0,01213
20 0,02245 0,02221 0,02146
30 0,03330 0,03342 0,03102
40 0,04389 0,04268 0,03871
50 0,05229 0,05245 0,04792
60 0,06400 0,06245 0,05971
a = 0,00224
Kurva baku yang digunakan dalam penelitian ini adalah kurva baku yang
dapat memberikan linearitas yang baik. Linearitas merupakan kemampuan suatu
metode (pada rentang tertentu) untuk mendapatkan hasil uji yang secara langsung
proporsional dengan konsentrasi (jumlah) analit di dalam sampel (Anonim, 2007).
Menurut Yuwono dan Indrayanto (2005), linearitas ditunjukkan dengan nilai
koefisien korelasi (r) > 0,999.
Pada penelitian ini, kurva baku yang dipilih adalah kurva baku replikasi
kedua karena memiliki nilai r yang paling baik. Persamaan kurva baku yang
digunakan adalah y = 1,00156 x + 0,00254 dengan nilai r sebesar 0,9998.
Hubungan korelasi antara kadar timbal dan absorbansi yang diperoleh dapat
Kurva Baku Timbal
Gambar 5. Absorbansi Logam Pb versus Kadar Timbal (Replikasi 2)
Berdasarkan gambar 5 di atas, dapat dilihat bahwa terjadi peningkatan
absorbansi seiring dengan meningkatnya kadar timbal dalam larutan sehingga
diperoleh linearitas yang baik.
C. Parameter Validitas Metode
Tujuan validasi metode penelitian ini adalah untuk mengetahui apakah
metode SSA yang digunakan untuk menentukan kadar timbal dalam pepaya
memiliki validitas yang baik. Hal ini dapat dilihat dari beberapa parameter yaitu
limit of detection (LOD), limit of quantitation (LOQ), akurasi, presisi, dan
linearitas.
1. Limit of detection(LOD) danlimit of quantitation(LOQ)
Penelitian ini termasuk metode analisis kategori II yang mencakup
prosedur analisis kuantifikasi impurities. Oleh karena itu, dilakukan penentuan
Detection limit merupakan kadar analit terkecil masih dapat terdeteksi
dan memberikan respon yang signifikan dibandingkan dengan respon blanko,
tetapi tidak perlu kuantitatif. Quantitation limit merupakan kuantitas terkecil
analit yang masih dapat memenuhi kriteria akurasi dan presisi. Rasio
signal-to-noise untuk detection limit adalah 2:1 atau 3:1 dan rasio signal-to-noise untuk
quantitation limitadalah 10:1 (Yuwono dan Indrayanto, 2005).
Pada penelitian ini penentuan LOD dan LOQ didasarkan pada
perhitungan absorbansi blanko berupa asam nitrat pH 2 yang digunakan sebagai
larutan asam pengencer. Hasil penetapan LOD dan LOQ yang diperoleh dapat
dilihat pada tabel VIII berikut dan perhitungannya dapat dilihat pada lampiran 4.
Tabel VIII. Hasil Pengukuran Absorbansi Blanko (Asam nitrat pH 2), LOD, dan LOQ
Replikasi Absorbansi Rata-rata
Absorbansi LOD LOQ
1 0,00059
2 0,00054
3 0,00056
0,00056 0,00168 0,00560
Berdasarkan tabel VIII, dapat diketahui nilai detection limit sebesar
0,00168 atau tiga kali absorbansi blanko dan quantitation limit sebesar 0,00560
atau 10 kali absorbansi blanko. Nilai terendah kurva baku ditentukan berdasarkan
quantitation limit yang diperoleh. Berdasarkan data pada tabel VI, dapat dilihat
bahwa absorbansi larutan timbal pada kadar 0,25 ppm lebih besar dari
quantitation limit sehingga hasil penetapan kadar timbal akan memiliki akurasi
2. Akurasi
Akurasi menunjukkan seberapa dekat hasil analisis yang akan diperoleh
dengan kadar analit yang sebenarnya. Menurut Snyder et al. (1997), ada tiga cara
untuk menetapkan recovery, yaitu: pembandingan standar, recoverypenambahan
analit ke dalam matriks kosong, atau adisi standar pada analit. Pada penelitian ini
metode yang digunakan untuk penetapanrecoveryadalah dengan melakukan adisi
standar pada analit dan penetapanrecoverybaku timbal.
Pada penetapan recovery baku timbal, digunakan tiga larutan dengan
konsentrasi yang berbeda, yaitu 0,25; 1,5; dan 3,0 ppm yang masing-masing
direplikasi tiga kali. Kadar timbal terukur diperoleh dengan cara memasukkan
nilai absorbansi ke persamaan y = 1,00156 x + 0,00254. Perhitungan penentuan
kadar timbal terukur serta recovery baku timbal dapat dilihat pada lampiran 5.
Hasil penetapanrecoverybaku timbal dapat dilihat pada tabel IX.
Tabel IX. DataRecoveryBaku Timbal
Kadar Timbal
Teoritis (ppm) Replikasi Absorbansi
Kadar Timbal Terukur (ppm)
% Recovery
1 0,00725 0,23515 94,06%
2 0,00730 0,23764 95,06%
0,25
3 0,00713 0,22916 91,66%
1 0,03330 1,53570 102,38%
2 0,03282 1,51173 100,78%
1,5
3 0,03314 1,52771 101,85%
1 0,06400 3,06840 102,28%
2 0,06490 3,11333 103,78%
3,0
3 0,06619 3,17773 105,92%
Hasil recovery baku timbal pada kadar 0,25 ppm adalah 91,66-95,06%,
pada kadar 1,5 ppm adalah 100,78-102,38%, dan pada kadar 3,0 ppm adalah
analit 100%, rata-rata recovery yang baik adalah 98-102%. Berdasarkan hasil
yang diperoleh, maka dapat dikatakan bahwa recovery pada penelitian ini baik
pada kadar 1,5 ppm karena memenuhi syaratrecoveryyang baik.
Pada metode standar adisi, analit yang digunakan terdapat dua kelompok,
yaitu kelompok yang belum diadisi dan sampel yang telah diadisi, masing-masing
direplikasi tiga kali. Larutan standar timbal yang ditambahkan pada analit adalah
1 μg/mL. Kedua kelompok ini kemudian dibandingkan untuk diketahui recovery
standar timbal yang ditambahkan. Kadar timbal diperoleh dengan cara
memasukkan nilai absorbansi ke persamaan y = 1,00156 x + 0,00254 sebagai nilai
y. Perhitungan penentuan kadar timbal serta recovery baku timbal dapat dilihat
pada lampiran 5. Hasil recovery dengan metode standar adisi dapat dilihat pada
Tabel X. HasilRecoveryKadar Timbal dengan Metode Standar Adisi
Sampel Sampel + Baku
Replikasi Absorbansi Rata-rata Absorbansi
Kadar Timbal
(μg/5 mL) Replikasi Absorbansi