3.1 Alat dan Bahan 3.1.1 Alat
a. Neraca analitik digital Mettler PM 480 b. Spektofotometer UV-Vis Shimadzu
c. Rotary evaporator Buchi
d. Inkubator Memmert
e. Autoklaf Himaraya
f. Laminar air flow Esco
g. Penangas air
h. Peralatan gelas Pyrex
i. Pipet volume Pyrex
j. Pipet tetes
k. Tabung reaksi Pyrex
l. Cawan petri m.Corong
n. Labu Ekstraksi Pyrex
o. Labu Takar Pyrex
p. Batang Pengaduk q. Botol vial
r. Bulb Pipet s. Blender
t. Gelas Beker Pyrex
u. Erlenmeyer Pyrex
v. Spatula
3.1.2 Bahan
Daun senduduk
Aquadest
Metanol
Etanol p.a
Etil asetat
n-Heksana
Diphenil Pikril Hidrazil (DPPH)
DMSO
Media Nutrien Agar
Media Mueller Hilton Agar
Media BHIB
Media Nutrien Broth
Asam Askorbat
FeCl3
NaOH
HCl
NH4OH
3.2 Prosedur Penelitian 3.2.1 Penyediaan Sampel
Daun yang diteliti adalah daun tumbuhan senduduk yang diperoleh dari daerah Tapus, Kabupaten Panti, Sumatera Barat. Daun tumbuhan senduduk ini dikeringkan di udara terbuka, lalu dihaluskan sampai diperoleh serbuk sebanyak 500 g.
3.2.2 Ekstrak Daun Senduduk
etil asetat. Endapan yang diperoleh berupa ekstrak padat metanol. Ekstrak etil asetat yang diperoleh dipekatkan dengan alat rotary evaporator sehingga diperoleh ekstrak pekat etil asetat. Ekstrak pekat etil asetat dilarutkan dengan metanol kemudian diekstraksi partisi dengan n-heksana sehingga terbentuk lapisan n-heksana dan metanol fraksi etil asetat. Masing-masing fraksi n-heksana dan ekstrak metanol fraksi fraksi etil asetat dipekatkan dengan alat rotari evaporator, sehingga diperoleh ekstrak pekat n-heksana dan ekstrak pekat metanol fraksi etil asetat.
3.2.3 Uji Antioksidan dengan Metode DPPH
3.2.3.1. Pembuatan Larutan DPPH 0,3 mM (BM=394,32g/mol)
Larutan DPPH 0,3 mM dibuat dengan melarutkan 11,82 mg serbuk DPPH dalam etanol p.a kemudian dimasukkan ke dalam labu takar 100 mL dan dicukupkan volumenya sampai tanda garis kemudian dihomogenkan.
3.2.3.2. Pembuatan Variasi Ekstrak Daun Senduduk a. Ekstrak n-Heksana
Ekstrak pekat n-heksana dibuat larutan induk 1000 mg/L, dengan melarutkan 0,025 g dengan pelarut etanol p.a dalam labu takar 25 mL. Larutan induk 1000 mg/L dilakukan pengenceran menjadi larutan 100 mg/L, dari larutan 100 mg/L dibuat variasi konsentrasi 10,20,40,80 mg/L untuk uji aktivitas antioksidan.
Perlakuan yang sama juga dilakukan terhadap ekstrak padat metanol dan ekstrak pekat metanol fraksi etil asetat.
3.2.3.3. Pengujian Aktivitas Antioksidan a. Pengujian larutan blanko
b. Pengujian aktivitas antioksidan sampel
Sebanyak 1 mL larutan DPPH 0,3 mM ditambahkan ke dalam masing-masing tabung reaksi yang berisi 2,5 mL larutan ekstrak n-Heksana dengan konsentrasi 10, 20, 40 dan 80 mg/L dan dihomogenkan. Dibiarkan selama 30 menit pada ruang gelap,kemudian diukur absorbansinya pada panjang gelombang maksimum 515 nm.
Perlakuan yang sama juga dilakukan terhadap variasi ekstrak padat metabol dan ekstrak pekat metanol fraksi etil asetat.
3.2.4. Uji Antibakteri Dengan Metode Difusi Agar 3.2.4.1. Pembuatan Media
a. Pembuatan media Nutrien Agar (NA)
Ditimbang sebanyak 20 g media NA kemudian disuspensikan ke dalam aquadest 1000 mL lalu dipanaskan sampai larut sempurna, kemudian dimasukkan masing-masing 10 mL media NA ke dalam 10 tabung reaksi untuk pembuatan media agar miring. Sterilkan media tersebut di dalam autoklaf pada suhu 121oC selama 15 menit.
b. Pembuatan media Nutrient Broth (NB)
Ditimbang sebanyak 13 g media NB dilarutkan ke dalam 100 mL aquadest. Dipipet masing-masing 10 mL ke dalam tabung reaksi. Sterilkan media tersebut di dalam autoklaf pada suhu 121oC selama 15 menit.
c. Pembuatan media Mueller Hilton Agar (MHA)
3.2.4.2. Pembuatan Inokulum Bakteri
Koloni bakteri E.coli dan S.aureus diambil dari bank mikrob menggunakan jarum ose kemudian disuspensikan ke dalam NB yang telah steril lalu di inkubasikan pada suhu 35±2oC selama 24 jam.
3.2.4.3. Pembuatan Kultur Bakteri
Inokulum bakteri diinokulasi pada permukaan media NA miring dengan jarum ose steril kemudian diinkubasi pada suhu 35±2 oC selama 24 jam.
3.2.4.4. Pembuatan Variasi ekstrak daun senduduk
Ekstrak n-Heksana
Sebanyak 2 g n-Heksana ditimbang kemudian dilarutkan ke dalam DMSO 4 mL kemudian diaduk hingga larut sehingga diperoleh konsentrasi 500mg/mL. Kemudian dibuat pengenceran dengan konsentrasi 400, 300, 200 dan 100 mg/mL. Perlakuan yang sama juga dilakukan terhadap ekstrak padat metanol dan ekstrak pekat metanol fraksi etil asetat.
3.2.4.5. Pengujian Aktifitas Antibakteri
3.3 Bagan Penelitian
3.3.1 Bagan Skrining Fitokimia Ekstrak Metanol Daun Senduduk
Ekstrak Metanol Daun Senduduk
Dimasukkan ke dalam tabung reaksi secukupnya Ditambah pereaksi untuk masing-masing uji
Ditambah
3.3.2 Pembuatan Ekstrak Metanol, Etil Asetat dan n-Heksana Daun Senduduk
500g Daun Senduduk
Diskrining fitokimia
Dimaserasi dengan metanol 4 L selama 24 jam
Disaring
Ampas Larutan Metanol
Dipekatkan dengan rotary evaporator
Ekstrak Pekat Metanol
Ditambah Etil Asetat Disaring
Larutan Etil Asetat Ekstrak Padat Metanol
Uji Antioksidan dan Antibakteri
Hasil Pengujian Dipekatkan
Ekstrak Pekat Etil Asetat
Dilarutkan dengan metanol Dipartisi dengan n-Heksana
larutan metanol dari fraksi etil asetat Larutan n-heksana
Dipekatkan
Ekstrak pekat metanol fraksi Etil asetat
Uji Antioksidan dan Antibakteri
Hasil Pengujian
Dipekatkan
Ekstrak pekat n-Heksana
Uji Antioksidan dan antibakteri
3.3.3 Uji Aktivitas Antioksidan Ekstrak Daun Senduduk Dengan Metode DPPH
3.3.3.1 Pembuatan larutan DPPH 0,3 mM
11,83 mg DPPH
Larutan DPPH 0,3 mM
Dimasukkan ke dalam labu takar 100 mL Ditambahkan etanol p.a hingga garis batas Dihomogenkan
Simpan di tempat yang gelap
3.3.3.2 Pembuatan variasi konsentrasi masing-masing ekstrak 0,025 g ekstrak pekat n-Heksana
Dimasukkan ke dalam labu takar 25 mL Ditambahkan etanol p.a hingga garis tanda Dihomogenkan
Larutan induk 1000 mg/L
Dipipet 5 mL larutan induk 1000 mg/L Dimasukkan ke dalam labu ukur 50 mL Ditambahkan etanol p.a hingga garis tanda Dihomogenkan
Larutan 100 mg/L
Dibuat variasi konsentrasi 10, 20, 40 dan 80 mg/L Dibuat pengenceran
3.3.3.4 Pengukuran nilai absorbansi blanko
1 mL larutan DPPH 0,3 mM
Hasil
Dimasukkan ke dalam tabung reaksi Ditambah 2,5 mL etanol p.a
Dihomogenkan
Dibiarkan selama 30 menit pada ruang gelap
Diukur absorbansi pada panjang gelombang 515 nm
3.3.3.5 Pengukuran nilai absorbansi sampel
1 mL larutan DPPH 0,3 mM
Hasil
Dimasukkan ke dalam tabung reaksi
Ditambah 2,5 mL ekstrak n-heksana konsentrasi 10 mg/L Dihomogenkan
Dibiarkan selama 30 menit pada ruang gelap
Diukur absorbansi pada panjang gelombang 515 nm
Catatan: Perlakuan yang sama juga dilakukan terhadap variasi konsentrasi 20; 40; dan 80 mg/L dari ekstrak n-heksana, ekstrak padat metanol dan ekstrak pekat metanol fraksi etil asetat.
3.3.4 Uji Aktivitas Antibakteri Ekstrak Daun Senduduk Dengan Metode Difusi Agar
3.3.4.1 Pembuatan Media
a. Pembuatan Media Nutrien Agar
20g media NA (Nutrien Agar)
Disuspensikan dengan 1000mL aquadest Dipanaskan sambil diaduk hingga mendidih
Disterilkan dengan autoklaf pada suhu 121 C selama 15 menit
b. Pembuatan Media Nutrien Broth
1,3 g media NB (Nutrien Broth)
Disuspensikan dengan 100 mL aquadest
Dipipet sebanyak 10 mL dan dimasukkan kedalam tabung Disterilkan dengan autoklaf pada suhu 121 C selama 15 menit
Media NB steril
c. Pembuatan Media MHA
19 g media MHA ( Mueller Hilton Agar)
Disuspensikan dengan 500 mL aquadest Dipanaskan sambil diaduk hingga mendidih
Disterilkan dengan autoklaf pada suhu 121 C selama 15 menit Media MHA steril
3.3.4.2 Pembuatan Inokulum Bakteri
10 mL Media NB steril
Dimasukkan bakteri secara aseptik dengan jarum ose Diinkubasi selama 24 jam pada suhu 35 C
Dibandingkan kekeruhan dengan standar Mcfarlan 510 nm
Inokulum Bakteri
3.3.4.3 Pembuatan Kultur Bakteri Inokulum Bakteri E.coli
Diambil dengan jarum ose steril inokulum bakteri Diinokulasi pada permukaan media NA miring Diinkubasi selama 24 jam pada suhu 35 C
Kultur Bakteri E. coli
3.3.4.4Pembuatan Variasi Konsentrasi dari Masing-Masing Ekstrak
2000 mg ekstrak pekat n-Heksana
Dilarutkan dengan 4 mL DMSO Dihomogenkan
Larutan 500 mg/mL
Dibuat variasi konsentrasi 400; 300; 200; dan 100 mg/mL
Dipipet 0,8 mL
3.3.4.5 Pengujian Aktivitas Antibakteri Media MHA pada cawan petri
Digoreskan kultur bakteri ke permukaan media MHA dengan menggunakan cutton steril
Dimasukkan kertas cakram yang telah direndam dengan variasi konsentrasi ekstrak n-Heksana
Diinkubasi selama 24 jam suhu 35 C
Diukur zona bening disekitar cakram dengan jangka sorong
Hasil
4.1 Hasil Penelitian 4.1.1 Skrining fitokimia
Ekstrak metanol dari daun senduduk yang diperoleh diuji skrining fitokimia untuk mengetahui adanya golongan senyawa alkaloid, flavonoid, tanin, saponin, terpenoid yang ditujukan pada tabel 4.1.
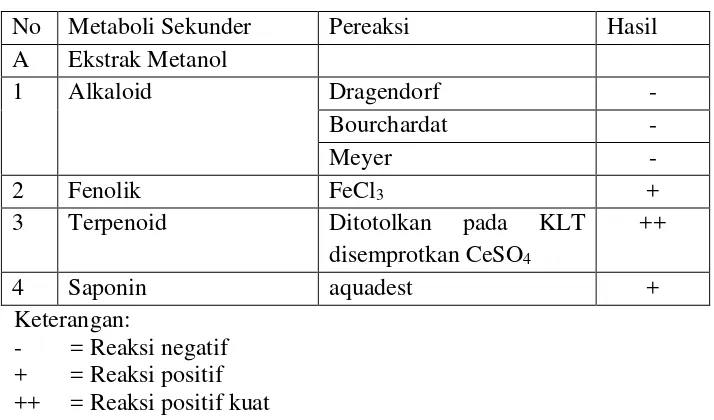
Tabel 4.1 Hasil Uji Skrining Fitokimia Daun Senduduk
No Metaboli Sekunder Pereaksi Hasil
A Ekstrak Metanol
1 Alkaloid Dragendorf -
Bourchardat -
Meyer -
2 Fenolik FeCl3 +
3 Terpenoid Ditotolkan pada KLT
disemprotkan CeSO4
++
4 Saponin aquadest +
Keterangan:
- = Reaksi negatif + = Reaksi positif ++ = Reaksi positif kuat
4.1.2 Hasil Uji Aktivitas Antioksidan
Tabel 4.2 Nilai % Peredaman dan Nilai IC50 dari masing-masing ekstrak
Konsentrasi (mg/L)
Nilai % Peredaman
Ekstrak Metanol Ekstrak Etil Asetat Ekstrak n-Heksana
0 0,0000 0,0000 0,0000
4.1.3 Hasil Uji Aktivitas Antibakteri
Pengujian aktivitas antibakteri pada ekstrak metanol, ekstrak metanol fraksi etil asetat dan ekstrak n-heksana daun senduduk dilakukan terhadap bakteri E. coli dan S. aureus dengan metoda difusi agar. Berikut hasil uji aktivitas antibakteri masing-masing ekstrak dengan konsentrasi tertentu.
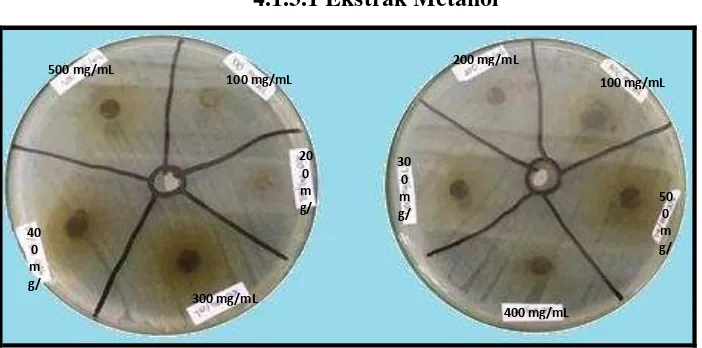
4.1.3.1 Ekstrak Metanol
Gambar 4.2 Zona Hambat Ekstrak Metanol Terhadap Bakteri S. aureus
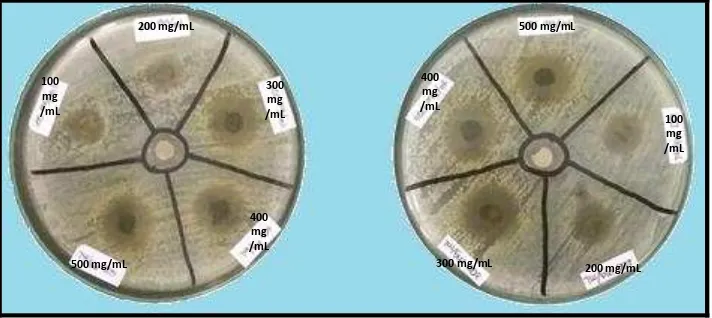
4.1.3.2 Ekstrak Pekat Metanol Fraksi Etil Asetat
Gambar 4.3 Zona Hambat Ekstrak Metanol Fraksi Etil Asetat Terhadap Bakteri E.coli
Gambar 4.4 Zona Hambat Ekstrak Metanol Fraksi Etil Asetat Terhadap Bakteri S. aureus
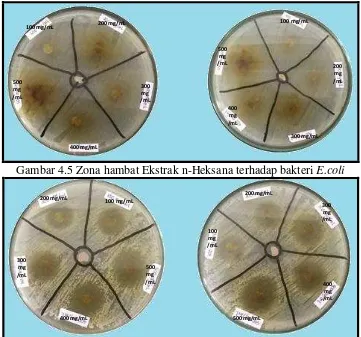
4.1.3.3 Ekstrak Pekat n-Heksana
Gambar 4.5 Zona hambat Ekstrak n-Heksana terhadap bakteri E.coli
Gambar 4.6 Zona Hambat Ekstrak n-heksana Terhadap Bakteri S. aureus Hasil penelitian uji antibakteri dengan mengukur zona hambat dari masing-masing konsentrasi. Hasil pengukuran diameter zona hambat dari uji aktivitas antibakteri dapat dilihat Table 4.3 sebagai berikut:
Tabel 4.3. Hasil Uji Aktivitas Antibakteri Ekstrak Metanol, Etil Asetat dan n-Heksana Daun Senduduk
No Konsentrasi (mg/mL)
Diameter zona hambat (mm) Ekstrak
E.coli S.aureus E.coli S.aureus E.coli S.aureus
1 100 - 8,80 - 9,75 - 12,95 4.2.1 Skrining Fitokimia
Uji fitokimia bertujuan untuk mengidentifikasi kandungan senyawa metabolit sekunder yang terdapat dalam sampel daun senduduk. Pada tabel 4.1 hasil skrining fitokimia metabolit sekunder yang terkandung dalam daun senduduk adalah flavonoid, fenolik, saponin, terpenoid dan steroid, sedangkan untuk alkaloid diperoleh hasil yang negatif karena sampel tidak mengalami perubahan warna yang sesuai dengan indikator.
Pengujian senyawa fenolik dilakukan dengan penambahan FeCl3 pada ekstrak metanol daun senduduk. Terjadi perubahan warna biru kehitaman yang terjadi pada saat penambahan FeCl3 yang menyatakan bahwa, daun senduduk mengandung senyawa fenolik. Perubahan warna biru kehitaman disebabkan karena terjadinya reaksi FeCl3 dengan gugus hidroksil yang ada pada senyawa fenolik.
Pada uji skrining fitokimia ekstrak daun senduduk, senyawa alkaloid
untuk uji Dragendorff, Mayer dan Bouchardat diperoleh hasil negatif, karena
tidak terbentuknya endapan pada tiap-tiap pereaksi yang ditambahkan.
Menurut Marliana (2005) terbentuknya endapan pada uji Meyer, Wagner ,
Dragendorff dan Bouchardat menandakan reaksi positif.
Pada pengujian terpenoid, hasil pada skrining fitokimia daun
senduduk menunjukkan hasil positif kuat dengan terjadinya perubahan
warna menjadi kecoklatan yang menunjukkan kandungan golongan
terpenoid. Analisis ini didasarkan pada kemampuan senyawa tersebut
membentuk warna dengan penambahan pereaksi CeSO4 1% dalam H2SO4
10%.
Hasil pengujian saponin pada ekstrak daun senduduk dengan
penambahan aquadest menunjukkan terbentuknya busa yang menyatakan
hasil positif. Menurut Robinson (1995) Saponin mengandung gugus
glikosida, timbulnya busa pada uji Forth menunjukkan adanya glikosida
yang mempunyai kemampuan membentuk buih dalam air yang terhidrolisis
4.2.2 Aktivitas Antioksidan
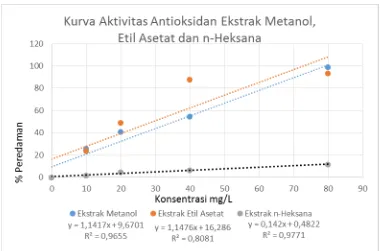
Berdasarkan Tabel 4.2, hubungan nilai konsentrasi dengan % peredaman dari ekstrak metanol, etil asetat dan n-heksana dapat dilihat pada Gambar 4.7 di bawah ini.
Gambar 4.7 Kurva Aktivitas Antioksidan Ekstrak Metanol, Etil Asetat dan n-Heksana
Pada Gambar 4.7, dibuat persamaan regresi linear antara konsentrasi mg/L sebagai sumbu x dengan nilai % peredaman sebagai sumbu y, sehingga dari persamaan regresi tersebut dapat ditentukan nilai IC50 dari masing-masing ekstrak. Pada persamaan regresi linear tersebut, dapat diketahui nilai slope ekstrak etil asetat dan ekstrak metanol adalah 1,1417 dan 1,1476 sehingga dapat dikatakan bahwa aktivitas antioksidan kedua ekstrak tersebut hampir sama dan lebih tinggi dari ekstrak n-heksana yang memiliki nilai slope 0,142.
Berdasarkan pada hasil pengujian aktivitas antioksidan dari ekstrak metanol, etil asetat dan n-heksana dengan metode DPPH, maka diperoleh nilai IC50 yang menunjukkan kekuatan aktivitas antioksidan dari masing-masing ekstrak. Hal tersebut dapat dilihat
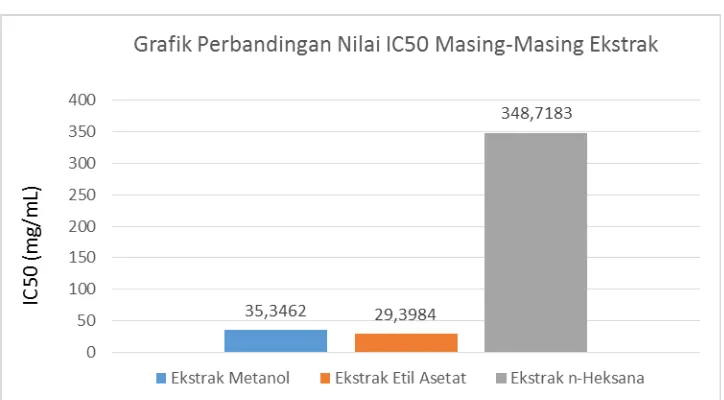
pada Gambar 4.8
Gambar 4.8 Grafik Perbandingan Nilai IC50 Masing-Masing Ekstrak Pada Gambar 4.8 diatas, aktivitas antioksidan ekstrak etil asetat lebih kuat dibanding ekstrak metanol dan ekstrak n-heksana. Kekuatan aktivitas antioksidan berbanding terbalik dengan nilai IC50 yaitu, semakin tinggi nilai IC50, maka semakin lemah aktivitas antioksidan pada ekstrak tersebut dan sebaliknya semakin rendah nilai IC50 maka semakin kuat aktivitas antioksidannya. Nilai IC50 merupakan kemampuan senyawa antioksidan menangkap 50% radikal bebas DPPH.
Hasil pengujian aktivitas antioksidan daun senduduk ekstrak metanol, etil asetat dan n-heksana dapat diklasifikasikan berdasarkan nilai IC50. Menurut Mulyani (2016), suatu senyawa dikatakan sebagai antioksidan sangat kuat jika nilai IC50 kurang dari 50 mg/L, 50-100 mg/L dinyatakan kuat dan 100-150 mg/L dinyatakan sedang dan 150-200 mg/L dinyatakan lemah. Klasifikasi hasil uji aktivitas antioksidan dari masing-masing ekstrak dapat dilihat pada Tabel 4.4.
Tabel 4.4 Klasifikasi Nilai IC50 Ekstrak Daun Senduduk Sampel Uji IC50 (mg/L) Klasifikasi
Ekstrak Metanol Sangat Kuat
Berdasarkan pada Tabel 4.4. tersebut, ekstrak metanol dan etil asetat dari daun senduduk dapat dikatakan sebagai antioksidan yang sangat kuat karena memiliki IC50 < 50 mg/L, sedangkan untuk ekstrak n-heksana dikatakan sebagai antioksidan sangat lemah karena memiliki nilai IC50 > 50 mg/L. Perbedaan aktivitas antioksidan ini dipengaruhi dari sifat pelarut yang digunakan.
Pada penelitian ini pelarut yang digunakan adalah metanol, etil asetat, dan n-heksana. Tujuan penggunaan tiga pelarut dengan polaritas yang berbeda adalah untuk mendapatkan senyawa aktif dari daun senduduk berdasarkan tingkat kepolarannya. Ekstraksi menggunakan pelarut dengan kepolaran yang berbeda akan menghasilkan komponen senyawa yang berbeda sehingga sifat antioksidan dan antibakteri yang dimiliki oleh setiap senyawa yang diperoleh dari ekstraksi tersebut juga berbeda (Pambayun et al., 2007). Ekstrak Etil asetat memiliki nilai IC50 lebih kecil karena etil asetat mampu mengekstraksi senyawa fenolik pada daun senduduk. Menurut Rahmat (2009) melaporkan bahwa pelarut etil asetat sangat cocok untuk mengekstraksi senyawa fenolik. Kebanyakan senyawa fenolik biasanya bersifat antioksidan, oleh karena itu pengukuran total fenolik dapat digunakan untuk memperkirakan aktifitas antioksidan suatu bahan.
Menurut Huang et al., (2005) aktivitas antioksidan berbanding lurus dengan total fenol, semakin tinggi kandungan fenol dalam suatu bahan semakin tinggi pula aktivitasnya sebagai antioksidan, Hal ini sesuai dengan hasil yang diperoleh dimana ekstrak etil asetat dan ekstrak metanol memiliki kandungan total fenolik yang lebih tinggi dibandingkan dengan ekstrak n-heksana.
4.2.3 Aktivitas Antibakteri
masing-masing ekstrak tersebut hanya efektif untuk bakteri S. aureus yang merupakan bakteri gram positif. Hal ini disebabkan tidak adanya komponen aktif yang mampu menghambat pertumbuhan bakteri E.coli dari masing-masing ekstrak tersebut, sehingga dapat dinyatakan bahwa ekstrak metanol, etil asetat dan n-heksana daun senduduk tidak efektif terhadap bakteri E. coli.
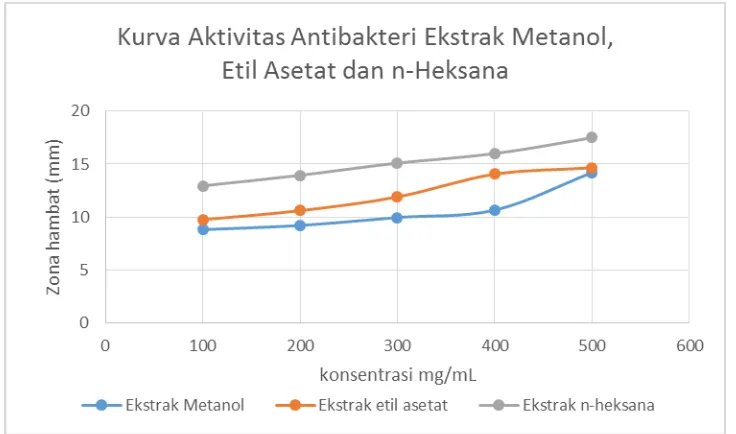
Berdasarkan hasil uji aktivitas antibakteri ekstrak metanol, etil asetat dan n-heksana dapat dibuat kurva hubungan konsentrasi (mg/mL) dengan diameter zona hambat (mm) terhadap bakteri S. aureus.
Gambar 4.9 Kurva Aktivitas Antibakteri Ekstrak Metanol, Etil Asetat dan n-Heksana Daun Senduduk Terhadap Bakteri S. aureus.
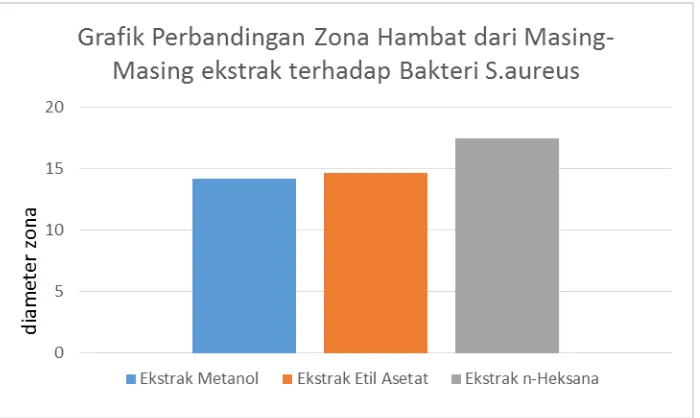
Gambar 4.10 Grafik Perbandingan Zona Hambat dari Masing-Masing Ekstrak Terhadap Bakteri S.Aureus
Berdasarkan Gambar 4.10 hasil pengujian dengan konsentrasi 500mg/mL diameter zona hambat terhadap bakteri S.aureus, ekstrak n-heksana memiliki rata-rata diameter zona hambat yang paling besar bila dibandingkan dengan ekstrak etil asetat dan ekstrak metanol. Ekstrak n-heksana, etil asetat dan metanol memiliki nilai 17,50 mm ;14,65 mm dan 14,20 mm. Hal ini menunjukkan bahwa ekstrak n-heksana mengandung komponen yang paling aktif bila dibandingkan dengan kedua ekstrak lainnya terhadap bakteri S.aureus. Namun, berdasarkan hasil diameter zona hambat ekstrak n-heksana, etil asetat dan metanol dapat dikategorikan efektif dengan nilai antara 13 sampai dengan 17 mm.
Menurut Clinical and laboratory Standars Institute (2012) menyatakan bahwa standar batas zona hambat antibiotik Cloramphenicol
yaitu diameter zona hambat ≥ 18 memiliki zona hambat sensitif atau
sangat efektif, antara 13 sampai dengan 17 mm memiliki zona hambat
intermediet atau efektif dan ≤ 12 mm memiliki zona hambat resisten atau
kurang efektif.
bahan tersebut. Metabolit sekunder yang terkandung di dalam masing-masing ekstrak memiliki efektifitas yang berbeda dalam menghambat pertumbuhan bakteri. Hal ini menyebabkan terjadinya perbedaan aktivitas antibakteri dari masing-masing ekstrak.
Hasil penelitian menyatakan bahwa komponen yang terkandung di dalam ekstrak n-heksana yang merupakan pelarut non polar memiliki aktivitas antibakteri yang lebih efektif terhadap S.aureus. Menurut Marjorie (1999) pelarut yang digunakan untuk ekstrak komponen aktif dalam sampel akan melarutkan komponen aktif sesuai sifat dan karakteristik pelarut. Untuk pelarut non polar seperti Chloroform umumnya akan menarik komponen terpenoid dan flavonoid.
Ekstrak pelarut organik daun senduduk mengandung campuran metabolit sekunder termasuk fenolik, saponin dan terpenoid/steroid. Menurut Paiva (2010) molekul-molekul tersebut berhubungan dengan sifat pertahanan dari tanaman tersebut, seperti perlindungan terhadap cekaman biotik dan abiotik dan pemeliharaan struktur dari tanaman. Pelarut polar seperti asam organik, semipolar, dan non polar digunakan untuk mengekstrak kandungan metabolit sekunder pada tanaman yang memiliki perbedaan dalam struktur polaritas. Ekstrak dari bahan tanaman yang sama dengan pelarut yang memiliki karakteristik berbeda memiliki sifat biologis yang berbeda.
Uji aktivitas antibakteri dapat dilakukan dengan metode difusi dan metode pengenceran. Disc diffusion test atau uji difusi disk dilakukan dengan mengukur diameter zona bening (clear zone) yang merupakan petunjuk adanya respon penghambatan pertumbuhan bakteri oleh suatu senyawa antibakteri dalam ekstrak. Syarat jumlah bakteri untuk uji kepekaan/sensitivitas yaitu 105-108 CFU/mL (Hermawan dkk, 2007).
5.1 Kesimpulan
1. Berdasarkan uji skrining fitokimia, daun senduduk mengandung senyawa flavonoid, terpenoid, tanin dan saponin.
2. Aktivitas antioksidan daun senduduk ekstrak pekat metanol fraksi etil asetat (IC50= 29,3984mg/L ) lebih tinggi dibandingkan dengan ektrak padat metanol (IC50=35,3462mg/L), dan ekstrak pekat n-heksana (IC50=348,7183mg/L).
3. Hasil uji aktivitas antibakteri menunjukkan bahwa ekstrak n-heksana, ekstrak pekat metanol fraksi etil asetat dan ekstrak padat metanol memberikan diameter zona hambat yang efektif terhadap bakteri S.aureus dengan diameter masing-masing 17,50 mm; 14,65 mm dan 14,20 mm pada konsentrasi 500mg/L , dan tidak efektif terhadap bakteri E.coli. Ekstrak n-heksana memiliki aktivitas antibakteri paling tinggi dibanding ekstrak padat metanol dan ekstrak pekat metanol fraksi etil asetat.
5.2 Saran