ANTAGONISME BAKTERI Pseudomonad fluorescens TERHADAP JAMUR PATOGEN Fusarium oxysporum f. sp. melonis DI RIZOSFER
PERKECAMBAHAN MELON
SKRIPSI
Diajukan untuk Memenuhi Sebagian Persyaratan
dalam Memperoleh Gelar Sarjana Pertanian
Program Studi Agroteknologi
Oleh :
Novita Galuh Rachmawati NPM: 1025010015
Kepada
FAKULTAS PERTANIAN
UNIVERSITAS PEMBANGUNAN NASIONAL “VETERAN” JAWA TIMUR
SURABAYA
ANTAGONISME BAKTERI Pseudomonad fluorescens TERHADAP JAMUR PATOGEN Fusarium oxysporum f. sp. melonis DI RIZOSFER
PERKECAMBAHAN MELON
Diajukan oleh :
Novita Galuh Rachmawati NPM: 1025010015
Telah dipertahankan di hadapan dan diterima oleh Tim Penguji Skripsi Program Studi : Agroteknologi. Fakultas Pertanian
Universitas Pembangunan Nasional “Veteran” Jawa Timur Pada tanggal 30 April 2014
Telah disetujui oleh :
Pembimbing : Tim Penguji :
1. Pembimbing Utama 1. Ketua
Dr. Ir. Penta Suryaminarsih, MP. Dr. Ir. Penta Suryaminarsih, MP.
2. Pembimbing Pendamping 2. Sekretaris
ANTAGONISM BACTERIA OF Pseudomonad fluorescens TO INHIBITING PATHOGENIC FUNGAL Fusarium oxysporum f . sp . melonis IN RHIZOSPHERE
OF MELON GERMINATION
Novita Galuh
Faculty of Agriculture UPN “Veteran” East Java, Surabaya
ABSTRACT
The aim of research was to prove antagonism bacteria of Pseudomonad fluorescens to inhibiting pathogenic fungal Fusarium oxysporum f. sp. melonis to result in defective. Research activities is undertaken in melon agricultural field in Technical Implementation Unit Agribusiness and Horticulture, Lebo, Sidoarjo; Karang Sinom Village, Indramayu; and Plant Protection Laboratory of Agriculture UPN "Veteran" East Java. This research carried out during October 2013 until February 2014. Method is arranged in a Randomized Completely Design with 3 treatments and 4 replications for antagonistic experiment bacteria of Pseudomonad fluorescens
to inhibiting pathogenic Fusarium oxysporum f. sp. melonis, colonization pattern and biological agents in rhizosphere of melon germination using descriptive and destructive methods. In antibiosis experiment bacteria of Pseudomonad fluorescens
from rhizosphere of melon germination to pathogenic Fusarium oxysporum f. sp.
melonis is used a Randomized Completely Design with 4 treatments and 4 replications. Isolation and screening method of bacteria of Pseudomonad fluorescens have been found 9 isolate and 3 isolate is Pseudomonad fluorescens
such as PfN2, PfN5 and PfN7. Antagonistic biological agents experiment to pathogenic fungal showed that PfN7 is the most effective inhibitor with inhibiting percentage 21.88 %, this isolate is used for the next experiment. The result of experiment with colonization pattern and biological agents in rhizosphere of melon germination show that biological agents were effective colonize in rhizosphere of melon germination. Result of statistic analyst showed that antibiosis of antagonist bacteria of Pseudomonad fluorescens from rhizosphere of melon germination have a significant influence for reducing pathogenic fungal Fusarium oxysporum f. sp.
melonis with inhibition zone, 2nd days after inoculating has inhibiting percentage 6.25 %, and 4th days after inoculating has significant inhibiting percentage 8.81 %. In 6th days after inoculating has inhibiting percentage 11.88 %, and the most inhibiting percentage is showed in 8th days after inoculating e.g. 18.88 %.
ANTAGONISME BAKTERI Pseudomonad fluorescens TERHADAP JAMUR PATOGEN Fusarium oxysporum f. sp. Melonis DI RIZOSFER
PERKECAMBAHAN MELON
Novita Galuh
Fakultas Pertanian UPN “Veteran” Jawa Timur, Surabaya ABSTRAK
Penelitian ini bertujuan untuk mengetahui antagonisme bakteri
Pseudomonad fluorescens terhadap Fusarium oxysporum f. sp. melonis yang dapat menyebabkan kerusakan cukup serius. Kegiatan penelitian dilaksanakan di lahan melon UPT Pengembangan Agribisnis dan Tanaman Hortikultura Lebo, Sidoarjo; Desa Karang Sinom, Indramayu; dan Laboratorium Kesehatan Tanaman Fakultas Pertanian, Universitas Pembangunan Nasional “Veteran” Jawa Timur. Penelitian dilakukan pada Oktober 2013 sampai dengan Februari 2014. Metode yang digunakan rancangan acak lengkap (RAL) dengan 3 perlakuan dan 4 ulangan pada
uji antagonistik bakteri Pseudomonad fluorescens terhadap patogen
Fusarium oxysporum f. sp. melonis, serta dalam pola kolonisasi agensia hayati dan patogen di rizosfer perkecambahan melon menggunakan metode diskriptif dan destruktif. Pada uji antibiosis bakteri Pseudomonad fluorescens dari rizosfer perkecambahan melon terhadap patogen Fusarium oxysporum f. sp. melonis
menggunakan rancangan acak lengkap (RAL) dengan 4 perlakuan dan 4 ulangan.
Penelitian dilakukan dengan cara isolasi dan screening bakteri
Pseudomonad fluorescens dimana didapatkan 9 isolat, 3 diantaranya merupakan bakteri Pseudomonad fluorescens yaitu isolat PfN2, PfN5, dan PfN7. Pada uji antagonistik agensia hayati terhadap patogen menunjukkan bahwa isolat PfN7 merupakan isolat yang mempunyai persentase daya hambat tertinggi sebesar 21.88 %, isolat tersebut dipergunakan dalam penelitian selanjutnya. Hasil penelitian perlakuan pola kolonisasi agensia hayati dan patogen di rizosfer perkecambahan melon menunjukkan bahwa bakteri agensia hayati dan patogen dapat mengkolonisasi rizosfer perkecambahan melon. Hasil analisis statistik menunjukkan bahwa antibiosis bakteri antagonis Pseudomonad fluorescens dari rizosfer perkecambahan melon memberikan pengaruh yang sangat berbeda nyata terhadap perkembangan jamur patogen Fusarium oxysporum f. sp. melonis dengan terbentuknya zona hambat, dimana pada perlakuan 2 HSI diperoleh daya hambat sebesar 6.25 %, dilanjutkan dengan perlakuan 4 HSI meunjukkan daya hambat yang cukup signifikan yaitu sebesar 8.81 %, kemudian diikuti oleh perlakuan 6 HSI sebesar 11.88 % dan daya hambat optimal ditunjukkan pada perlakuan 8 HSI sebesar 18.88 %.
KATA PENGANTAR
Puji syukur saya panjatkan kehadirat Allah SWT yang telah memberikan
rahmat serta karunia-Nya kepada saya sehingga saya berhasil menyelesaikan Hasil
Skripsi Penelitian ini yang berjudul “Antagonisme Bakteri Pseudomonad fluorescens
Terhadap Jamur Patogen Fusarium oxysporum f. sp. melonis Di Rizosfer
Perkecambahan Melon”.
Hasil skripsi penelitian ini dapat diselesaikan atas bantuan dan kerjasama
berbagai pihak. Oleh karena itu saya mengucapkan terima kasih kepada :
1. Orang tua yang telah mendukung dan mendoakan dalam menempuh
pendidikan semenjak awal.
2. Dr. Ir. Sukendah, MSc selaku Dekan Fakultas Pertanian dan Ir. Mulyadi, MS
selaku Ketua Program Studi Agroteknologi Fakultas Pertanian UPN “Veteran”
Jawa Timur.
3. Dr. Ir. Penta Suryaminarsih, MP selaku Dosen Pembimbing Utama dan
Ir. Wiwik Sri Harijani, MP selaku Dosen Pembimbing Pendamping.
4. Para Dosen dan staf kepegawaian Fakultas Pertanian yang telah
memfasilitasi dalam pembelajaran untuk bekal penelitian.
5. Rekan Mahasiswa Agroteknologi angkatan 2010-2011 yang telah
mendukung dan membantu selama ini.
Semoga Hasil Skripsi Penelitian ini dapat bermanfaat sebagai acuan dalam
melaksanakan penelitian.
Surabaya, 30 April 2014
DAFTAR ISI
DAFTAR TABEL……….... vi
DAFTAR GAMBAR………... vii
DAFTAR LAMPIRAN……… viii
I. PENDAHULUAN………... 1
1.1 Latar Belakang………... 1
1.2 Rumusan Masalah………. 3
1.3 Tujuan……….. 3
1.4 Manfaat……… 4
II. TINJAUAN PUSTAKA………. 5
2.1 Pengendalian Secara Hayati……… 5
2.2 Bakteri Pseudomonas sp……….. 7
2.3 Penyakit Layu Fusarium………... 10
2.3.1 Daur hidup penyebab penyakit………. 11
2.3.2 Gejala serangan……….. 12
2.4 Rizosfer………... 12
2.5 Hipotesis……….. 13
III. BAHAN DAN METODE PENELITIAN……….. 14
3.1 Tempat dan Waktu………. 14
3.2 Alat dan Bahan……… 14
3.2.1 Alat-alat……….... 14
3.2.2 Bahan-bahan……… 14
3.3 Metode Penelitian……… 15
3.3.2 Penelitian tahap II……… 16
3.4 Pelaksanaan……… 17
3.4.1 Penelitian tahap I………. 17
3.4.2 Penelitian tahap II……… 21
3.5 Pengamatan……….... 23
3.5.1 Persentase daya hambat……… 23
3.5.2 Pola kolonisasi akar……… 24
3.6 Analisis Data………... 25
IV. HASIL DAN PEMBAHASAN……….. 26
4.1 Isolasi dan Screening Bakteri Pseudomonad fluorescens………... 26
4.2 Isolasi Jamur Fusarium sp……….... 29
4.3 Uji Antagonistik Bakteri Pseudomonad fluorescens terhadap Fusarium oxysporum f. sp. melonis (FOM) secara In Vitro………. 30
4.4 Pola Kolonisasi Agensia Hayati dan Patogen di Rizosfer Perkecambahan Melon……….. 33
4.5 Uji Antibiosis Bakteri Pseudomonad fluorescens dari Rizosfer Perkecambahan terhadap Fusarium oxysporum f. sp. melonis secara In Vitro………. 37
V. KESIMPULAN DAN SARAN……….. 42
5.1 Kesimpulan……….. 42
5.2 Saran……… 42
DAFTAR PUSTAKA……….. 43
DAFTAR TABEL
Nomor Judul Halaman
1. Karakteristik koloni bakteri……….. 26
2. Zona hambat uji antagonistik... 30
3. Zona hambat uji antibiosis………... 38
DAFTAR GAMBAR
Nomor Judul Halaman
1. Denah percobaan pada uji antagonistik……… 15
2. Denah percobaan pada uji antibiosis………. 17
3. Cara pengukuran koloni Fusarium oxysporum untuk menghitung persentase daya hambat antibiosis………... 24
4. Uji Gram dengan KOH 3 %... 27
5. Uji Fluoresensi………... 28
6. Uji potato soft root………. 28
7. Koloni Fusarium sp……… 29
8. Uji Antagonistik Bakteri Pseudomonad fluorescens terhadap Fusarium oxysporum f. sp. melonis………... 31
9. Rata-rata persentase daya hambat antagonistik………... 32
10. Pola Kolonisasi 1 HSI………..…………. 34
11. Pola Kolonisasi 3 HSI……… 35
12. Pola Kolonisasi 5 HSI……… 37
DAFTAR LAMPIRAN
Nomor Judul Halaman
1. Jadwal Kegiatan……….……… 47
2. Komposisi Bahan Media………..………. 48
3. Gambar Alat dan Bahan Penelitian... 49
4. Perhitungan Analisis Varian Zona Hambat Uji Antagonistik…... 50
5. Perhitungan Analisis Varian Daya Hambat Uji Antagonistik.…..…………. 52
6. Perhitungan Analisis Varian Zona Hambat Uji Antibiosis..……… 54
I. PENDAHULUAN
1.1 Latar Belakang
Penyakit layu fusarium pada melon yang disebabkan oleh patogen
Fusarium oxysporum f. sp. melonis merupakan salah satu penyakit utama pada
tanaman melon yang menyebabkan kerusakan cukup serius (Semangun, 2004).
Fusarium oxysporum merupakan patogen tular tanah yang memiliki kisaran inang
yang luas, serta mempunyai kemampuan bertahan yang lama dalam tanah maupun
pada bagian tanaman yang telah mati, sehingga serangan Fusarium oxysporum sulit
untuk dikendalikan (Agrios, 1978).
Pengendalian serangan Fusarium oxysporum menggunakan fungisida dapat
menimbulkan masalah pencemaran lingkungan, gangguan keseimbangan ekologis
dan residu yang bersifat racun, disamping itu perlakuan fungisida membutuhkan
biaya yang besar karena dilakukan secara berulang dan dapat merangsang
timbulnya patogen baru yang lebih resisten terhadap fungisida serta matinya
mikroorganisme yang berguna bagi tanah (Rahaju, 2007).
Salah satu cara alternatif yang dapat dilakukan ialah melakukan
pengendalian secara hayati. Mikroorganisme pengendali penyakit tanaman yang
hidup pada daerah rizosfer sangat sesuai digunakan sebagai agensia hayati karena
rizosfer merupakan daerah akar tumbuhan yang terbuka terhadap serangan patogen
(Hasanudin, 2003). Bakteri Pseudomonad fluorescens merupakan salah satu
agensia hayati yang dapat ditemukan di daerah perakaran tumbuhan (rizosfer) dan
kebanyakan tidak dapat tumbuh dalam kondisi masam (pH 4,5) (Bradbury, 1986
Pseudomonad fluorescens mempunyai kemampuan menekan populasi
patogen dengan melindungi akar dari infeksi patogen tanah dengan cara
mengkolonisasi permukaan akar, menghasilkan senyawa kimia anti jamur, antibiotik,
siderofor dan kompetisi dengan patogen dalam penyerapan kation Fe (Supriadi,
2006). Siderofor berfungsi mengikat ion Fe3+ dari lingkungan sehingga patogen tidak
dapat memanfaatkan senyawa tersebut dan mengakibatkan pertumbuhan jamur
terhambat (Leong, 1988 dalam Hamdan, 1991). Menurut Mulyan (1997) kecepatan
kolonisasi akar oleh bakteri antagonis merupakan salah satu aspek penting dalam
menentukan aktifitas melindungi daerah perakaran.
Agensia hayati umumnya lebih efektif bila diaplikasikan sebagai perlakuan
preventif sebelum penyakit berkembang dan aplikasi lanjutan perlu dilakukan untuk
memperoleh penekanan penyakit yang dapat bertahan lama (Utkhede, 2005).
Namun keefektifan agensia hayati dapat dipengaruhi oleh faktor lingkungan, baik
biotik maupun abiotik (Someya, 2005).
Terminologi antibiosis identik dengan pengertian antibiotik yaitu senyawa
organik yang diproduksi oleh mikroorganisme yang dalam konsentrasi rendah dapat
mengganggu pertumbuhan dan aktivitas metabolisme mikroorganisme lain.
Antibiosis dalam pengendalian hayati merupakan mikroba yang mampu
menghamabat pertumbuhan mikroba lain dengan antibiotik yang diproduksinya
(Cook, 2002). Menurut Syamsuni (2006) khasiat antibiosis dapat dipisahkan
(diekstrak) agar lebih mudah dipergunakan dan disimpan. Dyah (2005), melaporkan
bahwa Pseudomonas fluorescens mampu menekan pernyakit layu yang disebabkan
Berdasarkan hasil-hasil penelitian yang telah ada maka perlu dilakukan
penelitian tentang antagonisme bakteri Pseudomonad fluorescens terhadap
Fusarium oxysporum f. sp. melonis di rizosfer perkecambahan melon.
1.2 Rumusan Masalah
(1) Apakah isolasi dan screening pada lahan melon di Unit Pelaksana Teknis
(UPT) Pengembangan Agribisnis dan Tanaman Hortikultura Lebo, Sidoarjo
akan menemukan bakteri Pseudomonad fluorescens yang mampu
menghambat patogen Fusarium oxysporum f. sp. melonis ?
(2) Apakah bakteri Pseudomonad fluorescens yang ditemukan, mampu
berkompetisi dengan patogen Fusarium oxysporum f. sp. melonis di rizosfer
perkecambahan melon ?
(3) Apakah bakteri Pseudomonad fluorescens di rizosfer perkecambahan melon
menghasilkan antibiosis ?
1.3 Tujuan
(1) Mendapatkan bakteri Pseudomonad fluorescens pada lahan melon di UPT
Pengembangan Agribisnis dan Tanaman Hortikultura Lebo, Sidoarjo yang
mampu menghambat patogen Fusarium oxysporum f. sp. melonis.
(2) Mengetahui pola kolonisasi bakteri Pseudomonad fluorescens dengan
patogen Fusarium oxysporum f. sp. melonis di akar perkecambahan melon.
(3) Mengetahui adanya kemampuan antibiosis pada Pseudomonad fluorescens
dalam menghambat Fusarium oxysporum f. sp. melonis di rizosfer
1.4 Manfaat
(1) Memperkaya ilmu pengetahuan, khususnya pengendalian hayati yang
berkaitan dengan antogonisme bakteri Pseudomonad fluorescens terhadap
Fusarium oxysporum f. sp. melonis.
(2) Memberikan informasi mengenai alternatif pengendalian hayati terhadap
Fusarium oxysporum f. sp. melonis penyebab penyakit layu pada melon
II. TINJAUAN PUSTAKA
2.1 Pengendalian Secara Hayati
Baker dan Cook (2002) mendefinisikan bahwa pengendalian hayati adalah
pengurangan jumlah inokulum atau penurunan aktivitas dari patogen penyebab
penyakit dengan introduksi agens antagonis, perbaikan kondisi lingkungan tumbuh
atau dengan modifikasi lingkungan yang dapat mendukung perkembangan agens
antagonis. Menurut Cook (2002) beberapa interaksi dalam pengendalian hayati
adalah sebagai berikut :
a. Antagonisme merupakan bentuk hubungan antara dua organisme, dimana
organisme yang satu merugikan organisme lainnya.
b. Antibiosis adalah mikroba yang mampu menghambat pertumbuhan mikroba
lain dengan antibiotik yang diproduksinya.
c. Antibiotik adalah senyawa organik yang diproduksi oleh organisme yang
mempunyai kemampuan baik menghambat pertumbuhan organisme lain.
d. Kompetisi adalah adanya persaingan antara organisme satu dengan yang
lain untuk memperebutkan ruang dan makanan, dimana salah satu
organisme mengalami penurunan pertumbuhan.
Pengendalian hayati (biological control) terhadap patogen yaitu
menghancurkan sebagian atau seluruh populasi patogen dengan organisme lain dan
selalu terjadi secara rutin di alam (Agrios, 1996). Beberapa jenis penyakit yang
patogennya tidak dapat berkembang pada lahan tertentu yang disebut tanah
supresif (suppressive soil). Pada dasarnya manusia telah melakukan pengendalian
hayati sejak manusia mengenal budidaya pertanian dan munculnya Organisme
bahwa pengendalian hayati yang dilakukan saat itu hanya bersifat percobaan
berdasarkan pengalaman, dengan pendekatan ilmiah yang terbatas.
Penggunaan organisme hidup sebagai agens antagonis dalam
mengendalikan organisme pengganggu tanaman (OPT) mulai dilakukan dengan
pendekatan ilmiah yang lebih jauh dan perkembangannya tampak semakin pesat.
Agens antagonis dapat berupa mikroorganisme yang dapat mempengaruhi
kemampuan bertahan atau berpengaruh negatif terhadap aktivitas patogen dalam
menimbulkan penyakit (Agrios, 1997).
Selain jamur dan bakteri dari genus Streptomyces dan Pseudomons, ada
pula agensia hayati yang telah diteliti untuk menghambat patogen yaitu Nematoda
mikofagus Aphelencus anenae memarasit Rhizoctonia dan Fusarium, dan amuba
Vampyrella memarasit cendawan patogenik Cochiliobolus sativus dan
Gaeumannomyces graminis. Belum seluruhnya dapat dijelaskan cara
mikroorganisme antagonis dapat mempengaruhi populasi patogen, tetapi menurut
Agrios (1996), umumnya mekanisme tersebut dihubungkan dengan salah satu dari
lima pengaruh berikut, yaitu:
a. Parasitisme dan membunuh patogen secara langsung,
b. Berkompetisi dengan patogen dalam hal nutrisi atau makanan,
c. Toksin yang langsung mempengaruhi patogen dengan zat antibiotik yang
dilepaskan oleh agens antagonis,
d. Toksin yang tidak langsung mempengaruhi patogen melalui zat yang
mudah menguap seperti etilen yang dilepaskan oleh aktivitas metabolik
antagonis,
2.2 Bakteri Pseudomonas sp.
Pseudomonas merupakan salah satu genus dari Famili Pseudomonadaceae.
Bakteri ini berbentuk batang lurus atau lengkung, ukuran tiap sel bakteri 0.5 - 0.11
µm x 1.5 - 4.0 µm, tidak membentuk spora dan bereaksi negatif terhadap pewarnaan
Gram, aerob, menggunakan H2 atau karbon sebagai energinya, kebanyakan tidak
dapat tumbuh dalam kondisi masam (pH 4,5) (Holt, 1994). Menurut Holt (1994),
klasifikasi bakteri Pseudomonas adalah sebagai berikut :
Kingdom : Bacteria
Phylum : Proteobacteria
Class : Gamma Proteobacteria
Order : Pseudomonadales
Family : Pseudomonadaceae
Genus : Pseudomonas
Pseudomonad fluorescens termasuk kedalam bakteri yang dapat ditemukan
dimana saja (ubiquitous), seringkali ditemukan pada bagian tanaman (permukaan
daun dan akar) dan sisa tanaman yang membusuk, tanah dan air (Bradbury, 1986
dalam Supriadi. 2006). Ciri yang mencolok dan mudah dilihat dari bakteri
Pseudomonad fluorescens adalah kemampuannya menghasilkan pigmen pyoverdin
dan atau fenazin pada medium King’s B sehingga terlihat berpijar bila terkena sinar
Ultra Violet (UV). Pseudomonad fluorescens telah dimanfaatkan sebagai agensia
hayati untuk beberapa jamur dan bakteri patogen tanaman.
Kemampuan bakteri Pseudomonad fluorescens dalam menekan populasi
patogen diasosiasikan dengan kemampuan untuk melindungi akar dari infeksi
patogen tanah dengan cara mengkolonisasi permukaan akar, menghasilkan
kation Fe (Supriadi, 2006). Beberapa hasil penelitian menyatakan bahwa
Pseudomonas fluorescens dapat mengendalikan : penyakit layu fusarium pada
tanaman pisang (Djatnika, 2003); penyakit virus kuning pada tanaman cabai
(Yulmira, 2009); penyakit layu bakteri (Ralstonia solanacearum) pada tanaman
kacang tanah (Suryadi, 2009).
Pseudomonad fluorescens yang hidup didaerah perakaran tanaman dapat
berperan sebagai jasad renik pelarut fosfat, mengikat nitrogen dan menghasilkan zat
pengatur tumbuh (ZPT) bagi tanaman (Fravel, 1988) sehingga dengan kemampuan
tersebut, Pseudomonas fluorescens dapat dimanfaatkan sebagai pupuk biologis
yang dapat menyediakan hara untuk pertumbuhan tanaman.
Pseudomonad fluorescens juga berperan sebagai pemacu pertumbuhan atau
Planth Growth Promoting Rhizobacteria (PGPR) karena menghasilkan ZPT dan
meningkatkan ketersediaan hara melalui produksi asam organik (Linderman dan
Paulizt, 1985 dalam Yulmira, 2009).
Pseudomonad fluorescens merupakan bakteri gram negatif yang sebagian
besar bersifat non-patogenik dan saprofitik pada tanah dan daerah rizosfer tanaman.
Pseudomonad fluorescens mengkolonisasi tanah, permukaan tanaman dan
memanfaatkan bahan organik sebagai sumber nutrisi untuk pertumbuhannya.
Bakteri ini memproduksi pigmen biru kehijauan pada saat kandungan Fe (besi) yang
rendah serta dapat tumbuh baik pada media yang mengandung garam-garam
mineral dengan tambahan sumber karbon yang beragam (Ratdiana, 2007).
Pseudomonad fluorescens merupakan agens antagonis yang potensial
dengan menghasilkan antibiotik dan siderofor. Siderofor berfungsi mengikat ion Fe3+
dari lingkungan sehingga patogen tidak dapat memanfaatkan senyawa tersebut dan
Antibotik tersebut berperan dalam menekan perkembangan patogen yang ada di
lingkungan pertanaman sehingga Pseudomonad fluorescens dapat berkembang
secara optimal (Mazolla, Cook, Thomashow, Weller, dan Pierson, 1992). Selain itu,
antibiotik yang dihasilkan oleh Pseudomonad fluorescens dapat mempengaruhi
populasi dari bakteri kelompok Pseudomonas lainnya (Natsch, 1997).
Duffy dan Defago (1998) melaporkan senyawa antibiotik yang dihasilkan
bakteri ini antara lain pyrrolnitrin, pyoluteorin (PLT), phenazine-1-carboxylase (PCA)
dan 2,4-diacetylploroglucinol (PHL). Hamdan (1991) menyatakan bahwa antibiotik
PCA menjadi faktor utama dalam menekan kejadian penyakit pada tanaman,
sedangkan, siderofor yang dihasilkan antara lain ptochelin dan pyovedrin. Keduanya
merupakan pigmen berwarna kuning kehijauan, tetapi pigmen yang dihasilkan oleh
pyovedrin lebih cerah daripada ptochelin.
Pseudomonad fluorescens banyak dilaporkan sebagai penghasil fitohormon
dalam jumlah yang besar khususnya Indole Acetic Acid (IAA) untuk merangsang
pertumbuhan (Watanabe, 1987 dalam Marwoso, 2005). Indole Acetic Acid
merupakan hormon pertumbuhan kelompok auksin yang sangat besar peranannya
dalam pertumbuhan tanaman (Heddy, 1986 dalam Marwoso, 2005). Dilaporkan oleh
Tjondronegoro, Natasaputra, Gumawan, Djaelani, Suwanto (1989), bahwa pengaruh
auksin antara lain memanjangkan dan membesarkan sel batang, menghambat
proses absisi yaitu pengguguran daun, merangsang pembentukan buah,
penghambat pucuk lateral yaitu menghambat pertumbuhan tunas ketiak dan dapat
merangsang pertumbuhan kambium serta membentuk pertumbuhan floem dan xilem
sekunder.
Beberapa contoh produk yang telah menggunakan agensia hayati
BlightBan A506, Conquer dan Victus. Produk tersebut tersedia dalam bentuk serbuk
dan cairan yang dapat langsung diaplikasikan ke tanaman (Cook, 2002).
2.3 Penyakit Layu Fusarium
Jamur Fusarium sp. merupakan patogen tular tanah atau soil borne pathogen
yang termasuk parasit lemah. Jamur ini menular melalui tanah atau rimpang yang
berasal dari tanaman sakit, dan menginfeksi melalui luka, dan dapat terjadi karena
pengangkutan benih, penyiangan, pembumbunan, atau karena serangga dan
nematode. Walaupun tanah sudah tertular, gejala penyakit belum tampak pada
tanaman karena memerlukan waktu beberapa bulan, apabila kondisi lingkungan
tidak menguntungkan, jamur bertahan hidup dalam bagian tanaman, pada saat
kondisi lingkungan menguntungkan, jamur akan tumbuh dan berkembang pada
bagian tanaman dan menular ke bagian tanaman lain (Agrios, 1997). Patogen ini
umumnya sulit dikendalikan karena memiliki kisaran inang yang luas, menurut
Agrios (1996) penyakit layu Fusarium dapat diklasifikasikan sebagai berikut :
Kingdom : Mycetae,
divisi : Mycota,
subdivisi : Deuteromycotina,
klas : Hypomycetes,
ordo : Hyphales (Moniliales),
family : Tuberculariaceae,
genus : Fusarium,
Fusarium sp. memiliki mikrokonidia tidak berwarna, bersel tunggal, berbentuk
bulat dengan panjang 6 - 15 µm dan berdiameter 3 - 5 µm, makrokonidia berbentuk
bulan sabit, tidak berwarna, mempunyai 3 - 5 sekat, masing-masing panjangnya
30 - 50 µm dan berdiameter 2 - 5 µm, dan klamidospora halus, berbentuk bola,
bersel tunggal yang menghasilkan miselium yang tua dan rata-rata berdiameter
10 µm. Ketiga jenis spora tersebut merupakan patogen tular tanah yang akan
menginfeksi tanaman. Setelah mengadakan infeksi, tanaman akan mati kemudian
jamur dan spora tersebut akan tetap berada di dalam tanah dimana jamur dapat
bertahan pada jangka waktu yang tidak terbatas (Lucas, 1985).
Miselium jamur ini bersekat terutama terdapat di dalam sel, khususnya di
dalam pembuluh kayu. Disamping itu jamur membentuk miselium yang terdapat
diantara sel-sel, yaitu dalam kulit dan di jaringan parenkim di dekat tempat terjadinya
infeksi (Semangun, 1994). Pada medium Potato Dextrose Agar (PDA) mula-mula
miselium berwarna putih, semakin tua warna menjadi krem atau kuning pucat, dalam
keadaan tertentu berwarna merah muda agak ungu. Miselium bersekat dan
membentuk percabangan. Beberapa isolat Fusarium akan membentuk pigmen biru
atau merah di dalam medium (Semangun, 2004).
2.3.1 Daur hidup penyebab penyakit
Patogen penyebab layu Fusarium, dapat menginfeksi tanaman melalui biji
yang terkontaminasi atau pencangkokan tanaman yang terinfeksi. Jamur ini dapat
menginfasi tanaman melewati sistem serabut akar dan mengganggu proses
pengambilan air dan mineral pada tanaman. Perkembangan infeksi dan penyakit
layu Fusarium, didukung oleh suhu tanah yang hangat (26 ºC) dan kelembapan
Inokulum patogen selain dapat masuk melalui akar dengan penetrasi
langsung atau melalui luka, didalam jaringan tanaman, patogen dapat berkembang
secara interseluler dan intraseluler (Winarsih, 2007).
Jamur Fusarium oxysporum f. sp. melonis aktif pada suhu antara 25 ºC dan
32 °C, karena jamur menghasilkan spora istirahat (chlamydospores). Jamur dapat
bertahan hidup di dalam tanah tidak terbatas, bahkan tidak ada tanaman inang
masih dapat tumbuh. Tanah asam (pH 5,0 - 5,6) dan amonium nitrogen (amonium
nitrat dan urea) mempercepat perkembangan penyakit (Varela dan Seif, 2004).
2.3.2 Gejala serangan
Gejala serangan yang diamati secara visual adalah tanaman dewasa layu.
Tanaman biasanya layu mulai dari daun bagian bawah dan anak tulang daunnya
menguning. Setelah infeksi daun-daun tanaman memucat, selanjutnya gejala
tersebut menjalar sampai 2 cm di atas permukaan tanah. Tanaman dapat menjadi
layu dan akhirnya mati (Semangun, 2000).
Gejala layu Fusarium ditandai dengan menguningnya daun yang lebih tua
kemudian berubah menjadi kecoklatan dan layu tanaman akan merambat dan diikuti
dengan runtuhnya tanaman. Jika batang yang terinfeksi dibelah jaringan vaskular
menunjukkan perubahan warna cokelat (Varela dan Seif, 2004).
2.4 Rizosfer
Istilah rizosfer menunjukkan bagian tanah yang dipengaruhi perakaran
tanaman (Subba Rao, 1994 ). Rizosfer dicirikan oleh adanya kegiatan mikrobiologis
dibandingkan kegiatan di dalam tanah yang jauh dari perakaran tanaman. Terdapat
lebih banyak jumlah bakteri, jamur dan actinomycetes dalam tanah yang termasuk
tanah, kelembaban tanah, pH, temperatur, umur serta kondisi tanaman dapat
mempengaruhi efek rizosfer.
Adanya organisme yang merugikan di sekitar akar tanaman yang sakit dan
organisme yang bermanfaat di sekitar akar tanaman yang sehat (Bruehl, 1987).
Menurut Wood (1989), rizosfer adalah bagian tanah di mana lebih banyak terdapat
bakteri di sekitar akar tanaman daripada tanah yang jauh dari akar tanaman.
Umumnya rizosfer dari kebanyakan tanaman mengandung bakteri Gram negatif,
tidak berspora, berbentuk batang, dan terdapat pada daerah rizoplan. Beberapa
genus bakteri ini adalah Pseudomonas, Arthrobacter, Agrobacterium, Azotobacter,
Mycobanterium, Flavobacterium, Cellulomonas, Micrococcus dapat ditemukan
dalam jumlah yang banyak namun ada juga yang tidak ditemukan sama sekali.
2.5 Hipotesis
(1) Diduga adanya bakteri Pseudomonad fluorescens yang dapat menghambat
Fusarium oxysporum f. sp. melonis pada lahan melon di UPT
Pengembangan Agribisnis dan Tanaman Hortikultura Lebo, Sidoarjo.
(2) Diduga Pseudomonad fluorescens mampu dalam mengkolonisasi akar
kecambah lebih cepat dibandingkan Fusarium sp.
(3) Diduga terdapat antibiosis Pseudomonad fluorescens yang menghambat
III. BAHAN DAN METODE PENELITIAN
3.1 Tempat dan Waktu
Kegiatan penelitian dilaksanakan di lahan melon UPT Pengembangan
Agribisnis dan Tanaman Hortikultura Lebo, Sidoarjo; dan Desa Karang Sinom,
Indramayu; serta Laboratorium Kesehatan Tanaman Fakultas Pertanian, Universitas
Pembangunan Nasional “Veteran” Jawa Timur. Penelitian dilakukan pada Oktober
2013 sampai dengan Februari 2014.
3.2 Alat dan Bahan 3.2.1 Alat-alat
Alat penelitian yang digunakan dalam penelitian ini adalah Laminar Air Flow
(LAF), cawan Petri berdiameter 9 cm, autoklaf (All American), obyek gelas, tabung
reaksi, gelas ukur, bunsen, pipet, jarum ose, scalpel, Erlenmeyer 250 ml, penggaris,
pinset, gunting, botol simpan, sprayer (botol semprot), mikroskop (Will Wetzlar),
timbangan analitik (Kern PCB), waterbath (Memment), growth chamber, cork borer,
dan kompor.
3.2.2 Bahan-bahan
Bahan penelitian yang digunakan dalam penelitian ini adalah isolat bakteri
Pseudomonad fluorescens, isolat jamur Fusarium oxysporum f. sp. melonis, benih
melon, tanah pasir, aquadest steril, aluminium foil, media King’s B, media Water
Agar (WA) 0,1 %, media cair King’s B, media Nutrient Agar (NA) (Merck), media
Potato Dextrose Agar (PDA) (Criterion), KOH 3 %, H2O2 5 %, alkohol 70 %, alkohol
95 %, tisu, kapas, kertas label, korek api, spirtus, parafilm, lactovenol blue,
3.3 Metode Penelitian 3.3.1 Penelitian tahap I :
Isolasi dan screening Pseudomonad fluorescens
Metode yang digunakan dalam isolasi dan screening mikroorganisme
Pseudomonad fluorescens adalah metode survei dan diskriptif. Dimana hasil isolasi
dan screening tersebut akan dilanjutkan dengan pengujian karakteristik
Pseudomonad fluorescens berdasarkan sifat gram, fluoresensi, dan pembusukan
kentang (potato soft root).
Uji antagonistik bakteri Pseudomonad fluorescens terhadap jamur patogen Fusarium oxysporum f. sp. melonis secara in vitro
Rancangan penelitian yang digunakan adalah Rancangan Acak Lengkap
(RAL). Pengujian tersebut terdiri dari 3 perlakuan dan 4 ulangan dengan
penempatan sebagaimana tampak pada denah percobaan yang tertera pada
Gambar 1 dengan perlakuan yang dimaksud adalah :
PfN2 adalah isolat Pseudomonad fluorescens 1
PfN5 adalah isolat Pseudomonad fluorescens 2
PfN7 adalah isolat Pseudomonad fluorescens 3
Gambar 1. Denah percobaan pada uji antagonistik. (1), (2), (3), (4) adalah ulangan
PfN2 (3) PfN5 (2) PfN2 (1)
PfN7 (2) PfN5 (3) PfN5 (1)
PfN2 (4) PfN7 (4) PfN5 (4)
Isolasi patogen Fusarium oxysporum f. sp. melonis
Metode yang digunakan dalam isolasi Fusarium oxysporum f. sp. melonis
adalah metode survei dan diskriptif. Dimana hasil yang diperoleh dibandingkan
dengan menggunakan buku taxonomi jamur Illustrated genera of imperfect fungi
(Barnett dan Hunter, 1972).
3.3.2 Penelitian tahap II :
Pola kolonisasi agensia hayati dan patogen
Metode yang digunakan dalam pola kolonisasi agensia hayati dan patogen di
rizosfer perkecambahan melon adalah metode diskriptif dan destruktif, dimana
pengamatan dilakukan secara mikroskopis dengan perlakuan :
Pa adalah aplikasi suspensi bakteri Pseudomonad fluorescens sebanyak 10 ml
Pb adalah aplikasi campuran suspensi bakteri Pseudomonad fluorescens sebanyak
5 ml dan Fusarium oxysporum f. sp. melonis sebanyak 5 ml
Pc adalah aplikasi suspensi Fusarium oxysporum f. sp. melonis sebanyak 10 ml
Uji antibiosis bakteri Pseudomonad fluorescens dari rizosfer perkecambahan melon terhadap Fusarium oxysporum f. sp. melonis secara in vitro
Rancangan penelitian yang digunakan dalam uji antibiosis bakteri
Pseudomonad fluorescens dari rizosfer perkecambahan melon terhadap jamur
patogen Fusarium oxysporum f. sp. melonis adalah Rancangan Acak Lengkap
(RAL). Pengujian tersebut terdiri dari 4 perlakuan dan 4 ulangan dengan
penempatan sebagaimana tampak pada denah percobaan yang tertera pada
Gambar 2 dengan perlakuan yang dimaksud adalah :
2 HSI adalah waktu suspensi agensia hayati 2 hari setelah inokulasi
6 HSI adalah waktu suspensi agensia hayati 6 hari setelah inokulasi
8 HSI adalah waktu suspensi agensia hayati 8 hari setelah inokulasi
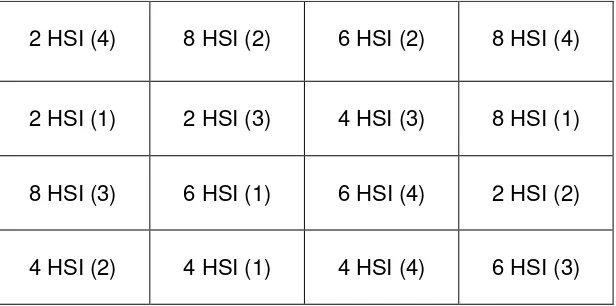
Gambar 2. Denah percobaan pada uji antibiosis. (1), (2), (3), (4), adalah ulangan
3.4 Pelaksanaan
3.4.1 Penelitian tahap I :
Isolasi dan screening bakteri Pseudomonad fluorescens
Mengambil tanah disekitar perakaran (rizosfer) tanaman melon yang sehat
diantara yang sakit beserta akarnya. Sampel tanah yang sudah diambil, kemudian
dimasukkan kedalam kantong plastik untuk dibawa ke laboratorium.
Isolasi sampel tanah dilakukan di laboratorium dengan cara menimbang
sampel tanah sebanyak 25 g, kemudian dimasukkan kedalam erlenmeyer yang
berisi 250 ml aquadest steril. Mengkocok erlenmeyer tersebut selama ± 15 menit
dengan menggunakan shaker, selanjutnya didiamkan selama 5 menit dan dilakukan
seri pengenceran sampai 10-9, dengan cara mengambil 1 ml suspensi awal dengan
menggunakan mikropipet, kemudian mencampurkan dengan 9 ml air steril kedalam
tabung reaksi dan melakukan pengkocokan kembali. Seri pengenceran dilakukan
2 HSI (4) 8 HSI (2) 6 HSI (2) 8 HSI (4)
2 HSI (1) 2 HSI (3) 4 HSI (3) 8 HSI (1)
8 HSI (3) 6 HSI (1) 6 HSI (4) 2 HSI (2)
dengan cara yang sama sampai dengan 10-9, kemudian menumbuhkan suspensi
tersebut pada media NA dan inkubasi bakteri selama 24 jam.
Mengambil koloni tunggal yang memperlihatkan karakter koloni yang
transparan sampai buram, bercahaya, berlendir (mucoid) dengan bentuk cembung
yang jelas (Schaad, 2001). Menumbuhkannya pada cawan petri yang berisi media
NA dengan cara digores, selanjutnya menginkubasi bakteri lagi selama 24 jam pada
suhu ruangan. Setelah mendapatkan isolat yang memperlihatkan karakter koloni
bakteri, maka dilanjutkan dengan pengujian karakteristik Pseudomonad fluorescens
berdasarkan sifat gram, fluoresensi, dan pembusukan kentang (potato soft root)
yaitu sebagai berikut :
a. Uji Gram
Membuat larutan KOH 3 % dengan cara melarutkan 0,3 g KOH kedalam
100 ml aquadest steril. Mengambil larutan KOH sebanyak 1 tetes kedalam gelas
benda, setelah itu mengambil koloni tunggal dari media NA yang telah ditumbuhkan,
kemudian menarik secara perlahan koloni tersebut yang telah dicelupkan pada
larutan KOH 3 %. Pengamatan dilakukan terhadap adanya perubahan masa bakteri
tersebut, yaitu perubahan masa bakteri menjadi berlendir dan tertarik ketika
diangkat, perubahan masa tersebut menunjukkan bahwa bakteri tersebut bersifat
gram negatif (Fahy and Hayward, 1983).
b. Uji Fluoresensi
Mengambil koloni tunggal pada media NA dan menumbuhkannya pada
cawan petri yang berisi media King’s B. Menginkubasi bakteri selama 24 jam pada
tersebut berpendar dan berwarna hijau maka menghasilkan pigmen fluorescens
(Brown, 1980).
c. Uji Potato Soft Root
Memotong buah kentang berbentuk kotak, kemudian mencelupkan kentang
tersebut ke dalam alkohol 70 %, lalu mencelupkan kembali ke dalam aquadest.
Mengambil koloni tunggal bakteri pada media NA dan menggoreskannya pada
bagian tengah kentang, setelah itu menaruh ke dalam cawan petri dan
menginkubasi selama 24 jam. Pengamatan dilakukan terhadap adanya perubahan
fisik kentang yang telah diinokulasi bakteri, berupa membusuk atau tidak membusuk
(Schaad, 2001).
Isolasi jamur Fusarium sp.
Mengambil tanaman melon yang menunjukkan gejala layu pada daun bagian
bawah yang menguning kecoklatan (Semangun, 2000); dan pada batang apabila
dibelah, jaringan vaskular menunjukkan perubahan warna coklat (Varela dan
Seif, 2004) beserta akarnya secara perlahan pada lahan melon di Desa Karang
Sinom, Indramayu. Sampel tanaman yang sudah diambil, kemudian dimasukkan
kedalam kantong plastik.
Melakukan isolasi sampel di laboratorium dengan cara membersihkan bagian
batang tanaman yang sakit menggunakan alkohol 70 %. Mengering anginkan,
kemudian memotong antara bagian kulit batang tanaman yang menunjukkan gejala
nekrosis dan yang sehat menggunakan scalpel. Menginokulasi potongan tersebut
pada media PDA. selanjutnya menginkubasi selama ± 5 hari (Sastrahidayat, 1994).
Memurnikan jamur patogen yang memiliki ciri morfologi koloni seperti jamur
muda dan membentuk percabangan di dalam media (Semangun, 2004). Selanjutnya
memperbanyak jamur Fusarium sp. pada media PDA.
Identifikasi jamur Fusarium oxysporum f. sp. melonis
Jamur Fusarium sp. yang sudah murni kemudian diidentifikasi berdasarkan
morfologi koloni dan pengamatan mikroskopis. Identifikasi dilakukan terhadap
warna, hifa, dan spora jamur tersebut. Hasil pengamatan morfologi jamur yang
diperoleh dibandingkan dengan morfologi jamur Fusarium oxysporum f. sp. melonis
menggunakan buku taxonomi jamur Illustrated genera of imperfect fungi (Barnett
dan Hunter, 1972).
Uji antagonistik bakteri Pseudomonad fluorescens terhadap jamur patogen Fusarium oxysporum f. sp. melonis secara in vitro
Pengujian antagonistik bakteri Pseudomonad fluorescens yang telah diisolasi
dari rizosfer melon dilakukan terhadap Fusarium oxysporum f. sp. melonis di
laboratorium. Uji antagonistik dilakukan dengan cara mensterilkan potongan kertas
cakram berdiameter 0.5 cm ke dalam autoklaf. Mencelupkan potongan kertas
cakram kedalam suspensi bakteri Pseudomonad fluorescens selama ± 10 menit,
kemudian meletakkan kertas cakram tersebut pada cawan petri yang berisi media
PDA. Pengambilan jamur Fusarium oxysporum f. sp. melonis dengan menggunakan
cork borer berdiameter 0.5 cm, dan meletakkan pada cawan petri yang sama
dengan posisi kedua isolat berhadapan dengan jarak 3 cm di tengah cawan petri
(Fokkema, 1976).
Menginkubasi selama 24 jam, selanjutnya melakukan pengamatan terhadap
mempunyai persentase daya hambat tertinggi akan digunakan dalam penelitian
tahap berikutnya.
3.4.2 Penelitian tahap II :
Inokulasi Pseudomonad fluorescens dan Fusarium oxysporum f. sp. melonis pada tanah pasir
Mensterilkan tanah pasir sebagai media tumbuh menggunakan autoklaf pada
suhu 121 ºC dengan tekanan 15 pcs (per square inci) selama ± 20 menit, untuk
bakteri Pseudomonad fluorescens umur 2 hari dilakukan seri pengenceran sampai
10-7, sedangkan untuk jamur Fusarium oxysporum f. sp. melonis umur 7 hari
dilakukan seri pengenceran sampai 10-6, setelah itu melakukan inokulasi yang
masing-masing menggunakan 10 ml per lubang tray (Olivain, Humber, Nahalkova,
Fatehi, Horidon, dan Alobouvete, 2006).
Aplikasi Benih Melon pada Tanah Pasir
Mensterilkan benih melon dengan cara merendam benih ke dalam alkohol
95 % selama 10 detik, kemudian merendam benih kedalam H2O2 5 % dengan
mengkocok selama ± 5 menit, selanjutnya membilas benih menggunakan aquadest
steril sebanyak 7 kali.
Mensterilkan kertas cakram berdiameter 9 cm menggunakan autoklaf,
kemudian membasahi kertas cakram menggunakan aquadest steril, selanjutnya
menginokulasi benih pada kertas cakram. Menginkubasi benih selama 4 hari dalam
keadaan gelap pada suhu ± 22 ºC. Benih yang telah berkecambah dengan ukuran
1 cm, ditanam pada tanah pasir yang telah diinokulasikan sesuai dengan perlakuan
Pengamatan pola kolonisasi pada akar perkecambahan melon
Pengamatan dilakukan pada hari ke-1, ke-3, dan ke-5 setelah inokulasi
dengan mencuci kecambah akar dari tanah yang menempel, selanjutnya melakukan
perendaman dengan KOH selama 60 menit. Mencuci kecambah akar menggunakan
aquadest steril, untuk memudahkan pemotretan terhadap pola koloni
Fusarium oxysporum f. sp. melonis dengan menggunakan metode scanning dengan
lactovenol blue. Bagian akar yang telah diperlakukan tersebut diletakkan pada gelas
benda cekung berisi media 0,1 % WA.
Melakukan pengamatan pola koloni Pseudomonad fluorescens dengan
mencuci kecambah akar menggunakan aquadest steril, melakukan perendaman
dengan KOH selama 60 menit, kemudian kembali mencuci kecambah akar
menggunakan aquadest steril, untuk memudahkan pemotretan terhadap pola koloni
Pseudomonad fluorescens dengan menggunakan metode scanning dengan
methylene blue, selanjutnya meletakkan bagian akar pada gelas benda cekung
berisi media cair King’s B.
Pengamatan pola koloni Fusarium oxysporum f. sp. melonis dan
Pseudomonad fluorescens dilakukan dengan mencuci kecambah akar dari tanah
yang menempel, selanjutnya melakukan perendaman dengan KOH selama 60
menit. Mencuci kecambah akar menggunakan aquadest steril, selanjutnya akar
kecambah dicelupkan kedalam lactovenol blue.selama 30 detik dan mencuci akar
kecambah dengan aquadest steril, akar kecambah yang telah dicuci dicelupkan
kedalam methylene blue selama 30 detik dan dicuci kembali dengan aquadest steril,
selanjutnya meletakkan bagian akar pada gelas benda cekung dan mengamati
Uji antibiosis bakteri Pseudomonad fluorescens dari rizosfer perkecambahan melon terhadap Fusarium oxysporum f. sp. melonis secara in vitro
Melakukan uji antibiosis dengan cara menimbang 1 g tanah yang
mengandung suspensi Pseudomonad fluorescens, kemudian dimasukkan ke dalam
10 ml aquadest steril, selanjutnya mengkocok selama 5 menit dan diendapkan
selama ± 3 jam.
Mensentrifus suspensi tanah tersebut dengan kecepatan ± 200 rpm selama
± 20 menit, selanjutnya mengambil supenatan yang telah mengandung bahan
antibiosis dan menyimpan dalam lemari es selama 24 jam. Mengambil jamur
Fusarium oxysporum f. sp. melonis dengan menggunakan cork borer berdiameter
0.5 cm, kemudian meletakkan pada cawan petri yang berisi media PDA.
Mensterilkan potongan kertas cakram berdiameter 0.5 cm, kemudian
dicelupkan ke dalam larutan antibiosis Pseudomonad fluorescens selama 10 menit
dan dikering anginkan, setelah itu meletakkan potongan kertas cakram pada cawan
petri yang sama, dengan posisi kedua isolat berhadapan dengan jarak 3 cm di
tengah cawan petri, selanjutnya melakukan inkubasi selama 24 jam.
3.5 Pengamatan
Pengamatan pada penelitian ini dilakukan secara destruktif dan parameter
yang diamati pada penelitian ini adalah sebagai berikut :
3.5.1 Persentase daya hambat
Pengamatan dilakukan terhadap jari-jari koloni jamur Fusarium oxysporum,
persentase daya hambat bakteri Pseudomonad flourescens terhadap patogen
I
=
R1-R2
R1
×100%
Keterangan :
I adalah Persentase daya hambat (%).
R1 adalah jari-jari koloni Fusarium oxysporum yang tumbuh berlawanan dengan
Pseudomonad fluorescens.
R2 adalah jari-jari koloni Fusarium oxysporum yang arahnya tumbuh menuju pusat
Pseudomonad fluorescens.
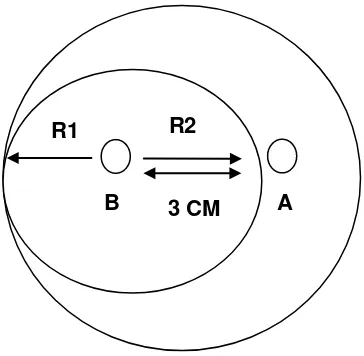
Gambar 3. Cara pengukuran koloni Fusarium oxysporum untuk menghitung persentase daya hambat antibiosis oleh mikroorganisme antagonis
Pseudomonad fluorescens.
A adalah inokulum antagonis Pseudomonad fluorescens
B adalah inokulum Fusarium oxysporum
R1 adalah jari-jari koloni Fusarium oxysporum yang tumbuh berlawanan dengan Pseudomonad fluorescens
R2 adalah jari-jari koloni Fusarium oxysporum yang arahnya tumbuh menuju pusat Pseudomonad fluorescens
3.5.2 Pola kolonisasi akar
Kolonisasi akar adalah suatu proses di mana bakteri diinokulasikan ke dalam
benih atau tanah, dapat bertahan hidup dan menggandakan diri, berasosiasi dengan
R1
B 3 CM R2
permukaan akar dan mengkoloni sistem akar yang sedang berkembang dalam tanah
(Baker dan Cook, 2002). Pengamatan dilakukan pada hari ke-1, ke-3, dan ke-5
setelah transplanting, pengamatan pada pola kolonisasi akar
Pseudomonad fluorescens menggunakan methylene blue dan media cair King’s B
sedangkan pada pola kolonisasi akar Fusarium oxysporum f. sp. melonis
pengamatan dilakukan menggunakan lactovenol blue dan media 0,1 % WA,
masing-masing pengamatan dilakukan secara mikroskopis.
3.6 Analisis Data
Data yang diperoleh dari hasil pengamatan dianalisis dengan uji varian
tunggal (one way anova) F pada taraf 5 %, apabila pada hasil analisis menunjukkan
bahwa F hitung > F tabel maka dilanjutkan dengan uji Beda Nyata Terkecil (BNT)
IV. HASIL DAN PEMBAHASAN
4.1 Isolasi dan Screening Bakteri Pseudomonad fluorescens
Hasil isolasi bakteri dari sampel tanah rizosfer melon diperoleh sembilan
koloni bakteri, yaitu Psudomonad fluorescens PfN1, PfN2, PfN3, PfN4, PfN5, PfN6,
PfN7, PfN8, dan PfN9 (Tabel 1.).
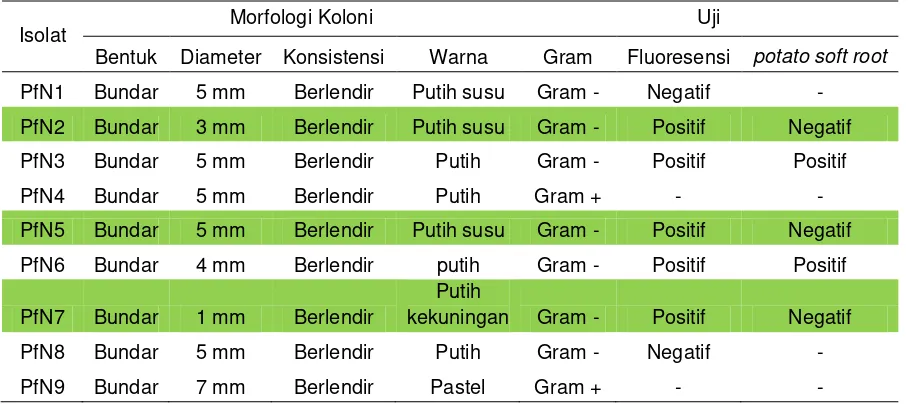
Tabel 1. Karakteristik Koloni Bakteri
Isolat Morfologi Koloni Uji
Bentuk Diameter Konsistensi Warna Gram Fluoresensi potato soft root
PfN1 Bundar 5 mm Berlendir Putih susu Gram - Negatif -
kekuningan Gram - Positif Negatif PfN8 Bundar 5 mm Berlendir Putih Gram - Negatif - PfN9 Bundar 7 mm Berlendir Pastel Gram + - -
Keterangan :
adalah bakteri Pseudomonad fluorescens
adalah tanda bahwa isolat tidak dilakukan uji lanjutan
Sembilan isolat dilakukan pengujian karakteristik Pseudomonad fluorescens
berdasarkan sifat gram, fluoresensi, dan pembusukan kentang (potato soft root).
Hasil kesembilan isolat menunjukkan bahwa isolat PfN2, PfN5, dan PfN7 merupakan
bakteri Pseudomonad fluorescens (Tabel 1.), ketiga isolat bersifat gram negatif
ditunjukkan dengan adanya campuran kental seperti lendir dan bila ditarik keatas
mengungkapkan bahwa Pseudomonad fluorescens merupakan bakteri gram negatif
yang sebagian besar bersifat non-patogenik dan saprofitik pada tanah dan daerah
rizosfer tanaman.
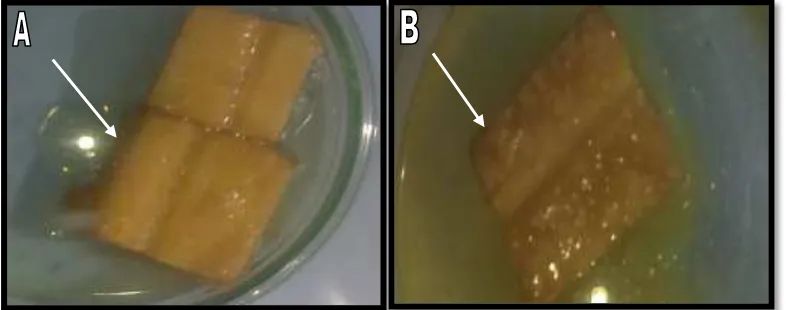
Gambar 4. Uji Gram dengan KOH 3 %. Reaksi postitif di tunjukkan dengan terbentunya lendir (A) dan reaksi negatif di tunjukkan dengan tidak terbentunya lendir (B)
Isolat PfN2, PfN5, dan PfN7 memiliki sifat fluorescens dimana isolat tersebut
mengeluarkan pendar berupa pigmen berwarna kuning kehijauan pada media King’s
B, pigmen tersebut membedakan bakteri yang termasuk ke dalam kelompok
Pseudomonad fluorescens dengan kelompok lain. Media King’s B merupakan media
yang sedikit mengandung ion Fe, sehingga bakteri yang temasuk ke dalam
kelompok Pseudomonad fluorescens akan membentuk siderofor yang fungsinya
mengikat ion Fe, siderofor dapat dideteksi dengan adanya pigmen warna kuning
kehiajuan yang berdifusi ke dalam medium King’s B. Pigmen yang berdifusi ke
dalam medium menjadi lebih jelas terlihat apabila diamati di bawah lampu UV
(Sands, 1990). Reaksi berpendarnya koloni sesuai dengan pendapat Brown (1980)
yang mengemukakan bahwa reaksi postif ditandai dengan adanya warna
Gambar 5. Uji Fluoresensi. Reaksi positif ditunjukkan dengan berpendarnya pigmen koloni bakteri berwarna hijau (A) dan reaksi negatif ditunjukkan dengan tidak berpendarnya pigmen koloni bakteri berwarna hijau (B).
PfN2, PfN5, dan PfN7 memiliki sifat avirulen yang ditandai dengan reaksi
negatif pada saat pengujian potato soft root, dimana pada kentang segar yang
diinokulasi dengan suspensi bakteri Pseudomonad flourescens menunjukkan bahwa
selama 24 jam setelah inokulasi tidak terjadi pembusukan.
4.2 Isolasi Jamur Fusarium sp.
Berdasarkan isolasi jamur dari batang bawah tanaman melon yang
menunjukkan gejala sakit layu fusarium didapatkan isolat Fusarium sp. melalui
identifikasi morfologi koloni dan pengamatan mikroskopis. Hasil pengamatan
menunjukkan bahwa morfologi jamur tersebut merupakan Fusarium oxysporum f. sp.
melonis, dimana miselium menunjukkan warna putih hingga kuning pada media
PDA. Hasil pengamatan mikroskopis Fusarium oxysporum f. sp. melonis
menunjukkan koloni tersebut memiliki makrokonidia berbentuk bulan sabit, tidak
berwarna, mempunyai 3 - 5 sekat, masing-masing berdiameter 2.5 µm – 4 µm dan
mikrokonidia tidak berwarna, berbentuk bulat dan berdiameter 3 µm (Gambar 7.).
2.5 µm
Gambar 7. A. Koloni Fusarium sp. pada media PDA umur 7 hari B. Fusarium sp. perbesaran 10 x 40.
a. Makrokonidia Fusarium sp. berdiameter 2.5 µm b. Mikrokonidia Fusarium sp. berdiameter 3 µm
Hal tersebut didukung oleh Semangun (2004) bahwa pada medium Potato
Dextrose Agar (PDA) mula-mula miselium berwarna putih, semakin tua warna
agak ungu, dan sesuai dengan buku taxonomi jamur Illustrated genera of imperfect
fungi (Barnett dan Hunter, 1972) serta didukung oleh Lucas (1985) bahwa jamur
Fusarium sp. memiliki mikrokonidia tidak berwarna, bersel tunggal, berbentuk bulat
dengan panjang 6 - 15 µm dan berdiameter 3 - 5 µm, makrokonidia berbentuk bulan
sabit, tidak berwarna, mempunyai 3 - 5 sekat, masing-masing panjangnya
30 - 50 µm dan berdiameter 2 - 5 µm, dan Klamidospora halus, berbentuk bola,
bersel tunggal yang menghasilkan miselium yang tua dan rata-rata berdiameter
10 µm.
4.3 Uji Antagonistik Bakteri Pseudomonad fluorescens terhadap Fusarium oxysporum f. sp. melonis (FOM) secara in vitro
Uji antagonistik bakteri Pseudomonad fluorescens terhadap jamur patogen
Fusarium oxysporum f. sp. melonis secara in vitro memperlihatkan adanya zona
bening di sekitar kertas cakram (Gambar 8.). Dari hasil perhitungan ANOVA
(Lampiran 4.) diketahui bahwa perlakuan zona hambat antagonistik bakteri
Pseudomonad fluorescens berbeda nyata terhadap pertumbuhan jamur patogen
Fusarium oxysporum f. sp. melonis.
Tabel 2. Zona Hambat yang Terbentuk dari Hasil Uji Antagonistik
Pseudomonad fluorescens terhadap Fusarium oxysporum f. sp. melonis
(7 hari setelah inokulasi)
Pembentukan zona bening terjadi kemungkinan karena adanya senyawa
antifungal yang dihasilkan oleh bakteri Pseudomonad fluorescens diantaranya
berupa pyrrolnitrin, phenazin-1-carboxylic acid, pyocyanin, dan
2,4-diacetylphloroglucinol.
Duffy dan Defago (1998) melaporkan bahwa senyawa antibiotik yang
dihasilkan bakteri Pseudomonad fluorescens antara lain pyrrolnitrin, pyoluteorin
(PLT), phenazine-1-carboxylase (PCA) dan 2,4-diacetylploroglucinol (PHL) yang
efektif menghambat perkembangan bakteri ataupun jamur patogen.
Gambar 8. Uji antagonistik bakteri Pseudomonad fluorescens terhadap
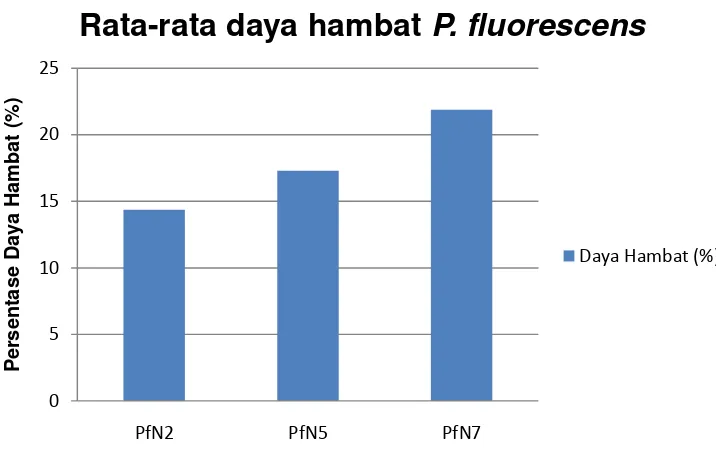
Hasil persentase daya hambat Pseudomonad fluorescens tidak berbeda
nyata terhadap Fusarium oxysporum f. sp. melonis, dari perhitungan didapatkan
isolat PfN7 mempunyai rata-rata daya hambat sebesar 21.88 %, diikuti dengan isolat
PfN5 sebesar 17.29 %, dan isolat PfN2 sebesar 14.36 %. Meskipun tidak berbeda
nyata, secara individual isolat-isolat bakteri Pseudomonad fluorescens cukup
mampu menghambat jamur patogen secara in vitro, kemampuan setiap isolat dalam
menghambat jamur patogen Fusarium oxysporum f. sp. melonis berbeda-beda,
kemungkinan disebabkan oleh jenis koloni ataupun strain bakteri tersebut.
Adanya penghambatan jamur patogen Fusarium oxysporum f. sp. melonis
disebabkan karena aktivitas antibiosis bakteri antagonis, dengan demikian hasil
pengujian diatas dipergunakan sebagai dasar dalam memilih isolat-isolat bakteri
yang mempunyai daya antagonistik yang lebih tinggi untuk dipergunakan dalam
pengujian selanjutnya.
Gambar 9. Rata-rata zona hambat dan persentase daya hambat antagonistik
Pseudomonad fluorescens terhadap jamur patogen (FOM)
4.4 Pola Kolonisasi Agensia Hayati dan Patogen di Rizosfer Perkecambahan Melon
Setelah didapatkan isolat Pseudomonad flourescens yang mempunyai daya
hambat tertinggi terhadap patogen, maka selanjutnya isolat PfN7 digunakan pada
perlakuan pola kolonisasi agensia hayati dan patogen di rizosfer perkecambahan
melon. Hasil penelitian menunjukkan bahwa bakteri agensia hayati dan patogen
dapat mengkolonisasi rizosfer perkecambahan melon. Masing-masing perlakuan
dengan menggunakan suspensi agensia hayati bakteri Pseudomonad fluorescens
dan suspensi patogen Fusarium oxysporum f. sp. melonis telah terlihat di dalam
jaringan akar kecambah pada hari pertama setelah inokulasi, sedangkan interaksi
antara campuran suspensi agensia hayati dan suspensi patogen belum terlalu
terlihat.
Gambar 10 memperlihatkan bahwa pola kolonisasi hari pertama setelah
inokulasi suspensi agensia hayati, patogen, serta pola kolonisasi campuran suspensi
agensia hayati dan suspensi patogen terlihat berbeda. Pola kolonisasi yang
ditunjukkan pada agensia hayati bakteri Pseudomonad fluorescens lebih mengarah
ke kiri akar kecambah, sedangkan pada pola kolonisasi jamur patogen
Fusarium oxysporum f. sp. melonis lebih condong mengarah ke kanan akar
kecambah.
Pola kolonisasi pada campuran suspensi agensia hayati dan patogen pada
hari pertama belum terlihat polanya, hal tersebut kemungkinan disebabkan oleh
waktu pertumbuhan yang singkat (1 hari) diantara kedua mikroba dan banyaknya
jumlah mikroba yang ada sehingga mempengaruhi aktivitas keduanya dalam
Gambar 10. Pola koloni agensia hayati dan patogen di rizosfer perkecambahan 1 HSI
K, adalah kontrol
Pa, adalah koloni bakteri Pseudomonad fluorescens (PfN7)
Pb, adalah koloni bakteri Pseudomonad fluorescens dan jamur patogen
Fusarium oxysporum f. sp. melonis Pc, adalah koloni patogen jamur Fusarium oxysporum f. sp. melonis
Pola kolonisasi 3 hari setelah inokulasi (HSI) memperlihatkan bahwa agensia
hayati bakteri Pseudomonad fluorescens dan Fusarium oxysporum f. sp. melonis
lebih banyak mengkolonisasi akar kecambah dibandingkan hari pertama, hal
tersebut disebabkan oleh proses periode mikroba dalam penempelan pada
permukaan akar telah cukup dan akar kecambah mulai memanjang sehingga
suspensi agensia hayati dan patogen 3 hari setelah inokulasi terlihat bahwa agensia
hayati Pseudomonad fluorescens mulai mendesak dari perkembangan patogen
Fusarium oxysporum f. sp. melonis, hal tersebut diperlihatkan dengan pola
kolonisasi agensia hayati yang mengarah ke tepi akar dan sebagian berada pada
tengah jaringan akar, sedangkan pola koloni patogen mulai berkurang
perkembangannya pada tengah jaringan akar kecambah melon (Gambar 11.).
Koloni Agensia Hayati
Serabut Akar
Koloni
Agensia Hayati
Koloni Patogen
Gambar 11. Pola koloni agensia hayati dan patogen di rizosfer perkecambahan 3 HSI
K, adalah kontrol
Pa, adalah koloni bakteri Pseudomonad fluorescens (PfN7) Pb, adalah koloni bakteri Pseudomonad fluorescens dan jamur
Pengamatan mikroskop pada pola kolonisasi akar 5 hari setelah inokulasi
menunjukkan bahwa bagian tepi koloni patogen Fusarium oxysporum f. sp. melonis
mulai tersdesak oleh bakteri antagonis Pseudomonad fluorescens. Hawker (1950)
menyatakan bahwa adanya kompetisi ruang dan makanan pada kedua mikroba
yang saling berinteraksi menyebabkan pertumbuhan salah satu mikroba terdesak di
sepanjang tepi koloninya. Adanya hambatan perkembangan pertumbuhan koloni
jamur patogen Fusarium oxysporum f. sp. melonis oleh bakteri antagonis
Pseudomonad fluorescens disebabkan karena pertumbuhan koloni bakteri antagonis
jauh lebih cepat dibanding jamur patogen (Gambar 12.). Hal ini didukung oleh
pernyataan Guo, Iersel, Chen, Brackket, dan Beuchat (2002) bahwa mikroba yang
tumbuh cepat mampu mengungguli dalam penguasaan ruang dan pada akhirnya
bisa menekan pertumbuhan mikroba lawannya.
Tingkat kolonisasi akar selain dipengaruhi oleh intrinsik bakteri antagonis
tersebut juga erat kaitannya dengan pengaruh cara aplikasinya (Raaijmakers, Sluis,
Hout M, Bakker, dan Schippers, 1995). Menurut Bakker, Pieterse, dan van Loon
(2007) ketika menempel pada akar tanaman, inokulum bakteri dapat menimbulkan
respon perlindungan pada tanaman, sehingga memungkinkan tanaman bertahan
terhadap serangan patogen tanaman.
Pertumbuhan akar kecambah dan periode aplikasi suspensi juga
mempengaruhi pola kolonisasi suatu mikroba, karena pada periode tumbuh mikroba
yang optimal dapat membantu penempelan mikroba pada permukaan akar dan jika
akar kecambah mulai memanjang maka mikroba dapat melakukan perbanyakan diri
Koloni Agensia Hayati
Koloni Patogen
Serabut Akar Koloni Patogen
Gambar 12. Pola koloni agensia hayati dan patogen di rizosfer perkecambahan 5 HSI
K, adalah kontrol
Pa, adalah koloni bakteri Pseudomonad fluorescens (PfN7)
Pb, adalah koloni bakteri Pseudomonad fluorescens dan jamur patogen
Fusarium oxysporum f. sp. melonis Pc, adalah koloni patogen jamur Fusarium oxysporum f. sp. melonis
4.5 Uji Antibiosis Bakteri Pseudomonad fluorescens dari Rizosfer Perkecambahan terhadap Jamur Fusarium oxysporum f. sp. melonis secara in vitro
Hasil analisis statistik menunjukkan bahwa antibiosis bakteri antagonis
Pseudomonad fluorescens dari rizosfer perkecambahan melon memberikan
Fusarium oxysporum f. sp. melonis (Lampiran 6.), dengan terbentuknya zona
hambat.
Terbentuknya zona hambat (Gambar 13.) menandakan bahwa bakteri
Pseudomonad fluorescens tersebut kemungkinan memproduksi suatu senyawa
antimikrobial baik berupa enzim, toksin maupun antibiosis. Antibiosis adalah mikroba
yang mampu menghambat pertumbuhan mikroba lain dengan antibiotik yang
diproduksinya, agens antagonis menunjukkan zona hambat yang jelas seperti yang
diungkapkan oleh Maria (2002), bahwa kriteria keefektifan hasil uji antibiosis secara
in vitro dilihat dari terbentuk atau tidaknya zona hambatan, yaitu zona bening di
antara patogen dan agens antagonis.
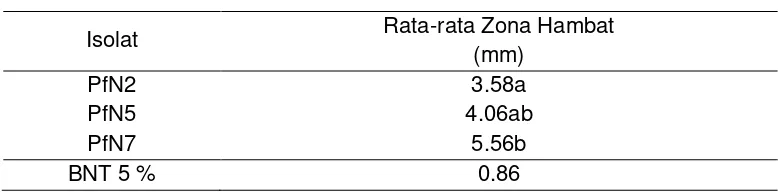
Tabel 3. Zona Hambat yang dihasilkan pada Uji Antibiosis
Perlakuan Rata-rata Zona Hambat
Keterangan : Angka yang diikuti oleh huruf sama, menunjukkan tidak berbeda nyata pada P = 0,05
Daya hambat antibiosis Pseudomonad fluorescens dari rizosfer
perkecambahan melon pada 2 HSI, 4HSI, 6 HSI, dan 8 HSI terhadap jamur patogen
Fusarium oxysporum f. sp. melonis ditampilkan pada Gambar 13. Dari hasil
perhitungan ANOVA (lampiran 7.) diketahui bahwa Fhitung > Ftabel pada taraf
Sehingga daya hambat antibiosis bakteri Pseudomonad fluorescens pada rizosfer
perkecambahan melon berbeda nyata terhadap Fusarium oxysporum f. sp. melonis.
Gambar 13. Uji antibiosis Pseudomonadfluorescens terhadap jamur patogen
Fusarium oxysporum f. sp. melonis (Pengamatan dilakukan hingga hari ke-7)
Tabel 4, menunjukkan bahwa persentase daya hambat antibiosis mengalami
peningkatan setiap perlakuannya, dimana pada perlakuan 2 HSI diperoleh daya
hambat sebesar 6.25 %, dilanjutkan dengan perlakuan 4 HSI meunjukkan daya
hambat yang cukup signifikan yaitu sebesar 8.81 %, kemudian diikuti oleh perlakuan
6 HSI sebesar 11.88 % dan daya hambat optimal ditunjukkan pada perlakuan 8 HSI
perkecambahan melon mempengaruhi daya hambat antibiosis pada patogen,
menurut. Menurut Dwidjoseputro (1994), faktor yang mempengaruhi daya hambat
antibiosis suatu mikroorganisme antara lain lama inkubasi dan aktivitas metabolisme
mikroorganisme.
Keterangan : Angka yang diikuti oleh huruf sama, menunjukkan tidak berbeda nyata pada P = 0,05
Daya hambat antibiosis kemungkinan dipengaruhi oleh adanya hubungan
antara waktu perkembagan bakteri di rizosfer, lama inkubasi, aktivitas metabolisme
bakteri, dan persediaan unsur hara pada tanah. Lama inkubasi mempengaruhi
perkembangan bakteri pada media tanam, sehingga bakteri mempunyai waktu untuk
memperbanyak diri dan menghasilkan antibiosis ataupun senyawa yang dapat
menghambat suatu patogen pada area rizosfer, dengan demikian waktu yang
optimal Pseudomonad fluorescens dalam menghasilkan antibiosis untuk
menghamabat Fusarium oxysprum f. sp. melonis yaitu pada hari kedelapan setelah
inokulasi. Menurt Soesanto (2008) bakteri Pseudomonad fluorescens mulai
mengeluarkan daya hambat dengan antibiosis yang optimum pada hari keenam
Suhu merupakan salah satu faktor lingkungan yang juga sangat menentukan
keberhasilan pengendalian patogen tumbuhan jika menggunakan agensia hayati.
Berdasarkan hasil penelitian, diperoleh bahwa secara umum penghambatan jamur
Fusarium oxysporum f. sp melonis dapat berlangsung dengan baik pada suhu 22 ºC.
Hal ini sesuai pernyataan Hamdan (1991) bahwa pertumbuhan dan produksi
antibiotik pyoverdin oleh Pseduomonas fluorescens yang efektif dilakukan pada
suhu 20 ºC – 30 ºC, bahkan pada kisaran tersebut kemampuan dapat menekan