STRUKTUR ATOM
DAN SISTEM
DEMOCRIT
US
DEMOCRIT
US
“Semua materi tersusun
dari partikel kecil yang
tidak dapat terbagi lagi
yang disebut
atomos
.
“Semua materi tersusun
dari partikel kecil yang
tidak dapat terbagi lagi
yang disebut
Teori
Atom
Dalton
Teori Atom Rutherford
Percobaan Rutherford
Sebagian besar volume atom merupakan ruang kosong Sebagian besar volume atom merupakan ruang kosong
Atom tersusun dari inti atom (proton
dan neutron) bermuatan positif dan elektron bermuatan negatif yang mengelilingi inti
Atom tersusun dari inti atom (proton
Bentuk- bentuk orbital
Bilangan kuantum utama
(n)
Kulit K
L
M
N
O
P
Q
Nilai
n
1
2
3
4
5
6
7
Menentukan besarnya tingkat energi
suatu elektron yang mencirikan
ukuran orbital
Menentukan besarnya tingkat energi
suatu elektron yang mencirikan
Bilangan kuantum azimut (l)
Harg
a l
0
1
2
3
4
5
6
Subku
lit
s
p
d
f
g
h
i
Menyatakan subtingkat energi
(subkulit) yang menunjukkan bentuk
orbital
Menyatakan subtingkat energi
Bilangan kuantum magnetik
(m)
Subk
ulit l Jumlah Orbital (2l + 1) m
s 0 1 0
p 1 3 -1, 0, +1
d 2 5 -2, -1, 0, +1, +2 f 3 7 -3, -2, -1, 0, +1,
+2, +3
Menentukan arah orientasi dari
orbital didalam ruang relatif terhadap
orbital lain
Menentukan arah orientasi dari
Bilangan kuantum spin (s) menyatakan rotasi elektron.
s dapat mempunyai nilai +½ (dinyatakan dengan tanda )
s dapat mempunyai nilai -½ (dinyatakan dengan tanda )
Bilangan kuantum spin (s) menyatakan rotasi elektron.
s dapat mempunyai nilai +½ (dinyatakan dengan tanda )
s dapat mempunyai nilai -½ (dinyatakan dengan tanda )
Bilangan kuantum spin tidak berhubungan secara langsung dengan tiga bilangan kuantum
lainnya
Bilangin kuantum spin
(s)
Partikel Penyusun Atom
Partik
el
Muata
n
Penemu
(gram)
Massa
Elektro
n
-
J.J. Thomson 9,11 x 10
-28
Proton
+
Goldstein
1,67 x 10
-24
Neutro
n
Netral
Chadwick
James
1,67 x 10
Lambang Unsur
Keterangan :
X = Lambang Unsur
A = Nomor Massa Z = Nomor Atom Keterangan :
X = Lambang Unsur
Nomor Atom (Z)
Nomor Massa (A)
Konfigurasi elektron
berdasarkan kulit atom
• Elektron mengelilingi inti pada lintasan/
kulit tertentu yang disebut kulit atau tingkat energi
• Konfigurasi elektron menyatakan susunan elektron pada atom
Nomo
r kulit Nama kulit
Jumlah elektron maksimu
m
1 K 2
2 L 8
3 M 18
4 N 32
5 O 50
6 P 72
Konfigurasi elektron beberapa
atom
Tanda
atom elektronJumlah Konfigurasi elektron
3Li 3 2 1
12Mg 12 2 8 2 17Cl 17 2 8 7
19K 19 2 8 8 1 31Ga 31 2 8 18 3
>> Jumlah elektron yang menempati kulit terluar disebut elektron valensi.
Aturan
menuliska
n
konfigurasi
elektron
KONFIGURASI ELEKTRON
BERDASARKAN ORBITAL
Aturan Aufbau
Elektron
mempunyai
kecenderungan
untuk menempati
subkulit dengan
tingkat energi
Larangan Pauli
Larangan pauli menyatakan bahwa
didalam satu atom tidak boleh
terdapat dua elektron dengan empat
bilangan kuantum yang sama
Kulit
n
l
m
s
L
2
0
0
+½
Aturan Hund
Diagram Orbital
1s 2s 2p
Pada orbital yang memiliki tingkat
energi sama, pengisian elektron dalam
orbital dilakukan dengan spin sejajar
terlebih dahulu (setengah penuh).
Contoh =
8O : 1s
22s
2Contoh penulisan konfigurasi
elektron
Ato
m
Konfigurasi elektron
2
He 1s
2[He]
4
Be 1s
22s
2[He] 2s
210
Ne 1s
22s
22p
6[Ne]
17
Cl 1s
22s
22p
63s
23p
5[Ne] 3s
23p
518
Ar 1s
22s
22p
63s
23p
6[Ar]
24Cr 1s
22s
22p
63s
23p
64s
13d
5[Ar] 4s
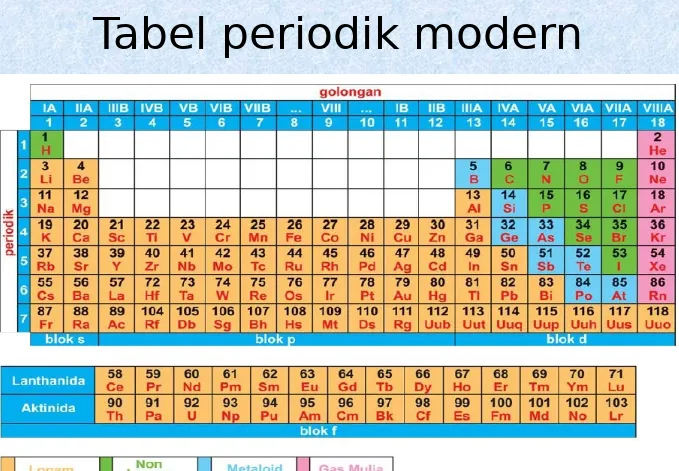
1SISTEM PERIODIK UNSUR
SISTEM PERIODIK UNSUR
Triade
Dobereiner
“Berdasarkan massa atom relatifnya,
unsur – unsur dapat dikelompokkan
ke dalam kelompok tiga unsur
dimana massa unsur yang ditengah
merupakan rata- rata dari massa
Teori Oktaf Newlands
“Jika unsur- unsur disusun berdasarkan kenaikan massa atom, maka sifat unsur
Penentuan periode dan
golongan
Konfigurasi elektron
valensi Golongan Utama Periode
ns1 IA n
ns2 IIA n
ns2 np1 IIIA n
ns2 np2 IVA n
ns2 np3 VA n
ns2 np4 VIA n
ns2 np5 VIIA n
ns2 np6 VIIIA n
Periode : Nomor kulit terluar
Periode : Nomor
kulit terluar Golongan : Jumlah elektron valensi Golongan : Jumlah
Jari- jari
atom
Jarak dari inti atom sampai kulit elektron terluar yang ditempati elektron
+
Jumlah kulit bertambah maka jari-jari makin besar
Jumlah kulit bertambah maka jari-jari makin besar
Jumlah kulit sama tetapi muatan inti makin besar, gaya tarik inti
terhadap elektron makin kuat, maka jari-jari makin kecil
Jumlah kulit sama tetapi muatan inti makin besar, gaya tarik inti
terhadap elektron makin kuat, maka jari-jari makin kecil
Energi ionisasi
Energi minimum yang dibutuhkan suatu atom untuk melepaskan satu elektron valensinya dalam wujud gas sehingga membentuk ion positif
+
-Jumlah kulit bertambah, jari-jari makin besar, tarikan inti lemah,
maka energi ionisasi kecil
Jumlah kulit bertambah, jari-jari makin besar, tarikan inti lemah,
maka energi ionisasi kecil
Muatan inti bertambah, tarikan inti makin kuat dan elektron terluar sulit lepas, maka energi
ionisasi besar
Muatan inti bertambah, tarikan inti makin kuat dan elektron terluar sulit lepas, maka energi
Afinitas elektron
Energi yang dihasilkan oleh suatu atom apabila suatu
atom menerima elektron valensi dari atom lain sehingga terbentuk ion
Jumlah kulit bertambah, jari-jari makin besar, tarikan inti lemah,
maka afinitas elektron kecil
Jumlah kulit bertambah, jari-jari makin besar, tarikan inti lemah,
maka afinitas elektron kecil
Muatan inti bertambah, tarikan inti makin kuat maka afinitas
elektron besar
Muatan inti bertambah, tarikan inti makin kuat maka afinitas
Keelektronegatifan
Kecenderunga n suatu atom
untuk menarik elektron valensi dari
atom lain dalam
Jumlah kulit bertambah, jari-jari makin besar, tarikan inti lemah,
maka keelektronegatifan kecil Jumlah kulit bertambah, jari-jari makin besar, tarikan inti lemah,
maka keelektronegatifan kecil Muatan inti bertambah, tarikan
inti makin kuat maka keelektronegatifan besar
Muatan inti bertambah, tarikan inti makin kuat maka
Logam dan
nonlogam
Logam
• Konduktor
• Warna mengkilap
khas logam
• Keras dan ulet
Nonlogam
• Non-konduktor
• Titik didih dan titik
leleh rendah Periode G o lo n g a
n Sifat logam
bertambah Sifat logam
bertambah nonlogam Sifat
bertambah Sifat
Kereaktif
an
Kereaktifan bertambah Kereaktifan bertambah
Kereaktifan menurun kemudian bertambah.
Golongan VIII A (gas mulia) tidak reaktif
Kereaktifan menurun kemudian bertambah.
Golongan VIII A (gas mulia) tidak reaktif
Bergantung pada kecenderungan
melepas atau menerima elektron