SKOR SELVESTER YANG DISEDERHANAKAN SEBAGAI PREDIKTOR KEJADIAN KARDIOVASKULAR MAYOR DALAM 30 HARI PADA PASIEN INFARK MIOKARD AKUT ELEVASI SEGMEN ST TANPA REPERFUSI DINI
TESIS PROFESI
Oleh
SYAIFULLAH NIM: 117115009
PEMBIMBING: 1. Prof. dr. HARRIS HASAN, SpPD, SpJP(K) 2. dr. ALI NAFIAH NASUTION, SpJP(K)
DEPARTEMEN KARDIOLOGI DAN KEDOKTERAN VASKULAR FAKULTAS KEDOKTERAN
UNIVERSITAS SUMATERA UTARA MEDAN
2017
SKOR SELVESTER YANG DISEDERHANAKAN SEBAGAI PREDIKTOR KEJADIAN KARDIOVASKULAR MAYOR DALAM 30 HARI PADA PASIEN INFARK MIOKARD AKUT ELEVASI SEGMEN ST TANPA REPERFUSI DINI
TESIS PROFESI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Spesialis Jantung dan Pembuluh Darah (SpJP)
dalam Program Studi Kardiologi dan Kedokteran Vaskular pada Fakultas Kedokteran Universitas Sumatera Utara
Oleh
SYAIFULLAH NIM: 117115009
DEPARTEMEN KARDIOLOGI DAN KEDOKTERAN VASKULAR FAKULTAS KEDOKTERAN
UNIVERSITAS SUMATERA UTARA MEDAN
2017
Judul Tesis : Skor Selvester Yang Disederhanakan Sebagai Predoktor Kejadian Kardiovaskular Mayor Dalam 30 Hari Pada Pasien Infark Miokard Akut Elevasi Segmen ST Tanpa Reperfusi Dini
Nama Mahasiswa : Syaifullah Nomor Registrasi : 117115009
Program Studi : Kardiologi dan Kedokteran Vaskuler
Menyetujui
Pembimbing I Pembimbing II
Prof. dr. Harris Hasan,Sp.PD, Sp.JP(K) dr. Ali Nafiah Nasution, Sp.JP(K) NIP. 195604051983031004 NIP. 198104142006041002
Mengetahui / Mengesahkan
Ketua Program Studi Ketua Departemen
Kardiologi dan Kedokteran Vaskuler Kardiologi dan Kedokteran Vaskuler
FK-USU / RSUP HAM Medan FK-USU/RSUP HAM Medan
dr. Ali Nafiah Nasution, Sp.JP(K) Prof. dr. Harris Hasan,Sp.PD, Sp.JP(K) NIP. 198104142006041002 NIP. 195604051983031004
Tanggal lulus: 5 September 2017
HALAMAN PERNYATAAN ORISINALITAS
SKOR SELVESTER YANG DISEDERHANAKAN SEBAGAI PREDIKTOR KEJADIAN KARDIOVASKULAR MAYOR DALAM 30 HARI PADA PASIEN INFARK MIOKARD AKUT
ELEVASI SEGMEN ST TANPA REPERFUSI DINI
TESIS PROFESI
Dengan ini saya menyatakan bahwa dalam tesis ini tidak terdapat karya yang pernah diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggi dan sepanjang pengetahuan saya tidak terdapat karya atau pendapat yang pernah dituliskan atau diterbitkan oleh orang lain, kecuali yang digunakan sebagai acuan referensi dan telah disebutkan dalam daftar pustaka.
Medan, September 2017
Syaifullah
UCAPAN TERIMA KASIH
Dengan memanjatkan puji dan syukur kehadirat Allah SWT,Tuhan Yang Maha Esa yang telah memberikan berkat dan rahmatNya sehingga penulis dapat menyelesaikan tesis ini. Tesis ini dibuat untuk memenuhi syarat kelulusan dalam Program Studi Kardiologi dan Kedokteran Vaskular di Fakultas Kedokteran Universitas Sumatera Utara.
Pada kesempatan ini perkenankanlah penulis menyatakan penghargaan dan ucapan terima kasih yang sebesar-besarnya kepada :
1. Rektor Universitas Sumatera Utara, Dekan Fakultas Kedokteran Universitas Sumatera Utara, dan Ketua TKP PPDS I Fakultas Kedokteran Universitas Sumatera Utara yang telah memberikan penulis kesempatan untuk mengikuti Program Pendidikan Spesialis Ilmu Penyakit Jantung dan Pembuluh Darah di Fakultas Kedokteran Universitas Sumatera Utara.
2. Prof.Dr.Harris Hasan, SpPD, SpJP(K), selaku Ketua Departemen Ilmu Penyakit Jantung dan Pembuluh Darah Fakultas Kedokteran Universitas Sumatera Utara/RSUP Haji Adam Malik Medan di saat penulis melakukan penelitian yang telah memberikan penulis kesempatan untuk mengikuti Program Pendidikan Spesialis Ilmu Penyakit Jantung dan Pembuluh Darah di Fakultas Kedokteran Universitas Sumatera Utara, serta sebagai pembimbing satu penulis dalam penyusunan tesis ini, yang dengan penuh kesabaran membimbing, mengoreksi, dan memberikan masukan-masukan berharga kepada penulis sehingga tulisan ini dapat diselesaikan.
3. Dr.Ali Nafiah Nasution, SpJP(K) selaku Ketua Program Studi PPDS Ilmu Penyakit Jantung dan Pembuluh Darah Fakultas Kedokteran Universitas Sumatera Utara serta pembimbing dua penulis yang telah memberikan bimbingan, kritik dan saran yang begitu berharga sehingga penulis dapat menyelesaikan tesis ini.
4. Guru-guru penulis : Prof.Dr.T.Bahri Anwar, SpJP(K); Prof.Dr.Sutomo Kasiman, SpPD, SpJP(K); Prof.Dr.Abdullah Afif Siregar, SpA(K), SpJP(K); Prof.Dr.Harris Hasan, SpPD, SpJP(K); Alm. Dr. Maruli T Simanjuntak SpJP(K); Dr.Nora C Hutajulu SpJP(K); DR. Dr. Zulfikri Mukhtar SpJP(K); Dr.Isfanuddin Nyak Kaoy, SpJP(K); Dr.P.Manik, SpJP(K); Dr.Refli Hasan, SpPD, SpJP(K); Dr.Amran Lubis, SpJP(K); Dr.Nizam Akbar, SpJP(K); Dr.Zainal Safri, SpPD, SpJP(K);
Dr.Andre Pasha Ketaren, SpJP(K); Dr.Andika Sitepu SpJP(K); Dr.Anggia Chairuddin Lubis, M.Ked (Kard), SpJP; Dr.Ali Nafiah Nasution, M.Ked (Kard), SpJP(K); Dr.Cut Aryfa Andra, M.Ked (Kard), SpJP(K), Dr. Hilfan Ade Putra Lubis, M.Ked (Kard), SpJP, Dr. Andi Khairul, M.Ked (Kard), SpJP, Dr. Abdul Halim Reynaldo, M.Ked (Kard), SpJP(K), Dr. Yuke Sarastri, M.Ked (Kard), SpJP, Dr. Teuku Bob Haykal, M.Ked (Kard), SpJP serta guru lainnya yang tidak dapat penulis sebutkan satu persatu, yang telah banyak memberikan masukan selama mengikuti program pendidikan profesi ini.
5. Direktur Rumah Sakit Umum Pusat Haji Adam Malik Medan yang telah memberikan kesempatan, fasilitas dan suasana kerja yang baik sehingga penulis dapat mengikuti Program Pendidikan Spesialis Ilmu Penyakit Jantung dan Pembuluh Darah.
6. Rekan-rekan sejawat sesama peserta PPDS Departemen Kardiologi dan Kedokteran Vaskular, terutama kepada dr. Mustika Fadhilah Sarahazti yang telah membantu dalam proses pengumpulan sampel penelitian ini. Juga kepada dr. Dika Ashrinda dan dr. Jaya Suganti yang telah membantu dalam analisis EKG sampel penelitian. Dan kepada dr. Zunaidi Syahputra, dr. Komaria atas masukan dan saran mengenai metodologi dan pengolahan data statistika terkait penyelesaian tesis ini.
7. Teman-teman Trickers Group: Dr. Denio Ridjab, Dr. Hadi Zulkarnain, Dr. Yuri Savitri, Dr. Agustina, Dr Arfian Amin Nasution, Dr. Joy Wulansari Purba, Dr. Sanny March Novalin Silaban yang telah memberikan semangat dan menjadi teman belajar yang menyenangkan selama menyelesaikan pendidikan di kardiologi.
8. Para perawat CVCU dan RIC, dan staf administrasi Ahmad Syafi’i, Zulkarnaen yang telah membantu terselenggaranya penelitian ini.
9. Kedua orang tua yang sangat penulis hormati dan sayangi, Solihin dan Nurliah, yang selama ini telah memberikan dukungan baik moril dan materi serta doa dan nasihat yang tulus agar penulis tetap semangat, sabar dan tegar dalam mengikuti pendidikan sampai selesai.
10. Mertua penulis Darwin Nasution dan Sri Ari Gustini, yang selama ini mendukung penulis dalam menyelesaikan pendidikan di kardiologi dengan baik.
11. Istri penulis dr. Utami Fitria Nasution yang selalu mendukung penulis dalam segala hal, memberikan semangat, dan mendukung penulis untuk menyelesaikan pendidikan kardiologi ini. Dan teruntuk anak penulis, Tasya Hanifah dan Muhammad Haqqi Alqodri, yang menjadi motivasi bagi penulis untuk dapat menyelesaikan pendidikan spesialis ini dengan baik.
Semoga Allah SWT membalas semua jasa dan budi baik mereka yang telah membantu penulis dalam menyelesaikan penelitian ini. Akhirnya penulis mengharapkan agar penelitian dan tulisan ini kiranya dapat bermanfaat bagi kita semua. Amin Ya Rabbal Alamin.
Medan, September 2017
Syaifullah
ABSTRAK
Latar Belakang: Skor Selevester yang disederhanakan merupakan penanda EKG yang dapat memprediksi ukuran infark miokard, dan kejadian kardiovaskular Mayor (KKvM) pada pasien infark miokard akut elevasi segmen ST (IMAEST) setelah reperfusi dini. Penelitian ini dilakukan untuk melihat apakah ada hubungannya Skor Selvester yang disederhanakan dengan KKvM pada IMAEST tanpa reperfusi dini.
Metode: Penelitian ini adalah studi retrospektif yang melibatkan 71 pasien IMAEST tanpa reperfusi dini dan menguji Skor Selvester yang disederhanakan sebagai prediktor KKvM selama dalam 30 hari. Nilai cutoff skor didapatkan dari kurva ROC.
Uji Chi-Square, Fisher’s exact dan regresi logistik dilakukan dalam menilai hubungan antara dua variabel atau lebih untuk mendapatkan rasio odds, p<0,05 dianggap signifikan.
Hasil: Pasien dengan KKvM dalam 30 hari memiliki Skor Selvester yang disederhanakan hari ke-4 rawatan yang lebih tinggi (12±2,3 vs 8±2,3; p<0,001). Nilai Cutoff yang didapatkan adalah 10,5. Uji regresi logistik menunjukkan bahwa Skor Selvester yang disederhanakan >10 merupakan faktor independen terhadap KKvM dalam 30 hari (p = 0,003; OR 4,9 ; 95% IK: 1,247 – 24,385).
Kesimpulan: Skor QRS yang disederhanakan merupakan prediktor independen KKvM 30 hari paska IMAEST tanpa reperfusi dini.
Kata Kunci: Skor Selvester, Skor QRS, Sindroma Koroner Akut, IMAEST, KKvM
ABSTRACT
Background: Selvester Score is a simple ECG markers that correlates with myocard infark size, and mayor adverse cardiac event (MACE) in ST Elevation Myocardial Infarction (STEMI) patient who performed early reperfusion. This Study carried out to see if there was any association between Simplified Selvester Score and MACE in 30- days after acute STEMI patients who were not performed early reperfusion therapy.
Method: We conducted a retrospective study among 71 STEMI patients who were not performed early reperfusion therapy and examined the relationship between Simplified Selvester Score and 30 days MACE. Cutoff point were taken from ROC curve. Chi- Squere, Fisher’s exact, and logistic regression test were used to examine the association between two variables and obtained odds ratio (OR). A value of p<0,05 was considered statistically significant.
Result: Patients with in-hospital MACE have higher Simplified Selvester Score at day- 4 hospitalization (12±2,3 vs 8±2,3; p<0,001). The optimum cutoff value in this study for Simplified Selvester Score was 10.5. In multivariate analysis, Simplified Selvester Score >10 remained significantly associated for MACE in 30-days after STEMI and appears to be strong predictor for MACE (p = 0,003; OR 4,9 ; 95% IK: 1,247 – 24,385).
Conclusion: This study showed relationship between Simplified Selvester Score and short-term MACE in STEMI patients who were not performed early reperfusion.
Simplified Selvester Score was independent predictor of short-term MACE in STEMI patients who were not performed early reperfusion.
Key words: Selvester Score, QRS Score, Acute Coronary Syndrome, STEMI, MACE
DAFTAR ISI
Halaman
Lembar Pengesahan ... i
Lembar Pernyataan Orisinalitas ... ii
Ucapan Terima Kasih ... iii
Abstrak ... vi
Abstract ... vii
Daftar Isi ... viii
Daftar Gambar ... x
Daftar Tabel ... xi
Daftar Singkatan dan Lambang ... xii
Daftar Lampiran ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Pertanyaan Penelitian ... 4
1.3 Hipotesis Penelitian ... 4
1.4 Tujuan Penelitian ... 5
1.4.1. Tujuan Umum ... 5
1.4.2. Tujuan Khusus ... 5
1.5 Manfaat Penelitian ... 5
BAB II TINJAUAN PUSTAKA ... 6
2.1 Sindroma Koroner Akut ... 6
2.2 Patogenesis Infark Miokard Akut ... 6
2.2.1 Perubahan Patologi Awal pada Infark Miokard Akut ... 7
2.2.2 Perubahan Patologi Lanjut pada Infark Miokard Akut ... 8
2.2.3 Remodeling Ventrikel Setelah Infak Miokard ... 9
2.2.3.1 Remodeling Fase Awal ... 10
2.2.3.2 Remodeling Fase Lanjut ... 11
2.3 Pengaruh Reperfusi Terhadap Perubahan Patologi ………14
2.4 Hubungan Ukuran Infark, Remodeling Ventrikel dan Prognosis Paska IMA ... 14
2.5 Kriteria EKG untuk menentukan Infark Miokard ... 18
2.6 Skor QRS Selvester untuk Memperkirakan Ukuran Infark Miokard ... 19
2.7 Penyederhanaan Skor Selvester dan Penerapannya ... 23 2.8 Hubungan Skor Selvester Yang Disederhanakan dengan
2.9 Kerangka Teori ... 30
2.10 Kerangka Konsep ... 31
BAB III METODE PENELITIAN ... 32
3.1 Desain Penelitian ... 32
3.2 Tempat dan Waktu ... 32
3.3 Populasi dan Sampel ... 32
3.4 Besar Sampel ... 32
3.5 Kriteria Inklusi dan Ekslusi ... 33
3.6 Definisi Operasional ... 33
3.7 Identifikasi Variabel ... 36
3.8 Alur Penelitian ... 37
3.9 Analisa Data ... 38
3.10 Etika Penelitian ... 39
3.11 Perkiraan Biaya ... 39
BAB IV HASIL PENELITIAN ... 40
4.1 Karakteristik Subjek Penelitian ... 40
4.2 Nilai Skor Selvester Yang Disederhanakan berdasarkan KKvM ... 43
4.3 Hubungan antara Skor QRS Awal Dengan KKvM 30 Hari Paska IMAEST ... 44
4.4 Nilai cuttoff Skor QRS Akhir terhadap KKvM dengan Kurva Receiving Operator Characteristic (ROC) ... 44
4.5 Hubungan antara Skor QRS Akhir Dengan KKvM 30 Hari Paska IMAEST ... 45
4.6 Analisis Bivariat Faktor-Faktor yang mempengaruhi KKvM ... 46
4.7 Analisis Multivariat Faktor-Faktor yang mempengaruhi KKvM ... 47
BAB V PEMBAHASAN ... 49
BAB VI PENUTUP 6.1 Kesimpulan ... 55
6.1 Saran ... 55
DAFTAR PUSTAKA ... 57
LAMPIRAN ... 65
DAFTAR GAMBAR
No. Judul Halaman
2.1 Remodeling ventrikel kiri paska infark miokard akut ... 13
2.2 Skema waktu reperfusi pada miokard yang mengalami infark …… 14
2.3 Perubahan volume akhir sitolik ventrikel kiri dan fraksi ejeksi ventrikel kiri setelah satu tahun berdasarkan ukuran infark ... 16
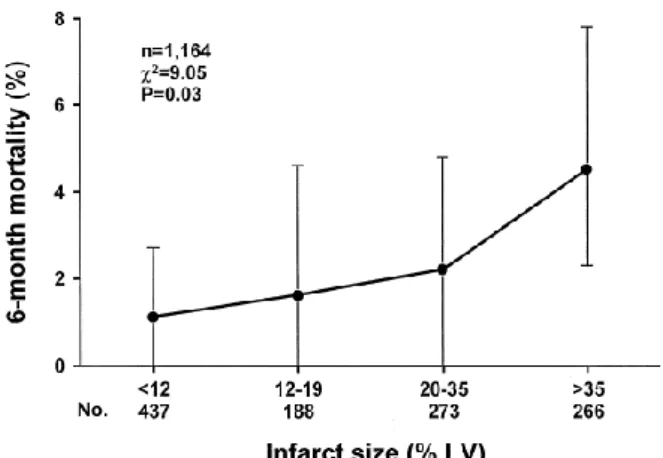
2.4 Hubungan mortalitas pasien paska IMAEST selama 6 bulan terhadap ukuran infark ... 17
2.5 Contoh simulasi infark miokard pada infark anterior ... 20
2.6 Gambaran EKG lead V6 pada simulasi komputer infark miokard ... 22
2.7.A Korelasi antara Skor Selvester denga luas infark berdasarkan hasil otopsi ... 23
2.7.B Korelasi antara estimasi fraksi ejeksi berdasarkan skor selvester dan berdasarkan angiogram ... 23
2.8 Identifikasi kompleks QRS ... 26
2.9 Diagram kerangka teori ... 30
2.10 Diagram kerangka konsep ... 31
3.1 Diagram alur penelitian ... 38
4.1 Kurva ROC skor QRS akhir terhadap KKvM 30 hari Paska IMAEST ... 45
DAFTAR TABEL
No. Judul Halaman
2.1 Lini Waktu Perubahan Patologis pada Infark Transmural ... 8 2.2 Sistem Pemberian Skor Selvester ... 22 2.3 Sistem Skor Selvester yang disederhanakan ... 24 3.1 Skor TIMI dengan presentase risiko kematian
dalam 30 hari paska IMAEST ... 34 3.2 Klasifikasi Klas Killip ... 35 4.1 Demografi dan Karakter Klinis Subjek Penelitian ... 40 4.2 Nilai Skor Selvester Yang Disedehanakan berdasarkan
KKvM 30 Hari ... 43 4.3 Nilai Skor Selvester Yang Disedehanakan berdasarkan
Kematian 30 Hari ... 43 4.4 Analisis Skor QRS Awal dan KKvM 30 Hari Paska IMAEST ... 44 4.5 Analisis Skor QRS Awal dan Kematian 30 Hari Paska IMAEST .... 44 4.6 Analisis Skor QRS Akhir dan Kematian 30 Hari Paska IMAEST ... 45 4.7 Analisis Skor QRS Akhir dan KKvM 30 Hari Paska IMAEST ... 46 4.8 Uji Bivariat Terhadap KKvM ... 47 4.9 Uji Multivariat Terhadap KKvM ... 48
DAFTAR SINGKATAN DAN LAMBANG
SINGKATAN NAMA
ACE : Angiotensin Converting Enzyme AIRE : Acute Infarction Ramipril Efficacy ANP : Atria Natriuretic Peptides
APEX-AMI : Assessment of pexelizumab in Acute Myocardial Infarction
APS : Angina Pektoris Stabil
APTS : Angina Pektoris Tidak Stabil
ATP : Adenosine Triphosphae
AUC : Area Under the Curve BNP : Brain Natriuretic Peptides
ceMRI : Contrast-enhanced magnetic resonance imaging EKA : Enzin Konversi Angiotensin
EKG : Elektrokardiografi
IKP : Intervensi Koroner Perkutan
IMA : Infark Miokard Akut
IMANEST : Infark Miokard Akut Non Elevasi ST Segmen IMAEST : Infark Miokardium Akut Elevasi ST Segmen KKvM : kejadian kardiovaskular mayor
LAFB : Left anterior fascicular block LBBB : Left Bundle Branch Block LVH : Left ventricular hypertrophy MAP : Mitogen-activated protein
Mm : millimeter
MMP : Matrix metalloprotease MRI : Magnetic Resonance Imaging
NYHA : New York Heart Association PKC : Protein kinase C
PMN : Polimorphonuclear
SOLVD : The Studies of Ventricular Dysfunction Preventiol Trial RAO : Right atrial overload
RBBB : Right bundle branch block
ROC : Receiving Operator Characteristic
RSUP HAM : Rumah Sakit Umum Pusat Haji Adam Malik SPSS : Statistical Package for the Social Science
SKA : Sindrom Koroner Akut
TGF-β1 : transforming growth factors β1) TIMI : Thrombolysis in Myocardial Infarction
VCG : Vectorcardiogram
WHO : World Health Organization
LAMBANG
n : besar sampel p : tingkat kemaknaan
α : alpha
β : beta
< : lebih kecil > : lebih besar
Zα : nilai baku alpha = 1,96 Zβ : nilai baku beta = 1,96
% : persentase
S : simpangan baku gabungan
X1-X2 = selisih rerata minimal yang dianggap bermakna
DAFTAR LAMPIRAN
Lampiran Halaman
1 Lembar Kerja Penelitian ... 65
2 Pengambilan Sampel Penelitian ... 67
3 Skor Selvster yang disederhanakan ... 68
4 Contoh perhitungan Skor Selvester Yang Disederhanakan ... 69
5 Alat Ukur Yang Dipakai Dalam Penelitian ... 71
6 Daftar Riwayat Hidup Peneliti ... 72
BAB I PENDAHULUAN
1.1 Latar Belakang
Penyakit kardiovaskular merupakan penyebab utama kematian di seluruh dunia. Pada Tahun 2013, sebanyak 17,3 juta penduduk meninggal dunia akibat penyakit kardiovaskular, meningkat sebesar 40,8% dari tahun 1990. WHO memperkirakan sebanyak 23,6 juta penduduk dunia meninggal akibat penyakit kardiovaskular pada tahun 2030. Penyakit jantung iskemik adalah kontributor utama meningkatnya angka kematian kardiovaskular (2,4 juta kematian setiap meningkatnya 5 juta kematian kardiovaskular) (Roth GA, 2015). Infark miokard akut dengan elevasi segmen ST (IMAEST) merupakan bentuk yang paling berbahaya dengan angka kematian yang paling tinggi. Selain kematian, pasien IMAEST juga meningkat risikonya untuk mengalami kejadian kardiovaskular mayor (KKvM) selama perawatan. Kejadian ini meliputi rawatan rumah sakit berulang, kejadian SKA berulang, gagal jantung, maupun aritmia (Jneid H, 2012).
Mortalitas pasien IMAEST yang dirawat dirumah sakit antara 6% dan 14%. Beberapa studi terakhir menunjukkan adanya penurunan mortalitas jangka panjang setelah kejadian IMAEST, sejalan dengan peningkatan terapi reperfusi, Intervensi Koroner Perkutan (IKP) primer, penggunanan antitrombotik terbaru dan pencegahan sekunder. Namun tetap saja angka kematiannya masih tinggi yaitu 12% pasien meninggal dunia dalam 6 bulan, dan angka ini masih lebih besar pada pasien dengan resiko yang lebih tinggi (Steg PG, 2012)
Prognosis pasien IMAEST sangat berhubungan dengan ukuran infark yang terjadi. Semakin besar ukuran infark, fungsi global ventrikel kiri akan semakin memburuk, dan semakin tinggi tingkat remodeling ventrikel kiri sehingga akan memperburuk prognosis pasien (braunwald, 2001). Penelitian yang dilakukan oleh Lonborg dkk menunjukkan bahwa pasien dengan ukuran infark ≥ 9,5% memiliki kejadian kardiovaskular yang lebih tinggi dibandingkan dengan ukuran infark< 9,5% (17% dibanding 6%) selama 807 hari follow up (Lonborg J,
2013). Sementara penelitian yang dilakukan oleh Hombach dkk menunjukkan bahwa pasien IMA dengan ukuran infark yang lebih luas memiliki ukuran volume akhir sistolik ventrikel kiri dan volume akhir diastolik ventrikel kiri yang lebih besar dan terjadi penurunan fraksi ejeksi ventrikel kiri pada baseline maupun setelah follow up baik pada infark anterior ataupun non-anterior (Hombach V, 2005). Dari 2 studi yang lebih kecil yaitu studi single centre terhadap 274 pasien dan studi multi-centre terhadap 249 pasien menunjukkan bahwa ukuran infark setelah IMA merupakan indikator prognosis yang lebih superior dibandingkan dengan fraksi ejeksi dan indeks volume akhir sistolik ventrikel (Burns RJ, 2002; Miller TD, 1995; Hodge DO, 1998). Oleh karena itu, ukuran infark merupakan suatu indikator prognosis yang sangat berguna dan dapat membantu menentukan strategi pencegahan sekunder pada pasien yang mengalami IMA (Van de werf , 2008).
Saat ini terdapat beberapa modalitas yang tersedia untuk menentukan ukuran luas infark miokard. Diantaranya adalah elektrokardiografi, biomarker jantung dan ekokardiografi yang secara tidak langsung dapat menentukan luas kerusakan otot jantung. Sedangkan pencitraan sidik perfusi dan contrast-enhanced magnetic resonance imaging (ceMRI) dapat mengukur luas infark miokard secara langsung. Elektrokardiografi (EKG) memiliki beberapa keuntungan dibandingkan modalitas yang lain, yaitu tidak invasif, murah, dapat diulang dan sangat umum tersedia sehingga dapat digunakan di fasilitas kesehatan dengan sarana dan prasarana yang terbatas (Geerse DA, 2009; Ideker RE, 1982).
Penentuan luas infark miokard melalui EKG dapat dilakukan dengan sistem pemberian skor. Telah banyak dikembangkan sistem pemberian skor yang mencoba memperkirakan luas kerusakan pada miokard. Selvester dkk telah mengembangkan suatu sistem skor berdasarkan simulasi komputer dari perubahan aktivasi jantung normal yang disebabkan oleh infark. Sistem skor ini menggunakan 54 kriteria/32 poin untuk memperkirakan ukuran miokard yang mengalami infark berdasarkan kriteria QRS pada sadapan aVL, I, II, aVF dan V1 hingga V6. Setiap poin dikembangkan untuk menggambarkan infark sebesar 3%
dari semua massa ventrikel kiri (Selvester RH, 1985). Dengan menggunakan modifikasi metode ini, Wagner dkk menyederhanakan kriteria Selvester untuk
memperkirakan ukuran infark miokard dari EKG 12 sadapan standar. Mereka menemukan bahwa sistem skor QRS dengan 29 poin memiliki spesifitas 98%
pada populasi untuk tidak menderita infark miokard (Wagner GS, 1982). Sistem skor QRS selvester yang dimodifikasi dan disederhanakan ini telah dibuktikan lebih baik dibandingkan sistem skor yang lain dalam menentukan ukaran infark miokard pada ventrikel kiri (Geerse DA, 2009; Pahlm US, 1998)
Skor QRS selvester juga memiliki nilai prognostik yang akurat pada pasien yang mengalami IMA. Penelitian oleh Simindokht dkk menemukan bahwa skor QRS yang dinilai pada saat pasien masuk unit gawat darurat berhubungan dengan angka kematian saat rawatan di rumah sakit (Moshar S, 2013). Penelitian yang dilakukan oleh Masami dkk juga menemukan bahwa pasien IMA dengan skor QRS yang lebih tinggi pada saat masuk rumah sakit yang dilakukan terapi reperfusi dalam waktu 6 jam setelah onset, memiliki aliran TIMI yang lebih rendah (Kosuge M, 2010). Penelitian yang dilakukan oleh Shiomi dkk pada 2.607 pasien IMAEST menemukan bahwa skor QRS yang lebih tinggi sebelum dilakukannya IKP primer memiliki ukuran infark yang lebih besar dan angka kematian setelah 5 tahun yang lebih tinggi (Shiomi H, 2017). Michael C dkk menunjukkan luas infark yang diperkirakan berdasarkan skor Selvester yang dinilai pada saat pasien pulang dari rumah sakit merupakan prediktor independen terhadap KKvM yang buruk termasuk kematian, gagal jantung, dan syok kardiogenik setelah 90 hari follow up pada pasien dengan IMAEST yang dilakukan intervensi koroner perkutan (Tjandrawidjaja MC, 2010). Sementara Huseyin U dkk menyatakan bahwa skor QRS yang tinggi merupakan prediktor independen kejadian kardiovaskular mayor (KKvM) setelah 30 hari pada pasien IMAEST yang dilakukan IKP primer (Uyarel H, 2006).
Studi Sebelumnya memang telah menunjukkan kemampuan Skor Selvester sebagai prediktor KKvM pada IMAEST. Namun studi tersebut dilakukaan pada pasien IMAEST dengan reperfusi dini. Meskipun terapi reperfusi dini (baik secara farmakologis maupun secara mekanik) sangat direkomendasikan dalam penanganan IMAEST, sekitar 21-46% penderita IMAEST pada beberapa studi justru tidak mendapatkannya. Onset yang terlambat, keterbatasan akses serta adanya kontraindikasi absolut merupakan penyebab yang paling sering dijumpai.
Sehingga terapi fibrinolitik maupun IKP primer tidak dapat dilakukan (Cohen M, 2010; Eagle KA, 2002). Penelitian yang dilakukan oleh Brahmana di RSUP HAM sebelumnya melaporkan hanya 8,2% pasien IMAEST yang mendapat terapi reperfusi dini (Brahmana T, 2013). Selain itu, sampai penelitian ini dilakukan belum ada suatu studi yang meneliti hubungan Skor Selvester yang disederhanakan ini dengan KKvM dalam 30 hari khusus pada pasien IMAEST tanpa reperfusi dini.
Berdasarkan hal-hal tersebut, penelitian ini bertujuan untuk menguji apakah terdapat hubungan antara Skor QRS Selvester yang disederhanakan dengan KKvM dalam 30 hari pada pasien IMAEST, serta apakah dapat digunakan sebagai salah satu parameter sederhana untuk menstratifikasi pasien yang berisiko mengalami KKvM.
1.2 Pertanyaan Penelitian
Berdasarkan uraian dalam latar belakang di atas, maka pertanyaan penelitian ini adalah: Apakah terdapat hubungan antara luas infark miokard yang dinilai berdasarkan Skor Selvester yang disederhanakan dengan KKvM dalam 30 hari pada pasien IMAEST tanpa reperfusi dini?
1.3 Hipotesis Penelitian
Hipotesis penelitian ini adalah: pasien-pasien yang memiliki Skor Selvester yang disederhanakan yang lebih tinggi memiliki angka KKvM dalam 30 hari yang lebih besar dibandingkan dengan pasien-pasien yang memiliki Skor Selvester yang disederhanakan yang lebih rendah pada pasien IMAEST tanpa reperfusi dini.
1.4. Tujuan Penelitian 1.4.1. Tujuan umum
Penelitian ini bertujuan untuk mengetahui apakah nilai Skor Selvester yang disederhanakan dapat digunakan sebagai prediktor KKvM dalam 30 hari pada pasien IMAEST tanpa reperfusi dini.
1.4.2. Tujuan Khusus
Tujuan khusus penelitian ini adalah :
1. Untuk mengetahui kemampuan Skor Selvester yang disederhanakan dalam mempediksi KKvM dalam 30 hari pada pasien IMAEST tanpa reperfusi dini.
2. Untuk mengetahui nilai cuttoff Skor Selvester yang disederhanakan yang dapat digunakan sebagai prediktor KKvM dalam 30 hari pada pasien IMAEST tanpa reperfusi dini.
3. Untuk mengetahui perbandingan Skor Selvester yang disederhanakan dengan prediktor lain yang mungkin berhubungan seperti skor TIMI dan parameter ekokardiografi.
1.5 Manfaat Penelitian
Hasil penelitian ini diharapkan memberikan manfaat sebagai berikut:
1. Kepada tenaga kesehatan: memberikan bukti ilmiah tentang nilai Skor Selvester yang dapat digunakan sebagai prediktor KKvM dalam 30 hari pada pasien IMAEST tanpa reperfusi dini.
2. Kepada masyarakat: Memberikan informasi prognostik kepada pasien IMAEST melalui modalitas yang cukup terjangkau, dalam mengidentifikasi pasien-pasien IMAEST yang memiliki resiko tinggi KKvM.
BAB II
TINJAUAN PUSTAKA
2.1 Sindroma Koroner Akut
SKA adalah istilah yang digunakan untuk mendeskripsikan simptom yang disebabkan oleh iskemik miokard. SKA yang menyebabkan nekrosis miokardium disebut infark miokard. Manifestasi SKA secara klinis dapat sebagai APTS, IMANEST atau IMAEST (Thygesen, 2012).
Diagnosis IMAEST akut ditegakkan apabila dijumpai kriteria berikut, yaitu; adanya nyeri dada khas angina (durasi nyeri lebih dari 20 menit, tidak berkurang dengan istirahat atau nitrat, nyeri dapat menjalar ke leher, rahang bawah atau lengan kiri, dapat disertai dengan gejala aktivasi sistem saraf otonom seperti mual, muntah atau keringat dingin), dijumpai elevasi segmen ST yang persisten atau adanya LBBB yang dianggap baru, peningkatan kadar enzim jantung akibat nekrosis miokard (CKMB dan troponin), serta dijumpai abnormalitas gerakan dinding regional yang baru pada pemeriksaan ekokardiografi (Steg PG, 2012).
2.2 Patogenesis Infark Miokard Akut
Oklusi pada arteri koroner yang berlangsung lama akan menyebabkan kerusakan otot jantung yang menetap dan kematian otot atau nekrosis. Infark transmural melibatkan seluruh ketebalan miokard yang disebabkan oleh oklusi total pada sebuah arteri koroner epikardial. Luas jaringan miokard yang mengalami infark ditentukan oleh : massa miokard yang mendapat perfusi dari pembuluh darah yang mengalami oklusi, durasi dan keparahan gangguan aliran darah koroner yang terjadi, kebutuhan oksigen miokard yang mengalami gangguan , pembuluh darah kolateral dan respon jaringan terhadap iskemia.
Perubahan patologis yang terjadi selama infark miokard dibagi dalam dua tahap, yaitu tahap awal yang terjadi segera setelah terjadinya infark dan tahap lanjut
yang merupakan bagian dari proses penyembuhan miokard dan remodeling (Rhee JW, 2011).
2.2.1 Perubahan Patologi Awal pada Infark Miokard Akut
Menurunnya konsentrasi oksigen pada miokard yang mendapat aliran dari pembuluh darah koroner yang mengalami oklusi akan menyebabkan pergeseran metabolisme aerob menjadi anaerob. Produksi fosfat berenergi tinggi akan menurun secara dramatis dan glikolisis anaerob akan menyebabkan penumpukan asam laktat yang menyebabkan penurunan PH, yang menyebabkan denaturasi protein dan kematian sel. Penurunan produksi fosfat berenergi tinggi seperti adenosine triphosphate (ATP) selanjutnya juga mempengaruhi kanal Na+ - K+ - ATPase transmembran yang menyebabkan peningkatan konsentrasi Na+ intrasel dan K+ ekstrasel. Meningkatnya konsentrasi Na+ intrasel akan menyebabkan edema sel dan kebocoran membran. Penumpukan kalsium intrasel pada miokard yang mengalami kerusakan diduga berperan dalam proses akhir kerusakan sel melalui aktifasi enzim-enzim degradasi lipase dan protease (Rhee JW, 2011).
Tanpa adanya intervensi, injuri sel yang menetap akan terjadi dalam 20 – 40 menit setelah terjadinya oklusi, dan ditandai oleh adanya defek pada membran. Enzim-enzim proteolitik akan keluar melalui membran sel yang rusak dan akan merusak miokard yang bersebelahan, dan akan melepaskan makromolekul tertentu dalam sirkulasi yang dapat berperan sebagai penanda klinis dari infark akut. Edema miokard terjadi setelah 4 – 12 jam, dengan adanya peningkatan permeabilitas vaskular dan peningkatan tekanan onkotik interstisial (oleh kartena kebocoran protein intrasel). Perubahan patologis awal dari injuri sel yang irreversible adalah adanya gambaran serat otot jantung yang bergelombang (wavy myofibers) yang merupakan gambaran edema intrasel yang memisahkan sel miokard yang mengalami defek, yang mengalami penarikan oleh sel-sel disekitarnya. Respon inflamasi akut yang ditandai dengan infiltrasi netrofil dimulai setelah 4 jam dan memperburuk proses kerusakan sel. Setelah 18 – 24 jam terjadi proses Nekrosis koagulasi (coagulation necrosis) yang ditandai dengan adanya pyknotic nuclei dan sitoplasma eosinophilic. Setelah 2 – 4 hari proses
nekrosis koagulasi total terjadi pada seluruh miokard yang mengalami defek (Rhee JW, 2011).
2.2.2 Perubahan Patologi Lanjut pada Infark Miokard Akut
Perubahan patologis selanjutnya pada perjalanan infrark miokard akut meliputi bersihan jaringan nekrotik miokard dan pembentukan kolagen untuk membentuk jaringan parut. Injuri miosit yang ireversibel tidak mengalami regenerasi, namun sel tersebut digantikan jaringan ikat. Invasi makrofag pada miokard yang mengalami inflamasi terjadi segera setelah infiltrasi netrofil dan membuang jaringan nekrotik. Periode resobsi jaringan ini dinamakan yellow softening. Bersihan fagosit, berkombinasi dengan dilatasi dan penipisan jaringan miokard yang mengalami infark menyebabkan kelemahan struktural dinding ventrikel yang dapat mencetuskan ruptur ventrikel pada tahap ini. Proses ini diikuti dengan fibrosis jaringan dan pembentukan jaringan parut telah lengkap terjadi pada minggu ke-7 setelah infark. Perubahan yang terjadi selama infark miokard akut ini ditunjukkan pada tabel 2.1. (Rhee JW 2011).
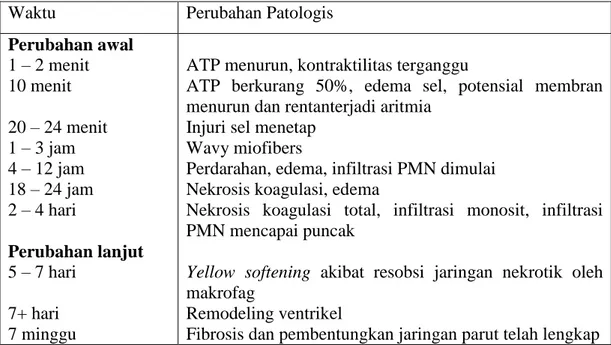
Tabel 2.1 Lini Waktu Perubahan Patologis pada Infark Transmural
Waktu Perubahan Patologis
Perubahan awal 1 – 2 menit 10 menit 20 – 24 menit 1 – 3 jam 4 – 12 jam 18 – 24 jam 2 – 4 hari
Perubahan lanjut 5 – 7 hari
7+ hari 7 minggu
ATP menurun, kontraktilitas terganggu
ATP berkurang 50%, edema sel, potensial membran menurun dan rentanterjadi aritmia
Injuri sel menetap Wavy miofibers
Perdarahan, edema, infiltrasi PMN dimulai Nekrosis koagulasi, edema
Nekrosis koagulasi total, infiltrasi monosit, infiltrasi PMN mencapai puncak
Yellow softening akibat resobsi jaringan nekrotik oleh makrofag
Remodeling ventrikel
Fibrosis dan pembentungkan jaringan parut telah lengkap
2.2.3 Remodeling Ventrikel Setelah Infark Miokard
Gagal jantung yang disebabkan oleh infark miokard masih menjadi penyebab utama morbiditas dan mortalitas pasien paska IMA. Hasil studi AIRE (Acute Infarction Ramipril Efficacy) melaporkan kejadian gagal jantung kongestif paska IMA sebesar 14% sedangkan studi SOLVD (The Studies of Ventricular Dysfunction Preventiol Trial) mendapatkan angka kejadian hampir 80%
(Erhardt L, 1997)
Walaupun penyebab terjadinya gagal jantung setelah infark miokard sangat kompleks, ukuran infark merupakan salah satu faktor penentu terjadinya gagal jantung. Suatu studi pada hewan percobaan menunjukkan bahwa ukuran infark berdasarkan hasil pencitraan MRI berhubungan dengan volume akhir sistolik ventrikel kiri dan fraksi ejeksi venrikel kiri. Studi yang lain juga menunjukkan hasil yang sama dimana ukuran infark memiliki hubungan linier dengan ukuran dan fraksi ejeksi ventrikel kiri, dan ukuran infark juga dapat memprediksi volume akhir sistolik ventrikel kiri (French BA, 2007).
Patofisiologi terjadinya gagal jantung paska infark miokard akut meliputi proses remodeling dan dilatasi ventrikel kiri, abnormalitas neurohormonal terutama sistem renin angiotensin aldosterone, dan aktivitas simpato adrenergik.
Remodeling ventrikel kiri adalah proses perubahan ukuran, bentuk dan fungsi ventrikel kiri yang diregulasi oleh faktor mekanikal, neurohormonal dan genetik (Sutton MGS, 2000). Proses remodeling setelah infark miokard akut secara klinis ditandai oleh peningkatan volume ventrikel kiri. Dilatasi ventrikel kiri diawali oleh proses ekspansi infark yang kemudian diikuti oleh proses hipertrofi. Proses ini akan mengakibatkan perburukan fungsi ventrikel kiri sehingga akan muncul tanda dan gejala gagal jantung dikemudian hari. Luaran klinis setelah infark miokard ditentukan oleh ukuran dan geometri ventrikel kiri yang diakibatkan proses remodeling ventrikel kiri (Zornoff LAM, 2009).
Salah satu faktor yang menentukan derajat remodeling ventrikel adalah ukuran infark. Walaupun remodeling dapat terjadi pada semua ukuran infark, namun pada umumnya terjadi pada ukuran infark yang luas. Sekurang-kurangnya ukuran infark sebesar 16%-20% dibutuhkan untuk terjadinya proses remodeling (Zornoff LAM, 2009). Reperfusi yang dilakukan selama periode dimana miokard
masih dapat diselamatkan dapat mengurangi ukuran infark dan berhubungan dengan perbaikan performa ventrikel (Pfeffer MA, 1990).
Berdasarkan waktu, proses remodeling paska infark dibagi menjadi dua fase yaitu fase awal (dalam 72 jam) dan fase lanjut setelah 72 jam. Fase awal melibatkan perluasan daerah infark (infark expansion), yang dapat mencetuskan terjadinya ruptur ventrikel dan terbentuknya aneurisma. Remodeling fase lanjut melibatkan ventrikel secara keseluruhan dan berhubungan dengan dilatasi, perubahan bentuk geometri ventrikel dan hipertrofi (Sutton MGS, 2000).
2.2.3.1 Remodeling Fase Awal
Pada fase awal remodeling paska infark miokard, terjadi ekspansi daerah infark. Kematian miosit akan diikuti oleh infiltrasi netrofil. Matrix metalloprotease (MMP) dan serin protease yang dilepaskan oleh netrofil akan menyebabkan degradasi kolagen intermiosit sehingga antar miosit akan saling terlepas (myocite sllipage). Proses ini menyebabkan dilatasi dan penipisan dinding ventrikel yang mengalami infark, yang selanjutnya menyebabkan peningkatan tekanan dinding (wall stress) sistolik dan diastolik ventrikel kiri. Peningkatan tekanan dinding ventrikel merupakan stimulus kuat terjadinya hipertrofi yang diperantarai oleh reseptor mekanik dan diteruskan oleh sinyal intrasel, melalui pelepasan angiotensin II. Angiotensin II akan meningkatkan pembentukan unit kontraktil miokard yang memulai proses hipertrofi (Sutton MGS, 2000).
Kematian miosit pada fase awal remodeling juga akan menyebabkan curah jantung menurun. Perubahan hemodinamik sirkulasi akibat penurunan curah jantung mencetuskan peningkatan aktifitas sistem saraf simpatis melalui sintesa katekolamin oleh kelenjar adrenal dan pelepasan katekolamin dari ujung saraf simpatis, aktivasi sitem renin-angiotensin-aldosteron dan stimulasi produksi atrial dan brain natriuretic peptides (ANP dan BNP). Stimulasi simpatis menyebabkan hiperkinetik daerah miokard yang tidak mengalami infark sehingga dapat mengkompensasai perburukan sirkulasi untuk sementara. Sebagai tambahan, natriuretic peptides menurunkan volume intravaskular dan resistensi vaskular sistemik, menormalkan pengisian ventrikel dan meningkatkan fungsi pompa ventrikel kiri untuk sementara (Sutton MGS, 2000).
2.2.3.2 Remodeling Fase Lanjut
Fase lanjut remodeling paska infark miokard meliputi hipertrofi miosit dan pembentukan jaringan parut (fibrosis) untuk menstabilkan tekanan dinding ventrikel yang meningkat dan mencegah deformitas yang berkelanjutan.
Hipertrofi sebenarnya merupakan proses respon adaptasi dalam remodeling paska infark, dengan cara mencegah peningkatan afterload, mencegah progresifitas dilatasi dan menstabilkan fungsi kontraksi ventrikel kiri. Hipertrofi distimuli oleh aktivasi neurohormonal, peregangan miokardium, dan aktivasi sistem renin-angiotensin local. Hipertrofi diperantarai oleh kaskade protein kinase C (PKC). Penurunan curah jantung paska infark miokard mengaktifasi sistem saraf simpatis melalui sintesa katekolamin oleh kelenjar adrenal dan pelepasan katekolamin dari ujung saraf simpatis, aktivasi sitem renin-angiotensin-aldosteron dan sekresi natriuretic peptides. Norepinefrin terlibat dalam proses hipertrofi baik secara langsung maupun tidak langsung. Stimulasi reseptor α1 menyebabkan hipertrofi melalui jalur sinyal Gαq. Aktifasi reseptor β1 pada apparatus jugstaglomerular mencetuskan pelepasan renin, yang akan meningkatkan produksi angiotensin II. Sebagai tambahan angiotensin II dan norepinefrin dapat meningkatkan pelepasan ET-1, yang juga merupakan stimulus terjadinya hipertrofi miokard. Reseptor norepinefrin, ET-1, dan angiotensin II melalui protein Gq menstimuli pembentukan dan pengaktifan protein kinase C (PKC) , faktor-faktor pertumbuhan (growth factors), dan mitogen-activated protein (MAP) kinase. Faktor – factor ini bersama-sama akan menyebabkan hipertrofi miosit (Sutton MGS, 2000).
Terjadinya proses fibrosis pada fase lanjut remodeling dipicu oleh transforming growth factors β1 (TGF-β1) yang dilepaskan oleh miosit yang mengalami injuri. TGF β1 memicu kemotaksis makrofag dan fibroblast dan proliferasi fibroblast. Makrofag yang mengalami aktivasi mengalami transformasi genetik untuk mengekspresikan gen Angiotensin Converting Enzyme (ACE), yang berperan dalam produksi angiotensin II local. TGF β1 juga menyebabkan transformasi fibroblast menjadi miofibroblas yang memiliki reseptor untuk angiotensin II, ET-1, dan TGF β1. Selanjutnya, miofibroblas dengan beberapa
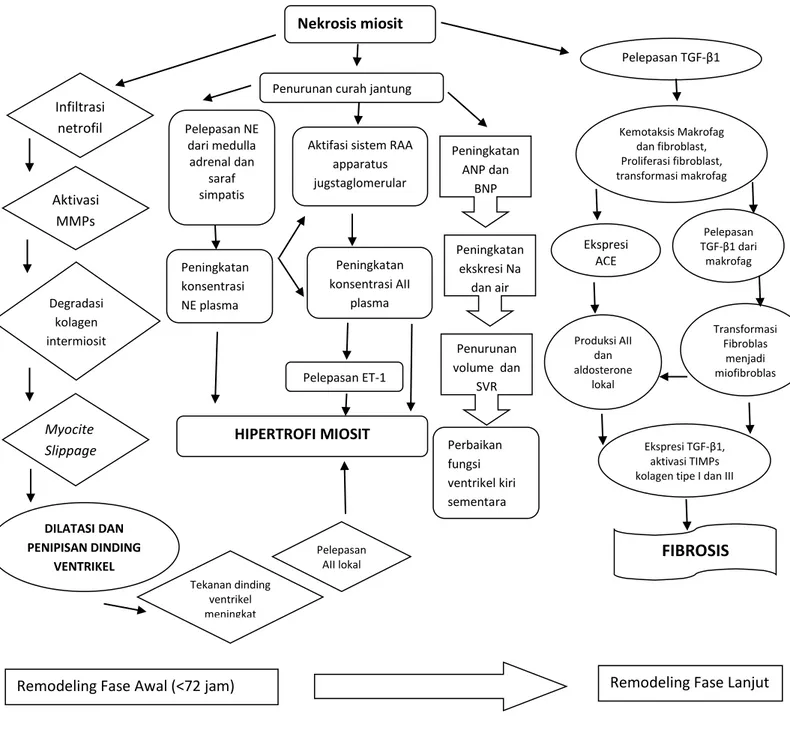
faktor seperti angiotensin II dan aldosterone akan mensintesa kolagen tipe I dan III sehingga terjadilah proses fibrosis. Pembentukan kolagen tipe I dan III ini terjadi terutama pada daerah infark, walaupun dapat juga terjadi pada miokard yang tidak mengalami infark. Kolagen tipe III meningkat pada hari ke-2 dan tetap meningkat selam 3 minggu. Tipe I kolagen meningkat pada hari ke-4 dan tetap mengalami peningkatan sampai 3 bulan. Kolagen terdeteksi melalui mikroskop pada hari ke-7 dan meningkat secara signifikan , sehingga pada hari ke-28 seluruh miosit yang mengalami nekrosis sudah digantikan oleh jaringan fibrotik. Adapun drajat fibrosis selanjutnya akan menentukan manefestasi dan progresi gagal jantung. Gambar 2.1 menunjukkan fase awal dan lanjut remodeling paska kejadian infark miokard (Sutton MGS, 2000).
Gambar 2.1 Remodeling ventrikel kiri paska infark miokard akut. MMPs, Matrix metalloproteinase; NE, nerepinefrin; AII, angiotensin II; RAA, renin-angiotensin- aldosteron; SVR, systemic vascular resistance (Sutton MGS, 2000).
Nekrosis miosit
Infiltrasi netrofil
Aktivasi MMPs
Degradasi kolagen intermiosit
Myocite Slippage
DILATASI DAN PENIPISAN DINDING
VENTRIKEL
Penurunan curah jantung
Pelepasan NE dari medulla adrenal dan
saraf simpatis
Peningkatan konsentrasi NE plasma
HIPERTROFI MIOSIT
Aktifasi sistem RAA apparatus jugstaglomerular
Peningkatan konsentrasi AII
plasma
Pelepasan ET-1
Peningkatan ANP dan
BNP
Peningkatan ekskresi Na
dan air
Penurunan volume dan
SVR
Perbaikan fungsi ventrikel kiri sementara
Pelepasan TGF-β1
Kemotaksis Makrofag dan fibroblast, Proliferasi fibroblast, transformasi makrofag
Ekspresi ACE
Produksi AII dan aldosterone
lokal
Ekspresi TGF-β1, aktivasi TIMPs kolagen tipe I dan III
FIBROSIS
Pelepasan TGF-β1 dari
makrofag
Transformasi Fibroblas
menjadi miofibroblas
Tekanan dinding ventrikel meningkat
Pelepasan AII lokal
Remodeling Fase Awal (<72 jam) Remodeling Fase Lanjut
2.3 Pengaruh Reperfusi Terhadap Perubahan Patologi
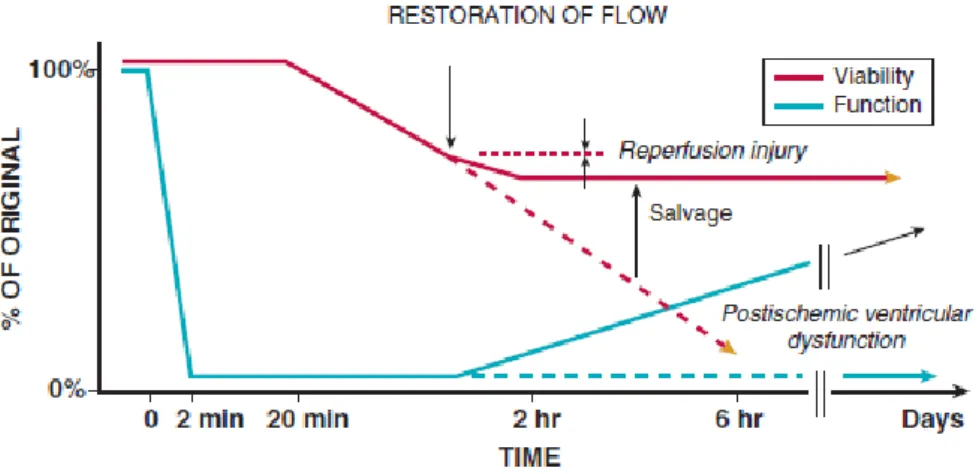
Apabila tindakan reperfusi dilakukan sesegera mungkin pada miokard yang sedang mengalami proses evolusi dari iskemia menuju infark, yaitu dalam 15 – 20 menit, akan berhasil mencegah perkembangan menjadi nekrosis. Setelah fase ini, jumlah miokard yang dapat diselamatkan (area yang beresiko) secara langsung tergantung dari total waktu terjadinya oklusi total arteri koroner, tingkat konsumsi oksigen, dan aliran darah kolateral. Infark yang mengalami reperfusi secara khas memiliki gambaran gabungan antara nekrosis, perdarahan pada miokard yang mengalami injuri irreversible, coagulation necrosis with contraction band, dan susunan sel yang mengalami distorsi pada daerah yang direperfusi (Braunwald E, 2012).
Reperfusi pada daerah infark mempercepat pelepasan protein inraseluler, oleh karenanya menghasilkan kadar puncak substansi-substansi yang lebih cepat dan lebih besar seperti CK-MB dan Troponin T dan I yang spesifik untuk jantung (Braunwald E, 2012).
Gambar 2.2 Skema waktu reperfusi pada miokard yang mengalami infark. Sekitar 30 menit setelah infark, injuri miokard berpotensi untuk diselamtkan. Setelah 6 jam , injuri miokard menyebabkan nekrosis yang irreversible (Braunwald E, 2012).
2.4 Hubungan Ukuran Infark, Remodeling Ventrikel, dan Prognosis Setelah IMA
Remodeling ventrikel, merupakan salah satu penentu ketahanan hidup pasien yang selamat paska mengalami serangan infark miokard, dan telah dihubungkan dengan luaran klinis pada beberapa studi mengenai gagal jantung
(French BA, 2007). Kostuk dkk melaporkan peningkatan mortalitas sebanyak tiga kali (24% dibanding 8%) pada pasien yang mengalami peningkatan ukuran jantung kiri berdasarkan hasil foto rontgen toraks dibandingkan dengan pasien dengan ukuran jantung yang normal. Selanjutnya, pada follow up selama satu tahun, 32% pasien dengan pembesaran jantung, dibandingkan hanya 2% pada pasien dengan ukuran jantung yang normal, mengalami simtom gagal jantung kelas III New York Heart Association (NYHA) dan angina (Kostuk WJ dkk, 1973).
White dkk menemukan angka ketahanan hidup paska infark miokard akut berhubungan terbalik dengan volume akhir diastolik dan sistolik ventrikel dan berhubungan dengan fraksi ejeksi ventrikel kiri. Prediktor kematian terkuat adalah volume akhir sistolik, dimana peningkatan progresif sebesar 25 ml dari volume akhir sistolik ventrikel kiri meningkatkan resiko kematian relatif secara eksponensial. Pasien yang selamat paska infark miokard dengan volume akhir sistolik sebesar 75ml memiliki resiko relatif kematian sebesar 2,5 kali, sedangkan pasien dengan volume akhir sistolik sebesar 125 ml resiko relatif kematian meningkat sebesar 5 kali, dibandingkan pasien dengan volume akhir sistolik normal (30 – 55 ml). Bahkan analisis multivariat menunjukkan volume ventrikel merupakan indikator yang kuat terhadap ketahanan hidup, lebih kuat dibandingkan keparahan lesi koroner (White HD, 1987; Hammermister KE, 1979) Apabila dihubungkan dengan ukuran infark, pada beberapa studi didapatkan bahwa volume ventrikel kiri paska infark miokard berhubungan dengan ukuran infark. Pada studi hewan percobaan, Pfeffer dkk menunjukkan hubungan linier antara ukuran infark dan volume ventrikel kiri (Pfeffer MA, 1985;
Pfeffer MA, 1979). Chareonthaitawee dkk juga menunjukkan adanya hubungan yang kuat antara ukuran infark yang diperoleh dari pencitraan sidik miokard technetium-99m sestamibi terhadap volume ventrikel kiri (r = 0,43 saat pulang rawatan rumah sakit menjadi r = 0,80 setelah 1 tahun) dan fraksi ejeksi ( r = -0,39 saat pulang rawatan menjadi r = -0,84 setelah 1 tahun follow up). Walaupun pada periode awal setelah onset infark, dimana proses remodeling baru dimulai, belum dijumpai korelasi yang bermakna (Chareonthaitawee P, 1995). Sementara penelitian yang dilakukan oleh Hombach dkk menunjukkan bahwa pasien
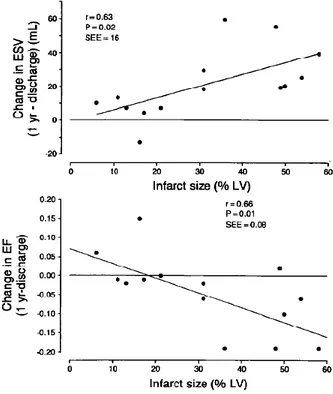
IMAEST dengan ukuran infark yang lebih luas ( > 12 %) memiliki ukuran volume akhir sistolik ventrikel kiri dan volume akhir diastolik ventrikel kiri yang lebih besar dan terjadi penurunan fraksi ejeksi ventrikel kiri pada baseline maupun setelah follow up baik pada infark anterior ataupun non-anterior (Hombach V, 2005). Penelitian yang dilakukan oleh Christian dkk juga menemukan bahwa ukuran infark berhubungan dengan volume akhir sistolik pada saat pulang dari rumah sakit (r = 0,71; p<0,0005) dan 6 minggu follow up (r = 0,63; p<0,005), fraksi ejeksi saat pulang dari rumah sakit (r = 0,87), 6 minggu (r = -0,81) dan 1 tahun (r = -0,76) (Christian TF, 1991).
Gambar 2.3 Perubahan volume akhir sitolik ventrikel kiri (atas) dan fraksi ejeksi ventrikel kiri (bawah) setelah satu tahun berdasarkan ukuran infark. Terdapat korelasi linier yang signifikan(Chareonthaitawee P, 1995).
Ukuran infark miokard pada pasien IMAEST berhubungan dengan kejadian kardiovaskular. Penelitian yang dilakukan oleh Lonborg dkk menunjukkan bahwa pasien IMAEST dengan ukuran infark ≥ 9,5% memiliki kejadian kardiovaskular yang lebih tinggi dibandingkan dengan ukuran infark < 9,5% (17% dibanding 6%) selama 807 hari follow up (Lonborg J,
2013). Dari 2 studi yang lebih kecil: studi single centre terhadap 274 pasien dan studi multi-centre terhadap 249 pasien menunjukkan bahwa ukuran infark setelah IMA merupakan indikator prognosis yang lebih superior dibandingkan dengan fraksi ejeksi dan indeks volume akhir sistolik ventrikel (Burns RJ, 2002; Miller TD, 1995; Hodge DO 1998). Burns dkk menemukan hubungan langsung antara ukuran infark 6 – 16 hari setelah onset nyeri dada pada pasien IMAEST yang diterapi dengan trombolitik dengan mortalias selama 6 bulan (χ2 = 9,05; p = 0,03).
Kelompok resiko tinggi adalah kelompok dengan ukuran infak > 35% dengan angka mortalitas 4,5%. Mereka menyimpulkan bahwa ukuran infark merupakan prediktor mortalitas penting baik pada infark anterior maupun non-anterior (Burns RJ dkk, 2002). Sementra Miller dkk juga menemukan hubungan yang signifikan antara ukuran infark dan angka kematian. Mortalitas selama 2 tahun sebesar 7%
untuk pasien dengan ukuran infark ≥ 12% dan 0% untuk pasien dengan ukuran infark < 12% pada 274 pasien dengan IMAEST, dimana 45% pasien dengan infark anterior, 46% dengan infark inferior dan 14% pasien tidak mendapat terapi reperfusi. Ukuran infark diperoleh pada saat pasien pulang dari rumah sakit dengan sidik perfusi miokard menggunakan99mTc-sestamibi (Miller TD, 1995).
Gambar 2.4 Hubungan mortalitas pasien paska IMAEST selama 6 bulan terhadap ukuran infark (Burns RJ, 2002).
2.5 Kriteria EKG Untuk Menentukan Infark Miokard
Telah diketahui secara umum bahwa prognosis paska infark miokard berhubungan dengan ukuran ventrikel kiri yang mengalami infark. Oleh karena itu sangat diperlukan metode yang dapat diandalkan untuk memperkirakan luas infark, baik yang akut atau yang telah terjadi sebelumnya. Selama lebih dari 80 tahun, elektrokardiogram (EKG) 12 sadapan telah digunakan sebagai standar untuk menentukan diagnosis dan lokasi infark miokard. Oleh karena pemeriksaan ini murah, tidak invasif, mudah diulang dan dapat dijumpai di rumah sakit besar maupun di praktek-praktek dokter, maka sangatlah penting untuk mengetahui sejauh mana EKG dapat digunakan untuk memperkirakan ukuran infark miokard (Geerse DA, 2009).
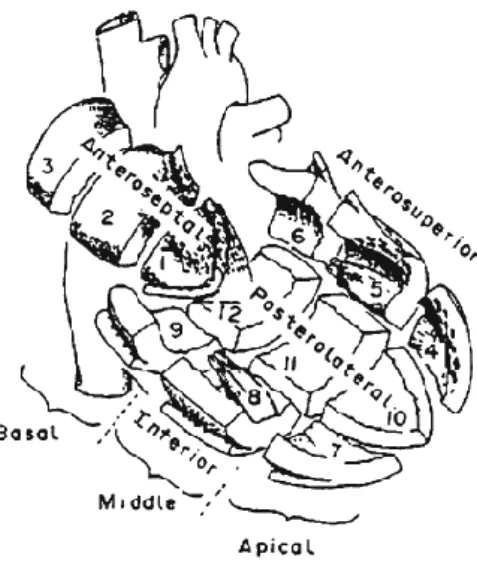
Infark miokard merupakan proses hilangnya aktifitas elektrik miokard yang disebabkan oleh nekrosis lokal atau regional. Setiap regio ventrikel diwakilkan oleh bagian tertentu pada gelombang QRS berdasarkan urutan aktivasi ventrikel. Pada keadaan normal, aktivasi ventrikel kiri dimulai dari septal dan dinding superior dan inferior ventrikel. Infark pada daerah ini akan menyebabkan abnormalitas pada 30 – 40 ms awal gelombang QRS. Regio posterolateral, bersebrangan dengan daerah septal diaktivasi antara 30 – 50 ms, infark pada daerah ini akan menyebabkan kelainan pada bagian tengah gelombang QRS.
Sedangkan basal ventrikel kiri diaktivasi pada tengah akhir gelombang QRS, sehingga infark pada daerah tersebut akan menyebabkan abnormalitas setelah 40 ms pada gelombang QRS. Dapat disimpulakan bahwa, perubahan EKG yang terjadi pada infark miokard ditentukan oleh lokasi infark yang mewakili gelombang QRS berdasarkan urutan aktivasinya. (Selvester RH, 2011).
Pada tahun 1930an telah ditegakkan kriteria EKG untuk mendiagnosis infark miokard berdasarkan perubahan pada awal gelombang QRS yaitu terbentuknya gelombang Q abnormal. Infark anteroseptal ditegakkan dengan dijumpainya gelombang Q pada sadapan V1-V3 dan infark inferior pada sadapan II, aVF dan III. Namun masih banyak perdebatan mengenai perubahan EKG pada infark lateral pada sadapan prekordial kiri (v4 - V6) dan sadapan I, aVL (Strauss DG, 2009). Kemudian pada tahun 1950 – 1960 berdasarkan studi-studi patologi, ditemukan bahwa kriteria klasik EKG untuk mendiagnosis adanya infark
miokard, yang hanya berdasarkan perubahan pada awal gelombang QRS memiliki sensitifitas yang rendah. Data tersebut menyatakan bahwa 40% - 50% dari semua infark dengan ukuran 2 cm atau lebih tidak berhubungan dengan kriteria klasik tersebut (Zinn WJ, 1950; Jhonson WJ, 1959; Woods JD 1963). Hal ini disebabkan karena 15% infark terbatas pada bagian basal miokard dan dinding posterolateral, yang teraktivasi pada bagian tengah dan akhir gelombang QRS, sehingga tidak menyebabkan perubahan pada awal gelombang dan tidak menyebabkan terbentuknya gelombang Q abnormal. Kemudian, 20% infark memiliki ukuran yang lebih kecil (2-3 cm) dan yang melibatkan hanya 10% dari ventrikel kiri, menunjukkan perubahan EKG pada bagian tengah atau akhir gelombang QRS, seperti takik pada gelombang QRS, penurunan amplitudo gelombang R, atau abnormalitas rasio R/S atau R/Q (Zinn WJ, 1950; Jhonson WJ, 1959; Woods JD, 1963; Selvester RH 2011). Sehingga diperlukan suatu kriteria untuk menentukan infark miokard yang memasukkan perubahan pada bagian tengah dan akhir gelombang QRS yang dapat mendeteksi infark miokard pada bagian posterolateral dan basal miokard dan infark dengan ukuran yang lebih kecil (2-3 cm) (Selvester RH, 2011).
2.6 Skor QRS Selvester untuk Memperkirakan Ukuran Infark Miokard Pada tahun 1965, Selvester dkk mengembangkan suatu model komputer digital untuk menghasilkan vectorcardiogram (VCG) yang sesuai dengan urutan depolarisasi jantung manusia, dengan membagi segmen ventrikel kiri menjadi 20 segmen dipol. Ketika depolarisasi ventrikel normal disimulasikan, model ini menghasilkan gambaran VCG yang normal. Dengan menambah kekuatan dipol yang mewakili ventrikel kiri atau ventrikel kanan, model ini juga berhasil menghasilkan VCG yang sesuai untuk kriteria hipertropi ventrikel kiri atau kanan (Selvester RH, 1967).
Berdasarkan keberhasilan model ini dalam mensimulasikan VCG normal dan hipertropi ventrikel, Selvester dan kawan – kawan melakukan simulasi infark miokard dengan mengurangi atau menghilangkan dipol yang mewakili hilangnya aktivitas listrik pada segmen miokard (Selvester RH, 1967). Kemudian dilakukan simulasi infark miokard berdasarkan lokasi dan ukuran yang berbeda pada
ventrikel sesuai dengan distribusi pembuluh darah koroner utama yaitu : anterior disamakan dengan arteri desendens anterior kiri, inferior dengan arteri desendens posterior dan posterolateral dengan arteri sirkumfleksa. Dari hasil percobaan kemudian didapati bahwa pada masing – masing sadapan EKG, ukuran perubahan QRS adalah proporsional dengan ukuran infark miokard yang disimulasikan (gambar 2.5) (Selvester RH, 2011).
Infark miokard ukuran sedang sampai besar pada lokasi- lokasi tersebut tidak hanya menimbulkan kelainan gelombang Q atau pada permulaan gelombang EKG pada sadapan yang berhubungan, tetapi juga perubahan gelombang QRS tengah dan akhir, bergantung pada bagian mana pada gelombang QRS, segmen infark tersebut teraktivasi (gambar 2.5). Infark miokard kecil sering tidak menimbulkan perubahan awal gelombang QRS tetapi menyebabkan takik (notching) pada gelombang QRS dan perubahan QRS pertengahan dan akhir (yaitu berkurangnya amplitudo R atau S dan gelombang R akhir pada sadapan V1 dan V2). Gelombang Q hanya terbentuk apabila segmen miokard yang mengalami infark terdepolarisasi pada 40ms pertama (Strauss DG, 2009; Selvester RH, 2011).
Gambar 2.5 Contoh simulasi infark miokard pada infark anterior. Program komputer mensimulasikan infark ventrikel kiri untuk menghasilkan vektokardiogram pada potongan horizontal, frontal dan sagital. EKG permukaan kemudian dihasilkan dari simulasi ini. Infark multiple dengan kombinasi ukuran yang bervariasi dapat disimulasikan melalui model ini (Selvester RH, 2011).
Kriteria untuk mendiagnosis infark miokard yang hanya berdasarkan gelombang Q abnormal memiliki sensitivitas yang rendah yaitu 55-60%.
Sensitivitas yang rendah ini disebabkan karena tidak memasukkan perubahan yang terjadi pada bagian tengah dan akhir gelombang QRS (Selvester RH dkk, 1982; Selvester RH, 2011). Berdasarkan simulasi ini kemudian dikembangkan suatu sistem skor QRS dengan menggunakan EKG untuk memperkirakan luas ukuran infark, termasuk perubahan yang terjadi pada bagian tengah dan akhir gelombang QRS, sehingga dapat dipakai untuk mendiagnosis infark miokard pada lokasi ventrikel yang teraktivasi setelah 40 ms (Selvester RH, 2011).
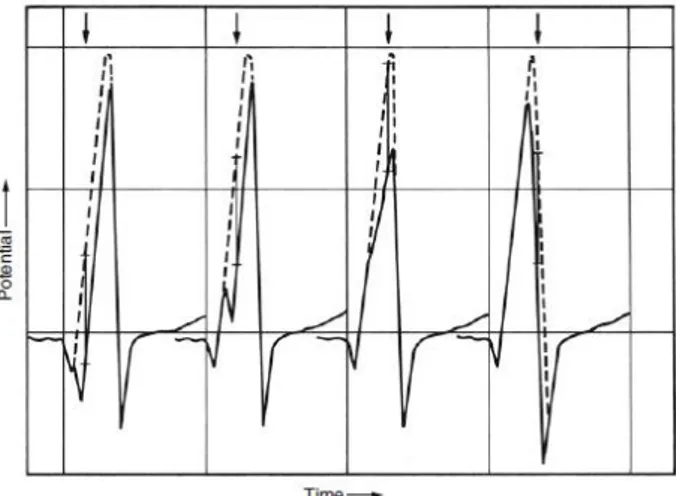
Gambar 2.6 Gambaran EKG lead V6 pada simulasi komputer infark miokard, dengan meletakkan infark ukuran 15 x 7 mm pada lokasi yang berbeda mulai dari inferior sampai posterolateral miokard. Garis putus-putus menunjukkan aktivasi normal tanpa infark. Gelombang EKG masing-masing panel didapatkan dengan menggeser lokasi infark ke arah luar,dari inferior ke posterolateral. Anak panah menunjukkan waktu saat depolarisasi miokard melewati daerah infark. Pada panel pertama dimana depolarisasi melewati daerah infark pada 15 - 40 ms pertama, terbentuk gelombang Q abnormal. Adanya cekungan dan penurunan gelombang R, perubahan rasio R/S juga merupakan tanda adanya infark, terutama pada dinding posterolateral ventrikel kiri yang teraktivasi setelah 40ms. Secara umum, infark pada segmen basal dan posterolateral miokard hanya menunjukkan perubahan pada bagian tengah dan akhir gelombang QRS, bahkan pada infark yang luas (Selvester RH, 2011)
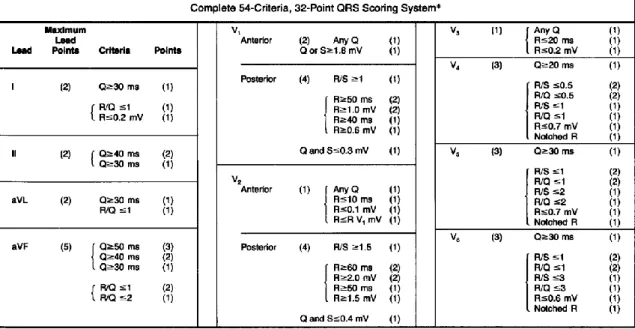
Berdasarkan pengamatan ini, pada tahun 1972 Selvester dan kawan-kawan kemudian mengembangkan sistem skor dengan 54 kriteria dengan 32 angka berdasarkan kriteria durasi gelombang Q dan R, amplitude gelombang R dan S, rasio R/Q dan R/S, dan takik QRS pada 10 dari 12 sadapan EKG (tabel 2.2). Nilai maksimum adalah 32 dan setiap 1 nilai mewakili 3% massa ventrikel kiri. Sistem
skor ini mewakili 96% ventrikel kiri dan telah diuji pada 100 ventrikulogram penderita penyakit jantung koroner yang telah terbukti secara angiografis (Selvester RH, 1982; Selvester RH, 2011).
Tabel 2.2 Sistem Pemberian Skor Selvester : 54 kriteria, 32 angka berdasarkan kriteria durasi gelombang Q dan R, amplitude gelombang R dan S, rasio R/Q dan R/S, dan takik (notch) QRS. Nilai maksimum adalah 32 dan setiap poin mewakili 3% massa ventrikel kiri (Selvester RH, 1982).
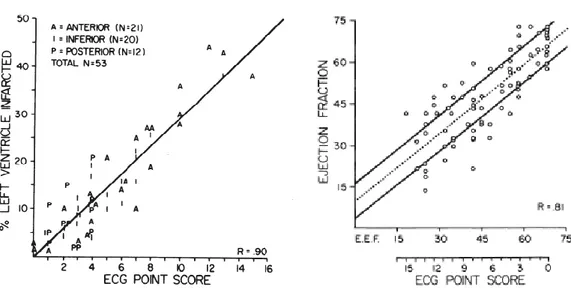
Ideker dkk kemudian melakukan validasi Skor Selvester dengan studi postmortem pada 54 subjek. Pasien dengan infark tunggal pada saat otopsi tanpa adanya hipertropi atau abnormlitas konduksi pada ECG dimasukkan dalam studi ini. Mereka menemukan korelasi yang baik antara Skor Selvester dengan luas infark pada masing-masing tiga pembuluh darah koroner utama, yaitu infark anterior dengan r = 0,93 ; infark inferior dengan r = 0,97 dan infark posterolateral dengan r = 0,83 (Ideker RE, 1979; Ruth WK, 1979; Selvester RH, 1982).
Selvester dan kawan – kawan kemudian melaporkan perubahan pada serial EKG pada pasien yang menjalani angiografi. Mereka menemukan bahwa serial EKG yang tidak mengalami perubahan berhubungan dengan ventrikulogram yang tidak berubah, sedangkan perubahan pada EKG akan menghasilkan perubahan pada ventrikulogram, dimana derajat perubahan EKG sebanding dengan perubahan fraksi ejeksi ventrikel kiri pada ventrikulogram. Selvester dkk juga melakukan
studi terhadap 85 pasien dengan oklusi total pada arteri koroner desendens anterior kiri dan stenosis ≤75% pada arteri koroner yang lain . Mereka menemukan kemampuan skor EKG dalam memprediksi fraksi ejeksi ventrikel kiri dengan koefisien korelasi sebesar 0,81 (Selvester RH, 1982).
A B
Gambar 2.7 A. Korelasi antara Skor Selvester denga luas infark berdasarkan hasil otopsi B. Korelasi antara estimasi fraksi ejeksi berdasarkan Skor Selvester dan berdasarkan angiogram (Ideker RE, 1979).
2.7 Penyederhanaan Skor Selvester dan Penerapannya
Pada tahun 1982, Wagner dan kawan-kawan melakukan penyederhanaan terhadap Skor Selvester. Beberapa kriteria yang terdapat pada sistem skor asli tidak dimasukkan. Kriteria kualitatif seperti takik tidak dievaluasi karena kesulitanya dalam menentukan defenisi yang tepat yang dapat diterapkan secara umum. Kriteria lain yang berdasarkan amplitudo absolut defleksi gelombang QRS juga tidak dimasukkan oleh karena variasi amplitudo tersebut yang luas pada populasi normal. Penyederhanaan ini menghasilkan 37 kriteria yang diaplikasikan pada 10 sadapan EKG. Kriteria berdasarkan pada durasi dan perbandingan amplitudo gelombang QRS. Tiap kriteria tersebut kemudian diberikan angka dengan angka maksimal yang dapat diperoleh sebesar 29 (tabel 2.3) (Wagner GS, 1982).
Wagner dan kawan-kawan kemudian melakukan validasi pada 349 subjek kontrol usia 20 – 50 tahun dengan ventrikulogram normal. Pasien dengan bukti
adanya hipertrofi ventrikel kanan atau kiri, blok cabang berkas kanan atau kiri tidak dimasukkan. Didapatkan spesifisitas sebesar 98% bila skor lebih dari 2 digunakan untuk mengidentifikasi adanya infark miokard (Wagner GS, 1982).
Tabel 2.3 Sistem Skor Selvester yang disederhanakan. Hanya kriteria dengan durasi dan perbandingan amplitudo gelombang QRS yang dimasukkan (Wagner GS, 1982).
Ideker dkk kemudian melakukan validasi antara Skor Selvester yang disederhanakan dengan ukuran infark yang diperoleh melalui pemeriksaan postmortem pada infark anterior, inferior dan lateral posterior. Mereka menemukan korelasi yang kuat (r = 0,9) antara Skor Selvester yang disederhanakan dengan ukuran infark (Selvester RH, 1982).
Pada aplikasi sistem Skor Selvester, durasi dan amplitudo kompleks QRS diukur pada 10 dari 12 sadapan, yaitu I, II, aVL, aVF, V1, V2, V3, V4, V5, dan V6. Pengukuran durasi QRS dalam milidetik dan dibuat secara horizontal sepanjang garis segmen PR. Pengukuran amplitudo dalam millivolt dan dibuat secara vertical walaupun segmen ST bergeser. Dari hasil pengukuran yang dilakukan manual ini didapatkan jumlah angka dari masing-masing kriteria pada tiap-tiap sadapan. Perekam elektrokardiografi dikalibrasi dengan amplitudo 10 mm / mv dan kecepatan 25mm/s, dengan frekuensi 0,05 sampai 100 Hz (Hindman NB, 1985).
Identifiksi bentuk gelombang harus dilakukan dengan teliti. Defleksi negatif pertama QRS adalah gelombang Q. Selanjutnya durasi dan amplitude diukur sebagai lebar dan dalam gelombang Q. Gelombang Q dengan takik jika didapatkan arah balik sebesar 0,05mV atau lebih didalam defleksi negatif awal.
Selanjutnya durasi gelombang Q diukur sepanjang garis isoelektrik PR sampai ke titik tepat dipuncak takik. Amplitudo gelombang Q diukur samapai ke titik terendah defleksi negatif yang mendahului takik. Gelombang R didefinisikan sebagai defleksi positif permulaan kompleks QRS. Gelombang R dengan takik jika dijumpai arah balik 0,05mV atau lebih dalam 40 ms pertama kompleks QRS.
Gambar 2.7 dibawah ini menunjukkan cara identifikasi kompleks QRS (Hindman NB, 1985; Selvester, RH 1985).
Gambar 2.8. A, Gelombang Q rata bila pada defleksi negative pertama tidak didapatkan arah balik 0,05 mV atau lebih mendahului gelombang R. B, Gelombang Q dengan takikjika didapatkan arah balik 0,05 mV atau lebih pada defleksi negative permulaan. Durasi diukur dari garis awal segmen PR sampai titik atas puncak takik. Amplitudo diukur dari titik terendah defleksi negatif yang mendahului takik sampai ke garis segmen PR. C, Tanda panah menunjukkan gelombang R dengan takik yang didefinisikan sebagai adanya arah balik 0,05 mV atau lebih pada 40 mS pertama kompleks QRS (Hindman NB, 1985).
.
Pembobotan didefinisikan sebagai jumlah angka yang dikumpulkan pada kriteria yang memenuhi syarat. Apabila pada sadapan yang sama terdapat beberapa kriteria durasi atau amplitudo, maka kriteria dengan bobot yang tertinggi yang dimasukkan. Contohnya, apabila durasi gelombang Q pada sadapan aVF adalah 50 mS, hanya skor 3 yang dihitung. Skor lain dengan durasi gelombang Q
< 50 mS pada sadapan aVF tidak dihitung. Kriteria rasio amplitudo terhadap gelombang Q atau R yang tidak memenuhi kriteria durasi pada lead yang sama tidak dihitung. Contohnya, apabila durasi gelombang Q pada sadapan I kurang dari 30 mS, kriteria rasio R/Q pada sadapan I tidak dihitung. Tetapi rasio amplitudo yang tidak melibatkan gelombang Q atau R (contohnya pada sadapan V4, V5 dan V6) harus dihitung tanpa memperhatikan durasi gelombang Q atau R (Hindman NB, 1985; Selvester RH 1985).
Secara teori, adanya blok fasikulus, blok cabang berkas dan hipertrofi ventrikel akan menyebabkan perubahan pada vektorkardiogram dan dapat mempengaruhi (menambah atau meniadakan) tanda-tanda infark pada EKG.
Dibawah ini adalah beberapa faktor perancu beserta kriterianya, yang harus diperhatikan sebelum memakai sistem skor QRS Selvester yang disederhanakan (Strauss DG, 2009; Loring Z, 2011):
LBBB – durasi QRS 140 ms (laki-laki) atau lebih dan 130 ms atau lebih (perempuan), QS atau rS di V1 dan V2 dengan perlambatan/takik pada QRS;
RBBB – durasi QRS 120 ms atau lebih dengan rR’ di V1 (atau qR’ pada infark anterior luas) dan S lebar di sadapan I, V5, dan V6;
LAFB – durasi QRS 100 ms atau lebih dan deviasi aksis ke kiri dan lebih dari 45o dengan rS pada sadapan aVF, dan/atau qR di aVL);
LVH – meningkatnya voltase QRS berdasarkan kriteria Sokolow-Lyon atau kriteria Cornell dan tidak memenuhi kriteria lain;
RAO (right atrial overload) – Gelombang P di V1 ≥0,1 mV atau di aVF
≥0,175 mV, dimana hanya defleksi positif gelombang P yang diukur.
2.8 Hubungan Skor Selvester Yang Disederhanakan dengan Prognostik pada Pasien IMAEST
Beberapa studi, telah menemukan hubungan pasien dengan infark miokard akut maupun kronis yang memiliki Skor Selvester yang disederhanakan yang lebih tinggi ternyata memiliki prognostik yang lebih buruk.
Jones dkk melakukan studi dengan menilai Skor Selvester pada 384 pasien sindroma koroner akut setelah pasien dirawat di rumah sakit. Mereka membagi Skor Selvester dalam 3 kategori berdasarkan estimasi luas infark, yaitu kecil, <
10% (skor 0 sampai 3), sedang, 10 sampai 21% ( skor 4 sampai 7) dan besar, >
21% (skor >7). Mereka menemukan hubungan yang signifikan antara Skor Selevester dengan kematian akibat penyakit jantung koroner setelah 60 hari dengan angka mortalitas pasien dengan Skor Selvester >7 dan usia >65 tahun sebesar 67% (Jones MG, 1990).
Fioretti dkk sebelumnya juga telah melakukan studi pada 474 pasien dengan infark miokard akut untuk mengetahui nilai prognostik Skor Selvester dan parameter EKG yang lain, seperti depresi segmen ST, elevasi segmen ST, dan interval QTc dari 12 sadapan EKG yang diperoleh saat pasien akan pulang dari