Amoksisilin Generik Bermerek Terhadap Kadar Malondialdehid (MDA) Hepar Rattus norvegicus Galur Sprague Dawley
Medula | Volume 7 | Nomor 4 | November 2017| 129
Perbandingan Pemberian Dosis Toksik Amoksisilin Generik Berlogo dengan
Amoksisilin Generik Bermerek terhadap Kadar Malondialdehid (MDA) Hepar
Rattus norvegicus
Galur
Sprague Dawley
Dyah Kartika Utami, Tri Umiana Soleha, Evi Kurniawaty Fakultas Kedokteran, Universitas Lampung
Abstrak
Dilema obat generik berlogo dan generik bermerek masih terjadi, sementara dokter di fasilitas kesehatan pemerintah diwajibkan meresepkan obat generik. Di Indonesia, amoksisilin adalah salah satu antibiotik yang sering diresepkan. Amoksisilin memiliki rantai bersifat elektronegatif serta cincin betalaktam yang dapat menyerang grup thiol sehingga menyebabkan terbentuknya Reactive Oxygen Species (ROS) yang memicu proses peroksidasi lipid dengan hasil akhir Malondialdehid (MDA). Tujuan penelitian ini adalah untuk membandingkan kadar MDA hepar Rattus norvegicus pada pemberian dosis toksik antara amoksisilin generik berlogo dan generik bermerek. Penelitian ini menggunakan 28 ekor
Rattus norvegicus galur Sprague Dawley jantan yang dibagi menjadi 1 kelompok kontrol (K) yang diberi akuades dan 6 kelompok perlakuan yang diberi amoksisilin sesuai tingkatan dosis. Kelompok perlakuan terdiri dari A1-A3 dan B1-B3 dengan tiga tingkatan dosis yaitu 205,6mg/kgbb; 411,2 mg/kgbb; dan 822,4 mg/kgbb. Perlakuan diberikan sehari tiga kali selama 14 hari. Hewan coba diterminasi dan diambil heparnya. Hepar dibuat homogenat dan diambil supernatannya kemudian diukur kadar MDA sesuai Metode Wills. Data dianalisis menggunakan Uji One Way ANOVA dan Post-Hoc LSD.
Hasil bermakna didapatkan pada perbandingan A3 dan B3 (p=0,000). Terdapat perbedaan kadar MDA hepar Rattus norvegicus galur Sprague Dawley antara pemberian dosis toksik amoksisilin generik berlogo dan generik bermerek.
Kata kunci: amoksisilin, generik, malondialdehid, reactive oxygen species
Comparison of Generic Amoxicillin and Branded Amoxicillin Toxic Dose
Administration toward Liver Malondialdehyde (MDA) Level Of Sprague
Dawley Strain Rattus norvegicus
Abstract
Dilemma between generic and branded drugs are still noticeable, meanwhile doctors in public healthcare are mandated to prescribe generic drugs. In Indonesia, amoxicillin is one of the most prescribed antibiotics. Amoxicillin has electronegative side chain and betalactam ring that attack thiol group, producing reactive oxygen species that induce lipid peroxidation and form malondialdehyde (MDA) as its end-product. This study purpose is to compare liver MDA level after toxic dose administration between generic and branded amoxicillin on Sprague Dawley strain Rattus norvegicus. This study uses 28 male rats that divided into 7 group. One control group (K) is given aquadest and 6 experimental group (A1-A3 and B1-B3) are given 3 different doses: 205,6mg/kg; 411,2 mg/kg; dan 822,4 mg/kg. Drugs and aquadest are given three times a day for 14 days. Rats are terminated and the liver is taken. Liver homogenates are made and the supernatants are analyzed using Wills Method to determine MDA level. The data is analyzed using One Way ANOVA and Post-Hoc LSD. Results are found to be significant between A3 and B3 (p=0.000). There is a difference in liver MDA level after toxic dose administration of generic and branded amoxicillin on Sprague Dawley strain Rattus norvegicus.
Keywords: amoxicillin, generic, malondialdehyde, reactive oxygen species
Korespondensi : Dyah Kartika Utami, alamat Lingkungan Pala Manis RT 001/006, Cibinong-Kab. Bogor, HP 081286847594, email kdyah74@yahoo.com
Pendahuluan
Obat merupakan salah satu unsur penting dalam upaya peningkatan kesehatan, pencegahan, diagnosis, pengobatan, dan pemulihan.1 Pemerintah mengatur penyediaan
obat generik di fasilitas pelayanan kesehatan pemerintah dan dokter yang bertugas wajib menulis resep obat generik sesuai indikasi medis bagi pasien rawat jalan maupun inap.2
Obat generik adalah obat dengan nama resmi International Non Propietary Names (INN)
yang ditetapkan dalam Farmakope Indonesia atau buku standar lainnya untuk zat berkhasiat yang dikandungnya, sedangkan obat paten adalah obat yang masih memiliki hak paten.2
Amoksisilin Generik Bermerek Terhadap Kadar Malondialdehid (MDA) Hepar Rattus norvegicus Galur Sprague Dawley
Medula | Volume 7 | Nomor 4 | November 2017| 130 Volume penjualan obat generik berlogo
tahun 2012 mencapai 38%. Angka tersebut masih berada di bawah obat generik bermerek. Hal ini dikarenakan obat generik bermerek memiliki strategi pemasaran, sehingga selisih harga dapat mencapai 50 hingga 200%.4-5
Di Indonesia, penggunaan antibiotik untuk terapi penyakit infeksi masih menjadi sorotan.6
Salah satu antibiotik yang paling sering diresepkan adalah Amoksisilin.7 Amoksisilin
diabsorpsi baik di saluran cerna, dimetabolisme di hepar, dan diekskresikan melalui ginjal.8
Amoksisilin dapat menimbulkan stres oksidatif di dalam tubuh. Stres oksidatif adalah adanya Reactive Oxygen Species (ROS) dengan kadar lebih tinggi dibandingkan antioksidan di dalam tubuh. Keadaan ini mengakibatkan rusaknya protein, lipid, dan DNA, sehingga mengubah struktur dan fungsi organisme.9 Jika pertahanan
oleh antioksidan gagal, maka ROS meningkat dan bereaksi dengan asam lemak polyunsaturated dan melepaskan metabolit aldehid yang toksik dan reaktif, seperti malondialdehid (MDA) yang merupakan produk akhir proses peroksidasi lipid.10
Malondialdehid merupakan salah satu senyawa yang sering dijadikan petunjuk adanya kerusakan akibat radikal bebas. Zat ini merupakan salah satu senyawa yang menggambarkan aktivitas oksidan (radikal bebas) dalam sel.11 Malondialdehid bersifat
mutagenik dan karsinogenik serta dapat menyebabkan putusnya rantai ganda DNA dan modifikasi pada RNA, protein, serta biomolekul lainnya.12-13 Berdasarkan latar belakang di atas,
penelitian ini dilakukan untuk meneliti perbandingan kadar MDA hepar antara Rattus norvegicus galur Sprague Dawley yang diberi amoksisilin generik berlogo dan generik bermerek dalam dosis yang sama.
Metode
Penelitian ini telah dilaksanakan di Laboratorium Biokimia dan Biologi Molekular Fakultas Kedokteran Universitas Lampung selama September hingga Desember 2015. Sampel yang digunakan pada penelitian ini adalah Rattus norvegicus jantan berusia 6-7 minggu dengan berat 100-200 gram. Penelitian ini merupakan penelitian eksperimental dengan rancangan Post Test Only Control Group Design. Pengambilan data telah dilakukan pada akhir
penelitian setelah masing-masing kelompok hewan coba diberi perlakuan dan diterminasi.
Sampel sebanyak 28 ekor Rattus norvegicus dibagi ke dalam 7 kelompok penelitian, masing-masing sebanyak 4 ekor tikus. Kelompok pertama adalah kelompok kontrol negatif (K), yaitu tikus yang hanya diberi akuades sehari tiga kali selama 14 hari. Kelompok berikutnya adalah kelompok generik (A) dan kelompok bermerek (B) yang masing-masing dibagi menjadi 3 kelompok dosis.
Perhitungan dosis amoksisilin didapat dari konversi dosis maksimal manusia menjadi dosis maksimal hewan coba menggunakan rumus Body Surface Area (BSA).14 Dari hasil
perhitungan, didapatkan dosis hewan maksimal per kali pemberian amoksisilin adalah 102,8 mg/kgbb. Amoksisilin diberikan secara bertingkat dengan kelipatan 1,2, dan 4 kali dosis. Kelompok generik berlogo-1 (A1) dan kelompok generik bermerek-1 (B1) mendapat dosis 102,8 mg/kgbb. Kelompok generik berlogo-2 (A2) dan kelompok generik bermerek-2 (B2) mendapat dosis 205,6 mg/kgbb. Kelompok generik berlogo-3 (Aberlogo-3) dan kelompok generik bermerek-berlogo-3 (Bberlogo-3) mendapat dosis 411,2 mg/kgbb.
Hewan coba diaklimatisasi selama 7 hari sebelum penelitian dimulai. Amoksisilin sesuai dengan dosis yang sudah ditentukan diberikan sehari tiga kali selama 14 hari menggunakan sonde lambung, sementara kelompok K diberikan akuades. Setelah perlakuan selesai, tikus diterminasi dan diambil heparnya. Hepar dibuat homogenat dan diambil supernatannya. Selanjutnya, pengukuran MDA dilakukan sesuai dengan metode Wills.15
Data hasil penelitian diuji normalitas datanya menggunakan uji Shapiro-Wilk karena jumlah sampel kurang dari 50, dilanjutkan dengan uji homogenitas varians menggunakan uji Levene. Data hasil penelitian akan dilakukan uji hipotesis numerik lebih dari 2 kelompok tidak berpasangan. Jika data yang berdistribusi normal, akan dilakukan uji One Way ANOVA, sedangkan uji alternatifnya adalah uji Kruskal-Wallis. Data hasil penelitian akan dianalisis untuk mengetahui perbedaan antar kelompok secara lebih rinci. hasil uji One Way ANOVA akan dilanjutkan dengan analisis Post Hoc LSD, sedangkan uji Kruskal-Wallis dilanjutkan dengan uji Mann-Whitney U.16
Amoksisilin Generik Bermerek Terhadap Kadar Malondialdehid (MDA) Hepar Rattus norvegicus Galur Sprague Dawley
Medula | Volume 7 | Nomor 4 | November 2017| 131 pendahuluan menunjukkan hasil bermakna
didapatkan pada dosis 205,6 mg/kgbb. Sehingga, tingkatan dosis yang digunakan pada penelitian adalah 205,6 mg/kgbb untuk A1 dan B1; 411,2 mg/kgbb untuk A2 dan B2; 822,4 mg/kgbb untuk A3 dan B3; dan akuades untuk kelompok K.
Hasil Penelitian
Gambar 1. Kurva Standar Malondialdehid (MDA)
Kurva standar pada Gambar 1 menghasilkan persamaan linier y=0.0119x-0.0007 dengan R2=0.0096. Hasil absorbasi
disubstitusi ke dalam persamaan sehingga didapatkan kadar MDA. Kadar MDA disajikan pada Tabel 1 dalam bentuk rerata masing-masing kelompok perlakuan.
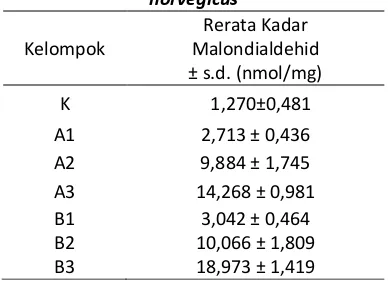
Tabel 1. Hasil Rerata Kadar MDA Hepar Rattus norvegicus
Kelompok
Rerata Kadar Malondialdehid ± s.d. (nmol/mg)
K 1,270±0,481
A1 2,713 ± 0,436
A2 9,884 ± 1,745
A3 14,268 ± 0,981
B1 3,042 ± 0,464
B2 10,066 ± 1,809
B3 18,973 ± 1,419
Data kadar MDA yang didapatkan dari hasil pengukuran dianalisis menggunakan perangkat lunak komputer. Data diuji normalitasnya menggunakan uji Saphiro-Wilk.
Hasil menunjukkan data berdistribusi normal, dengan kelompok K memiliki nilai p=0,391; A1 dengan p= 0,467; Kelompok A2 dengan p=0,364; Kelompok A3 dengan p=0,738; Kelompok B1 dengan p=0,976; Kelompok B2 dengan p=0,596; dan Kelompok
B3 dengan p=0,191. Setelah dilakukan uji normalitas, dilakukan uji varians menggunakan uji Levene. Uji menunjukkan varian data penelitian homogen dengan p=0,085. Oleh karena data berdistribusi normal dengan varian homogen, maka selanjutnya dilakukan uji komparatif menggunakan One Way ANOVA dilanjutkan dengan Post Hoc LSD.
Pada uji One Way ANOVA, didapatkan hasil bermakna dengan p=0,000. Analisis dilanjutkan dengan uji Post Hoc LSD yang dapat dilihat pada Tabel 2.
Tabel 2. Hasil Perbandingan Kadar MDA Antarkelompok Menggunakan Uji Post Hoc LSD
Kelompok p-value Kemaknaan
K dengan A1 0,101 Tidak Bermakna
K dengan A2 0,000 Bermakna
K dengan A3 0,000 Bermakna
K dengan B1 0,048 Bermakna
K dengan B2 0,000 Bermakna
K dengan B3 0,000 Bermakna
A1 dengan B1 0,700 Tidak Bermakna A2 dengan B2 0,831 Tidak Bermakna A3 dengan B3 0,000 Bermakna
Diketahui bahwa kelompok K memiliki
perbandingan yang signifikan dengan
kelompok perlakuan lain. Selanjutnya,
dilakukan perbandingan antara kelompok amoksisilin generik berlogo dan amoksisilin generik bermerek dengan dosis yang sama. Perbandingan kadar MDA antara kelompok A1 dan B1 serta A2 dan B2 tidak bermakna. Sementara hasil didapatkan bermakna pada perbandingan antara A3 dan B3.
Pembahasan
Dilakukan perbandingan antara
kelompok kontrol dengan kelompok perlakuan dan antara kelompok perlakuan dalam tingkatan dosis yang sama. Kadar MDA Kelompok K merupakan kadar terrendah dalam penelitian ini. Kelompok K sebagai
kontrol kemudian dibandingkan dengan
kelompok perlakuan. Hasil menunjukkan adanya nilai bermakna antara kelompok K dengan A2, A3, B1, B2 dan B3.
Adesanoye et al. membuktikan bahwa
kadar MDA hewan coba yang diberi
amoksisilin akan meningkat jika dibandingkan kelompok kontrol.17 Hasil yang sejalan juga
Amoksisilin Generik Bermerek Terhadap Kadar Malondialdehid (MDA) Hepar Rattus norvegicus Galur Sprague Dawley
Medula | Volume 7 | Nomor 4 | November 2017| 132
kadar MDA pada kelompok perlakuan
dikarenakan amoksisilin dapat membentuk
formasi radikal karena sifatnya yang
elektronegatif sehingga mampu mengambil electron grup karbonil. Selain itu, amoksisilin memiliki cincin betalaktam yang dapat merusak struktur grup thiol pada membrane dan enzim. Kerusakan polyunsaturated fatty acids (PUFA) yang esensial bagi integritas dan fungsi membran menyebabkan gangguan aktivitas mikrosom dan enzim intrinsic. Keadaan ini adalah onset dari peroksidasi lipid.17 Kadar MDA yang meningkat pada
kelompok kontrol mengindikasikan adanya akumulasi radikal bebas di dalam tubuh. Hal ini menyebabkan MDA menjadi indikator yang reliable terhadap stres oksidatif.12
Hasil perbandingan kadar MDA
kelompok K dan A1 tidak bermakna (p=0,101). Hasil ini dapat dikarenakan adanya mekanisme kompensasi tubuh tehadap stres oksodatif yang tejadi. Tubuh memiliki mekanisme untuk mengurangi kerusakan yang ditimbulkan oleh radikal bebas, salah satu caranya adalah dengan pertahanan antioksidan. Antioksidan
mampu mencegah ataupun mengurangi
dampak kerusakan sel yang disebabkan reaksi oksidatif dalam tubuh. Adanya radikal bebas
memicu peroksidasi lipid. Tubuh akan
menggunakan antioksidan yang ada di dalam tubuh beserta cadangan yang ada dalam organ, misalnya hepar dan jaringan adiposa. Konsumsi antioksidan dalam proses ini akan berlangsung terus menerus sampai pada titik dimana tubuh tidak dapat lagi berkompensasi, sehingga terjadi peroksidasi lipid yang signifikan18, yang mana dalam penelitian ini
terjadi pada kelompok perlakuan A2-A3 dan B1-B3.
Sel yang terpapar oleh ROS akan mengalami gangguan keseimbangan sel. Akan tetapi, sel memiliki kemampuan untuk
mengatasi paparan tersebut dengan
membentuk senyawa antioksidan. Pertahanan ini berlangsung sampai pada kondisi sel tidak dapat lagi mengatasi ROS. Senyawa ini akan menumpuk di dalam tubuh dan menimbulkan kerusakan pada sel yang akan berujung pada nekrosis ataupun apoptosis sel. Pada kondisi ini, kadar MDA mengalami peningkatan.11
Merujuk pada Tabel 2, dilakukan keduanya. Tubuh mampu mengatasi radikal
bebas yang terbentuk karena induksi
amoksisilin. Obat di dalam tubuh mengalami biotransformasi oleh sistem enzim CYP450 untuk kemudian diekskresikan oleh tubuh. Proses biotransformasi meliputi Fase I dan II yang dipengaruhi oleh beberapa aspek, antara lain genetik dan kadar antioksidan dalam tubuh. Peningkatan kadar obat dalam tubuh
menyebabkan proses biotransformasi
terinduksi, sehingga proses menjadi lebih cepat.19 Selain itu, tubuh memiliki antioksidan
yang diproduksi secara endogen maupun eksogen, di antaranya adalah superoxide dismutase (SOD), catalase (CAT), glutathion peroxidase (GPx), glutathion (GSH), flavonoid, mineral dan vitamin. Dalam keadaan sehat, oksidan dan antioksidan berada dalam keadaan seimbang.20
Perbandingan antara A3 dan B3 memiliki hasil yang bermakna. Hal ini mengindikasikan adanya perbedaan kadar MDA yang signifikan antara keduanya, yaitu antara amoksisilin generik berlogo dan generik bermerek. Perbedaan ini dapat dikarenakan adanya
perbedaan waktu paruh absorpsi, laju
absorpsi, waktu paruh eliminasi, dan laju eliminasi antara keduanya. Uji bioekuivalensi yang membandingkan amoksisilin generik berlogo dan generik bermerek menunjukkan
adanya perbedaan antara keduanya.
Amoksisilin generik berlogo memiliki waktu paruh absorpsi 2,25 jam dan waktu paruh
eliminasi 3,25 jam, sedangkan generik
bermerek memiliki waktu paruh absorpsi 1,75 jam dan waktu paruh eliminasi 5 jam.21
Amoksisilin generik bermerek berada di dalam tubuh lebih lama karena waktu paruh absopsi lebih cepat dan waktu paruh eliminasi lebih lambat, sehingga tubuh lebih lama terpapar dengan rantai elektronegatif milik amoksisilin yang menyebabkan kadar MDA lebih tinggi.
Amoksisilin Generik Bermerek Terhadap Kadar Malondialdehid (MDA) Hepar Rattus norvegicus Galur Sprague Dawley
Medula | Volume 7 | Nomor 4 | November 2017| 133
bahan aktif yang sama tetapi memiliki
vehikulum berbeda yang menyebabkan
perbedaan farmakokinetik dan
farmakodinamik. Perbedaan pharmaceutical properties pada antibiotik dapat menyebabkan
perbedaan profil farmakokinetik antar
keduanya, sehingga terdapat variasi dalam efikasi obat.22
Vehikulum yang berbeda menyebabkan
perbedaan kemampuan kelarutan obat
generik berlogo dan generik bermerek. Beberapa obat generik berlogo lebih cepat larut dibandingkan obat generik bermerek,
begitu pula sebaiknya. Hal ini akan
menyebabkan efek samping yang berbeda pula.23 Vehikulum yang berbeda menyebabkan
waktu pemecahan partikel obat yang berbeda
pula, sehingga kecepatan absorpsi tiap obat berbeda dan berdampak pada efikasi yang bervariasi antar obat.24 Peran variasi individu
juga menjadi faktor penting yang
menyebabkan perbedaan kadar MDA. Variasi ini misalnya kondisi penyakit lain, kemampuan first-pass metabolism, dan kondisi gastrointestinal.22
Simpulan
Terdapat perbedaan kadar
malondialdehid (MDA) hepar antara Rattus norvegicus galur Sprague Dawley yang diinduksi amoksisilin generik berlogo dan amoksisilin generik bermerek.
Daftar Pustaka
1. Kementerian Kesehatan RI. Kebijakan
Obat Nasional. Jakarta. 2006
2. Kementerian Kesehatan RI. Kewajiban
Menggunakan Obat Generik di Fasilitas
Pelayanan Kesehatan Pemerintah.
Jakarta. 2010
3. Raini M, Mutiatikum D, Lastari P. Uji disolusi dan penetapan kadar tablet loratadin inovator dan generik bermerek. Media Litbang Kesehatan. 2010; XX(2): 59-64.
4. Prabowo AWB, Vanany I. Analisis
kebijakan penggunaan obat generik di indonesia serta dampaknya pada biaya belanja obat masyarakat ( studi kasus
pada obat penyakit diabetes
menggunakan pendekatan sistem
dinamik). Jurnal Teknik ITS. 2012; 1(1): 592-4.
5. Direktorat Jenderal Bina Kefarmasian dan Alat Kesehatan. Kualitas Obat Generik Sama dengan Obat Bermerek [internet]. Kementerian Kesehatan RI; 2004 [Diakses pada 25 Juli 2015]. Tersedia dari: http://binfar.kemkes.go.id/2014/05/kualit as-obat-generik-sama-dengan-obat-bermerek/
6. Kementerian Kesehatan RI. Pedoman
Umum Penggunaan Antibiotik. Jakarta. 2011.
7. Adnyana IK, Murtini S, Roni A, Wardani IGAAK. Evaluation of antibacterial activity
and determination amoxicillin
concentration on generic and branded
products. International Journal of
Pharmacy and Pharmaceutical Sciences. 2013; 5(3): 1-5.
8. Katzung BG, Trevor AJ. Basic and Clinical Pharmacology 13th ed. San Diego: The McGraw-Hill Companies, Inc; 2014.
9. El-Tohamy MM. The mechanism by which
oxidative stress and free radical damage produces male infertility. Life Science Journal. 2012; 9(1): 674-88.
10. Aliahmat NS, Noor MRM, Yusof WJW, Makpol S, Ngah WZW, Yusof YAM, Dkk.
Antioxidant enzyme activity and
malondialdehyde levels can be modulated by Piper betle, tocotrienol rich fraction and Chlorella vulgaris in aging C57BL/6 mice. Clinics. 2012; 67(12): 1447-54. 11. Asni E, Harahap IP, Prijanti AR, Wanandi
SI, Jusman SWA, Sadikin M, Dkk. Pengaruh hipoksia berkelanjutan terhadap kadar malondialdehid, glutation tereduksi dan aktivitas katalase ginjal tikus. Maj Kedokt Indon. 2009; 59(12): 595-60.
12. Yang FL, Li XS, He BX, Yang XL, Li GH, Liu P, Dkk. Malondialdehyde level and some enzymatic activities in subclinical mastitis milk. African Journal of Biotechnology. 2011; 10(28): 5534-8.
13. Siddique Y, Ara G, Afzal M. Estimation of lipid peroxidation induced by hydrogen peroxide in cultured human lymphocytes.
Dose-response: a publication of
Amoksisilin Generik Bermerek Terhadap Kadar Malondialdehid (MDA) Hepar Rattus norvegicus Galur Sprague Dawley
Medula | Volume 7 | Nomor 4 | November 2017| 134
14. Reagan-shaw S, Nihal M, Ahmad N. Dose translation from animal to human studies revisited. The FASEB Journal.2007; 22: 659-61.
15. Ratya A. Pengaruh pemberian ekstrak daun sirsak (annona muricata l.) Terhadap kadar malondialdehid pada jaringan hati tikus putih yang diinduksi DMBA [Skripsi]. Universitas Lampung; 2014.
16. Dahlan MS. Statistik untuk kedokteran dan kesehatan: deskriptif, bivariat, dan multivariat, dilengkapi dengan aplikasi menggunakan spss edisi ke-5. Jakarta: Salemba Medika; 2013.
17. Adesanoye O, Ifezue A, Farombi E.
Influence of chloramphenicol and
amoxicillin on rat liver microsomal enzymes and lipid peroxidation. African Journal of Biomedical Research. 2014; 17(September): 135-42.
18. Hundekari IA, Suryakar AN, Rathi DB. Oxidative stress and antioxidant status in
acute organophosphorus pesticides
poisoning cases of North Karnataka (India): oxidative damage, haemoglobin level and total leukocyte. African Health Sciences. 2013; 13(1): 129-36.
19. Liska DJ. The detoxification enzyme systems. Altern Med Rev. 1998; 3(3): 187-198.
20. Irshad M, Chaudhuri PS.
Oxidant-antioxidant system: role and significance in human body [Abstrak]. Indian J Exp Biol. 2002; 40(11): 1233-9.
21. Wahyudin E, Naid T, Leboe DW. Studi bioekivalensi amoksisilin generik dan dagang menggunakan matriks urin. JST Kesehatan. 2012; 2(1): 85-91.
22. Del Tacca M, Pasqualetti G, Di Paolo A, Virdis A, Massimetti G, Gori G, Versari D,
Dkk. Lack of pharmacokinetic
bioequivalence between generic and branded amoxicillin formulations. A post-marketing clinical study on healthy volunteers. British Journal of Clinical Pharmacology. 2009; 68(1): 34-42.
23. Ameri MNA, Nayuni N, Anil Kumar KG, Perrett D, Tucker A, Johnston A, Dkk. The differences between the branded and generic medicines using solid dosage forms: in-vitro dissolution testing. Results in Pharma Sciences. 2012; 2(1): 1-8.
24. Mycek MJ, Harvey RA, Champe PC.