BAB II
KAJIAN PUSTAKA
2.1 PENUAAN 2.1.1 Definisi
Menua (aging) adalah suatu proses menghilangnya secara perlahan kemampuan jaringan untuk memperbaiki diri/mengganti diri dan mempertahankan struktur dan fungsi normalnya, sehingga tidak dapat bertahan serta memperbaiki kerusakan yang diderita. Dengan begitu manusia secara progresif akan kehilangan daya tahan terhadap infeksi, dan semakin banyak distorsi metabolik dan struktural, yang disebut sebagai penyakit degeneratif (seperti hipertensi, aterosklerosis, diabetes melitus, dan kanker), yang akan menyebabkan kita mengakhiri hidup dengan episode terminal yang dramatik seperti stroke, infark myokard, koma asidotik, metastasis kanker dan sebagainya (Darmojo, 1999).
2.1.2 Penyebab Penuaan
Banyak faktor yang menyebabkan orang menjadi tua melalui proses penuaan, yang kemudian menyebabkan sakit, dan akhirnya membawa kepada kematian. Pada dasarnya faktor itu dikelompokkan menjadi faktor internal dan eksternal. Beberapa faktor internal ialah radikal bebas, hormon yang berkurang, proses glikosilasi, metilasi, apotosis, sistem kekebalan yang menurun, dan genetik. Faktor eksternal yang utama ialah gaya hidup tidak sehat, diet tidak sehat, kebiasaan salah, polusi lingkungan, stres, dan kemiskinan (Pangkahila, 2007).
2.1.3 Teori Proses Penuaan
Banyak teori yang menjelaskan mengapa manusia mengalami proses penuaan. Tetapi, pada dasarnya semua teori itu dapat dibagi menjadi dua kelompok, yaitu wear and tear theory dan programmed theory (Goldmann and Klatz, 2003).
2.1.3.1 Wear and Tear Theory
Teori wear and tear pada prinsipnya menyatakan tubuh menjadi lemah lalu meninggal sebagai akibat dari penggunaan dan kerusakan yang terus menerus. Teori ini telah lama diperkenalkan oleh Dr. August Weismann, seorang ahli biologi dari Jerman pada tahun 1882. Menurut teori ini, tubuh dan selnya menjadi rusak karena terlalu sering digunakan dan disalahgunakan. Kerusakan tidak terbatas pada organ, melainkan juga terjadi di tingkat sel (Goldmann dan Klatz, 2003).
Hal ini berarti walaupun seseorang tidak pernah merokok, minum alkohol, dan hanya mengonsumsi makanan alami, dengan menggunakan organ tubuh secara biasa saja, pada akhirnya terjadi kerusakan. Penyalahgunaan organ tubuh membuat kerusakan lebih cepat. Karena itu, tubuh menjadi tua, sel merasakan pengaruhnya, terlepas dari seberapa sehat gaya hidupnya. Pada masa muda sistem pemeliharaan dan perbaikan tubuh mampu melakukan kompensasi terhadap pengaruh penggunaan dan kerusakan normal berlebihan (Goldmann dan Klatz, 2003).
Dengan menjadi tua, tubuh kehilangan kemampuan memperbaiki kerusakan karena penyebab apa pun. Banyak orang tua meninggal karena penyakit yang pada masa mudanya dapat ditolak. Teori ini meyakini pemberian suplemen yang tepat dan pengobatan yang tidak terlambat dapat membantu mengembalikan proses penuaan.
Mekanismenya dengan merangsang kemampuan tubuh untuk melakukan perbaikan dan mempertahankan organ tubuh dan sel (Goldman dan Klatz, 2003).
Teori wear and tear meliputi:
1. Teori Kerusakan DNA
Tubuh mempunyai kemampuan untuk memperbaiki diri (DNA repair). Proses penuaan sebenarnya berarti proses penyembuhan yang tidak sempurna dan sebagai akibat penimbunan kerusakan molekul yang terus menerus (Darmojo, 1999). Kerusakan DNA menumpuk dalam waktu lama, yang mencapai suatu keadaan dimana basis molekul sebanarnya sudah rusak berat. Kerusakan molekuler dapat terjadi karena faktor dari luar, seperti radiasi, polutan, asap rokok dan mutagen kimia (Pangkahila, 2007).
2. Teori Penuaan Radikal Bebas
Teori radikal bebas merupakan salah satu teori tentang penuaan, yang diperkenalkan oleh Gerschman kemudian dikembangkan oleh Denham Harman. Teori ini menekankan bahwa radikal bebas dapat merusak sel – sel tubuh manusia (Goldman dan Klantz, 2003). Radikal bebas adalah suatu molekul yang mempunyai satu atau lebih elekron yang tidak berpasangan pada orbital luarnya, bersifat sangat reaktif, dengan cara menarik elektron molekul yang ada disekitarnya, mengakibatkan terbentuknya senyawa radikal baru, sehingga akan terjadi reaksi rantai (Soeatmadji, 1998; Sadikin, 2001).
Kerusakan yang ditimbulkan akibat radikal bebas dimulai ketika lahir dan terus berlanjut hingga meninggal dunia. Ketika masih muda dampak yang ditimbulkan bersifat minor karena tubuh memiliki mekanisme perbaikan dan penggantian yang masih berfungsi baik untuk mempertahankan sel dan organ dalam keadaan sehat. Dengan bertambahnya usia akumulasi kerusakan akibat radikal bebas akan mengganggu metabolisme sel, menyebabkan mutasi sel yang dapat menimbulkan kanker dan kematian (Goldmann and Klatz, 2003). 3. Glikosilasi
Glikosilasi merupakan salah satu proses biokimia dalam tubuh yang menyebabkan perubahan fisik yang dramatis. Glikosilasi adalah reaksi non enzimatik antara senyawa glukosa dengan senyawa protein, menghasilkan glikotoksin atau Advanced Glycation End Product (AGEs), yang merupakan radikal bebas yang akan merusak jaringan tubuh. Proses ini semakin sering terjadi saat kita menua, terjadi tanpa bantuan enzim spesifik, yang menyebabkan glikosilasi menjadi sangat berbahaya (Roizen and Oz, 2009).
2.1.3.2 Programmed Theory
Teori ini menganggap di dalam tubuh manusia terdapat jam biologik, mulai dari proses konsepsi sampai ke kematian dalam suatu model terprogram (Darmojo, 1999). Peristiwa ini terprogram mulai dari sel sampai embrio, janin, masa bayi, anak-anak, remaja, dewasa, menjadi tua dan akhirnya meninggal (Pangkahila, 2007).
1. Teori Terbatasnya Replikasi Sel
Pada ujung chromosome strands terdapat struktur khusus yang disebut telomer. Setiap replikasi sel telomer memendek pada setiap pembelahan sel. Setelah sejumlah sel pembelahan sel, telomer telah dipakai dan pembelahan sel berhenti. Menurut Hayflick, mekanisme telomere tersebut menentukan rentang usia sel dan pada akhirnya juga rentang usia organisme itu sendiri (Pangkahila, 2007).
2. Proses Imun
Rusaknya sistem imun tubuh seperti: mutasi yang berulang atau perubahan protein pasca translasi, dapat menyebabkan berkurangnya kemampuan sistem imun tubuh mengenali dirinya sendiri (self recognition). Jika mutasi somatik menyebabkan terjadinya kelainan pada antigen permukaan sel, maka hal ini dapat menyebabkan sistem imun tubuh menganggap sel yang mengalami perubahan tersebut sebagai sel asing dan menghancurkannya. Perubahan inilah yang menjadi dasar terjadinya peristiwa autoimun. Salah satu bukti yang ditemukan ialah bertambahnya prevalensi auto antibodi pada orang lanjut usia (Darmojo, 1999).
3. Teori Neuroendrokin
Teori ini diperkenalkan Vladimir Dilman, PhD, berdasarkan peranan berbagai hormon bagi fungsi organ tubuh. Pada usia muda berbagai hormon bekerja dengan baik mengendalikan berbagai fungsi
organ tubuh, sehingga fungsi berbagai organ tubuh sangat optimal. Akan tetapi, ketika manusia menjadi tua, tubuh hanya mampu memproduksi hormon lebih sedikit sehingga kadarnya menurun. Akibatnya berbagai fungsi tubuh terganggu (Darmojo, 1999; Goldman dan Klatz, 2003). Terapi sulih hormon membantu untuk mengembalikan fungsi hormon tubuh sehingga dapat memperlambat proses penuaan (Goldman dan Klatz, 2003).
2.2 ANTI PENUAAN
Anti Aging Medicine (AAM) pertama kali diperkenalkan dan dikembangkan oleh American Academy of Anti-Aging Medicine (A4M) pada tahun 1993. Anti Aging Medicine adalah bagian ilmu kedokteran yang didasarkan pada penggunaan ilmu pengetahuan dan teknologi kedokteran terkini untuk melakukan deteksi dini, pencegahan, pengobatan, dan perbaikan ke keadaan semula berbagai disfungsi, kelainan, dan penyakit yang berkaitan dengan penuaan, yang bertujuan untuk memperpanjang hidup dalam keadaan sehat (Pangkahila, 2007).
Perkembangan ilmu Kedokteran Anti Penuaan (KAP) atau Anti Aging Medicine telah membawa konsep baru yang menyebabkan perubahan paradigma di dunia kedokteran.
1. Penuaan dapat dianggap sama dengan suatu penyakit yang dapat dicegah, diobati bahkan dikembalikan ke keadaan semula.
3. Manusia mengalami keluhan atau gejala penuaan karena kadar hormonnya menurun, bukan kadar hormon menurun karena manusia menjadi tua (Pangkahila, 2007).
Bila berbagai faktor penyebab penuaan dapat dihindari, proses penuaan tentu dapat dicegah, diperlambat, bahkan mungkin dihambat, dan kualitas hidup dapat dipertahankan, sehingga usia harapan hidup menjadi lebih panjang dengan kualitas hidup yang baik (Pangkahila, 2007).
Jika radikal bebas dapat diatasi dengan antioksidan, salah satu penyebab proses penuaan sudah dihambat. Jika gaya hidup tidak sehat ditinggalkan, diet tidak sehat dihindari, dan hormon yang berkurang diatasi dengan pengobatan, maka proses penuaan yang penting dapat disingkirkan (Pangkahila, 2007).
2.3 RADIKAL BEBAS 2.3.1 Definisi Radikal Bebas
Radikal bebas (free radical) adalah suatu senyawa atau molekul yang mengandung satu atau lebih elektron tidak berpasangan pada orbital luarnya, dapat bereaksi dengan molekul lain menimbulkan reaksi rantai yang sangat dekstruktif (Soeatmadji, 1998; Goldmann and Klatz, 2003). Pengertian radikal bebas dan oksidan sering dianggap sama karena keduanya memiliki kemiripan sifat, serta memiliki aktivitas yang sama dan memberikan akibat yang hampir sama, meskipun melalui proses yang berbeda (Suryohudoyo, 2000; Winarsi, 2010).
2.3.2 Sifat-sifat Radikal Bebas
Radikal bebas memiliki reaktifitas tinggi, adanya satu atau lebih elektron tidak berpasangan pada orbital luarnya, menyebabkan senyawa tersebut sangat reaktif mencari pasangan, dengan cara menyerang atau menarik elektron molekul yang berada di sekitarnya (Soeatmaji, 1998). Hal ini mengakibatkan terbentuknya senyawa radikal baru, dengan kata lain radikal bebas dapat mengubah suatu molekul atau senyawa menjadi suatu radikal bebas baru, dan seterusnya sehingga akan terjadi reaksi rantai (chain reactions) (Sadikin, 2001; Winarsi, 2010).
Pemahaman radikal bebas sebagai oksidan memang tidak salah. Sifat radikal bebas yang mirip dengan oksidan terletak pada kecenderungannya untuk menarik elektron. Pengertian oksidan dalam ilmu kimia adalah, senyawa penerima elektron (electron acceptor), yaitu senyawa yang dapat menerima atau menarik elektron, disebut juga oksidator, misalnya ion ferri (Fe +++)
Fe3+ + e- → Fe2+
Jadi sama halnya dengan oksidan, radikal bebas adalah penerima elektron. Itulah sebabnya dalam kepustakaan kedokteran, radikal bebas digolongkan dalam oksidan. Namun perlu diingat bahwa radikal bebas adalah oksidan tetapi tidak setiap oksidan adalah radikal bebas. Radikal bebas lebih berbahaya, dibandingkan dengan senyawa non radikal (Halliwell and Gutteridge, 1985; Suryohudoyo, 2000; Winarsi, 2010).
Reaktivitas dari radikal bebas baru akan berhenti bila ada peredam atau diredam (quenched) oleh senyawa yang bersifat antioksidan, seperti glutation (Winarsi, 2010).
•OH + GSH H2O + GS• (Radikal glutation)
GS• + GS• GSSG 2.3.3 Sumber Oksidan
Oksidan yang dapat merusak sel berasal dari berbagai sumber (Halliwell dan Gutteridge, 1985) yaitu :
1. Yang berasal dari tubuh sendiri, yaitu senyawa-senyawa yang sebenarnya berasal dari proses-proses biologik normal (fisiologis), namun oleh suatu sebab terdapat dalam jumlah besar.
2. Yang berasal dari proses peradangan
3. Yang berasal dari luar tubuh, seperti misalnya : obat-obatan dan senyawa pencemar (polutan).
4. Radiasi.
Tanpa disadari, dalam tubuh kita terbentuk radikal bebas secara terus menerus, baik melalui proses metabolisme sel normal, peradangan, kekurangan gizi, dan respon terhadap pengaruh dari luar, seperti polusi lingkungan, ultraviolet (UV), asap rokok dll. Dengan meningkatnya usia seseorang, pembentukan radikal bebas juga meningkat. Secara endogenus, hal ini bekaitan dengan laju metabolisme seiring dengan betambahnya usia. Bertambahnya glikolisis juga akan menyebabkan peningkatan oksidasi glukosa dalam siklus asam sitrat sehingga radikal bebas akan terbentuk lebih banyak. Secara eksogenus, kemungkinan tubuh terpapar dengan polutan juga semakin tinggi, seiring dengan meningkatnya usia seseorang. Kedua faktor tersebut secara sinergis meningkatkan jumlah radikal bebas dalam tubuh (Winarsi, 2010).
2.3.4 Tahap Pembentukan Radikal Bebas
Secara umum, tahapan reaksi pembentukan radikal bebas melalui tiga tahapan reaksi berikut
1. Tahap inisiasi, yaitu awal pembentukan radikal bebas, menjadikan senyawa non radikal menjadi radikal. Misalnya:
Fe ++ + H2O2 Fe +++ + OH- + •OH
R1 _H + •OH R1• + H2O
2. Tahap propagasi, yaitu pemanjangan rantai radikal, dimana reaksi berantai radikal bebas diperluas sehingga membentuk beberapa radikal bebas baru.
R2_H + R1• R2 • + R1_H R3_H + R2• R3 • + R2_H
3. Tahap terminasi, yaitu pembentukan non radikal dari radikal bebas, bereaksinya senyawa radikal dengan radikal lain atau dengan penangkap radikal, sehingga potensi propagasinya rendah..
R1 • + R1 • R1_R1 R2 • + R1 • R2_R1
R2 • + R2 • R2_R2 dan seterusnya (Winarsi, 2010) : 2.3.5 Senyawa Oksigen Reaktif
Pada dasarnya radikal bebas dapat terbentuk melalui dua cara, yaitu secara endogen (sebagai respon normal proses biokimia intrasel maupun ekstrasel) dan secara eksogen (misalnya dari polusi, makanan, serta injeksi ataupun absorpsi melalui kulit) (Supari, 1996).
Teraktivasinya oksigen dapat menyebabkan terbentuknya radikal bebas oksigen, yang disebut anion superoksida (O2● ). Secara invitro senyawa radikal ini akan
membentuk kompleks dengan senyawa organik. Banyak faktor yang menyebabkan senyawa tersebut membentuk kompleks, antara lain adanya sifat permukaan membran, muatan listrik, sifat pengikatan makromolekul, dan bagian enzim, substrat, maupun katalisator. Senyawa kompleks ini dapat terjadi pada berbagai sel yang masih normal maupun tidak normal atau telah teraktivasi (Belleville-Nabet, 1996).
Radikal bebas, yang sering disebut senyawa oksigen reaktif (SOR), dapat dibentuk melalui jalur enzimatis ataupun metabolik. Senyawa oksigen reaktif juga dapat diproduksi oleh sel dalam kondisi stres ataupun tidak stres. Pada kondisi tidak stres, terdapat keseimbangan antara proses pembentukan dan pemusnahan senyawa oksigen reaktif. Sementara pada kondisi stres oksidatif, pembentukan senyawa oksigen reaktif lebih tinggi dibandingkan dengan pemusnahannya. Akibatnya, sistem pertahanan tubuh terpacu untuk bekerja lebih keras untuk memusnahkan senyawa oksigen reaktif. Salah satu sistem pertahanan tubuh itu adalah sistem antioksidan enzimatis dan non enzimatis, yang bekerja menekan senyawa oksigen reaktif yang berlebihan. Oksigen teraktivasi juga dapat terbentuk karena fungsi enzim atau sistem transfer elektron terganggu. Sebagai akibatnya adalah gangguan metabolik yang mengakibatkan stres oksidatif (Winarsi, 2010).
Senyawa oksigen reaktif berasal dari oksigen (O2), yaitu senyawa yang sangat
digunakan organisme aerob untuk menghasilkan energi berupa ATP, melalui proses fosforilasi oksidatif dalam mitokondria, dengan reaksi sebagai berikut.
2NADH + 2H+ + O2 2NAD+ + 2H2O + energi
ADP + energi ATP
Dalam proses ini, 1 molekul oksigen akan tereduksi menjadi 2 molekul air menurut reaksi sebagai berikut.
O2 + 4H+ + 4e- 2H2O
Reduksi satu molekul oksigen menjadi dua molekul air terjadi dengan memindahkan empat elektron. Namun dalam keadaan tertentu, proses pemindahan elektron ini tidak terjadi secara sempurna, sehingga mengakibatkan terjadinya senyawa oksigen reaktif. Adapun tahapan pembentukan senyawa oksigen reaktif adalah sebagai berikut. O2 + e - O2-• O2 + e- + H+ • OOH O2 + 2e- + 2H + H2O2 O2 + 3e- + 3H + • OH + H2O O2 + 4e - + 4H + 2H2O
Dari tahapan reaksi tersebut, tampak bahwa radikal ion superoksida, radikal peroksil, hidrogen peroksida, dan radikal hidroksil terbentuk sebagai akibat pemindahan elektron yang kurang sempurna dalam proses reduksi oksigen (Winarsi, 2010).
Radikal bebas dan senyawa oksigen reaktif menyebabkan stres oksidatif yang mengakibatkan berbagai penyakit. Kejadian ini diawali oleh reaksi oksidasi dalam tubuh. Bahkan meningkatnya kejadian penyakit kardiovaskuler, aterosklerosis, diabetes melitus, dan kanker diyakini berkorelasi positif dengan tingginya radikal bebas dan senyawa oksigen reaktif dalam tubuh (Winarsi, 2010).
2.3.5.1 Radikal Ion Superoksida (O2●)
Radikal ion superoksida disebut juga anion superoksida. Senyawa ini diproduksi di beberapa tempat yang memiliki rantai transpor elektron. Oksigen teraktivasi dapat terjadi dalam berbagai bagian sel, termasuk mitokondria, kloroplas, mikrosom, glikosom, peroksisom, dan sitosol (Elstner, 1991).
Pembentukan radikal ion superoksida ini melalui beberapa mekanisme sebagai berikut (Cadenas and Packer, 2002 (a)):
1. Reaksi samping dalam reaksi yang melibakan Fe++, misalnya dalam proses: a. Fosforilasi oksidatif
b. Oksigenasi hemoglobin
c. Hidroksilasi oleh enzim monooksigenase (dalam sitokrom P450 dan
sitokrom b4)
d. Fe++ + O2 Fe+++ + O2•
-2. Reaksi dalam mitokondria dan granulosit yang dikatalisis oleh NADH/NADPH oksidase.
NADH + O2 NAD+ + H+ + O2•
-3. Reaksi yang dikatalisis oleh xantin oksidase (XO) XH + H2O + 2 O2 XO X-OH + 2 O2•- + 2 H+
Xantin Asam urat
Dalam keadaan normal, di dalam sel mamalia tidak terdapat enzim xantin oksidase. Enzim ini berasal dari enzim xantin dehidrogenase (XD) yang mengalami proteolisis dan berubah menjadi xantin oksidase (XO), ketika terjadi iskemia atau hipoksia.
XD XO + peptida
Xantin oksidase
Perubahan xantin dehidrogenase menjadi xantin oksidase bersifat irreversibel. Artinya bila suplai oksigen kembali normal maka akan terbentuk senyawa lain, yaitu ion superoksida yang lebih reaktif yang mengakibatkan kerusakan jaringan.
2.3.5.2 Radikal Peroksil (●OOH)
Sebetulnya ion superoksida tidak terlalu reaktif bila dibandingkan dengan bentuk perubahannya yang berupa radikal peroksil.
O2•- + H+ ●OOH
Radikal peroksil
Radikal peroksil ini sangat reaktif, dan akan membentuk radikal baru melalui reaksi sebagai berikut.
●OOH + XH ●X + H2O2
Dari reaksi ini terlihat bahwa radikal peroksil lebih berbahaya daripada H2O2 (Cadenas
and Packer, 2002 (a); Winarsi, 2007). 2.3.5.3 Hidrogen Peroksida (H2O 2)
Hidrogen peroksida (H2O2) terbentuk karena aktivitas enzim-enzim oksidase
yang mengkatalisis reaksi dalam retikulo endoplasmik (mikrosom) dan peroksisom. RH2 + O2 R + H2O2
Hidrogen peroksida merupakan senyawa oksidan yang sangat kuat dan dapat mengoksidasi berbagai senyawa dalam sel, seperti glutation.
2GSH + H2O2 GSSG + 2H2O
Hidrogen peroksida tidak hanya bersifat sebagai oksidator, melainkan juga dapat membentuk radikal bebas, bila bereaksi dengan logam transisi seperti Fe++ dan Cu+ dalam reaksi Fenton.
Fe++ + H2O2 Fe+++ + OH- + ●OH
Cu+ + H2O2 Cu ++ + OH- + ●OH
Efek negatif yang lain dari oksidator hidrogen peroksida adalah kemampuannya untuk membentuk ion hipoklorit (ClO-) melalui reaksi yang dikatalisis oleh enzim mieloperoksidase dalam sel inflamasi, seperti granulosit, monosit, dan makrofag (Cadenas and Packer, 2002 (a)).
H2O2 + Cl- H2O + ClO-
R + ClO- RO + Cl-
2.3.5.4 Radikal Hidroksil (●OH)
Keberadaan senyawa H2O2 dapat berbahaya bila bersama-sama ion superoksida
O2●- + H2O2 O2 + OH- + ●OH
Reaksi Haber-Weiss memerlukan ion Fe+++ atau Cu++ dan terjadi melaui dua tahap.
Fe+++ + O2●- Fe++ + O2
Fe+++ + H2O2 Fe+++ + OH- + ●OH
Dari berbagai bentuk senyawa oksigen reaktif tersebut, radikal hiroksil merupakan senyawa yang paling reaktif dan berbahaya. Radikal hidroksil bukan merupakan produk primer proses biologis, melainkan berasal dari H2O2 dan O2●-
(Cadenas and Packer, 2002 (a); Winarsi, 2007). 2.3.5.5 Singlet Oksigen (1O2)
Singlet oksigen merupakan bentuk oksigen yang memiliki reaktivitas jauh lebih tinggi dibandingkan dengan oksigen bentuk ground state. Senyawa ini akan terbentuk melaui reaksi yang dikatalisis oleh enzim-enzim (Cadenas and Packer, 2002 (a); Winarsi, 2007):
a. Enzim monooksigenase yang menggunakan sitokrom P450 dengan substrat
peroksida.
b. Enzim prostaglandin endoperoksida sintetase, yaitu suatu enzim yang bekerja dalam pembentukan prostaglandin dalam asam arakidonat.
c. Enzim mieloperoksidase, yang mengkatalisis reaksi hipoklorit dengan H2O2.
2.3.6 Stres Oksidatif
Tubuh dapat mengatasi radikal bebas, namun jika radikal bebas yang dihasilkan melebihi antioksidan dapat menyebabkan stres oksidatif (Wiyono, 2003). Stres
oksidatif adalah suatu keadaan ketika jumlah antioksidan tubuh kurang dari yang diperlukan, untuk meredam efek buruk radikal bebas, yang dapat merusak membran sel, protein dan DNA, dan berakibat fatal bagi kelangsungan hidup sel atau jaringan. Jika hal ini terjadi dalam waktu yang berkepanjangan, maka akan terjadi penumpukan hasil kerusakan oksidatif di dalam sel dan jaringan yang akan menyebabkan sel atau jaringan tersebut kehilangan fungsinya dan akhirnya mati (Bagiada, 2001).
2.3.6.1 Dampak Negatif Senyawa Oksigen reaktif
Senyawa oksigen reaktif merusak komponen sel, sehingga ketahanan integritas dan kehidupan sel terganggu. Dampak dari senyawa oksigen reaktif sangat luas dan mekanisme molekulernya masih belum terkuak secara jelas (Bagiada, 2001).
2.3.6.2 Dampak Negatif Radikal Hidroksil
Radikal hidroksil merupakan senyawa yang paling berbahaya. Merusak tiga jenis senyawa. yang penting untuk mempertahankan integritas sel (Halliwel dan Cross, 1994), yaitu:
a. Asam lemak tak jenuh yang merupakan komponen penting fosfolipid penyusun membran sel.
b. DNA, yang merupakan perangkat genetik
c. Protein, yang memegang berbagai peran penting, seperti enzim, reseptor, antibodi dan penyusun matriks serta sitoskeleton.
Dampak terhadap membran sel, dapat menyerang komponen penting membran sel seperti: asam linoleat, linolenat dan arakidonat, yang dapat menimbulkan reaksi rantai peroksidasi lipid. Terputusnya rantai asam lemak tidak jenuh menghasilkan
senyawa toksik seperti: aldehid, MDA, 9-OH noneal,etana, F2-Isoprostan dan lain-lain.
Juga dapat membentuk ikatan silang (cross-linking) (Cadenas and Packer, 2002 (a) (b); Winarsi, 2007).
Dampak terhadap DNA, hidroksilasi basa timin dan sitosin, pembukaan inti purin dan pirimidin serta terputusnya rantai fosfodiester DNA, replikasi sel terganggu. Terjadi mutasi, bila sistim perbaikan DNA terlampaui atau terjadi error prone (bila sistim perbaikan DNA salah) (Winarsi, 2007). DNA mitokondria (mtDNA) merupakan target utama senyawa oksigen reaktif (SOR). Paparan senyawa oksigen reaktif pada mtDNA, ditemukan pada penderita berbagai penyakit degeneratif yang berkaitan dengan aging. Akibatnya adalah penurunan fungsi mitokondria, dan bahkan kerusakan pada mtDNA. Kerusakan pada mitokondria , dapat digunakan sebagai biomarker pada penyakit-penyakit yang diakibatkan oleh senyawa oksigen reaktif (Yakes and Van Houten, 1997).
Dampak terhadap protein, terjadi reaksi dengan asam amino penyusun protein dan yang paling rawan adalah sistein (SH)= ikatan sulf hidril
RSH + •OH RS• + H2O
RS. + RS. R-S-S-R
Ikatan S-S (disulfida linkage), menyebabkan protein kehilangan aktivitasnya (Winarsi, 2007)
Melawan/membunuh organisme patogen yang dihasilkan oleh granulosit, makrofag dan monosit. Bila produksi oksidan berlebihan menimbulkan kerusakan jaringan (Bagiada, 2001).
2.3.7 Pengukuran Peroksidasi Lipid
Peroksidasi lipid terjadi dalam beberapa tahapan. Banyak teknik tersedia untuk mengukur tingkat peroksidasi, hilangnya substrat asam lemak penyebab terjadinya rantai peroksidasi lemak, sehingga prinsipnya secara sederhana pengukuran peroksidasi adalah untuk menguji hilangnya asam lemak, salah satunya dengan mengukur kadar f2-isoprostan, yang merupakan produk akhir yang toksik dari
peroksidasi lipid (Cadenas and Packer, 2002 (b)).
F2-isoprostan dapat ditemukan di jaringan dan cairan tubuh (termasuk urin)
manusia dan hewan, yang mengandung f2-isoprostan dan metabolitnya dalam tingkat
rendah ( ̴ 30-40 pg/mL di plasma segar manusia, ̴ 2 ng/mg kreatinin di urin manusia). Tingkat f2-isoprostan in vivo meningkat dalam kondisi stres oksidatif (misalnya dalam
plasma dan urin perokok, dalam nafas penderita asma, pada penderita diabetes, dalam cairan paru yang terpapar O2 tinggi, dalam plasma tikus yang kelebihan beban besi,
dan pada hewan yang diberi perlakuan dengan CCl4. Isoprostan juga dapat terbentuk
dalam makanan, tetapi berkontribusi sedikit untuk kadar plasma pada manusia (Cadenas and Packer, 2002 (a) (b)).
2.4 AKTIVITAS FISIK MAKSIMAL
Olahraga harus menjadi pusat setiap rencana kerja antioksidan yang efektif. Alasannya tanpa olahraga yang teratur, pertahanan dalam tubuh terhadap radikal
bebas, termasuk antioksidan endogen, seperti superoksida dismutase, glutation peroksidase, dan katalase dapat menjadi terlalu rapuh, untuk mempertahankan efek yang optimal (Cooper, 2001).
Namun penting melakukan jenis olahraga yang benar. Artinya mengandalkan olahraga dengan intensitas rendah, yang akan meminimumkan pengeluaran radikal bebas yang berlebihan saat latihan, dan pada saat yang sama meningkatkan jumlah enzim alami, atau antioksidan endogen (Cooper, 2001).
2.4.1 Olahraga Berintensitas Rendah
Olahraga dengan intensitas rendah adalah program olahraga hidup sehat yang paling efektif, termasuk membangun pertahanan melawan radikal bebas (Cooper, 2001). Untuk mendapatkan hasil maksimal dan risiko minimal pada pelatihan diperlukan kondisi lingkungan yang memadai dan takaran pelatihan yang tepat untuk setiap individu meliputi FITT, yaitu Frequency, Intencity, Type, Time. Frekuensi yang dianjurkan tiga hingga lima kali per minggu dengan intensitas kurang lebih 60-85% dari denyut jantung maksimal: 220 – umur (dalam tahun). Latihan didahului pemanasan selama 3-5 menit, dilanjutkan latihan inti 15-60 menit, diakhiri pendinginan 3-5 menit (Giam, 1993).
2.4.2. Latihan Fisik Berlebih
Pelatihan berlebih seringkali akibat dari (Hatfield, 2001): a. Volume latihan terlalu banyak.
b. Intensitas pelatihan terlalu tinggi. c. Durasi pelatihan terlalu panjang.
d. Frekuensi pelatihan terlalu sering
Saat ini, lebih banyak alasan untuk membatasi intensitas latihan, alasan utama pada bahaya yang disebabkan oleh kelebihan radikal bebas, yang mungkin terbentuk selama latihan fisik berat. Latihan dengan intensitas tinggi yang melelahkan dapat meningkatkan kemungkinan berbagai masalah kesehatan, seperti kanker, serangan jantung, katarak, penuaan dini, penurunan kekebalan, dan lain lain (Cooper, 2001).
Dr. Ralph Paffenbarger melakukan studi terhadap 16.936 pria alumni Harvard, berusia 35 sampai 74 tahun. Menurut laporan yang dimuat dalam The New England Journal of Medicine, ditemukan angka kematian lebih rendah bagi pria yang melakukan aktivitas fisik secara teratur, dibandingkan pria yang tidak pernah melakukannya. Laju kematian lebih rendah pada pria yang menghabiskan 2000 kalori atau lebih per minggu. Akan tetapi, pada tingkat intensitas tinggi, olahraga kurang bermanfaat. Angka kematian mulai meningkat diantara pria yang menghabiskan lebih dari 3000 kalori per minggu (Cooper, 2001).
2.4.3 Hubungan Latihan Berlebihan dan Kerusakan karena Radikal bebas
Pada keadaan normal, radikal bebas terbentuk secara amat perlahan, kemudian dinetralisasi oleh antioksidan dalam tubuh. Namun jika laju pembentukan radikal bebas sangat meningkat karena dipicu latihan yang berlebihan, jumlah radikal akan melebihi kemampuan sistem pertahanan tubuh, menyerang membran sel, sehingga terjadi kerusakan sel-sel pada otot dan tulang. Kerusakan dan peradangan jaringan yang sering menyertai olahraga yang menghabiskan tenaga, merupakan tanda paling jelas adanya kegiatan radikal bebas (Cooper, 2001).
2.4.4 Pembentukan Radikal Bebas Pada Latihan Fisik Berlebih Radikal bebas terbentuk selama berolahraga melalui dua cara: 1. Pelepasan Elektron
Saat berolahraga terjadi pelepasan elektron, olahraga berlebihan menyebabkan terjadi peningkatan konsumsi oksigen oleh tubuh 10-20 kali atau lebih. Dalam serat otot yang berkontraksi penggunaan oksigen dapat meningkat 100-200 kali di atas kebutuhan normal. Peningkatan oksigen yang luar biasa memicu pelepasan radikal bebas , terutama radikal superoksida (Clarkson, 2000; Cooper, 2001; Sauza, 2005).
2. Fenomena Reperfusion Injury
Saat berolahraga berat, darah yang mengalir dalam tubuh keluar dari berbagai organ yang tidak terlibat secara aktif dalam proses. Namun darah dialirkan ke otot skelet. Selama pengalihan aliran darah, sebagian atau seluruh bagian organ tubuh yang tidak terlibat dalam olahraga akan mengalami kekurangan oksigen secara tiba-tiba (hipoksia). Proses iskemia yang terjadi menyebabkan perubahan enzim xantin dehidrogenase menjadi xantin oksidase, dimana perubahannya bersifat ireversibel. Setelah berolahraga terjadi proses reperfusi, dimana darah bergerak kembali dengan cepat ke berbagai organ yang kekurangan aliran darah sehingga oksigen terpenuhi kembali, reaksi yang terjadi dipengaruhi oleh xantin oksidase. Reaksi ini menghasilkan radikal bebas sehingga menimbulkan reperfusion injury (injury yang terjadi setelah terjadinya reperfusi setelah mengalami iskemia (Langseth, 1996; Cooper 2001)).
2.4.5 Hasil Pengukuran Radikal Bebas Saat Berolahraga
Saat ini tidak terdapat penanda diagnosis tunggal untuk latihan fisik berlebih. Pemeriksaan yang tersedia untuk memeriksa respon biomarker terhadap latihan (Margonis et al., 2007). Pengukuran radikal bebas terutama pada proses oksidasi lemak, yang dikenal sebagai peroksidasi lipid. Proses ini membentuk sisa metabolisme, salah satunya dikenal sebagai thiobarbituric acid reactive substance (TBARS) (Cooper, 2001; Cadenas and Packer, 2002 (a)), yang merupakan tes yang tertua untuk mengukur peroksidasi lipid, merupakan pengujian yang sederhana, tetapi kesederhanaan melakukan uji ini memungkinkan kompleksitas kimianya (Cadenas dan Packer, 2002 (a)).
Pemeriksaan respon biomarker terhadap latihan ketahanan yang dilakukan pada 12 orang laki-laki berusia 21 tahun, yang dilakukan selama 12 minggu, dimana latihan pada masing-masing sesi dilakukan selama tiga minggu. Pada sesi pertama dilakukan latihan dua kali seminggu. Sesi kedua delapan kali seminggu. Sesi ketiga 14 kali seminggu. Diikuti istirahat total selama tiga minggu. Sampel darah atau urin dikumpulkan pada keadaan basal dan 96 jam pascalatihan terakhir pada tiap sesi. Hasilnya menunjukkan adanya leukositosis, peningkatan isoprostan dalam urin (7-fold), TBARS (56%), katalase (96%), gluthatione peroxidase, serta gluthatione yang teroksidasi (GSSG) (25%). Sebaliknya terjadi penurunan gluthatione tereduksi (GSH) (31%), GSH/GSSG (56%), dan kapasitas total antioksidan. Dapat disimpulkan, latihan fisik berlebih merangsang respon terhadap biomarker stres oksidatif (Margonis et al., 2007).
2.5 ANTIOKSIDAN 2.5.1 Definisi Antioksidan
Dalam pengertian kimia, senyawa antioksidan adalah senyawa pemberi elektron (elektron donors). Secara biologis, pengertian antioksidan adalah senyawa yang mampu menangkal atau meredam dampak negatif oksidan dalam tubuh. Antioksidan bekerja dengan cara mendonorkan satu elektronnya kepada senyawa yang bersifat oksidan sehingga aktivitas senyawa oksidan tersebut dihambat (Winarsi, 2007), termasuk enzim - enzim dan protein - protein pengikat logam (Pangkahila, 2007). 2.5.2 Klasifikasi antioksidan
2.5.2.1 Klasifikasi antioksidan secara umum
1. Antioksidan Enzimatis, misalnya enzim superoksida dismutase (SOD), katalase, dan glutation peroksidase.
2. Antioksidan Non Enzimatis
a. Antioksidan larut lemak, seperti -tokoferol, karotenoid, flavonoid, quinon, dan bilirubin.
b. Antioksidan larut air, seperti asam askorbat, asam urat, protein pengikat logam, dan protein pengikat heme. (Miyazaki et al., 2000; Winarsi, 2007).
Antioksidan enzimatis dan non enzimatis tersebut bekerja sama memerangi aktivitas senyawa oksidan dalam tubuh. Terjadinya stres oksidatif dapat dihambat oleh kerja enzim-enzim antioksidan dalam tubuh dan antioksidan non enzimatik (Miyazaki et al, 2000; Winarsi, 2007).
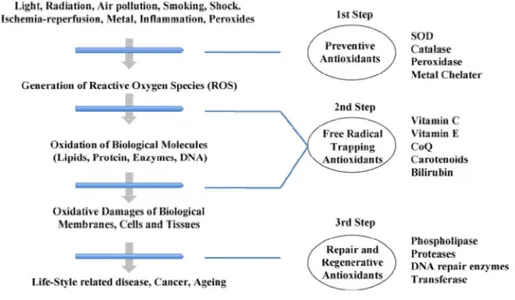
2.5.2.2 Klasifikasi berdasar mekanisme pencegahan dampak negatif oksidan 1. Antioksidan pencegah ( preventive antioxidants).
Pada dasarnya tujuan antioksidan jenis ini mencegah terjadinya radikal hidroksil, yaitu radikal yang paling berbahaya. Untuk membentuk radikal hidroksil diperlukan tiga komponen, yaitu : logam transisi Fe atau Cu, H2O2 dan O2• - Agar
reaksi Fenton ((Fe++(Cu+) + H2O2 Fe+++ ( Cu++ ) + OH - + • OH ))
tidak terjadi, maka harus dicegah keberadaan ion Fe++ atau Cu+ bebas. Untuk itu berperan beberapa protein penting, yaitu :
a. Untuk Fe transferin atau feritin
b. Untuk Cu : seruloplasmin atau albumin
Penimbunan O2• - dicegah oleh enzim superoksida dismutase (SOD) dengan
mengkatalisis reaksi dismutasi O2•-.
2O2 • - + 2H SOD H2O2 + O2
Enzim SOD melindungi sel-sel tubuh dan mencegah terjadinya proses peradangan yang diakibatkan oleh radikal bebas.
Penimbunan hidrogen peroksida (H2O2) dicegah melalui aktivitas dua enzim,
yaitu :
a. Katalase, yaitu enzim yang mengandung heme, yang mengkatalisis reaksi dismutasi H2O2 menjadi air dan oksigen, dimana katalase mampu
mengoksidasi satu molekul hidrogen peroksida menjadi oksigen, kemudian secara simultan mereduksi molekul hidrogen peroksida kedua menjadi air. 2H2O2 2H2O + O2
b. Peroksidase, yang mengkatalisis reaksi sebagai berikut : R + H2O2 RO + H2O
Diantara berbagai peroksidase, yang paling penting adalah gluthation peroksidase (GSPx), yang mengkatalisis reaksi :
2GSH + H2O2 GSSG + 2H2O
Apabila radikal hidroksil masih saja terbentuk, masih ada sarana lain untuk meredamnya, tanpa memberi kesempatan untuk memulai reaksi rantai dengan melibatkan senyawa-senyawa yang mengandung sulhidril seperti gluthation dan sistein.
Gluthation ( GSH ) :
GSH + • OH GS• + H2O
2GS• GSSG Sistein ( Cys-SH ) :
Cys-SH + •OH Cys-S • + H2O
2 Cys • Cys-S-S-Cys 2. Antioksidan pemutus reaksi rantai ( chain-breaking antioxidants).
Dalam kelompok antioksidan ini termasuk vitramin E (tokoferol), asam askorbat ( vitamin C ), β –karoten. Vitamin E dan β -karoten bersifat lipofilik, sehingga dapat berperan pada membran sel untuk mencegah peroksidasi lipid. Sebaliknya, vitamin C, gluthation dan sistein bersifat hidrofilik, dan berperan dalam sitosol ((Frei, 1999; Milner, 2000; Murray et al., 2000).
Gambar 2.1 Korelasi hubungan antioksidan dalam sistem biologi (Yuji et al, 2010) 2.6 PROPOLIS
Propolis atau lem lebah adalah suatu zat yang dihasilkan oleh lebah madu, mengandung resin dan lilin lebah, bersifat lengket yang dikumpulkan dari sumber tanaman, terutama dari bunga dan pucuk daun, untuk kemudian dicampur dengan air liur lebah (Marcucci et al., 2001, Salatino et al., 2005; Nakajima et al., 2009). Asal tanaman penghasil propolis belum dapat diketahui semuanya, yang saat ini diketahui adalah berasal dari getah resin tanaman kelompok pinus dan akasia. Propolis digunakan untuk menutup sel-sel atau ruang heksagonal pada sarang lebah. Biasanya, propolis menutup celah kecil berukuran 4-6 mm, sedangkan celah yang lebih besar diisi oleh lilin lebah. Dahulu peternak lebah di Amerika Serikat menganggap propolis sebagai bahan pengganggu, sebab melekat di tangan, pakaian, dan sepatu ketika cuaca panas, serta berubah keras dan berkerak ketika dingin (Salatino et al., 2005).
Salah satu jenis lebah yang mampu menghasilkan propolis dalam jumlah banyak yaitu jenis Trigona sp (Sabir, 2009). Spesies lebah madu yang juga aktif mencari propolis adalah Apis Mellifera (Salatino et al., 2005).Hanya lebah betina pekerja yang bertugas mencari polen sebagai bahan baku propolis, mengolah propolis dari berbagai bahan seperti pucuk daun, getah tumbuhan, dan kulit beragam tumbuhan seperti akasia dan pinus. Lebah jantan tidak mempunyai kantong polen di bagian tibia atau tungkai kaki dan tanpa kelenjar malam, itulah sebabnya tidak mampu mencari dan mengangkut polen ke sarang. Lebah madu cenderung menyesuaikan jadwal penerbangannya pada saat bunga-bunga dari spesies yang dikunjungi mulai mekar dan menghasilkan serbuk sari, dan di luar itu tetap berada di sarang (Ensiklopedi Indonesia, 2003).
Gambar 2.2. Lebah Penghasil Propolis
Propolis
2.6.1. Karakteristik Propolis
Warna propolis bervariasi, dari kuning, hijau hingga coklat tua, tergantung pada sumber tumbuhannya, seperti propolis Brazil (Cuba) berwarna kehijauan (Salatino, 2005). Propolis merupakan substansi resin alami yang mempunyai aroma wangi, sangat lengket pada suhu sarang saat baru dibentuk, mengeras pada suhu 150C, dan menjadi mudah pecah di bawah suhu 50C. Pada suhu 250-450 C, propolis bersifat lembut, elastis dan sangat lengket. Di atas suhu 450C, propolis semakin lengket seperti karet. Sementara pada suhu 600 dan 700-1000C propolis akan mencair (Krell, 1996).
Gambar 2.3. Propolis Trigona sp 2.6.2. Kandungan Propolis
Propolis terdiri dari resin (50%), wax (30%), essential oils (10%), pollen (5%), dan komponen organik (5%) (Gomez et al., 2006). Resin mengandung flavonoid, fenol, dan berbagai bentuk asam (Borelli et al., 2002). Salah satu ikatan fenol yang ada dalam propolis yaitu Caffeic Acid Phenethyl Ester (CAPE) (Viuda et al., 2008). CAPE merupakan sisi aktif flavonoid yang bekerja untuk memaksimalkan aktivitas scavenger terhadap radikal bebas, dengan cara menurunkan aktivitas radikal hidroksil (●OH) sehingga tidak terlalu reaktif lagi (Cadenas and Packer, 2002 (c)).
Propolis mengandung 16 asam amino essensial yang dibutuhkan untuk regenerasi sel. Dari semua asam amino yang terdapat dalam propolis, arginin dan prolin tergolong yang terbanyak, sekitar 45,8%. Propolis mengandung semua mineral, kecuali sulfur. Zat besi (Fe) dan seng (Zn) adalah kandungan yang terbanyak. Kandungan mineral ini sangat dipengaruhi oleh lingkungan tempat tumbuh tanaman. Propolis juga mengandung vitamin, di antaranya vitamin A, vitamin B (B1, B2, B6), vitamin C, vitamin E dan vitamin D (Krell, 1996; Wikipedia, 2010).
Gambar. 2.4. Chemical structures of the most important flavonoids found in honey and propolis (Viuda et al., 2008) .
2.6.3. Jenis-Jenis propolis
Berikut ini adalah beberapa bentuk propolis yang sudah diproduksi massal (Krell, 1996):
1. Propolis mentah, yaitu propolis tanpa melalui proses pematangan (mentah), bisa langsung dikonsumsi. Umumnya berbentuk bongkahan atau dibekukan.
Bongkahan besar propolis murni dapat dikunyah, seperti permen karet. Namun sebaiknya dikonsumsi dalam jumlah sedikit, jika berlebihan menyebabkan gangguan pada perut. Selain itu ada propolis mentah yang dihancurkan hingga menjadi butiran halus. Butiran halus biasanya dimasukkan dalam kapsul atau dicampur dengan makanan dan minuman.
2. Propolis cair, adalah propolis bentuk cair, yang telah diekstrak dengan jenis pelarut tertentu. Ada banyak jenis pelarut yang dapat digunakan, di antaranya etanol (alkohol), air, pelarut minyak sayur atau lemak hewan.
3. Propolis bubuk (powder). Sebelum diproses menjadi bentuk bubuk atau powder, propolis mentah (raw propolis) terlebih dahulu diekstrak dengan alkohol, air, atau ekstrak glikol. Bentuk propolis bubuk di pasaran dapat ditemukan dalam bentuk tablet atau kapsul.
4. Injeksi. Hingga kini ketersediaan propolis injeksi masih dalam penelitian.
5. Pasta dan minyak propolis. Salah satunya adalah pasta gigi propolis, yang bermanfaat untuk mencegah karies, radang gusi, dan sariawan. Selain dalam bentuk pasta, propolis juga bisa dicampur dengan minyak atau krim untuk dioleskan.
2.6.4.Ekstraksi Propolis
Ekstraksi propolis membutuhkan pelarut. Pemilihan cairan pelarut tergantung pada tujuan penggunaan propolis dan tehnik yang ada. Selama ini, ekstraksi propolis menggunakan ethanol, propilen glikol, atau air. Ethanol dan glikol dapat melarutkan seluruh zat aktif.
Bahannya merupakan propolis mentah, untuk mengetahui propolis mentah yang masih berkualitas adalah dengan mencampur propolis sebanyak setengah sendok teh dengan secangkir susu, lalu biarkan selama empat hari pada suhu hangat. Jika susu tetap segar, berarti propolis masih baik. Sebaliknya jika fisik susu berubah, berarti propolis sudah tidak baik. Cara pertama dilakukan dengan membersihkan propolis dan kotoran yang tampak, juga dari lilin yang berlebihan. Caranya propolis dihaluskan menjadi butiran kecil atau bubuk halus. Jika propolis terlalu lengket dan sulit dihaluskan, sebaiknya propolis disimpan dahulu dalam freezer atau lemari es selama beberpa jam hingga menjadi keras dan rapuh. Propolis yang lengket, bisa dibuat setipis mungkin untuk menigkatkan kontak permukaan antara alkohol dengan propolis, sehingga pelarutan mudah dilakukan.
Alat dan bahan yang digunakan untuk melakukan proses ekstraksi skala industri kecil sebagai berikut:
1. Botol berkapasitas besar yang dapat ditutup rapat.
2. Timbangan yang cukup sensitif untuk menimbang jumlah kecil. 3. Kertas filter, kain katun berlapis, atau bola kapas sebagai saringan. 4. Lemari es atau freezer, meski tidak terlalu pentng.
5. Sumber panas, seperti perangkat destilasi, pengering vakum, atau pengering beku, berguna untuk menguapkan pelarut (Krell, 1996).
2.6.5. Teknik Ekstraksi
Hingga kini belum ada standarisasi tentang konsentrasi, metode ekstraksi, dan jenis pelarut yang akan dipakai.
Tehnik Ekstraksi Propolis Alkohol
Ekstraksi propolis alkohol merupakan proses ekstraksi yang paling banyak dilakukan. Alkohol yang biasanya digunakan adalah etanol. Ekstrak propolis yang digunakan pada manusia, pemilihan jenis alkohol lebih berupa gin, rum, cachasa, arak atau cairan destilasi lainnya. Cairan alkohol ini memang mengandung kurang dari 70% alkohol, tetapi hasilnya tetap berkualitas .
Berdasarkan penelitian, ekstraksi yang menghasilkan zat aktif terbanyak adalah propolis yang dilarutkan dalam alkohol 70%. Semakin lama direndam dalam alkohol, propolis akan semakin larut. Idealnya, lama waktu pelarutan maksimum 2-3 minggu. Prosedur ekstraksi dengan alkohol:
a. Prosedur yang saat ini digunakan untuk industri skala kecil adalah dengan perbandingan propolis alkohol sebesar 5-10%. Artinya rasio berat propolis dengan berat pelarut berkisar 5-10%. Sementara itu, konsentrasi awal propolis yang akan diekstraksi tidak boleh lebih dari 30%, jika lebih ekstraksi akan kurang efisien dan kurang lengkap.
b. Timbang jumlah propolis dan hitung volume alkohol yang digunakan. Sebaiknya, berat alkohol ditimbang agar dapat dibandingkan dengan berat propolis. Secara sederhana, 1 liter alkohol 100% beratnya 800 gram, dan 1 liter alkohol 70% beratnya 860 gram. Menimbang alkohol lebih dipilih daripada menghitung volume alkohol karena lebih akurat.
c. Selanjutnya, alkohol dan propolis dimasukkan ke dalam satu wadah, tutup rapat, lalu kocok pelan-pelan. Pengocokan dilakukan sekali sampai dua kali setiap
harinya. Wadah disimpan dalam tempat yang gelap dan hangat, setidaknya selama tiga hari. Untuk hasil terbaik, biasanya ekstraksi memerlukan waktu 1-2 minggu. d. Untuk mempercepat proses ekstraksi, rebus campuran alkohol dengan propolis
selama delapan jam untuk melarutkan semua resin yang ada. Namun untuk mendapat kualitas ekstrak propolis yang terbaik, pemanasan ini sebaiknya dihindari.
e. Setelah disimpan, cairan disaring dengan kertas filter, kain halus, atau kapas. Kain dibuat berlapis agar penyaringan lebih efektif. Lebih baik lagi jika ditambahkan saringan lagi di bawahnya. Sisa saringan pertama masih bisa diekstrak lagi melalui prosedur yang sama. Untuk mendapat hasil yang maksimal, satu hari sebelum proses penyaringan, campuran propolis disimpan dalam lemari es, dengan suhu dibawah 4oC, tetapi jangan sampai membeku. Sebaiknya, saringan juga dibersihkan sebelum digunakan.
f. Hasil penyaringan akan berupa cairan jernih, bebas dari pertikel, dan berwarna cokelat tua atau sedikit kemerahan. Simpan hasil penyaringan dalam botol bersih berwarna gelap dan hampa udara. Jika botol tidak berwarna gelap, letakkan saja botol di tempat gelap, dingin, atau dibungkus dengan kain atau kertas, lalu jauhkan dari cahaya matahari.
Contoh:
Untuk membuat propolis alkohol 10%, campurkan satu bagian propolis dengan sembilan bagian alkohol. Jadi untuk 100 gram propolis, diperlukan campuran pelarut alkohol sebanyak 900 gram. Begitu juga untuk 1kg propolis, perlu ditambahkan 9 kg
alkohol. Sementara, untuk membuat propolis alkohol 55, perbandingan yang dibutuhkan adalah satu bagian propolis dengan 19 bagian alkohol. Untuk mengatasi mahalnya harga pelarut, konsentrasi ekstrak awal dibuat lebih tinggi (sekitar 30%) dan baru diencerkan lagi, tergantung pada tujuan penggunaannya.
Teknik Ekstraksi Propolis Glikol
Metode ini hampir sama dengan metode ekstraksi propolis alkohol, hanya berbeda dari jenis pelarutnya, yaitu glikol dalam bentuk propylene glycol. Perbandingan atau konsentrasi yang dipakai sebaiknya tidak melebihi 10%. Kekurangan teknik ekstraksi ini adalah membutuhkan suhu yang lebih tinggi saat melakukan proses penguapan pelarut, yang tentunya dapat membuat komponen di dalam propolis mudah menguap. Harga glikol biasanya lebih murah dari alkohol. Sayangnya, glikol tidak mudah diperoleh di semua tempat.
Teknik Ekstraksi Propolis Air
Ekstraksi propolis dengan air dilakukan dengan cara melarutkan propolis dalam air selama beberapa hari atau merebusnya dalam air. Metode ekstraksi propolis air sama persis dengan ekstraksi alkohol. Terbatasnya pemanfaatan ekstraksi propolis alkohol, terutama untuk dikonsumsi ibu hamil dan anak, konsumsi di negara muslim, atau faktor kesehatan tertentu, membuat ekstraksi propolis air menjadi penting.
Membuat Ekstrak Propolis di Rumah
Ekstraksi zat aktif dalam propolis juga bisa dilakukan di rumah. Bahannya propolis mentah, Bahan lain yang dibutuhkan adalah pelarut, dapat berupa alkohol, propilen glikol atau air. Cara yang digunakan sama seperti membuat ekstraksi propolis untuk
skala industri, hanya peralatan untuk pembuatan ekstraksi propolis di rumah lebih sederhana (Krell, 1996).
2.6.6 Manfaat dan Bukti Ilmiah Propolis
Propolis dan hasil produk lebah lainnya seperti madu, pollen dan royal jeli, bermanfaat untuk kesehatan. Di antaranya bermanfaat sebagai antioksidan, antibakteri, antiinflamasi, hepatoprotektif, antitumor, dan vasodilator (Viuda et al., 2008; Nakajima et al., 2009).
Manfaat Sebagai Antioksidan
Propolis merupakan produk alami yang mempunyai potensi antioksidan yang tinggi (Gheldof et al., 2002). Propolis mempunyai aktivitas antioksidan yang paling kuat dalam melawan radikal bebas (radikal H2O2, O2-, OH●) dibandingkan dengan hasil
produk lebah lainnya (Nakajima et al., 2009). Kandungan flavonoid di dalamnya dapat meredam efek buruk radikal bebas, dengan menghambat peroksidasi lipid melalui aktivasi peroksidase terhadap hemoglobin, yang merupakan antioksidan endogen (Mot et al., 2009).
Penelitian di Jepang menunjukkan bahwa kandungan Caffeic acid yang ada di dalam propolis mempunyai aktivitas antioksidan yang tinggi, yang dapat meningkatkan ekspresi glucose-6-phospate dehydrogenase (G6PD) yang dikenal sebagai gen antioksidan, lebih kuat dibandingkan vitamin E. Caffeic acid mempunyai aktivitas antioksidan 4-6 kali lebih kuat terhadap radikal H2O2 dan O2-, dibandingkan
vitamin C dan N-acetyl-cystein (NAC) (Nakajima et al., 2009). Potensi kekuatan antioksidan ekstrak propolis dan polen secara berturut-turut, yaitu; ekstrak propolis air,
ekstrak propolis etanol, polen. Seperti yang terlihat pada tabel di bawah ini (Nakajima et al.,2009).
Tabel 2.1. Antioxidant activities of bee products (Nakajima et al., 2009) IC50 (95% confidence limit)
Compounds H2O2 O2·- HO·
Brazilian green propolis (μg/ml)
WEP 0.24 (0.15– 0.34) 0.91 (0.64– 1.21) 4.12 (3.31–5.17) EEP 2.48 (1.65– 4.05) 0.79 (0.56– 1.04) 5.83 (4.99–6.87) Other bee products (μg/ml)
Pollen 9.99 (8.01– 12.3) 8.44 (6.64– 10.4) 57.6 (46.5–69.9) Royal jelly > 100 > 100 > 100 Constituents of propolis (μM)
3,4-di- O-Caffeoylquinic acid 0.52 (0.36– 0.70)
0.25 (0.18–
0.32) 1.86 (1.50–2.31) 3,5-di- O-Caffeoylquinic acid 0.33 (0.16–
0.53) 0.18 (0.13– 0.24) 2.02 (1.51–3.07) 3-Caffeoylquinic acid 0.22 (0.11– 0.35) 0.16 (0.11– 0.22) 2.38 (1.83–3.19) Artepillin C 1.44 (1.16– 1.76) 2.01 (1.38– 2.84) 51.9 (39.1–73.1) Baccharin > 100 > 100 > 100 Coumaric acid > 100 > 100 59.4 (39.1– 102.7) Drupanin 7.35 (5.28– 10.0) 5.24 (3.20– 8.00) 26.4 (17.4–43.4) Caffeic acid 0.28 (0.22– 0.36) 0.13 (0.11– 0.16) 1.82 (1.50–2.23) Quinic acid > 100 > 100 > 100 (bersambung)
IC50 (95% confidence limit)
Compounds H2O2 O2·- HO·
Constituents of royal jelly (μM)
10-Hydroxy decenoic acid > 100 > 100 > 100 Antioxidants (μM) Trolox 0.29 (0.11– 0.59) 0.36 (0.13– 0.75) 1.30 (0.97–1.77) NAC 1.84 (1.02– 4.37) 2.40 (1.46– 4.42) > 100 Ascorbic acid (Vitamin C) 1.53 (1.38–
1.70)
0.70 (0.50–
0.94) 2.07 (0.98–5.81) IC50: 50% inhibitory concentration, WEP: water extract of propolis, EEP: ethanol
extract of propolis, NAC: N-acetyl cysteine.
Manfaat Sebagai Antikanker
Caffeic Acid Phenethyl Ester (CAPE), salah satu bahan aktif dalam propolis, terbukti menghentikan pertumbuhan sel kanker. Hasil penelitian uji sitotoksik serbuk propolis dan madu propolis terhadap sel kanker rahim dan payudara di Laboratorium Penelitian dan Pengujian Terpadu (LPPT) Universitas Gajah Mada (UGM), menunjukkan propolis dapat menghambat sel kanker HeLa (sel kanker serviks), Siha (sel kanker uterus), T47D dan MCF7 (sel kanker payudara). Riset ilmiah itu membuktikan bahwa nilai LC50 62,5 µg/ml. Artinya, propolis dosis
15,625-62,5 µg/ml dapat menghambat aktivitas 50% sel kanker dalam kultur. Dimana nilai LC50 serbuk propolis lebih kecil dibandingkan madu propolis, yang berarti mempunyai
Uji potensi propolis dalam pengobatan tumor mammae pada tikus betina galur Sprague dawley yang diinduksi 7,12-dimethylbenz(a)anthracene (DMBA), menunjukkan bahwa propolis mampu mengobati tumor mammae melalui pengecilan diameter nodul. Sebanyak 40 tikus berumur lima pekan dibagi ke dalam tiga kelompok, yaitu: kelompok kontrol hanya diberi DMBA, kelompok P1 diberikan propolis setelah terpapar tumor, kelompok P2 propolis diberikan sebelum dan setelah terpapar tumor. DMBA dilarutkan dalam minyak jagung dan diinduksikan pada tikus dengan dosis 20 mg/kg bobot tubuh. Dosis propolis yang diberikan adalah 2,5 ml/kgbb, diberikan dua kali per hari selama satu bulan (Astuti dan Widyarini, 2009).
Hasilnya sebulan kemudian diukur, kelompok pertama perkembangan nodul atau benjolan pada tikus semakin membesar, mencapai 87,5% dari delapan ekor tikus yang tersisa. Kelompok kedua dan ketiga memberikan hasil nodul yang semakin mengecil, masing-masing mencapai 69,23% dan 66,66% dari hewan uji. Penelitian itu membuktikan terjadi pengecilan nodul dari diameter 1,8 cm menjadi 0,6 cm setelah satu bulan pemberian propolis (Astuti and Widyarini, 2009).
Manfaat Sebagai Antiinflamasi
Flavonoid yang terdapat di dalam propolis dapat menghambat Cyclooxygenase (COX) dan aktivitas lipo-oxygenase, serta membatasi aktivitas polygalacturonase (Raso et al, 2001; Borelli et al., 2002). Komponen lainnya, yakni Caffeic Acid Phenetyl Ester (CAPE), juga mempunyai aktivitas antiinflamasi dengan menghambat pengeluaran asam arakidonat pada membran sel, dimana menyebabkan penekanan
aktivasi Cyclooxygenase-1(COX-1) dan Cyclooxygenase-2 (COX-2), dan menghambat ekspresi gen dari COX-2 (Mirzoeva and Calder, 1996).
Manfaat sebagai Antiviral
Propolis mempunyai kapasitas untuk menghambat propagasi virus. Beberapa studi in vitro menunjukkan efek propolis pada DNA dan RNA berbagai virus, di antaranya Herpes Simpleks tipe 1 dan 2, Adenovirus tipe 2, virus Ostomatitis Vesikular dan virus Polio tipe 2. Efek diamati berdasarkan reduksi multiplikasi virus dan aksinya (Amoros et al., 1992).
Manfaat Sebagai Antibakteri
Penelitian aktivitas antibakteri flavonoid propolis Trigona sp terhadap bakteri Streptococcus mutans (in vitro), menunjukkan propolis Trigona sp secara signifikan (p<0,05) menghambat pertumbuhan Streptococcus mutans yang diinkubasi selama 24 dan 48 jam (Sabir, 2009).
Hasil penelitian yang dilakukan di bagian parasitologi Fakultas Kedpkteran Universitas Gajah Mada, menunjukkan propolis bermanfaat sebagai immunomodulator. Peneliti membagi tikus menjadi delapan kelompok, empat kelompok pertama diberikan 3,9 mg propolis oral setiap dua hari, selama dua minggu sebelum infeksi, empat kelompok lainnya tidak. Lalu kedua kelompok diberikan Plasmodium Berghei secara intraperitoneal. Setelah itu diberi terapi injeksi klorokuin selama tiga hari, dengan dosis berturut-turut 1,56 mg; 1,56 mg; 0,8 mg. Empat kelompok pertama juga diberikan propolis 3,9 mg setiap hari selain klorokuin. Evaluasi dengan menghitung persentase parasitemia setiap hari dimulai dari hari
pertama setelah infeksi, serta melihat efek parasitologiknya terhadap hati, limpa, ginjal dan otak. Hasilnya propolis tidak menghentikan infeksi, tetapi menghambat pertumbuhan Plasmodium Berghei di sel darah merah, dan memperpanjang harapan hidup dari tikus. Pemeriksaan patologik menunjukkan inflamasi ringan di hati, limpa, ginjal dan hati kelompok tikus yang diberi propolis, jadi propolis mengurangi kerusakan organ (Wijayanti et al., 2003).
Manfaat Sebagai Antiulkus
Propolis dan madu mempunyai kapasitas sebagai antiulkus. Flavonoid meningkatkan kadar prostaglandin pada mukosa, yang dapat meningkatkan efek proteksi pada mukosa lambung, sehingga mencegah ulserasi (Duarte et al, 2001). Penelitian lain menunjukkan ulkus berhubungan dengan Reactive Oxygen Species (ROS) (Marthin et al., 1998). Flavonoid dapat menghambat ROS dengan menghambat peroksidasi lipid, yang dapat meningkatkan aktivitas glutation peroksidase (Duarte et al., 2001).
2.6.7 Toksisitas Propolis
Penelitian di Fakultas Biologi Universitas Gajah Mada, membuktikan bahwa propolis sangat aman dikonsumsi. Uji toksisitas dilakukan untuk menentukan toksisitas propolis yang dikonsumsi berulang dalam waktu sampai tiga bulan. Dalam uji praklinis, LD50 propolis mencapai lebih dari 10.000 mg. LD50 adalah lethal dosage,
yaitu dosis yang mematikan separuh hewan percobaan. Jika dikonversi, dosis itu setara 7 ons sekali konsumsi untuk manusia dengan berat badan 70 kg. Faktanya, dosis konsumsi propolis di masyarakat sangat rendah, hanya 1-2 tetes dalam segelas air
minum. Efek konsumsi jangka panjang, tidak menimbulkan kerusakan pada darah, organ hati, dan ginjal. (Sarto and Saragih, 2009).
Penentuan toksisitas subkronik dilakukan dengan menggunakan mencit jantan, 21 ekor mencit dibagi menjadi tiga kelompok, masing-masing kelompok terdiri dari tujuh ekor, kelompok pertama adalah kelompok kontrol tanpa perlakuan, dua kelompok yang lain diperlakukan dengan dosis propolis 5.000 mg/kgbb dan 10.000 mg/kgbb setiap hari selama 30 hari. Hasil analisis menunjukkan tidak menimbulkan kematian mencit, tidak mempengaruhi berat badan, tidak mengganggu jumlah sel-sel darah dan kadar hemoglobin, tidak mengganggu fungsi hati dan ginjal (tidak mempengaruhi kadar SGOT, SGPT, kreatinin dan asam urat), tidak mempengaruhi kualitas sel-sel hati, ginjal dan lambung (Sarto and Saragih, 2009).
2.7 HEWAN COBA
2.7.1 Penggunaan tikus ( Rattus Norvegicus) di laboratorium
Penggunaan tikus atau rat ( Rattus Norvegicus) telah diketahui sifat-sifatnya dengan sempurna, mudah dipelihara, merupakan hewan yang relatif sehat dan cocok untuk berbagai macam penelitian. Terdapat beberapa galur atau varietas tikus yang memiliki kekhususan tertentu antara lain galur Sprague-dawley yang berwarna albino putih berkepala kecil dan ekornya lebih panjang daripada badannya dan galur Wistar yang ditandai dengan kepala besar dan ekor lebih pendek ( Malole and Pramono, 1989).
Tikus ( Rattus norvegicus ) galur wistar lebih besar dari famili tikus umumnya dimana tikus ini dapat mencapai 40 cm diukur dari hidung sampai ujung ekor dan
berat 140-500 gram. Tikus betina biasanya memiliki ukuran lebih kecil dari tikus jantan dan memiliki kematangan seksual pada umur 4 bulan dan dapat hidup selama 4 tahun ( Kusumawati, 2004)
Tikus laboratorium jantan jarang berkelahi seperti mencit jantan. Tikus dapat tinggal sendirian dalam kandang, asal dapat melihat dan mendengar tikus lain. Jika dipegang dengan cara yang benar, tikus-tikus ini tenang dan mudah ditangani di laboratorium. Pemeliharaan dan makanan tikus lebih mahal daripada mencit, tetapi tikus dapat berbiak sebaik mencit. Karena hewan ini lebih besar daripada mencit, maka untuk beberapa macam percobaan, tikus lebih menguntungkan (Smith and Mangkoewidjojo, 1988).
Dibandingkan dengan tikus liar, tikus laboratorium lebih cepat menjadi dewasa, tidak memperlihatkan perkawinan musiman, dan umumnya lebih mudah berkembang biak. Jika tikus liar dapat hidup dapat hidup 4-5 tahun, tikus laboratorium jarang hidup lebih dari 3 tahun (Smith and Mangkoewidjojo, 1988).
Umumnya berat tikus laboratorium lebih ringan dibandingkan berat tikus liar. Biasanya pada umur empat minggu beratnya 35-40 gram, dan berat dewasa rata-rata 200-250 gram, tetapi bervariasi tergantung pada galur. Tikus jantan tua dapat mencapai 500 gram, tetapi tikus betina jarang lebih dari 350 gram (Smith and Mangkoewidjojo, 1988).
Ada dua sifat yang membedakan tikus dari hewan percobaan lain. Tikus tidak dapat muntah, karena struktur anatomi yang tidak lazim di tempat esofagus bermuara
ke dalam lambung dan tikus tidak mempunyai kandung empedu (Smith and Mangkoewidjojo, 1988).
2.7.2 Pemantauan keselamatan tikus di laboratorium
Pemantauan keselamatan tikus di laboratorium (Smith and Mangkoewidjojo, 1988; Ngatidjan, 2006 ) antara lain :
a. Kandang tikus harus cukup kuat tidak mudah rusak, mudah dibersihkan (satu kali seminggu), mudah dipasang lagi, hewan tidak mudah lepas, harus tahan gigitan dan hewan tampak jelas dari luar. Alas tempat tidur harus mudah menyerap air pada umumnya dipakai serbuk gergaji atau sekam padi.
b. Menciptakan suasana lingkungan yang stabil dan sesuai dengan keperluan fisiologi tikus.(suhu, kelembaban dan kecepatan pertukaran udara yang ekstrim harus dihindari).
c. Untuk tikus dengan berat badan 200-300 gram luas lantai tiap ekor tikus adalah 600 cm2, tinggi 20,0 cm.