9
BAB II
KAJIAN PUSTAKA
A. Karbon Aktif
1. Pengertian Karbon Aktif
Karbon merupakan padatan berpori yang mengandung 85 – 95% karbon, dihasilkan dari bahan-bahan mengandung karbon dengan pemanasan pada suhu tinggi (Meilia, 2009). Untuk membuat karbon, dapat dilakukan dengan membakar bahan karbon pada tempat yang tertutup rapat, sehingga hanya terjadi proses pirolisis. Karbon selain dapat digunakan sebagai bahan bakar, juga menjadi alternatif absorbent.
Karbon aktif adalah karbon yang telah mengalami perlakuan khusus berupa proses aktifasi baik secara fisika maupun secara kimia. Aktifasi tersebut menyebabkan pori-pori yang terdapat pada struktur molekulnya terbuka lebar sehingga daya serapnya akan semakin besar untuk menyerap bahan yang berfase cair maupun berfase gas (Sembiring dkk, 2003).
Karbon aktif biasanya ditemukan dalam dua bentuk yaitu bentuk serbuk dan bentuk butiran. Dalam keadaan ini ukuran yang dipakai adalah mesh. Butiran serbuk berukuran kurang atau sama dengan 325 mesh digunakan untuk absorbsi dalam larutan. Sedangkan untuk butiran yang lebih besar berukuran diatas 325 mesh digunakan dalam pengabsorbsian gas dan uap (Nur Hidayati, 2006). Perbedaan ukuran partikel berpengaruh pada fungsi dari karbon aktif itu sendiri. Selain
10
penggunaannya yang berbeda, karbon aktif serbuk dan butiran juga mempunyai kelebihan dan kekurangan masing-masing. Gambar 1 merupakan karbon aktif dalam bentuk butiran.
Gambar 1. Karbon Aktif Butiran (Granule)
2. Struktur Pori Karbon Aktif
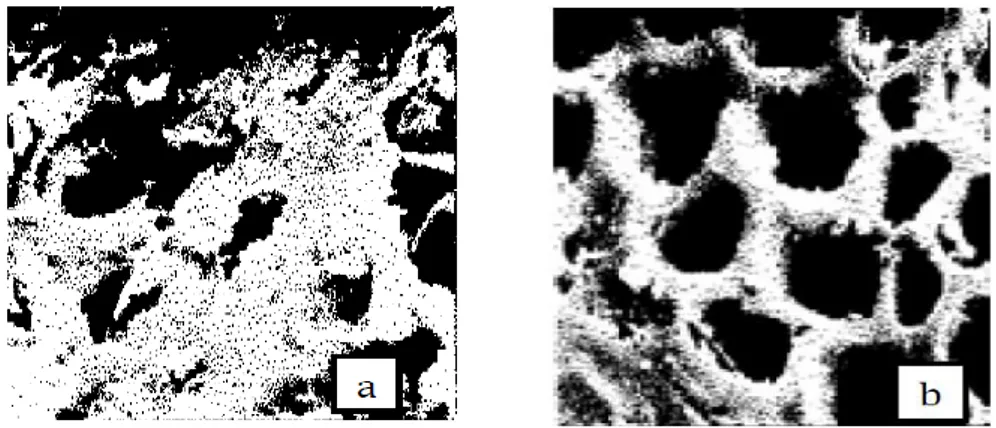
Karbon alami dan karbon aktif merupakan hasil pembakaran bahan seperti kayu, kulit, sabut kelapa, sekam padi, tempurung kelapa dan batu bara. Hanya yang membedakan adalah pemberian perlakuan khusus pada karbon aktif baik secara kimia maupun fisika agar rongga-rongga yang yang terdapat di dalamnya semakin terbuka sehingga daya serapnya semakin tinggi hal tersebut seperti ditunjukkan pada Gambar 2. Mutu karbon aktif dikatakan baik apabila kadar unsur karbon sangat tinggi, sedangkan kadar abu dan air di dalamnya sangat kecil (Unangalim A, 2012).
11
Gambar 2. Struktur Pori karbon a).Struktur Pori Karbon Tanpa Aktifasi b). Struktur Pori Karbon dengan Aktifasi
(Sumber : SinarTani edisi Edisi 6-12 Maret 2011 No.3400 Tahun 2004) Karbon aktif berwarna hitam, tidak berbau, tidak berasa dan mempunyai daya serap yang jauh lebih besar dibandingkan dengan karbon yang belum mengalami proses aktivasi serta mempunyai permukaan yang luas, yaitu antara 300 sampai 2000 m2/gram (Surya Effendy, 2004). Luas permukaan menyebabkan karbon mempunyai kemampuan menyerap gas dan uap atau zat yang berada di dalam suatu larutan (Zuhdi Syakuri, 2005).
Struktur pori pada karbon aktif menurut Elohansen Padang (2004) dapat dibagi menjadi 3 kelas yaitu makropori yang memiliki radius efektif lebih dari 50 nm, volumenya antara 0,2-0,5 cm3/g dan luas permukaan berkisar antara 0,5-2 m2/g, mesopori yang memiliki radius efektif antara 2-50 nm, volumenya antara 0,02-0,1 cm3/g dan luas permukaan merupakan 5% dari total luas permukaan karbon aktif, dan mikropor iyang memiliki radius efektif lebih kecil dari 2 nm, volumenya antara 0,15-0,5 cm3/g dan luas permukaan merupakan 95% dari total luas permukaan karbon aktif.
12 3. Proses Aktivasi
Proses aktifasi pada karbon berguna untuk meningkatkan daya serap (kemampuan absorbent) karbon tersebut, dengan pengaktifan tersebut akan menambah lebar lubang pori pada karbon tersebut sehingga bahan yang terserap juga akan semakin banyak (Sembiring dkk, 2003).. Metoda aktifasi terdiri dari dua macam, yaitu:
a. Aktifasi Kimia
Aktifasi ini merupakan proses pemutusan rantai karbon dari senyawa organik dengan pemakaian bahan-bahan kimia. Aktifator yang digunakan adalah bahan bahan kimia seperti : hidroksida, logam alkali, garam-garam karbonat, klorida, sulfat, fosfor dari logam alkali tanah, dan khususnya ZnCl2, asam-asam anorganik seperti H2SO4 H3PO4 (Unangalim A, 2012).
b. Aktifasi Fisika
Aktivasi fisika bertujuan untuk meregangkan pori-pori karbon sehingga ion-ion logam yang ada dalam limbah akan terjebak masuk dalam pori-pori tersebut. Pada penelitian sebelumnya, aktivasi fisika menggunakan pemanas atau pemanggang (oven). Suhu yang dipakai adalah 200 0C selama 60 menit dengan menempatkan karbon pada loyang. Suhu yang dipakai tidak terlalu tinggi, karena jika suhu yang digunakan terlalu tinggi akan merusak struktur karbon tersebut. Pemanasan bertujuan untuk mengurangi kadar air yang terdapat dalam karbon aktif (Yulia Robiatun K, 2014)
13 B. Bambu
Bambu (Bambuseae) seperti pada Gambar 3 dikenal oleh masyarakat memiliki sifat-sifat yang baik untuk dimanfaatkan, antara lain betangnya kuat, ulet, lurus, rata, keras, mudah dibelah, mudah dibentuk dan mudah dikerjakan serta ringan sehingga mudah diangkat. Selain itu bambu juga relatif murah karena banyak ditemukan di sekitar pemukiman pedesaan, bambu menjadi tanaman serbaguna bagi masyarakat pedesaan (Benefield, 1982).
Dari kurang lebih 1000 spesies bambu dalam 80 genera, sekitar 200 spesies dari 20 genera ditemukan di Asia Tenggara (Dransfield, 1995). Tanaman bambu Indonesia ditemukan di dataran rendah sampai pegunungan dengan ketinggian sekitar 300 m di atas permukaan air laut. Pada umumnya ditemukan ditempat-tempat terbuka dan daerahnya bebas dari genangan air (Siti Tias M, 2012).
Gambar 3. Bambu Wulung
Beberapa sifat kimia bambu meliputi kadar selulosa, lignin, pentosan, abu, silika. Kadar selulosa berkisar antara 42,4%-53,6%, kadar lignin bambu berkisar antara 19,8%-26,6%, sedangkan kadar pentosan 1,24%-3,77%, kadar abu 1,24%-3,77%, kadar silika 0,10%-1,78% (Krisdianto et al, 2000). Dari
14
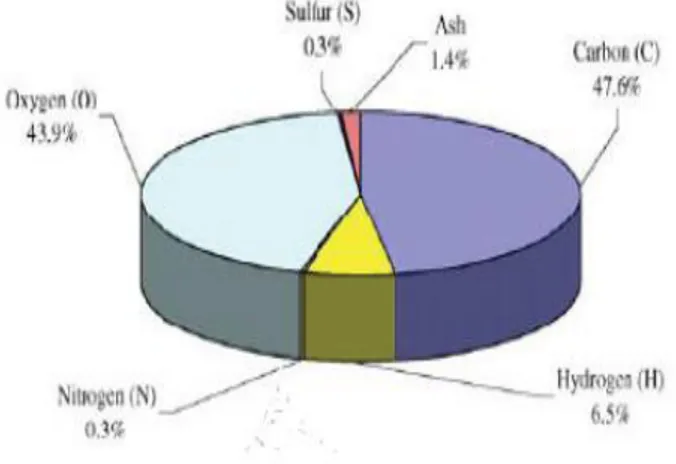
sifat lignoselulosa yang banyak mengandung karbon tersebut terlihat bahwa bambu memiliki kriteria sebagai bahan dasar dari karbon aktif. Gambar 4 menunjukkan elemen-elemen yang terdapat dalam bambu
Gambar 4. Elemen-Elemen yang Terdapat dalam Bambu (Choy et al, 2005)
C. Pasir Pantai Indrayanti
Pantai Indrayanti terletak di desa Tepus, kecamatan Tepus, Gunungkidul, Yogyakarta. Pantai ini memiliki keindahan alam, seperti pasir putih dan biota lautnya, seperti yang ditunjukan pada Gambar 5. Dibalik indahnya pasir putih pantai Indrayanti, ada banyak kandungan mineral seperti silika yang dapat dimanfaatkan sebagai absorben penjernihan air.
Dalam pasir pantai Indrayanti terkandung SiO2 (70,35%); Al2O3 (1,66%); Fe2O3 (8,96%); CaO (3,37%); dan MgO (1,64%) (Ega Tri Rimawati, 2014). Selain sebagai salah satu bahan bangunan, pasir juga sering digunakan sebagai salah satu komponen dalam proses penjernihan air. Biasanya pasir diletakkan pada bagian atas pada tahapan penyaringan karena dapat menangkap kotoran-kotoran sebelum menuju ke komponen penyaring
15
selanjutnya. Dalam hal penyaringan, pasir biasanya digunakan sebagai bahan pelapis dalam sistem penyaringan air (Unangalim A, 2012).
Gambar 5. Pantai Indrayanti di Desa Tepus, Kecamatan Tepus, Gunungkidul, DIY
D. Kerikil Kali Krasak
Kali Krasak merupakan nama sungai yang mengalir dari gunung Merapi ke arah barat daya hingga bermuara ke kali Progo. Kali Krasak seperti pada Gambar 6 terletak di daerah perbatasan antara Yogyakarta dengan Magelang. Di sekitar kali Krasak ini menjadi pusat jual beli pasir kasar (masih ada material batu dan kerikil) dan pasir halus, karena jumlah pasirnya yang sangat melimpah.
Kandungan silika dalam kerikil kali Krasak lebih dari 50% (Bambang Endroyo, 2007). Kerikil dapat digunakan sebagai salah satu bahan absorbent dalam proses filtrasi air. Biasanya kerikil diletakkan pada bagian paling atas setelah pasir pada tahapan penyaringan. Kerikil berguna untuk membantu proses aerosi oksigen dan menahan kotoran yang lebih besar sebelum menuju ke komponen penyaring selanjutnya. Kerikil juga dapat menyerap kandungan logam Fe (besi) dengan baik.
16
Gambar 6. Kali Krasak di Desa Tempel, Kecamatan Tempel, Kabupaten Sleman, DIY
E. Air LPPMP UNY
Lembaga pengembangan dan penjaminan mutu pendidikan UNY merupakan pusat penjaminan mutu, pengembangan kurikulum, instruksional dan sumber belajar, pusat layanan praktek pengalaman lapangan dan praktek kerja lapangan, pusat pengembangan profesi pendidik dan tenaga kependidikan serta profesi nonkependidikan, pusat pengembangan mata kuliah univester, pusat pengembangan bahasa, pusat pengembangan pendidikan karakter dan pengembangan kultur, pusat pengembangan karir, pusat pengembangan berkala ilmiah dan pusat pengembangan sekolah laboratorium ( http://lppmp.uny.ac.id/ ).
Air tanah LPPMP UNY merupakan sumber air yang digunakan untuk memenuhi kebutuhan karyawan, staf, dan pengunung LPPMP UNY. Air tanah LPPMP juga digunakan untuk memasak di taman kuliner Karangmalang. Selain digunakan untuk memasak air LPPMP UNY juga dimanfaatkan untuk air minum dan mandi. Sumber air LPPMP UNY terdapat di belakang gedung ini dan dialirkan ke dalam groundtank. Namun, kondisi air LPPMP UNY
17
sangat mudah kotor, berwana merah kekuningan, keruh dan agak berbau. Gambar 7 merupakan kondisi groundtank LPPMP UNY.
Gambar 7. Groundtank LPPMP UNY
F. Absorbsi
Absorbsi adalah proses terjebaknya suatu partikel terlarut yang berukuran kurang dari 10-9 m dan koloid berdiameter 10-9-10-6 m oleh bahan yang berpori (absorbent) (Nur Hidayati, 2006). Partikel-partikel pengotor masuk ke dalam rongga melalui pori-pori, sebagian terjebak di dalamnya. Terjebaknya partikel pada absorbent terjadi karena adanya gaya fisik dan gaya kimia. Gaya fisik terjadi pada absorbsi fisik, misalnya karena adanya gaya coloumb, yaitu gaya yang terjadi akibat interaksi partikel-partikel bermuatan. Gaya kimia, gaya yang mempengaruhi berupa ikatan kimianya. Proses absorbsi hanya bisa terjadi ketika bahan absorbent mempunyai rongga. Apabila tidak terdapat rongga pada absorben maka proses absorbsi tidak akan terjadi. Semakin besar pori atau rongga pada absorben maka daya serap pada partikelnya akan semakin besar (Yulia Robiatun K, 2014).
18
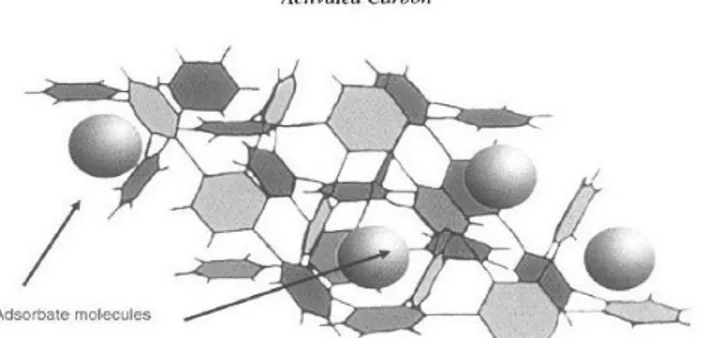
Gambar 8 merupakan gambaran proses terjebaknya partikel pengotor ke karbon aktif.
Gambar 8. Gambaran Proses Terjebaknya Partikel Pengotor ke Karbon Aktif. (Marsh, H., and Reinoso, F.R., 2006).
G. Adsorpsi
Adsorpsi merupakan suatu peristiwa terkontaknya pertikel padatan dan cairan pada kondisi tertentu sehingga sebagian partikel pengotor terjerap (menempel pada permukaan rongga) di permukaan padatan dan konsentrasi partikel pengotor yang tidak terjerap (menempel pada permukaan rongga) mengalami perubahan (Brown, 1950 dalam Unangalim A, 2012). Pada proses adsorpsi partikel pengotor menempel pada bagian pinggir dari bahan penyerap. Hal tersebut yang membedakan antara absorbsi dengan adsorpsi.
Pengertian absorbsi seringkali disalahartikan dengan adsorpsi. Sebenarnya kedua istilah tersebut saling berkaitan satu sama lain. Untuk adsorpsi adalah proses jerapan artinya partikel menjerap atau menempel pada permukaan partikel lainnya, sedangkan proses absorbsi adalah proses serapan. Sehingga dapat disimpulkan bahwa jerapan atau adsorpsi untuk sistem yang
19
tak berpori dan serapan atau absorbsi untuk sistem yang berpori (Dorfner dan Hartono, 1995).
H. Air
1. Air Tanah sebagai Sumber Air Bersih
Air merupakan salah satu kebutuhan essensial manusia yang kedua setelah udara untuk keperluan hidupnya. Air dapat berwujud padatan (es), cairan (air), dan gas (uap air). Air mempunyai rumus kimia H2O. Satu molekul air terbentuk dari dua atom hidrogen dan satu atom oksigen. Kandungan air di bumi sangat berlimpah, volume seluruhnya mencapai 1.400.000.000 km3 (Nur Hidayati, 2006).
Air tanah adalah air yang berada di dalam tanah. Air tanah diperoleh dengan cara menggali sumur atau dengan cara dipompa. Air tanah inilah yang dapat dimanfaatkan untuk kebutuhan sehari-hari seperti minum, mandi dan mencuci. Air tanah yang berasal dari air permukaan dan air hujan relatif lebih bersih. Hanya saja di sebagian wilayah di Indonesia, air tanah mungkin saja terlalu banyak mengandung bahan kimia tertentu. Contohnya pada daerah berpasir atau daerah yang terkena material vulkanik gunung berapi kandungan besi dalam air tinggi, pada daerah berkapur maka kemungkinan kandungan kalsium dalam air akan berlebihan.
20
2. Syarat-syarat Air Bersih sebagai Sumber Air Minum
Air tanah yang bisa dikonsumsi sebagai air bersih untuk air minum harus memenuhi standar air yang layak. Menurut Peraturan Menteri Kesehatan (Permenkes) RI Nomor 492 tahun 2010, air bersih adalah air yang digunakan untuk keperluan sehari-hari yang kualitasnya memenuhi syarat kesehatan dan dapat diminum apabila telah dimasak. Sedangkan air minum adalah air yang melalui proses pengolahan atau tanpa pengolahan yang memenuhi syarat kesehatan dan dapat langsung diminum.
Menurut Permenkes tahun 2010, bahwa tentang syarat-syarat dan pengawasan kualitas air minum, untuk bisa dikonsumsi manusia, air harus memenuhi syarat-syarat fisik, kimia, dan mikrobiologi, dimana air minum harus bebas dari bahan-bahan anorganik dan organik. Dengan kata lain kualitas air minum harus bebas bakteri, zat kimia, racun, limbah berbahaya, dan lain sebagainya.
Air yang memiliki kualitas rendah berpotensi menimbulkan masalah kesehatan yang bisa berdampak langsung maupun tidak langsung. Dampak yang lebih mengkhawatirkan, yaitu dampak kronis dari unsur-unsur kimia yang tidak aman bagi tubuh manusia, contohnya kanker, gangguan ginjal, gangguan hati dll (Nur Hidayati, 2006).
Menurut Permenkes tahun 2010, syarat-syarat kualitas air minum diantaranya:
21 a. Syarat Fisik
Syarat fisik diwujudkan dalam bentuk kekeruhan, bau, warna, dan rasa. Parameter fisik yang tidak langsung berhubungan dengan kesehatan, antara lain berupa bau, warna, jumlah zat padat terlarut, kekeruhan, rasa, dan suhu.
1) Suhu
Suhu air sebaiknya sejuk atau tidak panas, dan bila diminum dapat menghilangkan dahaga. Perubahan suhu air dipengaruhi oleh iklim, kedalaman air, lintang (latitude), ketinggian dari permukaan laut (altitude), kondisi geografis, dan sebagainya. Peningkatan suhu mengakibatkan peningkatan reaksi kimia, serta menyebabkan penurunan viskositas dan kelarutan gas dalam air (gas O2, CO2, N2, CH4, dan sebagainya) (Effendi, 2003). Berdasarkan Keputusan Menteri Kesehatan RI Nomor 492/MENKES/Per/IV/2010, diketahui bahwa suhu air minum idealnya sebesar ± 3 oC dari suhu udara di atas atau di bawah suhu udara.
2) Bau dan Rasa
Bau dan rasa terjadi secara bersamaan dan disebabkan oleh adanya bahan-bahan organik yang membusuk, organisme mikroskopik, serta senyawa kimia seperti fenol. Timbulnya rasa yang menyimpang biasanya disebabkan oleh adanya bahan kimia yang terlarut, dan rasa yang menyimpang tersebut
22
umumnya sangat dekat dengan baunya karena pengujian terhadap rasa air jarang dilakukan. Air yang mempunyai bau yang tidak normal juga dianggap mempunyai rasa yang tidak normal (Moersidik, 1999). Berdasarkan Keputusan Menteri Kesehatan RI Nomor 492/MENKES/Per/IV/2010, diketahui bahwa air bersih dan air minum tidak berbau dan tidak berasa. 3) Warna
Warna pada air disebabkan oleh adanya partikel hasil pembusukan bahan organik, bahan kimia, ion-ion metal alam (besi dan mangan), mikroorganik (plankton), humus yang terlarut di dalam air. Warna yang disebabkan bahan-bahan kimia disebut apparent color yang berbahaya bagi tubuh manusia. Warna yang disebabkan oleh mikroorganisme disebut true color
yang tidak berbahaya bagi kesehatan (Effendi, 2003). Alat yang digunakan untuk mengukur warna adalah kolorimetri. Satuan kolorimetri adalah TCU (True Color Unit). Air yang layak dikonsumsi harus jernih dan tidak berwarna. PERMENKES RI Nomor 492 Tahun 2010 menyatakan bahwa batas maksimal warna air yang layak minum adalah 15 skala TCU.
4) Jumlah Zat Padat Terlarut (TDS)
Padatan terlarut total (Total Dissolved Solid - TDS) adalah bahan–bahan terlarut (diameter < 10-9 m) dan koloid (diameter 10-9 – 10-6 m) yang berupa senyawa–senyawa kimia dan
bahan-23
bahan lain, yang tidak tersaring pada kertas saring berdiameter 0,45 µm. TDS terdapat di dalam air sebagai hasil reaksi dari zat padat, cair, dan gas di dalam air yang dapat berupa senyawa organik maupun anorganik. Materi anorganik berasal dari mineral, logam, dan gas yang terbawa masuk ke dalam air setelah kontak dengan materi pada permukaan dan tanah. Materi organik dapat berasal dari hasil penguraian vegetasi, senyawa organik, dan gas-gas anorganik yang terlarut. TDS disebabkan oleh bahan anorganik berupa ion-ion yang terdapat di perairan (Effendi, 2003). Menurut Permenkes nomor 492 tahun 2010, kadar maksimal TDS yang diperbolehkan sekitar 500 mg/L. b. Syarat Kimia
Syarat kimia terpenting yang perlu diperhatikan adalah kandungan bahan-bahan kimia di dalam air. Kandungan bahan kimia dalam air tidak boleh melebihi ambang batas.
1) Derajat Keasaman (pH)
Derajat keasaman suatu larutan atau yang disebut pH merupakan satu cara untuk menyatakan konsentrasi ion H+. pH air dimanfaatkan untuk menentukan indeks pencemaran dengan melihat tingkat keasaman atau kebasaan air, penentuan alkalinitas, dan karbondioksida (CO2). Semakin tinggi nilai pH, semakin tinggi pula nilai alkalinitas dan semakin rendah kadar CO2 bebas (Effendi, 2003). Air yang baik adalah air yang
24
bersifat netral (PH = 7). Air dengan pH kurang dari 7 dikatakan air bersifat asam, sedangkan air dengan pH di atas 7 bersifat basa. Pengukuran pH dapat dilakukan menggunakan kertas lakmus, kertas pH universal, larutan indikator universal (metode Colorimeter) dan pH meter (metode Elektroda Potensiometri). Menurut PERMENKES RI Nomor 492 Tahun 2010, batas pH minimum dan maksimum air layak minum berkisar 6,5-8,5. Tinggi rendahnya pH air dapat mempengaruhi rasa air. Air dengan pH kurang dari 7 akan terasa asam di lidah dan terasa pahit apabila pH melebihi 7.
2) Kandungan Bahan Kimia Organik dan Anorganik
Air yang baik memiliki kandungan bahan kimia organik dan anorganik dalam jumlah yang tidak melebihi batas yang ditetapkan. Dalam jumlah tertentu, tubuh membutuhkan air yang mengandung bahan kimia organik dan anorganik. Namun, apabila jumlah bahan kimia organik yang terkandung melebihi batas dapat menimbulkan gangguan pada tubuh. Hal itu terjadi karena bahan kimia organik yang melebihi batas ambang dapat terurai jadi racun berbahaya.
Bahan kimia organik tersebut antara lain NH4, H2S, SO4, dan NO3. Sedangkan, bahan-bahan kimia yang termasuk bahan kimia anorganik antara lain garam dan ionion logam (Fe, Al, Cr, Mg, Ca, Cl, K, Pb, Hg, Zn) (Effendi, 2003). Namun, pada
25
penelitian ini peneliti hanya mengukur kandungan logam Fe. Menurut PERMENKES RI Nomor 492 Tahun 2010, batas maksimal kadar Fe untuk air minum adalah 0,3 mg/L.
c. Syarat Mikrobiologi
Sumber-sumber air di alam pada umumnya mengandung bakteri, baik air permukaan, maupun air tanah. Kualitas air secara biologis ditentukan oleh jumlah mikroorganisme pathogen dan nonpathogen. Mikroorganisme pathogen bisa berwujud bakteri, virus, spora pembawa bibit penyakit. Sebaliknya yang nonpathogen meskipun relatif tidak berbahaya bagi kesehatan, kehadirannya akan menimbulkan rasa, dan bau yang tidak enak. Parameter kualitas air minum yang berhubungan langsung dengan kesehatan adalah berhubungan dengan mikrobiologi, seperti bakteri Escherichia coli (E.Coli) dan total coliform.
Total Coliform termasuk bakteri yang dapat ditemukan di lingkungan tanah dan air yang telah terpengaruh oleh air permukaan serta limbah pembuangan domestik. Bakteri coliform lainnya berasal dari hewan dan tanaman mati dan disebut dengan coliform nonfecal (Fardiaz, 1992).
Metode yang digunakan dalam menganalisa total coliform, yaitu metode tabung fermentasi atau Most Probable Number (MPN) dan metode penyaringan dengan membran. Prinsip analisa penyaringan dengan membran adalah berdasarkan sifat bakteri yang
26
berkembang biak dalam waktu 24 sampai 72 jam pada suhu 37oC dan suasana yang cocok yaitu pada media yang terdiri dari agar-agar (dari bahan yang netral) yang mengandung beberapa jenis zat kimia yang merupakan gizi bagi bakteri tertentu serta dapat mengatur nilai pH. Prinsip analisa MPN hampir sama dengan metode penyaringan dalam membran, tetapi bakteri tidak berkembang pada media agar-agar, melainkan dalam media tersuspensi pada kaldu yang mengandung gizi untuk pertumbuhannya. Bakteri-bakteri dapat dideteksi karena mampu memfermentasikan laktosa yang kemudian menghasilkan gas serta menyebabkan terjadinya perubahan pH (Fardiaz, 1992). Menurut Permenkes tahun 2010, air bersih sebagai air minum tidak boleh ada kandungan bakteri Coliform.
I. Besi (Fe)
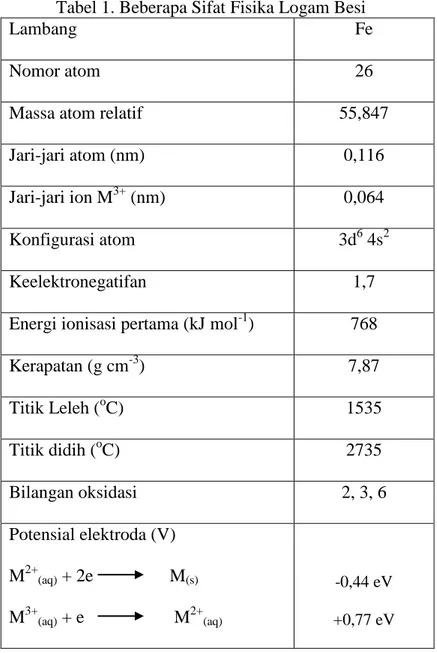
Besi (Fe) merupakan logam mikroelemen yang essensial, berwarna putih keperakan, liat, dan dapat dibentuk. Besi sangat berperan dalam proses fisiologik dan biokimiawi. Besi banyak ditemukan dalam makanan yang jumlahnya bervariasi dari yang rendah (dalam sayuran) dan yang tinggi (dalam daging). Kandungan yang rendah dari Fe dalam makanan akan menyebabkan naiknya efisiensi absorbsi Fe di dalam tubuh manusia, biasanya berkaitan dengan protein yang melibatkan kelompok hemoglobin. Beberapa sifat fisika logam besi ditunjukkan dalam Tabel 1 (Darmono, 1995).
27
Tabel 1. Beberapa Sifat Fisika Logam Besi
Lambang Fe
Nomor atom 26
Massa atom relatif 55,847
Jari-jari atom (nm) 0,116
Jari-jari ion M3+ (nm) 0,064
Konfigurasi atom 3d6 4s2
Keelektronegatifan 1,7
Energi ionisasi pertama (kJ mol-1) 768
Kerapatan (g cm-3) 7,87 Titik Leleh (oC) 1535 Titik didih (oC) 2735 Bilangan oksidasi 2, 3, 6 Potensial elektroda (V) M2+(aq) + 2e M(s) M3+(aq) + e M2+(aq) -0,44 eV +0,77 eV
Fe dalam air minum menimbulkan rasa kesat, warna kuning, pengendapan pada pipa, pertumbuhan bakteri dan kekeruhan. Fe dibutuhkan oleh tubuh dalam pembentukan hemoglobin. Akan tetapi dalam dosis besar logam Fe dapat merusak dinding usus yang akhirnya dapat menyebabkan kematian. Debu Fe juga dapat diakumulasi di dalam alveoli dan menyebabkan berkurangnya fungsi paru-paru (Mulyati, 2003). Fe berada dalam tanah dan batuan sebagai ferioksida (Fe2O3) dan ferihidroksida
28
(Fe2(OH)3). Air tanah mengandung besi terlarut berbentuk ferro (Fe2+). Jika air tanah dipompakan keluar dan kontak dengan udara (oksigen) maka besi (Fe2+) akan teroksidasi menjadi ferihidroksida (Fe2(OH)3). Ferihidroksida dapat mengendap dan berwarna kuning kecoklatan. Hal ini dapat menodai peralatan porselen dan cucian. Bakteri besi (Crenothrix dan Gallionella) memanfaatkan besi ferro sebagai sumber energi untuk pertumbuhannya dan mengendapkan ferihidroksida (Nur Hidayati, 2006).
Air tanah yang mengandung CO2 tinggi dan O2 yang terlarut sedikit, dapat mempercepat proses pelarutan besi dari bentuk tidak terlarut menjadi terlarut. Air tanah yang alkalinitasnya tinggi, biasanya memiliki konsentrasi besi rendah, karena besi teroksidasi dan mengendap pada pH tinggi. Kandungan besi yang tinggi sangat merugikan, karena dapat menyebabkan air teh menjadi hitam, sayuran yang direbus berwarna gelap, menimbulkan rasa logam/besi, astringent atau obat, dan merugikan jika dipakai dalam proses produksi. Tubuh memerlukan zat besi sebesar 14mg/hari, kekurangan besi dapat menyebabkan anemia, namun pemenuhan besi dalam air minum sedikit sekali karena kandungan besi dalam air tanah yang melebihi 0,3 mg/L dapat menyebabkan berbagai gangguan kesehatan hingga kematian.
(http://www.mail.archive.com/[email protected]/msg15305.html).
J. Pipa FAS (Filtrasi, Absorbsi, Sedimentasi)
Pipa FAS adalah alat berupa kolom yang digunakan untuk proses filtrasi, absorbsi, dan sedimentasi dengan pertukaran ion. Munculnya
29
pertukaran ion sebenarnya sudah tercatat sejak lama dalam kehidupan manusia. Gejala pertukaran ion berlangsung di seluruh alam semesta jauh lebih banyak dari pada molekul netral (Yulia Robiatun K, 2014).
Proses pertukaran ion dilakukan dengan menggunakan kolom penukar ion yaitu pipa FAS, yang ditunjukkan pada Gambar 9. Proses alirannya dapat dilakukan secara naik (upflow) atau turun (downflow) ataupun kedua-duanya. Selama aliran lewat kolom, ion-ion yang harus dipertukarkan berkontak secara kontinyu dengan penukar ion sehingga keseimbangan makin bergeser ke arah yang dikehendaki. Bahan-bahan absorbent dimasukkan ke dalam pipa FAS, bahan-bahan absorbat yang berbentuk cair dialirkan ke dalamnya.
Gambar 9. Pipa FAS
K. Sistem Transmisi Cahaya
Sistem transmisi cahaya biasa digunakan dalam bidang teknologi hamburan cahaya untuk mengetahui kondisi larutan. Dengan prinsip cahaya dirambatkan secara lurus kemudian ditabrakkan ke suatu larutan kemudian diteruskan agar menabrak detektor.
Cahaya yang datang dan melalui pinhole akan di pancarkan ke wadah yang berisi cairan. Kemudian cahaya yang sudah menabrak larutan dalam
30
wadah akan merambat lagi dengan kondisi yang berbeda dengan kondisi cahaya mula-mula menuju ke detektor cahaya (luxmeter). Dari detektor ini dapat dilihat dan dianalisis apa yang terjadi pada cahaya yang dipengaruhi oleh larutan yang dilewatinya. Detektor akan mengukur itensitas cahaya yang melewati larutan tersebut. Gambar 10 adalah skema alat transmisi cahaya yang digunakan pada penelitian ini.
Sistem transmisi cahaya pada penelitian ini digunakan untuk mengetahui efisiensi penyerapan karbon aktif, pasir aktif, dan kerikil aktif, serta campuran ketiga absorbent. Sistem transmisi cahaya dilakukan dengan cara melewatkan seberkas cahaya pada air yang telah diberi perlakuan, kemudian intensitas cahaya yang ditransmisikan terukur oleh luxmeter. Hasil yang diperoleh dibandingkan dengan intensitas cahaya transmisi oleh air bersih. Sehingga diperoleh efisiensi penyerapan ketiga absorbent terhadap partikel pengotor terlarut.
31
Gambar 10. Rangkaian Transmisi Cahaya Keterangan Gambar :
1. Sumber Cahaya ( Lampu Pijar ) 2. Detektor
3. Luxmeter
4. Hole (tempat berjalannya cahaya dari sumber ke sampel) 5. Hole (tempat berjalannya hamburan cahaya ke detektor) 6. Sumber tegangan PLN
7. Wadah sampel air
Luxmeter yang ditunjukkan pada Gambar 11 merupakan suatu alat yang digunakan untuk mengukur besarnya intensitas cahaya, dengan satuan 1x lux. Luxmeter memanfaatkan sebuah sensor yang sensitif terhadap cahaya untuk menangkap cahaya yang tersebar, kemudian mengubah cahaya tersebut menjadi electrical current (arus listrik). Ada dua macam bentuk luxmeter, yaitu luxmeter analog dan luxmeter digital. Luxmeter digital lebih mudah dibaca hasil pengukurannya dan memiliki ketelitian yang lebih baik daripada luxmeter analog.
7
2 3 1 6 5 432
Gambar 11. Luxmeter Digital
L. Spektrofotometri Ultra Violet – Tampak (UV-Vis)
Spektrofotometri merupakan bagian dari spektroskopi yaitu spektroskopi elektromagnetik. Alat yang digunakan untuk analisa spektrofotometri adalah spektrofotometer. Spektrofotometer adalah alat untuk mengukur transmitrans atau absorbans. Suatu contoh sebagai fungsi panjang gelombang, pengukuran terhadap suatu deretan. Contoh pada suatu panjang gelombang tunggal mungkin juga dapat dilakukan. Alat-alat demikian dapat dikelompokkan baik sebagai manual atau perekam, maupun sebagai sinar tunggal atau sinar rangkap. Biasanya dalam praktek alat-alat sinar tunggal dijalankan dengan tangan dan alat-alat sinar rangkap biasanya menonjolkan pencatatan spektrum absorpsi (R. A. Day, Jr. dan Underwood, A. L. , 1989).
Spektrofotometri UV-Vis yang ditunjukkan pada Gambar 12 adalah analisis kimia yang menggunakan spektrofotometer yang berdasarkan pada interaksi antara zat kimia dengan energi yang berupa penyerapan cahaya tampak dan atau cahaya ultraviolet ungu oleh suatu larutan berwarna (Nur Hidayati, 2006). Spektrofotometri UV-Vis menguraikan sinar dengan panjang gelombang 200-700 nm (Khopkar, 1990).
33
Gambar 12. Spektrofotometri UV-Vis
Prinsip dasar analisis spektrofotometri adalah pengukuran intensitas energi radiasi yang diserap oleh larutan berwarna. Terserapnya sinar radiasi yang dilewatkan pada populasi zat tersebut terjadi pengurangan intensitas cahaya. Pengurangan intensitas radiasi ini sebanding dengan jumlah radiasi yang diserap, sedangkan pengurangan intensitas cahaya sebanding dengan jumlah larutan yang dianalisi. Pengukuran intensitas radiasi yang diteruskan atau ditransmisi dapat digunakan untuk mengukur besarnya konsentrasi. Bila berkas sinar melalui medium, maka berkas sinar tersebut sebagian akan dipantulkan, diserap, dan diteruskan. Besarnya absorbansi tergantung panjang gelombang radiasi dan jarak medium yang dijalani oleh radiasi sinar (Hardjono Sastroamidjojo, 2001).
Menurut hukum Lambert Beer, jumlah radiasi tampak yang diserap akan ditransmisikan oleh larutan merupakan fungsi eksponensial dari konsentrasi zat dan tebal larutan. Berikut persamaannya:
34
I0 = Ia + It
I0 It Ia = I0 - It
Gambar 13. Cahaya Datang (I0), Cahaya Terserap (Ia), Cahaya Transmisi (It).
... (2) ... (3) Keterangan: A : Absorbansi
I0 : Intensitas cahaya yang masuk
Ia : Intensitas cahaya yang diserap
C : Konsentrasi (molar)
T : Transmitansi
b : Panjang jalan sinar (cm) It : Intensitas cahaya yang
ditransmisikan
Ɛ : Koefisien ekstingsi molar (molar-1 cm-1)
Ia
35
Secara garis besar spektofotometri teridi dari 4 bagian penting seperti pada Gambar 14 yang menunjukkan skema komponen penyusun spektofotometri UV-Vis (Cairns, 2009).
Gambar 14. Skema Komponen Penyusun Spektofotometri UV-Vis
Menurut Cairns (2009) komponen penyusun spektrofotometri UV-Vis, antara lain:
1. Sumber Tenaga Radiasi
Sumber energi radiasi terdiri dari benda yang tereksitasi hingga ke tingkat energi yang lebih tinggi oleh sumber listrik. Sumber radiasi ultraviolet, sumber radiasi yang banyak digunakan adalah lampu hidrogen dan lampu deuterium. Sumber radiasi terlihat yang biasa digunakan adalah lampu filamen tungsen yang menghasilkan radiasi kontinu dalam daerah antara 350 dan 2500 nm.
2. Monokromator
Monokromator merupakan serangkaian alat optik yang menguraikan radiasi polikromatik menjadi jalur-jalur yang efektif atau panjang gelombang-gelombang tunggal dan memisahkan panjang gelombang menjadi jalur-jalur yang sangat sempit.
36 3. Kuvet
Kuvet berfungsi untuk menempatkan larutan atau sampel yang biasanya berupa gas atau larutan, sehingga harus dapat memancarkan energi radiasi dalam spektra.
4. Detektor dan Pencatat
Detektor berfungsi untuk mengubah energi cahaya yang mengenai larutan menjadi energi listrik atau isyarat listrik tersebut. Detektor yang digunakan adalah detektor fotolistrik. Radiasi yang diserap adalah pada panjang gelombang 190-400 nm. Sedangkan pencatat berfungsi untuk menunjukkan isyarat listrik dari detektor, dan untuk memperlihatkan besarnya isyarat listrit tersebut.
M. TDS (Total Dissolved Solids) Meter
TDS meter seperti pada Gambar 15 adalah alat untuk mengukur partikel padatan ataupun non padatan yang terlarut di air minum yang tidak tampak oleh mata. Partikel padatan tersebut bisa berupa Besi, Aluminium, Tembaga, Mangan, sedangkan yang patikel non padatan bisa berupa mikro organisma dan lain-lain. Air minum adalah air yang melalui proses pengolahan ataupun tanpa proses pengolahan yang memenuhi syarat kesehatan dan yang digunakan untuk konsumsi manusia. TDS Meter sampai saat ini dapat mengguakan dua metode untuk mengukur kualitas suatu larutan yaitu: Gravimetry dan Electrical Conductivity (EC). Gravimetry adalah pemeriksaan jumlah zat dengan cara penimbangan hasil reaksi pengendapan.
37
Jumlah zat ditentukan dengan cara menimbang langsung massa zat yang dipisahkan dari zat-zat lain. EC atau konduktansi adalah ukuran kemampuan suatu bahan untuk menghantarkan arus listrik (Alaerts G, 1981).
Cara pengoperasian TDS meter adalah tekan tombol on/off pada TDS meter, kemudian mencelupkan TDS meter ke dalam air yang akan diukur kira-kira kedalaman 5 cm dan secara otomatis alat bekerja mengukur hasil berupa angka yang tertampil di display.
Gambar 15. TDS Meter
N. pH Meter
Alat elektronik yang digunakan untuk mengukur pH (keasaman atau alkalinitas) dari cairan (meskipun probe khusus terkadang digunakan untuk mengukur pH zat semi-padat) disebut pH meter seperti yang ditunjukkan pada Gambar 16. Sebuah pH meter terdiri dari sebuah elektroda (probe pengukur) yang terhubung ke sebuah alat elektronik yang mengukur dan menampilkan nilai pH.
Pada prinsipnya pengukuran suatu pH adalah didasarkan pada potensial elektro kimia yang terjadi antara larutan yang terdapat di dalam elektroda gelas (membrane gelas) yang telah diketahui dengan larutan yang terdapat
38
diluar elektroda gelas yang tidak diketahui. Hal ini dikarenakan lapisan tipis dari gelembung kaca akan berinteraksi dengan ion hydrogen yang ukurannya relatif kecil dan aktif, elektroda gelas tersebut akan mengukur potensial elektrokimia dari ion hydrogen atau diistilahkan dengan potential of hydrogen (Alaerts G, 1981). Untuk melengkapi sirkuit elektrik dibutuhkan suatu elektroda pembanding. Sebagai catatan, alat tersebut tidak mengukur arus tetapi hanya mengukur tegangan.
Cara pengoperasian pH meter adalah tekan tombol on/off pada pH meter, kemudian mencelupkan pH meter ke dalam air yang akan diukur kira-kira kedalaman 5 cm dan secara otomatis alat bekerja mengukur hasil berupa angka yang tertampil di display.
Gambar 16. pH meter
O. Kerangka Berpikir
Air yang layak minum harus memenuhi syarat Permenkes nomor 492 tahun 2010 baik secara fisik, kimiawi, dan mikrobiologi. Air yang keruh berwarna coklat kekuningan atau kemerahan dan berbau mengindikasikan adanya kandungan beberapa jenis logam termasuk Fe dan bakteri. Hal ini
39
serupa terjadi pada air sumur di groundtank LPPMP UNY, yang mana air berwarna coklat kekuningan dan berbau. Semakin tinggi nilai kadar logam Fe dalam air, maka kondisi air semakin keruh. Apabila kita mengkonsumsi air minum yang memiliki kandungan logam Fe dan total coliform yang tinggi, maka cepat atau lambat organ tubuh yang berfungsi untuk menyaring akan rusak dan bisa menyebabkan kematian. Untuk menanggulangi masalah tersebut, maka diperlukan cara pengolahan air groundtank LPPMP UNY yang tepat. Sehingga didapatkan air dengan kualitas yang memenuhi syarat kesehatan. Untuk itu peneliti memanfaatkan karbon aktif bambu, pasir aktif pantai Indrayanti dan kerikil aktif kali Krasak yang diharapkan dapat mengabsorbsi ion Fe, dan pertikel-partikel pengotor dalam air groundtank LPPMP UNY.
Salah satu cara pengolahan air LPPMP UNY dengan dilakukan penyaringan air menggunakan kolom penukar ion yaitu pipa filtrasi yang dirancang oleh peneliti. Pipa filtrasi terdiri dari lima pipa yang telah disusun dengan sambungan pipa. Dalam penelitian ini absorben yang digunakan adalah absorbent yang memiliki daya absorbsi yang tinggi, yaitu karbon aktif, pasir aktif dan kerikil aktif.
Pada penelitian ini digunakan karbon aktif dari bambu, pasir aktif pantai Indrayanti, dan kerikil aktif kali Krasak. Proses awal yang dilakukan adalah proses karbonisasi bambu. Kemudian ketiga absorben dirimbang atau dicuci hingga tidak adanya kotoran yang terdapat pada karbon bambu, pasir dan kerikil. Absorbent yang telah dicuci, dijemur hingga kadar air berkurang
40
(kering). Selanjutnya ketiga absorbent diaktivasi secara fisika dengan cara dipanaskan dalam oven dengan suhu 200oC selama 60 menit.
Proses penyaringan air dilakukan menggunakan volume masing-masing absorbent dan variasi perbandingan volume dan jenis ketiga absorbent. Kemudian dilakukan pengujian intensitas transmisi cahaya, jumlah zat padat terlarut, pH, suhu, kadar Fe, dan total coliform.