EFEK MOTORIK INFUSA AKAR MRICA KEPYAR (Phytolacca americana L.) PADA MENCIT JANTAN
DENGAN METODE ROTAROD TEST
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh:
Kristiningrum Hery Karuniawati
NIM : 038114119
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
EFEK MOTORIK INFUSA AKAR MRICA KEPYAR (Phytolacca americana L.) PADA MENCIT JANTAN
DENGAN METODE ROTAROD TEST
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh:
Kristiningrum Hery Karuniawati
NIM : 038114119
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2008
ii
iii
Bersukacitalah dalam pengharapan, Sabarlah dalam kesesakan,
dan Bertekunlah dalam doa ! ( Rm 12:12)
Segala perkara dapat kutanggung didalam
dia yang memberi kekuatan kepadaku (Flp
4:13)
Bermegahlah dalam kesengsaraan
, karena kita tahu, bahwa kesengsaraan itu menimbulkan
ketekunan,
dan ketekunan menimbulkan tahan uji
dan tahan uji menimbulkan pengharapan.
Dan pengharapan tidak mengecewakan,
karena kasih Allah telah dicurahkan di dalam hati kita
Kupersembahkan skripsi ini untuk :
Tuhan Yesus Kristus,
Ibu Bapak tercinta, Keluarga besarku,
Teman sahabatku
Dan Almamaterku
PRAKATA
Puji syukur kepada Tuhan Yang Maha Esa atas kasih dan anugerahnya,
sehingga penulis bisa menyelesaikan skripsi yang berjudul “Efek Motorik Infusa
Akar Mrica Kepyar (Phytolacca americana .L) pada Mencit Jantan dengan Metode
Rotarod Test “. Keberhasilan skripsi ini tidak lepas dari dukungan berbagai pihak
yang sangat membantu penulis dalam menyusun skripsi. Oleh karena itu penulis ingin
mengucapkan terima kasih kepada:
1. Rita Suhadi, M.Si, Apt selaku Dekan Fakultas Farmasi Universitas Sanata
Dharma.
2. Christine Patramurti, M.Si., Apt. selaku Ketua Program Studi Fakultas Farmasi
Universitas Sanata Dharma.
3. Drs. Mulyono, Apt. selaku dosen pembimbing yang telah meluangkan waktu,
tenaga dan atas masukan serta saran dalam penyusunan skripsi ini.
4. dr. Luciana Kuswibawati, M Kes selaku dosen penguji atas segala arahan, kritik,
saran dan waktunya.
5. Erna Tri Wulandari, M.Si., Apt., selaku dosen penguji atas segala arahan, kritik,
saran dan waktunya.
6. Ign. Y. Kristio Budiasmoro, S.Si, M.Si, selaku dosen pembimbing akademik atas
segala arahan, saran dan kritik.
vii
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini
tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan
INTISARI
Tonikum dalam masyarakat digunakan sebagai penyegar dan penambah tenaga. Efek motorik merupakan salah satu fungsi dari tonikum. Akar tanaman Mrica Kepyar salah satunya dimanfaatkan sebagai alteratif yaitu secara berangsur-angsur mengembalikan fungsi tubuh sebagaimana mestinya dan meningkatkan kesehatan dan vitalitas tubuh. Alteratif dikenal juga sebagai tonik.
Penelitian ini bertujuan memperoleh keterangan ada tidaknya efek motorik infusa akar Mrica Kepyar terhadap mencit jantan menggunakan metode rotarod test. Penelitian ini termasuk jenis penelitian eksperimental murni menggunakan rancangan acak lengkap pola satu arah. Subyek uji yang digunakan yaitu mencit jantan sebanyak 42 ekor yang terbagi dalam 6 kelompok. Kelompok I sebagai kontrol negatif menggunakan aquadest. Kelompok II sebagai kontrol positif menggunakan kafein dosis 65,72 mg/KgBW. Kelompok III-VI sebagai kelompok perlakuan menggunakan infusa akar Mrica Kepyar batang dengan dosis 4,40, 5,76, 7,54, dan 9,88 g/KgBW. Data yang dikumpulkan berupa waktu jatuh pertama mencit, jumlah kumulatif jatuh mencit dari rotarod selama (3x60) menit dan persen proteksi terhadap jatuh. Hasil diuji secara statistik menggunakan ANOVA satu arah dan uji Kruskal-Wallis dilanjutkan dengan uji LSD dan Mann-Withney dengan taraf kepercayaan 95% .
Hasil penelitian menunjukkan infusa akar Mrica Kepyar memiliki efek motorik pada mencit jantan. Efek motorik yang dihasilkan infusa akar Phytolacca americana L dosis 4,40 g/KgBB, 5,76 g/KgBB, 7,54 g/KgBB, dan 9,88 g/KgBB adalah 37,3%, 59,9% , 69,9% , dan 44,9%.
Kata kunci : Phytolacca americana L., tonikum, motorik, rotarod test
ABSTRACT
Tonicum, in society is used as freshner and energy force. Motoric effect is one function of tonicum. The root of Phytolacca americana .L is used as an alterative in folk medicine which will gradually restore the proper function of the body, and increase health & vitality. Alteratives are also known as tonics.
The research was done to observe the occurrence of motoric effect of Phytolacca americana L. root infusion toward male mice by using rotarod test method. The research was a pure experimental research with one way random design. The test subjects were 42 male mice and separated on 6 groups. Group I which was as a negative control used aquadest. Group II which was as a positive control used caffein 65,72 mg/kgBW. Groups III-VI which was as test groups used Phytolacca americana.L root infusion with dosage 4,40, 5,76, 7,54, and 9,88 g/kgBW/per day for four days. The data that were collected were the first fall time, cumulative (frequency)
fall from rotarod during 3x60 minutes, and the percentage of fall protection. They were analyzed using one way Anova and Kruskal-Wallis test with 95% significance level and were continued with LSD and Mann-Withney test.
The result of the study showed that the root of Phytolacca americana L. infusion have a motoric effect to male mice. The motoric effects which were produced by 4,40 g/KgBW, 5,76 g/KgBW, 7,54 g/KgBW, and 9,88 g/KgBW of Phytolacca americana L. root infusion were 37,3%, 59,9% , 69,9% , dan 44,9%.
Keywords : Phytolacca americana L., tonic, motoric, rotarod test
DAFTAR ISI
Halaman
HALAMAN JUDUL... . i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN... iii
HALAMAN PERSEMBAHAN ... iv
PRAKATA... v
PERNYATAAN KEASLIAN KARYA ... vii
INTISARI... viii
ABSTRACT... ix
DAFTAR ISI... x
DAFTAR TABEL... xiv
DAFTAR GAMBAR ... xviii
DAFTAR LAMPIRAN... xx
BAB I. PENDAHULUAN ... 1
A. Latar Belakang Masalah... 2
B. Permasalahan... 2
C. Keaslian Penelitian... 3
D. Manfaat Penelitian... 3
1. Manfaat teoritis... 3
2. Manfaat praktis... 3
E. Tujuan Penelitian... 4
1. Tujuan umum………. 4
2. Tujuan khusus……… 4
BAB II. PENELAAHAN PUSTAKA... 5
A. Tanaman Mrica Kepyar (Phytolacca americana L.) ... 5
1. Klasifikasi……… 5
2. Sinonim……… 5
3. Nama lain………... 5
4. Uraian tanaman……….. 6
5. Bagian yang digunakan ……….. 6
6. Kandungan kimia………. 6
7. Kegunaan………..………... 7
B. Efek Tonikum dan Fungsi Motorik..……… 7
C. Infusa ……….………. 8
D. Metode pengujian aktivitas motorik ... 8
1. Metode batang berputar (Rotarod test)………. 9
2. Metode” sangkar putar”... 9
3. Metode ketahanan berenang ... 9
F. Mekanisme lelah ... 10
G. Kafein ... 17
H. Keterangan Empiris... 19
BAB III. METODOLOGI PENELITIAN ... 20
A. Jenis dan Rancangan Penelitian………. 20
B. Variabel Penelitian………. 20
C. Definisi Operasional……….. 21
D. Bahan Penelitian………. 22
E. Alat Penelitian………. 22
F. Tata Cara Penelitian……… 23
1. Determinasi tanaman……….. 23
2. Pengumpulan dan pembuatan simplisia………. 23
3. Penyiapan hewan uji ………. 24
4. Pembuatan sediaan……….. 24
5. Penentuan dosis kafein ……… ……… 25
6. Penentuan rentang waktu setelah pemberian kafein ...……… 26
7. Penentuan dosis infusa akar Mrica Kepyar ……… 26
8. Penetuan rentang waktu setelah pemberian infusa akar Mrica Kepyar………... 28
9. Pengujian efek motorik... 28
10.Penentuan efek motorik ... 29
11.Analisis hasil ………..………. 29
BAB IV. HASIL DAN PEMBAHASAN... 30
A. Determinasi Tanaman... 30
B. Pengumpulan dan pembuatan simplisia……….. 30
C. Penyiapan hewan uji ………. ... 32
D. Pembuatan sediaan... 33
E. Uji Pendahuluan... 34
1. Penetapan dosis kafein... 34
2. Penetapan rentang waktu setelah pemberian kafein... 41
3. Penetapan rentang waktu setelah pemberian infusa... 46
4. Pengujian efek motorik ... 53
BAB V. KESIMPULAN DAN SARAN... 64
A. Kesimpulan... 64
B. Saran... 64
DAFTAR PUSTAKA ... ... 65
LAMPIRAN... ... 68
BIOGRAFI PENULIS... 97
DAFTAR TABEL
Halaman Tabel I Perbandingan potensi dari bahan aktif (xantine) dalam kopi,
teh, dan coklat... 18
Tabel II Rata-rata waktu jatuh pertama mencit dari rotarod pada
penentuan dosis kafein ... 35
Tabel III Hasil analisis variansi satu arah rata-rata waktu jatuh
pertama mencit pada penentuan dosis kafein ……… 36
Tabel IV Rata-rata jumlah jatuh kumulatif mencit dari rotarod
selama (3x60) menit dan persen proteksi pada penentuan
dosis kafein ………... 37
Tabel V Hasil analisis Kruskal-Wallis rata-rata jumlah kumulatif
jatuh mencit selama (3x60) menit dan persen proteksi pada
penentuan dosis kafein………... 38
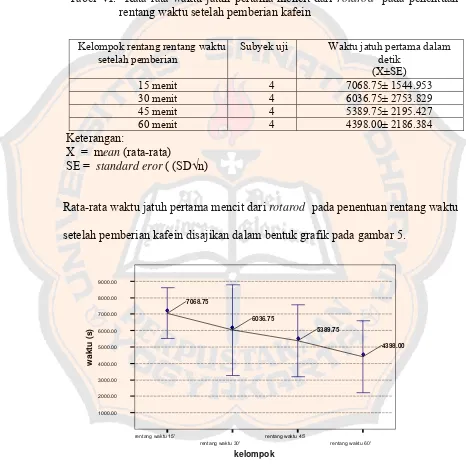
Tabel VI Rata-rata waktu jatuh pertama mencit dari rotarod pada
penentuan rentang waktu pemberian kafein... 39
Tabel VII Hasil analisis variansi satu arah rata-rata waktu jatuh
pertama mencit pada penentuan rentang waktu setelah
pemberian kafein……… 44
Tabel VIII Rata-rata jumlah kumulatif jatuh mencit selama (3x60)
menit dari rotarod pada penentuan rentang waktu setelah
pemberian kafein……….. 44
Tabel IX Hasil analisis variansi satu arah rata-rata jumlah kumulatif
jatuh mencit selama (3x60) menit pada penentuan rentang
waktu setelah pemberian kafein……… 45
Tabel X Rata-rata waktu jatuh pertama mencit dari rotarod pada
penentuan rentang waktu setelah pemberian infusa... 46
Tabel XI Hasil analisis variansi satu waktu jatuh pertama mencit
selama (3x60) menit pada penentuan rentang waktu setelah
pemberian infusa……… 48
Tabel XII Hasil uji LSD rata-rata waktu jatuh pertama mencit dari
rotarod pada penentuan rentang waktu setelah pemberian
infusa……… 48
Tabel XIII Rata-rata jumah kumulatif jatuh mencit selama (3x60)
pada penentuan rentang waktu setelah pemberian infusa … 50
Tabel XIV Hasil analisis Kruskal-Wallis rata-rata jumlah kumulatif
jatuh mencit selama (3x60) menit dan pada penentuan
rentang waktu setelah pemberian infusa………….……….. 51
Tabel XV Hasil uji Mann-Withney rata-rata jumlah kumulatif jatuh
mencit selama (3x60) menit pada penentuan rentang
waktu setelah pemberian infusa……… 52
Tabel XVI Data rata-rata waktu jatuh pertama mencit dari rotarod
pengujian efek motorik seluruh kelompok……... 53
Tabel XVII Hasil uji variansi satu arah rata-rata waktu jatuh pertama
mencit pada pengujian efek motorik seluruh kelompok
pada... 54
Tabel XVIII Hasil uji LSD waktu pertama jatuh mencit pada pengujian
efek motorik seluruh kelompok……….. 55
Tabel XIX Rata-rata jumlah kumulatif jatuh mencit selama (3x60)
menit dan persen proteksi pada pengujian efek motorik
seluruh kelompok ... 56
Tabel XX Hasil uji variansi analisis satu arah rata-rata jumlah
kumulatif jatuh mencit selama (3x60) menit pada
pengujian efek motorik seluruh kelompok ……… 59
Tabel XXI Hasil uji LSD rata-rata jumlah kumulatif jatuh mencit
selama (3x60) menit pada pengujian efek tonikum seluruh
kelompok………... 59
Tabel XXII Hasil uji Kruskal-Wallis persen proteksi pada pengujian
efek motorik seluruh kelompok………... 61
Tabel XXIII Hasil analisis uji Mann-Withney persen proteksi pada
pengujian efek motorik seluruh kelompok... 61
Tabel XIV Data rata-rata waktu pertama jatuh mencit, jumlah
kumulatif jatuh mencit selama (3x60) menit, dan persen
proteksi pada penentuan dosis kafein ……… 73
Tabel XV Tabel waktu pertama jatuh , jumlah kumulatif jatuh mencit
selama (3x60) menit dan persen proteksi pada pengujian
efek motorik seluruh kelompok……… 85
DAFTAR GAMBAR
Halaman Gambar 1. Diagram proses berantai dalam kontraksi otot... 11
Gambar 2. Kafein (1,3,7 trimetilxantin)... 17
Gambar 3. Diagram batang rata-rata waktu jatuh pertama mencit pada
penentuan dosis kafein ……… 35
Gambar 4. a. Diagram batang rata-rata jumlah kumulatif jatuh
pertama mencit selama (3x60) menit pada penentuan
dosis kafein ………
b. Diagram batang % proteksi pada penentuan dosis
kafein………..
37
37
Gambar 5. Grafik rata-rata waktu jatuh pertama mencit dari rotarod
pada penentuan rentang waktu setelah pemberian kafein .... 42
Gambar 6. Grafik rata-rata jumlah kumulatif jatuh mencit selama
(3x60) menit pada penentuan rentang rentang waktu setelah
pemberian kafein... 44
Gambar 7. Grafik rata-rata waktu jatuh pertama mencit dari rotarod
pada penentuan rentang waktu setelah pemberian infusa .... 47
Gambar 8. Grafik Rata-rata jumlah kumulatif jatuh mencit selama
(3x60) menit pada penentuan rentang waktu setelah
pemberian infusa……… 50
Gambar 9. Diagaram batang rata-rata waktu pertama jatuh mencit dari
rotarod pada pengujian efek motorik seluruh kelompok uji. 54
Gambar 10. a Diagram batang rata-rata jumlah kumulatif jatuh mencit
selama (3x60) menit dan persen proteksi pada
pengujian efek motorik seluruh kelompok………
b Digram batang persen proteksi proteksi pada pengujian
efek motorik seluruh kelompok……….
57
57
Gambar 11. Foto Tanaman Mrica Kepyar (Phytolacca Americana.L)… 69
Gambar 12. Foto akar, serbuk akar ...……. 70
Gambar 13. Foto infusa akar Mrica Kepyar……... 71
Gambar 13. Foto mencit diatas rotarod……… 72
DAFTAR LAMPIRAN
Halaman Lampiran 1. Surat pengesahan determinasi... 68
Lampiran 2. Foto tanaman Mrica Kepyar, akar dan serbuk akar Mrica
Kepyar, infusa akar Mrica Kepyar, mencit diatas rotarod ... 69
Lampiran 3. Data rata-rata waktu pertama jatuh mencit, jumlah
kumulatif jatuh mencit selama (3x60) menit, dan persen
proteksi pada penentuan dosis kafein ……… 73
Lampiran 4. Hasil analisis statistik waktu jatuh pertama mencit pada
penentuan dosis kafein……….. 75
Lampiran 5. Hasil analisis statistik rata-rata jumlah kumulatif jatuh
mencit selama (3x60) menit pada penentuan dosis kafein…. 76
Lampiran 6. Hasil analisis statistik persen proteksi pada penentuan dosis
kafein ………. 76
Lampiran 7. Data waktu pertama jatuh mencit dan jumlah kumulatif
jatuh mencit selama (3x60) menit……….. 78
Lampiran 8. Hasil analisis statistik waktu jatuh pertama jatuh mencit
pada penentuan rentang waktu setelah pemberian
kafein……….. 79
Lampiran 9. Hasil analisis statistik rata-rata jumlah kumulatif jatuh
mencit selama (3x60) menit pada penentuan rentang waktu
setelah pemberian kafein……… 79
Lampiran 10. Hasil analisis statistik waktu jatuh pertama jatuh mencit
pada penentuan rentang waktu pemberian infusa ………… 81
Lampiran 11. Hasil analisis data waktu jatuh pertama jatuh mencit pada
penentuan rentang waktu setelah pemberian infusa……… 82
Lampiran 12. Hasil analisis statistik waktu jatuh pertama mencit pada
pengujian efek motorik seluruh kelompok……….. 86
Lampiran 13. Hasil analisis statistik rata-rata jumlah kumulatif jatuh
mencit selama (3x60) menit pada pengujian efek motorik
seluruh kelompok………. 88
Lampiran 14. Hasil analisis rata-rata persen proteksi pada pengujian efek
motorik seluruh kelompok……… 90
BAB I PENGANTAR A. Latar Belakang
Perkembangan zaman yang semakin pesat diberbagai bidang saat ini
menyebabkan setiap individu harus berusaha lebih keras untuk memenuhi kebutuhan
hidupnya. Keadaan ini membutuhkan stamina tubuh yang prima untuk mendukung
aktifitas fisik maupun mental. Aktifitas fisik yang berlebihan dan tidak terkontrol
dapat menyebabkan penurunan daya tahan dan fungsi motorik tubuh, yang dapat
mengakibatkan tubuh mudah lelah dan terasa lemah. Fungsi motorik adalah fungsi
dari otot, susunan saraf pusat yang mempengaruhi dan menghasilkan gerak.
Efek tonikum merupakan perubahan yang terjadi karena pemberian zat
tonika. Zat tonika yaitu suatu senyawa yang dapat mengurangi kondisi kelemahan
dan tonus dari keseluruhan atau sebagian organ makhluk hidup. Tonikum popular di
masyarakat, terutama bagi mereka yang bekerja menguras tenaga serta pada
kelompok tertentu misalnya lanjut usia dan dalam proses penyembuhan. Efek
tonikum memiliki berbagai fungsi seperti stimulan pusat pernafasan, stimulan otot
jantung, peningkatan kecepatan metabolisme basal, dsb. Efek motorik merupakan
salah satu fungsi dari tonikum. Tonikum yang dikonsumsi akan mengurangi
kelemahan dan kelelahan pada fungsi motorik tubuh. Pada penelitian ini efek tonikum
yang diamati dibatasi pada fungsi motorik .
Dalam pengobatan tradisional akar tanaman Mrica Kepyar salah satunya
dimanfaatkan sebagai alteratif yaitu secara bergangsur-angsur mengembalikan fungsi
tubuh sebagaimana mestinya dan meningkatkan kesehatan dan vitalitas tubuh.
Alteratif dikenal juga sebagai tonik. Bentuk sediaan yang digunakan adalah infusa,
mengacu pada penggunaan akar mrica kepyar dimasyarakat yaitu rebusan. Kelebihan
sediaan infusa dibandingkan rebusan adalah pada sediaan infusa beberapa faktor
seperti keseragaman konsentrasi dan dosis dapat dikendalikan. Penelitian ini
bertujuan untuk memperoleh keterangan ada tidaknya efek motorik setelah konsumsi
infusa akar Mrica Kepyar dan besar efek motorik infusa akar Mrica Kepyar
(Anonim, 2006).
Kafein merupakan stimulan susunan yang saraf pusat yang memiliki efek
meningkatkan kapasitas kerja otot, menyebabkan penurunan rasa letih, dan
meningkatkan kesiagaan mental. Kafein telah digunakan secara luas di masyarakat
dalam minuman penambah tenaga, karenanya kafein dipilih sebagai kontrol positif
dalam penelitian ini. Metode yang digunakan adalah metode rotarod test. Metode ini
biasa dipakai untuk mengetahui fungsi otot yaitu aktivitas relaksasi karena pengaruh
suatu obat, metode ini juga menggambarkan koordinasi motorik yaitu dengan
mempertahankan keseimbangan diatas rotarod.
B.Permasalahan
1. Apakah infusa akar Mrica Kepyar memiliki efek motorik pada mencit jantan?
2. Berapa besar efek motorik infusa akar Mrica Kepyar pada mencit jantan melalui
C. Keaslian Penelitian
Penelitian Efek Motorik Infusa Akar Mrica Kepyar (Phytolacca americana
L.) pada Mencit Jantan dengan Metode Rotarod test sejauh pengetahuan penulis
belum pernah dilakukan. Penelitian yang pernah dilakukan antara lain disebutkan
dibawah ini.
1. Perbandingan Efek Tonikum Infusa Akar Talinum paniculatum Gaertn
(Ginseng Jawa) terhadap Akar Panax ginseng C. A Meyer (per oral) terhadap
Fungsi Motorik Mencit (Suhadi, 2000).
2. Efek Tonikum Infusa Akar Krokot Blanda (Talinum triangulare (Jacq) Willd) terhadap Fungsi Motorik pada Mencit Jantan dengan Metode Uji batang
berputar (Nyoman, 2005).
D. Manfaat Penelitian 1. Manfaat teoritis
Penelitian ini diharapkan dapat memberi manfaat bagi perkembangan ilmu
pengetahuan khususnya dibidang farmasi mengenai penggunaan obat tradisional
untuk mengurangi kelelahan akibat aktivitas fisik berlebih.
2. Manfaat praktis
Penelitian ini diharapkan dapat memberikan informasi kepada masyarakat tentang
ada tidaknya efek motorik infusa akar Mrica Kepyar untuk mengurangi kelelahan
E.Tujuan Penelitian 1. Tujuan umum
Untuk mendukung usaha pengembangan tanaman tradisional sebagai obat,
khususnya untuk mengurangi kelelahan akibat aktivitas fisik berlebih.
2. Tujuan khusus
a.Untuk mengetahui ada tidaknya efek motorik infusa akar Mrica Kepyar pada
mencit jantan.
b.Untuk mengetahui besar efek motorik infusa akar Mrica Kepyar melalui metode
BAB II
PENELAHAAN PUSTAKA
A. Phytolacca americana .L
1. Klasifikasi
Divisi : Spermatophyta
Subdivisi : Angiospermae
Kelas : Dicotyledonae
Bangsa : Caryophyllales
Suku : Phytolaccaceae
Marga : Phytolacca
Jenis : Phytolacca americana L. ( Anonim, 1999).
2. Sinonim :Phytolacca decandra (Anonim, 2006b), Phytolacca acinosa Roxb (Huang, 1993).
3. Nama lain
a. Nama daerah
Mrico Kepyar (jawa) (Anonim, 1999).
b. Nama asing
Pokeroot, Pokweed, Gargetweed, Pokeberry, Pigeonberry, Virginia poke,
Cancer root, American nightshade, Redweed, Shang Lu (Anonim, 2006c;
Huang, 1993).
4. Uraian tanaman
Umumnya ditanam sebagai tanaman hias atau kadang tumbuh liar di
pinggir-pinggir jalan atau di tepi hutan, dari ketinggian 10 m hingga 1000 m di
atas permukaan laut. Tumbuh pada bebagai jenis tanah asal memiliki drainase
yang baik dan cukup mengandung bahan organik. Berbunga pada bulan Juni-Juli,
panen dilakukan pada bulan Agustus – September
Terna menahun, tegak, tinggi 0,5-1 m. Batang bulat, berkayu, permukaan
kasar, berwarna coklat kehijauan. Daun tunggal, berseling, tangkai bulat, panjang
3-5 cm, helaian daun bentuk lonjong sampai lanset. Ujung dan pangkal daun
runcing, tepinya rata, panjang 5-15 cm, lebar 2-4 cm, pertulangan menyirip,
permukaan berkerut, hijau keunguan. Bunga majemuk, berbentuk bulir, di ketiak
daun, kelopak bentuk bintang, panjang 1-2 mm, hijau kecoklatan. Buahnya
tunggal bulat, kulitnya lunak, berdiameter 3-8 mm, permukaan licin dan berwarna
merah. Biji bulat, keras dan putih. Akar tunggang , berwarna kuning kecoklatan
(Anonim, 1999).
5. Bagian yang digunakan
Akar dalam keadaan segar atau setelah dikeringkan (Anonim, 1999).
6. Kandungan kimia
Tanaman mengandung caffeik-aldehid, kalsium oksalat, PAP
(Pokeweed–antiviral–protein), phytolaccanin, phytolaccasaponin, phytolaccasida,
phytolaccatoxin, phytolacacin, asam phytolaccinic,dan pokeberrygenin. Pada
esculentik, isobetanin, isoprebetanin. Pada akar mengandung gum, hemiselulosa,
asam jaligonik, asam oleanolat, asam oxymiristik, asam phytolaccogenik,
phytolaccagenin, tanin dan xylose (Duke, 2007). Akar mengandung alkaloid,
saponin, dan polifenol (Anonim, 1999).
7. Kegunaan
Pelancar haid : 30 g akar mrica kepyar segar dicuci , direbus dengan 200
ml air sampai mendidih selama 15 menit, disaring, setelah dingin diminum; eksim
: 15 g akar mrica kepyar segar dicuci, ditumbuk halus, ditempelkan pada bagian
yang sakit dan dapat diulang 2-3 kali sehari (Anonim, 1999). Sebagai alteratif
yaitu secara bergangsur-angsur mengembalikan fungsi tubuh sebagaimana
mestinya dan meningkatkan kesehatan dan vitalitas, juga sebagai purgatif dan
emetik. Protein antiviral yang terkandung dalam pokeweed digunakan dalam
pengobatan kanker (Anonim,2006b).
B. Efek Tonikum dan Fungsi Motorik
Adaptogen adalah suatu substansi yang dapat meningkatkan daya
tahan/vitalitas tubuh terhadap pangaruh buruk dari berbagai faktor fisik, kimia,
maupun biologik (Widharto,1994). Zat tonika adalah suatu senyawa yang
mengurangi kondisi kelemahan dan tonus dari keseluruhan atau sebagian organ
makhluk hidup (Suhadi, 2000). Efek tonikum adalah perubahan yang terjadi karena
adaptogen. Fungsi motorik adalah fungsi dari otot, susunan saraf pusat yang
mempengaruhi dan menghasilkan gerak (Anonim, 1995a).
C. Infusa
Infusa adalah sediaan cair yang dibuat dengan mengekstraksi simplisia
nabati dengan air pada suhu 900C selama 15 menit. Pembuatan: campur simplisia
dengan derajat halus yang sesuai dalam panci dengan air secukupnya, panaskan diatas
tangas air selama 15 menit terhitung mulai suhu mencapai 900C sambil sekali-sekali
diaduk. Serkai selagi panas melalui kain flanel, tambahkan air panas secukupnya
melalui ampas melalui ampas hingga diperoleh volume infusa yang dikehendaki.
Infusa Daun Sena dan infusa simplisia yang mengandung minyak atsiri diserkai
setelah dingin. Infusa Daun Sena, infusa Asam Jawa dan infusa simplisia lain yang
mengandung lendir tidak boleh diperas. Kecuali dinyatakan lain, dan kecuali untuk
simplisia yang tertera di bawah, infusa yang mengandung bukan bahan berkhasiat
keras, dibuat dengan menggunakan 10 % simplisia. Untuk pembuatan 100 bagian
infusa berikut, digunakan sejumlah yang tertera yaitu Kulit Kina 6 bagian, Daun
Digitalis 0,5 bagian, Akar Ipeka 0,5 bagian, Daun Kumiskucing 0,5 bagian, Sekale
D. Metode Pengujian Aktivitas Motorik
Beberapa metode pengujian aktivitas motorik antara lain:
1. metode batang berputar (Rotarod test) adalah suatu uji dimana hewan uji
diletakkan di atas batang horizontal yang berputar (rotarod). Uji ini biasanya
dipakai untuk mengetahui fungsi otot karena pengaruh suatu obat sedatif.
Data yang teramati adalah berapa lama hewan uji dapat bertahan di atas
rotarod (waktu) dan jumlah jatuh hewan uji dari rotarod per satuan waktu
(Cakraborty, Mahapatra, Chaudhuri, 1986 ; Turner, 1965).
2. metode “ sangkar putar”. Metode ini digunakan untuk mengetahui aktivitas
motorik mencit dengan mengamati kemampuan mencit memutar alat roda
sangkar putar. Mencit dipilih terlebih dahulu yang mampu memutar alat
sebanyak 150-300 putaran dalam waktu 15 menit. Setelah diberi air atau
sediaan uji oral, mencit ditempatkan pada alat sangkar putar, aktivitasnya
diamati selang 15 menit selama 90 menit dimulai 5 menit setelah mencit
ditempatkan pada alat (Kitada, 1981; Carson, 1999 cit., Suwendar, Sigit,
Sopiah, 2004).
3. metode ketahanan berenang. Aktivitas motorik mencit diuji dengan
membebani ekor mencit dengan benda seberat 2 gram, kemudian mencit
tersebut dimasukkan kedalam wadah berisi air 30 menit setelah pemberian
sediaan. Ketahanan berenang diukur berdasarkan waktu mencit mulai
berenang sampai tenggelam, yaitu mencit berada di bawah permukaan air
E. Mekanisme Lelah
Ketahanan kerja (endurance performance) mempengaruhi terjadinya
kelelahan, penurunan endurance performance menyebabkan kelelahan. Penurunan
kerja terletak pada otot dan berhubungan dengan konsumsi sumber energi. Sementara
sumber energi menurun, produk seperti asam laktat cendrung terakumulasi dan
menghambat protein untuk berkontraksi dan menurunkan kekuatannya. Lebih lanjut
salah satu penyebab penting kelelahan otot adalah kegagalan pembebasan Ca2+ yang
merupakan pemicu terjadinya kontraksi .
Kontaksi otot merupakan peristiwa berantai yang kompleks (Gambar 1)
Kontraksi volunter bermula di motor kortex dan sebuah potensial aksi (i)
mengaktivasi α motor neuron (ii) yang mengeksitasi otot melalui neuromuscular junction( iii). Potensial aksi otot di transmisikan sepanjang permukaan membran (iv)
dan menurun pada tubula T(v). Sebuah sensor voltasi pada tubula T menyebabkan
terbukanya channel Ca2+ pada retikulum sarkoplasma (vi) menyebabkan kenaikan
konsentrasi Ca2+ pada mioplasma. Kalsium terikat pada troponin (vii), mengaktivasi
crossbrigde cycling dan tenaga (viii), untuk relaksasi memerlukan penarikan kembali
Ca2+ ke dalam retikulum sarkoplasma (ix).
Otot mungkin lelah karena berbagai alasan yang berbeda. Sistem Saraf Pusat
mungkin mengalami kegagalan menghasilkan potensial aksi, potensial aksi otot
mungkin gagal karena perubahan ionik, pembebasan energi cadangan, kerusakan
otot, energi cadangan utama dalam serabut otot, yang menyebabkan akumulasi asam
laktat yang mengurangi fungsi otot. Untuk beberapa tipe kelelahan, terjadi
penumpukan asam laktat intraselulaselular dan asidosis dapat meghambat kontraksi
protein (Allen, Lannergren, Westerblad, 2003).
Gambar1. Diagram proses berantai dalam kontraksi otot (Allen dkk, 2003)
Asam laktat terbentuk pada otot dalam proses glikolisis. Pada pH normal
asam laktat akan terdisosiasi menjadi H+ dan C3H5O3-, tidak ada masalah selama
konsentrasi H+ tidak melampaui kemampuan mekanisme buffer tubuh, masalah
terjadi ketika konsentrasi asam laktat dan H+ melampaui kapasitas buffer tubuh dan
menurunkan pH darah. Masalah yang terjadi antara lain yaitu munculnya rasa sakit,
penurunan kerja, dan kelelahan otot. Rasa sakit terjadi karena stimulasi terhadap
ujung saraf nyeri di otot pada penumpukan ion H+. Penurunan kerja terjadi karena
pada pH rendah ion H+ akan menginaktifkan enzim yang terlibat dalam
energi menurun sehingga terjadi penurunan kerja. Kelelahan otot terjadi karena pH
rendah menghambat aktin-miosin ATPase, enzim yang bertanggungjawab memecah
ATP dan menyediakan energi untuk kontraksi otot dan ion H+ juga menganggu aksi
dan pembebasan Ca2+ yang diperlukan untuk kontraksi otot, sehingga menyebabkan
penurunan kekuatan dan kecepatan kontraksi otot (Plowman dan Smith, 2003 ).
Meskipun demikian, terdapat tipe kelelahan lain dimana tidak terjadi
penumpukan asam laktat. Kita perlu mempertimbangkan sumber energi dalam
serabut otot. Adenosin Tri Posfat merupakan sumber energi universal dalam sel dan
digunakan langsung oleh crossbridge dan pompa ion, meskipun demikian ATP hanya
mampu memberikan energi untuk kontraksi maksimal selama 2-3 s. Ketika otot
kehabisan ATP, maka otot tidak dapat dapat berkontraksi dan menjadi sangat kaku
sehingga memicu kelelahan, jika terjadi terus menerus dapat menyebabkan kerusakan
otot. Untuk mengindari kehabisan ATP, otot memiliki berbagai macam sumber energi
cadangan dan sangat efektif menjaga konsentrasi ATP tidak pernah turun sekitar
20% dari level istirahat normal pada otot yang dilelahkan secara maksimal. Energi
cadangan yang paling mudah dimanfaatkan adalah fosfokreatinin yang secara
langsung mengisi kembali ATP dan suplainya berlangsung selama 10-20 menit.
Sumber lain yang penting adalah glikogen yang secara cepat dipecah secara
anaerobik Glikogen juga dapat dipecah secara aerobik tetapi lebih lama, dan
menghasilkan cukup ATP untuk kontraksi otot mendekati rata-rata 30-60 menit.
yang sangat besar tetapi sangat lamban. Ketika glikogen yang tersimpan habis, otot
harus melanjutkan pada metabolisme lemak.
Pada lari 100m dengan durasi yang pendek dan kecepatan tinggi, terkadang
terjadi kelelahan, asam laktat hanya terbentuk sedikit selama aktivitas pendek seperti
ini, sebagian besar energi didapatkan dari pemecahan posfokreatinin. Pemecahan
fosfokreatinin mengkonsumsi ion H+ sehingga berefek pH mioplasma tidak berubah
sepanjang lari. Salah satu produk pemecahan fosfokreatinin adalah ion fosfat yang
dapat menekan fungsi otot, mengurangi sensitivitas Ca2+ dari protein kontraktil (gbr.1
vii) dan kemampuan protein kontraktil untuk memproduksi tenaga (gbr.1 viii).
Akumulasi ion fosfat tersebut yang kemungkinan menyebabkan kelelahan selama lari
100 m.
Kontraksi maksimal berkelanjutan terjadi ketika mengangkat sesuatu yang
sangat berat kelelahan secara cepat terjadi dalam aktivitas seperti ini. Sebagai
tambahan aliran darah menuju otot yang aktif berhenti selama kontaraksi maksimal,
jadi tidak terdapat pasokan oksigen maupun pengangkutan metabolit atau ion.
Kelelahan berat terjadi dan otot melemah secara cepat. Kelelahan ini disebabkan
perubahan distribusi ion diatas membran sel. Setiap potensial aksi berhubungan
dengan masuknya ion Na + ke dalam sel dan keluarnya ion K+ dari sel, akibatnya ion
K+ cendrung terakumulasi diluar serabut saraf dan hasilnya adalah depolarisassi dan
ganguan aktivasi elektrik dari sel otot. Akumulasi K+ ekstraselular ini kemungkinan
menjadi besar dalam lumen tubula T dimana ion K+ hanya terdifusi lebih lambat hal
konsekuensinya adalah penurunan level Ca2+ dan penurunan aktivasi pada pusat
serabut saraf .
Pada percobaan suatu serabut otot terisolasi yang distimulasi sampai lelah
terjadi kegagalan pembebasan Ca2+ dari retikulum sarkoplasma, penyebab pasti belum
diketahui, hipotesis terbaru adalah bahwa retikulum sarkoplasma gagal melepaskan
Ca2+ kemungkinan karena Ca2+ dan fosfat dalam retikulum sarkoplasma melebihi
solubilitas produk Ca2+ fosfat dan mengendap, dengan demikian mengurangi Ca2+
bebas untuk dibebaskan. Mekanisme ini hanya berjalan karena fosfat pada
mioplasma naik secara substantial selama kelelahan dan dapat memasuki retikulum
sarkoplasma. Hal ini berkaitan dengan kerja yang berlangsung mendekati kapasitas
maksimum dari otot dan melibatkan jalur aerobik dan anaerobik ATP. Kegagalan
pembebasan Ca2+ juga terjadi pada saat otot kekurangan glikogen, hal ini biasa terjadi
pada pelari maraton.
Pemulihan lelah ditemukan sangat komplek, dengan komponen yang cepat
dan lambat. Komponen cepat disebabkan oleh pembalikan bentuk metabolit yang
menyebabkan lelah sebagai contoh pembersihan asam laktat dan restorasi
fosfokreatinin akan mengurangi kelebihan ion fosfat. Asam laktat akan dioksidasi
menjadi asam piruvat dan NAD+ akan akan direduksi menjadi NADH2, kemudian
digunakan kembali pada glukoneogenesis. Proses ini berlangsung cepat dan lengkap
dalam menit. Komponen yang lebih lambat mebutuhkan beberapa hari agar otot
kembali pada kapsitas normalnya. Percobaan dengan otot terisolasi memperkirakan
aksi normal, dan retikulum sarkoplasma dalam keadaan normal dimuati Ca2+ tetapi
coupling antara potensial aksi dan Ca2+ rusak, suatu dugaan adalah beberapa proses
aktivasi Ca2+ mungkin merusak protein dalam pembebasan Ca2+, hal ini biasa terjadi
pada latihan olahraga yang berlebihan (Allen dk.,2003) .
Adenosin merupakan konstituen selular normal yang diatur terutama oleh
ATP dan nukleotida lainnya. Konsentrasi adenosin dalam otot dan plasma meningkat
selama kontraksi otot. Konsentrasi adenosisn juga meningkat secara terus menerus di
otak sepanjang kelelahan dan menurun pada waktu tidur (Davis dkk, 2003).Adenosin
terbentuk secara intraselular dari ATP. Adenosin tidak berada dalam vesikel tetapi
dibebaskan dengan eksositosis terutama oleh transpor carier perantara. Konversi
sejumlah kecil ATP menghsilkan sejumlah besar adenosin. Adenosin Tri Fosfat
dikemas dalam vesikel dan dibebaskan dengan eksositosis sebagai transmiter
konvensional, tetapi juga dapat menerobos sel dalam kondisi kerusakan sel, ATP
yang terbebas secara cepat diubah menjadi adenosin. Adenosin menghasilkan efek
melalui pasangan reseptor G protrein (dengan subtype reseptor A1,A2, dan A3)
sementara ATP beraksi pada reseptor P2x dan P2y
Ada dua tipe purin reseptor yaitu reseptor P1 (subtype A1, A2 , dan A3)
reseptor ini berespon terhadap adenosin, dan jaringan pasangan reseptor G protein
(GPCRs) untuk menstimulasi atau menghambat adenilat silase, berada dibeberapa
jaringan berbeda. Reseptor P2 (subtype P2x dan P2y), masing-masing dengan
beberapa devisi selanjutnya , berespon terhadap ATP atau ADP. Efek utama adenosin
1. Vasodilatasi, termasuk pembuluh jantung (A2) kecuali pada ginjal,
dimana reseptor A1 menghasilkan vaso konstriksi: infus adenosin
menyebabkan penurunan tekanan darah.
2. Menghambat agregasi platelet (A2)
3. Menghambat konduksi arterioventricular jantung (A1) dan pengurangan
kekuatan kontraksi
4. Bronkokonstrikasi, terutama pada subjek asma, efek antiasma dari
metilxantin sebagian mencerminkan antagonisme reseptor A1
5. Pembebasan mediator dari mast sel (A3) berkontribusi pada
bronkokonstriksi
6. Menstimulasi afferent neoron terutama pada jantung (A2) adenosin
dibebaskan sebagai respon pada ischemia diduga sebagai suatu
mekanisme nyeri angina, badan carotid afferent juga distimulasi
menghasilkan reflek hiperventilasi.
7. Menghambat pembebasan transmiter pada beberapa saraf pusat dan
perifer (A1) , pada CNS adenosin mendesak aksi depresan pre- dan post
sinapsis, mengurangi aktivitas motorik, menekan pernafasan menginduksi
tidur, dan mengurangi kecemasan, semua efek berlawanan dengan efek
metilxantine.
8. Proteksi neuron pada ischemia serebral kemungkinan melalui inhibisi
metilxantin merupakan antagonisme beberapa efek adenosin, beraksi pada kedua
reseptor A1 dan A2 (Rang, Dale, Ritter, Moore, 2003).
F. Kafein
Gambar 2. Kafein (1,3,7 trimetilxantin)
Kafein termasuk dalam senyawa metilxantin. Kafein adalah serbuk putih tidak berbau, berasa pahit. Kafein diperoleh dari ekstraksi bahan alam atau melalui
sintesis kimia. Kafein dialam berupa alkaloid (Dollory, 1999). Kafein terdapat dengan
kadar tinggi dalam kopi, teh, minuman kola, permen coklat dan cocoa (Mycek,
Harvey, Champe, 1997 ).
Metilxantin dapat bekerja melalui berbagai mekanisme termasuk translokasi
kalsium, penghambatan fosfodiesterase, dan antagonis reseptor adenosin. Walaupun
konsentrasi yang diperlukan untuk memberikan aksi translokasi kalsium,
penghambatan fosfodiesterase di luar kisaran dosis farmakologis secara in vivo.
Senyawa xantin yang lain adalah teofilin yang ditemukan dalam teh dan teobromin
yang ditemukan didalam coklat. Dari ketiganya kafein dan teofilin memiliki efek N
N N
N
H3C
O
3
CH3
O
yang poten pada susunan saraf pusat, sedangkan efek teobromin relatif kecil.
Stimulan minor ini, terutama kafein dan teofilin, terbukti memiliki nilai medis,
mereka menstimulasi susunan saraf pusat, beraksi pada ginjal sebagai diuretik,
menstimulasi otot jantung dan merelaksasi otot polos. Orang yang memiliki asma
tercatat bahwa mereka bisa bernafas dengan lebih mudah setelah meminum secangkir
teh. Teofilin memiliki efek terbesar pada sistem kardiovaskular. Efek utama kafein
adalah meningkatkan kecepatan dan kejernihan dalam berfikir. Tabel I meringkas
potensi relatif efek biologis dari kafein, teofilin, dan teobromin .
Tabel I. Perbandingan potensi dari bahan aktif (xantine) dalam kopi, teh, dan coklat
Efek fisiologi xantine Urutan potensi (besar ke kecil)
Stimulan susunan saraf pusat Kafein = teofilin > teobromin Efek stimulan pada pusat pernafasan Kafein > teofilin > teobromin Meningkatkan kapasitas kerja otot Kafein > teofilin > teobromin Stimulasi otot jantung Teofilin > kafein > teobromin
Aksi diuretik Teofilin > kafein > teobromin
Relaksasi otot polos bronki Teofilin paling poten Meningkakan kecepatan metabolisme basal Kafein paling poten
(Witters, 1983)
Kisaran dari efek kafein secara akut diberikan pada dosis 300-600 mg,
termasuk stimulan susunan syaraf pusat menyebabkan penurunan rasa letih dan
meningkatkan kesiagaan mental, kenaikan tekanan darah dan cardiac output,
diuresis, kenaikan asam lemak bebas, dan pembebasan katekolamin dari medula
adrenal. Toleransi terjadi pada jantung, ginjal, dan, susunan saraf pusat pada
penggunaan kronik. Kafein diabsorbi seluruhya secara cepat setelah pemberian oral,
dengan konsentrasi puncak diantara 5 dan 90 menit. Metilxantin dimetabolisme
dalam hati dan metabolitnya kemudian dikeluarkan dalam urin. Jalur metabolsme
kafein pada orang dewasa adalah demetilasi 1, 3, dan 7 membentuk theobromin,
paraxantine, dan theofilin, produk demetilasi ini ditemukan dalam plasma setelah
pemberian kafein, ketiga produk ini akan mengalami biotransformasi lebih lanjut.
Produk metabolit primer minor termasuk 1,3,7 asam trimetilurik dan derivat urasil
(Dollory, 1999). Efek samping kafein termasuk didalamnya nyeri pencernaan, mual,
diutesis, takikardia, dan stimulasi saraf pusat (agitasi, jitteriness, tremor, dan
konvulsi). Efek samping dosis sedang menyebabkan insomnia, ansietas, dan agitasi.
Penggunaan kronik lebih dari 500 mg kafein per hari dapat menyebabkan demam
ringan yang tidak teratur, insomia, anoreksia, ansietas, dan iritasi. Pada dosis tingi
memperlihatkan toksisitas berupa mutah dan konvulsi. Dosis sekitar 10 g untuk
kafein menimbulkan aritmia jantung (Dollory, 1999; Mycek dkk., 1997).
G. Keterangan Empiris
Penelitian ini bersifat eksploratif untuk mendapatkan keterangan ada tidaknya
efek motorik infusa akar Mrica Kepyar pada mencit jantan dengan metode rotarod
BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian tentang efek motorik infusa akar Mrica Kepyar pada mencit
jantan dengan metode rotarod test merupakan jenis penelitian eksperimental murni
dengan menggunakan rancangan acak lengkap pola searah.
B. Variabel Penelitian
1. Variabel bebas dalam penelitian ini adalah dosis infusa akar Mrica Kepyar yang
diberikan pada mencit jantan.
2. Variabel tergantung dalam penelitian ini adalah lama jatuh pertama mencit dari
rotarod, jumlah kumulatif jatuh mencit dari rotarod selama (3x60) menit, dan
persen proteksi .
3. Variabel pengacau terkendali dalam penelitian ini adalah :
a. hewan uji mencit jantan galur Swiss Webster, umur 2-3 bulan, berat badan
20–30 g, jenis kelamin jantan.
b. bahan uji yaitu akar Mrica Kepyar. yang dipanen dari tempat tumbuh dan
pada waktu yang sama dan diperlakukan sama.
c. Proses pembuatan infusa akar Mrica Kepyar.
d. Kafein (sebagai kontrol positif) diperoleh dari laboratorium Kimia Analisis
dan Instrumental, Fakultas Farmasi, Universitas Sanata Dharma.
4. Variabel pengacau tak terkendali
Variabel pengacau tak terkendali dalam penelitian ini adalah keadaan fisiologis
hewan uji.
C. Definisi Operasional
1. Akar Mrica kepyar adalah simplisia yang berasal dari akar Mrica Kepyar, bagian
yang diambil adalah mulai pangkal akar sampai ujung akar.
2. Efek motorik adalah salah satu fungsi dari efek tonikum. Efek tonikum
merupakan perubahan yang terjadi karena pemberian zat tonika. Efek tonikum
memiliki berbagai fungsi seperti stimulan pusat pernafasan, stimulan otot jantung,
peningkatan kecepatan metabolisme basal, dan peningkatan kapsitas kerja otot.
Efek tonikum yang diamati pada penelitian ini dibatasi pada fungsi motorik .
3. Infusa dalam penelitian ini adalah sediaan cair yang dibuat dengan mengekstraksi
simplisia nabati dengan air pada suhu 900C selama 15 menit. Pembuatan dengan
mencampur 30 g serbuk akar Mrica Kepyar dengan derajat halus yang tertentu
(lihat butir 3) dalam panci dengan 100 ml air, panaskan diatas tangas air selama
15 menit terhitung mulai suhu mencapai 900C sambil sekali-sekali diaduk.
Diserkai selagi panas melalui kain flanel, tambahkan air panas secukupnya
melalui ampas melalui ampas hingga diperoleh volume infusa 100 ml. Pembuatan
4. Serbuk akar Mrica Kepyar yaitu serbuk akar Mrica Kepyar yang di ayak dengan
menggunakan ayakan yang jumlah lubang setiap incinya adalah 35 diukur searah
panjang kawat.
D. Bahan Penelitian
1. Hewan uji yang digunakan adalah mencit jantan galur Swiss Webster, umur 2-3
bulan, berat badan 20-30 diperoleh dari Laboratorium Farmakologi dan
Toksikologi, Fakultas Farmasi, Universitas Sanata Dharma Yogyakarta.
2. Bahan uji yang digunakan adalah akar Mrica Kepyar yang diperoleh dari CV
Indmira, Kaliurang Yogyakarta.
3. Kontrol negatif yang digunakan adalah aquadest yang diperoleh dari Laboratorium
Farmakologi dan Toksikologi, Fakultas Farmasi, Universitas Sanata Dharma
Yogyakarta.
4. Kontrol positif yang yang digunakan adalah kafein (Brataco Chemica, No batch.
J185/00) kualitas farmasetis diperoleh dari laboratorium Kimia Analisis dan
Instrumental, Fakultas Farmasi, Universitas Sanata Dharma.
E. Alat Penelitian
1. Pisau berbahan stainlesstel, talenan kayu, penggaris, baki berpori.
2. Tampah dan kain hitam.
3. Oven (Memmert)
5. Ayakan
6. Peralatan infusa yaitu panci infusa, termometer (YENACO 0C), pengaduk,
pengaduk, penangas listrik (Maspion), kain flanel, beker glass 100 ml (Pyrex),
sendok.
7. Neraca g/mg balance (Mettler PM 4600 Deltarange ), Neraca analitik (Mettler
Toledo AB 204)
8. Rotarod dengan kecepatan putar 11 kali putar per menit dengan diameter 3 cm
panjang 32,5 cm yang disekat menjadi 5 bagian.
9. Spuit injeksi peroral ukuran 1 ml (Terumo)
10.Stopwatch (Alba).
11.Kamera digital (Canon).
F. Tata Cara Penelitian 1. Determinasi tanaman
Determinasi tanaman Mrica Kepyar dilakukan di Laboratorium Kebun
Obat, Fakultas Farmasi, Universitas Sanata Dharma.
2. Pengumpulan dan pembuatan simplisia
Pembuatan simplisia akar Mrica Kepyar adalah dengan memanen akar
tanaman Mrica Kepyar dari CV Indmira, Kaliurang, Yogyakarta pada usia 9
bulan, pada bulan Juli, pada waktu pagi hari. Bahan uji yang diperoleh disortasi
dari bagian yang rusak dan pengotor (tanah), kemudian dicuci dengan air bersih
kemudian dirajang ± 3 mm, dan dikeringkan dengan tidak terkena sinar matahari
langsung. Bahan uji yang cukup kering dimasukkan dalam oven pada suhu ±
50°C hingga benar- benar kering, yaitu bisa dipatahkan dengan tangan. Simplisia
kering diserbuk dengan mesin penyerbuk dan diayak dengan ayakan yang sesuai.
3. Penyiapan hewan uji
Hewan uji mencit jantan galur Swiss Webstar, usia 2-3 bulan, berat-badan
20-30 g diperoleh dari laboratorium Farmakologi-Toksikologi Fakultas Farmasi,
Universitas Sanata Dharma. Mencit sebanyak 42 ekor dikelompokan secara acak
menjadi 6 kelompok.
4. Pembuatan sediaan
a. Larutan kafein 0.11 % b/v sebanyak 50 ml , dibuat dengan melarutkan 0.0550
g kafein dalam aquadest sampai 50 ml
b. Larutan kafein 0.13 % b/v sebanyak 50 ml , dibuat dengan melarutkan 0.0650
g kafein dalam aquadest sampai 50 ml
c. Larutan kafein 0.16 % b/v sebanyak 50 ml , dibuat dengan melarutkan 0.0800
g kafein dalam aquadest sampai 50 ml
d. Larutan kafein 0.19 % b/v sebanyak 50 ml , dibuat dengan melarutkan 0.0950
g kafein dalam aquadest sampai 50
e. Larutan kafein 0.23 % b/v sebanyak 50 ml , dibuat dengan melarutkan 0.0115
g kafein dalam aquadest sampai 50 ml
f. Infusa dibuat dengan menimbang 30 g serbuk akar Mrica Kepyar dan
sampai 900C, setelah 15 menit dari suhu 900C disaring dengan kain flanel
tanpa diperas. Volume yang dibuat adalah 100 ml jika terjadi kekurangan
volume, tambahkan aquadest panas melalui ampas pada kain flanel hingga
diperoleh volume 100 ml. Kadar yang diharapkan adalah 30% b/v.
5. Penentuan dosis Kafein
Dalam penelitian ini, kafein digunakan sebagai kontrol positif. Dosis
terapi kafein adalah 300-600 mg untuk manusia 70 kg (Dollery, 1999).
Konversi dosis ke mencit dengan berat badan 20 g dengan faktor konversi
manusia dengan berat badan 70 kg ke mencit 20 g adalah 0,0026 (Anonim,
2005)
Dosis = (300-600) mg x 0,0026
= (0.78-1.56) mg / 20 gBB
= (39-78) mg/KgBB
selanjutnya peringkat dosis ditentukan dengan cara mengalikan dosis dengan
faktor pengali, yang diperoleh berdasarkan rumus berikut
(1)
1 −
=
nSD
LD
F
Keterangan :
F = increment factor n = jumlah peringkat dosis
LD = Large Dose ( dosis tertinggi) SD = Small Dose (dosis terendah)
1 5
39
− =
Diperoleh
F = 1.19
Dosis kafein yang diujikan yaitu 39 mg/KgBB, 46,41 mg/KgBB, 55,23
mg/KgBB, 65,72 mg/KgBB, dan 78,20 mg/KgBB.
7. Penentuan rentang waktu setelah pemberian kafein
Rentang waktu setelah pemberian kafein ditentukan untuk mengetahui
rentang waktu pemberian dimana senyawa uji telah terabsorbsi dengan
optimal sehingga dapat segera menimbulkan efek. Penentuan rentang waktu
aetelah pemberian kafein dilakukan dengan menggunakan kafein dosis 65,72
mg/KgBB yang memberikan rata-rata waktu pertama jatuh paling besar dan
jumlah kumulatif jatuh mencit dari rotarod paling kecil, dengan variasi selang
waktu yaitu 15 menit, 30 menit, 45 menit, dan 60 menit. Dari keempat selang
waktu tersebut dicari selang waktu yang dapat memberikan waktu pertama
jatuh mencit dari rotarod paling besar dan rata-rata jumlah kumulatif jatuh
mencit dari rotarod selama (3x60) menit paling sedikit. 8. Penentuan dosis infusa akar Mrica Kepyar
Dari literatur diperoleh penggunaan akar Mrica Kepyar
dimasyarakat di Indonesia adalah 30 g akar segar (Anonim,1999),
dikonversikan ke manusia berat badan 70 kg : 30 50x 70
mg = 38,18 g akar
Konversi dosis ke mencit dengan berat badan 20 g dengan factor
konversi manusia dengan berat badan 70 kg ke mencit 20 g adalah 0,0026
(Anonim, 2005) :
Dosis = 38.18 g x 0.0026
= 0.09927 g/20 g BB
Penyusutan berat simplisia setelah pengeringan dan adalah 11%
Penyusutan = 11/100 x 0.09927 g
= 0.01092 g
Berat serbuk yang diperlukan
(0.09927 - 0.01092) g = 0.08835 g/20gBB
Dosis yang diperoleh yaitu 4.42 g/KgBB, digunakan sebagai dosis terendah.
Konsentrasi infusa akar Mrica Kepyar yang dipergunakan dalam
penelitian ini adalah 30%. Volume pemberian minimal untuk mencit 30 g
diperoleh dengan rumus
)
selanjutnya peringkat dosis ditentukan dengan cara mengalikan volume
pemberian dengan faktor pengali, yang diperoleh berdasarkan rumus (1)
dengan LD volume tertinggi (1ml yaitu volume pemberian maksimum pada
1 4
44 . 0
00 , 1
− =
F = 1.31
Volume pemberian infusa yang diujikan adalah adalah 0,44 ml, 0,58 ml,
0,76 ml, 0,99 ml untuk mencit 30 g.
9. Penentuan rentang waktu setelah pemberian infusa akar Mrica Kepyar
Rentang waktu setelah pemberian infusa ditentukan untuk
mengetahui rentang waktu pemberian dimana senyawa uji telah terabsorbsi
dengan optimal sehingga dapat segera menimbulkan efek. Penentuan
rentang waktu setelah pemberian infusa dilakukan dengan menggunakan
infusa dengan volume pemberian 0,76 ml/30gBB yang memberikan jumlah
kumulatif jatuh mencit dari rotarod selama (3x60) menit paling sedikit,
dengan variasi selang waktu yaitu 15 menit, 30 menit, 45 menit, dan 60
menit. Dari keempat selang waktu tersebut dicari selang waktu yang dapat
memberikan waktu pertama jatuh mencit dari rotarod paling besar dan
rata-rata jumlah kumulatif jatuh mencit dari rotarod paling kecil.
10. Pengujian efek motorik
Hewan uji diadaptasi terlebih dahulu selama 4 hari setiap hari selama
5 menit di atas rotarod. Pemberian larutan uji dilakukan selama 4 hari. Pada
hari ke 4, mencit diadaptasikan selama 5 menit diatas rotarod dan diberi
larutan uji secara oral, didiamkan ± 15 menit agar larutan diabsorbsi,
uji sebelumnya sudah dipuasakan 1x 24 jam. Pengambilan data berupa waktu
pertama jatuh mencit, jumlah jatuh kumulatif mencit selama 3x60 menit.
11. Penentuan Efek Motorik
Efek motorik dihitung dengan menggunakan persamaan Handershot
dan Forsaith, yaitu:
% Proteksi = 100 – [(P/K) x 100%] (2)
Keterangan:
P = rata-rata jumlah kumulatif jatuh mencit kelompok perlakuan
K = rata-rata jumlah kumulatif jatuh mencit kelompok kontrol negatif.
12. Analisis Hasil
Data yang dikumpulkan untuk uji efek motorik infusa akar Mrica
Kepyar adalah waktu jatuh pertama dan rata-rata jumlah kumulatif jatuh
mencit dari rotarod selama 3x60 menit. Data dianalisis dengan
Kolmogorov-Smirnov untuk melihat distribusi data. Analisis dilanjutkan dengan analisis
variansi satu arah dengan taraf kepercayaan 95% atau yang sesuai untuk
mengetahui apakah terdapat perbedaan antar kelompok. Selanjutnya
dilakukan Post Hoct test untuk mengetahui perbedaan tersebut bermakna atau
BAB IV PEMBAHASAN A. Determinasi Tanaman
Determinasi tanaman dilakukan di laboratorium Kebun Obat, Fakultas
Farmasi, Universitas Sanata Dharma secara makroskopik. Determinasi dilakukan
dengan cara membandingkan ciri-ciri morfologi tanaman Mrica Kepyar yang
digunakan dengan acuan yang ada. Acuan yang digunakan yaitu buku Inventaris
Tanaman Obat Indonesia edisi V dan situs Classification for Kingdom Plantae Down
to Species Phytolacca americana L. http://plants.usda.gov/java/Plants Profile for
Phytolacca americana (American pokeweed). Hasil menunjukkan bahwa tanaman
yang digunakan dalam penelitian adalah Phytolacca americana L. (Anonim, 1999;
Anonim, 2006a).
B. Pengumpulan dan Pembuatan Simplisia
Tanaman Mrica kepyar yang dipanen akarnya merupakan tanaman budidaya,
sehingga keseragaman umur saat panen, lingkungan tempat tumbuh, dan jenis dapat
ditentukan sehingga diperoleh mutu simplisia yang seragam. Akar Mrica Kepyar
yang diperoleh disortasi dari bagian yang rusak, pengotor (tanah) dan dicuci dengan
air bersih yang mengalir. Tanah mengandung bermacam-macam mikroba dalam
jumlah tinggi, pembersihan simplisia dari tanah yang terikut dapat mengurangi
jumlah mikroba awal. Pencucian dilakukan untuk menghilangkan tanah dan pengotor
lain yang melekat pada bahan simplisia. Bahan simplisia kemudian ditiriskan dan
dirajang, perajangan bahan simplisia dilakukan untuk mempermudah dan
mempercepat proses pengeringan, penyimpanan, dan penyerbukan. Perajangan
dilakukan dengan pisau dari bahan stainlesstell dengan ketebalan ± 3 mm. Alat dari
logam dihindari karena diperkirakan akan merusak senyawa aktif seperti fenol,
glikosida, dsb. Bahan simplisia diiris denga ketebalan ± 3 mm, untuk menghindari
terjadinya face hardening pada saat pengeringan, yakni bagian luar masih kering,
tetapi bagian dalam masih basah, hal ini disebabkan penguapan bahan di permukaan
air jauh lebih cepat daripada difusi air dari dalam ke permukaan, sehingga permukaan
bahan menjadi keras dan menghambat pengeringan selanjutanya. Face hardening
dapat terjadi karena irisan bahan simplisia yang terlalu tebal dan dapat
mengakibatkan kebusukan simplisia, jika irisan terlalu tipis dapat mengakibatkan
berkurang atau hilangnya zat berkasiat akibat penguapan pada pengeringan. Bahan
simplisia kemudian dikeringkan dengan tidak terkena sinar matahari langsung. Bahan
uji yang cukup kering dimasukkan dalam oven pada suhu ± 50°C hingga benar-benar
kering, yaitu bisa dipatahkan dengan tangan. Pengeringan dilakukan untuk
mengurangi kadar air dalam simplisia sehingga didapatkan simplisia yang tidak
mudah rusak dan dapat disimpan dalam waktu lebih lama. Air yang masih tersisa
dalam simplisia dapat memfasilitasi enzim tertentu dalam sel bekerja menguraikan
senyawa aktif sesaat setelah sel mati, selain itu dapat memicu tumbuhnya kapang dan
jasad renik lainnya sehingga dapat menurunkan mutu simplisia, dengan mengurangi
kadar air dapat menghentikan reaksi enzimatik pada bahan simplisia. Bahan simplisia
melebihi 60°C , pada penelitian ini dipilih suhu pengeringan 50°C. Simplisia kering
diserbuk dengan mesin penyerbuk dan diayak dengan yang di ayak dengan
menggunakan ayakan yang jumlah lubang setiap incinya adalah 35 diukur searah
panjang kawat. Penyerbukan dilakukan untuk memperluas permukaan yang
bersentuhan dengan larutan penyari, sehingga proses penyarian berjalan optimal.
Penyarian merupakan peristiwa pemidahan massa, zat aktif yang semula berada
dalam sel ditarik oleh cairan penyari sehingga terjadi larutan zat aktif dalam cairan
penyari tersebut. Semakin kasar serbuk simplisia semakin semakin panjang jarak
yang ditempuh untuk memindahkan zat aktif sehingga zat aktif yang tertinggal dalm
sel semakin banyak. Penyerbukan yang terlalu halus akan menyebabkan banyak
dinding sel pecah sehingga menyebabkan zat yang tidak diinginkan terikut dalam
penyrian, oleh karena itu diperlukan derajat halus yang tepat untuk memperoleh hasil
penyarian yang baik. Menurut materia medika pembuatan serbuk untuk percobaan
laboratorium keculi dinyatakan lain seluruh simplisia harus diayak menjadi serbuk
4/18. Jenis pengayak dinyatakan dengan nomor yang menunjukan jumlah lubang tiap
cm dihitung searah panjng kawat. Pada penelitian ini serbuk di ayak dengan
menggunakan ayakan yang jumlah lubang setiap incinya adalah 35 diukur searah
panjang kawat.
C. Penyiapan hewan uji
Hewan uji yang dipilih adalah mencit jantan galur Swiss Webstar, usia 2-3
Farmakologi-Toksikologi Fakultas Farmasi, Universitas Sanata Dharma. Pada penelitian ini
digunakan mencit dengan galur Swiss Webster karena karakternya yang lebih mudah
beradaptasi dan tidak mudah stress dibandingkan dengan BAPSI. Mencit sebanyak
42 ekor dikelompokan secara acak menjadi 6 kelompok. Setelah dikelompokan,
mencit diadaptasikan dalam kandang yang baru selama 3 hari, setelah itu
diadaptasikan diatas rotarod 5 menit setiap hari selama 4 hari, dengan tujuan
membiasakan mencit diatas rotarod, sehingga pada saat perlakuan jumlah jatuh yang
dihitung adalah karena lelah bukan karena faktor tidak terbiasa pada mencit. Mencit
dipuasakan sehari, setelah itu baru diberi perlakuan. Mencit dipuasakan dengan
tujuan menghidari interaksi sediaan uji dengan makanan pada pencernakaan mencit,
yang dapat mempengaruhi efek yang dihasilkan .
D. Pembuatan Sediaan
Larutan kafein dibuat dengan melarutkan serbuk kafein dengan aquadest
dingin, karena kafein mudah larut dalam aquadest. Pada penentuan dosis kafein ,
dibuat 5 konsentrasi larutan kafein yaitu 4 0.11 % b/v, dibuat dengan melarutkan
0.0550 g kafein dalam aquadest sampai 50 ml, 0.13 % b/v, dibuat dengan melarutkan
0.0650 g kafein dalam aquadest sampai 50 ml, 0.16 % b/v dibuat dengan melarutkan
0.0800 g kafein dalam aquadest sampai 50 ml, 0.19 % b/ , dibuat dengan melarutkan
0.0950 g kafein dalam aquadest sampai 50, dan 0.23 % b/v, dibuat dengan melarutkan
Infusa dibuat dengan menimbang 30 g serbuk akar Mrica Kepyar, serbuk
kemudian dibasahi dengan aquadest dengan volume 100 ml. Pembasahan serbuk
bertujuan untuk memberikan kesempatan sebesar-besarnya kepada cairan penyari
untuk memasuki pori-pori dalam simplisia sehingga mempermudah penyarian.
Serbuk akar yang telah ditambahkan aquadset kemudian dipanaskan sampai 900C,
setelah 15 menit dari suhu 900C disaring dengan kain flanel tanpa diperas. Penyarian
dilakukan saat bahan masih saat cairan masih panas dan tidak diperas karena
mengandung lendir. Volume yang dibuat adalah 100 ml jika terjadi kekurangan
volume, ditambahkan aquadest panas melalui ampas pada kain flanel hingga
diperoleh volume 100 ml. Kadar infusa pada umumnya adalah 10 %b/v , tetapi pada
penelitian ini dibuat simplisia dengan kadar 30% b/v. Pemberian pada mencit secara
per oral terbatas pada volume maksimum pemberian 1 ml untuk mencit 30 g, untuk
memperoleh dosis tertendah yang harus diberikan pada mencit yaitu 4.42 g/ KgBB
dengan kadar infusa 10% akan melebihi batas pemberian maksimal sehingga kadar
infusa yang dibuat adalah 30 % b/v .
E. Uji Pendahuluan 1. Penentuan dosis kafein
Penentuan dosis kafein dilakukan untuk menetapkan dosis kafein yang
dapat memberikan efek motorik yaitu dosis kafein yang memberikan rata-rata
waktu jatuh pertama mencit dari rotarod dan proteksi paling besar dan rata-rata
diberikan 5 variasi dosis kafein pada 5 kelompok masing-masing terdiri dari 7 ekor
mencit jantan, yaitu dosis 39 mg/KgBB, 46,41 mg/KgBB, 55,23 mg/KgBB, 65,72
mg/KgBB, dan 78,20 mg/KgBB. Pemberian kafein dilakukan secara per oral.
Rata-rata waktu jatuh pertama mencit dari rotarod pada penentuan dosis kafein dapat
dilihat pada tabel II dan disajikan dalam bentuk diagram batang pada gambar 3.
Tabel II.Rata-rata waktu jatuh pertama mencit dari rotarod pada penentuan dosis kafein
Keterangan:
Kelompok uji Subyek
uji
Waktu jatuh pertama dalam detik
(X±SE) Kafein dosis 39,00 mg/KgBB 7 6299,86 ± 1592,359 Kafein dosis 46,41 mg/KgBB 7 7028,71 ± 1532,930 Kafein dosis 55,23 mg/KgBB 7 5928,00 ± 1437,013 Kafein dosis 65,72 mg/KgBB 7 9086,43 ± 1235,839 Kafein dosis 78,20 mg/KgBB 7 5354,71 ± 1553,866
X = mean (rata-rata)
SE = standard eror ( (SD√n)
Error Bars show Mean +/- 1.0 SE
kafein 39.00 mg/KgBB
kafein 46.41 mg/KgBB
kafein 55.23mg/KgBB
kafein 65.72mg/KgBB
kafein 78.20 mg/KgBB
kelompok
6299.86 7028.71 5928.00 9086.43 5354.71
Untuk melihat adanya perbedaan rata-rata waktu jatuh pertama mencit pada
kelima kelompok tersebut dilakukan analisis variansi satu arah dengan taraf
kepercayaan 95%. Hasil analisis variansi satu arah rata-rata waktu jatuh pertama
mencit dari rotarod pada penentuan dosis kafein disajikan pada tabel III.
Tabel III. Hasil analisis variansi satu arah rata-rata waktu jatuh pertama mencit pada penentuan dosis kafein
Sumber variansi
Jumlah kuadrat
Derajat bebas
Rata-rata Kuadrat
F hitung
Probrabilitas
Antar kelompok
58528177 4 14632044,31 0,960 0,444
Dalam kelompok
4,57 x 108 30 15249198,58
Berdasarkan hasil analisis variansi satu arah pada tabel III diperoleh
probabilitasnya adalah 0,444 (>0,05), hal ini menunjukkan bahwa rata-rata waktu
jatuh pertama mencit pada kelima kelompok dosis tersebut tidak terdapat
perbedaan.
Rata-rata jumlah kumulatif jatuh mencit dari rotarod selama (3x60) menit
dan persen proteksi pada penentuan dosis kafein ditunjukkan pada tabel IV .
Rata-rata jumlah kumulatif jatuh mencit dari rotarod selama (3x60) menit dan persen
proteksi pada penentuan dosis kafein juga disajikan dalam bentuk diagram pada
Tabel IV. Rata-rata jumlah jatuh kumulatif mencit dari rotarod selama (3x60)menit dan persen proteksi pada penentuan dosis kafein
Kelompok uji Subyek uji
jumlah kumulatif jatuh selama (3x60) menit
(X±SE)
Persen proteksi ( X±SE)
Kafein dosis 39,00 mg/KgBB 7 1,6±0,649 72,4± 11,400
Kafein dosis 46,41 mg/KgBB 7 3,0 ±1,464 47,4± 25,680
Error Bars show Mean +/- 1.0 SE
kafein 39.00 mg/KgBB
kafein 46.41 mg/KgBB
kafein 55.23mg/KgBB
kafein 65.72mg/KgBB
kafein 78.20 mg/KgBB
kelompok
Error Bars show Mean +/- 1.0 SE
kafein 39.00 mg/KgBB
kafein 46.41 mg/KgBB
kafein 55.23mg/KgBB
kafein 65.72mg/KgBB
kafein 78.20 mg/KgBB
kelompok
72.4 47.4 72.4 90.0 19.8
(a) (b)
Gambar 4. (a) Diagram batang rata-rata jumlah kumulatif jatuh pertama mencit selama (3x60) menit pada penentuan dosis kafein
Untuk melihat adanya perbedaan rata-rata jumlah kumulatif jatuh mencit
selama (3x60) menit dan persen proteksi pada kelima kelompok dosis dilakukan
analisis n sampel bebas (uji Kruskal-Wallis), tidak digunakan analisis variansi satu
arah karena distribusai data tidak normal. Hasil analisis Kruskal-Wallis jumlah
kumulatif jatuh mencit dari rotarod selama (3x60) menit dan persen proteksi pada
penentuan dosis kafein disajikan pada tabel V.
Tabel V. Hasil analisis Kruskal-Wallis rata-rata jumlah kumulatif jatuh mencit selama (3x60) menit dan persen proteksi pada penentuan dosis kafein
jumlah kumulatif jatuh (3x60) menit
% proteksi
Chi –Square 4,889 4,889
Derajat bebas 4 4
Probrabilitas 0,299 0,299
Berdasarkan hasil analisis Kruskal-Wallis pada tabel V diperoleh
probabilitas pada data rata-rata jumlah kumulatif jatuh menit adalah 0,299 (>0,05)
dan persen proteksi adalah 0,299 (>0,05), hal ini menunjukkan bahwa rata-rata
jumlah kumulatif jatuh mencit selama (3x60) menit dan persen proteksi pada
kelima kelompok dosis tersebut tidak terdapat perbedaan, tetapi dapat dilihat dari
gambar 3 dan 4 dosis kafein 65,72 mg/KgBB memberikan rata-rata waktu jatuh
pertama mencit dari rotarod dan persen proteksi paling besar dan rata-rata jumlah
jatuh kumulatif mencit dari rotarod selama (3x60) menit paling kecil, sehingga
Kafein dapat mengurangi kelelahan pada fungsi motorik mencit karena
kafein merupakan antagonis reseptor adenosin. Adenosin menghasilkan efek
melalui pasangan reseptor G protein dengan subtype reseptor A1, A2, dan A3.
Efek adenosin pada reseptor A1 salah satunya adalah mendesak aksi depresan,
mengurangi aktivitas motorik, menekan pernafasan, menginduksi tidur, dan
mengurangi kecemasan. Semua efek tersebut berlawanan dengan efek metilxantin.
Target untuk protein G adalah adenilat silase enzim yang bertanggung
jawab terhadap pembentukan cAMP (siklik 3’5’ adenosin monofosfat), fosfolipase
C yaitu enzim yang bertanggung jawab terhadap pembentukan inositol fosfat, dan
kanal ion.
Siklik 3’5’ adenosin monofosfat (cAMP) adalah mediator intraseluler.
Siklik 3’5’ adenosin monofosfat disintesis didalam sel dari ATP dibantu adenilat
silase, cAMP di inaktivasi oleh enzim fosfodiestrase dengan dihidrolisis menjadi 5
AMP. Siklik 3’5’ adenosin monofosfat akan mengaktivasi protein kinase. Protein
kinase akan mengakativasi enzim-enzim yang terlibat dalam metabolisme lemak
dan glikogen di hati. Protein kinase akan mengaktifkan lipase sehingga terjadi
peningkatan pemecahan lemak, menginaktifkan glikogen sintesase sehingga
mengurangi sintesis glikogen, dan mengaktifkan phosforilkinase yang
mengakibatkan kenaikan pemecahan glikogen menjadi glukosa. Proses ini
mengubah energi cadangan (lemak dan glikogen) menjadi glukosa sebagai sumber
energi kontraksi otot. Metilxantin bekerja dengan menghambat enzim