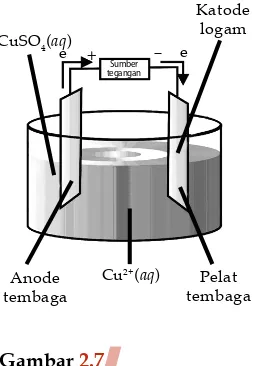
Bab 2 Reaksi Redoks dan Elektrokimia
Teks penuh
Gambar

Garis besar
Dokumen terkait
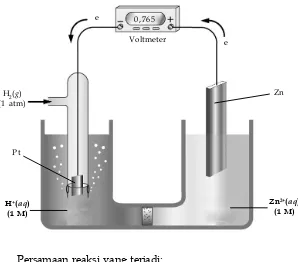
Karena semua data berlangsung reaksi reduksi maka untuk anode reaksi redoks dibalik dan harga potensial sel menjadi berlawanan dari nilai sebelumnya jika +
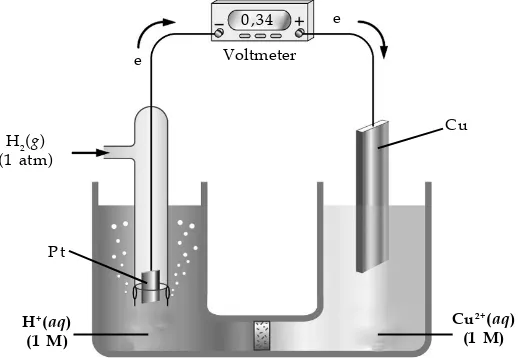
→ Potensia l elektroda dikaitkan dengan reaksi reduksi sehingga elektroda yang lebih mudah mengalami reduksi dibandingkan terhadap hidrogen, potensial elektrodanya bertanda negatif
Dari pernyataan berikut, reaksi setengah sel yang paling tepat untuk menyatakan reaksi pada elektroda negatif dari sel tersebut di atas adalah:.. Reaksi reaksi berikut ini, manakah
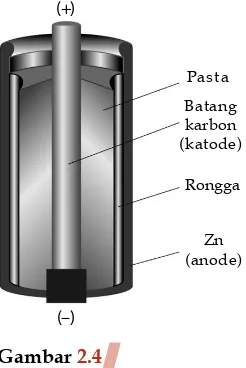
Pada elektrolisis larutan seng sulfat diguna- kan elektrode karbon, Pernyataan yang benar berdasarkan elektrolisis di atas, adalah ..... Pada elektrolisis yang bertujuan untuk
Reaksi oksidasi logam dapat ditekan dengan menyuplai elektron dari luar, dengan cara menempatkan materi lain yang lebih reaktif sebagai anode korban atau
Reaksi pada katode dan anode untuk sel elektrolisis dengan elektrolit larutan dan elektrode reaktif tergantung pada kompetisi potensial elektrode standar dari anion,
Suatu reaksi disebut disproporsionasi atau atutoredoks jika terdapat satu zat yang mengalami reaksi oksidasi dan reaksi reduksi sekaligus, dengan kata lain, oksidator dan
sel ) ialah besarnya beda potensial atau besarnya potensial yang dihasilkan dari dua buah elektroda (katoda dan anoda) yang dihubungkan oleh suatu penghantar. Karena pada