FRAKSINASI DAN KARAKTERISASI EKSTRAK ETIL
ASETAT AGF SERTA KAJIAN POTENSINYA SEBAGAI
BIONUTRIEN PADA PERTUMBUHAN TANAMAN CABAI
MERAH KERITING (Capsicum annum L.)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains dalam Bidang Kimia
Oleh:
Astri Rizki Nurmala NIM. 0909026
PROGRAM STUDI KIMIA JURUSAN PENDIDIKAN KIMIA
FAKULTAS PENDIDIKAN MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS PENDIDIKAN INDONESIA
FRAKSINASI DAN KARAKTERISASI EKSTRAK ETIL
ASETAT AGF SERTA KAJIAN POTENSINYA SEBAGAI
BIONUTRIEN PADA PERTUMBUHAN TANAMAN CABAI
MERAH KERITING (Capsicum annum L.)
Oleh
Astri Rizki Nurmala
Sebuah skripsi yang diajukan untuk memenuhi salah satu syarat memperoleh gelar Sarjana Sains pada Fakultas Pendidikan Matematika dan Ilmu Pengetahuan Alam
© Astri Rizki Nurmala 2013 Universitas Pendidikan Indonesia
November 2013
Hak Cipta dilindungi undang-undang.
ASTRI RIZKI NURMALA
FRAKSINASI DAN KARAKTERISASI EKSTRAK ETIL
ASETAT AGF SERTA KAJIAN POTENSINYA SEBAGAI
BIONUTRIEN PADA PERTUMBUHAN TANAMAN CABAI
MERAH KERITING
(Capsicum annum L.)
Disetujui dan Disahkan Oleh:
Pembimbing I
Drs. Yaya Sonjaya, M.Si NIP. 196502121990031002
Pembimbing II
Dr. Iqbal Musthapa, M.Si NIP. 197512232001121001
Mengetahui,
Ketua Jurusan Pendidikan Kimia FPMIPA UPI
ABSTRAK
Penelitian yang dilakukan bertujuan untuk mengetahui golongan metabolit sekunder yang terkandung dalam ekstrak etil asetat fraksi gabungan (FG) AGF serta potensinya sebagai bionutrien pada laju pertumbuhan dan hasil panen tanaman cabai merah keriting (Capsicum annum L.). Metode ekstraksi yang digunakan adalah maserasi menggunakan pelarut etil asetat. Fraksinasi dilakukan dengan metode kromatografi vakum cair (KVC), sedangkan analisis dan karakterisasi dilakukan dengan kromatografi lapis tipis (KLT), skrining fitokimia, dan spektroskopi FTIR. FG bionutrien AGF diaplikasikan sebagai pupuk organik cair dengan dosis 2 mL/L dan 10 mL/L, pelarut etil asetat digunakan sebagai blanko. Kontrol positif tanaman dilakukan dengan pemberian pupuk majemuk phonska dan pestisida “curacron EC 500” untuk mengetahui pola pertumbuhan tanaman cabai merah keriting dengan perlakuan seperti oleh petani. Hasil penelitian menunjukkan bahwa ekstrak etil asetat AGF memiliki metabolit sekunder dari golongan alkaloid, terpenoid, flavonoid, dan tanin. Hal tersebut didasari oleh hasil skrining fitokimia, analisis KLT, dan spektrum IR. Berdasarkan data pertumbuhan tanaman menunjukkan bahwa FG 2 bionutrien AGF memberikan pengaruh positif terhadap produktifitas tanaman dengan konstanta laju pertumbuhan tertinggi yaitu 0,1702 minggu-1 dengan jumlah buah cabai terbanyak yaitu 82 buah dengan massa terberat yaitu 186,6042 gram. Tanaman blanko etil asetat memiliki konstanta laju pertumbuhan 0,1617 minggu-1 dan hasil panen sebanyak 24 buah dengan massa buah 52,9547 gram. Berdasarkan hasil penelitian dapat disimpulkan bahwa FG 2 bionutrien AGF memberikan hasil terbaik pada laju pertumbuhan, jumlah buah, dan massa buah cabai merah keriting. FG 2 bionutrien AGF ini selain dapat digunakan sebagai pupuk organik cair juga berpotensi sebagai biopestisida.
Kata kunci: Bionutrien AGF, Kromatografi, Maserasi, Pupuk Organik Cair,
iii
ABSTRACT
The aims of this research is to determine the classification of secondary metabolites ethyl acetate extract AGF. The extraction method used in this research is maceration with ethyl acetate. Fractionation was conducted by using vacuum liquid chromatography (VLC), characterization of ethyl acetate extract AGF using thin layer of chromatography (TLC), phytochemical screening, and FTIR spectroscopy. Ethyl acetate extract of bionutrien AGF was applied as a liquid organic fertilizer with a dose of 2mL/L and 10 mL/L, the solvent ethyl acetate was used as a negative control. For positive control using “Phonska” as fertilizer and "Curacron EC 500" as pesticides to determine the growth of plant. The results of phytochemical screening, TLC analysis, and IR spectra, we can determine ethyl acetate extract AGF containing several secondary metabolites such as alkaloids, terpenoids, flavonoids, and tannins. The data of plant growth, the combined fraction number 2 of AGF bionutrien have positive impact toward the yield productivity with a constant growth rate of 0,1702 week-1 and the yield comes to the highest number, there are 82 pieces of chilies with the heaviest mass of 186,6042 grams. Ethyl acetate plants have constant growth rate 0,1617 week-1 and the yield reaches 24 pieces with the mass of 52,9547 grams.
Key words: Bionurien AGF, Chromatography, Maceration, Liquid Organic
DAFTAR ISI
PERNYATAAN ... i
ABSTRAK ... ii
ABSTRACT ... iii
KATA PENGANTAR ... iv
UCAPAN TERIMA KASIH ... v
DAFTAR ISI ... vi
DAFTAR TABEL ... x
DAFTAR GAMBAR ... xi
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Rumusan Masalah ... 2
1.3 Tujuan Penelitian ... 3
1.4 Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Bionutrien ... 4
2.2 Tinjauan Tanaman AGF ... 7
2.3 Metabolit Sekunder pada Tanaman ... 7
2.3.1 Alkaloid ... 7
2.3.2 Terpenoid ... 8
2.3.3 Tanin ... 9
2.3.4 Flavonoid ... 9
2.4 Laju Pertumbuhan Tanaman ... 10
2.5 Profil Tanaman Cabai Merah Keriting dan Cara Budidayanya di Pot .... 12
2.5.1 Pembibitan atau Penyemaian ... 13
vii
2.5.1.2 Tahap Penyemaian ... 14
2.5.2 Penanaman Cabai di Pot ... 14
2.5.3 Pemeliharaan Tanaman Cabai ... 15
2.5.3.1 Pemupukan ... 15
2.5.3.2 Penyiraman ... 15
2.5.3.3 Pemasangan Ajir ... 16
2.5.3.4 Pewiwilan (Prunning) Tunas Air ... 16
2.5.4 Pengendalian Hama dan Penyakit pada Tanaman Cabai ... 16
2.5.5 Panen Cabai ... 18
2.6 Metode Ekstraksi dan Pemisahan ... 19
2.6.1 Metode Ekstraksi ... 19
2.6.2 Metode Pemisahan ... 19
2.6.2.1 Kromatografi Lapis Tipis (KLT) ... 20
2.6.2.2 Kromatografi Vakum Cair (KVC) ... 20
BAB III METODE PENELITIAN ... 21
3.1 Objek atau Lokasi Penelitan ... 21
3.2 Alat dan Bahan ... 21
3.2.1 Alat ... 21
3.2.2 Bahan ... 22
3.3 Alur Penelitian ... 22
3.3.1 Penyiapan Sampel Serbuk Tanaman AGF ... 24
3.3.2 Ekstraksi Bionutrien AGF dengan Metode Maserasi ... 24
3.3.3 Pemisahan Bionutrien AGF dengan Metode Kromatografi Vakum Cair (KVC) ... 24
3.3.4 Analisis Bionutrien AGF dengan Metode Kromatografi Lapis Tipis (KLT) ... 26
3.3.5 Karakterisasi Bionutrien AGF dengan Skrining Fitokimia dan Spektroskopi FTIR ... 26
3.3.5.2 Karakterisasi Bionutrien AGF dengan Spektroskopi FTIR ... 28
3.3.6 Aplikasi Bionutrien AGF pada Tanaman Cabai Merah Keriting (Capsicum annum L.) ... 28
3.3.6.1 Tahap Persiapan Aplikasi Bionutrien AGF pada Tanaman Cabai Merah Keriting ... 28
3.3.6.2 Tahap Aplikasi Bionutrien AGF pada Tanaman Cabai Merah Keriting ... 30
BAB IV HASIL DAN PEMBAHASAN ... 33
4.1 Penyiapan Sampel Serbuk Tanaman AGF ... 33
4.2 Ekstraksi Serbuk Tanaman AGF dengan Metode Maserasi ... 34
4.3 Fraksinasi Bionutrien AGF dengan Metode Kromatografi Vakum Cair (KVC) ... 35
4.4 Analisis Fraksi Bionutrien AGF dengan Metode Kromatografi Lapis Tipis (KLT) ... 37
4.5 Karakterisasi Konsentrat Etil Asetat Fraksi Gabungan Bionutrien AGF dengan Skrining Fitokimia ... 41
4.6 Karakterisasi Konsentrat Etil Asetat Fraksi Gabungan Bionutrien AGF dengan Metode Spektroskopi Fourier Transform-Infra Red (FTIR) ... 42
4.6.1 Hasil Analisis Spektrum FTIR untuk FG 1 Bionutrien AGF ... 42
4.6.2 Hasil Analisis Spektrum FTIR untuk FG 2 Bionutrien AGF ... 43
4.6.3 Hasil Analisis Spektrum FTIR untuk FG 3 Bionutrien AGF ... 44
4.6.4 Hasil Analisis Spektrum FTIR untuk FG 4 Bionutrien AGF ... 45
4.6.5 Hasil Analisis Spektrum FTIR untuk FG 5 Bionutrien AGF ... 46
4.7 Hubungan antara Hasil Karakterisasi Skrining Fitokimia dengan Spektroskopi FTIR pada Fraksi Gabungan Bionutrien AGF ... 47
4.8 Aplikasi Konsentrat Etil Asetat Bionutrien AGF pada Tanaman Cabai Merah Keriting (Capsicum annum L.) ... 49
ix
4.8.1.1 Pertumbuhan Tinggi pada Tanaman Cabai Merah Keriting
yang diberi Bionutrien AGF ... 50
4.8.1.2 Pertumbuhan Panjang dan Lebar Daun pada Tanaman Cabai Merah Keriting yang diberi Bionutrien AGF ... 54
4.8.1.3 Jumlah Buah dan Massa Buah Cabai Hasil Panen pada Tanaman Cabai Merah Keriting yang Diberi Bionutrien AGF 61 4.8.2 Penentuan Konstanta Laju Pertumbuhan Tanaman Cabai Merah Keriting (Capsicum annum L.) yang Diberi Bionutrien AGF ... 63
4.8.3 Hubungan antara Laju Pertumbuhan Tanaman dengan Hasil Panen Cabai Merah Keriting ... 65
BAB V KESIMPULAN DAN SARAN ... 69
5.1 Kesimpulan ... 69
5.2 Saran ... 69
DAFTAR PUSTAKA ... 70
LAMPIRAN-LAMPIRAN ... 76 RIWAYAT HIDUP
BAB I PENDAHULUAN
1.1 Latar Belakang
Tanaman membutuhkan nutrisi untuk pertumbuhan dan perkembangannya.
Nutrisi yang dibutuhkan tanaman meliputi unsur hara makro dan mikro
(Perwitasari, B., Tripatmasari, M., Wasonowati, C., 2012). Salah satu cara yang
dapat dilakukan untuk memenuhi kebutuhan nutrisi tanaman adalah dengan
penggunaan bionutrien. Bionutrien adalah nutrisi untuk tanaman yang merupakan
suatu pupuk organik cair yang diperoleh dari proses ekstraksi senyawa-senyawa
essensial tanaman tropis yang potensial (Pratama, H.A., 2011). Penggunaan
bionutrien pada tanaman dapat meningkatkan pertumbuhan dan kualitas tanaman
tanpa merusak kesuburan tanah maupun menyebabkan pencemaran tanah dan air
(Nurzaman, H., 2010).
Tanaman yang berpotensi sebagai bionutrien sebagian besar memiliki
kemiripan ciri-ciri tanaman, seperti daun lebat dan berwarna hijau mengkilap,
memiliki bau yang khas, memiliki daya tahan yang cukup tinggi, serta memiliki
kandungan N, P, dan K yang tinggi (Taufik, I., 2011). Sampai saat ini, bionutrien
yang telah ditemukan antara lain berasal dari tanaman AGF, KPD, MHR, CAF,
RPS-GE, BCS, BGI, RSR, JPR, dan ARH.
Salah satu bionutrien yang baru-baru ini dikaji adalah bionutrien dengan
kode AGF. Fadlie, M. (2011) mengekstraksi tanaman AGF dengan pelarut etanol,
etil asetat, diklorometana, dan n-heksana. Hasil menunjukkan bahwa ekstrak AGF
berpotensi sebagai bionutrien karena mengandung kadar NPK yang tinggi. Hasil
dari analisis terhadap ekstrak AGF etanol yaitu kadar nitrogen sebesar 1117 ppm,
kadar fosfor sebesar 835 ppm, dan kadar kalium sebesar 4316,875 ppm (Fadlie,
M., 2011). Ketika bionutrien ekstrak AGF etanol diaplikasikan pada tanaman
cabai merah keriting (Capsicum annum L.) mampu meningkatkan laju
2
Selain itu, hasil analisis terhadap kadar NPK untuk ekstrak AGF etil asetat
yaitu kadar nitrogen sebesar 357 ppm, kadar fosfor sebesar 930 ppm, dan kadar
kalium sebesar 10,255 ppm. Ekstrak AGF etil asetat mampu meningkatkan laju
pertumbuhan tanaman cabai merah keriting sebesar 0,1354 minggu-1 dan
berpotensi sebagai biopestisida karena kelompok tanaman yang diberi ekstrak
AGF etil asetat tidak terserang layu fusarium dan busuk phytophora, serta
menunjukkan massa hasil panen buah cabai sebesar 367,4 gram per tanaman
(Fadlie, M., 2011).
Keberhasilan bionutrien AGF sebagai pupuk organik dan biopestisida
tersebut dianggap memiliki potensi yang sangat baik untuk dikembangkan. Nur,
A.A (2013) memisahkan dan memurnikan ekstrak AGF etil asetat, telah diketahui
bahwa metabolit sekunder yang terkandung dalam fraksi B ekstrak AGF etil asetat
yaitu kariofilena dan squalen yang merupakan senyawa turunan terpen. Oleh
karena itu, perlunya penelitian lanjutan untuk mengetahui golongan metabolit
sekunder dalam fraksi-fraksi lainnya yang memiliki potensi sebagai biopestisida
yang terkandung dalam ekstrak etil asetat bionutrien AGF. Penelitian ini dimulai
dengan mengekstrak tanaman AGF, kemudian pemisahan komponen menjadi
fraksi-fraksi gabungan dengan metode kromatografi vakum cair (KVC). Fraksi
gabungan bionutrien AGF etil asetat tersebut dianalisis dan dikarakterisasi dengan
kromatografi lapis tipis (KLT), skrining fitokimia, dan spektroskopi FTIR.Selain
itu, konsentrat etil asetat fraksi gabungan bionutrien AGF diaplikasikan pada
tanaman cabai merah keriting untuk mengetahui potensinya sebagai bionutrien
pada tanaman cabai merah keriting (Capsicum annum L.).
1.2 Rumusan Masalah
Berdasarkan uraian yang telah dikemukakan di atas, masalah yang akan
diteliti dapat dirumuskan sebagai berikut:
1. Golongan metabolit sekunder apa sajakah yang terkandung dalam ekstrak
etil asetat fraksi gabungan bionutrien AGF berdasarkan KLT, skrining
3
2. Bagaimana potensi konsentrat etil asetat fraksi gabungan bionutrien AGF
terhadap laju pertumbuhan dan hasil panen pada tanaman cabai merah
keriting (Capsicum annum L.)?
1.3 Tujuan Penelitian
Ditinjau dari rumusan masalah di atas, penelitian ini bertujuan untuk
mengetahui:
1. Golongan metabolit sekunder yang terkandung dalam ekstrak etil asetat
fraksi gabungan bionutrien AGF berdasarkan KLT, skrining fitokimia, dan
karakterisasi FTIR.
2. Potensi konsentrat etil asetat fraksi gabungan bionutrien AGF terhadap
laju pertumbuhan dan hasil panen pada tanaman cabai merah keriting
(Capsicum annum L.).
1.4 Manfaat Penelitian
Dengan dilakukannya tahap ekstraksi dan pemisahan, tahap analisis, dan
karakterisasi, serta tahap aplikasi ekstrak etil asetat fraksi gabungan bionutrien
AGF ini, diharapkan penelitian ini dapat:
1. Menjadi rujukan informasi mengenai golongan metabolit sekunder yang
terdapat dalam tanaman AGF, sehingga nantinya dapat meningkatkan
kualitas dan keefektifitasan bionutrien AGF.
2. Memperoleh nutrien alternatif yang ramah lingkungan dan dapat
meningkatkan produktivitas tanaman pertanian khususnya cabai merah
21
BAB III
METODE PENELITIAN
3.1 Objek dan Lokasi Penelitian
Objek atau bahan yang digunakan untuk penelitian ini adalah tanaman
dengan kode AGF yang diperoleh dari daerah Taman Sari Bandung dan
Banyuresmi Garut. Penelitian berlangsung sekitar 8 bulan, terhitung dari Maret
2013 sampai Oktober 2013. Penelitian ini terdiri dari empat tahap utama yaitu
tahap preparasi sampel, tahap ekstraksi dan pemisahan, tahap analisis dan
karakterisasi, serta tahap aplikasi.
Tempat penelitian pada masing-masing tahapan berbeda-beda, antara lain:
Tahap preparasi sampel, ekstraksi, dan analisis dilakukan di Laboratorium Riset
Kimia Lingkungan FPMIPA UPI Bandung, tahap pemisahan dilakukan di
Laboratorium Kimia Organik dan Biokimia FPMIPA UPI Bandung, tahap
karakterisasi dilakukan di Laboratorium Kimia Instrumen FPMIPA UPI Bandung,
sedangkan tahap aplikasi dilakukan di Kebun Riset Kimia Lingkungan FPMIPA
UPI Bandung.
3.2 Alat dan Bahan 3.2.1 Alat
Alat-alat yang digunakan dalam penelitian ini adalah lumpang dan alu,
neraca analitik, gelas kimia 3 L, spatula, batang pengaduk, labu Erlenmeyer
berpenghisap, corong Buchner, kertas saring, botol semprot, pemanas listrik,
magnetic stirrer, set alat destilasi, set alat penguap berputar vakum (vacuum
rotary evaporator), pompa vakum, set alat freeze dryer Eyela FD-5N, botol kaca
1 L, botol pial 100 mL, mikro pipet 5mL, labu erlemeyer 150 mL, gelas ukur 100
mL, staining jar, chamber, set alat kromatografi kolom vakum cair (KVC)
diameter 7 cm, UV box, tabung reaksi, rak tabung, penjepit tabung, ember,
semprotan tanaman, plastik wrap, aluminium foil, penggaris, meteran, pot ukuran
22
takemura soil pH and moisture tester tipe DM-15, spektrofotometer FT-IR
(Fourier Transform-Infra Red) Shimadzu 8400.
3.2.2 Bahan
Pada penelitian ini, bahan utama yang digunakan adalah tanaman AGF
yang telah dibersihkan, dikeringkan, ditumbuk halus, dan diayak sebanyak 1 kg.
Bahan kimia yang digunakan dalam penelitian ini terdiri dari bahan-bahan teknis.
Untuk tahap pemisahan, bahan dengan kualitas teknis didestilasi terlebih
dahulu sebelum digunakan sehingga diperoleh bahan-bahan redestilasi.
Bahan-bahan yang digunakan pada tahap pemisahan adalah etil asetat teknis, n-heksana
teknis, diklorometana teknis, metanol teknis, aquades, aseton, silica gel 60 GF254
for TLC, silica gel 60 230–400 mesh for CC. Pada skrining fitokimia digunakan
pereaksi Mayer, pereaksi Wagner, HCl 1%, larutan FeCl3, Pb asetat 10%,
kloroform, H2SO4 2M. Sedangkan pada tahap aplikasi digunakan air keran, tanah,
pupuk kompos, pupuk phonska, dan pestisida “curacron EC 500”.
3.3 Alur Penelitian
Penelitian ini dibagi menjadi empat tahap utama. Tahap pertama yaitu
tahap preparasi sampel tanaman AGF. Tahap kedua adalah tahap ekstraksi dan
pemisahan dengan menggunakan: Metode Maserasi dan Kromatografi Vakum
Cair (KVC). Selanjutnya tahap ketiga adalah tahap analisis dan karakterisasi
dengan Kromatografi Lapis Tipis (KLT), skrining fitokimia, dan spektroskopi
FTIR. Tahap terakhir adalah aplikasi konsentrat etil asetat fraksi gabungan hasil
dari tahap pemisahan bionutrien AGF pada tanaman cabai merah keriting
(Capsicum annum L.) untuk mengetahui potensinya sebagai bionutrien pada
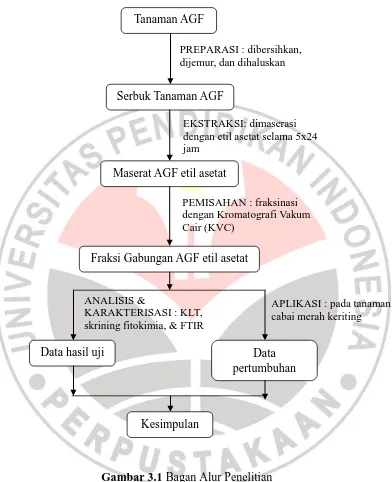
pertumbuhan tanaman cabai merah keriting. Bagan dari alur penelitian secara
23
PREPARASI : dibersihkan, dijemur, dan dihaluskan
Maserat AGF etil asetat
ANALISIS &
KARAKTERISASI : KLT, skrining fitokimia, & FTIR
Data hasil uji Data
pertumbuhan Tanaman AGF
Serbuk Tanaman AGF
EKSTRAKSI: dimaserasi dengan etil asetat selama 5x24 jam
PEMISAHAN : fraksinasi dengan Kromatografi Vakum Cair (KVC)
Fraksi Gabungan AGF etil asetat
APLIKASI : pada tanaman cabai merah keriting
Kesimpulan
24
Uraian dari masing-masing langkah kerja yang dilakukan adalah sebagai berikut:
3.3.1 Penyiapan Sampel Serbuk Tanaman AGF
Sampel tanaman AGF yang akan digunakan dibersihkan terlebih dahulu
dari kotoran seperti tanah dan tanaman parasit lain. Setelah itu dipotong bagian
akarnya dan dijemur di bawah sinar matahari sampai kering. Selanjutnya tanaman
dihaluskan dengan cara ditumbuk dengan lumpang dan alu hingga menjadi
serbuk. Serbuk tanaman AGF kemudian diayak agar serbuk tersebut memiliki
ukuran yang homogen dan halus sebelum dimaserasi.
3.3.2 Ekstraksi Bionutrien AGF dengan Metode Maserasi
Metode yang digunakan untuk mengekstrak AGF adalah dengan metode
maserasi. Metode maserasi merupakan metode ekstraksi cair-padat. Serbuk
tanaman AGF ditimbang sebanyak 1 kg kemudian diekstraksi menggunakan
pelarut etil asetat. Pelarut etil asetat yang digunakan adalah sebanyak 4 liter pada
hari pertama atau hingga seluruh serbuk terendam. Setelah satu hari proses
perendaman, filtrat kemudian disaring menggunakan corong Buchner sehingga
diperoleh ekstrak AGF etil asetat dan residunya. Residu yang dihasilkan
dimaserasi kembali dengan etil asetat sebanyak 3 liter. Kemudian disaring dan
residu yang diperoleh dimaserasi kembali dengan 1 liter etil asetat selama 3 x 24
jam. Filtrat hasil maserasi keseluruhan dipekatkan menjadi 1 liter menggunakan
alat penguap berputar vakum (vacuum rotary evaporator). Ekstrak AGF
kemudian difreeze drying sehingga diperoleh pasta AGF untuk tahapan
pemisahan.
3.3.3 Pemisahan Bionutrien AGF dengan Metode Kromatografi Vakum Cair (KVC)
Tahapan pemisahan dalam penelitian ini dilakukan menggunakan metode
kromatografi vakum cair (KVC). Sebelum dilakukan proses pemisahan dilakukan
terlebih dahulu kromatografi lapis tipis (KLT) untuk menentukan eluen yang
25
Pasta bionutrien AGF yang telah ditentukan eluennya dengan metode
KLT, dilakukan pemisahan dengan metode KVC. Berdasarkan hasil KLT, eluen
untuk memisahkan senyawa dalam pasta bionutrien AGF adalah n-heksana dan
etil asetat dengan perbandingan sebagai berikut; 10:0 sebanyak 2 kali elusi, 8:2
sebanyak 4 kali elusi, 7:3 sebanyak 4 kali elusi, 6:4 sebanyak 3 kali elusi, 3:7
sebanyak 3 kali elusi, dan 0:10 sebanyak 2 kali elusi. Setiap kali elusi, eluen yang
digunakan sebanyak 100 mL. Adapun langkah kerja yang dilakukan adalah
sebagai berikut:
Sebanyak 10 gram pasta dari hasil ekstraksi tanaman AGF diimpregnasi
menggunakan pelarut aseton ke dalam 10 gram silica gel 60 230-400 mesh for
CC. Mula-mula silica gel dimasukkan ke dalam lumpang kemudian sedikit demi
sedikit ditetesi AGF yang telah dilarutkan dalam aseton sambil terus diaduk
menggunakan alu. Didiamkan selama 1 malam agar silica yang diimpregnasi
tersebut kering.
Sebanyak 100 gram silica gel 60 230–400 mesh for CC dimasukkan ke
dalam kolom pada set alat KVC. Silica tersebut dihisap dengan menggunakan
vakum sampai padat dan tidak terdapat rongga dalam silica. Permukaan kolom
diratakan dan dikondisikan agar tidak ada celah dalam kolom. Sebelum sampel
dimasukkkan, permukaan kolom dilapisi kertas saring dan kolom dielusi terlebih
dahulu menggunakan pelarut yang paling non polar (n-heksana) sampai eluat
yang keluar tidak berwarna. Setelah itu, silica gel yang telah diimpregnasi
dimasukkan kedalam kolom kemudian diratakan dan diletakkan kertas saring di
atas permukaan silica impreg. Sampel pada kolom dielusi dengan eluen yang
telah ditentukan. Eluat ditampung dalam botol terpisah sesuai dengan volume
eluen yang digunakan, kemudian diberi label. Pada tahap ini diperoleh beberapa
fraksi yang kemudian akan digabungkan berdasarkan kemiripan pola pemisahan
26
3.3.4 Analisis Bionutrien AGF dengan Metode Kromatografi Lapis Tipis (KLT)
Tahap analisis yang dilakukan adalah dengan metode KLT. Adapun
langkah kerja yang dilakukan adalah sebagai berikut:
Kromatografi lapis tipis digunakan dalam penentuan eluen yang tepat
untuk proses pemisahan (fraksinasi) dengan teknik KVC. Selain itu, KLT juga
digunakan untuk menganalisis senyawa hasil pemisahan dengan KVC telah
terpisah dengan baik atau telah murni.
Dalam pengerjaannya, lempeng tipis dengan adsorben silika gel 60 F254
disiapkan dengan ukuran panjang 5 cm sedangkan lebarnya disesuaikan dengan
jumlah fraksi yang akan ditotolkan. Pada bagian atas dan bawah lempeng diberi
garis batas dengan jarak 0,5 cm dari tepi lempeng. Sampel yang akan dianalisis
ditotolkan pada bagian tengah garis batas bawah dengan menggunakan pipa
kapiler. Lakukan penotolan berulang kali hingga cukup tebal dan dibiarkan
beberapa saat agar kering.
Chamber atau staining jar diisi dengan eluen yang akan digunakan untuk
mengelusi lempeng tipis, dihomogenkan, dan didiamkan beberapa saat dengan
kondisi tertutup agar chamber atau staining jar jenuh dengan uap eluen. Lempeng
tipis yang telah disiapkan sebelumnya, kemudian dimasukkan ke dalam chamber
atau staining jar dengan menggunakan pinset hingga bagian bawah lempeng
tercelup sebagian. Lempeng tipis tersebut diletak tegak bersandar pada dinding
chamber atau staining jar kemudian ditutup.
Apabila eluen yang telah naik hingga mencapai garis batas atas maka
proses KLT dihentikan dengan cara mengangkat lempeng dari chamber atau
staining jar menggunakan pinset. Lempeng kemudian dibiarkan kering di udara
terbuka. Noda pada lempeng diamati di bawah sinar UV.
3.3.5 Karakterisasi Bionutrien AGF dengan Skrining Fitokimia dan Spektroskopi FTIR
27
3.3.5.1 Karakterisasi Bionutrien AGF dengan Skrining Fitokimia
Fraksi gabungan (FG) bionutrien AGF hasil dari tahap pemisahan,
diidentifikasi komponen fitokimianya dengan metode uji warna. Uji fitokimia ini
bertujuan untuk mengetahui kelompok senyawa metabolit sekunder yang
terkandung di dalam FG bionutrien AGF. Skrining fitokimia ini dilakukan
terhadap metabolit sekunder golongan alkaloid, tanin, flavonoid, dan terpenoid.
Adapun prosedur kerja yang dilakukan adalah sebagai berikut:
A. Identifikasi Alkaloid
Sebanyak 3 mL konsentrat etil asetat FG bionutrien AGF dimasukkan
masing-masing ke dalam tabung reaksi A dan B. Kemudian dicampurkan
dengan 3 mL HCl 1 % di dalam steam bath. Tabung reaksi A ditambahkan
pereaksi Mayer dan tabung rekasi B ditambahkan pereaksi Wagner.
Terbentuknya endapan putih mengindikasikan adanya alkaloid (Kavit
Mehta, B.N. Patel, B.K. Jain, 2013).
Pembuatan Pereaksi Mayer
Sebanyak 1 gram KI dilarutkan dalam 20 mL aquades. Kemudian
ditambahkan 0,2 gram HgCl2 dan diaduk hingga larut (Fadlie M., 2011).
Pembuatan Pereaksi Wagner
Sebanyak 2,5 gram I2 dan 2 gram KI dimasukkan ke dalam 10 mL
aquades. Kemudian dilarutkan dan diencerkan dengan aquades hingga
mencapai volume 200 mL ( Diana K.M., Pringgenies D., Karna O.R.,
2012)
B. Identifikasi Tanin
Sebanyak 2 mL konsentrat dicampurkan dengan 2 mL aquades. Campuran
tersebut ditambahkan sedikit larutan FeCl3. Terbentuknya endapan hijau
28
C. Identifikasi Flavonoid
Sebanyak 1 mL Pb asetat 10% ditambahkan ke dalam 1 mL konsentrat lalu
dikocok. Timbulnya endapan kuning mengindikasikan konsentrat positif
mengandung flavonoid (Kavit Mehta, et.al., 2013).
D. Identifikasi Terpenoid
Ke dalam 2 mL konsentrat ditambahkan 2 mL kloroform dan dievaporasi
hingga kering. Setelah itu, ditambahkan 2 mL H2SO4 2M dan dipanaskan
kembali selama 2 menit. Terbentuknya warna keabu-abuan menunjukkan
adanya terpenoid (Kavit Mehta, et.al., 2013).
3.3.5.2 Karakterisasi Bionutrien AGF dengan Spektroskopi FTIR
FG bionutrien AGF dikarakterisasi dengan spektrofotometer FTIR untuk
mengetahui gugus fungsi yang kemungkinan ada dalam senyawa yang terdapat
pada FG bionutrien AGF. Alat spektroskopi FTIR yang digunakan adalah FT-IR
Shimadzu 8400.
3.3.6 Aplikasi Bionutrien AGF pada Tanaman Cabai Merah Keriting (Capsicum annum L.)
Pada tahap aplikasi digunakan konsentrat etil asetat FG bionutrien AGF.
Aplikasi ini dilakukan untuk mengetahui potensi FG bionutrien AGF pada
tanaman pertanian khususnya cabai merah keriting (Capsicum annum L.) di
lapangan. Tahap aplikasi ini dilakukan di Kebun Riset Kimia Lingkungan
FPMIPA UPI.
3.3.6.1 Tahap Persiapan Aplikasi Bionutrien AGF pada Tanaman Cabai Merah Keriting
Budidaya cabai merah keriting dimulai dari tahapan persiapan benih
hingga penanaman. Tahap persiapan benih cabai merah keriting untuk aplikasi
29
cabai yang memiliki kualitas baik. Penyortiran biji cabai tersebut dilakukan
dengan cara merendam biji cabai di dalam air selama 1 malam. Biji yang
digunakan adalah biji yang tenggelam karena mengindikasikan kualitas biji yang
baik. Setelah itu, biji cabai diperam terlebih dahulu agar lebih cepat berkecambah
dan nantinya saat proses penyemaian hanya akan diambil benih cabai yang telah
berkecambah saja.
Gambar 3.2. Biji Cabai Merah Keriting Pada Tahap Penyortiran dan Pemeraman
Setelah tahap penyortiran dan pemeraman, tahap selanjutnya adalah
penyemaian. Akan tetapi, sebelumnya dipersiapkan terlebih dahulu media yang
akan digunakan untuk persemaian. Media yang digunakan adalah tanah dan
kompos dengan perbandingan 2:1. Media tanam tersebut dimasukkan ke dalam
botol bekas air mineral 1L yang telah dipotong dengan tinggi ± 12 cm. Kemudian
benih cabai yang telah berkecambah dimasukkan ke dalam media tanam tersebut.
Gambar 3.3 Media Semai dan Tahap Penyemaian Cabai Merah Keriting
Biji cabai merah keriting
Penyortiran biji cabai merah keriting
Pemeraman biji cabai merah keriting Biji yang
tenggelam
Biji yang terapung
30
3.3.6.2 Tahap Aplikasi Bionutrien AGF pada Tanaman Cabai Merah Keriting
Pada tahap aplikasi ini dibuat pengelompokkan tanaman yang
masing-masing terdiri dari lima tanaman. Pengelompokkan tanaman tersebut adalah
sebagai berikut:
1. Tanaman yang diberi FG 1 bionutrien AGF diberi kode 1A, 1B, 1C, 1D, 1E.
2. Tanaman yang diberi FG 2 bionutrien AGF diberi kode 2A, 2B, 2C, 2D, 2E.
3. Tanaman yang diberi FG 3 bionutrien AGF diberi kode 3A, 3B, 3C, 3D, 3E.
4. Tanaman yang diberi FG 4 bionutrien AGF diberi kode 4A, 4B, 4C, 4D, 4E.
5. Tanaman yang diberi FG 5 bionutrien AGF diberi kode 5A, 5B, 5C, 5D, 5E.
Untuk mengetahui pengaruh pelarut yang digunakan maka dilakukan
perlakuan pada kelompok tanaman yang diberi blanko etil asetat dengan kode
ET1, ET2, ET3, ET4, ET5. Sedangkan untuk mengetahui pola pertumbuhan
tanaman yang diberikan perlakuan seperti oleh petani maka dilakukan perlakuan
pada kelompok tanaman yang diberi pupuk phonska dan pestisida “curacron EC
500” dengan kode K1, K2, K3, K4, K5. Setiap kelompok tanaman mendapatkan perlakuan yang berbeda ditampilkan pada tabel 3.1.
Tabel 3.1 Pembagian Kelompok Tanaman dan Perlakuan yang Diberikan Kelompok
tanaman Perlakuan Phonska Pestisida Bionutrien
I FG 1 Bionutrien AGF X X √
II FG 2 Bionutrien AGF X X √
III FG 3 Bionutrien AGF X X √
IV FG 4 Bionutrien AGF X X √
V FG 5 Bionutrien AGF X X √
VI Blanko Etil Asetat (ET) X X X
VII Kontrol Positif (K) √ √ X
31
Tanaman yang diberi perlakuan dengan bionutrien AGF dan blanko etil
asetat tidak diberi pestisida untuk melihat ketahanan tanaman terhadap penyakit
dan hama. Berikut ini adalah konsentrat etil asetat FG bionutrien AGF dan blanko
etil asetat yang akan digunakan untuk aplikasi:
Gambar 3.4 Bionutrien AGF dan Blanko Etil Asetat yang akan
Digunakan untuk Aplikasi
Tanaman cabai merah keriting mulai diberikan perlakuan saat dalam tahap
penyemaian yaitu ketika umur cabai 26 hari setelah tanam (HST) atau pada
minggu pertama pengamatan dengan dosis 2 mL/L air. Pemberian dosis yang
rendah ini dipertimbangkan dari umur tanaman yang masih muda. Akan tetapi,
pemberian bionutrien AGF tetap dilakukan untuk menjaga bibit tanaman dari
serangan penyakit dan hama. Hal tersebut berdasarkan penelitian yang telah
dilakukan oleh M.Fadlie (2011) yang menyatakan bahwa ekstrak AGF etil asetat
berpotensi sebagai biopestisida. Setelah tanaman cabai merah keriting mencapai
umur 54 HST, diberikan perlakuan dengan dosis 10 mL/L air. Hal ini
dimaksudkan agar kondisi tanaman cabai sudah kuat setelah dipindahkan dari
tempat pembibitan ke dalam pot sehingga siap menerima perlakuan uji dengan
dosis yang sesuai.
Gambar 3.5 Tanaman Cabai Merah Keriting saat Berumur 26 HST dan 54 HST
Tanaman cabai merah keriting berumur 26 HST
32
Pemupukan pada tanaman dilakukan dengan selang waktu satu minggu
sekali dengan cara disemprot dan disiram. Adapun parameter pertumbuhan
vegetatif yang diamati adalah:
1. Tinggi tanaman (cm), diukur dari pangkal akar hingga pangkal pucuk daun
paling atas.
2. Lebar daun (cm), diukur dari sisi daun ke sisi daun lainnya.
3. Panjang daun (cm), diukur dari ujung daun sampai ke pangkal daun.
4. Jumlah buah cabai (buah), dihitung dari mulai cabai yang memiliki panjang
± 2 cm.
5. Bobot cabai (gram) yang dihasilkan setelah panen.
Selain itu, dilakukan pengamatan terhadap hama dan penyakit yang menyerang
tanaman cabai merah keriting. Pengamatan dilakukan dari satu minggu sebelum
diberikan perlakuan dan terus dilakukan hingga panen. Adapun layout penanaman
cabai merah keriting di pot untuk aplikasi tersebut tergambar dalam skema berikut
:
50 cm
30 cm
30 cm
30 cm
30 cm
69
BAB V
KESIMPULAN DAN SARAN
5.1Kesimpulan
Berdasarkan penelitian dan pembahasan yang telah dilakukan, maka dapat
dapat ditarik kesimpulan sebagai berikut:
1. Hasil analisis dan karakterisasi dengan KLT, skrining fitokimia, dan
spektroskopi IR menunjukkan bahwa FG 1 bionutrien AGF mengandung
metabolit sekunder golongan alkaloid dan terpenoid. FG 2 sampai 4
bionutrien AGF didominasi oleh golongan alkaloid, flavonoid, dan terpenoid.
FG 5 bionutrien AGF mengandung golongan alkaloid, tanin, dan terpenoid.
2. Data aplikasi bionutrien AGF pada tanaman cabai merah keriting
menunjukkan bahwa kelompok tanaman FG 2 bionutrien AGF memiliki
konstanta laju pertumbuhan tertinggi yaitu 0,1702 minggu-1 dengan jumlah
buah cabai terbanyak yaitu 82 buah dan massa buah terberat yaitu 186,6042
gram.
3. FG 2 bionutrien AGF selain dapat digunakan sebagai pupuk organik cair juga
berpotensi sebagai biopestisida.
5.2 Saran
Untuk pemanfaatan bionutrien AGF lebih lanjut disarankan beberapa hal
sebagai berikut:
1. Sebaiknya dilakukan tahap pemisahan pada FG 2 bionutrien AGF untuk
mengetahui senyawa yang berperan sebagai biopestisida dan senyawa yang
dapat meningkatkan kepedasan cabai.
2. Setelah dilakukan uji organoleptik, perlu dilakukan penentuan kadar capsaicin
70
DAFTAR PUSTAKA
Alan, H.D. (2007). Forage Growth and Its Relationship to Grazing Management.
Lafayette: Departement of Renewable Source, University of Southwestern
Lousiana.
Ambarwati, R. (2007). Ekstraksi Bionutrien dari tanaman MHR dan Aplikasinya
pada tanaman caisin. Program Studi Kimia Jurusan Pendidikan Kimia
FPMIPA UPI, Bandung: Tidak Diterbitkan.
Arora, R., Gill, N. S., Chauhan, G., Rana, A.C. (2011). An Overview about
Versatile Molecule Capsaicin. International Journal of Pharmaceutical
Sciences and Drug Research 3(4), Halaman 280-286.
Asih, N.A., Purwanto I.H., Wahyudi A. (2001). Cabai Hot Beauty. Jakarta: PT.
Penebar Swadaya.
BPTP Lampung. (2008). Teknologi Budidaya Cabai Merah. Bogor: Agro Inovasi.
Castellan, G. W. (1983). Physical Chemistry. New York: Addison-Wesley
Publishing Company, Inc.
Chen, Jen-Hshuan. (2006). The Combined Use of Chemical and Organic
Fertilizers and/or Biofertilizer for Crop Growth and Soil Fertility. Taiwan:
Department of Soil and Environmental Sciences, National Chung Hsing
University
Clark, Jim. (2007). Kromatografi Lapis Tipis. [Online]. Tersedia: http://
www.chem.try.org/materi/instrumen_analisis/kromatografi
71
Coll, J., Bowden, B. (1986). The Application of Vacuum Liquid Chromatography
to the Separation of Terpene Mixtures. Journal of Natural Products, 49
(5), pp 934-936.
Dewi, S.M., Suryanti. V., Suyono. (2005). Skrining Fitokimia dan Analisis
Kromatografi Lapis Tipis Komponen Kimia Buah Labu Siam (Sechium
edule Jacq. Swartz.) dalam Ekstrak Etanol. Surakarta: Jurnal Biofarmasi
3 (1): 26-31 edisi Februari 2005.
Diana, K.M., Pringgenies, D., Karna, O.R. (2012). Uji Fitokimia dan Toksisitas
Ekstrak Kasar Gastropa (Telescopium telescopium) terhadap Larva
Artemia salina. Semarang: Journal Of Marine Research. Volume 1,
Nomor 2, Tahun 2012, Halaman 58-66.
Fadlie, M. (2011) Kajian Potensi Ekstrak Tumbuhan dengan Kode AGF sebagai
Bionutrien yang Diaplikasikan pada Tanaman Cabai Merah Keriting
(Capcisum Annum L.). Skripsi. Program Studi Kimia Jurusan Pendidikan
Kimia FPMIPA UPI, Bandung: Tidak Diterbitkan.
Harborne, J.B., (1987). Metode Fitokimia: Penemuan Cara Modern
Menganalisis Tumbuhan. Terjemahan K. Padmawinata dan I. Soediro,
Bandung: Penerbit ITB.
Hayati, E.K, dkk. (2010). Fraksinasi dan Identifikasi Senyawa Tanin pada Daun
Belimbing Wuluh (Averrhoa Bilimbi L.). Jurnal Kimia Volume 4, Nomor
2, Juni 2010: 193-200.
Herbert, R.B. (1995). Biosynthesis of Secondary Metabolites, Eecond edition.
New York: Chapman and Hall.
Hostettmann, K., Hostettmann, M., Marston, A. (1995). Cara Kromatografi
Preparatif, Penggunaan Pada Isolasi Senyawa Alam. Bandung: Institut
72
Indrakusuma. (2000). Pupuk Organik Cair Supra Alam Lestari. Yogyakarta: PT.
Surya Pratama Alam.
Juliana, V. (2010) Isolasi dan Karakterisasi Senyawa Turunan Terpenoid dari
Fraksi n-Heksan Momordica charantia L. Skripsi. Program Studi Kimia
Jurusan Pendidikan Kimia FPMIPA UPI, Bandung: Tidak Diterbitkan.
Juliastuti, D. (2007). Pembuatan Bionutrien KPD dan Aplikasinya pada Tanaman
Caisin (Brassica juncea). Skripsi. Program Studi Kimia Jurusan
Pendidikan Kimia FPMIPA UPI, Bandung: Tidak Diterbitkan.
Kavit, Mehta., B.N. Patel, B.K. Jain. (2013). Phytochemical Analysis of Leaf
Extract of Phyllanthus fraternus. Research Journal of Recent Science
Volume 2, 7 Februari 2013.
Khopkar, S.M. (2003). Konsep Dasar Kimia Analitik. Jakarta: Universitas
Indonesia.
Kistinnah, I., Sri, E.L. (2009). Biologi, Makhluk Hidup dan Lingkungannya.
Jakarta: Pusat Perbukuan Departemen Pendidikan Nasional.
Kurniasih, E. (2009). Kajian Tentang Potensi Tanaman RSP-GE Sebagai Bahan
Dasar Pembuatan Bionutrien yang Diaplikasikan pada Tanaman Pakcoy
(Brassica rapa). Skripsi. Program Studi Kimia Jurusan Pendidikan Kimia
FPMIPA UPI, Bandung: Tidak Diterbitkan.
Lakitan., B. (2010). Dasar-Dasar Fisiologi Tumbuhan. Jakarta: Rajawali Pers.
Lee, J. S., H. J. Lee, S. H. Lee. (2002). Decomposition and 15 N Fate of Rice
Straw in Pody Soil. Korean Journal Crop Science.
Lenny, S. (2006). Senyawa Flavonoid, Fenil Propanoid, dan Alkaloid. Karya
73
Lenny, S. (2006). Senyawa Terpenoida dan Steroida. Karya Ilmiah pada
Departemen Kimia FMIPA Universitas Sumatera Utara.
Lourdes, M., Edith, G., Erika, V.T. (2011). Chemical and Pharmacological
Aspects of Capsaicin. Journal Molecules 16, 1253-1270.
Novi, Kristanti, A., dkk., (2008). Fitokimia. Surabaya : Airlangga University
Press.
Nur, Atthariq. A. (2013) . Isolasi dan Identifikasi Senyawa Metabolit Sekunder
dalam Bionutrien AGF. Skripsi. Program Studi Kimia Jurusan Pendidikan
Kimia FPMIPA UPI, Bandung: Tidak Diterbitkan.
Nur, R.F. (2011) Kajian Potensi Tanaman RSR sebagai Bahan Dasar Bionutrien
yang Diaplikasikan pada Tanaman Cabai Merah Keriting (Capcisum
Annum L.). Skripsi. Program Studi Kimia Jurusan Pendidikan Kimia
FPMIPA UPI, Bandung: Tidak Diterbitkan.
Nurul, R.L., Winarsih, Sri, R.L. (2012). Pemanfaatan Sampah Organik sebagai
Bahan Pupuk Cair untuk Pertumbuhan Tanaman Bayam Merah
(Alternanthera ficoides). LenteraBio Vol. 1 No. 3 September 2012:139–
144, Jurusan Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam
Universitas Negeri Surabaya.
Nurzaman, H. (2010). Kajian Tentang Potensi Dual Bionutrien CAF dan MHR
yang Diaplikasikan pada Tanaman Kentang (Solanum tuberosum L.).
Skripsi Sarjana pada Program Studi Kimia Jurusan Pendidikan Kimia
FPMIPA UPI Bandung : tidak diterbitkan.
Oktaviani, Maulida. (2011). Penggunaan Metode Freezing (-4oC) dengan
74
1803] Bornet Et Flahault 1886. Skripsi. Departemen Biologi FMIPA UI,
Depok. Tidak diterbitkan.
Pandiangan, Dingse. (2009). Produksi Metabolit Sekunder Alkaloid Secara In
Vitro. Bandung: Unpad Pess.
Perwitasari B., Tripatmasari M., Wasonowati C. (2012). Pengaruh Media Tanam
dan Nutrisi Terhadap Pertumbuhan dan Hasil Tanaman Pakchoi
(Brassica juncea L.) dengan Sistem Hidroponik. Jurnal Agrovigor Volume
5, Nomor 1, Maret 2012.
Pelczar, Michael. (2005). Dasar-Dasar Mikrobiologi. UI-Press : Jakarta.
Prajnanta, F. (2010). 38 Kiat Sukses Bertanam Cabai di Musim Hujan. Depok;
Penebar Swadaya.
Pratama, H.A. (2011). Kajian Potensi Bionutrien Hasil Ekstraksi Tanaman ARH
dengan Variasi Tingkat Kepolaran Pelarut dan Aplikasinya pada Cabai
Merah Keriting (Capsicum annum L). Skripsi. Program Studi Kimia
Jurusan Pendidikan Kimia FPMIPA UPI Bandung: tidak diterbitkan.
Prihmantoro, H. (1996). Memupuk Tanaman Buah. Cetakan I. Jakarta: Penebar
Swadaya.
Priyadi, Sukendro, S. (2011). Memulai Usaha Si Pedas Cabai Rawit di Lahan
dan Pot. Yogyakarta: Cahaya Atma Pustaka.
Samadi, B. (2007). Budidaya Cabai Merah Secara Komersial. Yogyakarta:
Yayasan Pustaka Nusatama.
Sastradiharja, S., Firmanto, B.H. (2011). Praktis Bertanam Cabai Merah Keriting
Organik dalam Polybag. Bandung: Angkasa Press.
Sempurna, F. I. (2008). Kajian Potensi Tanaman CAF sebagai Bionutrien untuk
75
(Solanum tuberosum). Skripsi. Program Studi Kimia Jurusan Pendidikan
Kimia FPMIPA UPI, Bandung: Tidak Diterbitkan.
Simanungkalit, R.D.M dan R. Saraswati. (2006). Pupuk Organik dan Pupuk
Hayati. Bandung: Balai Besar Penelitian dan Pengembangan Sumberdaya
Lahan Pertanian.
Stoenoiu, C.E., Bolboaca, A.D., Jantschi, L. (2006). Mobile Phase Optimization
for Steroid Separation. Medinformatics.
Sutanto, Rachman. (2005) . Dasar-Dasar Ilmu Tanah, Konsep dan Kenyataan.
Yogyakarta: Kanisius.
Taufik, I. (2011). Kajian Potensi Tumbuhan BDI sebagai Bionutrien untuk
Pertumbuhan dan Perkembangan Tanaman Cabai Merah Keriting
(Capcisum Annum var. Longum). Skripsi. Program Studi Kimia Jurusan
Pendidikan Kimia FPMIPA UPI, Bandung: Tidak Diterbitkan.
Wahyudi dan Topan, M. (2011). Panen Cabai di Pekarangan Rumah. Cetakan
Pertama. Jakarta: Agro Media Pustaka.
Widodo, N. (2007). Isolasi dan Karakterisasi Senyawa Alkaloid yang Terkandung
dalam Jamur Tiram Putih (Pleurotus ostreatus). Skripsi. FMIPA
Universitas Negeri Semarang, Semarang.
Yulipriyanto, H. (2010). Biologi Tanah dan Strategi Pengelolaannya. Yogyakarta:
Graha Ilmu.
Zainaldi, A. (2011). Kajian Tentang Potensi Maserat Tumbuhan ISM sebagai
Bionutrien dan Aplikasinya dalam Budidaya Tanaman Cabai Merah
Keriting (Capcisum Annum var. Longum). Skripsi. Program Studi Kimia