This post was republished to MA NURUL JADID PAITON at 9:08:48 AM 7/5/2021
KIMIA-X-IPA
1 Suatu zat padat dilarutkan dalam air, ternyata larutannya dapat menghantarkan arus listrik.
Pernyataan yang tepat untuk menerangkan peristiwa ini adalah ….
A Dalam air zat padat itu terurai menjadi ion-ion B Dalam air zat padat itu terurai menjadi atom-atom C Dalam air zat padat itu terurai menjadi molekul-molekul
D Air menjadi mudah terionisasi bila ada zat yang terlarut didalamnya E Air menjadi konduktor listrik bila ada zat yang terlarut didalamnya 2 Larutan di bawah ini yag mempunyai daya hantar listrik paling baik adalah ....
A Asam cuka B Alkohol C Asam sulfat D Minyak tanah E Gula
3 Data pengamatan daya hantar listrik beberapa larutan dalam air sebagai berikut:
Larutan Lampu
menyala
Pengamatan lain
P - Ada gelembung
gas
Q Terang Ada gelembung
gas
R - Ada gelembung
gas
S Terang Ada gelembung
gas
T - -
U - -
V Terang Ada gelembung
gas
W - Ada gelembung
gas Yang tergolong elektrolit lemah adalah larutan ….
A P,Q,dan R B R,S, dan T C P,R,dan T D U,V, dan W E P,R, dan W
4 Beberapa larutan di bawah ini:
A. H2SO4 0,1 M D. C6H12O6 0,1 M B. CCl4 0,1 M E. CO(NH2)2 0,1 M
C. HCl 0,1 M
Yang menimbulkan nyala terang pada lampu adalah ….
A A dan B B A dan C C B dan C D C dan D E D dan E
5 Perhatikan persamaan reaksi berikut:
Senyawa gas karbondioksida (CO) pada persamaan reaksi tersebut mengalami oksidasi karena ….
A Jumlah elektronnya bertambah B Jumlah oksigennya berkurang C Jumlah hidrogennya berkurang D Jumlah elektronnya berkurang E Jumlah oksigennya bertambah
6 Perhatikan beberapa persamaan reaksi redoks berikut!
Persamaan reaksi redoks yang mengalami kenaikan bilangan oksidasi adalah ….
A (1) B (2) C (3) D (4) E (5)
7 Perhatikan beberapa senyawa crom berikut!
1) Cr2O3 2) Na2CrO4 3) CrO 4) CrO3 5) Na2Cr2O7
Bilangan oksidasi Cr terkecil terdapat pada senyawa ....
A (1) B (2) C (3) D (4) E (5)
8 Besi banyak digunakan untuk pagar rumah atau konstruksi banginan. Jika tidak dicat akan cepat berkarat. Proses perkaratan besi dengan oksigen sehingga menghasilkan karat, dengan reaksi
4Fe(s) + 3O2(g) + 6H2O(l) → 2Fe2O3. 3H2O Yang sebenarnya terjadi adalah ….
A Besi sebagai oksidator B Air sebagai oksidator C Oksigen mengoksidasi besi D Besi mengalami reduksi E Besi menerima elektron
9 Reaksi berikut yang termasuk reaksi oksidasi adalah ….
A 2K + O2 → 2 K2O B 2Na2O2 → 2 Na2O + O2
C 2NiO + C → 2 Ni + CO2 D 2AgO → 2Ag + O2
E Ag → Ag+ + e-
10 Semua reaksi berikut merupakan reaksi redoks, kecuali ….
A Kayu dibakar menjadi arang
B Asam klorida dengan natrium hidroksida menjadi garam dapur C Logam dengan asam menghasilkan gas hidrogen
D Besi dan oksigen menjadi karat besi
E Karbon dengan oksigen menjadi gas karbon dioksida
11 Pernyataan yang benar tentang reaksi oksidasi reduksi adalah...
A Reduksi adalah reaksi peningkatan bilangan oksidasi B Oksidasi adalah reaksi penurunan bilangan oksidasi C Oksidasi adalah peristiwa penangkapan elektron
D Reaksi redoks ditandai dengan peningkatan dan penurunan bilangan oksidasi E Zat yang mengalami oksidasi maka dikatakan melepas oksigen
12 Berikut adalah rumus nitrogen dalam berbagai unsur maupun senyawa.
N2 → NO → NO2-
→ NO3-
Urutan bilangan oksidasi N dari N2 adalah ….
A 0, +2, +3, +5 B 0, +2, +4, +5 C 0, +3, +4, +5 D -3, 0, +1, +3 E -3, +1, +2, +3
13 Reaksi yang menunjukkan perubahan bilangan oksidasi adalah ….
A NaOH + CH3COOH → CH3COONa + H2O B AgNO3 + NaCl → AgCl + NaNO3
C Hg(NO3)2 + Sn → Hg + Sn(NO3)2 D OH- + Al(OH)3 → AlO2-
+ 2 H2O E HCl + NaOH → NaCl + H2O
14 Cangkang kerang merupakan sumber bahan pembentuk gunung kapur, yaitu senyawa kalsium karbonat (CaCO3). Bilangan oksidasi karbon dalam senyawa tersebut adalah ….
A +1 B +2
C +3 D +4 E +5
15 Berdasarkan reaksi berikut 2KI + Cl2 → I2 + 2KCl, pernyataan yang tepat adalah ….
A Bilangan oksidasi I berubah dari 0 menjadi -1 B Bilangan oksidasi I berubah dari -1 menjadi 0 C Bilangan oksidasi K berubah dari -1 menjadi -2 D Bilangan oksidasi Cl berubah dari -1 menjadi 0 E Bilangan oksidasi Cl berubah dari -1 menjadi +1 16 Unsur logam yang memiliki biloks +5 terdapat pada ion ….
A PO33-
B MnO4- C SbO43-
D CrO42- E Cr2O72-
17 Besarnya penurunan bilangan oksidasi bromin pada reaksi reduksi BrO3- menjadi Br- adalah
….
A 2 B 3 C 4 D 5 E 6
18 Di antara reaksi berikut, yang tergolong bukan reaksi redoks adalah ….
A SnCl2 + 2HgCl2 → SnCl4 + Hg2Cl2 B CaCO3 + 2HCl → CaCl2 + H2O + CO2
C 2FeCl3 + H2S → 2FeCl2 + 2HCl + S D Zn + 2HCl → ZnCl2 + H2
E 2S + 2O2 → 2SO3
19 Bilangan oksidasi unsur Cr dalam K2Cr2O7 sama dengan bilangan oksidasi unsur Mn dalam
….
A MnO B MnO2
C MnSO4 D KMnO4
E K2MnO4
20 Pada persamaan reaksi MnO2 + 2H2SO4 + 2NaI → MnSO4 + Na2SO4 + 2H2O + I2 zat yang berperan sebagai pengoksidasi adalah ….
A NaI B MnO2 C H2SO4
D MnSO4 E Na2SO4
21 Senyawa yang berperan sebagai oksidator pada reaksi:
2KMnO4(aq) + 16HCl(aq) → 2MnCl2(aq) + 2KCl(aq) + 5Cl2(g) + 8H2O(l) adalah ….
A HCl karena mengoksidasi unsur Mn dalam KMnO4 menjadi Mn dalam MnCl2
B HCl karena klor mengalami penurunan bilangan oksidasi
C KMnO4 karena mangan mengalami peningkatan bilangan oksidasi D KMnO4 karena mengoksidasi ion Cl- dalam HCl menjadi Cl2 E KMnO4 dan HCl karena sama-sama bereaksi membentuk MnCl2
22 Beberapa reaksi sebagai berikut:
1. Zn + HCl → ZnCl2 + H2
2. 2 H2 + O2 → 2 H2O 3. H2 + 2 Na → 2 NaH 4. 2 H2O2 → 2 H2O + O2
Hidrogen yang mengalami oksidasi, reduksi dan tidak mengalami perubahan bilangan oksidasi secara berturut-turut adalah ….
A 1, 2, dan 4 B 1, 3, dan 4 C 2, 1, dan 4 D 3, 1, dan 4 E 3, 2, dan 4
23 Dengan melihat perubahannya, zat-zat berikut yang tidak dapat bertindak sebagai oksidator adalah ….
A Cl- → ClO2-
B ClO3- → Cl2 C SO42-
→ SO2
D CrO72- → Cr3+
E MnO4-
→ Mn2+
24 Perhatikan beberapa senyawa belerang berikut!
1. SO42-
2. SO32-
3. SO22- 4. S2O62- 5. S2O32-
Bilangan oksidasi S terbesar terdapat dalam senyawa ...
A (1) B (2) C (3) D (4) E (5)
25 Rumus kimia dari timah(II) sulfat adalah ….
A Sn(SO4)2
B SnSO4 C Sn2SO4 D SnS2
E SnS
26 Penamaan senyawa berikut yang tidak benar adalah ….
A MgCl2 = magnesium diklorida B Hg2Cl2 = raksa(I) klorida
C Na2SO4 = natrium sulfat D Na2O = natrium oksida E BCl3 = boron triklorida
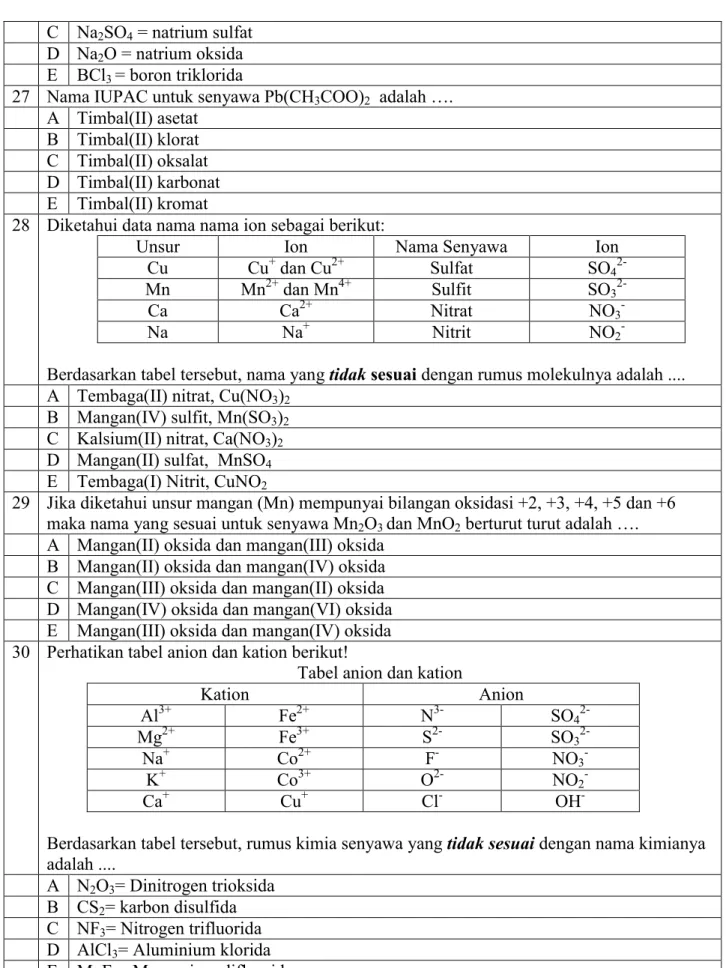
27 Nama IUPAC untuk senyawa Pb(CH3COO)2 adalah ….
A Timbal(II) asetat B Timbal(II) klorat C Timbal(II) oksalat D Timbal(II) karbonat E Timbal(II) kromat
28 Diketahui data nama nama ion sebagai berikut:
Unsur Ion Nama Senyawa Ion
Cu Cu+ dan Cu2+ Sulfat SO42-
Mn Mn2+ dan Mn4+ Sulfit SO32-
Ca Ca2+ Nitrat NO3-
Na Na+ Nitrit NO2-
Berdasarkan tabel tersebut, nama yang tidak sesuai dengan rumus molekulnya adalah ....
A Tembaga(II) nitrat, Cu(NO3)2 B Mangan(IV) sulfit, Mn(SO3)2
C Kalsium(II) nitrat, Ca(NO3)2 D Mangan(II) sulfat, MnSO4
E Tembaga(I) Nitrit, CuNO2
29 Jika diketahui unsur mangan (Mn) mempunyai bilangan oksidasi +2, +3, +4, +5 dan +6 maka nama yang sesuai untuk senyawa Mn2O3 dan MnO2 berturut turut adalah ….
A Mangan(II) oksida dan mangan(III) oksida B Mangan(II) oksida dan mangan(IV) oksida C Mangan(III) oksida dan mangan(II) oksida D Mangan(IV) oksida dan mangan(VI) oksida E Mangan(III) oksida dan mangan(IV) oksida 30 Perhatikan tabel anion dan kation berikut!
Tabel anion dan kation
Kation Anion
Al3+ Fe2+ N3- SO42-
Mg2+ Fe3+ S2- SO32-
Na+ Co2+ F- NO3-
K+ Co3+ O2- NO2-
Ca+ Cu+ Cl- OH-
Berdasarkan tabel tersebut, rumus kimia senyawa yang tidak sesuai dengan nama kimianya adalah ....
A N2O3= Dinitrogen trioksida B CS2= karbon disulfida C NF3= Nitrogen trifluorida D AlCl3= Aluminium klorida E MgF2= Magnesium difluorida
31 Jika diketahui nomor atom 15P, 8O, 7N dan 9F, maka nama senyawa P2O5 dan NF5 adalah .…
A Difosfor pentaoksida dan nitrogen(III) fluorida B Difosfor pentaoksida dan nitrogen pentafluorida C Fosfor(II) pentaoksida dan nitrogen(III) fluoride D Fosfor(IV) pentaoksida dan nitrogen tetrafluorida E Fosfor(IV) pentaoksida dan nitrogen(III) fluorida 32 Perhatikan tabel anion dan kation berikut!
Tabel anion dan kation
Kation Anion
Al3+ Fe2+ N3- SO42-
Mg2+ Fe3+ S2- SO32-
Na+ Co2+ F- NO3-
K+ Co3+ O2- NO2-
Ca+ Cu2+ Cl- OH-
Rumus molekul dari kobalti sulfat dan ferro nitrit berturut-turut adalah ….
A CoSO4 dan Fe(NO2)3 B Co2(SO4)3 dan Fe(NO3)2
C Co3(SO4)2 dan Fe(NO3)2 D CoSO4 dan Fe(NO2)2
E Co2(SO4)3 dan Fe(NO2)2
33 Salah satu senyawa yang digunakan dalam pembuatan sel baterai adalah NH4Cl. Senyawa tersebut dapat dibuat melalui reaksi: (NH4)2SO4 + 2NaCl → Na2SO4 + 2NH4Cl
Nama senyawa NH4Cl tersebut adalah ….
A Ammonium sulfat B Natrium klorida C Ammonium karbonat D Natrium sulfat E Ammonium klorida
34 Perhatikan persamaan reaksi berikut:
a Fe2O3 + b CO cFe + d CO2 Persamaan reaksi setara jika a, b, c dan d berturut-turut adalah ....
A 2, 3, 1, 3 B 1, 3, 2, 3 C 1, 2, 3, 1 D 3, 2, 1, 3 E 1, 2, 3, 1
35 Jika tetapan Avogadro = L dan massa molar gas ammonia maka dalam 10 gram gas ammonia terdapat molekul sebanyak ….
A 10 B 10 L C
D 10 gL E
36 Unsur X sebanyak 3,01 × 1023 atom mempunyai massa 2 gram. Massa molar unsur X adalah
….
A 4 gram/mol B 10 gram/mol C 20 gram/mol D 40 gram/mol E 80 gram/mol
37 Jumlah atom yang terdapat dalam 0,5 mol gas hidrogen adalah ….
A 6,02 × 10-23 atom B 3,01 × 1022 atom C 3,01 × 1023 atom D 6,02 × 1023 atom E 12,04 × 1023 atom
38 Pada keadaan STP sebanyak 180 gram air (H2O) akan menempati volume ruangan sebesar ....
A 22,4 liter B 2,44 liter C 4,88 liter D 224 liter E 244 liter
39 Pada suhu 27 0C dan tekanan 3 atmosfer, massa air (H2O) yang menempati volume 82 liter adalah ....
(Ar H = 1, Ar O = 16, R = 0,082 atm L mol- K-) A 90 gram
B 180 gram C 270 gram D 360 gram E 450 gram
40 Perhatikan persamaan reaksi berikut!
2H2 (g) + O2 (g) 2H2O (g)
Jika 20 gram gas H2 direaksikan dengan oksigen berlebih pada suhu 0 0C dan P = 1 atm, maka volume H2O yang terbentuk sebanyak .... (Ar H = 1 ; O = 16)
A 22,4 liter B 224 liter C 2,44 liter D 24,4 liter E 244 liter