BAB II
TINJAUAN PUSTAKA II.1. Stroke
II.1.1. Definisi
Stroke secara klasik dikarakteristikkan sebagai defisit neurologik yang
berhubungan dengan cedera fokal akut pada sistem saraf pusat (SSP) oleh sebab
vaskular, yang meliputi infark serebral, perdarahan intraserebral (PIS) dan
perdarahan subarakhnoid (PSA), dan merupakan penyebab utama kecacatan dan
kematian di seluruh dunia. Menurut definisi terbaru, stroke adalah suatu episode
disfungsi neurologik akut yang diduga disebabkan oleh iskemia atau perdarahan,
berlangsung >24 jam atau hingga meninggal, namun tanpa adanya bukti yang
cukup untuk diklasifikasikan sebagai salah satu dari yang tersebut diatas (Sacco,
2013).
Stroke iskemik adalah tanda klinis disfungsi atau kerusakan jaringan otak
yang disebabkan kurangnya aliran darah ke otak sehingga mengganggu
kebutuhan darah dan oksigen di jaringan otak (disitasi oleh Sjahrir,2003). Definisi
terbaru menyebutkan stoke iskemik adalah suatu episode disfungsi neurologik
yang disebabkan infark serebral fokal, infark spinal atau infark retina (Sacco,
2013).
Stroke hemoragik terdiri dari perdarahan intraserebral (PIS) dan
perdarahan subarakhnoid (PSA). Definisi stroke yang disebabkan PIS adalah
tanda klinis disfungsi neurologis yang berkembang cepat yang berhubungan
dengan pengumpulan darah fokal di dalam parenkim otak atau sistem ventrikuler
yang tidak disebabkan oleh trauma. Sedangkan definisi stroke yang disebabkan
oleh karena perdarahan pada ruang subarakhnoid (ruang antara membran
arakhnoid dan piamater pada otak dan medulla spinalis), yang tidak disebabkan
trauma (Sacco, 2013).
II.1.2. Epidemiologi
Setiap tahun sekitar 795.000 orang di Amerika Serikat mengalami stroke
baru ataupun berulang. Sekitar 610.000 merupakan serangan pertama dan
185.000 serangan berulang. Rata-rata setiap 40 detik, 1 orang di Amerika Serikat
terserang stroke (Go,2013).
Wanita memiliki resiko seumur hidup yang lebih tinggi untuk mendapatkan
stroke dibandingkan dengan pria. Pada Framingham Heart Study diketahui bahwa
resiko seumur hidup untuk mendapatkan stroke pada orang berusia 55-75 tahun
adalah 1 dari 5 orang pada wanita (20-21%), dan 1 dari 6 orang pada pria
(14-17%) (Go, 2013).
Laporan European Journal of Neurology pada tahun 2006 mengungkapkan
bahwa di beberapa negara Uni Eropa, seperti Islandia, Norwegia, dan Swiss,
insidensi stroke diperkirakan 101.2 sampai 239.3/100.000 (1,1 juta orang setiap
tahunnya). WHO memperkirakan insidensi stroke ini akan meningkat dari 1.1 juta
di tahun 2000 menjadi 1,5 juta jiwa pada 2025 berdasarkan proyeksi populasi
penduduk (Truelsen, 2006).
Di Indonesia, insiden stroke sebesar 51.6/100.000 penduduk. Penderita
laki-laki lebih banyak daripada perempuan, dan profil usia di bawah 45 tahun :
11.8%, usia 45-64 tahun: 54.2% dan usia lebih dari 65 tahun : 33.5%. Stroke
menyerang usia produktif dan usia lanjut, yang berpotensi menimbulkan masalah
baru dalam pembangunan kesehatan secara nasional di kemudian hari (Guideline
Studi dari World Health Organization (WHO) menunjukkan bahwa
dibandingkan dengan etnis Kaukasia, etnis Asia memiliki prevalensi stroke yang
relatif lebih tinggi. Insidens stroke di Asia berada dalam rentang 182 hingga 342
per 100.000 populasi.Kejadian stroke di Asia juga diprediksi akan meningkat dari
tahun ke tahun dikarenakan dengan perubahan gaya hidup dan peningkatan usia
harapan hidup (Taqui, 2007).
II.1.3. Klasifikasi
Dikenal bermacam-macam klasifikasi stroke, berdasarkan atas gambaran
klinik, patologi anatomi, sistem pembuluh darah dan stadiumnya (Misbach, 2011).
a. Berdasarkan patologi anatomi dan penyebabnya :
1. Stroke Iskemik
a. Serangan iskemik sepintas (transient ischemic attack/TIA)
b. Trombosis serebri.
c. Emboli serebri.
2. Stroke Hemoragik
a. Perdarahan intraserebral.
Terminologi perdarahan intraserebral dan parenkimal
menunjukkan perdarahan yang langsung terjadi di dalam jaringan
otak. Penyebabnya paling sering adalah hipertensi, dengan
kebocoran (leakage) darah dari kerusakan arteriol oleh karena
peningkatan tekanan darah. Bleeding diatheses, atau kecenderungan untuk terjadinya perdarahan (bleeding tendency),
khususnya dari pemakaian antikoagulan, atau dari trauma,
obat-obatan, malformasi vaskular dan vaskulopati (seperti cerebral
Perdarahan parenkim terjadi pada regio yang terlokalisasi di otak.
Derajat kerusakan otak tergantung pada lokasi, kecepatan,
volume dan tekanan dari perdarahan tersebut (Caplan, 2009).
b. Perdarahan subarakhnoid (PSA).
Pada PSA, darah keluar dari vascular bed ke permukaan otak dan
menyebar secara cepat melalui jalur cairan serebrospinalis (CSS)
ke dalam ruang subaraknoid. Perdarahan paling sering berasal
dari aneurisma atau malformasi arteri-vena, namun bleeding
diatheses atau trauma juga dapat menyebabkan PSA. Aneurisma
yang ruptur melepaskan darah secara cepat pada tekanan darah
sistemik, secara tiba-tiba meningkatkan tekanan intrakranial (TIK),
sementara perdarahan oleh karena sebab yang lain biasanya
lebih lambat dan pada tekanan yang lebih rendah. Darah di dalam
ruang subarakhnoid selalu mengandung substansi yang
menyebabkan vasokonstriksi arteri-arteri basal otak yang
berhubungan langsung dengan CSS (Caplan, 2009).
b. Berdasarkan stadium/ pertimbangan waktu :
1. Transient Ischemic Attack (TIA) : suatu gangguan akut dari fungsi fokal
serebral yang gejalanya berlangsung <24 jam dan disebabkan oleh
trombus atau emboli.
2. Stroke in evolution (progressing stroke) : gejala/tanda neurologis fokal
terus memburuk setelah 48 jam. Defisit neurologis yang timbul
berlangsung secara bertahap dari yang ringan menjadi lebih berat.
3. Complete stroke : kelainan neurologis yang ada sifatnya sudah
c. Berdasarkan sistem pembuluh darah :
1. Sistem karotis
2. Sistem vertebro-basilar (Misbach, 2011).
d. Trial of Org 10172 in Acute Stroke Treatment (TOAST) dan Stroke Data Bank
Classifications :
1. Large-artery atherosclerosis (embolus/thrombosis) : bukti klinis adanya
disfungsi kortikal, subkortikal, batang otak ataupun serebellum dengan
ditemukannya lebih dari 50% distribusi lesi atau oklusi pembuluh darah
intrakranial atau ekstrakranial dengan CT-scan atau MRI pada infark
lebih dari 1.5 cm.
2. Cardioembolism, bukti klinis adanya disfungsi kortikal, subkortikal,
batang otak ataupun serebelum dengan ditemukannya pada CT atau
MRI lesi lebih dari 1.5 cm dan ditemukannya salah satu resiko tinggi
(misalnya : atrial fibrillation atau katup jantung mekanik) atau resiko
sedang kelainan jantung (misalnya : lone atrial fibrillation atau patent
foramen ovale) pada pemeriksaan diagnostik (EKG, echocardiography). 3. Small-vessel occlusion (lacunar infarct), bukti klinis sindrom lakunar
(gangguan motorik murni, gangguan sensorik murni, ataksia
hemiparesis dan dysarthria-clumsy hand) dengan hasil CT atau MRI
yang normal atau kurang dari 1.5 cm pada area yang diperdarahi
arteri-arteri perforantes kecil. Keterlibatan arteri-arteri besar dan jantung harus
disingkirkan.
4. Stroke of other determined etiology, yaitu stroke yang disebabkan oleh
hematologi dan penyebab stroke yang jarang setelah pemeriksaan
diagnostik. Kategori lain harus disingkirkan.
5. Stroke of undetermined etiology (cryprogenic). Diagnosis ini jika ada 2
atau lebih etiologi stroke, setelah pemeriksaan lengkap menghasilkan
tidak ada sumber penyebab yang paling mungkin, atau pasien
menjalani pemeriksaan yang belum lengkap (disitasi oleh Gofir, 2009).
e. Klasifikasi menurut Bamford (1992) :
1. Total Anterior Circulation Infarct (TACI)
Infark tipe TACI ini penyebabnya adalah emboli kardiak atau trombus
arteri ke arteri. Gambaran klinisnya berupa : hemiparesis dengan atau
tanpa gangguan sensorik (kontralateral sisi lesi), hemianopia
(kontralateral sisi lesi), dan gangguan fungsi luhur (disfasia, gangguan
visuo-spatial, hemineglek, agnosia, apraksia).
2. Partial Anterior Circulation Infarct (PACI)
Gejala lebih terbatas pada daerah yang lebih kecil dari sirkulasi serebral
pada sistem karotis, yaitu : defisit motorik/sensorik dan hemianopia,
defisit motorik/sensorik disertai gejala fungsi luhur, gejala fungsi luhur
dan hemianopia, defisit motorik/sensorik murni yang kurang ekstensif
dibanding infark lakunar (hanya monoparesis-monosensorik), gangguan
fungsi luhur saja.
3. Lacunar Infarct (LACI), disebabkan infark pada arteri kecil di dalam otak
(small deep infarct), dengan tanda-tanda klinis : tidak ada defisit visual,
gangguan fungsi luhur dan gangguan fungsi batang otak, adanya defisit
pure motor stroke (PMS), pure sensory stroke dan ataksik hemiparesis (termasuk ataksia dan paresis unilateral, dysarthria syndrome)
4. Posterior Circulation Infarct (POCI), oklusi terjadi pada batang otak dan
atau lobus oksipitalis, dengan gejala klinis berupa disfungsi saraf otak,
satu atau lebih sisi ipsilateral dan gangguan motorik/ sensorik
kontralateral, gangguan sensorik/ motorik bilateral, gangguan gerakan
konjugat mata (horizontal atau vertikal), disfungsi serebelar tanpa
gangguan long-tract ipsilateral, isolated hemianopia atau buta kortikal
(disitasi oleh Gofir, 2009).
II.1.4. Patofisiologi
II.1.4.1. Patofisiologi Stroke Iskemik
Pada stroke iskemik, berkurangnya aliran darah ke otak menyebabkan
hipoksemia daerah regional otak dan menimbulkan reaksi reaksi berantai yang
berakhir dengan kematian sel-sel otak dan unsur-unsur pendukungnya (Misbach,
2007).
Secara umum daerah regional otak yang iskemik terdiri dari bagian inti
(core) dengan tingkat iskemia terberat dan berlokasi di sentral. Daerah ini akan
menjadi nekrotik dalam waktu singkat jika tidak ada reperfusi. Di luar daerah core
iskemik terdapat daerah penumbra iskemik. Sel-sel otak dan jaringan
pendukungnya belum mati akan tetapi sangat berkurang fungsi-fungsinya dan
menyebabkan juga defisit neurologis. Tingkat iskemiknya makin ke perifer makin
ringan. Daerah penumbra iskemik, diluarnya dapat dikelilingi oleh suatu daerah
hiperemik akibat adanya aliran darah kolateral (luxury perfusion area). Daerah
penumbra iskemik inilah yang menjadi sasaran terapi stroke iskemik akut supaya
pada faktor waktu dan jika tidak terjadi reperfusi,daerah penumbra dapat
berangsur-angsur mengalami kematian (Misbach,2007)
II.1.4.2. Patofisiologi Stroke Hemoragik
Perdarahan pada parenkim otak selalu didahului oleh kerusakan pada
arteri-arteri penetrating serebral kecil dan arteriol akibat hipertensi. Dilatasi
aneurisma yang kecil terjadi pada teritori vaskular penetrating pasien hipertensi,
dan pada beberapa pasien, ini merupakan titik lemah yang akan mengalami ruptur
saat terjadi peningkatan tekanan arterial. Kebocoran dari pembuluh-pembuluh
darah kecil ini menghasilkan efek tekanan lokal yang tiba-tiba terhadap kapiler
dan arteriol di sekitarnya yang selanjutnya akan menyebabkan pembuluh darah
tersebut pecah. Efek bola salju (avalanche-type effect) terjadi, dimana
pembuluh-pembuluh darah yang pecah ini akan menambah volume pada perdarahan yang
membesar secara gradual. Akumulasi darah di sekeliling hematoma seperti bola
salju yang menggelinding menuruni bukit, volumenya akan semakin banyak.
Tekanan darah yang tinggi dan efek bola salju ini akan memperbesar perdarahan,
sementara tekanan jaringan lokal akan menjadi tampon terhadap perdarahan
(Caplan, 2009)
Peningkatan volume hematoma secara gradual ini akan menyebabkan
perburukan klinis secara gradual hingga hematoma mencapai ukuran akhirnya.
Bila hematoma cukup besar, akan menimbulkan peningkatan tekanan intrakranial.
Pasien dengan PIS biasanya memburuk dalam 24-48 jam pertama setelah gejala
awal. Perburukan ini disebabkan oleh berlanjutnya perdarahan, namun paling
sering oleh karena perkembangan edema di sekitar lesi, efek lesi terhadap aliran
Perdarahan subarakhnoid hampir selalu secara tiba-tiba meningkatkan TIK.
Tekanan darah sistemik dan volume darah harus dipertahankan atau ditambah
untuk menjaga perfusi otak dalam menghadapi peningkatan TIK. Setelah
perdarahan inisial, 3 resiko utama yang mempengaruhi kejadian selanjutnya:
rebleeding, vasokonstriksi dan hidrosefalus. Sekali dinding luar pembuluh darah yang abnormal (aneurisma atau malformasi vaskular) rusak, pembuluh ini akan
rentan terhadap rebleeding. Perdarahan selanjutnya akan mengancam hidup
karena peningkatan TIK dan jumlah darah pada CSS. Arteri yang terkena darah
yang bercampur dalam CSS selalu berkonstriksi. Vasokonstriksi bisa lokal atau
lebih difus dan sering menyebabkan iskemia, edema otak dan infark. Darah di
dalam CSS dapat menyumbat membran absortif dan menyebabkan hidrosefalus
komunikans dan dilatasi seluruh sistem ventrikular (Caplan, 2009).
II.2. Keparahan Stroke.
Manajemen yang berhasil dari penyakit yang menimbulkan disabilitas,
termasuk stroke, harus memperoleh manfaat dari penggunaan sistem klasifikasi
untuk menentukan pengaruh pengobatan, terutama pengobatan darurat. Agar
pasien stroke yang bertahan hidup dapat menerima perawatan terbaik, sistem
klasifikasi keluaran stroke yang komprehensif dibutuhkan untuk menentukan
intervensi terapi yang tepat. Pengembangan sistem klasifikasi ini didasarkan pada
keyakinan bahwa defisit neurologis selalu menimbulkan gangguan fungsi
permanen, disabitas dan penurunan kualitas hidup. Defisit neurologis yang terjadi
mengenai berbagai domain neurologis, sebagai berikut :
a. Motorik : merupakan defisit yang paling sering ditemukan, biasanya
mengenai wajah, lengan dan tungkai bawah, sendiri atau dalam berbagai
b. Sensorik : defisit dapat berupa hilangnya sensasi hingga hilangnya
persepsi yang lebih kompleks. Pasien dapat mengeluhkan numbness,
tingling atau perubahan sensitivitas. Gangguan sensori yang lebih kompleks dapat berupa astereognosis dan agrafia.
c. Penglihatan : stroke dapat menyebabkan monocular vision loss,
hemianopia homonim atau cortical blindness.
d. Bahasa : gangguan bahasa dapat berupa disfasia, dengan gangguan pada
pemahaman, penamaan, repetisi, fluency, membaca atau menulis.
e. Kognisi : berupa gangguan memori, atensi, orientasi, kalkulasi dan
konstruksi.
f. Afek : depresi merupakan gangguan afek yang sering terjadi paska stroke.
Gejalanya berupa hilangnya energi, kurangnya minat, selera makan dan
insomnia.(Kelly-Hayes, 1998)
Oleh karena heterogenisitas dari gejala stroke dan keparahannya, terdapat
banyak kemungkinan kategori pengukuran keluaran stroke. Beberapa yang
banyak digunakan adalah Canadian Neurologic Scale (CNS), National Institutes of
Health Stroke Scale (NIHSS), dan Scandinavian Stroke Scale (SSS) (Williams, 2009). Skor NIHSS sering digunakan untuk mengukur keparahan gejala stroke,
dengan skor >20 lebih prediktif untuk keluaran yang buruk (Tsao, 2005).
Berdasarkan klasifikasi sekuele penyakit dari WHO (World Health
Organization), skala keluaran dikarakteristikkan sebagai alat untuk mengukur impairments, disabilities atau handicaps. Impairment adalah konsekuensi fisik dari disfungsi organ yang spesifik, disability adalah kesulitan yang dialami pasien
untuk melakukan aktifitas normal oleh karena impairment-nya, dan handicap
tersebut mempengaruhi sosial individu, profesi atau peran dalam keluarga. Pada
stroke, impairment biasanya dinilai dengan skala ordinal (misalnya NIHSS),
disability dinilai dengan skala instrumental activities of daily living (IADL) seperti Barthel Index (BI), sedangkan handicap, meskipun jarang dinilai dalam percobaan klinis stroke, dinilai dengan skala health-related quality of life (HRQL) (Williams,
2009).
Beberapa parameter keparahan suatu stroke perdarahan intraserebral
meliputi skor NIHSS, skor Skala Koma Glasgow (SKG), volume lesi dan lamanya
perawatan di rumah sakit (Ramirez-Moreno, 2009).
Skala Koma Glasgow (SKG) dikembangkan untuk menentukan derajat
kesadaran pada pasien cedera kepala. Skala ini memiliki 3 komponen, yaitu:
respons buka mata (skor 1-4), respons verbal (skor 1-5) dan respons motorik
(skor 1-6), dan telah diterima sebagai skor prognostik, baik pada pasien trauma
maupun non-trauma yang mengalami penurunan kesadaran. Penilaian derajat
kesadaran pada stroke akut penting untuk manajemen klinis dan sebagai salah
satu indikator prognostik (Weir, 2003). Penilaian SKG pre-hospital tampaknya juga
merupakan prediktor yang baik dari keparahan stroke, berkorelasi dengan
keberhasilan yang lebih tinggi dari tindakan intervensi endovaskuler, keluaran
fungsional saat pasien keluar dari rumah sakit, juga berkorelasi dengan kematian
dalam 90 hari (Weaver, 2012)
Modified Rankin Scale (mRS) adalah pengukuran disabilitas global yang telah digunakan secara luas oleh klinisi untuk mengevaluasi pemulihan stroke dan
sebagai primary end point dalam randomized clinical trials (RCTs) dari terapi
stroke akut. Nilai mRS sebagai end-point RCT telah diteliti pada beberapa
penggunaan skala, kesingkatan dan interpretabilitasnya dalam konteks penelitian
stroke (Banks, 2007). Modified Rankin Scale merupakan skala yang paling sering
digunakan untuk pengukuran keluaran pada penelitian stroke. Skala ini menjadi
sangat populer oleh karena validitasnya, relatif efisien, dan umumnya diterima
dengan baik untuk pengkategorian dikotomi pasien stroke yang dependen dan
independen (Williams, 2009).
II.3. Low-Density Lipoprotein Cholesterol (LDL-C)
Low-density lipoprotein cholesterol (LDL-C) adalah salah satu dari 4 kelompok utama lipoprotein yang merupakan molekul pengangkut lipid di dalam
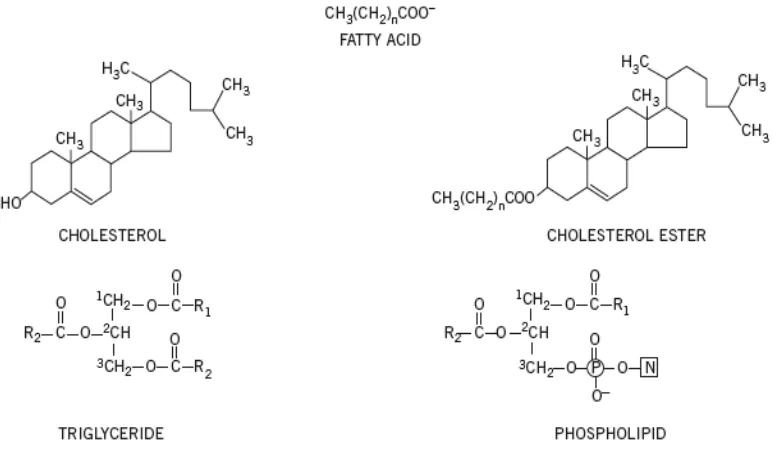
darah. Lipid plasma terdiri dari triasilgliserol atau trigliserida (16%), fosfolipid
(30%), kolesterol (14%), kolesteril ester (36%) dan sedikit fraksi asam lemak
bebas (free fatty acid) sebanyak 4% (Mayes, 2003). .
Lipoprotein adalah protein plasma yang mentranspor lipid yang tidak larut dalam air. Lipoprotein dikategorikan atas kilomikron, β-lipoprotein (low-density
lipoproteins, LDL), pre-β-lipoprotein (very-low-density lipoproteins, VLDL), dan
a-lipoprotein (high-density a-lipoproteins, HDL). Apoa-lipoprotein A terutama terdiri dari
HDL, kilomikron, dan VLDL. Apolipoprotein B adalah komponen utama LDL
Gambar 1. Struktur lipid. P= fosfat, N= basa nitrogen, R= asam lemak. Dikutip dari : Crook, M.A. 2012. Clinical biochemistry and metabolic medicine. CRC press. Taylor & Francis Group, Florida.
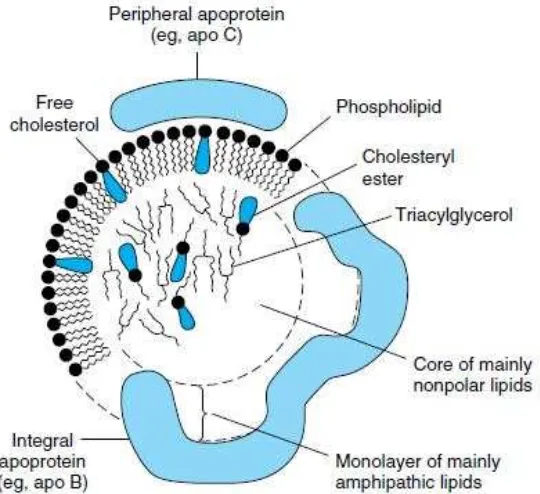
Lipoprotein merupakan makromolekul sferoidal yang memiliki inti hidrofobik
yang mengandung fosfolipid, anti-oksidan yang larut dalam lemak, vitamin, dan
kolesteril ester, dan memiliki lapisan luar yang hidrofilik, yang mengandung
kolesterol bebas, fosfolipid dan molekul apolipoprotein. Lipoprotein utama yang
mengangkut trigliserida adalah kilomikron dan VLDL, sedangkan lipoprotein yang
Gambar 2. Struktur umum lipoprotein plasma. Sejumlah kecil kolesteril ester dan triasilgliserol ditemukan di lapisan permukaan dan sedikit kolesterol bebas di inti.
Dikutip dari : Mayes, P.A., Botham, K.M. 2003. Lipid Transport and Storage. In: Murray
RK, Granner DK, Mayes PA, Rodwell VW. Harper’s Illustrated Biochemistry. 26th ed.
Lange Medical Books/McGraw-Hill Companies. P. 205-211.
Lipoprotein diklasifikasikan berdasarkan densitas apungnya (buoyant
density) yang berbanding terbalik dengan ukurannya. Semakin besar rasio lipid terhadap protein, ukurannya semakin besar dan densitasnya semakin rendah.
Kilomikron, VLDL dan IDL (intermediate-density lipoprotein) kaya akan trigliserida,
memiliki ukuran yang besar dan menimbulkan tampilan yang keruh pada plasma.
Kilomikron merupakan lipoprotein yang paling besar dan paling rendah kepadatan
lipoproteinnya, berfungsi membawa lipid eksogen dari usus ke seluruh sel.
Very-low-density lipoproteins (VLDL) membawa lipid endogen dari hati ke sel-sel tubuh. Intermediate-density lipoprotein (IDL) yang bersifat sementara dan terbentuk selama konversi VLDL menjadi LDL normalnya tidak dijumpai dalam plasma.
memiliki ukuran yang lebih kecil. Low-density lipoprotein (LDL) terbentuk dari
VLDL dan membawa kolesterol ke sel-sel. High density lipoprotein (HDL)
merupakan lipoprotein paling padat dan terlibat dalam transpor kolesterol dari sel
kembali ke hati (reverse cholesterol transport) (Crook, 2012).
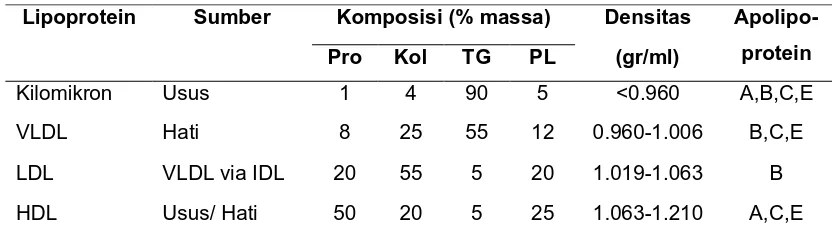
Tabel 1. Karakteristik lipoprotein
Lipoprotein Sumber Komposisi (% massa) Densitas
Apolipo-protein
Kol= kolesterol, HDL= high density lipoprotein, IDL= intermediate-density lipoprotein, LDL= low density lipoprotein, PL= fosfolipid, Pro= protein, TG= trigliserida, VLDL= very low-density lipoprotein.
Dikutip dari : Crook, M.A. 2012. Clinical biochemistry and metabolic medicine. CRC press. Taylor & Francis Group, Florida, dan Biggerstaff,K.D., Wooten, J.S. 2004. Understanding lipoproteins as transporters of cholesterol and other lipids. Advan in Physiol Edu. 28:105-106.
Lipid utama pada lipoprotein adalah kolesterol bebas dan kolesterol
teresterifikasi (C) dan trigliserida (TG). Metabolisme TG, LDL-C dan HDL-C
digambarkan sebagai berikut. Pada metabolisme TG, lemak dari makanan yang
terhidrolasi memasuki sel-sel intestinal (enterosit) via transporter asam lemak. TG
bersama dengan kolesterol ester dan isoform apolipoprotein B (ApoB) B48
bergabung dengan kilomikron (chylomicron, CM) oleh microsomal TG-transporter
protein (MTTP) melalui suatu jalur vesikuler. CM disekresi melalui sistem limfatik, memasuki vena cava dan bersirkulasi hingga mereka berinteraksi dengan
ApoC3. Asam lemak bebas yang dilepaskan memasuki sel-sel perifer secara
inkomplit. Di adiposit, enzim-enzim termasuk acyl-CoA: diacylglycerol acyltransferase (DGAT) mensintesa kembali TG, yang dihidrolisa oleh adipose TG lipase (ATGL) dan hormone sensitive lipase (HSL). Sisa CM (CM remnants, CMR)
diambil oleh reseptor LDL (LDLR) hepatik, bila LDLR tidak ada maka ia akan
diambil oleh LDLR-related protein (LRP1). Di sel-sel hepar (hepatosit), TG
bergabung dengan kolesterol dan isoform ApoB100 menjadi VLDL; TG yang ada
di VLDL dihidrolisa oleh LPL, melepaskan asam lemak dan sisa VLDL (IDL) yang
dihidrolisa oleh hepatic lipase (HL) sehingga menghasilkan LDL (Hegele, 2009).
Pada metabolisme LDL-C, sterol di lumen intestinal memasuki enterosit via
Niemann-Pick C1-like 1 (NPC1L1) transporter dan beberapa disekresi kembali oleh heterodimeric ATP-binding cassette transporter G5/G8 (ABCG5/G8). Di
enterosit, kolesterol bersatu dengan TG membentuk CM. Di hepatosit, kolesterol
digunakan kembali atau disintesa kembali de novo, dengan
3-hydroxy-3-methylglutaryl coenzyme A reductase (HMGCR). LDL mengalami proses endositosis oleh sel-sel perifer dan hepatosit melalui reseptor LDL (LDLR),
dibantu oleh suatu adaptor protein (AP). Proprotein convertase subtilisin/ kexin
type 9 (PCSK9), ketika bergabung dengan LDLR, mendaur-ulang LDLR dari endosome mengakibatkan degradasinya (X) (Hegele, 2009).
Pada metabolisme HDL-C, HDL, via ApoA1 memperantarai transpor
kolesterol kembali melalui interaksi dengan ATP-binding cassete A1 (ABCA1) dan
endothelial lipase (LIPG), memasuki hepatosit via scavenger receptor class B type 1 (SRB1) (Hegele, 2009).
High density lipoprotein (HDL) membawa kolesterol yang berlebih kembali ke hepar, dimana kolesterol dipecah dan diekskresikan dari dalam tubuh dalam
bentuk empedu. Oleh karena kerjanya yang membuang kolesterol yang berlebih,
HDL lebih disukai. Low-density lipoprotein (LDL) juga membawa kelebihan
kolesterol, namun ia bertendensi untuk membawa kelebihan ini ke arteri-arteri,
yang akan menyebabkan pembentukan aterosklerosis. Oleh karenanya diperlukan
kadar LDL yang rendah untuk menurunkan resiko penyakit-penyakit oleh
aterosklerosis (Wilson, 2008).
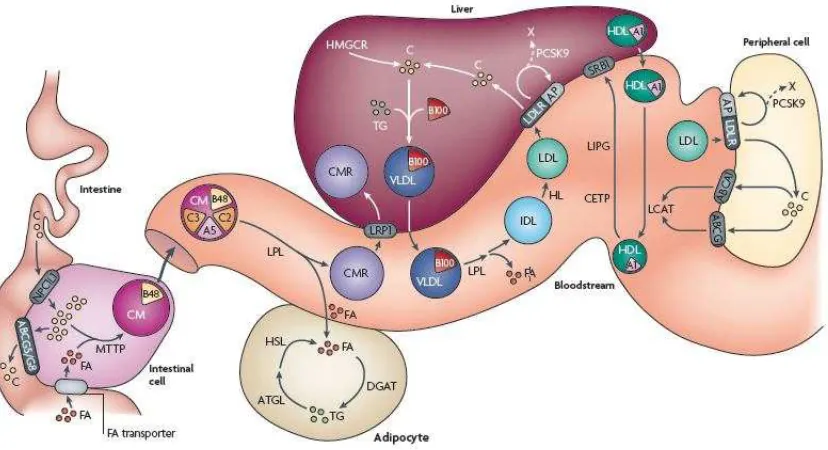
Gambar 3. Metabolisme lipoprotein.
Konsentrasi LDL-C plasma dapat dihitung dengan menggunakan
persamaan Friedewald dan sering digunakan di laboratorium klinik, sebagai
berikut :
LDL-C = Kolesterol total – (HDL-C) – (Trigliserida) 2.2
Persamaan ini diasumsikan tepat bila pasien berpuasa dan konsentrasi trigliserida
tidak melebihi 4.5 mmol/L (397 mg/dl). Bila tidak, kadar kilomikron akan membuat
persamaan ini tidak akurat (Crook, 2012).
Nilai LDL-C optimal : <100 mg/ dl (<2,6 mmol/l), near optimal : 100-129
mg/dl (2,6-3,35 mmol/l), borderline high risk : 130-159 mg/dl (3,36-4,11 mmol/l),
dan high risk : >159 mg/dl (>4,11 mmol/l). Nilai normal HDL-C : 40-60 mg/dl
(1,04-1,55 mmol/l), nilai >60 mg/dl dianggap memiliki resiko negatif untuk penyakit
jantung, dan nilai <40 mg/dl dianggap sebagai faktor resiko mayor untuk penyakit
jantung (Jellinger, 2012).
II.4. Hubungan Low-Density Lipoprotein Cholesterol dan Stroke.
Efek kadar kolesterol serum terhadap resiko stroke iskemik dan hemoragik
telah diteliti pada beberapa studi. Studi epidemiologik menunjukkan bahwa kadar
serum kolesterol total dan subfraksinya merupakan determinan stroke, namun
hubungannya relatif lemah. Peningkatan kadar kolesterol total dan penurunan
HDL-C merupakan predisposisi stroke iskemik pada usia lanjut (Sarti, 2000).
Kadar kolesterol yang tinggi secara konsisten berhubungan dengan
penyakit aterosklerosis arteri ekstra dan intrakranial. Arteri intrakranial diketahui
kurang rentan terhadap paparan kadar kolesterol yang tinggi dibandingkan arteri
oksidasi, yang akan menyebabkan partikel ini ditangkap oleh makrofag dan
kemudian melepaskan mediator-mediator yang menginduksi respons proliferatif di
dalam pembuluh darah. Dalam perkembangan selanjutnya, proliferasi sel-sel
myointimal dan kerusakan dinding sel menyebabkan deposisi elastin dan kolagen
dan oklusi pembuluh darah (Sarti, 2000).
Kadar kolesterol serum yang tinggi, khususnya LDL-C meningkatkan
agregasi platelet dengan menstimulasi platelet-activating factor (PAF),
meningkatkan deposisi platelet di trombus pada infark serebral eksperimental dan
menurunkan respons vasodilatasi pembuluh darah besar in vitro. Observasi ini
menunjukkan adanya mekanisme tambahan terhadap deposisi kolesterol pada
plak aterosklerotik (Sarti, 2000).
Pemeriksaan ultrasonografi beresolusi tinggi telah menunjukkan bahwa
penebalan dinding pembuluh darah tunika intima pada arteri karotid dan arteri
serebri media merupakan prediktor stroke. Hubungan antara aterosklerosis karotid
dan kadar LDL-C juga telah ditemukan di beberapa studi, dan studi RCT
(randomized controllled trials) mengenai penggunaan statin menunjukkan adanya
regresi plak aterosklerotik atau penurunan perkembangan aterosklerosis pada
arteri karotid (Koren-Morag, 2002)
Kadar LDL-C yang rendah diketahui merupakan salah satu faktor resiko
terjadinya perdarahan intraserebral (Sturgeon, 2007). Konsumsi alkohol yang
berlebihan dapat menyebabkan malnutrisi dan penyakit hati, dan telah diduga
sebagai penghubung yang menjelaskan kemungkinan hubungan kadar kolesterol
yang rendah dengan peningkatan resiko stroke hemoragik (Sarti, 2000).
Kadar LDL-C yang rendah juga berhubungan dengan peningkatan resiko
<80 mg/dl memiliki peningkatan resiko kematian 2 kali dibandingkan dengan
pasien dengan LDL-C >140 mg/dl (Noda, 2009). Penelitian lain juga menemukan
bahwa kadar LDL-C yang rendah (<100 mg/dl) berhubungan dengan peningkatan
resiko kematian pasien oleh karena perdarahan intraserebral (HR= 3.07, IK 95%,
1.04-9.02, p=0.042) (Ramirez-Moreno, 2009).
Penelitian Rodriguez-Luna (2011) mengukuhkan penelitian sebelumnya.
Mereka menemukan bahwa kadar LDL-C yang rendah berhubungan dengan
peningkatan perkembangan hematoma (hematoma growth, GH), deteriorasi
neurologik awal (early neurological deterioration, END) dan kematian dalam 3
bulan. Early neurological deterioration didefinisikan sebagai peningkatan poin
NIHSS > 4 poin atau kematian dalam 24 jam setelah onset stroke. Pada studi ini,
kadar LDL-C <95 mg/dl menjadi prediktor yang kuat terjadinya HG, END dan
mortalitas dalam 3 bulan pada pasien dengan perdarahan intraserebral akut
(Rodriguez-Luna, 2011).
Mekanisme yang menjelaskan hubungan LDL-C dan perdarahan
intraserebral masih belum jelas. Penjelasan yang mungkin untuk hubungan ini
adalah adanya peran kolesterol serum dalam mempertahankan integritas
pembuluh darah. Kadar kolesterol yang rendah berhubungan dengan
perkembangan nekrosis sel otot polos tunika media, sehingga menurunkan
resistensi terhadap ruptur dinding pembuluh darah. Selanjutnya, kolesterol
memodifikasi kemampuan agregasi platelet dengan aksinya pada platelet
activating factor (PAF), sehingga kolesterol yang rendah dapat menurunkan agregasi platelet, sehingga mempredisposisi perkembangan perdarahan
Teori lain menyebutkan, kolesterol dan trigliserida memainkan peranan
struktural penting pada membran sel. Dijumpai adanya peningkatan kerapuhan
eritrosit (erythrocyte fragility) in vitro dan in vivo dengan penurunan kadar
kolesterol. Diduga kadar kolesterol yang rendah menyebabkan kelemahan dinding
endotelium yang akan menimbulkan kerapuhan arterial, perdarahan atau
perbaikan yang lebih lambat setelah terjadinya perdarahan-perdarahan kecil.
Endotelium yang lemah juga lebih cenderung mengalami mikroaneurisma, yang
merupakan temuan patologik utama pada perdarahan serebral (Sturgeon, 2007).
Arteriolosklerosis dikarakteristikkan dengan angionekrosis sel-sel otot polos
dan peningkatan dalam basement membrane-like substance di lapisan luar sel-sel
otot polos arteri intraserebral di basal ganglia, talamus dan batang otak. Diet yang
tinggi kolesterol menurunkan angionekrosis dan mencegah terjadinya stroke
hemoragik pada tikus percobaan yang hipertensif, dan asupan lemak jenuh yang
lebih tinggi, yang menyebabkan peningkatan kadar LDL-C telah dibuktikan
menurunkan resiko perdarahan intraparenkimal pada orang-orang Jepang dan