BAB II
TINJAUAN PUSTAKA
II.1. STROKE
II.1.1. Definisi
Stroke adalah suatu episode dari disfungsi neurologis yang
disebabkan oleh iskemik atau hemoragik, berlangsung selama > 24 jam
atau meninggal, tetapi tidak memiliki bukti yang cukup untuk
diklasifikasikan (Sacco dkk, 2013).
Stroke iskemik adalah episode disfungsi neurologis disebabkan
infark fokal serebral, spinal, dan infark retinal. Dimana infark Sistem Saraf
Pusat (SSP) adalah kematian sel pada otak, medulla spinalis, atau sel
retina akibat iskemik, berdasarkan :
Patologi, pencitraan atau bukti objektif dari injury fokal iskemik pada
serebral, medula spinalis atau retina pada suatu distribusi vaskular
tertentu.
Atau bukti klinis dari injury fokal iskemik pada serebral, medulla
spinalis atau retina berdasarkan gejala yang bertahan ≥ 24 jam atau meninggal dan etiologis lainnya telah di eksklusikan (Sacco dkk,
2013).
Stroke hemoragik adalah disfungsi neurologis yang berkembang
cepat yang disebabkan oleh kumpulan darah setempat pada parenkim
otak atau sistem ventrikular yang tidak disebabkan oleh trauma (Sacco
II.1.2. Epidemiologi
Penyakit serebrovaskular menduduki peringkat kedua penyebab
kematian di dunia, angka mortalitasnya meningkat tiap tahunnya sekitar
20% (Enders dkk, 2009). Pada tahun 2001 sampai 2011 sekitar 795.000
orang di Amerika Serikat menderita stroke setiap tahunnya dimana sekitar
610.000 adalah serangan pertama dan 185.000 stroke berulang dimana
stroke merupakan satu dari 20 penyebab kematian di Amerika Serikat
(Goldstein dkk, 2011; Mozaffarian dkk, 2015).
Berdasarkan hasil penelitian Perhimpunan Dokter Spesialis Saraf
Indonesia (PERDOSSI) cabang Medan dari 562 pasien stroke pada 25
Rumah Sakit di Sumatera Utara, didapatkan kejadian stroke tidak berbeda
jauh antara perempuan dan laki-laki dimana kejadian pada perempuan
sebesar 296 orang (52,7%) dan laki-laki 266 orang (47,3%) dengan
rata-rata usia 59 tahun (20–95 tahun). Keluhan utama pasien terbanyak adalah penurunan kesadaran berjumlah 198 kasus (35,3%), diikuti hemiparesis
sinistra 134 kasus (23,8%), dan hemiparesis dextra 133 kasus (23,7%).
Faktor risiko terbesar adalah hipertensi berjumlah 497 kasus (88,4%),
diikuti diabetes melitus 155 kasus (27,6%), penyakit jantung 98 kasus
(17,4%), dislipidemia 161 (28,6%), merokok 193 (34,3%). Berdasarkan
hasil Computed Tomography (CT) scan kepala infark berjumlah 302 kasus
(53,7%), hemoragik 152 kasus (27%), infark hemoragik 12 kasus (2,1%),
II.1.3. Faktor Risiko
Faktor- faktor risiko untuk terjadinya stroke dapat diklasifikasikan
sebagai berikut :
1. Non modifiable risk factors :
a. Usia
b. Jenis Kelamin
c. Keturunan / genetik
2. Modifiable risk factors
a. Behavioral risk factors
1. Merokok
2. Unhealthy diet : lemak, garam berlebihan, asam urat, kolesterol,
low fruit diet.
3. Alkoholik
4. Obat – obatan: narkoba (kokain), antikoagulansia, antiplatelet, obat kontrasepsi.
b. Physiological risk factors
1. Penyakit hipertensi
2. Penyakit jantung
3. Diabetes Mellitus
4. Infeksi/lues, arthritis, traumatik, Acquired Immune Deficiency
Syndrome (AIDS), lupus
5. Gangguan ginjal
6. Kegemukan (obesitas)
8. Kelainan anatomi pembuluh darah
9. Dan lain-lain (Sjahrir, 2003).
II.1.4. Klasifikasi
Dasar klasifikasi yang berbeda – beda diperlukan, sebab setiap jenis stroke mempunyai cara pengobatan, pencegahan dan prognosis
yang berbeda, walaupun patogenesisnya sama.
A. Berdasarkan patologi anatomi dan penyebabnya :
1) Stroke iskemik
a. Transient Ischemic Attack (TIA)
b. Thrombosis serebri
c. Emboli serebri
2) Stroke Hemoragik
a. Perdarahan intraserebral
b. Perdarahan subaraknoid
B. Berdasarkan stadium / pertimbangan waktu
1) Transient Ischemic Attack (TIA)
2) Stroke in evolution
3) Completed stroke
C. Berdasarkan sistem pembuluh darah
1) Sistem karotis
2) Sistem vertebrobasiler
D. Klasifikasi Bamford untuk tipe infark yaitu :
1) Partial Anterior Circulation Infarct (PACI)
3) Lacunar Infarct (LACI)
4) Posterior Circulation Infarct (POCI) (Misbach dan Jannis, 2011).
E. Klasifikasi Stroke Iskemik berdasarkan kriteria kelompok peneliti
Trial of ORG 10172 in Acute Stroke Treatment (TOAST)
1) Aterosklerosis Arteri Besar
2) Kardioembolisme
3) Oklusi Arteri Kecil
4) Stroke Akibat dari Penyebab Lain yang Menentukan
a. Non-aterosklerosis Vaskulopati
• Non inflamasi
• Inflamasi non infeksi • Infeksi
b. Kelainan Hematologi atau Koagulasi
5) Stroke Akibat dari Penyebab Lain yang Tidak Dapat Ditentukan
(Sjahrir, 2003).
II.1.5. Patofisiologi
II.1.5.1. Patofisiologi Stroke Iskemik
Iskemik otak mengakibatkan perubahan dari sel neuron otak secara
bertahap, yaitu :
Tahap 1 :
a. Penurunan aliran darah otak.
b. Pengurangan oksigen.
c. Kegagalan energi.
Tahap 2 :
a. Eksitoksisitas dan kegagalan homeostasis ion.
b. Spreading depression.
Tahap 3 : Inflamasi
Respon inflamatorik pada stroke iskemik akut mempunyai pengaruh
buruk yang memperberat bagi perkembangan infark serebri. Berbagai
penelitian menunjukkan adanya perubahan kadar sitokin pada penderita
stroke iskemik akut. Sitokin adalah mediator peptida molekuler,
merupakan protein atau glikoprotein yang dikeluarkan oleh suatu sel dan
mempengaruhi sel lain dalam suatu proses inflamasi, contohnya limfokin
dan interleukin [IL-1 beta, IL-6, IL-8, Tumor Necrosis Factor – alpha
(TNF-α)] yang merupakan sitokin pro inflamatorik. Adanya IL-8 tersebut merupakan diskriminator terkuat yang membedakan kasus stroke dengan
non stroke. Produksi sitokin yang berlebihan mengakibatkan plugging
mikrovaskuler serebral dan pelepasan mediator vasokonstriktif endotel
sehingga memperberat penurunan aliran darah, juga mengakibatkan
eksaserbasi kerusakan Blood Brain Barrier (BBB) dan parenkim melalui
pelepasan enzim hidrolitik, proteolitik dan produksi radikal bebas yang
akan menambah neuron yang mati
Tahap 4 : Apoptosis (Sjahrir, 2003).
II.1.5.2. Patofisiologi Stroke Hemoragik
Perdarahan intraserebral biasanya timbul karena pecahnya
mikroaneurisma (Berry aneurysm) akibat hipertensi maligna. Hal ini paling
Hipertensi kronik menyebabkan pembuluh arteriol berdiameter 100 – 400 mikrometer mengalami perubahan patologi pada dinding pembuluh darah
tersebut berupa lipohialinosis, nekrosis fibrinoid serta timbulnya aneurisma
tipe Bouchard (Caplan, 2009).
Perdarahan intraserebral sekunder (sekitar 12 sampai 22% dari
seluruh kejadian perdarahan intraserebral) disebabkan oleh penyebab lain
selain pecahnya pembuluh darah kecil, misalnya, aneurisma, malformasi
arteri-vena, transformasi hemoragik stroke iskemik, dan neoplasma
(Brouwser dan Goldstein, 2012).
II.1.6 Diagnosis Stroke
II.1.6.1. Pemeriksaan Klinis
Pengetahuan tentang neuroanatomi dan anatomi pembuluh darah
penting untuk diagnosis klinis stroke. Sebelum membedakan kejadian
stroke, dokter pertama kali harus bertanya apakah temuan disebabkan
oleh proses nonvaskular, seperti tumor otak, gangguan metabolisme,
infeksi, demielinisasi, keracunan, atau cedera traumatis yang menyerupai
stroke. Data yang berbeda digunakan untuk menjawab dua pertanyaan ini
sangat berbeda. Dalam menentukan mekanisme stroke pertanyaan
"what?" dan temuan klinis paling bermanfaat:
1. Ekologi : riwayat penyakit terdahulu, riwayat penyakit sekarang, dan
riwayat penyakit keluarga.
2. Keberadaan dan sifat selama stroke atau Transient Ischemic Attack
(TIA)
4. Temuan sementara dan progresif (apakah terjadinya stroke tiba-tiba
dengan defisit pada kejadian awal stroke? Apakah defisit makin
meningkat, memburuk, atau tetap sama setelah onset? Jika itu
memburuk, apakah ini terjadi secara bertahap, remitting, atau progresif ?
Apakah ada fluktuasi normal atau abnormal?)
5. Gejala seperti sakit kepala, muntah, dan penurunan tingkat kesadaran
dapat menyertai (Caplan, 2009).
Defisit neurologis mencerminkan lokasi dan ukuran lesi pada
pasien dengan stroke iskemik dan perdarahan. Hemiplegia merupakan
tanda klasik pada semua penyakit serebrovaskular, apakah di bagian otak
atau batang otak, tetapi masih banyak manifestasi lain, termasuk
gangguan mental, numbness dan defisit sensoris, afasia, gangguan
lapang pandang, diplopia, dizziness, disartria, dan sebagainya (Ropper
dkk, 2014).
II.1.6.2. Pemeriksaan Radiologi
Pemeriksaan radiologi yang penting adalah pemeriksaan foto
thoraks yang dapat memperlihatkan keadaan jantung, apakah ada
pembesaran ventrikel kiri yang merupakan salah satu tanda hipertensi
kronis pada penderita stroke dan adakah kelainan lain pada jantung.
Selain itu dapat mengidentifikasi kelainan paru yang potensial
mempengaruhi oksigenasi serebral dan dapat memperburuk prognosis
(Misbach dan Jannis, 2011).
Pemeriksaan kedua adalah CT scan dapat menunjukkan gambaran
perdarahan subaraknoi d, gumpalan di dalam dan sekitar aneurisma,
daerah infark yang mengalami nekrosis dan malformasi arteriovenous.
Magnetic resonance imaging (MRI) juga menunjukkan lesi. Selain itu,
menunjukkan aliran pada pembuluh darah, hemosiderin, dan pigmen besi,
serta perubahan-perubahan yang dihasilkan dari nekrosis iskemik dan
gliosis (Ropper dkk, 2014).
II.2. HIPERTENSI
II.2.1. Definisi
Hipertensi ditegakkan apabila terjadi peningkatan rata-rata dua
atau lebih tekanan darah yang menetap di atas batas normal yang
disepakati, yaitu Tekanan Darah Diastolik (TDD) ≥ 90 mmHg atau Tekanan Darah Sistolik (TDS) ≥ 140 mmHg (Chobanian dkk, 2004). Lebih dari 90% hipertensi bersifat idiopatik (hipertensi esensial/primer),
sedangkan 5-10% diketahui penyebabnya (hipertensi sekunder)
(Goldszmidt dan Caplan, 2009).
Penelitian yang dilakukan Sastri dkk (2013) pada pasien stroke
menurut faktor risiko hipertensi sebesar 82.80% pada pasien rawat inap di
Bagian Penyakit Dalam RSUD Kabupaten Solok Selatan periode 1
Januari 2010 – 31 Juni 2012 dengan penderita berusia di atas 50 tahun (81,25%) dan penderita yang berusia di bawah 50 tahun (18,75%).
Penelitian lainnya yang dilakukan oleh Mochammad Bahrudin pada tahun
2009 di RSU Haji Surabaya, yang mana didapatkan kejadian tertinggi
usia dibawah 50 tahun, dengan puncaknya pada usia 51-60 tahun (Sastri
dkk, 2013).
Menurut The Seventh Report of The Joint National Committee on
Prevention, Detection, Evaluation and Treatment of High Blood Pressure
(JNC 7) klasifikasi tekanan darah pada orang dewasa terbagi menjadi
kelompok normal, prahipertensi, hipertensi derajat 1, dan derajat 2
(Chobanian dkk, 2004).
Tabel 1. Klasifikasi Tekanan Darah Menurut JNC 7
Klasifikasi Tekanan Darah TDS (mmHg) TDD (mmHg)
Normal < 120 < 80
Prehipertensi 120-139 80-89
Hipertensi derajat 1 140-159 90-99
Hipertensi derajat 2 ≥ 160 ≥ 100
Dikutip dari : Chobanian, A.V., Bakris, G.L., Black, H.R., Cushman, W.C., Green. L.A., Izzo, J.L. 2004. The Seventh Report of the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure. National Institute of Health Publication. U.S. pp 1-65.
Pada tahun 2013, The Eighth Report of The Joint National
Committee on Prevention, Detection, Evaluation and Treatment of High
Blood Pressure (JNC 8) telah mengeluarkan guideline terbaru mengenai
tatalaksana hipertensi atau tekanan darah tinggi. Dimana secara umum,
JNC 8 ini memberikan 9 rekomendasi terbaru terkait dengan target
tekanan darah dan golongan obat hipertensi yang direkomendasikan,
tetapi definisi hipertensi dan prehipertensi tidak dijelaskan (Tabel 2)
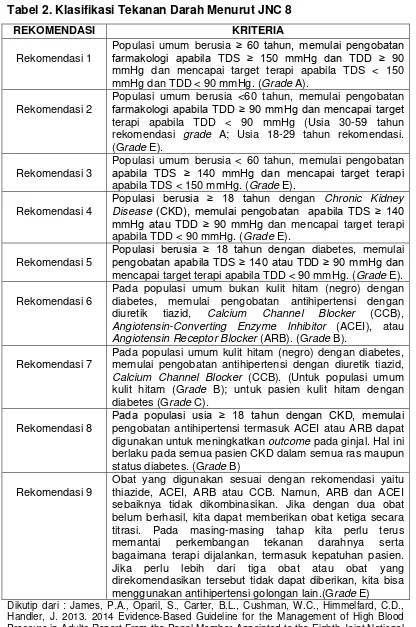
Tabel 2. Klasifikasi Tekanan Darah Menurut JNC 8
Populasi umum berusia <60 tahun, memulai pengobatan
farmakologi apabila TDD ≥ 90 mmHg dan mencapai target
terapi apabila TDD < 90 mmHg (Usia 30-59 tahun
apabila TDS < 150 mmHg. (Grade E).
Rekomendasi 4
Populasi berusia ≥ 18 tahun dengan Chronic Kidney Disease (CKD), memulai pengobatan apabila TDS ≥ 140
mmHg atau TDD ≥ 90 mmHg dan mencapai target terapi apabila TDD < 90 mmHg. (Grade E).
Rekomendasi 5
Populasi berusia ≥ 18 tahun dengan diabetes, memulai
pengobatan apabila TDS ≥ 140 atau TDD ≥ 90 mmHg dan
mencapai target terapi apabila TDD < 90 mmHg. (Grade E).
Rekomendasi 6
Pada populasi umum bukan kulit hitam (negro) dengan diabetes, memulai pengobatan antihipertensi dengan diuretik tiazid, Calcium Channel Blocker (CCB), Angiotensin-Converting Enzyme Inhibitor (ACEI), atau Angiotensin Receptor Blocker (ARB). (Grade B).
Rekomendasi 7
Pada populasi umum kulit hitam (negro) dengan diabetes, memulai pengobatan antihipertensi dengan diuretik tiazid, Calcium Channel Blocker (CCB). (Untuk populasi umum kulit hitam (Grade B); untuk pasien kulit hitam dengan diabetes (Grade C).
Rekomendasi 8
Pada populasi usia ≥ 18 tahun dengan CKD, memulai
pengobatan antihipertensi termasuk ACEI atau ARB dapat digunakan untuk meningkatkan outcome pada ginjal. Hal ini berlaku pada semua pasien CKD dalam semua ras maupun status diabetes. (Grade B)
Rekomendasi 9
Obat yang digunakan sesuai dengan rekomendasi yaitu thiazide, ACEI, ARB atau CCB. Namun, ARB dan ACEI sebaiknya tidak dikombinasikan. Jika dengan dua obat belum berhasil, kita dapat memberikan obat ketiga secara titrasi. Pada masing-masing tahap kita perlu terus memantai perkembangan tekanan darahnya serta bagaimana terapi dijalankan, termasuk kepatuhan pasien. Jika perlu lebih dari tiga obat atau obat yang direkomendasikan tersebut tidak dapat diberikan, kita bisa menggunakan antihipertensi golongan lain.(Grade E)
Masih ada beberapa klasifikasi dan pedoman penanganan
hipertensi lain dari World Health Organization (WHO), International
Society of Hypertension (ISH), dan European Society of Hypertension
(ESH, bersama European Society of Cardiology), British Hypertension
Society (BSH), dan Canadian Hypertension Education Program (CHEP)
(Yogiantoro, 2006).
II.2.2. Patofisiologi
Berdasarkan penyebabnya, hipertensi dibagi menjadi 2 golongan
yaitu, hipertensi primer yang tidak diketahui penyebabnya atau idiopatik
dan hipertensi sekunder yaitu hipertensi yang disebabkan penyakit lain
(Lee dkk, 2011).
II.2.2.1. Hipertensi Primer
Sampai sekarang pengetahuan tentang patogenesis hipertensi
primer terus berkembang karena belum dapat jawaban yang memuaskan
yang dapat menerangkan terjadinya peningkatan darah. Tekanan darah
dipengaruhi oleh Cardiac Output (CO) dan Total Peripheral Resistence
(TPR) dimana tekanan darah = CO x TPR, sedangkan CO adalah jumlah
stroke volume (SV) x Heart Rate (HR). SV ditentukan oleh kontraktilitas
jantung, venous return ke jantung (preload), kontraktilitas ventrikel kiri
mengalirkan darah ke aorta (afterload) (Lee dkk, 2011).
Banyak faktor patofisiologi telah terlibat dalam kejadian hipertensi,
yaitu peningkatan aktivitas sistem saraf simpatis, mungkin terkait dengan
peningkatan paparan stres psikososial, kelebihan produksi dari natrium
adekuat diet harian kalium dan kalsium, peningkatan sekresi renin dengan
peningkatan produksi angiotensin II dan aldosteron, defisiensi vasodilator,
seperti prostasiklin, Nitrit Oksida (NO) dan natriuretik peptida, perubahan
ekspresi sistem kallikrein – kinin yang mempengaruhi tonus pembuluh darah, kelainan resistensi pembuluh darah, termasuk lesi pembuluh ginjal,
diabetes melitus, resistensi insulin, obesitas, perubahan reseptor
adrenergik yang mempengaruhi denyut jantung, tonus pembuluh darah,
dan perubahan transportasi ion (Oparil dkk, 2003).
Penelitian perubahan genetik monogenik terbaik mengenai
penyebab hipertensi misalnya Liddle Syndrome, dimana gangguan yang
jarang terjadi tetapi secara klinis penting di mana aktivasi membran sel
kanal natrium menyebabkan hipertensi berat. Aktivasi aktivasi membran
sel kanal natrium telah ditemukan terjadinya mutasi pada subunit kanal
mengakibatkan retensi natrium di ginjal meningkat (Oparil dkk, 2003).
Ginjal dapat menginduksi volume-based hypertension dengan
mempertahankan kelebihan natrium dan air sebagai akibat dari (1)
kegagalan untuk mengatur aliran darah di ginjal; (2) gangguan kanal ion
(misalnya, penurunan basolateral Na-K-ATPase), yang secara langsung
menyebabkan retensi natrium; atau (3) regulasi hormon yang tidak tepat.
Sebagai contoh, Renin Angiotensin Aldosteron (RAA) adalah pengatur
hormon penting resistensi vaskular perifer. Tingkat renin pada pasien
hipertensi (dibandingkan dengan orang-orang normotensi) 25% di bawah
normal, sekitar 60% pasien normal, dan 10 hingga 15% pada hipertensi.
bahkan tingkat normal tidak sesuai pada penderita hipertensi. Dengan
demikian, kelainan peraturan sistem ini mungkin memainkan peran dalam
beberapa individu dengan hipertensi (Lee dkk, 2011).
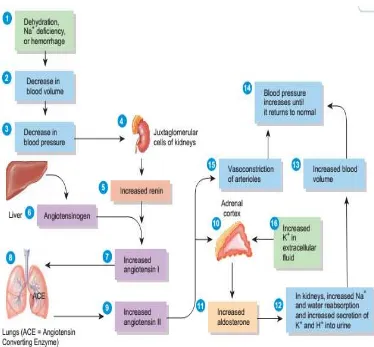
Mekanisme terjadinya hipertensi adalah melalui terbentuknya
angiotensin II dari angiotensin I oleh Angiotensin I Converting Enzyme
(ACE). ACE memegang peran fisiologis penting dalam mengatur tekanan
darah. Darah mengandung angiotensinogen yang diproduksi hati.
Selanjutnya oleh hormon renin (diproduksi oleh sel juxtaglomerular) akan
diubah menjadi angiotensin I. Oleh ACE yang terdapat di paru-paru,
angiotensin I diubah menjadi angiotensin II. Angiotensin II inilah yang
memiliki peranan penting dalam menaikkan tekanan darah melalui dua
aksi utama. Aksi pertama adalah vasokonstriksi arteriol serta
meningkatkan sekresi Antidiuretik Hormon (ADH) dan rasa haus (Wilson,
2006).
Antidiuretik Hormon (ADH) diproduksi di hipotalamus dan bekerja
pada ginjal untuk mengatur osmolalitas dan volume urin. Dengan
meningkatnya ADH, sangat sedikit urin yang dieksresikan ke luar tubuh,
sehingga menjadi pekat dan tinggi osmolalitasnya. Untuk
mengencerkannya, volume cairan ekstraseluler akan ditingkatkan dengan
cara menarik cairan dari bagian intraseluler. Akibatnya, volume darah
meningkat yang pada akhirnya akan meningkatkan tekanan darah. Aksi
kedua adalah menstimulasi sekresi aldosteron dari korteks adrenal.
Aldosteron merupakan hormon steroid yang memiliki peranan penting
mengurangi eksresi Natrium Cloride (NaCl) dengan cara mereabsorpsinya
dari tubulus ginjal. Naiknya konsentrasi NaCl akan diencerkan kembali
yang pada gilirannya akan meningkatkan volume dan tekanan darah
(Wilson, 2006).
Gambar 1. Patogenesis Hipertensi Melalui Sistem Renin Angiotensin Aldosteron dan Antidiuretik Hormon (ADH).
Dikutip dari :Tortora, G.J., Derrickson, B. 2009. The Endocrine System. In: Roesch, B. (eds). Principles of Anatomy and Physiology. 12th edition. Willey&Son Inc. United States. pp 642-688.
Hormon insulin mungkin memainkan peran dalam terjadinya
hipertensi. Banyak orang dengan hipertensi, terutama mereka yang
kegagalan dalam transportasi insulin menjadi glukosa ke jaringan (disebut
resistensi insulin). Sebagai hasilnya, kadar glukosa serum naik,
merangsang pankreas untuk melepaskan insulin tambahan. Peningkatan
kadar insulin dapat berkontribusi untuk hipertensi melalui peningkatan
aktivasi simpatik atau stimulasi hipertrofi sel otot polos pembuluh darah,
yang meningkatkan tahanan vaskular. Hipertrofi sel otot polos dapat
disebabkan oleh efek mitogenik langsung insulin atau melalui peningkatan
kepekaan terhadap platelet-derived growth factor (Lee dkk, 2011).
II.2.2.2. Hipertensi Sekunder
Meskipun hipertensi primer mendominasi gambar klinis, penyebab
struktural atau penyebab hormonal hipertensi sekunder dapat ditemukan
dalam persentase kecil dari pasien sekitar 5% kasus hipertensi telah
diketahui penyebabnya,. Identifikasi penyebab hipertensi sekunder
penting karena kondisi yang mendasarinya mungkin memerlukan terapi
yang berbeda dari yang diberikan untuk hipertensi primer dan sering dapat
disembuhkan. Selain itu, jika hipertensi sekunder yang tidak terkontrol,
menyebabkan perubahan kardiovaskular yang pada akhirnya akan terus
berkembang menjadi hipertensi primer meskipun penyakit yang
mendasarinya sudah teratasi. Meskipun bentuk sekunder harus
dipertimbangkan dalam pemeriksaan pasien hipertensi, ada petunjuk
bahwa pasien tertentu mungkin memiliki salah satu kondisi yang
menyertai.
1) Usia. Jika pasien hipertensi berkembang sebelum umur 20 atau
2) Beratnya. Hipertensi sekunder sering menyebabkan tekanan darah
akan meningkat secara dramatis, sedangkan kebanyakan pasien
hipertensi primer biasanya ringan sampai sedang.
3) Onset. Bentuk hipertensi sekunder sering muncul tiba-tiba di pasien
yang sebelumnya normotensif, sedangkan pada hipertensi primer
bersifat progresif perlahan.
4) Tanda-tanda dan gejala yang terkait. Proses yang menginduksi
hipertensi dapat mempunyai beberapa karakteristik lainnya, melalui
riwayat dan pemeriksaan fisik. Sebagai contoh, bruit arteri ginjal
dapat didengar pada perut pada pasien dengan stenosis arteri ginjal.
5) Riwayat keluarga. Pasien dengan hipertensi primer sering memiliki
hipertensi pada keturunan tingkat pertama, sedangkan hipertensi
sekunder lebih sering terjadi secara sporadik (Gray dkk, 2005).
Tabel 3. Hipertensi Sekunder
Penyebab Hipertensi Sekunder
Penyakit Parenkim Ginjal Penyakit Renovaskular
Penyakit Endokrin : Aldosteronisme primer, Sindrom Cushing,Hiperplasi adrenal kongenital, Feokromositoma
Koarktasio aorta
Kaitan dengan kehamilan Obat-obatan
Dikutip dari : Gray, H.H., Dawkins, K.D., Morgan, J.M., Simpson, I.A. 2005. Lecturer Notes: Cardiology, Dalam: Agoes, A., Rachmawati D.A. (eds). Lecturer Notes Kardiologi : Hipertensi. Edisi keempat. Penerbit Erlangga. Surabaya. Hal 57-69.
II.2.3. Diagnosis dan Gambaran Laboratorium
Evaluasi pasien hipertensi memiliki tiga tujuan: (1) untuk menilai
gaya hidup dan mengidentifikasi faktor-faktor risiko kardiovaskular lain
panduan pengobatan; (2) untuk mencari penyebab tekanan darah tinggi;
dan (3) untuk menilai adanya atau tidak adanya kerusakan organ target
dan penyakit kardiovaskular (Chobanian dkk, 2004).
Semua pasien yang dicurigai menderita hipertensi atau pasien
yang sudah pasti hipertensi, harus diambil anamnesis dan pemeriksaan
fisik yang menyeluruh. Beberapa pasien juga akan memerlukan
pemeriksaan penunjang yang lebih kompleks, misalnya pasien dengan
hipertensi maligna, hipertensi sekunder, dan pasien dengan keadaan
khusus (Gray dkk, 2005).
Anamnesis meliputi :
a. Lama menderita hipertensi dan derajat tekanan darah.
b. Indikasi adanya hipertensi sekunder
1) Keluarga dengan riwayat penyakit ginjal (ginjal polikistik).
2) Adanya penyakit ginjal, infeksi saluran kemih, hematuri,
pemakaian obat-obatan analgesik, dan lain-lain.
3) Episode berkeringat, sakit kepala, kecemasan, palpitasi
(feokromositoma).
4) Episode lemah otot dan tetani (aldosteronisme).
c. Faktor-faktor risiko
1) Riwayat hipertensi atau penyakit kardiovaskular pada pasien
atau keluarga pasien.
2) Riwayat dislipidemia pada pasien atau keluarga pasien.
3) Riwayat diabetes mellitus pada pasien atau keluarga pasien.
5) Pola makan.
6) Obesitas
d. Gejala kerusakan organ
1) Otak dan mata : sakit kepala, vertigo, gangguan penglihatan,
transient ischemic attacks, defisit sensoris atau motoris.
2) Jantung : palpitasi, nyeri dada, sesak, edema tungkai.
3) Ginjal : haus, poliuria, nokturia, hematuria.
4) Arteri perifer : ekstremitas dingin, klaudikasio intermiten
e. Pengobatan antihipertensi sebelumnya
f. Faktor-faktor pribadi, keluarga dan lingkungan
Pemeriksaan fisik selain memeriksa tekanan darah juga untuk
evaluasi penyakit penyerta, kerusakan organ target, serta kemungkinan
adanya hipertensi sekunder.
Pengukuran tekanan darah :
a. Pengukuran rutin di kamar periksa.
b. Pengukuran 24 jam (Ambulatory Blood Pressure Monitoring-ABPM)
c. Pengukuran sendiri oleh pasien
Pemeriksaan penunjang pasien hipertensi terdiri dari :
a. Tes darah rutin,
b. Glukosa darah (sebaiknya puasa),
c. Profil lipid,
d. Asam Urat,
e. Fungsi ginjal,
g. Urinalisis,
h. Elektrokardiogram,
i. Enzim jantung.
Pada pasien hipertensi, beberapa pemeriksaan untuk menentukan
adanya kerusakan organ dapat dilakukan secara rutin, sedang
pemeriksaan lainnya hanya dilakukan bila ada kecurigaan yang didukung
oleh keluhan dan gejala pasien. Pemeriksaan untuk mengevaluasi adanya
kerusakan organ target meliputi :
a. Jantung
1) Pemeriksaan fisik,
2) Foto polos dada,
3) Elektrokardiografi
4) Ekokardiografi.
b. Pembuluh darah
1) Pemeriksaan fisis termasuk perhitungan pulse pressure,
2) Ultrasonografi karotis
3) Fungsi endotel (masih dalam penelitian).
c. Otak
1) Pemeriksaan neurologis,
2) Computed Tomography (CT) scan kepala atau Magnetic
Resonace Imaging (MRI).
d. Mata
e. Fungsi Ginjal
1) Pemeriksaan fungsi ginjal dan penentuan adanya protein
uria, mikroalbuminuria/makroalbuminuria serta rasio albumin
kreatinin urin,
2) Perkiraan laju filtrasi glomerulus (Gray dkk, 2005).
II.2.4. Hipertensi Terhadap Risiko Stroke
Hipertensi yang terjadi pada penderita stroke apabila terjadi
peningkatan rata-rata dua atau lebih tekanan darah yang menetap di atas
batas normal yang disepakati, yaitu Tekanan Darah Diastolik (TDD) ≥ 90 mmHg atau Tekanan Darah Sistolik (TDS) ≥ 140 mmHg pada waktu sebelum atau 4 minggu setelah terjadinya stroke atau jika mereka
menerima obat anti hipertensi sebelum terjadinya stroke (Vemmos dkk,
2004).
Penelitian yang dilakukan Lohano dkk (2014), hampir 52.3 % dari
pasien memiliki hipertensi dengan laki-laki lebih sering. Data ini konsisten
dengan studi sebelumnya mengenai gender yang menunjukkan dominasi
antara laki-laki, dan dilaporkan pada pria telah menurun dari 2,8% pada
tahun 2006 menjadi 2,5% di tahun 2009, dan kemudian meningkat
menjadi 2,7% di 2010 oleh Idris dkk (2006) yang disitasi pada penelitian
Lohano dkk (2014). Penelitian ini juga menyatakan 281 total pasien stroke
memiliki faktor risiko hipertensi dimana 147 (52.3%) perdarahan
intraserebral, 128 (45,5%) stroke iskemik, dan 6 pasien (2.2%)
total pasien terdapat 158 (56,2%) memiliki faktor risiko diabetes melitus,
153 (54,8%) perokok, dan 139 (49,5%) obesitas.
Menurut Khan JA dkk yang disitasi dari penelitian Lahano dkk
(2014) dan Vohra dkk (2000) melaporkan 26% dari pasien dengan umur
15-45 tahun menderita stroke. Sedangkan, menurut American Heart
Association, stroke dapat terjadi pada setiap usia tapi risiko ganda setiap
dekade setelah usia 55.
Sebagian besar pasien di Pakistan dengan stroke memiliki penyakit
komorbiditas seperti hipertensi, diabetes melitus, rokok, dislipidemia, dan
obesitas. Dalam penelitian ini, tekanan darah tinggi adalah faktor risiko
untuk stroke iskemik yang lebih dari stroke hemoragik. Namun hipertensi
lebih sering terlihat dalam penanganan pasien yang mengalami iskemik.
Bagaimanapun hipertensi merupakan faktor risiko tersering pada stroke
iskemik tetapi hasilnya tidak mencapai nilai yang signifikan (Lahano dkk,
2014).
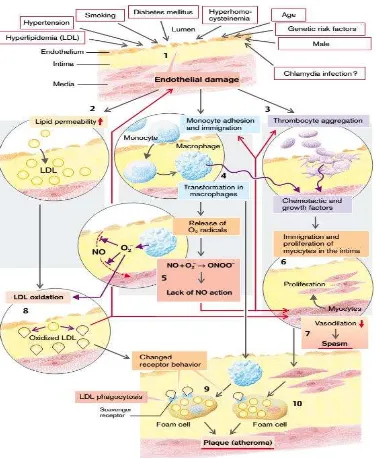
Aterosklerosis merupakan penyebab lebih dari separuh kematian di
negara-negara maju di Barat. Penyakit ini merupakan penyakit arteri yang
berkembang secara perlahan, dengan penebalan intima terjadi akibat
penumpukan fibrosa yang secara bertahap akan menyempitkan lumen
dan secara bertahap menjadi tempat perdarahan dan pembentukan
trombus (Silbernagl, 2007).
Akibat penimbunan plak adalah penyempitan lumen yang
menyebabkan iskemik dan kekauan dinding pembuluh darah,
menyebabkan emboli perifer (contohnya stroke) serta perdarahan ke
dalam plak (penyempitan oleh hematom) dan dinding pembuluh darah.
Karena melemah, dinding pembuluh darah melebar (aneurisma), dan
bahkan mengalami ruptur dengan menimbulkan perdarahan, yang
berbahaya ke jaringan sekitarnya, misalnya dari aorta atau pembuluh
darah otak (perdarahan intraserebral yang hebat) (Silbernagl, 2007).
Gambar 2. Response to Injury Hypothesis of Atherosclerosis Genesis
II.3. DISLIPIDEMIA
II.3.1. Definisi
Dislipidemia adalah kelainan metabolisme lipid yang ditandai
dengan peningkatan maupun penurunan fraksi lipid dalam plasma.
Kelaianan fraksi lipid yang utama adalah kenaikan kadar kolesterol total,
kolesterol Low Density Lipoprotein (LDL), trigliserida, serta penurunan
kadar kolesterol High Density Lipoprotein (HDL) (Jellinger dkk, 2012).
Menurut klasifikasi National Cholesterol Education Panel Adult
Treatment Panel (NCEP-ATP) ke III kriteria dislipidemia adalah penurunan
kadar kolesterol HDL ≤ 40 mg/dl, peningkatan kadar kolesterol LDL ≥ 100 mg/dl, peningkatan kadar kolesterol total ≥ 200 mg/dl, peningkatan kadar trigliserida ≥ 150 mg/dl (Grundy dkk, 2002).
II.3.2. Kolesterol Total
Penelitian yang dilakukan di Amerika, pada laki-laki berusia antara
35 dan 57 tahun, risiko kematian akibat perdarahan intrakranial adalah
tiga kali lebih tinggi pada mereka dengan kolesterol total kurang dari 4,13
mmol/L daripada orang dengan kadar yang lebih tinggi. Orang
Jepang-Amerika di Hawaii, insiden perdarahan intraserebral adalah meningkat
2,55 kali lipat pada pria dengan kolesterol total kurang dari 4,89 mmol/L
(Suh dkk, 2001).
II.3.3. Kolesterol Low Density Lipoprotein (LDL)
Low Density Lipoprotein (LDL) dianggap sebagai salah satu faktor
risiko kardiovaskular yang lebih penting, dan LDL dikenal memiliki potensi
memulai peradangan dan pembentukan plak dalam dinding pembuluh
darah, yang menghambat aliran darah di arteri. Kolesterol LDL
adalahfaktor yang kuat dalam reaki oksidasi daripada kolesterol total dan
kolesterol HDL, dimana mengendalikan kadar kolesterol LDL pada pasien
dengan stroke iskemik dapat memperbaiki prognosis mereka (Tian dkk,
2014).
II.3.4. Kolesterol High Density Lipoprotein (HDL)
Kolesterol High Density Lipoprotein (HDL) sebagai antioksidan,
memainkan peran penting dalam patogenesis stroke iskemik akut dengan
menghambat oksidasi fosfolipid dan aktivitas LDL yang dimodifikasi. Hal
ini juga ditetapkan bahwa peningkatan kadar dan/atau fungsi HDL dan
apolipoprotein dapat melindungi pembuluh darah besar terhadap cedera
(Tian dkk, 2014).
Pada penelitian selama 10 tahun yang dilakukan di Jepang, pria
dan wanita menunjukkan bahwa kadar kolesterol HDL rendah (< 30 mg/dL
[0,78 mmol/L]) menyebabkan dan secara independen meningkatan risiko
stroke secara signifikan, terutama stroke iskemik. Selain itu, penelitian The
Copenhagen City Heart Study mengungkapkan bahwa kolesterol HDL
terkait dengan insiden stroke non-hemoragik Relative Risk (RR), 1,18 tiap
penurunan 10 mg/dL [0,26 mmol/L]). Pasien dengan rendahnya kadar
kolesterol HDL menunjukkan 3 kali risiko lebih tinggi pada semua stroke
II.3.5. Trigliserida
Meskipun mekanisme hubungan antara kadar trigliserida dan
perdarahan intraserebral tidak diketahui, ada beberapa penjelasan yang
mungkin. Beberapa penelitian mengatakan bahwa kadar trigliserida tinggi
mendukung keadaan prothrombotik karena memiliki hubungan yang positif
dengan vitamin K bergantung faktor koagulasi VII dan IX, dan dengan
penghambatan aktivitas plasminogen dan viskositas darah (Wieberdink
dkk, 2011).
II.3.6. Rasio Kolesterol Total/ High Density Lipoprotein (HDL)
Terdapat bukti bahwa rasio kolesterol total/HDL adalah prediktor
signifikan penyakit kardiovaskular, dan prediksi risiko yang lebih kuat
daripada kolesterol total atau kolesterol HDL sendiri. Namun, hubungan
kolesterol total, kolesterol HDL dan rasio kolesterol Total/HDL dengan
resiko jenis stroke kurang jelas. Beberapa penelitian telah menemukan
bahwa peningkatan kolesterol total dapat meningkatkan risiko semua
stroke dan terutama risiko stroke iskemik, sedangkan penelitian lain telah
menemukan tidak ada hubungan atau terdapat hubungan yang lemah
pada risiko stroke (Zhang dkk, 2012).
II.3.7. Dislipidemia Terhadap Risiko Stroke
Bukti hubungan kausal profil lipid dan stroke tidak konsisten dan
kebanyakan studi skala besar risiko kolesterol dan stroke tidak
membedakan antara stroke iskemik dan hemoragik (Bharosay dkk, 2014).
Dalam penelitian yang dilakukan oleh Tian dkk (2014), kadar
kejadian stroke iskemik akut. Dislipidemia merupakan faktor risiko besar
untuk PJK tetapi perannya dalam patogenesis stroke iskemik masih belum
jelas. Dilaporkan oleh Kurt dkk (2007) dan Shahar dkk (2003) bahwa
kadar kolesterol total, kolesterol LDL, dan kolesterol HDL yang terkait
dengan faktor risiko untuk stroke iskemik.
Shahar dkk (2003) dan Bowman dkk (2003) melaporkan kurangnya
hubungan antara lipid dan stroke. Dari 296 penderita stroke dan kontrol,
menemukan bahwa kadar kolesterol total, trigliserida maupun kolesterol
HDL dikaitkan dengan risiko stroke iskemik, meskipun rasio total
kolesterol/kolesterol HDL yang tinggi meningkatkan risiko (Bowman dkk
(2003).
II.4. MEROKOK
II.4.1. Definisi
Merokok adalah menghisap rokok, dimana rokok merupakan salah
satu produk tembakau yang dimaksudkan untuk dibakar dan dihisap
dan/atau dihirup asapnya, termasuk rokok kretek, rokok putih, cerutu atau
bentuk lainnya yang dihasilkan dari tanaman nicotiana tabacum, nicotiana
rustica, dan spesies lainnya atau sintetisnya yang asapnya mengandung
nikotin dan tar, dengan atau tanpa bahan tambahan (Peraturan
Pemerintah Republik Indonesia, 2012).
Tembakau menyebabkan penyakit dan bertanggung jawab dalam
kematian yang terjadi di negara-negara dengan penghasilan tertinggi
seperti Amerika Serikat maupun di dunia global (Jha dkk, 2014). Secara
drastis setelah usia 65 tahun, ini secara langsung berhubungan dengan
penyakit yang berkaitan dengan merokok (Shah dan Cole, 2010).
Perokok dapat dibagi menjadi perokok ringan (1-9 batang per hari),
perokok moderat (20-39 batang per hari), perokok berat (> 40 batang
rokok per hari) (Agus dan Tjahyana, 2011). Sedangkan berdasarkan
waktunya menurut National Health Interview Survey (NHIS) tahun 2007
dapat dibagi menjadi current smoker adalah merokok > 100 batang
selama hidupnya, setiap harinya, atau beberapa hari. Former smoker
adalah seseorang yang merokok > 100 batang selama hidupnya, dan
sekarang sudah berhenti merokok. Never smoker adalah seseorang yang
tidak pernah merokok ≥ 100 batang selama hidupnya (Ponniah, 2008).
II.4.2. Rokok Terhadap Risiko Stroke
Penelitian yang dilakukan oleh Shah dan Cole (2010) yang
dilakukan pada seluruh etnis dan populasi menunjukkan sebuah
hubungan yang kuat antara merokok dan risiko stroke, dimana perokok
memiliki setidaknya dua sampai empat kali lipat terjadinya risiko stroke
dibandingkan dengan bukan perokok atau individu yang telah berhenti
merokok lebih dari 10 tahun sebelumnya.
Dalam satu studi Zhang dkk (2005) pada 526 kasus stroke yang
dilaporkan bahwa wanita yang tinggal bersama suami yang merokok
dapat meningkatkan risiko terjadinya stroke dan prevalensi meningkat
dengan peningkatan intensitas dan durasi suami merokok. Suami
batang per hari 1,32 (95% CI: 1,01-1,72), dan ≥20 batang per hari 1,62 (95% CI: 1,28-2,05)
Berdasarkan penelitian cross sectional yang dilakukan pada 91
pasien stroke pada tahun 2013, terdiri dari 71 perokok aktif dan 41 pasien
yang berhenti merokok. Didapatkan insiden terjadinya stroke iskemik
(n=46) lebih besar daripada stroke hemoragik (n=42), hal ini disebabkan
rokok mengurangi aliran darah serebral, yang dapat meningkatkan risiko
pembentukan bekuan dan risiko stroke berikutnya melalui fenomena
perlambatan aliran atau stasis (Lahano dkk, 2014).
Selain itu karboksihemoglobinemia, peningkatan agregasi
trombosit, peningkatan kadar fibrinogen, berkurangnya kolesterol HDL,
dan efek toksik langsung dari senyawa seperti 1,3-butadiena, dapat
mempercepat aterosklerosis dalam hewan model. Paparan asap
tembakau pada percobaan juga telah dikaitkan dengan perkembangan
aterosklerosis yang diukur dengan ultrasound model B pada dinding arteri
karotis, juga pada kerusakan awal arteri pada dilatasi endotelium arteri
brakialis. Pada akhirnya, patogenesis terjadinya stroke meningkat pada
populasi yang terpapar asap rokok disertai dengan proses aterogenesis
(Shah dan Cole, 2010).
II.5. ASAM URAT
II.5.1. Definisi
Asam urat adalah produk akhir degradasi nukleotida purin, yang
5-phosphoribosyl-1-pyrophosphate (PRPP) menjadi determinan mayor
biosintesis asam urat (Fauci dkk, 2009).
Kadarnya normal bila dalam rentang 2,5-8 mg/dl pada pria dan
1,5-6,0 mg/dl pada wanita (Kratz dkk, 2004). Belum ada kadar yang diterima
secara universal, namun biasanya didefinisikan sebagai hiperurisemia bila
kadar asam urat > 6,8 mg/dL (Kim dkk, 2009).
II.5.2. Asam Urat Terhadap Risiko Stroke
Dalam penelitian prospektif selama 12-15 tahun pada 5700 laki-laki
dan perempuan dari populasi umum dengan menyingkirkan faktor risiko
diabetes melitus dan penyakit kardiovaskular, dalam 87 µmol/L
peningkatan serum asam urat secara signifikan berhubungan dengan
peningkatan stroke iskemik (31%) pada laki-laki, menyebabkan
peningkatan risiko kematian pada laki-laki (11%) dan perempuan (16%).
Hal ini disebabkan serum asam urat memilik dampak yang
membahayakan dalam fungsi platelet dan menyebakan disfungsi endotel
(Storhaug dkk, 2013).
Menurut Vannorsdall dkk (2008) peningkatan serum asam urat
berhubungan dengan stroke iskemik disebabkan oleh kegagalan tonus
vaskular dan disfungsi endotel yang menyebabkan terbentuknya iskemik
pada akhirnya cairan serebropinal melewati blood brain bariier dan
menyebabkan edema.
Penelitian oleh Chen dkk (2009) pada pasien penyakit
kardiovaskular dan stroke iskemik dengan rata-rata usia ± 51,5-11,5
dari peserta, dengan dominasi laki-laki (39,7% pria, wanita 11.3%). kadar
asam urat serum meningkat seiring pertambahan usia pada wanita tetapi
tidak pada pria. Kadar asam urat meningkat pada 81.3% laki-laki antara 5
dan 9 mg/dl, tetapi kebanyakan wanita (88.8%) memiliki kadar asam urat
< 7 mg / dl.
Zhang dkk (2010) melakukan penelitian tentang hubungan antara
kadar asam urat dengan outcome klinis pada 585 pasien stroke dewasa
muda di Cina. Didapatkan bahwa kadar asam urat yang rendah lebih
banyak dijumpai pada pasien stroke derajat berat (p=0,02). Pasien
dengan infark serebri yang disebabkan oleh sumbatan pada pembuluh
darah kecil memiliki kadar asam urat yang lebih tinggi (p=0,01) dan skor
mRS yang lebih rendah (p<0,01), dan sebaliknya kadar asam urat yang
paling rendah dan skor mRS yang tertinggi dijumpai pada pasien dengan
infark serebri kardiogenik.
II.6. OBESITAS
II.6.1. Definisi
Menurut The Practical Guide: Identification, Evalution, and
Treatment of Overweight and Obesity in Adults obesitas adalah apabila
Indeks Massa Tubuh (IMT) ≥ 30 kg/m2 dimana obesitas ini merupakan salah satu isu kesehatan global yang paling serius (Wadden dkk, 2002).
Prevalensi obesitas telah meningkat selama 2 dekade. Pada tahun
2008, 1,5 milyar orang dewasa (umur ≥20 tahun) adalah overweight dan lebih dari 200 juta orang dan hampir 300 juta wanita adalah obes dimana
abdominal fat, indeks massa tubuh, serta lingkar pinggang dan panggul
(Hussein dkk, 2012).
II.6.2. Klasifikasi
Indeks Massa Tubuh yaitu suatu pengukuran antropometrik
sederhana dimana berat badan dibagi dengan kuadrat tinggi badan, yang
merupakan suatu alat skrining untuk overweight dan obesitas yang paling
sering digunakan. Indeks Massa Tubuh sering digunakan karena
berkaitan erat dengan kadar lemak tubuh. Pengukurannya relatif mudah
dan murah serta merupakan suatu metode yang non invasif untuk menilai
status gizi seseorang (Duncan dkk, 2009; Bigaard dkk, 2005).
Indeks Massa Tubuh merupakan metode pengukuran yang
direkomendasikan oleh World Health Organization (WHO) untuk menilai
massa lemak tubuh. Dimana Indeks Massa Tubuh menghasilkan suatu
pengukuran total lemak tubuh yang lebih akurat bila dibandingkan dengan
pengukuran berat badan saja (Wadden dkk, 2002).
Indeks Massa Tubuh dapat dinilai dari hasil berat badan (BB) dalam
kilogram (kg) dibagi dengan kuadrat tinggi badan (TB) dalam meter (m).
Dapat disederhanakan dalam rumus berikut (Wadden dkk, 2002; Suyono
dkk, 2011).
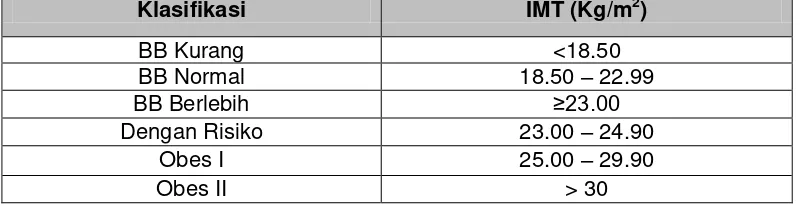
Tabel 4. Klasifikasi IMT berdasarkan WHO dalam The Asia-Pacific Perspective : Redifining Obesity and Its Treatment
Klasifikasi IMT (Kg/m2)
BB Kurang <18.50
BB Normal 18.50 – 22.99
BB Berlebih ≥23.00
Dengan Risiko 23.00 – 24.90
Obes I 25.00 – 29.90
Obes II > 30
Dikutip dari : Suyono S, Waspadji S, Soegondo S, Soewondo P, Subekti I, Semiardji G, dkk. 2011. Konsensus Pengelolaan dan Pencegahan Diabetes Melitus Tipe 2. Perkumpulan Endokrinologi Indonesia.
II.6.3. Obesitas Terhadap Risiko Stroke
Obesitas dan stroke adalah dua masalah utama kesehatan
masyarakat di seluruh dunia, obesitas dan khususnya obesitas abdomen
berperan utama dalam patogenesis beberapa metabolik, jantung dan
gangguan medis serebrovaskular (Hussein dkk, 2012).
Jaringan adiposa tidak lagi dilihat sebagai sebuah repositori pasif
untuk penyimpanan triasilgliserol dan menjadi sumber asam lemak bebas
(Free Fatty Acids / FFAs). Pre-adiposit berkembang menjadi adiposit
matur. Adiposit matur merupakan organ parakrin dan endokrin aktif yang
mensekresi sejumlah mediator untuk proses metabolisme. Senyawa yang
mempengaruhi adipogenesis diantaranya lipoprotein lipase, cholesterol
ester transfer protein, angiotensinogen, faktor komplemen, interleukin-6
(IL-6), prostaglandin, Tumor Necrosis Factor-alpha (TNF-), dan NO (Smith dan Minson, 2012).
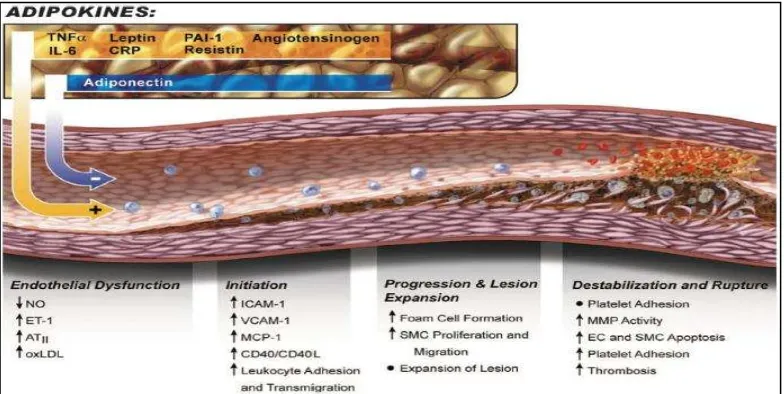
Jaringan adiposa diakui sebagai sumber yang kaya mediator
proinflamasi yang dapat langsung menyebabkan cedera atau injuri
pro-inflamasi atau adipokin diantaranya TNF-, IL-6, leptin, Plasminogen Activator Inhibitor-1 (PAI-1), angiotensinogen, resistin, dan C-Reactive
Protein (CRP) (Gambar 3). Di sisi lain, NO dan adiponektin memberikan
perlindungan terhadap inflamasi dan resistensi insulin yang berkaitan
dengan obesitas (obesity-linked insulin resistance) (Smith dan Minson,
2012).
Gambar 3. Adipokin Anti- dan Pro-Inflamatori.
Diunduh dari : Smith, M., M., Minson, C., T., 2012. Obesity and Adipokines: Effect on Sympathetic Overactivity. J Physiol. 590 (8);1787-1801.
II.7. DIABETES MELITUS
II.7.1. Definisi
Menurut American Diabetes Association (ADA) tahun 2010,
diabetes melitus merupakan suatu kelompok penyakit metabolik dengan
karakteristik hiperglikemia yang terjadi karena kelainan sekresi insulin,
kerja insulin, atau kedua – duanya (Suyono dkk, 2011).
Diabetes Melitus (DM) adalah suatu penyakit metabolik yang
peningkatan frekuensi buang air kecil, dan peningkatan rasa haus serta
lapar (Zychowska dkk, 2013; Tjokroprawiro, 2007).
II.7.2. Klasifikasi
Diabetes melitus diklasifikasikan berdasarkan etiologinya menjadi
empat jenis yaitu diabetes melitus tipe 1, diabetes melitus tipe 2, tipe
spesifik lainnya, dan gestasional diabetes seperti yang terlihat pada tabel
5 di bawah ini. Diabetes melitus tipe 1 adalah diabetes yang
dikarakteristikan dengan defisiensi insulin yang berkaitan dengan lesi
destruktif pada sel β pankreas, biasanya terjadi pada usia muda, tetapi dapat terjadi pada semua usia. Diabetes melitus tipe 2 adalah diabetes
yang disebabkan oleh kombinasi dari penurunan sekresi insulin dan
sensitivitas terhadap insulin. Tahap awal dari diabetes melitus tipe 2
dikarakteristikan oleh resistensi insulin sehingga menyebabkan
peningkatan kadar glukosa post-prandial. Biasanya terjadi pada dewasa,
di mana penderita diabetes tipe ini umumnya mengalami obesitas dan
kurang beraktivitas (Ryden dkk, 2007).
Tabel 5. Klasifikasi Diabetes Melitus Berdasarkan Etiologinya
JENIS DIABETES ETIOLOGI
Diabetes tipe 1 Destruksi sel β pankreas sehingga terjadi defisiensi insulin absolut
yang dapat disebabkan oleh proses autoimun ataupun idiopatik
Diabetes tipe 2 Disebabkan oleh berbagai hal, mulai dari resistensi insulin disertai defisiensi insulin relatif sampai gangguan sekresi insulin disertai resistensi insulin
Diabetes tipe spesifik lainnya
Defek genetik fungsi sel β pankreas
Defek genetik kerja insulin
Penyakit eksokrin pankreas
Endokrinopati
Paparan obat atau zat kimia
Infeksi
Imunologi yang jarang
Sindrom genetik lain yang berkaitan dengan diabetes melitus
Gestasional diabetes
II.7.3. Diagnosis
Diagnosis diabetes melitus ditegakkan atas dasar pemeriksaan
kadar glukosa darah. Diagnosis tidak dapat ditegakkan atas dasar adanya
glukosuria. Untuk menentukan diagnosis dari diabetes melitus perlu
dilakukan pemeriksaan kadar glukosa darah secara enzimatik dengan
bahan darah plasma vena. Penggunaan bahan darah utuh (whole blood),
vena, ataupun kapiler tetap dapat dipergunakan dengan memperhatikan
angka – angka kriteria diagnostik yang berbeda sesuai pembakuan oleh WHO. Sedangkan untuk tujuan pemantauan hasil pengobatan dapat
dilakukan dengan menggunakan pemeriksaan glukosa darah kapiler
dengan glukometer (Suyono dkk, 2011).
Berbagai keluhan dapat ditemukan pada penderita diabetes
melitus. Kecurigaan adanya diabetes melitus perlu dipikirkan apabila
terdapat keluhan klasik seperti poliuria, polidipsia, polifagia, dan
penurunan berat badan yang tidak dapat dijelaskan sebabnya. Keluhan
lain dapat berupa lemah badan, kesemutan, gatal, mata kabur, dan
disfungsi ereksi pada pria, serta pruritus vulvae pada wanita (Suyono dkk,
2011).
Diagnosis dari diabetes melitus dapat ditegakkan melalui tiga cara
seperti yang terangkum dalam tabel 6 di bawah ini. Pertama jika keluhan
klasik ditemukan, maka pemeriksaan glukosa plasma sewaktu > 200
mg/dL sudah cukup untuk menegakkan diagnosis diabetes melitus. Kedua
Meskipun TTGO dengan beban 75 g glukosa lebih sensitif dan spesifik
dibanding dengan pemeriksaan glukosa plasma puasa, namun
pemeriksaan ini memiliki keterbatasan tersendiri. TTGO sulit untuk
dilakukan berulang – ulang dan dalam praktek sangat jarang dilakukan karena membutuhkan persiapan khusus. Pemeriksaan Hemoglobin A1c
(HbA1c) juga telah direkomendasikan oleh ADA pada tahun 2011 sebagai
salah satu kriteria dalam mendiagnosis diabetes melitus. Kadar HbA1c ≥ 6,5 % yang pemeriksaannya dilakukan pada sarana laboratorium yang
telah distandarisasi menjadi salah satu kriteria dalam mendiagnosis
diabetes melitus (Suyono dkk, 2011).
Tabel 6. Kriteria Diagnosis Diabetes Melitus
KRITERIA KETERANGAN
1 Gejala klasik diabetes + Kadar glukosa plasma sewaktu ≥ 200 mg/dL (11,1 mmol/L)
Keterangan : glukosa plasma sewaktu merupakan hasil pemeriksaan sesaat pada suatu hari tanpa memperhatikan waktu makan terakhir
2 Gejala klasik diabetes + Kadar glukosa plasma puasa ≥ 126 mg/dL (7,0 mmol/L)
Keterangan : Puasa diartikan penderita tidak mendapat kalori tambahan sedikitnya 8 jam
3 Kadar glukosa plasma 2 jam pada TTGO ≥ 200 mg/dL (11,1 mmol/L)
Keterangan : TTGO yang dilakukan dengan standar WHO, menggunakan beban glukosa yang setara dengan 75 gram glukosa anhidrus yang dilarutkan dalam air
* Pemeriksaan kadar HbA1c ≥ 6,5 % pada sarana laboratorium yang telah terstandarisasi dengan baik
Dikutip dari : Suyono S, Waspadji S, Soegondo S, Soewondo P, Subekti I, Semiardji G, dkk. 2011. Konsensus Pengelolaan dan Pencegahan Diabetes Melitus Tipe 2 Di Indonesia 2011. Perkumpulan Endokrinologi Indonesia.
II.7.4. Diabetes Melitus Terhadap Risiko Stroke
Diabetes Melitus (DM) merupakan risiko mayor pada stroke dan
berhubungan dengan meningkatnya angka mortalitas. Telah dikemukakan
didapatkan 2,5 - 3,5 kali lebih tinggi pada DM dibandingkan bukan DM dan
risiko relatif dari stroke pada pasien dengan DM mencapi maksimum pada
grup umur muda 40-55 tahun dan proporsi wanita lebih besar sehingga
sangat penting untuk mendeteksi dan mengobati pasien DM usia muda
dan wanita sedini mungkin (Basjiruddin, 2009).
Pada penelitian berbasis populasi di Finland, DM merupakan faktor
risiko untuk infark serebri dengan RR 3,26 dengan topik di subkortikal atau
infark lakunar akibat kelainan vaskular yang kecil sesuai dengan
patofisiologi stroke pada DM, sedangkan perdarahan intraserebral atau
subaraknoid jarang dijumpai (Zafar dkk, 2007).
Walaupun hubungan erat antara DM dan penyakit vaskular belum
dimengerti secara jelas, hilangnya peranan pengubahan pengaturan dari
endotel dapat dilibatkan dalam patogenesis komplikasi vaskular pada DM.
Patogenesis ini tampaknya berhubungan dengan beban glikasi
(glucosetoxicity) dan oksidasi berlebihan, gangguan fungsi endotel,
kegagalan fibrinolisis, dan resistensi indulin selanjutnya diikuti dengan
komplikasi makrovaskular (Basjiruddin, 2009).
Pada DM yang lama juga akan terjadi ketidakseimbangan antara,
faktor vasodilator dan konstriktor, mediator tromboik dan fibrinolitik, serta
bahan-bahan penghambat dan perangsang pertumbuhan yang berkaitan
dengan penurunan produksi pelepasan dan atau aktifasi NO yang pada
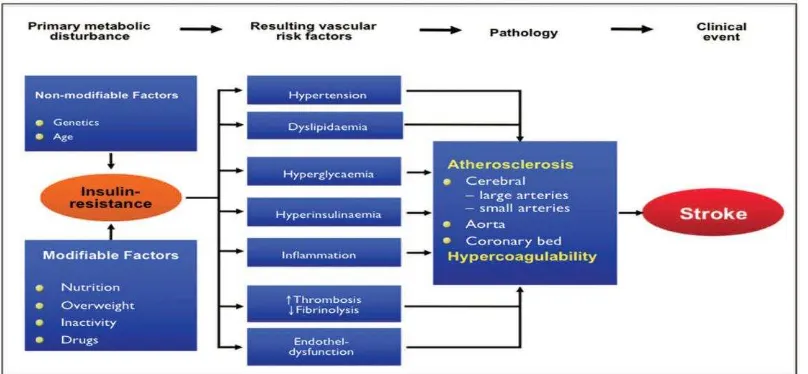
Gambar 4. Insulin Resisten dan Perkembangannya Menjadi Stroke
Dikutip dari : Sander, D., Sander, K., Poppert, H. 2008. Stroke In Type 2 Diabetes. British Journal of Diabetes and Vascular Disease. 8: 222-229.
Capes dkk melaporkan stress hiperglikemi menjadi prediksi risiko
kematian yang lebih tinggi paska stroke dan rendahnya perbaikan
fungsional pada pasien yang bertahan hidup lebih lama. Pada pasien
dengan kadar glukosa darah puasa lebih dari 13,4 mmol/L dan kadar
HBA1c lebih dari 10% risiko stroke kira-kira lebih tinggi 2 kali lipat
dibandingkan dengan kontrol metabolik baik. Terdapat hubungan yang
bermakna antara peningkatan kadar glukosa puasa, postprandial, dan
HBA1c dan insiden stroke, yang tidak tergantung pada faktor tradisional
kardiovaskular lainnya dengan tipe diabetes melitus tipe 2 (Basjiruddin,
2009).
II.8. RIWAYAT STROKE DALAM KELUARGA
II.8.1. Riwayat Stroke Dalam Keluarga Terhadap Risiko Stroke
Menurut Mvundura dkk (2010) riwayat stroke dalam keluarga
merupakan faktor independen terjadinya stroke 4 kali lipat pada orang
dalam keluarga sedang atau rendah. Penelitian ini mendefinisikan risiko
dalam keluarga menjadi tiga: tinggi, sedang, rendah.
Risiko tinggi jika terjadinya stroke akut pada satu atau lebih kerabat
pertama (ibu, ayah, atau saudara kandung), dua atau lebih kerabat
kedua (bibi, paman, atau kakek--nenek), sedikitnya satu kerabat
kedua dengan stroke akut dan dua atau lebih kerabat kedua
dengan stroke lama.
Risiko sedang jika kerabat pertama dengan stroke lama, kerabat
pertama dengan stroke lama dan kerabat kedua dengan stroke
akut, hanya satu kerabat pertama dan kerabat kedua mengalami
stroke lama, dua atau lebih kerabat kedua dengan stroke lama.
Risiko rendah jika tidak dijumpai riwayat stroke dalam keluarga
pada setiap onset atau riwayat keluarga yang tidak diketahui, hanya
satu kerabat kedua dengan stroke lama dari kedua garis keturunan,
satu dari kerabat kedua dengan stroke akut dari kedua garis
keturunan.
Hasil dari studi kasus kontrol dan kasus-kasus sebelumnya
menunjukkan bahwa riwayat keluarga positif stroke (FHstroke) merupakan
faktor risiko independen untuk terjadinya stroke lakunar. Fenotip stroke
lakunar dapat dibedakan berdasarkan adanya patogenesis infark
asimtomatik lakunar yaitu lesi iskemik pada white matter atau perdarahan
otak (microbleeds). Penelitian tentang riwayat keluarga berperan sebagai
faktor risiko stroke. Penelitian di mana stroke telah diklasifikasikan oleh
keluarga positif stroke adalah faktor risiko independen untuk stroke
lakunar, terutama pada pasien usia muda (Knottnerus dkk, 2011).
Pada manusia, penelitian pada manusia kembar telah
menunjukkan bahwa riwayat keluarga positif stroke adalah faktor risiko
untuk stroke, kembar monozigot lebih cenderung menjadi penyerta
daripada kembar dizigot (OR, 1,65; 95% CI 1.2 hingga 2.3) (Flossmann
dkk, 2004).
Menurut penelitian Seshadri dkk (2010) penderita stroke usia
kurang dari 65 tahun meningkatkan risiko empat kali lipat terjadinya stroke
pada keturunannya (HR 3.79; 95% CI 1.90–7.58) sedangkan penderita dengan stroke usia lebih dari 65 tahun meningkatkan risiko hanya dua kali
II.9. KERANGKA TEORI
Dislipidemia Asam Urat Diabetes Melitus
Hipertensi Obesitas
Aterosklerosis lebih dari separuh kematian di negara-negara maju di Barat. Penyakit arteri yang berkembang secara perlahan, dengan penebalan intima
penumpukan fibrosa yang secara bertahap akan menyempitkan lumen dan secara bertahap tempat perdarahan dan pembentukan trombus (Silbernagl dan Lang, 2007).
Penelitian yang dilakukan oleh Suh dkk, yang menilai risiko relatif kejadian stroke hemoragik terhadap hipertensi derajat III di Korea menunjukkan 33,3 % dibandingkan pasien dengan tensi normal (Sturgeon dkk, 2007).
Sebagian besar pasien di Pakistan dengan stroke memiliki penyakit komorbiditas seperti hipertensi, diabetes melitus, rokok, dislipidemia, dan obesitas. Dalam penelitian ini, tekanan darah tinggi adalah faktor risiko untuk stroke iskemik yang lebih dari stroke hemoragik. (Lahano dkk, 2014)
Penumpukan fibrosa menyempitkan lumen iskemik dan kekauan dinding pembuluh darah, pembentukan trombus yang menyumbat lumen emboli perifer serta perdarahan ke dalam plak
Merokok disebabkan oleh sumbatan pada pembuluh darah kecil memiliki kadar asam urat yang lebih tinggi proporsi wanita lebih besar sehingga sangat penting untuk untuk infark serebri dengan Relative Risk 3,26 dengan Penelitian yang dilakukan di
Amerika, pada laki-laki berusia plak dalam dinding pembuluh darah, yang menghambat aliran darah di arteri (Tian dkk, 2014).
II.10. KERANGKA KONSEP
Stroke
Merokok
Dislipidemia Asam Urat Diabetes Melitus
Hipertensi Riwayat Stroke
Dalam Keluarga Obesitas