111
PENGARUH DOSIS DAN LAMA PEMBERIAN EKSTRAK ETANOL PEGAGAN
(
Centella asiatica) TERHADAP KADAR GULA DARAH DAN DERAJAT INSULITIS
TIKUS MODEL DIABETES MELITUS TIPE 2
The Effect of Ethanol Extract of Centella asiatica
on Blood Glucose Level and
Degree of Insulitis on Rats Diabetes Melitus Type 2
Fitria Dhenok Palupi1,2*, Brian Wasita2,3, Adi Magna Patriadi Nuhriawangsa3,4 1 Program Diploma III Gizi, Politeknik Kesehatan TNI AU Adisutjipto, Jl. Majapahit (Janti) Blok-R, Lanud Adisutjipto, Yogyakarta, Indonesia 2Clinical Nutrition, Ilmu Gizi, Pascasarjana Universitas Sebelas Maret 3 Bagian Patologi Anatomi, Fakultas Kedokteran Universitas Sebelas Maret
4Program Studi Peternakan, Fakultas Pertanian Universitas Sebelas Maret Jl. Ir. Sutami 36A, Surakarta, Indonesia
*e-mail: fitria.dhenok@gmail.com
Submitted: June 4th, 2018, revised: October 26th, 2018, approved: November 13th, 2018 ABSTRACT
Background. Diabetes mellitus is a major public health problem with an increasing prevalence each year. Insulitis is an inflammatory pathophysiologic state of the pancreatic langerhans island that plays an important role in maintaining blood glucose homeostasis and correlates with the development of type 2 diabetes mellitus. Centella asiatica is a plant containing antioxidant pentacyclic triterpenes that have antioxidant, antiinflammatory, and antimicrobial activity.
Objective. To analyze the effect of ethanol extract of Centella asiatca on blood glucose level and degree of insulitis on Wistar male rat induction sreptozotocin-nicotinamide. Methods. This study consisted of six treatments: normal control (K-), diabetes control (K+), ethanol extract of Centella asiatica dose 300 mg/ kg bodyweight (P1), ethanolic extract of Centella asiatica dose 600 mg/ kg bodyweight (P2), ethanol extract of Centella asiatica dose 1.200 mg/ kg bodyweight (P3), and metformin drug dose 45 mg/ kg bodyweight (P4), rats terminated for 28 days and 35 days in laboratory of PSPG UGM Yogyakarta. Statistical analysis using analysis of variance (ANOVA) and advanced test using Duncan multiple range test (DMRT) to determine the difference between control group and treatment group. Result. The result showed that the extract of ethanol contains asiaticoside active substance and antioxidant activity 86.81%. Administration of ethanol extract of pegagan decreased blood glucose level for 28 days (p= 0.001) and 35 days (p= 0,001). Provision of ethanol extract of pegagan decreased the degree of insulitis at 35 days (0.008), but not significant at 28 days (p= 0.368). Conclusion. Provision ethanol extract of Centella asiatica dose 600 mg/kg bodyweight most efficient in lowering blood glucose level and degree of insulitis so as to prevent hyperglycemia and inflammation condition than oral antidiabetic drug with side effect.
Keywords: blood glucose level, Centella asiatica, diabetes mellitus type 2, inflammation ABSTRAK
Latar Belakang. Diabetes melitus merupakan masalah utama kesehatan masyarakat dengan
prevalensi yang meningkat tiap tahun. Insulitis merupakan keadaan patofisiologis inflamasi
dari pulau langerhans pankreas yang berperan penting dalam mempertahankan homeostasis glukosa darah dan berkorelasi dengan perkembangan diabetes melitus tipe 2. Centella asiatica merupakan tanaman yang mengandung antioksidan jenis pentacyclic triterpenes yang mempunyai
aktivitas antioksidan, antiinflamasi, dan antimikroba. Tujuan. Menganalisis pengaruh pemberian ekstrak etanol pegagan terhadap kadar gula darah dan derajat insulitis tikus Wistar jantan induksi
sreptozotocin-nicotinamide. Metode. Penelitian ini terdiri atas enam perlakuan yaitu kontrol normal (K-), kontrol diabetes (K+), ekstrak etanol pegagan dosis 300 mg/kg BB (P1), ekstrak etanol pegagan dosis 600 mg/kg BB (P2), ekstrak etanol pegagan dosis 1.200 mg/ kg BB (P3), dan pemberian obat metformin dosis 45 mg/kg BB (P4), tikus diterminasi pada lama pemberian 28 hari dan 35 hari di laboratorium PSPG UGM Yogyakarta. Analisis statistik menggunakan analysis of variance (ANOVA) dan uji lanjut menggunakan Duncan multiple range test (DMRT) untuk mengetahui perbedaan antara kelompok kontrol dan kelompok perlakuan. Hasil. Hasil penelitian menunjukkan bahwa ekstrak etanol pegagan mengandung zat aktif asiaticoside dan aktivitas antioksidan 86,81%. Pemberian ekstrak etanol pegagan menurunkan kadar gula darah pada lama pemberian 28 hari (p=0,001) dan 35 hari (p=0,001). Pemberian ekstrak etanol pegagan
menurunkan derajat insulitis pada lama pemberian 35 hari (0,008), namun tidak signifikan pada
lama pemberian 28 hari (p=0,368). Kesimpulan. Esktrak etanol pegagan dosis 600 mg/kg BB paling efisien dalam menurunkan kadar gula darah dan derajat insulitis sehingga mencegah
kondisi hiperglikemia dan inflamasi dibandingkan obat oral antidiabetes dengan efek samping
yang ditimbulkannya.
Kata kunci: kadar gula darah, Centella asiatica,diabetes melitus tipe 2, inflamasi
Inflamasi dapat disebabkan karena peningkatan Reactive Oxygen Species (ROS) selama DM. ROS dapat mengaktifkan Nuclear Factor Kappa B (NF-kB) yang merupakan faktor transkripsi dalam mengatur ekspresi
gen proinflamasi seperti TNF-α, IL-6, dan CRP.
Disamping itu, kondisi DM dapat meningkatkan ketersediaan asam lemak bebas karena proses lipolisis. Peningkatan asam lemak bebas akan mengaktifkan sistem kekebalan tubuh untuk
melepaskan sitokin IL-6, TNF-α, dan ekspresi IL-1β di islet pankreas. Proses inflamasi kronik
akan menyebabkan fibrosis dan apoptosis sel-β
pankreas.8–10
Insulitis merupakan keadaan patofisiologis inflamasi dari pulau langerhans pankreas yang
berperan penting dalam mempertahankan homeostasis glukosa darah dan berkorelasi dengan perkembangan diabetes melitus.11
Inflamasi merupakan salah satu jalur penting
pada patogenesis dan komplikasi penyakit DM
tipe 2. Terapi antiinflamasi dapat menurunkan
konversi dari prediabetes menjadi diabetes dan progresivitas penyakit DM tipe 2.12 Studi pada
pasien DM tipe 2 menunjukkan bahwa terapi
antiinflamasi memperbaiki hiperglikemia dan fungsi sel-β pankreas.13
Salah satu manajemen hiperglikemik yang sering digunakan adalah penggunaan terapi obat
PENDAHULUAN
Diabetes Melitus (DM) merupakan suatu kelompok penyakit metabolik yang ditandai dengan hiperglikemia akibat kelainan sekresi insulin, kerja insulin, atau kedua-duanya.1
Kenaikan prevalensi DM diperkirakan lebih tinggi di negara berkembang dibandingkan negara maju.2 Penyakit ini merupakan masalah utama
kesehatan masyarakat, prevalensi di dunia tahun 2014 sebanyak 9 persen, di Indonesia prevalensinya meningkat dari 1,1 persen (2007) menjadi 2,4 persen pada tahun 2013. Sebanyak 31 provinsi (93,9 %) menunjukkan kenaikan prevalensi DM yang cukup berarti. DM menjadi salah satu penyebab 82 persen kematian di seluruh dunia dari total penyakit tidak menular. Di Indonesia terjadi 6 persen kematian akibat DM dari total 1.551.000 kematian.3–5
Pasien DM akan mengalami hiperglikemia
yang menyebabkan respon senyawa inflamasi
melalui mediasi sitokin. Sitokin akan merusak sensitivitas insulin dan keseimbangan glukosa.6
Inflamasi terjadi setelah terjadi peningkatan
glukosa darah yang ditandai dengan peningkatan marker peradangan yaitu C Reactive Protein (CRP), interleukin (IL)-6, IL-18, IL-1β, dan Tumor Necrosis Factor Alfa (TNF-α).7
113 113 oral dan injeksi insulin.14 Terapi menggunakan
obat oral menimbulkan berbagai efek samping. Obat metformin menimbulkan gangguan gastrointestinal seperti kembung, mual, muntah, dan diare serta mengurangi penyerapan vitamin B12 di usus halus. Obat vildagliptin dan alogliptin menyebabkan disfungsi hati.15 Oleh sebab itu,
diperlukan agen terapi baru melalui penggunaan sediaan herbal yang efektif, relatif lebih murah, rendah efek samping dan toksisitas.16
Pegagan (Centella asiatica) merupakan tanaman yang mengandung antioksidan dengan komponen utama pentacyclic triterpenes (asam asiatic, asam madecassic, asiaticoside, dan
madecassoside). Pegagan terbukti mempunyai aktivitas antioksidan, antiinflamasi, dan antimikroba.17 Daun pegagan juga mengandung
klorofil yang berpeluang dikembangkan sebagai
bahan suplemen pangan atau pangan fungsional. Ekstrak etanol daun pegagan dosis 300 mg/kg BB selama 28 hari terbukti menurunkan kadar gula darah dan lipid serta meningkatkan produksi insulin pada tikus diabetes melitus tipe 2.18 Studi
pada tikus induksi emulsi lipid menunjukkan bahwa ekstraksi pegagan menggunakan etanol 80 % dosis 1000 mg dan 2000 mg menurunkan kadar glukosa plasma, trigliserida, dan kolesterol total.19
Tanaman pegagan mengandung antioksidan di seluruh bagian tanaman mulai daun sampai akar.20 Senyawa aglikon triterpen dalam pegagan
bersifat nonpolar yang apabila berikatan dengan 3 molekul gula masih tetap kecil kelarutannya dalam air dan lebih larut dalam etanol 70 %.21
Proses ekstraksi menggunakan etanol terbukti lebih baik dibandingkan dengan metanol dan air. Etanol dapat melarutkan dengan baik senyawa aglikon triterpen terutama kandungan fenolik, asiaticoside, dan madecassoside.22
Lama pemberian ekstrak pegagan selama 28 hari terbukti memberikan efek antihiperglikemik.23
Hal ini sejalan dengan penelitian Muchtaromah
et al. bahwa pemberian ekstrak pegagan
selama 28 hari lebih efektif dibandingkan 42 hari dalam memperbaiki histopatologi otak tikus DM. Interaksi antara dua variabel yaitu lama pemberian dan bentuk sediaan dalam penelitian
tersebut tidak berpengaruh secara signifikan.24
Oleh sebab itu, maka peneliti menggunakan lama pemberian 28 hari dan 35 hari.
Berdasarkan berbagai permasalahan di atas yaitu peningkatan prevalensi diabetes dan adanya efek samping terapi obat kimia, maka diperlukan pengembangan agen terapi baru menggunakan tanaman pegagan. Selain itu, peningkatan permintaan terhadap sediaan
herbal antidiabetes terutama penduduk di negara berkembang ikut melatarbelakangi penelitian ini.25,26 Tujuan penelitian adalah menganalisis
pengaruh dosis dan lama pemberian ekstrak etanol pegagan (Centella asiatica) pada keseluruhan tanaman terhadap kadar gula darah dan derajat insulitis tikus diabetes melitus tipe 2 induksi streptozotocin (STZ) 65 mg/kg berat badan dan nicotinamide (NA) 230 mg/kg berat badan.
METODE
Desain Penelitian, Waktu, dan Tempat Penelitian
Penelitian ini merupakan jenis penelitian eksperimental laboratorik pada hewan coba tikus dengan post test with control group. Rancangan percobaan yang digunakan adalah Rancangan Acak Lengkap (RAL) Faktorial yaitu dosis dan lama pemberian ekstrak etanol pegagan. Pembuatan dan analisis ekstrak pegagan dilakukan di Lembaga Penelitian dan Pengujian Terpadu (LPPT) Unit 1 Universitas Gadjah Mada Yogyakarta. Pemeliharaan dan perlakuan hewan coba dilakukan di Unit Pemeliharaan Hewan Percobaan (UPHP) Universitas Gadjah Mada Yogyakarta. Penelitian dilaksanakan pada bulan Februari-Agustus tahun 2017.
digital analitik dengan satuan miligram, bekker glass 250 cc, kabinet driyer, ultraturaq, vacum rotary evaporator, waterbath, cawan porselin, vortex, sentrifugator, plate silikagel F254, dan spektrofotometer Vitalab micro.
Tahap Penelitian
Tanaman pegagan diperoleh dari Merapi Farma Herbal, Kaliurang, Provinsi Daerah Istimewa Yogyakarta. Simplisia keseluruhan tanaman pegagan mulai akar dan daun diekstrak menggunakan etanol 70% dengan metode
remaserasi menurut modifikasi Nugroho et al.
serta Pramono dan Adjiastuti.21,27 Standarisasi
ekstrak etanol pegagan pada penelitian ini yaitu mengandung zat aktif asiaticoside dan memiliki aktivitas antioksidan 86,81%.
Tikus terlebih dahulu diaklimatisasi selama satu minggu untuk pengontrolan kondisi hewan coba. Tikus dipelihara dalam ruangan khusus diletakkan di kandang polypropyelene
higienis dengan enam tikus per kandang besar yang kemudian diberi pembatas transparan sehingga satu tikus menghuni satu kandang kecil individu. Tikus dipelihara pada ruangan dengan pengendalian suhu (27-29oC), 12 jam
lampu terang dan 12 jam siklus gelap (lampu dinyalakan pada jam 07.00 WIB). Pakan yang diberikan berupa pakan berbentuk pellet jenis AD II dan air minum reverse osmosis diberikan secara ad libitum. Prosedur pembuatan tikus model DM tipe 2 berdasarkan review Ghasemi
et al. yaitu memuasakan tikus Wistar (Rattus norvegicus) selama satu malam. Tikus kemudian diinjeksi dengan NA 230 mg/kg berat badan intraperitonial yang dilarutkan dalam normal salin. Setelah lima belas menit, tikus diinjeksi STZ dosis tunggal sebesar 65 mg/kg BB intraperitonial yang dilarutkan dalam penyangga asam sitrat dingin pH 4,5. Tikus dinyatakan hiperglikemia jika kadar glukosa darah sewaktu >150 mg/dL setelah tiga hari pasca induksi.28
Pengukuran kadar gula darah dengan metode Glucose Oxidase Phenol Aminoantipyrina Jumlah dan Cara Pengumpulan Sampel
Hewan coba yang digunakan dalam penelitian ini adalah tikus putih jantan jenis Rattus norvegicus strain wistar berumur 8 minggu, berat badan berkisar 200 ± 50 gram yang diperoleh dari UPHP Universitas Gadjah Mada Yogyakarta. Penelitian ini telah memperoleh persetujuan etik dari Komisi Etik Hewan No 129/II/HREC/2017 RSUD Dr. Moewardi. Sampel diambil secara randomisasi dengan metode Simple Random Sampling (SRS) dari populasi terjangkau, dengan syarat harus sesuai dengan kriteria. Kriteria inklusi pada penelitian ini yaitu tikus dalam kondisi sehat yang diperoleh melalui pemeriksaan fisik dan pemeriksaan kadar glukosa darah awal. Tikus sebanyak 36 ekor dibagi menjadi 6 kelompok: kelompok kontrol tikus normal (K-); kelompok kontrol tikus diabetes induksi NA-STZ (K+); kelompok perlakuan ekstrak etanol pegagan dosis 300 mg/ kg BB (P1); kelompok perlakuan ekstrak etanol pegagan dosis 600 mg/kg BB (P2); kelompok perlakuan ekstrak etanol pegagan dosis 1.200 mg/kg BB (P3); kelompok perlakuan obat oral antidiabetes metformin 45 mg/kg BB (P4), dan diterminasi pada lama pemberian 28 hari dan 35 hari.
Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian adalah makanan hewan percobaan
yaitu pellet (AD2) dan minuman standar Reserve
Osmosis (RO), tanaman pegagan (Centella asiatica), Streptozotocin (Nacatalai tesque inc, Kyoto, Jepang), Nicotinamide (Nacatalai tesque inc, Kyoto, Jepang), aquabides, Phosphat Buffer Saline (PBS), chloroform, air, metanol, etanol 70%, Glucose GOD FS kit dari Diagnostic System International (Diasys, Holzheim, Germany), bahan penatalaksanaan jaringan untuk sediaan histopatologi dan bahan pengecatan
hematoxylin-eosin (HE). Alat yang digunakan dalam penelitian ini adalah set kandang perlakuan, surgery set, alat sonde, timbangan
115 115 Peroxidase (GOD-PAP) dilakukan di laboratorium
PSPG UGM Yogyakarta. Dilakukan pengambilan sampel darah vena melalui mata (medial canthus sinus orbitalis) menggunakan mikrohematokrit dan ditampung ke dalam ependorop sebanyak 0,5 ml. Pengukuran kadar gula darah dilakukan empat kali, pengukuran awal (hari ke-0), untuk memastikan tikus dalam keadaan sehat dengan indikator kadar gula normal (65-135 mg/dl); pengukuran kedua, untuk memastikan tikus sudah mengalami hiperglikemia pada hari ke-3 pasca induksi; pengukuran ketiga untuk memastikan penurunan kadar gula darah tikus diabetes melitus tipe 2 pasca perlakuan yaitu hari ke 28 hari dan 35 hari.29
Nekropsi dilakukan dengan menyayat kulit dan otot abdominal hingga rongga perut terbuka. Organ pankreas segera diambil sebelum detak
jantung berhenti. Pengambilan organ pankreas dilakukan pada hari ke-28 dan 35 hari setelah pemberian ekstrak pegagan.30
Pembuatan preparat histopatologi pada organ pankreas dilakukan dengan prosedur
Muntiha yaitu melalui proses fiksasi, rehidrasi, embedding, blocking, dan proses pemotongan
sediaan blok parafin. Sediaan kemudian diwarnai
dengan Hematoxylin-Eosin (HE). Derajat Insulitis
merupakan inflamasi yang terjadi pada daerah
pankreas dinilai berdasarkan hasil pengecatan HE pada keseluruhan lapang pandang dengan
perbesaran lemah (100x) maupun perbesaran kuat (400x) oleh dua orang Patolog.31 Skor
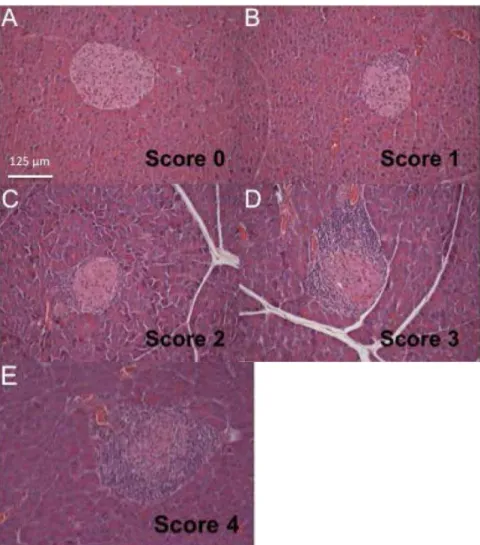
inflamasi berdasarkan kriteria Guttierez et al.:
skor 0= tidak ada inflamasi; skor 1= peri-islet
insulitis; skor 2= intermediate insulitis; skor 3=
intraislet insulitis; skor 4= complete islet insulitis
(Gambar 1).32
6
6
sediaan blok parafin. Sediaan kemudian diwarnai dengan Hematoxylin-Eosin (HE). Derajat Insulitis merupakan inflamasi yang terjadi pada daerah pankreas dinilai berdasarkan hasil pengecatan HE pada keseluruhan lapang pandang dengan perbesaran lemah (100x) maupun perbesaran kuat (400x) oleh dua orang Patolog.31 Skor inflamasi berdasarkan kriteria Guttierez et al.: skor 0= tidak
ada inflamasi; skor 1= peri-islet insulitis; skor 2= intermediate insulitis; skor 3= intraislet insulitis; skor 4= complete islet insulitis(Gambar 1).32
Gambar 1. Skor Derajat Insulitis Pankreas Tikus (Sumber: Guttierez et al.) Pengolahan dan Analisis Data
Multiple Range Test (DMRT) untuk mengetahui perbedaan antara kelompok kontrol dengan perlakuan. Data derajat insulitis tidak memenuhi syarat normalitas dan terdapat perbedaan
signifikan dilanjutkan uji mann-whitney. semua data dianalisis dengan tingkat kepercayaan 95% (p< 0,05) menggunakan perangkat lunak SPSS 20.
HASIL
Tabel 1 dan Gambar 3 menunjukkan hasil analisis statistik one way anova pada tingkat kepercayaan 95% bahwa dosis pemberian ekstrak etanol pegagan memberikan pengaruh signifikan terhadap rerata kadar gula darah tikus model diabetes melitus tipe 2 pada lama pemberian 28 hari dan pada lama pemberian 35 hari dengan nilai p yang sama yaitu p= 0,001 (p< 0,05). Analisis lanjut menggunakan DMRTpada lama pemberian 28 hari menunjukkan kelompok Pengolahan dan Analisis Data
Analisis data dilakukan dengan menguji normalitas data (uji shapiro wilk) dan homogenitas data (uji levene) untuk syarat uji analysis of variance (ANOVA). Data kadar gula darah dilakukan uji ANOVA untuk mengetahui perbedaan rerata antara kelompok. Selanjutnya,
apabila hasilnya signfikan dilanjutkan uji Duncan 8
8
Gambar 2. Bagan Kerangka Alur Penelitian Pengaruh Dosis dan Lama Pemberian Ekstrak Etanol Pegagan (Centella Asiatica) terhadap Kadar Gula Darah dan Derajat Insulitis Pankreas Tikus Model DM Tipe 2
Cek kadar gula darah dan berat badan 3 hari pasca injeksi STZ Cek kadar gula darah dan berat badan 3 hari pasca injeksi STZ
Diet standar + Metformin 45 mg
/kg BB/hr Diet standar + EEP
dosis 1.200 mg/kg BB/hr Diet standar + EEP
dosis 600 mg/kg BB/hr Diet standar + EEP
dosis 300 mg/kg BB/hr Term. 35 hr 3 ekor Term. 28 hr 3 ekor Term. 35 hr 3 ekor Term. 28 hr 3 ekor Term. 35 hr 3 ekor Term. 28 hr 3 ekor Term. 35 hr 3 ekor Term. 28 hr 3 ekor
Cek kadar gula darah dan berat badan 3 hari pasca injeksi STZ Diet standar + aquades 10 ml/kg BB/hari
Cek kadar gula darah, koleksi organ pankreas, pembuatan preparat histopatologi. Observasi dan analisis derajat insulitis.
Uji statistik, analisis data, dan kesimpulan Term. 35 hr 3 ekor Term. 28 hr 3 ekor Term. 35 hr 3 ekor Term. 28 hr 3 ekor
36 ekor tikus putih strain Wistar umur 8 minggu, berat badan 150-250 gram
Adaptasi selama 7 hari, dikelompokkan secara randomisasi. Cek berat badan dan kadar gula darah
Kel. K- (6 ekor) Kel. K+ (6 ekor) Kel. P1 (6 ekor) Kel. P2 (6 ekor) Kel. P3 (6 ekor) Kel. P4 (6 ekor) Penyangga asam sitrat Injeksi Nicotinamide 230 mg/kg berat badan + STZ 65 mg/kg berat badan secara intraperitonial
Gambar 2. Bagan Kerangka Alur Penelitian Pengaruh Dosis dan Lama Pemberian Ekstrak Etanol Pegagan (Centella Asiatica) terhadap Kadar Gula Darah dan Derajat Insulitis
Pankreas Tikus Model DM Tipe 2
K+ berbeda dengan kelompok K-, P1, P2, P3, dan P4; kelompok K- berbeda dengan kelompok P1, P2, P3, dan P4; kelompok P1 berbeda dengan kelompok P2, P3, dan P4; kelompok P2 berbeda dengan kelompok P3 dan P4. Analisis lanjut pada lama pemberian 35 hari sama dengan analisis pada lama pemberian 28 hari. Rerata kadar gula darah kelompok kontrol normal lebih rendah dibandingkan semua kelompok lainnya pada lama pemberian 28 hari dan 35 hari. Rerata kadar gula darah kelompok perlakuan
117 117 ekstrak etanol pegagan dosis 300 mg/kg BB,
600 mg/kg BB,1.200 mg/kg BB, dan kontrol obat metformin lebih rendah dibandingkan kelompok kontrol diabetes pada lama pemberian 28 dan 35
hari. Kadar gula darah pada kelompok perlakuan ekstrak etanol pegagan dosis 1.200 mg/kg BB relatif sama dengan kelompok kontrol metformin pada lama pemberian 28 hari dan 35 hari.
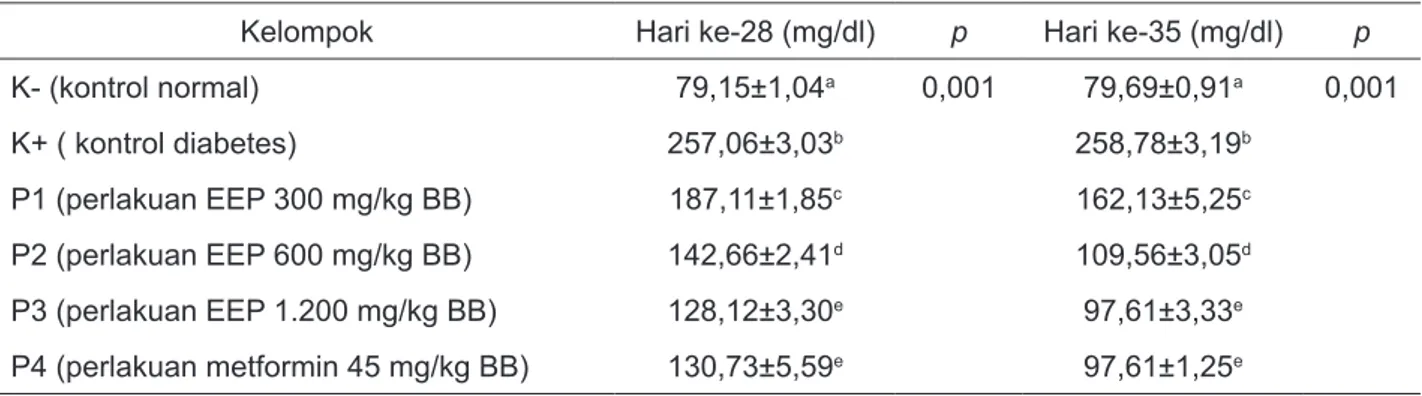
Tabel 1. Pengaruh Dosis dan Lama Pemberian Esktrak Pegagan terhadap Kadar Gula Darah Tikus Model Diabetes Melitus Tipe 2 pada Lama Pemberian 28 Hari dan 35 Hari
Kelompok Hari ke-28 (mg/dl) p Hari ke-35 (mg/dl) p
K- (kontrol normal) 79,15±1,04a 0,001 79,69±0,91a 0,001 K+ ( kontrol diabetes) 257,06±3,03b 258,78±3,19b P1 (perlakuan EEP 300 mg/kg BB) 187,11±1,85c 162,13±5,25c P2 (perlakuan EEP 600 mg/kg BB) 142,66±2,41d 109,56±3,05d P3 (perlakuan EEP 1.200 mg/kg BB) 128,12±3,30e 97,61±3,33e P4 (perlakuan metformin 45 mg/kg BB) 130,73±5,59e 97,61±1,25e
Keterangan : EEP = ekstrak etanol pegagan; Nilai merepresentasikan rata-rata ± SD; N=3.
a,b,c,d,e, Notasi yang berbeda pada kolom yang sama menunjukkan perbedaan yang signifikan (p< 0,05).
0 50 100 150 200 250 300 K‐ K+ P1 P2 P3 P4 Kadar Gula Darah (mg/dl ) Hari ke ‐ 28 Hari ke ‐ 35
Gambar 3. Pengaruh Dosis dan Lama Pemberian Esktrak Pegagan terhadap Kadar Gula Darah Tikus Model Diabetes Melitus Tipe 2 pada Lama Pemberian 28 Hari dan 35 Hari
Tabel 2, Gambar 4 dan Gambar 5 menunjukkan hasil analisis statistik kruskal-wallis pada tingkat kepercayaan 95% bahwa dosis pemberian ekstrak etanol pegagan memberikan pengaruh yang tidak signifikan
terhadap derajat inflamasi tikus model diabetes
melitus tipe 2 pada lama pemberian 28 hari p=
0,368 (p> 0,05), namun signifikan pada lama
pemberian 35 hari p= 0,008 (p< 0,05). Analisis lanjut menggunakan mean whitney pada lama pemberian 35 hari menunjukkan bahwa kelompok K- berbeda dengan kelompok K+,
namun tidak berbeda dengan kelompok P1, P2, P3, dan P4; kelompok P1 tidak berbeda dengan kelompok K+ dan kelompok K-, namun berbeda dengan kelompok P2, P3, dan P4; kelompok P2 dan P3 tidak berbeda dibandingkan kelompok P4, tetapi berbeda dengan kelompok K+. Derajat insulitis kelompok tikus normal lebih ringan dibandingkan kelompok tikus DM tipe 2, namun relatif sama dengan kelompok ekstrak etanol pegagan dosis 600 mg/kg BB, 1.200 mg/
kg BB, dan kelompok kontrol obat metformin pada lama pemberian 35 hari. Derajat insulitis kelompok ekstrak etanol pegagan dosis 300 mg/kg BB lebih tinggi dibandingkan kelompok ekstrak etanol pegagan dosis 600 mg/kg BB, 1.200 mg/kg BB, dan kelompok kontrol obat metformin. Derajat insulitis kelompok ekstrak etanol pegagan dosis 600 mg/kg BB dan 1.200 mg/kg BB relatif sama dengan kelompok kontrol obat metformin pada lama pemberian 35 hari.
Tabel 2. Pengaruh Dosis dan Lama Pemberian Esktrak Pegagan terhadap Derajat Insulitis Tikus Model Diabetes Melitus Tipe 2 pada Lama Pemberian 28 Hari dan 35 Hari
Dosis Lama Pemberian 28 hari Median p 35 hari Median p K- (kontrol normal) 0 0,368 0ac 0,008 K+ ( kontrol diabetes) 1 3b P1 (perlakuan EEP 300 mg/kg BB) 1 1ab P2 (perlakuan EEP 600 mg/kg BB) 1 0c P3 (perlakuan EEP 1.200 mg/kg BB) 1 0c P4 (perlakuan metformin 45 mg/kg BB) 1 0c
Keterangan : EEP= ekstrak etanol pegagan; skor 0= tidak ada inflamasi; skor 1= peri islet insulitis; skor 2= intermediate insulitis; skor 3= intraislet insulitis; Nilai merepresentasikan rata-rata ± SD; N=3
a,b,c, Notasi yang berbeda pada kolom yang sama menunjukkan perbedaan yang signifikan (p< 0,05).
119 119
P1 (skor 1) P2 (skor 1)
P3 (skor 1) P4 (skor 1)
Keterangan : K- = Kelompok kontrol normal; K+ = kelompok kontrol DM; P1= kelompok perlakuan Ekstrak Etanol Pegagan (EEP) 300 mg/kg BB; P2 = kelompok perlakuan EEP 600 mg/kg BB; P3 = kelompok perlakuan EEP 1.200 mg/kg BB; P4 = kelompok perlakuan metformin 45 mg/kg BB; skor 0 = tidak ada inflamasi; skor 1 = inflamasi ringan.
Gambar 4. Gambaran Histopatologi Pankreas Tikus Tiap Kelompok pada Lama Pemberian 28 Hari
PEMBAHASAN
Pemberian ekstrak etanol pegagan pada penelitian ini telah berhasil menurunkan kadar gula darah pada tikus DM tipe 2 pada lama pemberian 28 hari maupun 35 hari. Pemberian ekstrak etanol pegagan juga berhasil menurunkan kadar gula darah menjadi normal pada perlakuan ekstrak etanol pegagan dosis 1.200 mg/kg BB pada lama pemberian 28 dan 35 hari serta dosis 600 mg/kg BB pada lama pemberian 35 hari. Menurut Kusumawati kadar gula darah tikus normal berkisar atara 65-135 mg/dl.29 Hasil penelitian ini sejalan dengan
penelitian Kabir et al. (2014), pemberian ekstrak etanol pegagan dosis 250 mg/kg BB, 500 mg/ kg BB, dan 1.000 mg/kg BB dua kali sehari
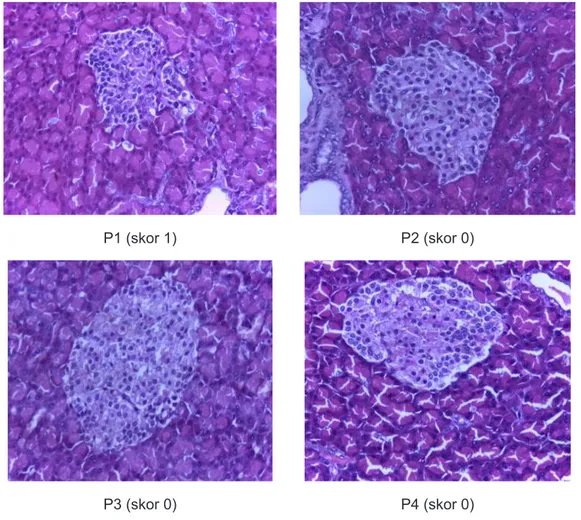
P1 (skor 1) P2 (skor 0)
P3 (skor 0) P4 (skor 0)
Keterangan : K- = Kelompok kontrol normal; K+ = kelompok kontrol DM; P1= kelompok perlakuan Ekstrak Etanol Pegagan (EEP) 300 mg/ kg BB; P2 = kelompok perlakuan EEP 600 mg/ kg BB; P3 = kelompok perlakuan EEP 1.200 mg/ kg BB; P4 = kelompok perlakuan metformin 45 mg/ kg BB; skor 0 = tidak ada inflamasi; skor 1 = inflamasi ringan; skor 3 = inflamasi berat.
Gambar 5. Gambaran Histopatologi Pankreas Tikus Tiap Kelompok pada Lama Pemberian 35 Hari
selama 28 hari menurunkan konsumsi pakan, berat badan, konsumsi air tikus, dan kadar glukosa darah. Selanjutnya, studi Maulidiani
et al. juga menunjukkan bahwa ekstrak etanol daun pegagan dosis 300 mg/kg BB mampu menurunkan kadar gula darah dalam plasma tikus induksi STZ.23
Penurunan kadar glukosa darah akibat efek pegagan kemungkinan disebabkan karena zat aktif yang terdapat dalam pegagan yaitu triterpenoid. Ekstrak etanol pegagan mengandung asiatic acid yang merupakan derivative triterpenoid dari pegagan. Aciatic acid memiliki aktivitas farmakologi seperti antioksidan33 dan hepatoprotektif.34 Pasien
121 121 diketahui mengalami penurunan jalur sinyal
Phosphatidylinositide 3-Kinase (PI3K)/Akt yang diperlukan untuk regulasi insulin.35 Penelitian
in vivo Ramachandran dan Saravanan menunjukkan bahwa asiatic acid berperan sebagai antidiabetes melalui peningkatan glikolisis dengan mengembalikan aktivitas enzim kunci seperti heksokinase, glukosa-6-fosfat dehidrogenase (G6PDH), dan PK.36 Penelitian
Ramachandran dan Saravaran juga menunjukkan bahwa asiatic acid terbukti meningkatkan sekresi insulin dengan cara meningkatkan jalur sinyal PI3 Kinase/Akt. Disamping itu, senyawa tersebut juga memperbaiki respon glukosa melalui peningkatan protein GLUT-4 otot, IR, IRS-1, dan IRS 2.37
Pemberian ekstrak etanol pegagan pada penelitian ini telah berhasil menurunkan derajat insulitis yang merupakan salah satu indikator terjadinya perbaikan sel beta pankreas. Pemberian ekstrak pegagan dosis 600 mg/kg BB dan 1.200 mg/kg BB pada lama pemberian 35 hari memperbaiki kerusakan pulau langerhans pankreas akibat induksi STZ dengan menghambat proses peradangan (insulitis).
Serbukan infiltrat pada pankreas lebih sedikit
pada kelompok tikus yang diberi perlakuan ekstrak etanol daun pegagandibanding dengan kelompok kontrol diabetes (Gambar 5). Hasil penelitian ini sejalan dengan studi Oyenihi et al. ekstrak metanol pegagan 500 mg/kg BB dan metformin 300 mg/kg BB mengurangi kadar
sitokin proinflamasi (IL1-β, IL-6, TNF-α, dan
MCP-1) pada organ hati tikus model diabetes melitus tipe 2.38
Mekanisme pegagan dalam menurunkan
inflamasi pada penelitian ini dikaitkan dengan
aktivitas antioksidannya. Pegagan (Centella asiatica) merupakan tanaman yang mengandung antioksidan dengan komponen utama pentacyclic triterpenes.17 Ekstrak etanol pegagan pada
penelitian ini terbukti mengandung zat aktif
asiaticoside dan memiliki aktivitas antioksidan
yang cukup tinggi yaitu 86,81%. Studi Nurlaily et al. menunjukkan bahwa komponen asiaticoside
dan madecassoside pada pegagan terbukti
menghambat penanda inflamasi COX-1 dan
COX-2 serta menekan produksi PQ2 pada studi
in vitro.22 Selain itu, penelitian Pakdeechote
menunjukkan bahwa kandungan asam asiatic pada pegagan mempunyai efek antiinflamasi
melalui penurunan produksi ROS dan sitokin
inflamasi dengan meningkatkan bioavaibilitas
NO pada tikus model sindrom metabolik.30
Pemberian ekstrak etanol pegagan (Centella asiatica) dosis 600 mg/kg BB/hari
dengan lama pemberian 35 hari paling efikasi
dalam menurunkan kadar gula darah dan derajat insulitis. Oleh sebab itu, dosis 600 mg/kg BB/ hari dapat dilanjutkan untuk uji coba secara klinis kepada manusia melalui faktor konversi dosis. Menurut Reagan-Shaw et al. konversi dosis dari tikus ke manusia yang paling tepat menggunakan metode Body Surface Area (BSA) atau normalisasi permukaan tubuh. Metode BSA telah disesuaikan dengan berbagai parameter biologi termasuk pemanfaatan oksigen, pengeluaran kalori, metabolisme basal, volume darah, sirkulasi protein plasma, dan fungsi ginjal.39 Pemberian ekstrak etanol pegagan
dosis 600 mg/kg BB/hari menggunakan tikus wistar pada penelitian ini setara dengan dosis 0,1 gram/kg BB/hari pada manusia. Apabila manusia dengan berat badan 50 kg maka akan membutuhkan ekstrak etanol pegagan dengan dosis 5 gram/kg BB/hari.
KESIMPULAN
Ekstrak etanol pegagan memiliki kandungan antioksidan dan asiaticoside yang bekerja
sebagai antiinflamasi dan antidiabetes melalui
penurunan derajat insulitis sehingga dapat mencegah perkembangan penyakit diabetes melitus akibat kondisi hiperglikemia. Ekstrak etanol pegagan dosis 600 mg/kg BB/hari paling efektif dalam menurunkan kadar gula darah dan
derajat insulitis yang dapat menjadi salah satu alternatif dalam mencegah kondisi hiperglikemia
dan inflamasi secara aman dibandingkan obat
oral antidiabetes dengan efek samping yang ditimbulkannya.
SARAN
Perlu dilakukan uji skrining fitokimia ekstrak
etanol pegagan untuk mengetahui lebih banyak jenis antioksidan yang terkandung didalamnya. Penelitian lebih lanjut dengan menggunakan
penanda inflamasi yang lain untuk mengetahui jalur efek antiinflamasi ekstrak etanol pegagan
pada tikus model diabetes melitus tipe 2.
UCAPAN TERIMA KASIH
Terimakasih disampaikan kepada Unit Pengembangan Hewan Percobaan (UPHP) UGM Yogyakarta, Laboratorium Penelitian dan Pengujian Terpadu (LPPT) UGM Yogyakarta, Laboratorium Patologi Anatomi UNS Solo. Penulis mengucapkan terimakasih kepada Agus Heri Santoso, STP, M.Si yang telah memberikan bimbingan dan arahan kepada penulis sehingga penelitian dapat terlaksana dan jurnal ini tersusun dengan baik.
DAFTAR PUSTAKA
1. American Diabetes Association. Diagnosis and Classification of Diabetes Mellitus. Diabetes Care.2010;1:S62-S69.
2. Shaw JE, Sicree RA, Zimmet PZ. Global Estimates of the Prevalence of Diabetes for 2010 and 2030. Diabetes Res Clin Pract.2010;87(1):4-14.
3. Kemenkes RI. Riset Kesehatan Dasar. Jakarta: Badan Litbang Kesehatan;2013. 4. World Health Organization. Global Status
Report on Noncommunicable Disease. Geneva: World Health Organization;2014. 5. W o r l d H e a l t h O r g a n i z a t i o n . Noncommunicable Disease Country
Profiles 2014. Geneva: World Health Organization;2014.
6. Ikmal SIQS, Huri HZ, Vethakkan SR, Ahmad WAW. Potential Biomarkers of Insulin Resistance and Atherosclerosis in Type 2 Diabetes Mellitus Patients with Coronary Artery Disease. International Journal of Endocrinology.2013:1-11.
7. Node K, Inoue T. Postprandial Hyperglycemia as an Ethiological Factor in Vascular Failure. Cardiovascular Diabetology.2009;8(23):1–10.
8. Donath MY, Boni-schnetzler M, Ellingsgaard H, Halban PA, Ehses JA. Cytokine Production by Islets in Health and Diabetes: Cellular Origin, Regulation and Function. Trends Endocrinol Metab.2010;21(5):261–7. 9. Oever IAM, Raterman HG, Nurmohamed
MT, Simsek S. Endothelial Dysfunction,
Inflammation, and Apoptosis in Diabetes
Mellitus. Mediators Inflamm. 2010:1-15. 10. Montané J, Cadavez L, Novials A. Stress
and the Inflammatory Process : A Major
Cause of Pancreatic Cell Death in Type 2 Diabetes. Diabetes, Metabolic, and Obesity: Targets and Therapy 2014. 2014;7:25-34. 11. Coppieters KT, Dotta F, Amirian N,
Campbell PD, Kay TWH, Atkinson MA, et al. Demonstration of Islet-autoreactive CD8 T Cells in Insulitic Lesions from Recent Onset and Long-term Type 1 Diabetes Patients. J Exp Med. 2012;209(1):51-60.
12. Agrawal NK, Kant S. Targeting Inflammation
in Diabetes: Newer Therapeutic Options. World J Diabetes. 2014;5(5):697-710. 13. Larsen CM, Faulenbach M, Vaag A,
Ehses JA, Seifert B, Mandrup-poulsen T, et al. Interleukin-1–Receptor Antagonist in Type 2 Diabetes Mellitus. N Engl J Med. 2007;356(15):1517-26.
14. Inzucchi SE, Bergenstal RM, Buse JB, Diamant M, Ferrannini E, Nauck M, et al.
123 123 Management of Hyperglycemia in Type 2
Diabetes: A Patient-centered Approach: Position Statement of the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2012;35(6):1364-79.
15. Marín-Peñalver JJ, Martín-Timón I, Sevillano-Collantes C, Cañizo-Gómez FJ Del. Update on the Treatment of Type 2 Diabetes Mellitus. World J Diabetes. 2016;7(17):354-95. 16. Chauhan PK, Pandey IP, Dhatwalia VK,
Singh V. Antidiabetic Effect of Ethanolic
and Methanolic Leaves Extract of Centella asiatica on Alloxan Induced Diabetic Rats. Int J Pharm Bio Sci. 2010;6(2):1-6.
17. Yasurin P, Sriariyanun M, Phusantisampan T. Review : The Bioavailability Activity of Centella asiatica. KMUTNB Int J Appl Sci Technol. 2016;9(1):1-9.
18. Maulidiani, Abas F, Khatib A, Perumal V, Suppaiah V, Ismail A, et al. Metabolic Alteration in Obese Diabetes Rats upon
Treatment with Centella asiatica Extract. J Ethnopharmacol. 2016;180:60-9.
19. Supkamonseni N, Thinkratok A, Meksuriyen D, Srisawat R. Hypolipidemic and Hypoglycemic Effects of Centella asiatica
(L.) Extract in Vitro and in Vivo. Indian J Exp Biol. 2014;52(10):965-71.
20. Lokanathan Y, Omar N, Ahmad Puz NN, Saim A, Hj Idrus R. Recent Updates in Neuroprotective and Neuroregenerative Potential of Centella asiatica. Malaysian J Med Sci. 2016;23(1):4-14.
21. Pramono S, Ajiastuti D. Standardisasi Ekstrak Herba Pegagan (Centella asiatica (L.). Urban Berdasarkan Kadar Asiatikosida secara KLT-densitometri Densitometric Method. Majalah Farmasi Indonesia. 2004;15(3):118-23.
22. Nurlaily A, Noor Baitee AR, Musalmah
M. Comparative Antioxidant and Anti-Inflammatory Activity of Different Extracts
of Centella asiatica (L.) Urban and Its Active Compounds, Asiaticoside and Madecassoside. Med & Health. 2012;7(2):62-72.
23. Kabir AU, Samad MB, D’Costa M, Akhter F,
Ahmed A, Hannan J.M.A. Anti-hyperglycemic Activity of Centella asiatica is Partly Mediated by Carbohydrase Inhibition and Glucose-Fiber Binding. BMC Complementary and Alternative Medicine. 2014. http://www. biomedcentral.com/1472-6882/14/31. 24. Muchtaromah B, Ahmad M, Suyono,
Romaidi, Bahri S, dan Kumalasari H.P. Dosage and Administration Length of
Centella Asiatica (L.) Urban Decrease the Level of SOD and MDA and Improve Brain Histological Condition of Rats. Jurnal Teknologi (Sciences & Engineering).
2016;78(5):57-61.
25. Medagama B, Bandara R. The Use of Complementary and Alternative Medicines (CAMs) in the Treatment of Diabetes Mellitus: Is Continued Use Safe and Effective? Nutr J. 2014; 13(1):102-10.
26. Ranasinghe P, Jayawardana R, Galappaththy P, Constantine GR, Gunawardana NDV,
Katulanda P. Review Article Efficacy and
Safety of “True” Cinnamon (Cinnamomum zeylanicum) as a Pharmaceutical Agent in Diabetes: A Systematic Review and Meta-analysis. Diabet Med. 2012;1480-92. 27. Nugroho AE, Lindawati NY, Herlyanti K,
Widyastuti L, Pramono S. Anti-diabetic Effect of a Combination of
Andrographolide-enriched Extract of Andrographis Paniculata
(Burm f.) Nees and Asiaticoside-enriched
Extract of Centella asiatica L. in High
Fructose-fat Fed Rats. Indian J Exp Biol. 2013;51(12):1101–18.
28. Ghasemi A, Khalifi S, Jedi S.
Streptozotocin-nicotinamide-induced Rat Model of Type 2 Diabetes. Acta Physiologica Hungarica. 2014;101(4):408-20.
29.
Kusumawati D.
Bersahabat dengan
Hewan Coba.
Yogyakarta: Gadjah Mada
University Press;2016
.30. Pakdeechote P, Bunbupha S, Kukongviriyapan U, Prachaney P, Khrisanapant W, Kukongviriyapan V. Asiatic Acid Alleviates Hemodynamic and Metabolic Alterations via Restoring eNOS/
iNOS Expression, Oxidative Stress, and
Inflammation in Diet-induced Metabolic Syndrome Rats. Nutrients. 2014;6(1):355-70.
31. Muntiha M. Teknik Pembuatan Preparat Histopatologi dari Jaringan Hewan dengan Pewarnaan Hematoksilin dan Eosin. Temu Teknis Fungsional non Peneliti. Bogor: Balai Penelitian Veteriner. 2001;156-63.
32. Gutierrez DA, Fu W, Schonefeldt S, Feyerabend TB, Ortiz-Lopez A, Lampi Y, et al. Type 1 Diabetes in NOD Mice Unaffected by Mast Cell Deficiency. Diabetes. 2014;63(11):3827-34.
33. Lee C, Olson P, Evans RM. Minireview : Lipid Metabolism, Metabolic Diseases, and
Peroxisome Proliferator-Activated Receptors. Endocrinology. 2003;144(6):2201-07. 34. Ma K, Zhang Y, Zhu D, Lou Y. Protective
Effects of Asiatic Acid Against
D-galactosamine/lipopolysaccharide-induced Hepatotoxicity in Hepatocytes
and Kupffer Cells Co-cultured System via
Redox-regulated Leukotriene C4 Synthase Expression Pathway. Eur J Pharmacol. 2009;603(1-3):98-107.
35. Rice KM, Kakarla SK, Mupparaju SP, Paturi S, Katta A, Wu M, et al. Shear Stress Activates Akt During Vascular Smooth Muscle Cell Reorientation. 2010;55:85-90.
36. Ramachandran V, Saravanan R. Efficacy
of Asiatic Acid, a Pentacyclic Triterpene on Attenuating the Key Enzymes Activities of Carbohydrate Metabolism in Streptozotocin-induced Diabetic Rats. Phytomedicine. 2013;20(3-4):230-6.
37. Ramachandran V, Saravanan R. Glucose Uptake Through Translocation and Activation of GLUT4 in PI3K/Akt Signaling Pathway by Asiatic Acid in Diabetic Rats. Human and Experimental Toxicology. 2015;34(9):884-93.
38. Oyenihi AB, Chegou NN, Oguntibeju OO, Masola B. Centella asiatica Enhances
Hepatic Antioxidant Status and Regulates Hepatic Inflammatory Cytokines in Type
2 Diabetic Rats. Pharmaceutical Biology. 2017;55(1):1671-78.
39. Reagan-Shaw S, Nihal M, Ahmad N. Dose Translation from Animal to Human Studies Revisited. The Faseb Journal. 2016;22(3):659–61.