LAPORAN PRAKTIKUM TEKNIK PASCA PANEN I
(Kesetimbangan Massa)
Oleh :
Nama : Candra Melati
NPM : 240110140057
Hari, Tanggal Praktikum : Selasa, 15 September 2015 Co.Ass : 1. Aditya Ramadhan
2. Cindy Almas R 3. Jeremia Kristian 4. Prisilia Ratna S 5. Shayana Junita
LABORATORIUM PASCA PANEN DAN TEKNOLOGI PROSES TEKNIK DAN MANAJEMEN INDUSTRI PERTANIAN
FAKULTAS TEKNOLOGI INDUSTRI PERTANIAN UNIVERSITAS PADJADJARAN
2015
BAB I PENDAHULUAN
1.1 Latar Belakang
Sebagaimana yang diketahui dalam teori bahwa dalam suatu sistem tertutup maupun dalam reaksi kimia segala sesuatu yang masuk akan sama dengan yang keluar baik massa maupun energi hal ini berkaitan dengan hukum kekekalan massa dan hukum kekekalan energi dimana massa maupun energi akan tetap dalam jumlah yang sama ketika ia masuk meskipun dengan perubahan wujud dan bentuk.
Dalam praktikum kali ini akan dibahas mengenai aplikasi dari kesetimbangan massa dengan menggunakan proses pengentalan dan pencairan bahan. Bahan yang digunakan adalah larutan gula.
1.2 Tujuan
1. Mempelajari kesetimbangan massa pada proses pengentalan dan pencairan
2. Mempelajari keadaan sistem steady dan unsteady state dengan larutan gula
3. Menentukan model neraca massa steady state pada air massa dan unsteady state pada komponen gula
4. Mempelajari dan menerapkan analisis kesetimbangan massa dalam teknik unit operasi dalam penanganan hasil pertanian
BAB II
TINJAUAN PUSTAKA
2.1 Kesetimbangan Massa
Hukum Kekekalan Massa atau Hukum Lavoiser menyatakan massa zat-zat sebelum reaksi sama dengan massa zat-zat sesudah reaksi. Dengan kata lain,dalam reaksi kimia, Untuk suatu proses kimiawi di dalam suatu sistem tertutup, massa dari reaktan harus sama dengan massa produk.
Hukum kekekalan massa diformulasikan oleh Antoine Lavoisier pada tahun 1789. Oleh karena hasilnya ini, ia sering disebut sebagai bapak kimia modern. Sebelumnya, Mikhail Lomonosov (1748) juga telah mengajukan ide yang serupa dan telah membuktikannya dalam eksperimen. Sebelumnya, kekekalan massa sulit dimengerti karena adanya gaya buoyan atmosfer bumi. Setelah gaya ini dapat dimengerti, hukum kekekalan massa menjadi kunci penting dalam mengubah alkemi menjadi kimia modern. Ketika ilmuwan memahami bahwa senyawa tidak pernah hilang ketika diukur, mereka mulai melakukan studi kuantitatif transformasi senyawa. Studi ini membawa kepada ide bahwa semua proses dan transformasi kimia berlangsung dalam jumlah massa tiap elemen tetap.
2.2 Pengentalan dan Pencairan
Pengentalan merupakan proses pengurangan kadar air pada suatu larutan dengan car melakukan penguapan air yang tergandung dalam larutan tersebut atau dengan penambahan zat terlarut pada larutan tersebut.
Pengenceran adalah proses mengurangi konsentrasi zat terlarut dalam larutan, biasanya dengan menambahkan pelarut yang berlebih. Proses pembuatan larutan dari zat padatnya disebut dengan pengenceran. Begitu pula dengan proses pembuatan larutan dari zat pekatnya disebut dengan pengenceran. (Khopkar, 1990)
2.3 Steady dan Unsteady
Keadaan steady state adalah keadaan keseimbangan setelah proses berjalan selama beberapa periode. Probabilitas pada keadaan ini disebut probabilitas steady state yang nilainya tetap (konstan). Sedangkan unsteady state
merupakan kebalikan dari steady state, dimana suatu system berubah terhadap waktu.
2.4 Refraktometer
Refractometer adalah alat yang digunakan untuk mengukur kadar / konsentrasi bahan terlarut misalnya : Gula, Garam, Protein dsb. Prinsip kerja dari refractometer sesuai dengan namanya adalah dengan memanfaatkan refraksi cahaya. Refractometer ditemukan oleh Dr. Ernst Abbe seorang ilmuwan dari German pada permulaan abad 20. Konsentrasi larutan akan berpengaruh secara proporsional terhadap sudut refraksi. Pada prakteknya Refractometer akan ditera pada skala sesuai dengan penggunaannya. Sebagai contoh Refractometer yang dipakai untuk mengukur konsentrasi larutan gula akan ditera pada skala gula. Begitu juga dengan refractometer untuk larutan garam, protein dll. Konsentrasi bahan terlarut sering dinyatakan dalam satuan Brix(%) yaitu merupakan persentasi dari bahan terlarut dalam sample (larutan air). Kadar bahan terlarut merupakan total dari semua bahan dalam air, termasuk gula, garam, protein, asam dsb. Pada dasarnya Brix(%) dinyatakan sebagai jumlah gram dari cane sugar yang terdapat dalam larutan 100g cane sugar. Jadi pada saat mengukur larutan gula, Brix(%) harus benar-benar tepat sesuai dengan konsentrasinya.
BAB III
METODOLOGI PENGAMATAN DAN PENGUKURAN
3. 1 Alat dan Bahan 3.1.1 Alat
Alat yang digunakan pada praktikum kali ini adalah : 1. Bejana berhubungan untuk diisi air dan larutan gula 2. Stopwatch untuk mengukur waktu
3. Refraktometer untuk mengukur kadar bahan dalam satuan brix 4. Pengaduk untuk mengaduk larutan
3.1.2 Bahan
Bahan yang digunakan pada praktikum kali ini adalah : 1. Air
2. Gula pasir
3. Kertas tissue
3. 2 Prosedur Percobaan
1. Membuka jepitan pada selang yang menghubungkan kedua gelas ukur yang berisi air serta larutan gula
2. Menghitung watunya menggunakan stopwatch.
3. Mengaduk air (untuk proses pengentalan) atau larutan gula (untuk proses pencairan) ketika menghitung debitnya dengan pengaduk
4. Menutup kembali selang yang menghubungkan kedua gelas ukur untuk sementara setelah terbuka selama satu menit
5. Mencatat perubahan volume pada salah satu gelas ukur (tergantung proses pengentalan atau pencairan)
6. Mengambil sedikit air atau air gula pada pengaduk dan meneteskan pada refraktometer dan melihat nilai kadar air dan gula yang terdapat pada refraktometer dalam satuan brix (sebagai xf)
8. Membuka kembali selang dan mengaduk air atau larutan gula dengan pengaduk
9. Mengambil sampel air atau larutan gula dan meneteskan pada refraktometer untuk melihat kadarnya setelah mencapai waktu 3 menit 10. Mengulangi prosedur ke-9 sebanyak delapan kali sampai mencapai
waktu pada menit ke-27
11. Mencatat setiap hasil (nilai kadar dalam refraktometer) pada tabel
12. Membuat grafik konsentrasi air dan konsentrasi larutan gula dengan persamaan ln(xf-xt) terhadap waktu (t)
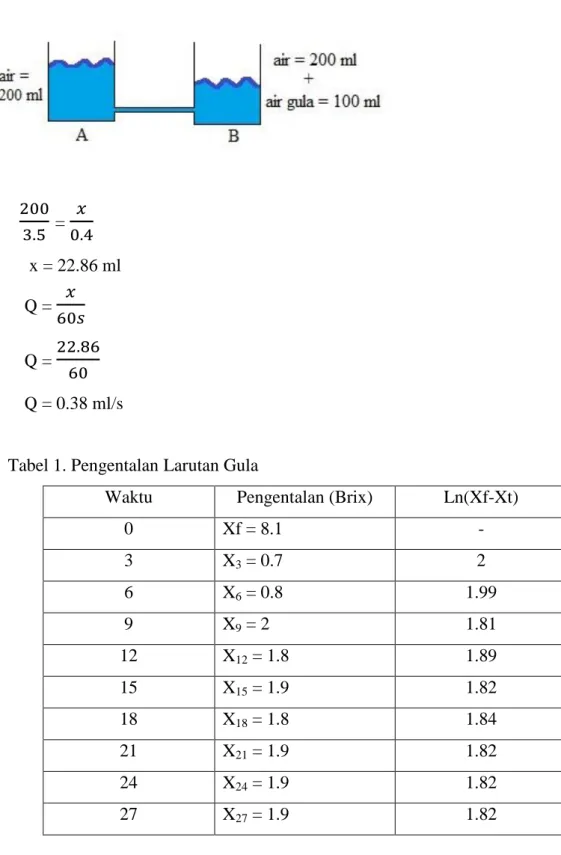
BAB IV HASIL PERCOBAAN 4. 1 Pengentalan = x = 22.86 ml Q =
Q = Q = 0.38 ml/s
Tabel 1. Pengentalan Larutan Gula
Waktu Pengentalan (Brix) Ln(Xf-Xt)
0 Xf = 8.1 - 3 X3 = 0.7 2 6 X6 = 0.8 1.99 9 X9 = 2 1.81 12 X12 = 1.8 1.89 15 X15 = 1.9 1.82 18 X18 = 1.8 1.84 21 X21 = 1.9 1.82 24 X24 = 1.9 1.82 27 X27 = 1.9 1.82
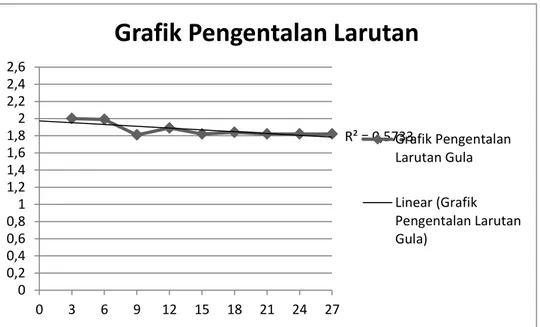
Grafik 1. Pengentalan Larutan 4. 2 Pengenceran Q =
Q = Q = 1 ml/s R² = 0,5733 0 0,2 0,4 0,6 0,8 1 1,2 1,4 1,6 1,8 2 2,2 2,4 2,6 0 3 6 9 12 15 18 21 24 27
Grafik Pengentalan Larutan
Grafik Pengentalan Larutan Gula Linear (Grafik Pengentalan Larutan Gula)
R² = 0,971 -20 -15 -10 -5 0 5 10 15 0 3 6 9 12 15 18 21 24 27
Grafik Pengenceran Larutan
Grafik Pengentalan Larutan
Linear (Grafik Pengentalan Larutan)
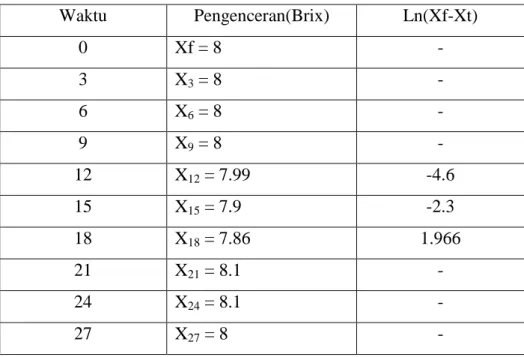
Tabel 2. Pengenceran Larutan Gula
Waktu Pengenceran(Brix) Ln(Xf-Xt) 0 Xf = 8 - 3 X3 = 8 - 6 X6 = 8 - 9 X9 = 8 - 12 X12 = 7.99 -4.6 15 X15 = 7.9 -2.3 18 X18 = 7.86 1.966 21 X21 = 8.1 - 24 X24 = 8.1 - 27 X27 = 8 -
4.3 Responsi
1. Pada evaporasi minyak bawang, bahan dimasukkan sebanyak 10000 kg/hari dengan kadar minyak 38%. Produk yang dihasilkan mengandung minyak bawang sebesar 74%. Hitung berat produk dan air yang teruapkan. Diketahui : Finput = 10000 kg/hari Km1 = 38% Km2 = 74% Ditanya :
a.) P (berat produk) b.) W (air yang teruapkan)
Jawab : a.) P (Produk) F = W + P 38% (10000) = 0 + 74%(P) P = P = 5153.135135 kg/hari
b.) W (air yang teruapkan) F = W + P W = F – P W = 10000-5153.135135 W = 4864.864865 kg/hari EVAPORASI W(air) Finput P(produk) Km2 = 74% Km1 = 38%
2. Dalam pembuatan selai buah-buahan dengan kandungan padatan 14% dibuat bubur dan dicampur dengan gula (1.22 kg gula/1 kg buah) dan pektin (0.0025 kg pektin/1 kg buah). Kemudian bahan dikurangi kadar airnya dengan pengeringan vacuum sehingga kadar air produk 33%. Untuk buah-buahan sebanyak 1000kg, berapa bahan yang keluar dari pencampuran, air teruapkan dan jumlah produk.
Diketahui :
Fbuah = 1000 kg
Fgula = 1.22 kg gula/1 kg buah Fpektin= 0.0025 kg pektin/ 1 kg buah Kp1 = 14%
Kap = 33%
Kp2 = 100% - 33% = 67% (kadar)
Ditanya :
a.) Pc (Bahan campuran) b.) W (air yang teruapkan) c.) Jumlah Produk
Jawab :
a.) P (bahan yang keluar dari campuran) F = W + P (1.22 x 1000) + (0.0025 x 1000) = 0 + 67%(P) 1362.5 kg = 0.67P Pengeringan Vacuum W(uap) Fbuah Fgula Fpektin P(produk) Kp2 = 33% Kp1 = 14%
P = 2033.582 kg
b.) W (air yang teruapkan) F = W + P
W = F – P
W = (Fgula.Fbuah + Fpektin.Fbuah + Fbuah) – P
W = ((1.22 x 1000) + (0.0025 x 1000) + 1000) – 2033.582 W = (1220 + 2.5 + 1000) – 2033.582 W = 2222.5 – 2033.582 W = 188.918 kg c.) Jumlah produk Jumlah Produk = W + P = 188.918 + 2033.582 = 2222.5 kg
3. Hitung jumlah udara yang harus diberikan untuk mengeringkan 107 g bahan dari kadar air 80% menjadi 5%. Udara yang masuk mempunyai kelembaban 0.002 kg uap air/kg udara dan udara keluar dengan kelembaban 0.3 kg uap air/ kg udara.
Diketahui : Fs = 107 g = 0.107 kg Ka1 = 15% Ka2 = 7% Ws1 = 0.8/(1-0.8) = 4 Ws2 = 0.05/(1-0.05) = 0.526
Wa1 = 0.002 kg uap air/ kg udara
Wa2 = 0.3 kg
Ditanya : Fa ?
Jawab : (Fa. Wa1) + (Fs. Ws1) = (Fa. Wa2) + (Fs. Ws2) (Fa x 0.002) + (0.107 x 4) = (Fa x 0.3) + (0.107 x 0.0526) 0.428 – 0.0056282 = 0.298Fa Fa = Fa = 1.417355034 kg
4. Komoditi pertanian dengan kadar air 20% dikeringkan sehingga mencapai kadar air 9%, menggunakan pengering tipe air flow drier. Udara pengering yang sudah digunakan untuk mengeringkan dialirkan kembali dan dicampur dengan udara yang berasal dari pemanas. Jika kelembaban udara dari pemanas 0.01 kg uap air/ kg udara dan kelembaban udara dari pengeringan digunakan lagi 0.1 kg uap air/kg udara dan kelembaban udara, untuk bahan sebanyak 107 kg/jam, berapa udara masuk yang dibutuhkan/jam, udara yang direcycle dan jumlah produk kering.
Dryer Fa. Wa1 Fa.Wa2 Fs. Ws2 Fs. Ws1 Fbahan= 107 kg/jam Kain = 20% Wf. Wc Kaout= 9% Fr.Wr Air flow drier
Diketahui : Kain = 20%
Kaout= 9%
Fbahan= 107 kg/jam
Wa’= 0,1 kg uap air/1 kg udara Wc= 0,03 kg uap air/1 kg udara Wf= 0,01 kg uap air/1 kg udara Ditanyakan :
a. Udara yang dibutuhkan (Ff) b. Udara yang direcycle (Fr) c. Jumlah produk kering (P)
Jawab :
a. (Ff + Fr) x Wc + Fbahan xWbahan = Fbahan’xWbahan’ + (Ff + Fr) x Wr
⁄ ⁄
(Ff + Fr) x Wc + Fbahan xWbahan = Fbahan’xWbahan’ + (Ff + Fr) x Wr
0,03 (Ff + Fr) + 107 x 0,176 = 107 x 0,075 + 0,1 (Ff + Fr) 0,03 (Ff + Fr) + 18,832 = 8,025 + 0,1 (Ff + Fr) 18,832 – 8,025 = 0,1 (Ff + Fr) – 0,03 (Ff + Fr) 10,807 = 0,07 (Ff + Fr) Fr = 154,386 – Ff . . . (1) b. Fc x Wc = Ff xWf + Fr x Wr (154,386 x 0,03) = Ff (0,01) + (154,386 - Ff) (0,1) 4,632 = 0,01 Ff + 15,4386 – 0,1 Ff 0,1 Ff – 0,01 Ff = 15,438 – 4,632 0,09 Ff = 10,806 ⁄
c. Substitusikan ke persamaan 1 : Fr = 154,386 – Ff = 154,386 – 120,067 = 34,319 kg/jam d. F = W + P 107 x 85% = 93% x P + 0 ⁄
BAB V PEMBAHASAN
Pada praktikum yang dilaksanakan kali ini membahas mengenai kesetimbangan massa dengan menghitung kadar dari larutan gula dengan menggunakan refraktometer. Kadar larutan yang dihitung terdiri dari kadar larutan ketika dilakukan proses pengentalan dan kadar larutan ketika dilakukan proses pengenceran. Perhitungan dilakukan setiap 3 menit.
Dari segi bentuk grafik yang terbentuk, dapat disimpulkan bahwa terjadi ketidakakuratan dari percobaan kali ini. Hal ini dapat terlihat dari grafik yang bentuknya tidak linear masih ada data yang kadarnya naik turun, seperti dalam pengentalan, begitupun yang terjadi pada pengenceran. Grafik yang terbentuk dalam percobaan kali ini bentuknya tidak beraturan. Seharusnya semakin lama waktu pengentalan, maka semakin tinggi nilai kadar bahannya. Begitu pula pada proses pengenceran, semakin lama waktu pengenceran maka semakin rendah nilai kadar bahannya.
Nilai kadar awal dari pengentalan gula adalah 8,1 Brix dan nilai akhirnya sebesar 1,9 brix, disini terjadi penurunan kadar gula yang sangat drastis pada awal pembukaan kran di menit 0-3 namun kembali naik dari nilai di menit ke 3, normal di menit berikutnya sesuai dengan keadaan bahwa pengentalan terjadi dengan naiknya nilai dari kadar bahan. Di menit ke 12 terjadi penurunan kembali, namun penurunan kali ini tidak begitu drastis dan nilai ini terus naik turun di angka 1,8-1,9 sampai pada menit ke 21 yang selanjutnya bersifat konstan sampai dengan menit ke 27. Maka, dapat diketahui bahwa pengukuran kali ini dirasa kurang akurat, hal ini dibuktikan dengan nilai dari kadar bahannya yang naik turun atau tidak terus menerus naik. Hal ini dapat disebabkan karena pembacaan nilai pada refraktometer yang dilakukan oleh praktikan kurang tepat atau teliti, terdapat kemungkinan bahwa mata pengamat tidak lurus ke depan sehingga pembacaannya kurang akurat, juga kemungkinan penggunaan refraktometer kurang bersih sehingga dapat mempengaruhi nilainya.
Untuk pengenceran larutan gula, nilai awalnya sebesar 8 brix dan nilai akhirnya tetap 8, namun disetiap menitnya tidak konstan 8 dibeberapa menit
terjadi nilai kadar yang naik turun seperti di menit ke 12 nilai kadarnya mengalami sedikit penurunan di angka 7,99 begitupun di menit ke 15 menjadi 7,9 serta di menit ke 18 menjadi 7,86. Hal ini bersesuaian bahwa pada pengenceran terjadi penurunan nilai kadar bahan, namun di menit ke 21 terjadi kenaikan menjadi 8,1 sampai pada menit ke-24 dan turun kembali ke nilai awak di angka 8 pada menit ke 27, lalu dapat dikatakan pula bahwa larutan gula ini jenuh di nilai 8 karena nilai yang naik maupun turun tidak jauh berkisar dari nilai 8. Kenaikan nilai bahan yang terjadi di menit ke 21 tentu tidak bersesuaian dengan teori bahwa dalam pengenceran terjadi penurunan nilai dari kadar bahan, maka dapat diketahui bahwa pengukuran kali ini dirasa kurang akurat, hal ini dibuktikan dengan nilai dari kadar bahannya yang naik turun atau tidak terus menerus turun. Hal ini dapat disebabkan karena pembacaan nilai pada refraktometer yang dilakukan oleh praktikan kurang tepat atau teliti, terdapat kemungkinan bahwa mata pengamat tidak lurus ke depan sehingga pembacaannya kurang akurat, juga kemungkinan penggunaan refraktometer kurang bersih sehingga dapat mempengaruhi nilainya.
Waktu pada pengukuran kali ini sama yaitu 27 menit namun perubahan pada nilai pengentalan dan pengenceran jauh berbeda, dimana pada pengenceran terjadi perubahannya relatif berlangsung lama dan perubahannya sangat sedikit sehinga dapat dikatakan bahwa laju pengenceran larutan lebih lama dibandingkan dengan laju pengentalan larutan.
Dalam praktikum juga terdapat beberapa kendala yaitu keterbasan peralatan praktikum. Alat yang tersedia hanya dua buah saja, yang terdiri dari satu alat untuk pengentalan dan satu alat lainnya untuk pengenceran. Selain itu, peralatan yang digunakan pun kondisinya sudah tidak baik sehingga dapat memicu ketidakakuratan dalam proses percobaan. Selang yang seharusnya dapat mengalirkan air dari gelas ukur ke gelas ukur yang lainnya terjepit sehingga air yang akan mengalir tertahan. Refraktometer juga hanya satu sehingga menyebabkan pemakaian harus dilakukan secara bergantian. Hal tersebut menyebabkan tidak efisiennya waktu praktikum.
BAB VI PENUTUP
6. 1 Kesimpulan
1. Semakin tinggi nilai kadar bahan dalam larutan maka semakin pekat atau semakin besar pula kekentalan dalam larutan tersebut
2. Semakin rendah nilai kadar bahan dalam larutan maka semakin cair larutan tersebut
3. Perubahan nilai dari pengentalan maupun pengenceran dipengaruhi oleh waktu
6. 2 Saran
1. Sebelum melakukan praktikum, sebaiknya praktikan sudah memahami prosedur yang akan dilaksanakan agar praktikum berjalan dengan lancar dan efektif.
2. Agar hasilnya menjadi akurat, pada saat melakukan praktikum, praktikan harus teliti dan serius karena hasil yang akan didapatkan benar-benar tergantung dengan ketelitian praktikan.
3. Sebaiknya peralatan praktikum tersedia lengkap dan kondisinya baik sehingga percobaan dapat lebih akurat dan praktikum yang dilakukan lebih efisien.
4. Sebaiknya larutan tidak hanya satu jenis agar praktikan dapat membandingkan laju pengenceran dan pengentalannya.
DAFTAR PUSTAKA
Khopkar S. M., 1990, Konsep Dasar Kimia Analitik, Universitas Indonesia : Jakarta
“Hukum Kekekalan Massa”. 20 September 2015. https://id.wikipedia.org/wiki/Hukum_kekekalan_massa
“Hukum Kekekalan Massa pada Reaksi Kimia”. 20 September 2015. http://ardra.biz/sain-teknologi/ilmu-kimia/hukum-kekekalan-massa-pada-reaksi-kimia/
Triyadi, Rikky. “Pengentalan dan Penguapan Produk”. 20 September 2015
http://triyadirikky06.blogspot.co.id/2011/10/pengentalan-dan-penguapan-produk.html
Utami, Gusti A.A Mirah. “Analisis Markov”. 20 September 2015 http://gustimirah.blogspot.co.id/2009/12/analisis-markov.html
Refraktometer. 20 September 2015.
LAMPIRAN
Gambar 1. Refraktometer Gambar 2. Batang Pengaduk