OPTIMASI METODE BIOANALISIS KAFEIN DALAM SAMPEL DARAH ORANG JAWA DENGAN METODE KROMATOGRAFI CAIR KINERJA
TINGGI FASE TERBALIK
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Jonathan Ronny Kurniawan
NIM : 138114126
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
OPTIMASI METODE BIOANALISIS KAFEIN DALAM SAMPEL DARAH ORANG JAWA DENGAN METODE KROMATOGRAFI CAIR KINERJA
TINGGI FASE TERBALIK
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Jonathan Ronny Kurniawan
NIM : 138114126
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
HALAMAN PERSEMBAHAN
Kupersembahkan karya ini untuk
Tuhan Yesus Kristus yang selalu memberikan hal yang terbaik
untukku,
Orang tua ku yang telah mengasihi aku dan membesarkan
aku dari aku kecil dengan penuh kasih sayang,
Sahabat-sahabatku yang selalu mendukungku,
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi saya yang berjudul “Optimasi Metode Bioanalisis Kafein dalam Sampel Darah Orang Jawa dengan Metode Kromatografi Cair Kinerja Tinggi Fase Terbalik” tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, dengan mengikuti ketentuan sebagaimana layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarisme dalam naskah ini, maka saya bersedia menanggung segala sanksi sesuai peraturan perundang-undangan yang berlaku.
Yogyakarta, 9 Januari 2017 Penulis
LEMBAR PERNYATAAN PERSETUJUAN
PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma :
Nama : Jonathan Ronny Kurniawan
Nomor Mahasiswa : 138114126
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul :
“OPTIMASI METODE BIOANALISIS KAFEIN DALAM SAMPEL DARAH
ORANG JAWA DENGAN METODE KROMATOGRAFI CAIR KINERJA
TINGGI FASE TERBALIK”
Beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di Internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini saya buat dengan sebenarnya.
Dibuat di Yogyakarta
Pada tanggal : 9 Januari 2017
Yang menyatakan
PRAKATA
Puji dan syukur penulis panjatkan kehadirat Tuhan Yang Maha Esa, atas berkat,
cinta kasih dan penyertaan-Nya penulis dapat menyelesaikan penelitian dan penyusunan naskah skripsi yang berjudul “Optimasi Metode Bioanalisis Kafein dalam Sampel Darah Orang Jawa dengan Metode Kromatografi Cair Kinerja Tinggi Fase Terbalik”. Skripsi ini merupakan salah satu syarat untuk memperoleh gelar Sarjana Farmasi (S.Farm) di Fakultas Farmasi Universitas Sanata Dharma,
Yogyakarta.
Penulis menyadari bahwasannya dalam penyusunan naskah ini tidak lepas dari
bantuan dan dukungan berbagai pihak, oleh karena itu pada kesempatan ini penulis
hendak menyampaikan terimakasih kepada :
1. Ibu Aris Widayati, M.Si., Ph.D., Apt., selaku Dekan Fakultas Farmasi,
Universitas Sanata Dharma, Yogyakarta.
2. Ibu Dr. Christine Patramurti, M.Si., Apt., selaku dosen pembimbing utama atas
kesabaran, bimbingan, pengarahan, dan dukungan selama penelitian hingga
penyusunan naskah skripsi ini.
3. Bapak Florentinus Dika Octa Riswanto, M.Sc., selaku dosen pembimbing
pendamping atas kesabaran, bimbingan, pengarahan, dan dukungan selama
penelitian hingga penyusunan naskah skripsi ini.
4. Bapak Maywan Hariono, M.Si., Ph.D., Apt., selaku dosen penguji yang telah
memberikan kritik dan saran yang membangun hingga skripsi ini tersusun.
5. Ibu Dr. Dewi Setyaningsih, M.Sc., Apt., selaku dosen penguji yang telah
memberikan kritik dan saran yang membangun hingga skripsi ini tersusun.
6. Ibu Dita Maria Virginia, S.Farm., M.Sc., Apt., selaku Dosen Pembimbing
Akademik atas bimbingan selama ini.
8. Keluarga tersayang Bapak Sugiono, Ibu Veronica Setyawati, Kakak Jessica
Novia Fransisca dan Linda Evelina Larisa, atas segala kasih, cinta, nasehat,
saran, dukungan, dan doa yang selalu mengiringi langkah penulis.
9. Teman skripi bioanalisis kafein, Suryatmoko Agung, terimakasih untuk
dukungan dan bantuannya selama ini.
10. Sahabat-sahabat penulis, Kadek Ida Krisnadewi, Ivana Tunggal, RR Kirana
Andranilla, Yohanes Medika, Lia Elisa, Cindy dan Regina Eva Angelista,
terimakasih untuk kebersamaan yang terjalin, semangat dan dukungan selama ini.
11. Teman-teman “Kos Wiratha” atas kebersamaannya selama ini.
12. Serta semua pihak yang telah banyak membantu penulis dalam menyelesaikan
naskah skripsi ini, namun tidak dapat penulis sebutkan satu per satu.
Penulis menyadari bahwa tidak ada manusia yang sempurna, demikian juga
untuk skripsi ini yang masih jauh dari kata sempurna. Oleh karena itu penulis
mengharapkan adanya kritik dan saran yang membangun, sehingga skripsi ini
dapat berguna bagi perkembangan ilmu pengetahuan serta bagi para pembaca.
Yogyakarta, Desember 2016
ABSTRAK
Metabolisme kafein pada orang jawa terjadi secara lambat sehingga berpotensi menyebabkan toksisitas, oleh karena itu penting untuk dilakukan Therapeutic Drug Monitoring (TDM). TDM dilakukan untuk menentukan dosis obat yang efektif dalam darah sehingga dapat memonitor terjadinya toksisitas. TDM perlu pengembangan metode baru untuk analisis kafein pada orang jawa sehingga dapat digunakan untuk analisis rutin. Tujuan dari penelitian ini untuk mengembangkan metode baru untuk analisis kafein dalam sampel darah jawa menggunakan Kromatografi Cair Kinerja Tinggi (KCKT) fase terbalik. Standar internal (SI) yang digunakan dalam penelitian ini adalah asetanilida. Pengembangan metode yang dilakukan dalam penelitian ini adalah optimasi komposisi fase gerak dan kecepatan alir fase gerak. Optimasi komposisi fase gerak menggunakan aqua bidestilata:metanol dengan perbandingan 40:60; 50:50; dan 60:40 serta kecepatan alir 0,5 mL/menit dan 1,0 mL/menit. Fase diam yang digunakan adalah Phenomenex® C18 kolom (dimensi 250 x 4,6 mm, ukuran partikel 5 µm). Deteksi UV dilakukan setelah pemisahan kromatografi pada 255 nm. Parameter yang digunakan pada penelitian ini adalah nilai faktor tailing, resolusi, waktu retensi, HETP dan koefisien variansi (CV) dari nilai faktor tailing, waktu retensi dan HETP. Hasil penelitian menunjukkan komposisi fase gerak yang optimal adalah aquabidestilata: metanol (50:50) dan laju alir optimum fase gerak adalah 1,0 mL / menit.
ABSTRACT
A slow metabolism of caffeine in Javanese increases its potential of toxicity, therefore it is important to do Therapeutic Drug Monitoring (TDM). TDM is aimed to determine drug level in the blood, so it can control toxicity. TDM needs a development of new methods for the analysis of caffeine in the Javanese, so it can be applied for routine analysis. The aim of this study was developing new method for analysis of caffeine in javanese blood sample using reverse phase High Performance Liquid Chromatography (HPLC). Internal standard (IS) used in this research was acetanilide. The method development performed in this research were optimization of mobile phase composition and its flow rate. The optimization of mobile phase composition using re-distiled water: methanol in the ratio of 40:60; 50:50; and 60:40 then a flow rate 0.5 mL/minute and 1,0 mL/minute. The stationary phase being used was Phenomenex® C18 column (dimensions 250x4.6 mm, particle size 5m). The UV
detection was performed after chromatographic separation at 255 nm. The Parameter being used in this study are value of tailing factor, resolution, retention time, HETP and the coefficient of variance (CV) of those individual parameters. The results indicated that the optimum mobile phase composition was re-destiled water : methanol (50:50) with optimum flow rate of mobile phase is 1.0 mL/minute.
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
PERNYATAAN PERSETUJUAN PUBLIKASI ... vi
PRAKATA ... vii
Pembuatan larutan baku kafein ... 3
Pembuatan larutan standar internal (SI) ... 3
Penentuan panjang gelombang pengamatan kafein dan SI ... 3
Optimasi sistem Kromatografi Cair Kinerja Tinggi (KCKT) ... 4
DAFTAR TABEL
Tabel I. Nilai tailing factor dan waktu retensi dari kafein dan kandidat SI (asetanilida,
nikotinamida, papaverin) pada optimasi………..………..………....8
Tabel II. Nilai tf dan tR kafein dan SI pada berbagai tingkat…...………..………...12
Tabel III. Data nilai tailing factor kafein dan SI (asetanilida), nilai waktu retensi
kafein dan SI (asetanilida), nilai resousi kafein dan SI (asetanilida), dan nilai
DAFTAR GAMBAR
Gambar 1. Kromatogram tumpang tindih antara blanko plasma dengan senyawa
kafein dan beberapa kandidat SI (asetanilida, nikotinamida dan papaverin)
menggunakan sistem KCKT yang optimum (fase diam kolom C18:250 x
4,6 mm, 5µm; fase gerak campuran aquabidestilata : metanol dengan
perbandingan 60:40; kecepatan alir 1,0 mL/menit………7
Gambar 2. Tumpang tindih spektrum senyawa kafein dan asetanilida. Pembacaan
absorbansi menggunakan spektrofotometer UV pada panjang gelombang
200nm - 400nm……….………8
Gambar 3. Kromatogram senyawa: Kafein dan SI Asetanilida dalam sampel plasma
menggunakan sistem KCKT yang optimum (fase diam C18:250 x 4,6 mm,
5µm; fase gerak campuran aquabidestilata : metanol dengan perbandingan
50:50; kecepatan alir 1,0 mL/menit; detektor UV 255 nm………...9
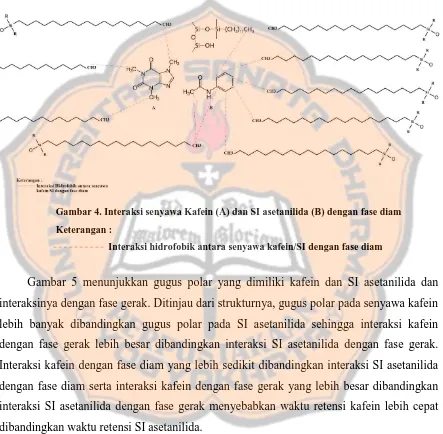
Gambar 4. Interaksi senyawa kafein dan SI asetanilida dengan fase
diam…...……..………..………..………..………..…10
Gambar 5. Senyawa kafein dan SI asetanilida dengan gugus polarnya serta interaksinya dengan fase gerak aquabidestilata (H2O) dan metanol
DAFTAR LAMPIRAN
Lampiran 1. Surat ijin penelitian skripsi oleh dinas perizinan kota Yogyakarta …...15
Lampiran 2. Hasil pembacaan absorbansi senyawa kafein dan SI asetanilida
menggunakan spektrofotometer UV.…… ………....………16
Lampiran 3. Hasil pembacaan absorbansi senyawa kafein dan SI papaverin
menggunakan spektrofotometer UV………...………..……….…17
Lampiran 4. Hasil pembacaan absorbansi senyawa kafein dan SI nikotinamida
menggunakan spektrofotometer UV……….……….……18
Lampiran 5. Sertifikat analisis working standar kafein………...……19
Lampiran 6. Surat permohonan ijin penelitian dan pengambilan data…...…….……20
Lampiran 7. Surat permohonan bahan penelitian dari PMI kota Yogyakarta…….…21
Lampiran 8. Kuisioner donor darah ………..…………..………22
Lampiran 9. Campuran kafein dan nikotinamida mengunakan fase gerak
aquabidestilata:metanol (40:60) kecepatan alir 0,5 mL/menit ...……..26
Lampiran 10. Campuran kafein dan nikotinamida mengunakan fase gerak
aquabidestilata:metanol (50:50) kecepatan alir 0,5 mL/menit ..…...…27
Lampiran 11. Campuran kafein dan nikotinamida mengunakan fase gerak
aquabidestilata:metanol (60:40) kecepatan alir 0,5 mL/menit .………28
Lampiran 12. Campuran kafein dan nikotinamida mengunakan fase gerak
Lampiran 13. Campuran kafein dan nikotinamida mengunakan fase gerak
aquabidestilata:metanol (50:50) kecepatan alir 1,0 mL/menit………..30
Lampiran 14. Campuran kafein dan nikotinamida mengunakan fase gerak
aquabidestilata:metanol (60:40) kecepatan alir 1,0 mL/menit …….…31
Lampiran 15. Kromatogram papaverin 4 g/mL mengunakan fase gerak
aquabidestilata:metanol (50:50) kecepatan alir 1,0 mL/menit ...…..…32
Lampiran 16. Kromatogram papaverin 4 g/mL mengunakan fase gerak
aquabidestilata:metanol (60:40) kecepatan alir 1,0 mL/menit …….…33
Lampiran 17. Kromatogram asetanilida 8 g/mL mengunakan fase gerak
aquabidestilata:metanol (50:50) kecepatan alir 1,0 mL/menit …….…34
Lampiran 18. Kromatogram asetanilida 8 g/mL mengunakan fase gerak
aquabidestilata:metanol (60:40) kecepatan alir 1,0 mL/menit …….…35
Lampiran 19. Kromatogram blanko plasma A mengunakan fase gerak
aquabidestilata:metanol (50:50) kecepatan alir 1,0 mL/menit …….…36
Lampiran 20. Kromatogram blanko plasma B mengunakan fase gerak
aquabidestilata:metanol (50:50) kecepatan alir 1,0 mL/menit …….…37
Lampiran 21. Kromatogram blanko plasma C mengunakan fase gerak
aquabidestilata:metanol (50:50) kecepatan alir 1,0 mL/menit …….…38
Lampiran 22. Kromatogram blanko plasma D mengunakan fase gerak
Lampiran 23. Kromatogram blanko plasma E mengunakan fase gerak
aquabidestilata:metanol (50:50) kecepatan alir 1,0 mL/menit …….…40
Lampiran 24. Seri 1 (kafein 1,6 g/mL dan asetanilida 4 g/mL) replikasi 1
mengunakan fase gerak aquabidestilata:metanol (50:50) kecepatan alir
1,0 mL/menit ...….………..…….…….…….…….…….…….…….…41
Lampiran 25. Seri 1 (kafein 1,6 g/mL dan asetanilida 4 g/mL) replikasi 2
mengunakan fase gerak aquabidestilata:metanol (50:50) kecepatan alir
1,0 mL/menit ...….………..…….…….…….…….…….…….…….…42
Lampiran 26. Seri 1 (kafein 1,6 g/mL dan asetanilida 4 g/mL) replikasi 3
mengunakan fase gerak aquabidestilata:metanol (50:50) kecepatan alir
1,0 mL/menit ...….………..…….…….…….…….…….…….…….…43
Lampiran 27. Seri 2 (kafein 8 g/mL dan asetanilida 8 g/mL) replikasi 1
mengunakan fase gerak aquabidestilata:metanol (50:50) kecepatan alir
1,0 mL/menit .….………....…….…….…….…….…….…….…….…44
Lampiran 28. Seri 2 (kafein 8 g/mL dan asetanilida 8 g/mL) replikasi 2
mengunakan fase gerak aquabidestilata:metanol (50:50) kecepatan alir
1,0 mL/menit .….………....…….…….…….…….…….…….…….…45
Lampiran 29. Seri 2 (kafein 8 g/mL dan asetanilida 8 g/mL) replikasi 3
mengunakan fase gerak aquabidestilata:metanol (50:50) kecepatan alir
Lampiran 30. Seri 3 (kafein 18 g/mL dan asetanilida 12 g/mL) replikasi 1
mengunakan fase gerak aquabidestilata:metanol (50:50) kecepatan alir
1,0 mL/menit .….………....…….…….…….…….…….…….…….…47
Lampiran 31. Seri 3 (kafein 18 g/mL dan asetanilida 12 g/mL) replikasi 2
mengunakan fase gerak aquabidestilata:metanol (50:50) kecepatan alir
1,0 mL/menit .….………....…….…….…….…….…….…….…….…48
Lampiran 32. Seri 3 (kafein 18 g/mL dan asetanilida 12 g/mL) replikasi 3
mengunakan fase gerak aquabidestilata:metanol (50:50) kecepatan alir
1,0 mL/menit .….………....…….…….…….…….…….…….…….…49
Lampiran 33. Kromatogram Uji Kesesuaian Sistem 1 (kafein 12 g/mL dan
asetanilida 8 g/mL) mengunakan fase gerak aquabidestilata:metanol
(50:50) kecepatan alir 1,0 mL/menit .….………....…….… ……….…50
Lampiran 34. Kromatogram Uji Kesesuaian Sistem 2 (kafein 12 g/mL dan
asetanilida 8 g/mL) mengunakan fase gerak aquabidestilata:metanol
(50:50) kecepatan alir 1,0 mL/menit .….………....…….… ……….…51
Lampiran 35. Kromatogram Uji Kesesuaian Sistem 3 (kafein 12 g/mL dan
asetanilida 8 g/mL) mengunakan fase gerak aquabidestilata:metanol
(50:50) kecepatan alir 1,0 mL/menit .….………....…….… ……….…52
Lampiran 36. Kromatogram Uji Kesesuaian Sistem 4 (kafein 12 g/mL dan
asetanilida 8 g/mL) mengunakan fase gerak aquabidestilata:metanol
Lampiran 37. Kromatogram Uji Kesesuaian Sistem 5 (kafein 12 g/mL dan
asetanilida 8 g/mL) mengunakan fase gerak aquabidestilata:metanol
(50:50) kecepatan alir 1,0 mL/menit .….………....…….… ……….…54
Lampiran 38. Kromatogram Uji Kesesuaian Sistem 6 (kafein 12 g/mL dan
asetanilida 8 g/mL) mengunakan fase gerak aquabidestilata:metanol
(50:50) kecepatan alir 1,0 mL/menit .….………....…….… ……….…55
Lampiran 39. Perhitungan konsentrasi larutan seri pada tahap optimasi pemisahan
kafein dan SI asetanilida dalam plasma .….………....…….……….….56
Lampiran 40. Perhitungan konsentrasi larutan seri pada tahap uji kesesuaian sistem
………....57
Lampiran 41. Contoh perhitungan konsentrasi kafein dan asetanilida dari
penimbangan, perhitungan konsentrasi larutan stok dan perhitungan
PENDAHULUAN
Kafein merupakan zat psikoaktif dan juga berperan sebagai stimulan sistem saraf
pusat (Joewana, 2005). Konsumsi kafein yang berlebihan menyebabkan peningkatan
hormon stress, peningkatan tekanan darah, cemas, pusing, kelelahan dan gangguan tidur
(Pedak, 2009). Waktu paruh dari kafein adalah 3,5 jam, tetapi metabolisme kafein pada
orang yang memiliki penyakit liver atau ibu hamil lebih lambat sehingga waktu paruhnya
lebih lama (Key dan Hayes, 1996). Kecepatan metabolisme obat dipengaruhi oleh
beberapa faktor, yaitu induksi enzim, inhibisi enzim, usia, penyakit, dan faktor genetik
(Neal, 2006). Kecepatan metabolisme obat dipengaruhi oleh faktor genetik, salah satunya
adalah perbedaan komposisi enzim pada ras/suku yang berbeda sehingga menyebabkan
perbedaan kemampuan metabolisme obat.
Enzim Sitokrom P450 2A6 (CYP2A6) merupakan enzim yang bertanggung jawab
terhadap metabolisme beberapa obat seperti kafein, efavirenz, letrozole, nikotin,
pilocarpine dan tegafur. CYP2A6*4 adalah salah satu alel dari enzim CYP2A6 yang
merupakan alel non aktif sehingga menyebabkan penurunan kecepatan metabolisme kafein
(Anonim, 2012). Polimorfisme genetis enzim CYP2A6 dengan frekuensi alel CYP2A6*4
yang tinggi secara signifikan menurunkan kemampuan metabolisme kafein sehingga
kemampuan metabolisme kafein menjadi lambat. Berdasarkan penelitian Patramurti, dkk
(2015) dikatakan adanya polimorfisme genetik dimana frekuensi alel CYP2A6*4 pada
orang jawa tinggi jumlahnya sehingga kemampuan memetabolisme kafein pada orang jawa
menjadi lambat. Metabolisme kafein yang lambat pada orang jawa berpotensi terjadinya
toksisitas, sehingga dapat dikatakan pentingnya dilakukan Therapeutic Drug Monitoring
(TDM). TDM sangat penting dalam bidang farmasi untuk mengukur kadar obat dalam
aliran darah selama interval waktu tertentu. TDM penting dilakukan untuk menentukan
dosis obat yang efektif dalam darah, sehingga dapat mencegah terjadinya keadaan toksik
atau keracunan obat di dalam tubuh. TDM melibatkan pengukuran konsentrasi obat pada
berbagai sampel biologis seperti darah (Kang dan Lee, 2009). Metode yang spesifik untuk
aplikasi TDM senyawa kafein pada orang jawa diperlukan untuk menghasilkan data yang
representatif, efektif, efisien, akurat dan presisi. Perlu dilakukan pengembangan metode
baru untuk analisis kafein pada orang jawa sehingga dapat digunakan untuk analisis rutin.
Metode analisis kafein yang sudah pernah dilakukan oleh peneliti terdahulu dapat
Pada penelitian jurnal oleh Alvi dan Hammami (2011) dilakukan analisis kafein
dalam plasma sintetik menggunakan fase gerak kalium fosfat dan asetonitril dengan
perbandingan 83:17. Panjang gelombang pada penelitian tersebut diatur sebesar 274 nm.
Waktu retensi senyawa kafein yang dihasilkan < 10 menit, namun resolusi antara puncak
senyawa kafein dengan puncak senyawa lain yang berdekatan sehingga belum memenuhi
persyaratan analisis. Plasma sintetik yang digunakan pada penelitian tersebut kurang
representatif jika digunakan untuk aplikasi TDM pada orang jawa karena sampel plasma
sintetik memiliki komposisi yang berbeda dengan sampel darah orang jawa. Hasil analisis
akan lebih representatif jika menggunakan sampel darah orang jawa.
Pada penelitian skripsi oleh Irmanto (2008) dilakukan analisis kafein menggunakan
instrumen KCKT fase terbalik dengan fase gerak aquabidestilata dan metanol. Penelitian
tersebut diawali dengan tahap optimasi. Fase gerak aquabidestilata dan metanol pada
penelitian tersebut dijadikan acuan sebagai fase gerak pada penelitian ini.
Berdasarkan review artikel oleh Patil (2012), disebutkan beberapa penelitian tentang
analisis kafein menggunakan berbagai sampel seperti minuman kopi, plasma sintetik,
campuran obat dan teh. Berdasarkan review tersebut, analisis senyawa kafein dapat
dilakukan dengan menggunakan metode KCKT fase terbalik, metode KCKT elusi gradien
dan metode UHPLC. Pada penelitian ini juga digunakan metode KCKT fase terbalik.
Pengembangan metode diperlukan untuk kepentingan analisis kafein. Pengembangan
metode ini dilakukan melalui dua tahapan yaitu optimasi metode dan validasi metode.
Sebelum dilakukan validasi metode perlu dilakukan tahapan optimasi terlebih dahulu.
Penelitian yang dilakukan yaitu optimasi pada sistem KCKT untuk mendapatkan parameter
optimasi yang optimal. Parameter optimasi tersebut meliputi nilairesolusi senyawa kafein
dan SI asetanilida dengan senyawa lain yang puncaknya berdekatan, tailing factor (kafein
dan SI asetanilida) , waktu retensi (kafein dan SI asetanilida), nilai HETP (kafein dan SI
asetanilida), dan nilai koefisien variansi (CV) dari tailing factor, waktu retensi dan HETP
untuk kafein dan SI asetanilida.
METODE PENELITIAN Bahan
Sampel plasma darah orang jawa dari PMI kota Yogyakarta, metanol (p.a grade) (E
Merck), aquabidestilata, baku kafein (sertifikat analisis working standard,
no.002/WS/RD/I/2012, MA USP 34), baku asetanilida, baku nikotinamida dan baku
Alat
KCKT Shimadzu LC-2010C dengan detektor sinar UV, kolom C18 merek
Phenomenex® (250 x 4,6 mm, ukuran partikel 5µm), seperangkat komputer (merek Dell
B6RDZIS Connexant system RD01-D850 A03-0382 JP France S.A.S, printer HP Deskjet
1000 J110a), Spektrofotometer UV Shimadzu UV-1800, milipore, ultrasonikator Retsch
tipe : T460 (Schwing 1 PXE, FTZ-Nr, C-066/83, HF-frequ:35 kHz), timbangan analitik
SCALTEC (max 60/210 g, min 0,001 g; d = 0,01/0,1 mg), penyaring Whatman 0,45 µm,
alat vakum GAST, sentrifugator Thermo scientific Heraeus Pico 17/21 dan
peralatan-peralatan gelas.
Metode
Optimasi pemisahan senyawa kafein dan SI pada sistem KCKT fase terbalik
dilakukan dengan berbagai komposisi fase gerak yang terdiri dari campuran
aquabidestilata : metanol dengan perbandingan 40:60; 50:50 dan 60:40. Selain
perbandingan komposisi fase gerak, dilakukan juga optimasi kecepatan alir fase gerak pada
0,5 dan 1,0 mL/menit. Volume injeksi sejumlah 20 L. Plasma darah yang didapatkan dari
PMI kota Yogyakarta disimpan pada pendingin dengan temperatur -70 oC.
Pembuatan Larutan Stok dan Intermediet Kafein
Sejumlah kafein ditimbang seksama lebih kurang sebanyak 20 mg dan dilarutkan
pada pelarut metanol 50% dalam labu takar volume 5 mL sehingga didapat larutan stok
kafein dengan konsentrasi 4 mg/mL. Dari larutan stok kafein, dibuat larutan intermediet
kafein dengan konsentrasi 800 g/mL. Larutan stok dan intermediet kafein selalu dibuat
baru.
Pembuatan Larutan Standar Internal (SI)
Pada penelitian ini dilakukan optimasi pemilihan SI, adapun SI yang digunakan
adalah nikotinamida, papaverin dan asetanilida. Masing-masing SI tersebut ditimbang
seksama lebih kurang sebanyak 20 mg dan dan dilarutkan pada pelarut metanol 50% dalam
labu takar volume 5 mL sehingga didapat konsentrasi 4 mg/mL. Untuk memudahkan
pengenceran di tahap selanjutnya maka dibuat larutan intermediet SI dengan konsentrasi
320 g/mL. Larutan stok dan intermediet masing-masing kandidat SI selalu dibuat baru.
Penentuan Panjang Gelombang Pengamatan Kafein dan SI dengan Spektrofotometer UV
µg/mL. Masing-masing larutan seri kafein tersebut dibaca absorbansinya menggunakan
spektrofotometer UV pada panjang gelombang antara 200-400 nm.
Larutan seri SI dibuat dengan cara mengencerkan larutan intermediet SI 320 g/mL
menggunakan pelarut metanol 50% sehingga didapatkan konsentrasi 4, 8, dan 12 µg/mL
untuk SI asetanilida; 10, 15, dan 20 µg/mL untuk SI nikotinamida; dan 2, 4, dan 6 µg/mL
untuk SI papaverin. Masing-masing larutan seri SI tersebut dibaca absorbansinya
menggunakan spektrofotometer UV pada panjang gelombang antara 200-400 nm.
Spektrum yang dihasilkan ditumpang tindihkan, lalu dipilih panjang gelombang
pengamatan yang akan digunakan untuk deteksi pada sistem KCKT baik pada kafein
maupun SI.
Optimasi Sistem KCKT
Optimasi pemilihan standar internal. Larutan kerja kafein dibuat dengan mengencerkan
larutan intermediet kafein 800 g/mL menggunakan pelarut metanol 50 % sehingga
didapatkan konsentrasi larutan kafein 10 µg/mL. Larutan disaring menggunakan milipore
lalu diawaudarakan menggunakan ultrasonikator sehingga larutan kerja kafein siap
diinjeksikan ke sistem KCKT.
Larutan kerja SI dibuat dengan mengencerkan larutan intermediet SI 320 g/mL
menggunakan pelarut metanol 50 % sehingga didapatkan konsentrasi larutan SI 8 µg/mL
untuk SI asetanilida; 10 g/mL untuk SI nikotinamida dan 4 g/mL untuk SI papaverin.
Larutan di saring menggunakan milipore lalu diawaudarakan menggunakan ultrasonikator
sehingga larutan kerja SI siap diinjeksikan ke sistem KCKT.
Larutan blanko plasma dibuat dengan mengambil plasma darah sebanyak 600 µL,
kemudian dipindahkan ke dalam tube, lalu ditambahkan 400 µL pelarut metanol 50 %,
divortex selama 30 detik. Dari tube tersebut, larutan diambil sebanyak 500 µ L lalu
ditambahkan metanol sebanyak 1500 µ L dalam tabung sentrifugasi. Sehingga didapatkan
volume total 2000 µL. Lalu tabung sentrifugasi divortex selama 30 detik dan disentrifugasi
selama 10 menit dengan kecepatan 10000 rpm. Cairan supernatan dipisahkan, kemudian
disaring dengan millipore. Selanjutnya dilakukan diawaudarakan menggunakan
ultrasonikator selama 5 menit sehingga supernatan siap di injeksikan ke sistem KCKT.
Sejumlah 20,0 L masing-masing larutan tersebut (larutan kerja kafein, larutan kerja SI
dan larutan blanko plasma) diinjeksikan ke sistem KCKT secara terpisah dengan berbagai
komposisi fase gerak dan kecepatan alir. Tumpang tindih dari kromatogram larutan kerja
SI yang menghasilkan tailing factor dan pemisahan puncak terbaik dari senyawa lain yang
berdekatan dipilih untuk dijadikan SI pada penelitian ini.
Optimasi komposisi fase gerak dan kecepatan alir dalam pelarut. Kromatogram
larutan kerja kafein dan larutan kerja SI yang didapat pada tahap optimasi pemilihan
standar internal ditumpang tindih, lalu diamati waktu retensi, tailing factor dan pemisahan
puncaknya. Komposisi fase gerak dan kecepatan alir yang menghasilkan waktu retensi,
tailing factor dan pemisahan puncak terbaik dipilih untuk digunakan pada penelitian ini.
Optimasi pemisahan kafein dan SI Asetanilida dalam plasma. Diambil plasma darah
sebanyak 600 µL, kemudian dipindahkan ke dalam tube, lalu ditambahkan 200 µL larutan
seri SI asetanilida, dan 200 µL larutan seri kafein. dan divortex selama 30 detik. Adapun
konsentrasi larutan seri kafein dan larutan seri SI asetanilida yang ditambahkan yaitu
larutan seri kafein 32 µg/mL dengan larutan seri SI asetanilida 80 µg/mL; larutan seri
kafein 160 µg/mL dengan larutan seri SI asetanilida 160 µg/mL; dan larutan seri kafein
360 µg/mL dengan seri SI asetanilida 240 µg/mL. Dari tube tersebut, larutan diambil
sebanyak 500 µ L lalu ditambahkan metanol sebanyak 1500 µ L dalam tabung sentrifugasi
sehingga didapatkan volume total 2000 µL. Lalu tabung sentrifugasi divortex selama 30
detik dan disentrifugasi selama 10 menit dengan kecepatan 10000 rpm. Cairan supernatan
dipisahkan, kemudian disaring dengan millipore. Selanjutnya dilakukan diawaudarakan
menggunakan ultrasonikator selama 5 menit sehingga supernatan siap di injeksikan ke
sistem KCKT.
Sejumlah 20,0 L masing-masing supernatan yang telah disiapkan, diinjeksikan pada
sistem KCKT dengan komposisi fase gerak dan kecepatan alir optimum. Kromatogram
yang dihasilkanlalu diamati bentuk puncak nya dengan melihat nilai waktu retensi, tailing
factor (tf) serta nilai Rs dari kafein maupun SI dengan senyawa lain yang berdekatan.
Kondisi sistem KCKT dikatakan optimum jika kromatogram yang dihasilkan mempunyai
nilai tf <2; Rs >2,0 serta tR < 10 menit. SI yang menghasilkan parameter optimum terbaik
dipilih untuk dijadikan SI pada penelitian ini.
Uji Kesesuaian Sistem KCKT
Diambil plasma darah sebanyak 600 µL, kemudian dipindahkan ke dalam tube, lalu
ditambahkan 200 µL larutan seri SI asetanilida, dan 200 µL larutan seri kafein. Adapun
konsentrasi larutan seri kafein dan larutan seri SI asetanilida yang ditambahkan yaitu; seri
kafein 240 µg/mL dan seri SI asetanilida 160 µg/mL. Selanjutnya divortex selama 30 detik.
1500 µ L dalam tabung sentrifugasi. Sehingga didapatkan volume total 2000 µ L. Lalu
tabung sentrifugasi divortex selama 30 detik dan disentrifugasi selama 10 menit dengan
kecepatan 10000 rpm. Cairan supernatan dipisahkan, kemudian di millipore. Selanjutnya
diawaudarakan menggunakan ultrasonikator selama 5 menit. Supernatan siap di injeksikan
ke sistem KCKT.
Sejumlah 20,0 L masing-masing supernatan yang telah disiapkan tersebut,
diinjeksikan pada sistem KCKT sebanyak 6 kali replikasi dengan komposisi fase gerak dan
kecepatan alir optimum.
Pengamatan dilakukan pada panjang gelombang pengamatan kemudian diamati
kromatogram kafein hasil pemisahan dan dilihat nilai waktu retensi (kafein dan SI
asetanilida), nilai tf (kafein dan SI asetanilida), Rs kafein dengan puncak senyawa lain
yang terdekat, Rs SI asetanilida dengan puncak senyawa lain yang terdekat, nilai CV dari
waktu retensi (kafein dan SI asetanilida) dan nilai CV dari tf (kafein dan SI asetanilida).
Kondisi sistem KCKT dikatakan optimum jika kromatogram yang dihasilkan
mempunyai nilai tf <2; Rs >2,0 serta tR < 10 menit.
HASIL DAN PEMBAHASAN
Sampel biologis yang dianalisis pada penelitian ini berupa sampel plasma darah dari
subjek keturunan suku jawa. Penggunaan sampel plasma darah orang keturunan suku jawa
penting sehingga metode analisis menjadi lebih spesifik.
Preparasi merupakan langkah yang sangat penting pada analisis sebelum larutan
sampel dianalisis menggunakan metode KCKT. Teknik preparasi sampel plasma darah
pada penelitian ini mengacu pada penelitian yang dilakukan oleh Alvi dan Hammami
(2011). Sampel plasma pertama kali dispike dengan senyawa kafein dan SI karena subjek
uji tidak diberi perlakuan untuk mengkonsumsi kafein. Protein pada plasma diendapkan
dengan bantuan penambahan metanol dan sentrifugasi. Sampel plasma harus disaring
menggunakan microsyringe untuk menghilangkan kontaminasi zat yang mungkin ada
dalam sampel sebelum diinjeksikan pada KCKT. Ultrasonikasi dilakukan untuk
menghilangkan gelembung udara pada sampel yang dapat mengacaukan pembacaan
absorbansi. Larutan yang akan dianalisis menggunakan KCKT harus jernih dan bebas dari
kontaminasi zat atau gelembung udara karena jika masih terdapat kontaminasi zat atau
Optimasi pemilihan standar internal dilakukan sebelum optimasi sistem KCKT.
Optimasi sistem KCKT pada penelitian ini dilakukan dengan optimasi berbagai
perbandingan komposisi fase gerak aquabidestilata : metanol dan optimasi kecepatan alir
fase gerak campuran aquabidestilata : metanol. Kandidat standar internal yang dioptimasi
adalah asetanilida, nikotinamida dan papaverin. Berdasarkan kromatogram yang dihasilkan
pada Gambar 1, senyawa nikotinamida tidak dapat dijadikan standar internal karena
memiliki puncak yang bertabrakan dengan puncak senyawa dalam blanko plasma. Puncak
senyawa asetanilida dan papaverin terpisah dari puncak noise dalam blanko plasma.
Puncak senyawa papaverin yang dihasilkan memiliki waktu retensi yang dekat dengan
puncak senyawa kafein, sedangkan puncak senyawa asetanilida memiliki waktu retensi
yang cukup jauh dengan senyawa kafein sehingga senyawa asetanilida dipilih sebagai SI
pada penelitian ini.
Gambar 1. Kromatogram tumpang tindih antara blanko plasma dengan senyawa kafein dan beberapa kandidat SI (asetanilida, nikotinamida dan papaverin) menggunakan sistem KCKT
yang optimum (fase diam kolom C18:250 x 4,6 mm, 5µm; fase gerak campuran aquabidestilata :
metanol dengan perbandingan 60:40; kecepatan alir 1,0 mL/menit
Berdasarkan spektrum yang dihasilkan oleh spektrofotometer UV pada pembacaan
absorbansi senyawa kafein dan asetanilida, dipilih panjang gelombang pengamatan untuk
senyawa kafein dan SI asetanilida yaitu 255 nm. Spektrum hasil pembacaan oleh
Gambar 2. Tumpang tindih spektrum senyawa kafein dan asetanilida. Pembacaan absorbansi menggunakan spektrofotometer UV pada panjang gelombang 200nm - 400nm
Kondisi optimum sistem KCKT yang dapat memisahkan kafein, SI dan matriks
sampel plasma dioptimasi pada berbagai perbandingan komposisi fase gerak dan kecepatan
alir. Kecepatan alir yang dioptimasi pada sistem KCKT menggunakan kecepatan alir 0,5
mL/menit dan 1,0 ml/menit menggunakan fase gerak aquabidestilata:metanol dengan
perbandingan 40:60; 50:50 dan 60:40. Pada kecepatan alir 0,5 mL/menit, waktu retensi
yang dihasilkan lebih lama dibandingkan pada kecepatan alir 1,0 mL/menit. Selain itu pada
kecepatan alir 0,5 ml/menit dihasilkan puncak yang melebar. Sedangkan pada kecepatan
alir 1,0 ml/menit dihasilkan puncak yang lebih sempit dan waktu retensi yang lebih cepat,
sehingga kecepatan alir 1,0 ml/menit dipilih sebagai kecepatan alir optimum pada
penelitian ini. Data tailing factor dan waktu retensi dari kafein dan kandidat SI
(asetanilida, nikotinamida, papaverin) pada optimasi fase gerak dan kecepatan alir dapat
Komposisi fase gerak yang dioptimasi pada sistem KCKT yaitu perbandingan
komposisi fase gerak aquabidestilata:metanol dengan perbandingan 40:60; 50:50 dan
60:40 dengan kecepatan alir 1,0 ml/menit. Untuk komposisi fase gerak
aquabidestilata:metanol dengan perbandingan 60:40 dihasilkan puncak dengan pemisahan
paling baik dibandingkan pada komposisi fase gerak dengan perbandingan 50:50 dan
40:60. Namun pada perbandingan komposisi fase gerak 60:40 waktu retensi dari standar
internal asetanilida terlalu lama yaitu mendekati 10 menit. Waktu retensi dikatakan efektif
jika kurang dari 10 menit. Untuk perbandingan komposisi fase gerak
aquabidestilata:metanol dengan perbandingan 50:50 menghasilkan pemisahan yang lebih
baik dibandingkan pada perbandingan komposisi fase gerak 40:60. Selain itu pada
perbandingan komposisi fase gerak 50:50 dihasilkan waktu retensi dari standar internal
dibawah 7 menit (cukup cepat). Sehingga komposisi fase gerak aquabidestilata:metanol
dengan perbandingan 50:50 dipilih sebagai komposisi fase gerak optimum.
Gambar 3. Kromatogram senyawa: Kafein dan SI Asetanilida dalam sampel plasma
menggunakan sistem KCKT yang optimum (fase diam kolom C18:250 x 4,6 mm, 5µm; fase
gerak campuran aquabidestilata : metanol dengan perbandingan 50:50; kecepatan alir 1,0 mL/menit; detektor UV 255 nm
Keterangan : Data 1 (blanko plasma)
Data 2 (seri 1) : kafein 1,6 µg/mL; asetanilida 4 µg/mL Data 3 (seri 2) : kafein 8 µg/mL; asetanilida 8 µg/mL Data 4 (seri 3) : kafein 18 µg/mL; asetanilida 12 µg/mL
Puncak senyawa kafein dan SI asetanilida dalam kromatogram mempunyai nilai tf
kurang dari 2, hal ini menunjukkan bahwa kafein dan SI asetanilida tidak cukup kuat
tertahan dalam kolom dan dapat keluar serentak dari kolom (Snyder dkk., 2010). Nilai tR
kafein dan SI asetanilida pada Gambar 3 adalah kurang dari 10 menit. Hal ini
menunjukkan bahwa kedua senyawa tersebut dapat keluar dengan cepat dari kolom. Nilai
tR senyawa kafein lebih cepat dibandingkan senyawa SI asetanilida, hal ini disebabkan
dan fase gerak yang digunakan. Pada penelitian ini digunakan metode KCKT fase terbalik,
sehingga semakin polar suatu senyawa maka interaksi dengan fase geraknya semakin kuat
dan dapat dikatakan waktu retensinya semakin cepat.
Gambar 4 menunjukkan interaksi kafein atau SI asetanilida dengan fase diam.
Interaksi kafein dengan fase diam lebih sedikit dibandingkan interaksi SI asetanilida
dengan fase diam.
Gambar 4. Interaksi senyawa Kafein (A) dan SI asetanilida (B) dengan fase diam
Keterangan :
Interaksi hidrofobik antara senyawa kafein/SI dengan fase diam
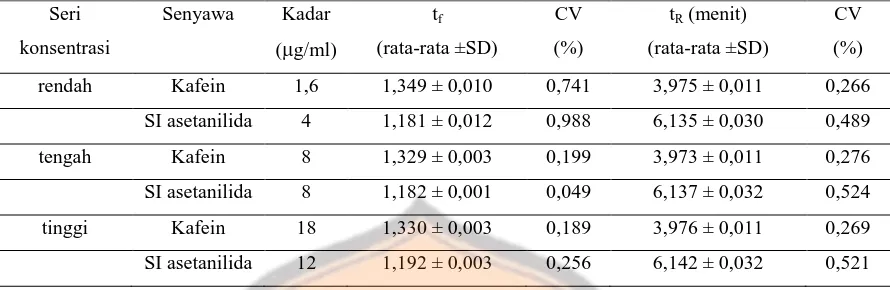
Gambar 5 menunjukkan gugus polar yang dimiliki kafein dan SI asetanilida dan
interaksinya dengan fase gerak. Ditinjau dari strukturnya, gugus polar pada senyawa kafein
lebih banyak dibandingkan gugus polar pada SI asetanilida sehingga interaksi kafein
dengan fase gerak lebih besar dibandingkan interaksi SI asetanilida dengan fase gerak.
Interaksi kafein dengan fase diam yang lebih sedikit dibandingkan interaksi SI asetanilida
dengan fase diam serta interaksi kafein dengan fase gerak yang lebih besar dibandingkan
interaksi SI asetanilida dengan fase gerak menyebabkan waktu retensi kafein lebih cepat
Gambar 5. Senyawa Kafein (A) dan SI Asetanilida (B) dengan gugus polarnya ( )
serta interaksinya dengan fase gerak aquabidestilata (H2O) dan metanol (CH3OH)
Keterangan :
Interaksi kafein/SI dengan pelarut aquabidestilata
Interaksi kafein/SI dengan pelarut metanol
Hasil kromatogram untuk senyawa kafein dan SI asetanilida menunjukkan
pemisahan puncak yang sempurna dengan puncak senyawa lain yang berdekatan. Hal ini
ditunjukkan dengan nilai Rs > 2,0 mengidentifikasikan bahwa puncak senyawa dapat
terpisah dengan baik dengan senyawa lain yang puncaknya berdekatan (Snyder dkk.,
2010).
Pada tahap optimasi pemisahan kafein dan SI asetanilida dalam sampel plasma,
digunakan 3 seri konsentrasi kafein maupun SI asetanilida menggunakan fase gerak
aquabidestilata dan metanol dengan perbandingan 40:60; 50:50 dan 60:40 serta kecepatan
alir 0,5mL/menit dan 1,0 mL/menit. Penggunaan 3 seri konsentrasi bertujuan untuk
membandingkan tinggi puncak kromatogram sebagai acuan seberapa besar kadar yang
akan digunakan pada tahap validasi metode. Nilai tailing factor dan waktu retensi yang
didapatkan dari sistem KCKT fase terbalik dengan fase gerak perbandingan
aquabidestilata:metanol dengan perbandingan 50:50 dan kecepatan alir 1,0 ml/menit telah
memenuhi persyaratan analisis baik untuk kafein maupun SI (asetanilida), data disajikan
Tabel II. Nilai tf dan tR kafein dan SI pada berbagai tingkat
Keterangan : masing-masing senyawa dalam setiap kadar direplikasi sebanyak 3 kali.
Berdasarkan uji kesesuaian sistem didapatkan rata-rata nilai tailing factor kafein
yaitu 1,332; rata-rata waktu retensi kafein adalah 4,005 menit, rata-rata resolusi kafein
dengan senyawa lain yang puncaknya terdekat yaitu 2,029, rata-rata nilai tailing factor SI
(asetanilida) yaitu 1,197, rata-rata waktu retensi SI (asetanilida) adalah 6,251, rata-rata
resolusi SI (asetanilida) dengan senyawa lain yang puncaknya terdekat untuk replikasi 1, 2
dan 3 yaitu 8,468 sedangkan rata-rata resolusi SI dengan senyawa lain yang puncaknya
terdekat untuk replikasi 4, 5 dan 6 yaitu 5,723. Nilai resolusi SI (asetanilida) pada replikasi
1, 2 dan 3 jauh berbeda dengan nilai resolusi SI (asetanilida) pada replikasi 4, 5 dan 6
karena puncak terdekat dari SI asetanilida pada replikasi 1, 2 dan 3 merupakan puncak
senyawa kafein yang memiliki waktu retensi sekitar 4,0 menit, sedangkan puncak terdekat
dari SI asetanilida pada replikasi 4, 5 dan 6 terdapat puncak senyawa lain pada waktu
retensi sekitar 4,4 menit. Pada replikasi 4, 5 dan 6 terbaca puncak noise blanko plasma
pada waktu retensi sekitar 4,4 menit, sedangkan pada replikasi 1, 2 dan 3 tidak terbaca
puncak noise pada waktu retensi sekitar 4,4 menit. Hal tersebut menyebabkan resolusi pada
uji kesesuaian sistem untuk SI pada replikasi 1, 2 dan 3 memiliki nilai resolusi yang lebih
tinggi dibandingkan resolusi uji kesesuaian sistem pada replikasi 4, 5 dan 6. Berdasarkan
penjelasan tersebut dapat dikatakan bahwa metode ini telah memenuhi kriteria tailing
factor yang baik yaitu dibawah 2,0; waktu retensi yang efektif yaitu dibawah 10 menit dan
resolusi yang baik yaitu diatas 2,0. Dari uji kesesuaian sistem tersebut didapatkan CV
untuk parameter tailing factor, waktu retensi dan Height Equivalent of a Theoretical Plate
(HETP) baik untuk kafein maupun SI menunjukkan CV < 2% sehingga dapat dikatakan
memenuhi kriteria batasan koefisien variansi untuk uji kesesuaian sistem. Data
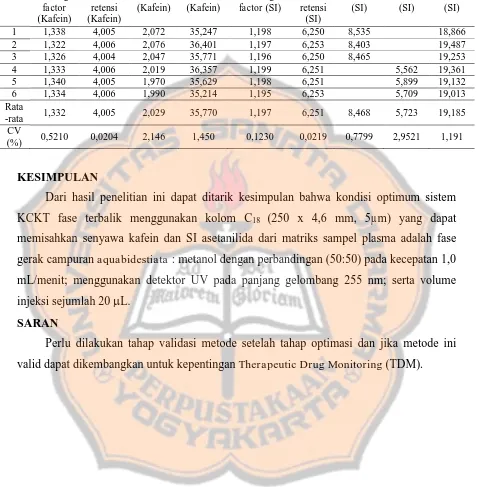
Tabel III. Data nilai tailing factor kafein dan SI (asetanilida), nilai waktu retensi kafein dan SI (asetanilida), nilai resousi kafein dan SI (asetanilida), dan nilai HETP kafein dan SI (asetanilida) pada
uji kesesuaian sistem
Dari hasil penelitian ini dapat ditarik kesimpulan bahwa kondisi optimum sistem
KCKT fase terbalik menggunakan kolom C18 (250 x 4,6 mm, 5µm) yang dapat
memisahkan senyawa kafein dan SI asetanilida dari matriks sampel plasma adalah fase
gerak campuran aquabidestiata : metanol dengan perbandingan (50:50) pada kecepatan 1,0
mL/menit; menggunakan detektor UV pada panjang gelombang 255 nm; serta volume
injeksi sejumlah 20 L.
SARAN
Perlu dilakukan tahap validasi metode setelah tahap optimasi dan jika metode ini
DAFTAR PUSTAKA
Alvi, S.N., dan Hammami, M., M, 2011. Validated HPLC Method for Determination of Caffeine Level in Human Plasma using Synthetic Plasma: Application to Bioavailability Studies, Journal of Chromatographic Science. (49), 292-296.
Anonim, 2012. CYP2A6, https://www.pharmgkb.org/gene/PA121?tabType=tabVip, diakses pada 11 November 2016.
Gandjar, I.G., dan Rohman, A., 2007. Kimia Farmasi Analisis. Penerbit Pustaka Pelajar, Yogyakarta, 242-246, 326-327, 379-381, 385-386, 388.
Irmanto, A.R., 2008, Validasi Penetapan Kadar Campuran Parasetamol, Propifenazon dan Kafein dengan Metode Kromatografi Cair Kinerja Tinggi Fase Terbalik.
Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta, 33-70.
Joewana, S., 2005. Gangguan Mental dan Perilaku Akibat Penggunaan Zat Psikoaktif. Edisi 2, Penerbit Buku Kedokteran EGC, Jakarta, 71.
Kang, J.S., dan Lee, M.H., 2009. Overview of Therapy Drug Monitoring, The Korean Journal of Internal Medicine. (24), 1-10.
Kee, J.L., dan Hayes, E.L., 1996. Farmakologi Pendekatan Proses Keperawatan. Penerbit Buku Kedokteran EGC, Jakarta, 200.
Neal, M.J., 2006. At a Glance Farmakologi Medis, Erlangga Medical Series. Edisi V, Jilid 1, Jakarta, 14-15.
Patil, P.N., 2012. Caffein in Various Sample and Their Analysis HPLC, International Journal of Pharmaceutical Sciences Review and Article. (18), 76-83.
Patramurti, C., Sugiyanto., Nurrochmad A., dan Martono, S., 2015. Polymorphisme of Cytochrome P450 2A6 (CYP2A6*1 and CYP2A6*4) Among Javanese Indonesian Smoker and Non Smoker, Indonesian Journal of Pharmacy. (26), 11-19.
Pedak, M., 2009. Metode Supernol Menaklukkan Stress. Penerbit Hikmah, Jakarta, 109. Snyder, L.R., Kirkland, J.J., dan Dolan, J.W., 2010. Introduction to Modern Liquid
LAMPIRAN
Lampiran 9. Campuran kafein dan nikotinamida mengunakan fase gerak
Lampiran 10. Campuran kafein dan nikotinamida mengunakan fase gerak
Lampiran 11. Campuran kafein dan nikotinamida mengunakan fase gerak
Lampiran 12. Campuran kafein dan nikotinamida mengunakan fase gerak
Lampiran 13. Campuran kafein dan nikotinamida mengunakan fase gerak
Lampiran 14. Campuran kafein dan nikotinamida mengunakan fase gerak
Lampiran 15. Kromatogram papaverin 4 g/mL mengunakan fase gerak
Lampiran 16. Kromatogram papaverin 4 g/mL mengunakan fase gerak
Lampiran 17. Kromatogram asetanilida 8 g/mL mengunakan fase gerak
Lampiran 18. Kromatogram asetanilida 8 g/mL mengunakan fase gerak
Lampiran 19. Kromatogram blanko plasma A mengunakan fase gerak
Lampiran 20. Kromatogram blanko plasma B mengunakan fase gerak
Lampiran 21. Kromatogram blanko plasma C mengunakan fase gerak
Lampiran 22. Kromatogram blanko plasma D mengunakan fase gerak
Lampiran 23. Kromatogram blanko plasma E mengunakan fase gerak
Lampiran 39. Perhitungan konsentrasi larutan seri pada tahap optimasi pemisahan kafein dan SI asetanilida dalam plasma
Larutan seri kafein/SI sebanyak 200 L diencerkan menjadi 1000 L (pengenceran 5 kali)
1000 L tersebut diambil 500 L lalu diencerkan menjadi 2000 L (pengenceran 4 kali)
sehingga siap diinjeksikan pada sistem KCKT
Total pengenceran : 5 x 4 = 20 kali pengenceran
M1 V1 = M2 V2
Dari larutan seri kafein :
32 g/mL x 200 L = 6,4 g/mL x 1000 L 6,4 g/mL x 500 L = 1,6 g/mL x 2000 L
Jadi konsentrasi kafein yang diinjek pada sistem KCKT yaitu 1,6 g/mL
160 g/mL x 200 L = 32 g/mL x 1000 L 32 g/mL x 500 L = 8 g/mL x 2000 L
Jadi konsentrasi kafein yang diinjek pada sistem KCKT yaitu 8 g/mL 360 g/mL x 200 L = 72 g/mL x 1000 L
72 g/mL x 500 L = 18 g/mL x 2000 L
Jadi konsentrasi kafein yang diinjek pada sistem KCKT yaitu 18 g/mL
Dari larutan seri SI Asetanilida :
80 g/mL x 200 L = 16 g/mL x 1000 L 16 g/mL x 500 L = 4 g/mL x 2000 L
Jadi konsentrasi SI asetanilida yang diinjek pada sistem KCKT yaitu 4 g/mL
160 g/mL x 200 L = 32 g/mL x 1000 L 32 g/mL x 500 L = 8 g/mL x 2000 L
Jadi konsentrasi SI asetanilida yang diinjek pada sistem KCKT yaitu 8 g/mL
240 g/mL x 200 L = 48 g/mL x 1000 L 48 g/mL x 500 L = 12 g/mL x 2000 L
Lampiran 40. Perhitungan konsentrasi larutan seri pada tahap uji kesesuaian sistem
Larutan seri kafein/SI sebanyak 200 L diencerkan menjadi 1000 L (pengenceran 5 kali)
1000 L tersebut diambil 500 L lalu diencerkan menjadi 2000 L (pengenceran 4 kali)
sehingga siap diinjeksikan pada sistem KCKT
Total pengenceran : 5 x 4 = 20 kali pengenceran
M1 V1 = M2 V2
Dari larutan seri kafein :
240 g/mL x 200 L = 48 g/mL x 1000 L 48 g/mL x 500 L = 12 g/mL x 2000 L
Jadi konsentrasi kafein yang diinjek pada sistem KCKT yaitu 12 g/mL
Dari larutan seri SI Asetanilida :
160 g/mL x 200 L = 32 g/mL x 1000 L 32 g/mL x 500 L = 8 g/mL x 2000 L
Lampiran 41. Contoh perhitungan konsentrasi kafein dan asetanilida dari
penimbangan, perhitungan konsentrasi larutan stok dan perhitungan konsentrasi larutan intermediet
Perhitungan konsentrasi larutan stok kafein/SI
20 mg kafein/SI dilarutkan dengan pelarut hingga 5 mL Konsentrasi larutan stok kafein/SI = 20 mg / 5 mL = 4 mg/mL
Perhitungan konsentrasi larutan intermediet kafein 800 g/mL
1000 L larutan stok kafein 4 mg/mL diencerkan dengan pelarut hingga 5 mL Konsentrasi larutan intermediet kafein = 4 mg/mL x 1000 L / 5mL = 800 g/mL
Perhitungan konsentrasi larutan intermediet asetanilida 320 g/mL
BIOGRAFI PENULIS
Penulis skripsi dengan judul “Optimasi Metode
Bioanalisis Kafein dalam Sampel Darah Orang Jawa
dengan Metode Kromatografi Cair Kinerja Tinggi Fase
Terbalik” memiliki nama lengkap Jonathan Ronny
Kurniawan, lahir di Wonosobo pada tanggal 14 Agustus
1995, merupakan anak ke tiga dari tiga bersaudara
pasangan Sugiono dan Veronica Setyawati. Pendidikan
formal yang ditempuh penulis yaitu TK. Kristen
Wonosobo (1999-2001), pendidikan tingkat Sekolah Dasar di SD. Kristen 03 Wonosobo
(2001-2007), pendidikan Sekolah Menengah Pertama di SMP. Remaja Parakan
(2007-2010), pendidikan Sekolah Menengah Atas di SMA. Kristen Satya Wacana Salatiga
(2010-2013). Selama menempuh pendidikan SMA, penulis pernah berprestasi mengikuti
olimpiade astronomi tingkat kota Salatiga dan mendapatkan juara 3, selain itu penulis juga
pernah menjadi juara 1 tingkat kota Salatiga dalam lomba paduan suara SMA. Penulis
melanjutkan pendidikan sarjana di Fakultas Farmasi Universitas Sanata Dharma pada
tahun 2013. Semasa perkuliahan, penulis mengikuti berbagai UKF yaitu paduan suara
fakultas veronica dan bulu tangkis. Penulis terlibat dalam berbagai kepanitiaan antara lain;
Divisi Konsumsi Desamitra 3 dan 4 (2013), Divisi Pendaftaran Insadha 2015 dan Divisi
Konsumsi Cara Belajar Insan Aktif (2015). Penulis pernah mengikuti Latihan
Kepemimpinan I (2013). Penulis juga pernah menjadi asisten praktikum Kimia Analisis