Akta Kimindo Vol.2 No.1.Oktobir 2006: 9- 24
AKTA KIMI
A
I
N
DO
NE6IA
sorpsi Ion Logam Pb(lI) Pada Membran Selulosa-Khitosan Terikat Silang*
Bimbing Herwanto dan Eko Santoso**
Laboratorium Kimia Fisika
Jurusan Kimia, Institut Teknologi Sepuluh Nopember, Kampus ITS Keputih, Surabaya 60111
TRAK
Membran komposit selulosa-khitosan terikat silang dibuat dengan cara melapisi kertas saring
rhatman Grade 4 dengan larutan khitosan dan glutaraldehid 0,02% sebagai agen pengikat silangnya.
'onsentrasi larutan khitosan divariasi dengan larutan khitosan 1%, 2% dan 3%. Pengaruh zat PEG
iloetilen glikol) sebagai zat porogen juga diamati dengan menambahkan 5% PEG dan 10% PEGke dalam
rutan khitosan 3%. Adsorpsi ion Pb(lI) pada membran selulosa-khitosan terikat silang dilakukan dalam
oses rendam. Adsorpsi logam Pb(lI) dilakukan pada suhu kamar dengan pH 5 sebagai pH optimal dengan
rentang konsentrasi 100-1000 ppm. Model isoterm adsorpsi Iogarn Pb(lI) dikaji dengan 2 model isoterm
yaitu isoterm Langmuir dan Freundlich. Model isoterm yang sesuai dengan data eksperimen diuji dengan
metode regresi tinier. Data menunjukkan bahwa adsorpsi logam Pb(ll) sesuai dengan model isoterm
- eundlich. Kapasitas adsorpsi terbesar dihasilkan pada membran selulosa-khitosan 1% dan kapasitas
adsorpsi terendah dihasilkan pada membran selulosa-khitosan 3% dengan PEG 10%. Hasil menunjukkan
hwa kadar khitosan 1% memiliki kapasitas adsorpsi yang terbesar pada membran komposit selulosa
-itosan terikat silang dan penambahan kadar PEG dapat menurunkan kapasitas adsorpsi pad a membran
komposit selulosa-khitosan terikat silang.
Kata kunci : Membran khitosan selulosa-kitosan terikat silang, adsorpsi isoterm. kapasitas adsorpsi
ABSTRACT
The cellulose-cross linked chitosan composite membranes have been prepared by coating chitosan
solution onto the grade 4 Whatman filter paper and glutaraldehide as a cross linking agent. The
concentrations of chitosan solution were varied 1%, 2%, and 3%. Effect of polyethylene glycol (pEG) as a
porogen agent was studied by the addition of 5% and 10% of PEG respectively into the chitosan solution
3%. The adsorption of Pb (11)ions by the cellulose-cross linked chitosan rnernbrarie was done in a batch
ocess, The adsorption of Pb (11)metal was done at the room temperature and pH 5 as a optimum pH.The
concentration range of Pb (11)was varied 100-1000 ppm. The isotherm adsorption model of Pb (11)was
studied by both the isotherm model of Langmuir and Freundlich. The isotherm model was in accordance
ith the data of experiment by the regression linear method. The experiment data showed that the
adsorption of Pb (11)more suitable to the Freundlich isotherm model. The highest capacity of adsorption
vas show by the cellulose-chitosan 1% membrane and the lowest capacity adsorption was showed by the
cellulose-chitosan 3% membrane with PEG 10%. The results showed that the concentration 1% of chitosan
gave the highest adsorption capacity of cellulose-cross linked chitosan membrane and the addition of PEG
decreased the adsorption capacity of cellulose-cross linked chitosan membrane.
Keywords: cellulose-cross linked chitosan composite membranes, isoterm adsorption, capacity of adsorption
• Makalah ini disajikan pada Seminar Nasional Kimia VIII.di Surabaya 8 Agustus 2006
•. Corresponding author Phone: 031·5943353·; Fax: 031· 5928314-: e-rnau: .
lahirnya banyak penelitian seputar adsorpsi logam
berat pada/ khitosan murni dan khitosan
termodikasi. Khitosan murni pada umumnya
digunakan sebagai biosorben togarn berat dalam
bentuk serpihan ( flakes) (Jonsson-Charrier dkk.,
1996) dan serbuk ( powder t) (Lima and Airoldi,
2000), sedangkan bentuk khitosan termodifikasi
meliputi khitosan ikatsilang (Cao dkk., 2002), dan
dipadukan dengan material pendukung alumina
menjadi komposit alumina khitosan (Boddu and
Smith, 2002).
Hasil penelitian menunjukkan bahwa
kemampuan adsorpsi khitosan terhadap logam
berat sangat dipengaruhi oleh sifat fisika-kimiawi
khitosan. Khitosan tak berikat silang mempunyai kapasitas adsorpsi lebih besar dari pada khitosan
berikat silang, tetapi khitosan berikat silang
mempunyai ketahanan fisik terhadap asam yang
lebih baik dari pad a khitosan tak berikat silang
(Wan Ngah dkk., 2002). Serbuk khitosan dengan
ukuran partikel yang lebih kecil mempunyai
kapasitas adsorpsi yang lebih besar dari pada
serbuk dengan ukuran partikel lebih besar
(Karthikeyan dkk., 2004). Selain itu, pola isoterm
adsorpsi Iogarn berat pada khitosan, yaitu
l.angrnuir dan Freundlich, sangat dipengaruhi oleh
jenis logam be rat yang diamati (Wan Ngah dkk.,
2002).
Penelitian ini mengkaji kesetimbangan
isoterm adsorpsi ion logam berat Pb(lI) pada
membran komposit selulosa-khitosan
berikatsilang, dimana khitosan sebagai bahan
aktif adsorben dan selulosa berfungsi sebagai
material pendukung. Selulosa dipilih sebagai
bahan pendukung karena termasuk bahan
biopolimer dengan struktur kimiawi yang mirip
dengan khitosan, dimana kemiripan struktur
kimiawi khitosan dan selulosa akan menjadikan
kedua biopolimer bersifat kompatibel dan
mempunyai gaya adhesi yang baik. Bahan
selulosa yang digunakan dalam penelitian ini
adalah kertas sa ring Whatman grade 4 dengan
diameter retensi partikel 20-25 mm. Sebagai
agen pengikat silang akan digunakan
glutaraldehid 0,02% dan sebagai bahan
pembentuk pori pada membran akan digunakan
polietilen glikol 5-10%. Membran komposit akan
dibuat dengan cara melapisi permukaan selulosa
(kertas sating) dengan khitosan berikatsilang.
Ketebalan lapisan khitosan pada permukaan
selulosa akan divariasi dengan mengatur
konsentrasi khitosan 1%-3%dalam larutan asam asetat 1%. Isoterm adsorpsi logam berat pada
komposit selulosa-khitosan berikat silang
dilakukan dengan sistem rendam, yakni komposit
akan direndam dalam larutan logam dengan
varasi konsentrasi 100-1000 ppm pada suhu
kamar selama 24 jam sehingga terjadi
kesetimbangan adsorpsi. Jumlah logam yang
tidak terserap oleh komposit, diukur dengan
Bimbing dan Eko-Adsorpsi Ion Logam Pb(lI) Pada Membran Selulosa-Khitosan Terikat Silang
PENDAHULUAN
Logam dapat membahayakan bagi
kehidupan manusia jika konsentrasi melebihi
batas ambang yang diijinkan. Air limbah dari
perindustrian dan pertambangan merupakan
sumber utama polutan togarn berat. Namun
demikian, meskipun konsentrasinya belum
melebihi batas ambang, keberadaan togarn berat
telah diketahui bersifat akumulatif dalam sistem biologis (Quek dkk., 1998).
Berbagai metoda telah dikembangkan
untuk memisahkan logam berat dari air limbah,
antara lain meliputi metoda pengendapan kimia,
filtrasi mekanik, penukar ion, elektrodeposisi,
oksidasi reduksi, sistem membran, dan adsorpsi
fisik. Namun rnasing-nrasing metoda tersebut
secara inheren mempunyai kelebihan dan
keterbatasan. Beberapa tahun terakhir telah
dilakukan penelitian seputar polimer ala m
(biopolimer) yang mampu mengikat logam berat
limbah melalui pembentukan senyawa kompleks
sehingga biopolimer dapat berfungsi sebagai
adsorben untuk memisahkan Iogarn berat dari air
meskipun konsentrasinya sangat rendah. Salah
satu biopolimer yang saat ini banyak diteliti
sebagai adsorben togarn berat dari air limbah
adalah khitosan.
Khitosan adalah poli 2-Amino-2- 0eoksi-l3-O-Glukosa,merupakan turunan dari khitin,
poli-/3-N-asetil-O-glukosamin, yang merupakan suatu
amino polisakarida alami paling berlimpah di alam, merupakan biopolimer yang terdapat pada
bahan pendukung (kulit cangkang) binatang
moluska, krustakhea, dan insekta. Khitosan
didapatkan melalui proses deasetilasi dari khitin, dimana gugus asetil pada khitin, oleh hidrogen
diubah menjadi gugus amin dengan penambahan
larutan basa kuat berkonsentrasi tinggi ( Planas,
2002; Bastaman, dkk., 1990 ) Kitosan
mempunyai kelarutan yang baik dalam
asam-asam organik encer, sedangkan kitin tidak larut
dalam air dan kebanyakan pelarut organik, larut
dalam heksafloroaseton, heksafloro isopropanol
dan dimetilasetamid yang mengandung 5% LiCl.
Terkait dengan kelarutan tersebut, kitosan
menjadi lebih menarik dan mempunyai aplikasi
yang lebih luas daripada kitin (Kumar, 2000).
Keberadaan gugus amida dalam khitin
dan gugus amina dalam khitosan telah
menjadikan khitin dan khitosan sebagai adsorben
yang mampu mengikat logam berat. Hasil
penelitian menunjukkan bahwa khitosan dapat mengikat logam berat 4 sampai 5 kali lebih besar
dari khitin. Hal ini terkait cengan adanya gugus
amina terbuka sepanjang rantai khitosan (Yang
and Zall, 1984) sehingga khitosan lebih mudah
berinteraksi dengan larutan berpelarut air ( lebih
hidrofilik ) dari pada khitin (Kurnar, 2000).
Kemampuan khitosan membentuk senyawa
komplek dengan logam berat telah mendorong
Kimindo Vot.2No. 1Oktober 2006 : 9-24
spektrofotometer serapan atom. Untuk
-mendapatkan adsorpsi yang optimum maka pH larutanlogam akan divariasi antara 2-6. Isoterm adsorpsi logam berat pada membran komposit
selulosa-khitosan berikatsilang akan diuji dengan dua model isoterm adsorpsi, yaitu Langmuir dan Freundlich, menggunakan metoda regresi linear
<tan kapasitas adsorpsi membran kompossit
selulosa-khitosan berikat silang akan dihitung berdasarkan model isoterm yang sesuai setelah <Dujidengan metoda regresi linear.
Tujuan penelitian ini adalah mengkaji pengaruh kadar khitosan dan pengaruh kadar PEG pada membran komposit terhadap pola
isoterm adsorpsi dan kapsitas adsorpsi logam
Pb(II) pada membran komposit selulosa-khitosan berikatsilang.
~ETODOLOGIPERCOBAAN
Alat
Peralatan yang digunakan pada penelitian ini adalah labu berJeher tiga,
kondensor, pemanas, termometer,
spektrofotometer JASCO FT/JR 5300, beaker
glass 1000 ml, beaker glass 2000 ml, geJasukur,
corong buchner, pengaduk, stirer, oven pengering.
labu pengenceran 500 ml, kertas pH universal,
gelas arloji, tabung gas nitrogen, alat refluks, viskometer oswald, erlenmeyer, ayakan 325
mesh, lumpang porselen besar, alu, kertas saring Whatmangrade4 dan pompa vakum.
Bahan
Bahan-bahan yang diperlukan dalam penelitian ini adalah serbuk limbah udang, NaOH, larutan HCI, aquades, aquabides, gas nitrogen, asam asetat glasial, PEG (poli etilen glikol), gluteraldehid, padatan logarn Pb(N03)2 dan larutan HN031%.
PROSEDURKERJA
Isolasi Khitin Dari Limbah Udang
Kulit udang dicuci dan dikeringkan lalu digiling dengan stone ware sampai halus kemudian dilakukan pengayakan dengan ukuran 325 mesh. Cuplikan serbuk udang ditambah
larutan NaOH dengan perbandingan 1:10 (w/v) dimasukkan ke dalam bejana yang dilengkapi pengaduk dan termometer yang diletakkan pada penangas. Campuran dipanaskan selama 2 jam pada suhu 65 QCsambil diaduk lalu didinginkan pada suhu kamar dan dicuci dengan aquades hingga netral. Larutan disaring sehingga diperoleh residu, selanjutnya dioven pada temperatur 100
QChingga kJring. Residu kering yang diperoleh ditambah larutan HCI IN dengan perbandingan 1:15 (w/v) dimasukkkan ke beker gelas didiamkan selama 30 menit pada suhu kamar. Setelah itu dicuci sampai netral dengan aquades
lalu disaring dengan corong Buchner. Hasil yang
©Kimia ITS - HKI Jatim
diperoleh dikeringkan pada suhu 100 QC dan dikarakterisasi dengan FTIR.
/
Transformasi Khitin Menjadi Khitosan
Serbuk khitin dimasukkan ke labu gelas leher tiga yang dilengkapi dengan termometer (skala 300 QC)dan pengaduk magnetik (ukuran 3 cm). Ke dalam labu tersebut dimasukkan larutan NaOH 50% dengan perbandingan 1:10 (w/v) . Labu ditaruh dalam penangas air yangdiletakkan di atas hotplate yang mempunyai pengatur kecepatan putar terhadap magnet stirer yang telah dimasukkan dalam labu. Kemudian dilakukan proses refluks khitin pada temperatur 100GC sambil dialirkan gas N2 selama 1 jam. Setelah itu larutan didinginkan lalu dicuci dengan aquades sampai pH netral. Larutan yang diperoleh kemudian disaring, residu dikeringkan dalam oven pada suhu 100 GC. Proses refluk diulangi setiap satu jam selama lima kali. Hasil yang diperoleh dikarakterisasi dengan FTIR dan viskorneter.
Karakterisasi Viskometer Dengan Metode Viskositas.
Pembuatan larutan buffer yaitu : 0,3 M asam asetat dicampurkan dengan 0,1 M NaOH, selanjutnya farutan buffer diuji dengan viskometer. Pada tahap berikutnya larutan buffer ditambahkan dengan 0,3 g khitosan, distirer hingga khitosan terlarut lalu diuji dengan viskometer. Demikian juga dilakukan pada larutan buffer dengan 0,35 g ; 0,4 g ; 0,4 g dan 0,5 g khitosan.
Preparasi Larutan Khitosan Dan Larutan Khitosan-PEG
Untuk larutan khitosan, sebanyak 1% khitosan ditambahkan dalam asam asetat 1%. Larutan kemudian dicampur sampai homogen dengan stirer. Perlakuan tersebut diulang dengan khitosan 2% dan khitosan 3%
Untuk larutan khitosan-PEG, sebanyak 3% khitosan ditambahkan dalam asam asetat 1%. Kemudian ditambah dengan larutan PEG 5% dengan rasio 1:1 (v/v). Larutan kemudian dicampur sampai homogen dengan stirer. Perlakuan tersebut diulangi dengan larutan PEG 10%.
Preparasi Membran Selulosa Khitosan Ikat Silang Kertas saring Whatman grade 4 (sebelumnya dipotong menjadi 8 bagian yang sama besar selanjutnya ditimbang ) lalu direndam dalam larutan khitosan (1%, 2%, 3%, 3% PEG5%dan 3% PEG 10%) selama 30 menit . Setelah itu diambil dan direndam dalam larutan NaOH1 M selama 24 jam. Kemudian diambil dan dicuci dengan aquades sampai netral. Selanjutnya direndam dalam gluteraldehid 0,02% selama 24 jam.. Hasil yang diperoleh dicuci
-
---
~
HASIL DAN PEMBAHASAN Isolasi Khitin dari Limbah Udang.
Pacrc:; penelitian ini pembuatan khitin diperoleh dari limbah udang berupa kulit udang.
Tahap awal isolasi khitin dari limbah udang
adalah proses deproteinasi yang berfungsi untuk
menghilangkan kandungap proteinnya dengan
eara serbuk udang yang berwarna eoklat muda kekuningan dieampurkan ke dalam larutan NaOH
3,5% pada temperatur 65 QC.
Langkah selanjutnya adalah proses
dimineralisasi dimana serbuk limbah udang yang
telah dideproteinnasi tersebut dieampurkan
dengan larutan HCI yang berfungsi untuk
rnenghilangkan senyawa anorganik dalam kulit
udang. Kandungan mineral yang utama adalah
CaC03 (40-50 %) dan sedikit Ca3(P04)2.Garam
tersebut dapat dihilangkan dengan
menggunakan larutan HCt. Reaksi yang terjadi
dapat digambarkan sebagai berikut :
Bimbing dan Eko-Adsorpsi Ion Logam Pb(lI) Pada Membran Selulosa-Khitosan Terikat Silang
dengan aquades lalu dikeringkan dan ditimbang,
lalu diuji dengan SEM, diukur ketebalan dan
porositasnya.
Pada uji porositas ini, digunakan
piknometer yang mempunyai volume 25,237 ml
selanjutnya piknometer diisi aquades dan
ditimbang. Kemudian membran komposit
direndam dalam aquades selama 24 jam,
selanjutnya rnasing-rnasing membran komposit
dipotong
-potong
kemudian dimasukkan kedalam piknometer dan ditimbang.
Prosentase porositas dapat dihitung
dengan menggunakan persamaan :
%porositas = volume air terserap x 100 %
volume membran
={[(wmbHwk)]/p air} x 100%
(vm)
dimana,
volume membran (vm)
=
v pikno (25,237 ml) - volume air (va)
keterangan :
wmb
=
berat membran basahwk =berat membran kering
Adsorpsi Logarn Berat. Penentuan pH Optimal.
Sebanyak 25 ml larutan logam Pb(lI) 100 ppm diturunkan sampai pH 2 (dilakukan dengan
penambahan HCI). Kemudian dimasukkan
membran komposit (dengan perlakuan khitosan
3%) sambil direndam selama 24 jam. Larutan
kemudian dianalisa dengan MS. Perlakuan
tersebut diulang dengan variasi pH 3, 4, 5, dan 6.
Pengaruh Kadar Khitosan pada Membran
Sebanyak 25 ml larutan togarn Pb(lI) 100
ppm pada pH optimal ditambahkan membran
komposit (perlakuan khitosan 1%) dan direndam dalam larutan logam selama 24 jam. Larutan logam kemudian dianalisa dengan MS. Perlakuan tersebut diulang dengan konsentrasi larutan
logarn 200-1000 ppm. Prosedur tersebut juga
dilakukan untuk khitosan 2%dan 3%.
Pengaruh Kadar Porogen (PEG).
Sebanyak 25 ml larutan logam Pb(lI) 100
ppm pada pH optimal ditambahkan membran
komposit (perlakuan khitosan 3%, 5% PEG) dan direndam dalam larutan logam selama 24 jam.
Larutan logam kemudian dianalisa dengan MS.
Perlakuan tersebut diulang dengan konsentrasi
larutan logam 200-1000 ppm. Prosedur tersebut
juga dilakukan untuk khitosan 3%, 10% PEG.
12
CaC03+2 HCI ~ H2C03+CaCb
H2C03 ~ C02+H20
Tahapan ini berakhir dengan ditandai
seluruh serbuk telah mengendap dansudah tidak
terbentuk lagi busa. Serbuk yang diperolehdieuei
dengan aquades sampai pH netral dengan
ditandai tampilan fisik filtrat bening agak keputih - putihan. larutan kemudian disaring hingga diperoleh residu berupa khitin yang selanjutnya dikeringkan dalam oven pada temperatur 100 QC
sampai tidak ada Iagi kandungan airnya. Pada
tahap ini diperoleh khitin yang berwarna eoklat muda kekuningan.
Transformasi Khitin Menjadi Khitosan
Transformasi khitin. menjadikhitosan merupakan proses terlepasnya asetil pada gugus
amida hingga menjadi gugus amina.
Perbandingan gugus amida dan gugus amina
pada rantai polimer tersebut biasa disebut dengan derajat diasetilasi. Pada proses ini khitin
direfluks dengan dialiri gas N2 yang bertujuan
untuk menghindari terjadinya oksidasi pada saat
reaksi berlangsung. Pada proses diasetilasi khitin
menjadi khitosan dalam penelitian ini dibuat
bertahap tiap satu Jam sebanyak lima kali. Hasil
refluks jam pertama diambil dan kembali direfluks
dengan kondisi yang sama hingga didapat
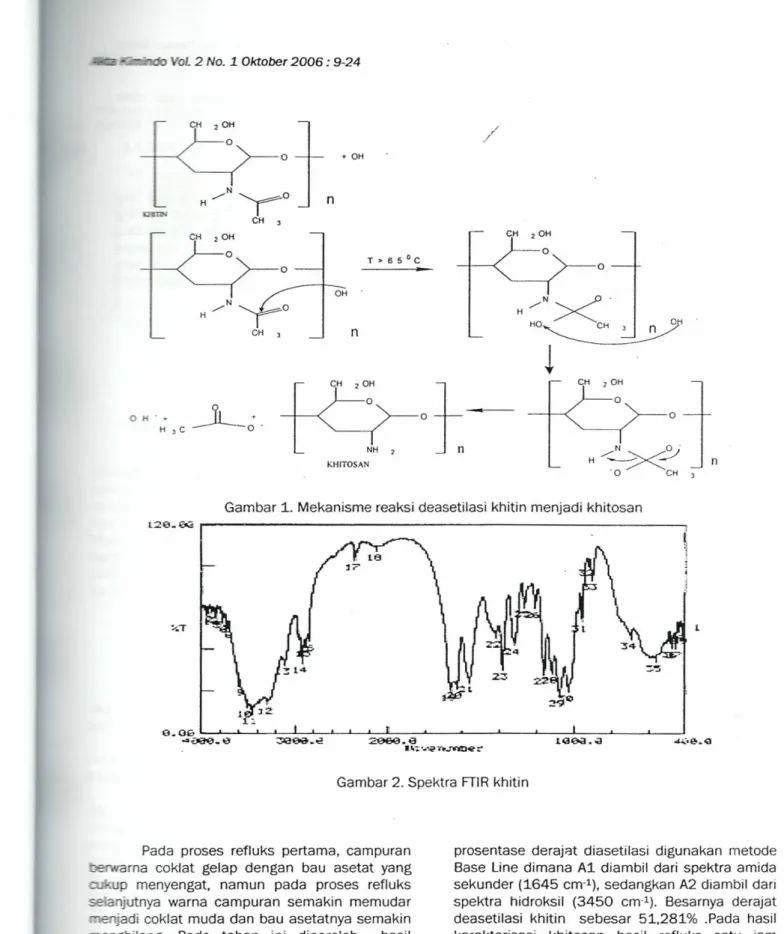
khitosan refluks setiap satu jam selama lima kali. Mekanisme reaksi deasetilasi khitin menjadi
khitosan seperti yang ditunjukkan pada
Gambar 1.
n CH 2OH
°
t-0 NH 2 KHITOSAN oL2No.i Oktober 2006 :9-24 • OH CH 2OH o OH o CH 3 OH'. ~. H 3CO'/
CH 2 OH o o H/NX' HO~J
Gambar 1. Mekanisme reaksi deasetilasi khitin menjadi khitosan
Gambar 2.Spektra FTIR khitin
Pada proses refluks pertama, campuran
oerwarna coklat gelap dengan bau asetat yang
p menyengat, namun pada proses refluks
seianjutnya warna campuran semakin memudar
~adicoklat muda dan bau asetatnya semakin
menghilang. Pada tahap ini diperoleh hasil
uks setiap satu jam selama lima kali untuk
6analisa dengan FTIR dan sebagian besar hasil
- -osanil?idigunakan untuk preparasi membran.
Data HasilSpektra FTIR
Setelah diperoleh khitin dan khitosan dari aasil refluks setiap satu jam selama lima kali
tersebet, kemudian dilakukan karakterisasi
- gan FTIR. Adapun hasil karakterisasi khitin
d
c
:
;
l
a
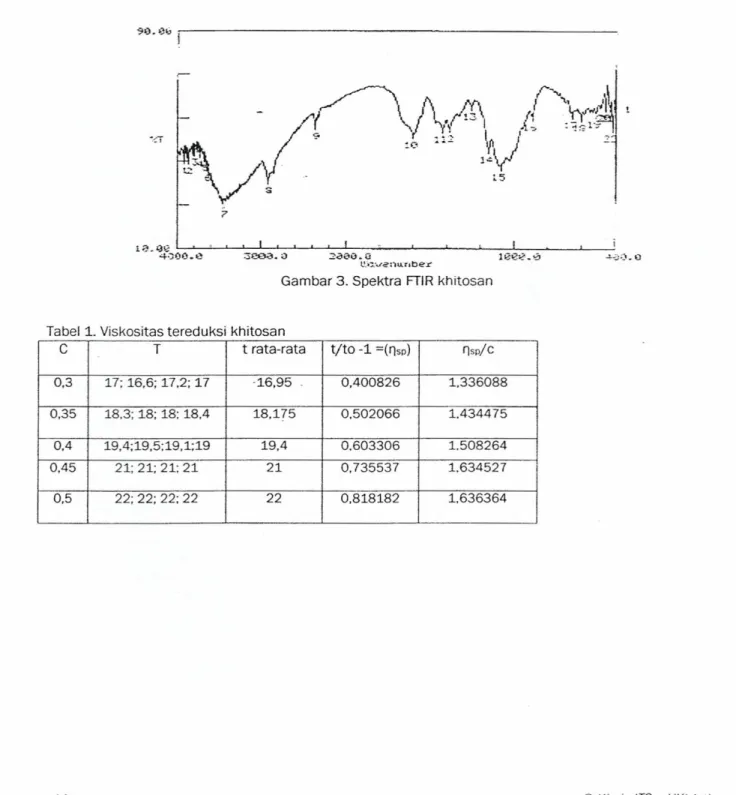
dilihat pada Gambar 2. Dari Gambar 2.dihitung besarnya derajat deasetilasi pada
dan untuk mengetahui besarnya
Kimia
r
r
s
-
HKf Jatimprosentase derajat diasetilasi digunakan metode
Base Line dimana A1 diambil dari spektra amida
sekunder (1645 cm'1),sedangkan A2 diambil dari
spektra hidroksil (3450 crrr-). Besarnya derajat deasetilasi khitin sebesar 51,281% .Pada hasil
karakterisasi khitosan hasil refluks satu jam
selama lima kali ditunjukkan pada Gambar 3. Oari Gambar 3 tersebut dapat ditentukan besarnya derajat deasetilasi pada khitosan satu jam
selama lima kali.
Besarnya prosentase derajat deasetilasi
dihitung dengan menggunakan metode base line
yaitu sebesar 85,61% . Khitosan hasil refluks
setiap satu jam selama lima kali ini mempunyai
nilai derajat deasetilasi yang cukup tinggi yang selanjutnya hasil khitosan tersebut digunakan untuk preparasi membran.
Bimbing dan Eko-Adsorpsi Ion Logarn Pb(lI) Pada Membran Selulosa-Khitosan Terikat Silang
Data Hasil Pengukuran Viskositas
Hasil data pengukuran dengan metode viskositas pada viskometer kapiler Oswald digunakan untuk menghitung massa molekul rata
-rata polimer khitosan. Pada penentuan besarnya viskositas ini, dibuat terlebih dahulu larutan buffer yaitu : 0,3 M asam asetat dicampurkan dengan O,~ M NaOH, selanjutnya larutan buffer diuji dengan viskometer. Pada tahap berikutnya larutan buffer ditambahkan dengan 0,3 g khitosan, distirer hingga khitosan terlarut lalu diuji dengan viskometer. Demikian juga dilakukan pada larutan buffer dengan 0,35 g ; 0,4 g dan
0,5 g khitosan, sehingga diperoleh hasil data sebagai berikut :
.
/
Pada larutan Buffer: toi = 12,2s ; t02= 12,1s;
t03 =~2s ;to rata-rata =12.1s.
Dari tabel 1, kita pisa mengetahui nilai viskositas intrinsik (rj) yang diperoleh melalui kurva Ilsp/c (viskositas tereduksi) vs c kemudian dicari dari harga intersepnya. Hubungan viskositas intrinsik dengan massa molekul rata-rata viskositas dinyatakan dengan persamaan Mark-Houwink-Sakurada [Ill = K.Mva
90• .;)'j I
""--::I
r
i;J_qe- I! !, I , I ! , J ,! I I i
+:)00.0) ..)COi'I.o 2,adO.0 H<e0.';; -L:.::0.0
c..~'",".:-nu:(lbe-r
Gambar 3. Spektra FTIR khitosan
Tabel 1.Viskositas tereduks-- -- - - i khitosan
C T t rata-rata
tjto
-1 =(Ilsp) Ilsp/C0.3 17;16.6; 17,2;17 -16,95 0,400826 1.336088 0,35 18,3;18;18;18,4 18.175 0.502066 1.434475 0.4 19,4;19,5;19.1;19 19,4 0,603306 1.508264 0,45 21;21; 21; 21 21 0,735537 1.634527 0.5 22;22;22;22 22 0,818182 1.636364 14 ©Kimia ITS - HKI Jatim
s
:
Kimindo Vol. 2 No. 1 Oktober 2006: 9-24
pungrafik antara Ilsp/cvs c adalah sebagai
berikut :
0,1 0,2 0,3 0,4 0,5 0,6
c
Gambar4. Viskositastereduksi khitosan Oari persarnaan garis Gambar 4 bisa diketahui intersepnya: [11]
=
0,8695, dengan persamaan Mark-Hauwink-Sakurada tersebut dapat diketahui besarnya massa molekulrata-rata khitosan, dimana K dan a adalah konstanta ark-Hauwink-Sakurada.Untuk larutan khitosan
narga K adalah 1,424.10 ·3dan harga a adalah
0,96 sehingga nila Mv bisa diketahui sebagai
berikut:
My= 0.8695 1/0.96
1,424.10.3
Mv= 797,687 g/rnot
Jadi massa molekul rata-rata viskositas dari khitosan sebesar 797,687 g/rnol.
Preparasi Larutan Khitosan Oan Larutan Khitosan-PEG
Pada pembuatan larutan khitosan digunakan larutan asam asetat 1%yang berfungsi sebagai pelarut. Oalam hal ini untuk pembuatan larutan khitosan 1% digunakan 2 g khitosan dalam 200 ml larutan asam asetat 1%, lalu larutan tersebut distirer sampai homogen.
Oemikian juga dilakukan pada larutan khitosan 2% dan 3%. Pada larutan khitosan 3 % lebih kental daripada larutan khitosan 2% dan 1%,
dimana hal ini dipengaruhi oleh besarnya kandungankhitosannya.
Pada pembuatan larutan khitosan
oengan PEG ini, digunakan khitosan 3% dan
ditambahkan PEG sebanyak 5%, demikian juga
dilakukan pada larutan khitosan PEG10%. Pada
larutan khitosan 3%-PEG 10 % ini merupakan
larutan paling kental dan agak sukar larut
dibandingkan dengan larutan khitosan 1%. 2%. 3% dan 3%-PEG 5%, hal ini dipengaruhi oleh besarnyakandungan PEG.
©Kimia ITS - HKI Jatim
Preparasi Membran Khitosan-Selulosa Terikat Sila?g
Pada proses pembuatan membran khitosan -selulosa terikat silang ini dibuat dengan sistem Batch yaitu dengan merendam kertas saring dalam larutan khitosan. Pada pembuatan membran komposit ini digunakan kertas saring Whatman Grade 4 yang telah dipotong-potong, Selanjutnya masing-masing potongan ditirnbang, dan direndam dalam larutan khitosan 1%,2%, 3%. 3%-PEG5% dan 3%-PEG 10%selama 30 menit, supaya larutan khitosan menempel sernpurna pada selulosa (kertas saring). Kemudian rnasing-masing potongan tersebut diambil lalu direndam dalam larutan NaOH1 M selama 24 jam. dimana dalam hal ini
NaOH berfungsi sebagai koagulan. Setelah itu diambil dan dicuci dengan aquades sampai pH netral. Tahap berikutnya direndam dalam gluteraldehid 0,02% selama 24 jam yang
berfungsi sebagai agen pengikat silang, kemudian dicuci dengan aquades lalu dikeringkan dan diperoleh membran komposit. Pada tahap berikutnya membran komposit khitosan terikat silang tersebut dianalisa dengan SEM. diukur
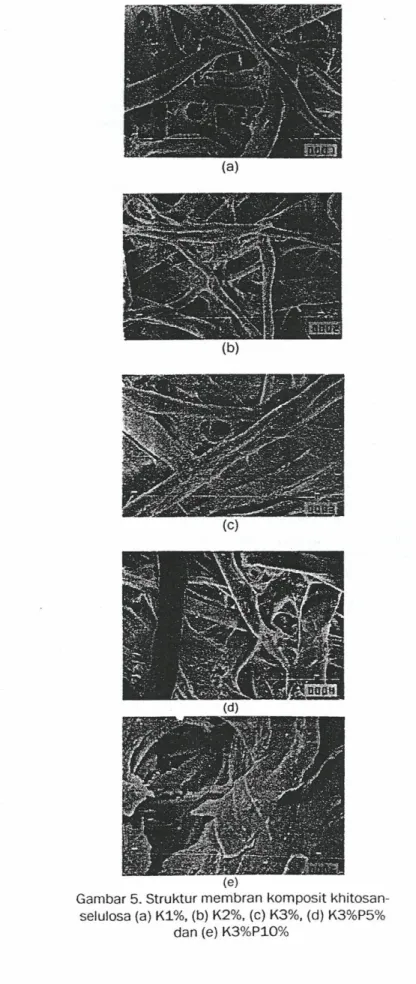
ketebalan dan porositasnya. Analisa SEM
Pada analisa SEM ini digunakan alat JSM Tl00 dengan perbesaran 1000 kali dan diperoleh data pada Gambar 5. Oari Gambar 5 ditunjukkan bahwa pada rnembran komposit khitosan-selulosaterikat silang Kl% mempunyai bentuk pori dan situs spesifik yang menyebar serta lebih banyak dibandingkan bentuk membran komposit khitosan-selulosa yang lain. Sedangkan pada membran komposit khitosan -selulosa terikat silang K3% Pl0% mempunyai
bentuk pori dan situs spesifiknya yang lebih sedikit dibandingkan membran komposit khitosan-selulosa yang lain. Hal ini dipengaruhi oleh kadar khitosannya maupun penambahan kadar PEG.
Analisa Ketebalan dan Porositas
Pada analisa ketebalan membran komposit ini diamati dengan menggunakan alat Microhardness Tester FM, dan diperoleh hasil data sebagai berikut:
Tabel 2 Ketebalan Membran
Membran Ketebalan (urn) Rata-rata (urn)
Kl% 8.6 6.7 7.7 7.67 K2% 9 10.5 9,2 9.57 K3% 10.2 13.9 11.9 12.00 K3%P5% 25.1 24.1 26.2 25.13 ... -K3%Pl0% 25.6 26.7 25.5 25.93 15
-"._._... _.- .._.
Bimbing dan Eko-Adsorpsi Ion Logam Pb(II) Pada Membran Selulosa-Khitosan Terikat Silang
Berdasarkan Tabel 2 terlihat bahwa
masmg-maslng permukaan untuk setiap
membran mempunyai ketebalan yang berbeda-beda, sehingga ketebalan diperoleh melalui rata-rata ketebalan membran. Dari data yang diperoleh menunjukkan ~ahwa pada membran komposit khitosan Kl% mempunyai ketebalan yang rendah dibandingkan dengan membran komposit yang lain, sedangkan pad a membran
komposit khitosan K3%Pl0% mempunyai
ketebalan yang lebih besar dibandingkan membran komposit yang lain.
Pada analisa porositas ini digunakan piknorneter yang mempunyai volume 25,237 ml dan membran komposit direndam dalam air selama 24 jam Setelah dilakukan pengukuran, maka diperoleh densitas air seperti ditunjukkan pada Tabel 3 .
Tabel 4 menunjukkan bahwa pada membran khitosan 3%-PEG 10% mempunyai prosentase porositas yang tinggi dibandingkan membran komposit yang lain, hal ini dipengaruhi oleh besarnya kandungan PEG yang mampu meningkatkan prosentase porositasnya.
(a)
(b)
Adsorpsi Logam Pb (11)
Pada proses adsorpsi logam berat Pb(lI) dengan membran komposit khitosan-selulosa terikat silang ini dilakukan dengan merendam membran komposit ke dalam larutan iogam Pb(II). Kemampuan membran komposit selulosa dalam proses adsorpsi togarn Pb(II) diperoleh berbagai karakteristik membran komposit meliputi : pH optimum, pengaruh kadar khitosan pada membran, "dan pengaruh kadar PEG.
(c)
Penentuan Ph Optimum
Pada penelitian ini setiap analisa MS terhadap adsorpsi togam berat Pb (11) oieh membran komposit digunakan kurva kalibrasi sebagai acuan analisa sampel. Konsentrasi kurva kalibrasi yang digunakan antara 0 sampai 100 ppm dan diperoleh data seperti pada tabel 5.
(e)
Gambar 5.Struktur membran komposit khitosan -selulosa (a) Kl%, (b) K2%, (c) K3%, (d) K3%P5%
dan (e) K3%Pl0%
16 ©Kimia ITS - HKI Jatim
1
-:
0
0
Kimindo Vol. 2 No. 1. Oktober 2006: 9-24
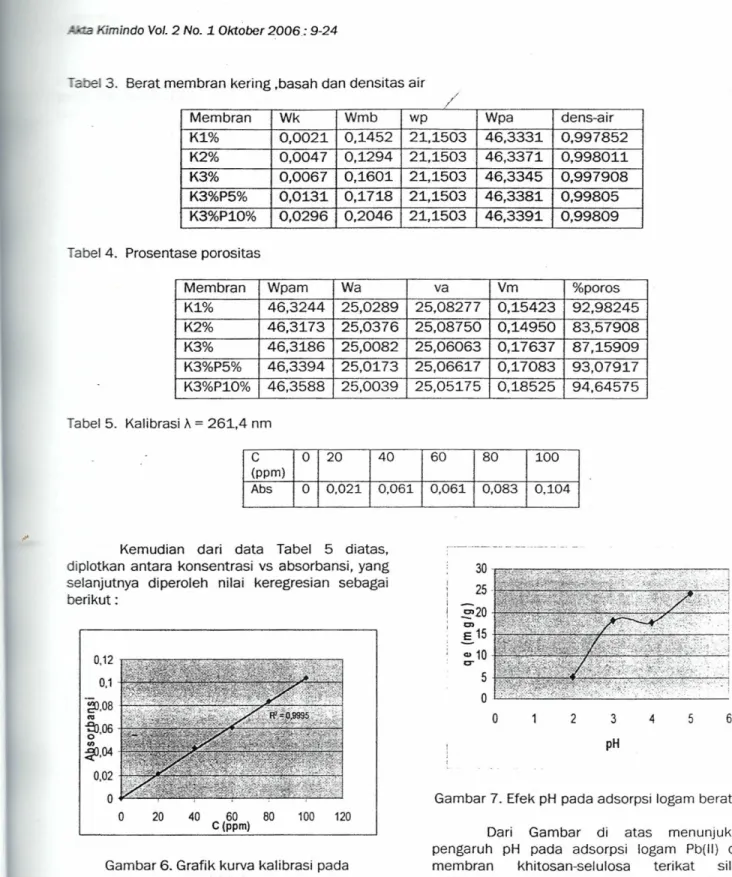
abel3. Seratmembrankering ,basah dandensitas air
/
Membran Wk Wmb wp Wpa dens-air
K1.% 0,0021. 0,1.452 21.,1.503 46,3331. 0,997852 K2% 0,0047 0,1.294 21,1.503 46,3371. 0,99801.1 K3% 0,0067 0,1601. 21,1503 46,3345 0,997908 K3%P5% 0,0131. 0,171.8 21,1503 46,3381. 0,99805 K3%P10% 0,0296 0,2046 21.,1503 46,3391 0,99809 Tabel4. Prosentaseporositas
Membran Wpam Wa va Vm %poros
K1% 46,3244 25,0289 25,08277 0,15423 92,98245 K2% 46,3173 25,0376 25,08750 0,1.4950 83,57908 K3% 46,31.86 25,0082 25,06063 0,1.7637 87,1.5909 K3%P5% 46,3394 25,0173 25,06617 0,17083 93,07917 K3%P1.0% 46,3588 25,0039 25,05175 0,18525 94,64575 Tabel5. KalibrasiA
=
261,4 nmc
0 20 40 60 80 100 (ppm) Abs 0 0,021 0,061 0,061 0,083 0,104Kemudian dari data Tabel 5 diatas,
diplotkan antara konsentrasivs absorbansi,yang
selanjutnya diperoleh nilai keregresian sebagai berikut: 30 25 ~20 Cl E 15 '" 10 c -S 0 0 2 3 4 5 6 pH 0,12 0,1 '~,08
'"
~,06'"
~,04 0,02o
o
Gambar7.Efek pHpada adsorpsilogamberatPb
20 40 60 80 100 120
C(ppm)
Oari Gambar di atas menunjukkan
pengaruh pH pada adsorpsi logam Pb(II)oleh membran khitosan-selulosa terikat silang
sehinggadapat dijelaskan bahwaadsorpsipaling
rendah terjadi pada pH 2 dan adsorpsi yang
maksimum diperoleh pada pH 5. Jadi yang
digunakan sebagai pH optimum merupakan pH yang mempunyai kapasitas adsorpsi yang maksimum yaitu pH 5 dan selanjutnya pH
tersebutdigunakansebagai acuanuntuk adsorpsi
logam Pb (11) pada membran khitosan-selulosa terikatsilang.
Gambar6. Grafikkurva kalibrasi pada
A=261,4 nm
Oari kurva kalibrasi Gambar 6
mempunyainilaikeregresian0,9995. Halinitelah memenuhi sebagaikalibrasi untuk setiap analisa sampel dengan MS yaitu menggunakan "
=
261,4nm.(Pada penentuan pH optimum ini
digunakanrange pH 2-5 dan untuk mengetahui
kapasitas adsorpsi digunakan Persamaan 2.3,
sehinggadiperolehhasildata sebagaiberikut: PengaruhKadarKhitosan PadaMembran
Pada pengaruh kadar khitosan pada membranini, masing-masing membrankomposit K1%, K2%, K3%, K3% P5% dan K3% Pl0%,
Bimbing dan Eko-Adsorpsi Ion Logarn Pb(lI) Pada Membran Selulosa-Khitosan Terikat Silang
direndam selama 24 jam dengan berbagai variasi
konsentrasi dari 100 ppm hingga 1000 ppm .
Kemudian dianalisa
dengan MS
dan diperolehhasil data masing-rnastng membran komposit
sebagai berikut : Hasil analisa membran
khitosan-selulosa terikat
sttang
Kl% , diperoleh sepertitampak pada Gambar 8.
12000 10000 !!! 8000 Cl
.s
6000 Cl> 4000 0-2000o
o
100 200 300 400 500 600 Ce(mgll)Gambar 8. Plot antara Ce vs qe pada membran komposit 1\1%
Karakteristik isoterm diketahui dari
daerah awal yang ditunjukkan dengan cekungan
kurva terhadap sumbu konsentrasi. Dari Gambar
8, terlihat cekungan kurva isoterm mencapai
puncak secara terus menerus seiring dengan
meningkatnya konsentrasi akhir atau konsentrasi
kesetimbangan (Ce). Hasil konsentrasi tersebut
dapat digunakan untuk menganalisa kedua
isoterm baik Langmuir maupun Freundlich.
I 0,4 0,3 G> ~0,2 Cl> <.> 0,1 100 200 300 400 500 600 Ce
Gambar 9. Adsorpsi isoterm bentuk Langmuir
Persamaan Langmuir didefinisikan: qe=
Ce.KL j b.Ce+ 1, sehingga diperoleh plot antara
Ce vs Cejqe seperti tampak pada Gambar 9 yang
menunjukkan bahwa pada adsorpsi isoterm ini
tidak sesuai jika digunakan model Langmuir
karena mempunyai nilai keregresian 0,1992 yang
jauh mendekati 1. 18 10 8 '" 6
0-.=
4 2 0, 0 2 4 6 8 InceGambar 10. Adsorpsi isoterm bentuk Freundlich
Persamaan Freundlich didefinisikan: qe
== KF.Cel/n ,sehingga diperoleh plot antara In Ce
vs In qe seperti tampak pada Gambar 1.0. Pada
pengeplotan ini menghasilkan garis lurus yang
mempunyai nilai keregresian 0,9525 ,
menunjukkan bahwa adsorpsi isoterm ini sesuai
dengan model Freundlich. Hasil tersebut
menyatakan bahwa persamaan Freundlich
memberikan data yang lebih baik daripada
persamaan Langrnuir dengan penjabaran data
pada semua tingkat konsentrasi. Hasil
pengeplotan tersebut diperoleh persamaan
sehingga niiJi KF dan 1.jn dapat ditentukan
rnasing-rnasiig sebesar 0,017374 dan 2,0673.
Dari data KF dan ljn tersebut dapat ditentukan
besarnya kc.rasitas adsorpsi (qe) secara teori
yang selanju: -Iya dibandingkan dengan kapasitas
adsorpsi (qe: eksperimen seperti tampak pada
Gambar 11. 'jari Gambar 11 rl}enunjukkan bahwa
pada mernt-nn khitosan-selulosa terikat silang
K1%, serna- .n besar konsentrasi logam Pb(lI)
semakin be.ar pula kapasitas adsorpsi yang
terjadi pada membran khitosan-selulosa terikat
silang K1%. hal ini sesuai mengikuti isoterm
model Freun.mch. 12000 r-r-r-:- , ",
,
"
,
,
:
::,
<
~
c
;
;~:"
;
;~~:
~;
:'
1
10000 ".' ,:",i/
.-;
~
-~
,
-
.:
·-
t
J
::
.
!~'
1
8000 : -:::jt'-i
•
qe (eksp)~
.i,,;
;
:
-
-
-* qe (teori) S6000 "/' :~
~
.
C54000 ~--- -:--..L'IL::-_~---! 2000 I '1>/' 'T I o.'---+::-:::.
'
,
-
:
-
,
o ! 200 400 600 Ce(mg/l)Gambar 11.. Efek konsentrasi terhadap adsorpsi
logam Pb(lI) pada membran khitosan-selulosa
terikat silang Kl%.
Analisa membran komposit untuk
khitosan-selulosa terikat silang K2% diperoleh
hasil seperti tampak pada Gambar 12.
8
Bimbing dan Eko-Adsorpsi Ion Logarn Pb(lI) Pada Membran Selulosa-Khitosan Terikat Silang
Hasil analisa membran khitosan-selulosa
terikat silang K3% , diperoleh seperti tampak
pada Gambar 16 . Karakteristik isoterm diketahui
dari daerah awal yang ditunjukkan dengan
cekungan kurva terhadap sumbu konsentrasi.
Dari Gambar 16, cekungan kurva isoterm
mencapai puncak secara terus menerus seiring
dengan meningkatnya konsentrasi akhir atau
konsentrasi kesetimbangan (Ce). Hasil
konsentrasi tersebut dapat digunakan untuk
menganalisa kedua isoterm baik Langmuir
maupun Freundlich. 2000 _1500 en en
Elooo
<1> 0"500 100 200 300 400 500 600 Ce (mgIL)Gambar 16. Plot antara Ce vs qe pada membran
komposit K3%.
Persamaan Langmuir didefinisikan: qe =
Ce.KL
I
b.Ce + 1, sehingga diperoleh plot antaraCe vs Ce/qe seperti tampak pada Gambar 17.
Dari gambar tersebut ditunjukkan bahwa pada
adsorpsi isoterm ini tidak sesuai jika digunakan
model Langmuir karena mempunyai nilai
keregresian 0,1934 yangjauh mendekati 1.
25 _20 en ~15 ~ 10
h':
'
?
i't.:
i
.
"
t::r 5 " ...H 100 200 300 400 500 600 Ce (mg/l)Gambar 17.Adsorpsi isoterm bentuk Langmuir.
20 6
'"
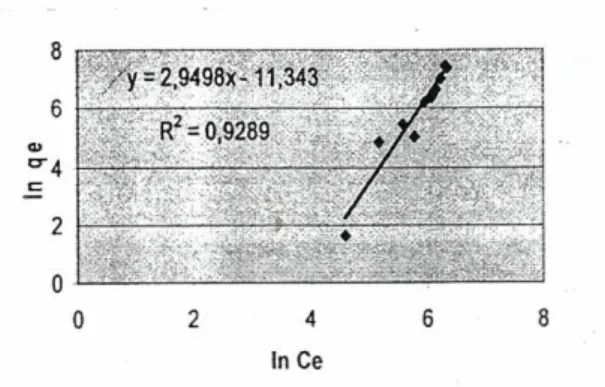
0"4 c: 2 2 4 8 In Ce 6Gambar 18. Adsorpsi isoterm bentuk Freundlich.
Persamaan Freundlich didefinisikan
qe
=
KF.Cel/n ,sehingga diperoleh plot antaraIn Ce vs In qesepertrtarnpak pada Gambar 18,
Pengeplotan ini menghasilkan garis lurus yang
mempunyai nilai keregresian 0,9289,
menunjukkan bahwa adsorpsi isoterm ini sesuai
dengan model Freundlich. Hasil tersebut
menyatakan bahwa persamaan Freundlich
memberikan data yang lebih baik daripada
persamaan langmuir dengan penjabaran data
pada semua tingkat konsentrasi. Hasil
pengeplotan tersebut diperoleh persamaan
sehingga nilai KF dan
l/n
dapat ditentukanmasing-masing sebesar 1,18522.10.5 dan
2,9498. Dart-data KF dan
l/n
tersebut dapatditentukan besarnya kapasitas adsorpsi (qe)
secara teori yang selanjutnya dibandingkan
dengan kapasitas adsorpsi (qe) eksperimen
seperti tampak pada Gambar 19.
.
.
~
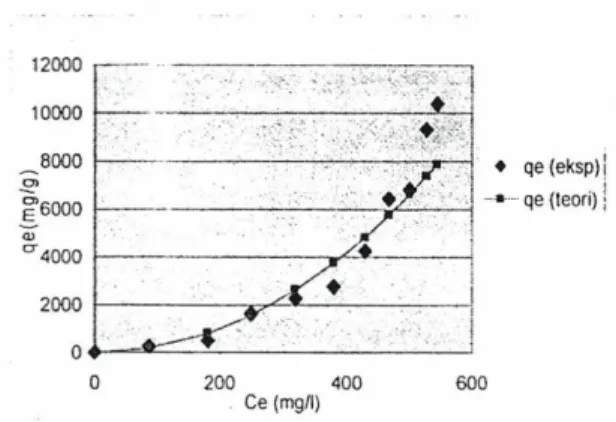
s: • el:sperirren 100 200 :lOO 400 500 600 ce (rrgIl)Gambar 19, Efek konsentrasi terhadap adsorpsi
logam Pb(lI) pada membran knttosan-setulosa
terikat silang K3%,
Dari Gambar 19 menunjukkan bahwa
pad a membran khitosan-selulosa terikat silang
K3%, semakin besar konsentrasi logam Pb(lI)
semakin besar pula kapasitas adsorpsi yang
terjadi pada membran khitosan-selulosa terikat
silang K3%. Hal ini sesuai dengan isoterm model
Freundlich.
Hasil analisa membran krutcsan-selutosa terikat silang K3%P5% .diperoleh seperti tampak
pad a Gambar 20 .
g
!;l;::aKmrld<JVo/.2 No. 1Oktober 2006: 9-24
_1500
"'"
=
e
100
J
100
200
300
Ce(mg/l)400
persamaan Langmuir dengan penjabaran data pactasemua tingkat konsentrasi.
8 7 6 5
••
"'4
E 3 2· 1 o o 2 4 6 8 ---'..'-'.' •..._-. .---.---_._---_._---_ ..._
_
.._
-Gambar20. Plot antara Ce vs qe pada membrankomposit K3%P5%.
Karakteristik isoterm diketahui dari daerahawal yang ditunjukkan dengan cekungan rvaterhadap sumbu konsentrasi. Oari Gambar
20 cekungan kurva isoterm mencapai puncak
secara terus menerus seiring dengan meningkatnya konsentrasi akhir atau konsentrasi esetimbangan (Ce). Hasil konsentrasi tersebut dapat digunakan untuk menganalisa kedua
isoterm baik Langmuir maupun Freundlich. ---_ ..
_
...-.-. -----0,4
0,3
Cl>~02
",'
u0,1"'
:
.'
:
;
'
:"
":
:
"
:
;
',
100
200
300
400
In ceGambar 22. Adsorpsi isoterm bentuk Freundlich. Hasil pengeplotan tersebut diperoleh persamaansehingga nilai KF dan 1/n dapat ditentukan masing-masing sebesar 8,216957 dan 0,8423. Oari data KF dan 1/n tersebut dapat ditentukan besamya kapasitas adsorpsi (qe) secara
teori:
yang selanjutnya dibandingkan dengan kapasitas .adsorpsi (qe) eksperimen seperti tampak pada Gambar 23.1500 ~1000 E "'500 CT • qeteori • qe(eks) Ce
Gambar21.Adsorpsi isoterm bentuk Langmuir.
Persamaan Langmuir didefinisikan
sebagaiqe
=
Ce.KL/ b.Ce + 1, sehingga diperolehplot antara Ce vs Ce/qe seperti tampak pada Gambar 21. Gambar tersebut ditunjukkan bahwa pada adsorpsi isoterm ini tidak sesuai jika
gunakan model Langmuir karena mempunyai
nilaikeregresian 0,3406 yangjauh mendekati 1.
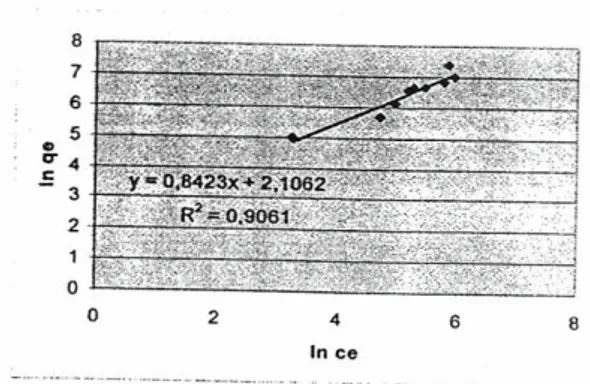
Persamaan Freundlich didefinisikan: qe =KF.Ce1/n ,sehingga diperoleh plot antara In Ce
vs In qe seperti tampak pada Gambar 22.
Pengeplotan ini menghasilkan garis lurus yang
mempunyai nilai keregresian 0,9061,
menunjukkan bahwa adsorpsi isoterm ini sesuai
engan model Freundlich. Hasil tersebut
menyatakan bahwa persamaan Freundlich
memberikan data yang lebih baik daripada
~ Kimia ITS - HKI Jatim
100 200 300
Ce (mgll)
400
Gambar 23. Efek konsentrasi terhadap adsorpsi logam Pb(lI)pada membran khitosan-selulosa
terikat silang K3%P5%.
OariGambar 23 ditunjukkan bahwa pada membran khitosan-selulosa terikat snang K3%P5%,semakin besar konsentrasi logam Pb(lI) semakin besar pula kapasitas adsorpsi yang terjadi pada membran khitosan-selulosaterikat silang K3%P5%. Hal ini sesuai dengan isoterm model Freundlich.
Hasil analisa membran khitosan-selulosa
,terikat silang K3%P10% , diperoleh seperti tampak pada Gambar 24 dibawah ini.
-...;:
-Bimbing dan Eko-Adsorpsi Ion Logam Pb(II) Pada Membran Selulosa-Khitosan Terikat Silang
200 ~150 .
~
Cl .E100 G> 0-50o
o
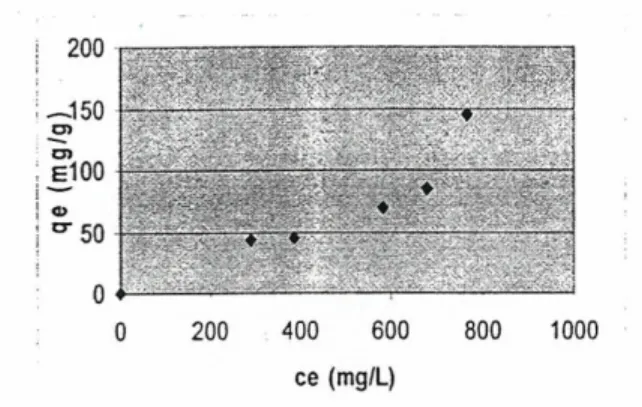
400 600 ce(mg/L) 800 1000 200Gambar24.Plotantara Ce vs qe pada membran
komposit K3%P10%.
Karakteristik isoterm diketahui dari
daerah awal yang ditunjukkan dengan cekungan
kurva terhadap sumbu konsentrasi. Dari Gambar
24, cekungan kurva isoterm mencapai puncak
secara terus menerus seiring dengan
meningkatnya konsentrasi akhir atau konsentrasi
kesetimbangan (Ce). Hasil konsentrasi tersebut
dapat digunakan untuk menganalisa kedua
isoterm baik Langmuir maupun Freundlich.
20 15 G> ~10
'
"
c..> 5 400 600 800 1000 200 CeGambar25. Adsorpsi isoterm bentuk Langmuir.
PersamaanLangmuir didefinisikan: qe=
Ce.KL/ b.Ce + 1,sehingga diperoleh plot antara
Ce vs Ce/qe seperti tampak pada Gambar 25,
yang menunjukkan bahwa pada adsorpsi isoterm
ini tidak sesuai jika digunakan model Langmuir
karena mempunyai nilai keregresian 0,1292 yang
jauh mendekati1. 22
~
--6 5 4 Cl> 0"3 c:-2
1
o
·
o
2 4 6 8 InceGambar 26. Adsorpsi isoterm bentuk Freundlich.
Persamaan Freundlich didefinisikan: qe
=KF.Cel/n ,sehingga diperoleh plot antara In Ce
vs In qe seperti tampak pada Gambar 25 Pada
pengeplotan ini menghasilkan garis lurus yang
mempunyai nilai keregresian 0,8492,
menunjukkan bahwa adsorpsi isoterm ini sesuai
dengan model Freundlich. Hasil tersebut
menyatakan bahwa persamaan Freundlich
memberikan data yang lebih baik daripada
persamaan Langmuir dengan penjabaran data
pada semua tingkat konsentrasi. Hasil
pengeplotan tersebut diperoleh persamaan
sehingga nilai KF dan l/n dapat ditentukan
masing-masing sebesar 0,055699 dan 1,1443.
Dari data KF dan l/n tersebut dapat ditentukan
besarnya kapasitas adsorpsi (qe) secara teori
yang selanjutnya dibandingkan dengankapasrtas
adsorpsi (qe) eksperimen seperti tampak pada
Gambar 27.
Dari Gambar 27 menunjukkan bahwa
pada membran khitosan-selulosa terikat silang
K3%P10%, semakin besar konsentrasi logam
Pb(II)semakin besar pula kapasitasadsorpsi yang
terjadi pada membran khitosan-selulosa terikat
silang K3%P10%,halini sesuai mengikutiisoterm
model Freundlich • qe(eksp) ~qeteori
1
r
o~~~~=-
~-
-
~
--
~
140t
~
~
j
::
:;+;
;
.
r
~
T~7:
;
-
-
::
::
---
::
:
j
_~12017":'~~¥~++~~~~~
lo
o
b,·""',·.,"""",~~~~S-;~~~ 0> E 80j---,~-7'-;"'-~~~~F~:-
eo
r-c---:--r--'-'---'--,---: er 40j---,,
~
,<
---
~
:-
'
-
-
_-
---
<
20r--7"'---:---'---jo~
~~
~
~
~~
-
-
~
~
o
200 400eco
800 1000 ce(mg/l)Gambar 27. Efek konsentrasiterhadap adsorpsi
logam Pb(lI)pada membrankhitosan-selulosa
terikat silang K3%P10%.
•
~~ ~wru'ndovot.2 No. 1 Oktober 2006 : 9·24
Darisemua analisa membran di atas dapat
ingkan pengaruh kadar khitosan pada
membran komposit K1%, K2% dan K3%.
Besarnya kandungan kadar khitosan
berhubungan dengan besarnya kapasitas
adsorpsi,dapat ditunjukkan seperti pada Gambar
28.
7000
Co
0-kapasitas adsorpsi yang besar dibandingkan
dengan membran K3% dan K3% P10%,tetapi
dilihat secara trendline kurva menunjukkan
bahwa membran K3%mempunyainilaikapasitas
adsorpsi yang terus meningkat dibandingkan
dengan K3% P5% dan K3% P10%, hal ini
menunjukkan pengaruh bahwa penambahan PEG
akan menurunkan kapasitas adsorpsi membran
komposit. 6000 5000 4000 3000 2000 1000 100 200 300 400 Ce 600 R 500 _.---_.._- ---- ---_.._- -- ...._- ---
-eKhitosan 1% • Khitosan 2% Khitosan 3%
Gambar28. Kapasitasadsorpsi membran
komposit K1%,K2%dan K3%.
Dari Gambar 28 ditunjukkan bahwa
membran komposit K1% mempunyai nilai
kapasitas adsorpsiyanglebih besar dibandingkan
dengan membran komposit K2%dan K3%,dalam
hal ini kadarprosentasekhitosan terendan akan
mempunyaikapasitas adsorspsiyang terbesar.
4.5.3 Pengaruhkadar PEG
Dari analisa membran dapat
dibandingkan pengaruh kadar PEG pada
membran komposit K3%, K3%P5% dan
K3%P10%. Besarnya pengaruh kandungan PEG
pada membran komposit berhubungan dengan
besarnya kapasitas adsorpsi, dapat ditunjukkan
sepertipadaGambar 29. 2000 1800 1600 1400 1200 ~ 1000 800 600 400 200 0 0 200 ( 800 1000
Gambar 30.Kapasitas adsorpsi membran
komposit K1%,K2%,K3%,K3%,
P5%dan K3%P10%.
Dari Gambar 30, ditunjukkan bahwa
membran komposit K1% mempunyai kapasitas
adsorpsi yang terbesar dibandingkan dengan
membrankompositK2%,K3%,K3%P5%danK3%
P10%. Hal ini menunjukkan bahwa kapasitas
adsorpsi dipengaruhi kadar' khitosannya dan
pengaruh kadar PEG yaitu pada membran
komposit selulosa ini kadar khitosan terendah
mempunyai kapasitas adsorpsi terbesar dan
penambahan PEG pada membran komposit
selulosa ini memiliki pengaruh menurunkan
kapasitas adsorpsi.
400 600
KESIMPULAN
Adsorpsi membran khitosan-selulosa
terikat silang pada ion logam Pb(lI) dilakukan
padakondisi larutan pH 5.Kemampuanmembran
untuk mengadsorpsi logam telah dipelajari
dengan meninjau beberapa aspek seperti
pengaruh kadar khitosan serta pengaruh
penambahan PEG. Metode adsorpsi dilakukan
dengan sistem bath dan analisa kesetimbangan
adsorpsi ditinjau berdasarkan dua isoterm
adsorpsi, yaitu Langmuir dan Freundlich. Pada
adsorpsi ionlogamPb(ll)oleh membran komposit menunjukkan bentuk term isoterm Freundlich,
sehingga besarnya kapasitas adsorpsi sebanding
dengan besarnya konsentrasi larutan logam.
.Membran khitosan-selulosa terikat silang K1%
mempunyai harga kapasitas adsorpsi terbesar
dibandingkan membran komposit yang lain. Hal
ini menunjukkan kandungan kadar khitosan terendah pada membran komposit selulosa ini
23
Co
Khitosan
3
~
i
.
,
.
Khitosan 3%5%PEG • Khitosan 3%10%PEGGambar29. Kapasitas adsorpsimembran
kompositK3%,K3%P5%danK3%P10%.
Dari Gambar 29 menunjukkan bahwa membran komposit K3%P5% mempunyai nilai
----
=
=
-
-Josson-Charier, M., Guibal, E., Roussy,J., 1996, Vanadium,(IV)Sorption by Chitosan : Kinetics and Equi1'ibrum,Wal. Res., 30, 2, pp. 6285-6290
Karthikeyan, G., Anbalagan, K., Andal,N. M., 2004, Adsorption Dynamics and Equilibrum Studies of Zn (11) opto Chitosan, Indian J.,
Chem.Sci., 116, 2, pp 119-127
Kumar, M. N.V., 2000, A review of Chitin and Chitosan Applications, Reactive and Functional Polymers,46, pp. 1-27
Lima, I. S. and Airoldi, C., 2000, A Thermodynamics Investigation and Chitosan Divalent Cation Interactions, Thermochimica Acta,421, pp.133-139
Planas, M. Ruiz, 2002, Development of Techniques Based on Natural Polymerfor the Recovery of Precious Metals, Thesis Doctoral, Universitat Politecnica de Catalunya
Quek, S. Y., 1998, The Use of Sago Waste for the Sorption of Lead and Cooper, Water SA, vol. 24, no. 33, pp 251-256
Wan Ngah, W. S., 2002, Removal Copper(11) Ions from Aqueous Solution onto Chitosan and Cross-linked Chitosan Beads, Reactive and Functional Polymers,50,181-190
Yang, T. C. and Zall, R. R., 1984, Adsorption of Metals by Natural Polymers Generated from Sea Food ProcessingWaste,Ind. Eng. Chem.
Prod. Res.Oev., 23, pp.168-172
Bimbing dan Eko-Adsorpsi Ion Logam Pb(lI) Pada Membran Selulosa-Khitosan Terikat Silang
mempunyai kapasitas adsorpsi yang terbesar serta penambahan PEG mempunyai pengaruh menurunkan kapasitas adsorpsi membran-khitosan selulosa terikat silang, dimana.nilai D tergaritung pada kuatnya karakteristik poridalam hidrogel. Meningkatnya koefisien difusi dengan temperatur ini mengikuti kinetik Arrhenius, dengan energi aktifasi pada orde 25 sampai 30 kj/mol. Nilai ini sedikit lebih tinggi daripada energi aktifasi untuk difusi molekul kecil daiam air, dan karena itu, mikroviskositas gel dapat berperan utama dalam proses transport parasetamol pada khitosan hidrogel. Eksponen Power Law untuk pelepasan kinetik yang sudah diperhitungkan antara 0,43 dan 0,55, menunjukkan bahwa proses transport larutan gel dapat dibuat oleh difusi Fickian.
DAFTARPUSTAKA
Bastaman, 1990, Penelitian Limbah Udang sebagai Bahan Industri Khitin dan Khitosan, BBIHP,Bogor
Boddu,V. M.and Smith, E. D., 2002, A Composite Chitosan Biosorbent for Adsorption of Heavy Metals from Wastewaters,
www.asc2002.com/manuscripts/E/EP-01 Standby.pdf
Cao, Z., Ge, H. and Lai, S., 2002, Studies on Synthesis and Adsorption Properties of Chitosan Cross Linked by Gluteraldehydeand CU(II) as Template Under Microwave Irradiation, European Polymer Journal, 37, pp. 2141-2143