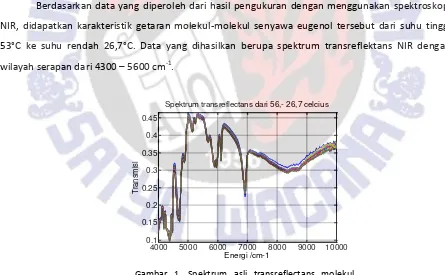
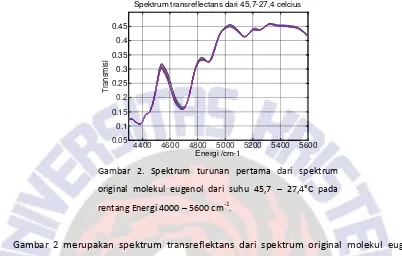
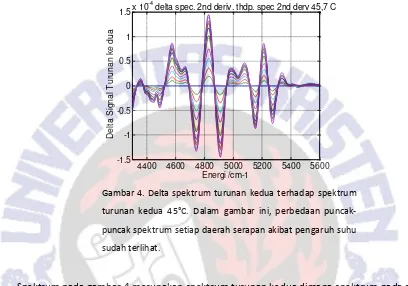
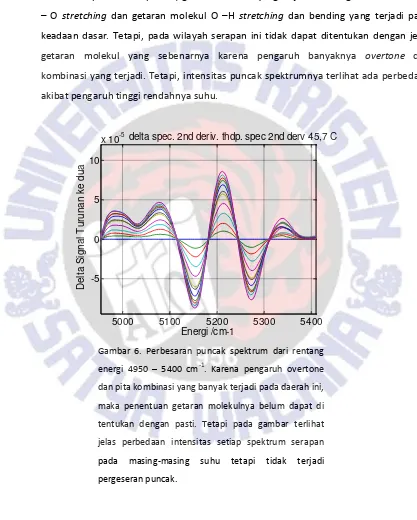
PENGARUH SUHU TERHADAP SERAPAN INFRAMERAH DEKAT SENYAWA EUGENOL
Teks penuh
Gambar



Dokumen terkait
Terkait Problematika pengembangan kurikulum bahasa Arab di MTs Darul Hikmah, yaitu dari segi beberapa guru yang kurang berpartisipasi dalam pengembangan kurikulum, sebagian pengurus
Tujuan pada penelitian ini adalah untuk mengetahui faktor-faktor yang mempengaruhi kinerja operasional terminal Becora, membuat rekomendasi guna meningkatan kinerja Terminal
Metode Penelitian Penelitian ini dilaksanakan dengan menggunakan pendekatan kuantitatif, dengan desain yang digunakan adalah Quasi Exsperimental Design Long Maching Hartati,
Latar belakang penelitian ini adalah rendahnya tingkat pemahaman Tema 7 Subtema 1 Pembelajaran 1. Hal tersebut diketahui pada saat wawancara dengan guru pengampu pembelajaran
pipa di dalamnya, fluida tersebut mengalir melalui cincin yang berbentuk silinder pipa, maupun silinder dalam dan silinder luar.Karena kedua aliran fluida melintas penukar panas
Kompresor atau blower jenis Roots mempunyai dua buah rotor yang masing-masing mempunyai dua buah gigi (Lobe) dan bentuknya mirip dengan kepongpong. Kedua rotor berputar
Dalam tahapan ini akan dilakukan analisa kelangsingan inti kedap air dengan metoda elemen hingga dengan menggunakan analisis couple antara deformasi/tegangan dan aliran dalam
Dengan segala kerendahan hati penulis mengucapakan puji syukur kehadirat Allah SWT, Sang pemilik alam semesta yang telah melimpahkan rahmat dan hidayah-Nya, sehingga penyusunan