BAB II
KAJIAN PUSTAKA
2.1. Definisi infeksi HIV
Infeksi HIV adalah infeksi yang disebabkan oleh human immunodeciency
virus(HIV). Sedangkan acquired immune deficiency syndrome (AIDS) adalah
kumpulan gejala dan tanda klinis akibat menurunnya daya tahan tubuh yang disebabkan oleh HIV(Levy, 2009).
2.2. Morfologi HIV
Human immunodeficiency virus (HIV) termasuk dalam retrovirus anggota
subfamili lentiviridae. Inti HIV mengandung 2 rantai RNA tunggal yang terikat pada protein gag (gag-derived protein) p24. Inti HIV terkandung di dalam dua lapisan lipid. Selubung (envelope) virus mengandung glycoprotein 120 dan glycoprotein transmembran 41. Komponen gp 120 dan gp 41 yang berperan penting dalam adesi HIV pada sel inang. Virus ini memiliki 3 gen yang diperlukan dalam replikasi yaitu gag, pol, env. Terdapat 6 gen tambahan pengatur ekspresi virus yangpentingdalam patogenesis (Tzu dan Ching, 2012).
.
2.3. Patogenesis
HIV terutama terdapat dalam cairan tubuh. Cairan tubuh yang potensial mengandung HIV adalah darah, cairan sperma, cairan vagina dan air susu ibu. Cara penularan dapat melalui jarum suntik, tusukan, atau abrasi mukosa selama hubungan seksual, transfusi darah, transplantasi organ dan penularan dari ibu ke anak (Levy, 2009).
Reseptor utama infeksi HIV-1 adalah CD4, ko-reseptor seperti CCR5 dan CXCR4. Sasaran Infeksi HIV-1 adalah pada sel imun CD4+ yang meliputi sel T CD4+, dendritic cell (DC), makrofag, monosit, timosit, dan sel microglia. HIV-1 juga menginvasi usus, menurunkan jumlah sel T CD4+ dan menyebabkan kerusakan jaringan limfoid. HIV terus bereplikasi dan menghindari respons anti-virus host, Hal tersebut mengakibatkan terjadinya penurunan respons imun, dan terjadi dominasi virus (Levy, 2009). Setelah jangkitan infeksi, kemudian HIV-1 menjadi laten pada sel tertentu seperti pada sel T CD4+ resting memory, sel Gambar 2.1 Gambar struktur Human Immunodeficiency Virus(Tzu dan Ching, 2012)
dendritik (DC), monosit, dan makrofag. Sel T CD4+ naïve, sel pluripoten
progenitor pada sumsum tulang, sel CD4+, dan makrofag pada cairan seminalis
juga dilaporkan sebagai reservoir infeksi laten. Reservoir yang lain meliputi sel mikroglobial dan sel makrofag pada cranial nerve system (CNS). HIV pada sel sel
reservoirtersebut sangat sulit dijangkau dengan terapi cARV(Levy, 2009)
Replikasi HIV-1 sangat erat hubungannya dengan kemampuan transkripsi sel host, serta pengaruh dari jaringan kompleks sitokin proinflamasi dan imunoregulator. TNF-α berperan penting dalam patogenesis HIV-1, yang merangsang transkripsi HIV-1 baik pada makrofag dan sel T. Sitokin proinflamasi lain seperti interleukin-1 (IL-1), IL-2, dan IL-6 juga merangsang replikasi HIV-1 (Le Saout dkk., 2012; Reuter Ma dkk., 2012)
2.4. Replikasi HIV
Replikasi HIV hanya terjadi pada sel CD4 yang aktif. Sel CD4 yang terinfeksi, teraktivasi dan mereplikasikan virus disebut sebagai productively
activated cell. Sedangkan sel CD4 yang teraktivasi tetapi tidak terinfeksi dan tidak
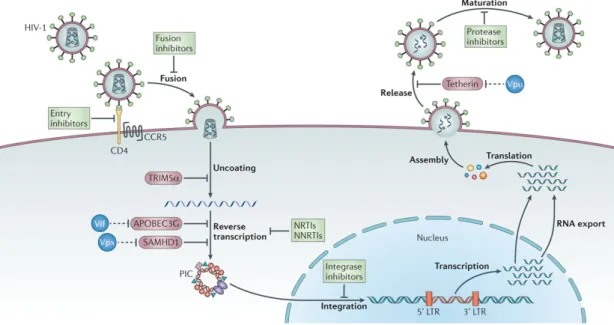
mereplikasikan HIV disebut uninfected activated cell atau bystander cell.Siklus replikasi HIV pada sel inang diawali dari perlekatan gp 120 pada molekul reseptor CD4 dan diikuti oleh ikatan antara gp 41 pada koreseptor CCR5 atau CXCR4. Setelah terjadi fusi dengan sel CD4, kemudian kompleks preintegrasi dalam caspid yang terdiri dari RNA virus dan enzim-enzim dilepaskan ke dalam sitoplasma sel CD4. Setelah itu terjadi transkripsi balik RNA virus menjadi DNA oleh enzim reverse transcriptase. DNA hasil transkripsi balik tersebut kemudian diintegrasikan pada DNA sel CD4 oleh enzyme integrase. DNA hasil transkripsi
balik tersebut juga memerantarai aktivasi sel CD4 agar terjadi proses integrasi yang efektif. DNA sel CD4 yang telah diintegrasikan dengan DNA virus kemudian mentranskripsikan mRNA untuk selanjutnya menghasilkan protein melalui translasi. Enzim protease selanjutnya memfragmentasikan rantai protein tersebut sesuai kebutuhan HIV. Semua komponen protein inti virus dibuat dengan cara yang sama dan komponen protein permukaan dibentuk melalui proses budding sampai terbentuk virus baru yang lengkap (Barre-Sinoussi F dkk., 2013)
Gambar 2.2Siklus Replikasi HIV(Barre-Sinoussi F, dkk 2013)
2.5. Inflamasi kronis pada infeksi HIV
Inflamasi kronis merupakan inflamasi yang berlangsung dalam jangka waktu lama dimana terjadi kerusakan jaringan ikat dan proses perbaikan yang terjadi secara simultan dan berulang. Terdapat 3 faktor yang mendorong terjadinya inflamasi kronis yaitu: 1) HIV, 2) translokasi microbial dan berkurangnya integritas mukosa saluran cerna, 3) koinfeksi dan infeksi CMV.
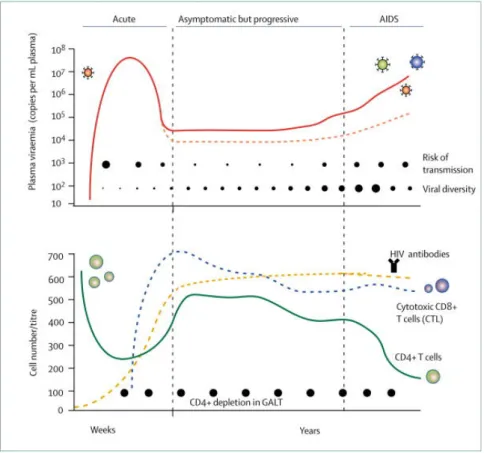
Inflamasi limfoid da dengan p anemia pe model yan G 2.6. Per Pe asimptoma yang tidak bervariasi infeksi ak dan ikuti respons im sekitar 3 tersebut m an berbagai atogenesi a enyakit kron ng dikeluark Gambar 2.3 rjalanan ala rjalanan ala atik, sampa k mendapat antara beb kut HIV-1, oleh penu mun baik h minggu set menyebabkan i penyakit k anemia pen nis pada pas kan oleh Ipp
3Inflamasikr amiah infek amiah infek ai pada AID terapi, wak erapa bulan viral load urunan juml humoral ma telah onset n penuruna kronis yang nyakit kron sien infeksi p H dkk ,(20 ronis pada i ksi HIV ksi HIV berv
DS sebagai ktu antara m n sampai 17 (VL) meni lah CD4. aupun selula infeksi. Se an jumlah C g lain (Ipp H nis secara HIV secara 014) infeksi HIV variasi mula manifestas mulai terinfe 7 tahun, den ingkat secar Kemudian ar. Antibod elama jang CD4, fibros H dkk.,201 umum, m a teoritis ter V (Ipp H dkk ai dari fase si lebih lanj eksi sampai ngan media ra cepat dal n diikuti de di spesifik H ka waktu sis jaringan 4). Bila dik maka patoge rmasuk di d k. 2014) klinis laten njut. Pada p terjadinya A an 10 tahun lam tiga mi engan timbu HIV-1 terde tersebut, p n ikat kaitan enesis dalam n atau pasien AIDS n.Pada inggu ulnya eteksi pasien
tetap berpotensi menularkan HIV-1 dalam periode jendela (windows periode) walaupun kadar virus dan antibodi tidak terdeteksi. Setelah masa tersebut, akan terbentuk respons imun terhadap HIV-1 dan mengendalikan replikasi virus \selama jangka waktu kurang lebih 5-10 tahun(Levy, 2009).
Selama fase akut, sel T CD4 kembali membaik, yang dapat berlangsung lebih dari 10 tahun, dengan replikasi virus yang dipertahankan tetap rendah, dibawah batas terdeteksi. VL akan stabil pada kadar tertentu selama beberapa waktu. Apabila penyakit progresif, sel T CD4+ secara gradual akan menurun. Pasien dengan hitung sel T CD4+ ≤200 sel/mm3 lebih mudah mengalami infeksi opportunistik dan keganasan dan berkembang menjadi AIDS (Simon dkk., 2006)
2.7. Klasifikasi klinis infeksi HIV
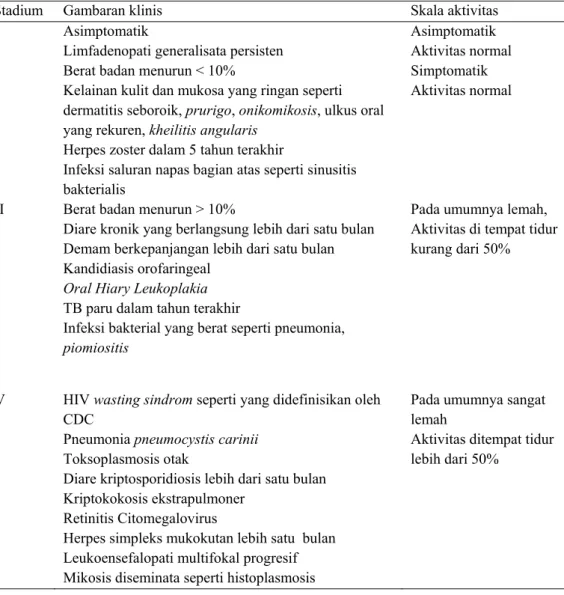
WHO padatahun 2007, telah mengembangkan definisi kasus dan stadium klinis HIV untuk negara – negara dengan sumber daya terbatas. Penentuan stadium berdasarkan klinis yang menjadi pedoman dalam diagnosis, evaluasi dan tatalaksana HIV/AIDS dan tidak memerlukan pemeriksaan hitung sel CD4.Stadium tersebut didefinisikan berdasarkan gejala dan kondisi klinis spesifik pada remaja dan dewasa yang berusia ≥ 15 tahun.
Tabel 2.1Stadium Klinis Infeksi HIV pada Dewasa Menurut WHO (Depkes RI, 2011)
Stadium Gambaran klinis Skala aktivitas
I Asimptomatik
Limfadenopati generalisata persisten
Asimptomatik Aktivitas normal II Berat badan menurun < 10%
Kelainan kulit dan mukosa yang ringan seperti dermatitis seboroik, prurigo, onikomikosis, ulkus oral yang rekuren, kheilitis angularis
Herpes zoster dalam 5 tahun terakhir
Infeksi saluran napas bagian atas seperti sinusitis bakterialis
Simptomatik Aktivitas normal
III Berat badan menurun > 10%
Diare kronik yang berlangsung lebih dari satu bulan Demam berkepanjangan lebih dari satu bulan Kandidiasis orofaringeal
Oral Hiary Leukoplakia TB paru dalam tahun terakhir
Infeksi bakterial yang berat seperti pneumonia, piomiositis
Pada umumnya lemah, Aktivitas di tempat tidur kurang dari 50%
IV HIV wasting sindrom seperti yang didefinisikan oleh CDC
Pneumonia pneumocystis carinii Toksoplasmosis otak
Diare kriptosporidiosis lebih dari satu bulan Kriptokokosis ekstrapulmoner
Retinitis Citomegalovirus
Herpes simpleks mukokutan lebih satu bulan Leukoensefalopati multifokal progresif Mikosis diseminata seperti histoplasmosis
Pada umumnya sangat lemah
Aktivitas ditempat tidur lebih dari 50%
Kandidiasis di esofagus, trakea dan paru Mikobakteriosis atipikal diseminata Septisemia salmonelosis non tifoid Tuberkulosis di luar paru
Limfoma Sarkoma kaposi Ensefalopati HIV
2.8. Terapi Kombinasi ARV 2.8.1. Definisi
Terapi kombinasi ARV atau dikenal dengan nama highly active
antiretroviral therapy (HAART) adalah terapi yang mengandung paling sedikit
tiga jenis obat ARV dari dua jenis klas yang berbeda (Arts EJ dan Hazuda DJ, 2012).
Keberhasilan terapi cARV dalam menekan replikasi virus mengakibatkan pemulihan sistem imun dan perbaikan klinis, yang berdampak terhadap perbaikan kualitas hidup dan menekan penularan lebih lanjut. Disamping itu keberhasilan tersebut juga diikuti dengan timbulnya berbagai konsekuensi dari inflamasi kronik.
2.8.2 Jenis ARV
Perkembangan pengobatan ARV pada pasien terinfeksi HIV/AIDS merupakan salah satu perkembangan paling dramatis dalam sejarah pengobatan penyakit infeksi. Pada tahun 1987 Zidovudin merupakan jenis ARV yang pertama kali diperkenalkan, kemudian diikuti oleh didanosine dan zalcitabine. Sejak tahun 1996 mulai diperkenalkan terapi kombinasi ARV (Arts EJ dan Hazuda DJ, 2012).
Sampai sekarang terdapat 5 klas ARV yang telah disetujui oleh Food and
Drug Administration (FDA): (1) Nucleoside/nucleotide-analog reverse transcriptase inhibitors (NRTI), seperti zidovudin, lamivudine, stavudine, dan
didanosine; (2) Non-nucleoside reverse transcriptase inhibitors (NNRTI) seperti nevirapine, efavirenz, dan delavirdine; (3) Protease inhibitors (PI) seperti nelfinavir, ritonavir, lopinavir, dan indinavir; (4) integrase inhibitor: raltegravir (5) Fusion inhibitor (FI) T-20 seperti enfuvirtide(Arts EJ dan Hazuda DJ, 2012).
2.8.3 Kegagalan Terapi ARV
Apabila setelah memulai pemakaian terapi minimal 6 bulan dengan kepatuhan yang baik, tetapi tidak terjadi respon terapi yang diharapkan, maka perlu dipikirkan kemungkinan terjadi gagal terapi. (Kemenkes RI Ditjen P2PL, 2014b) Kriteria gagal terapi ditentukan berdasarkan kriteria klinis, imunologis dan virologis.
- Kegagalan klinis adalah munculnya penyakit infeksi oportunistik baru atau berulang stadium klinis WHO 4.
- Kegagalan imunologis adalah gagal mencapai dan mempertahankan jumlah CD4 yang adekuat, Didefinisikan sebagai berikut:
- CD4 turun ke nilai awal atau nilai yang lebih rendah dibandingkan CD pada awal terapi ARV
- Atau CD4 tetap <di bawah 100 sel/mm3 setelah satu tahun pengobatan.
- Atau Penurunan CD4 sebesar lebih dari 50% dari nilai tertinggi yang pernah dicapai selama terapi ARV
- Kegagalan virologis: bila viral load tetap > 1.000 copies/ml berdasarkan 2 kali pemeriksaan HIV RNA dengan jarak waktu 3 – 6 bulan.
Pada daerah dengan sumber daya terbatas dan pemeriksaan viral loadtidak bisa rutin diterapkan sebelum memulai terapi cARV, maka kriteria gagal ditegakkan dari kriteria klinis dan didukung dengan kriteria imunologis.
2.9. Manifestasi gangguan hematologi pada HIV
Manifestasi kelainan hematologis pada infeksi HIV sangat bervariasi dapat berupa gangguan hematopoesis, sitopenia dan koagulopati. Anemia merupakan kelainan hematologis yang sering dijumpai yaitu sekitar 37.5% ( De Santis dkk., 2011). Anemia akibat penyakit kronik merupakan jenis anemia yang paling sering dijumpai pada pasien HIV termasuk yang sudah mendapat terapi cARV.
2.10. Definisi dan klasifikasi derajat berat anemia
Definisi anemia mengacu pada kadar hemoglobin yang normal. Kadar hemoglobin normal pada laki-laki adalah 16 ± 2 g/dl, sedangkan pada perempuan adalah 14 ± 2 g/dl. Terdapat beberapa sistem gradasi untuk menilai derajat berat anemia, yaitu sistem gradasi yang dibuat oleh AIDS Clinical Trials Group, World
Health Organization, dan the National Cancer Institute. Konsentrasi hemoglobin
bukan merupakan satu-satunya determinanyang mempengaruhi beratnya gejala yang dialami. Dengan demikian manifestasi klinis harus dipertimbangkan dalam menentukan derajat berat anemia
Anemia pada penyakit kronik adalah anemia yang dijumpai pada penyakit kronik tertentu yang khas ditandai oleh gangguan metabolism besi yaitu hipoferemia sehingga penyediaan besi yang dibutuhkan untuk sintesis hemoglobin berkurang akan tetapi cadangan besi di sumsum tulang masih cukup (Bakta, 2006). Pada umumnya anemia ini berderajat ringan sampai sedang dengan gambaran morfologi normokromik normositer, namun dapat juga menjadi hipokromik-normositer, namun dengan memberatnya progresivitas penyakit, anemia yang berlangsung lama, atau yang terjadi pada populasi yang membutuhkan besi lebih banyak, maka dapat menjadi hipokromik-mikrositer (Ganz dan Nemeth, 2009; Roy, 2010). Secara biokimiawi, anemia ini ditandai oleh kadar serum iron yang rendah, menurunnya kadar total iron binding capacity, kadar saturasi transferin menurun, namun cadangan besi masih cukup dalam sumsum tulang (Price dan Schirier,2010; Roy, 2010)
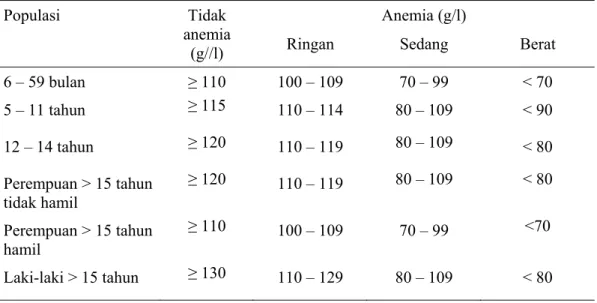
Tabel 2.2 Kadar hemoglobin untuk diagnosis anemia pada daerah dengan ketinggian setinggi permukaan laut (WHO, 2011)
Populasi Tidak anemia
(g//l)
Anemia (g/l)
Ringan Sedang Berat
6 – 59 bulan ≥ 110 100 – 109 70 – 99 < 70 5 – 11 tahun ≥ 115 110 – 114 80 – 109 < 90 12 – 14 tahun ≥ 120 110 – 119 80 – 109 < 80 Perempuan > 15 tahun tidak hamil ≥ 120 110 – 119 80 – 109 < 80 Perempuan > 15 tahun hamil ≥ 110 100 – 109 70 – 99 <70 Laki-laki > 15 tahun ≥ 130 110 – 129 80 – 109 < 80
2.11. Prevalensi dan faktor risiko anemia pada pasien HIV
Prevalensi anemia pada infeksi HIV sangat bervariasi yaitu antara 1 – 95%. Hal ini disebabkan oleh perbedaan lokasi penelitian, heterogennya penelitian kohort dan definisi anemia yang dipergunakan (Belperio dan Rhew, 2004) Di Cina prevalensi anemia pada pasien HIV yang akan memulai cARV adalah 38.9% masing masing secara berurutan anemia ringan, sedang dan berat adalah 19.2%, 17.1% dan 2.6%, dengan analisis regresi logistic berganda menunjukkan etnis Uyghur, perempuan, kadar CD4 yang rendah, IMT yang rendah , riwayat TB berkaitan dengan prevalensi anemia yang lebih tinggi (Mitiji P dkk., 2014). Prevalensi anemia di Ethiopia, dilaporkan adalah 35%, prevelensi lebih tinggi secara bermakna pada pasien dengan kadar CD4 yang lebih rendah (Ferede danWondimeneh, 2013).Di Ethiopia dijumpai prevalensi anemia pada pasien HIV adalah 23.1%. Prevalensi pada pasien yang belum mendapat cARV dan yang sudah mendapat cARV adalah masing masing adalah 29.9% dan 16.2% (P=0.014). Prediktor anemia pada pasien yang belum mendapat cARV adalah: adanya infeksi oportunistik (P=0.004, 95% CI=1.69–15.46), hitungsel CD4 < 200 cells/ul (P=0.001, 95% CI=2.57–36.89) dan tinggal di pedesaan (P=0.03, 95% CI=1.12–10.39). sedangkan prediktor pada pasienyang sudah mendapat cARV adalah regimen (ZDV/3TC/NVP) (P=0.019, 95% CI=0.01–1.24) dan lama pemakaian cARV (P=0.007, 95% CI=0.003–0.40.24) (Mail LG,2013)
Penelitian mengenai insiden anemia pada pasien HIV yang mendapat cARV dilaporkan berturut turut adalah 24.3 dan 8.1 per 100 person years pada kohort berbasis ZDV dan non-ZDV setelah 6 bulan follow up dan 12.5 dan 5.3 per
100 person years setelah 24 bulan follow up. Prediktor terjadinya anemia adalah ZDV, kadar Hb awal yang rendah, IVDU, kadar CD4 < 200 sel/ul dan AIDS (Curkendall dkk., 2007). Penelitian retrospektif di klinik VCT Nusa Indah RS Sanglah Denpasar dijmpai prevalensi anemia pada pasien HIV yang mendapat cARV berbasis ZDV adalah 30.8% dengan morfologi makrositer sebesar 7.9% dan non makrositer sebesar 22.9% (Wibawa dan Merati, 2010)
2.12. Etiopatogenesis Anemia pada pasien HIV
Penyebab anemia pada pasien dengan HIV adalah multifaktorial. Etiopatogenesis anemia pada infeksi HIV dapat dibedakan menjadi (Volberding PA dkk., 2004) :
1. Penurunan produksi sel darah merah: penurunan produksi sel darah merah yang merupakan konsekuensi dari infiltrasi ke sumsum tulang oleh keganasan, infeksi, pemakaian obat-obat mielosupresi, infeksi HIV sendiri, penurunan produksi eritropoetin endogen, respon eritropoetin yang blunted atau hipogonadism
2. Peningkatan destruksi sel darah merah: peningkatan destruksi sel darah merah yang prematur bisa terjadi pada limfa atau sistem sirkulasi. Anemia hemolitik bisa disebabkan oleh autoantibodi pada sel darah merah, sindroma hemopagositosis, disseminated intravascular coagulation, trombotic thrombocytopenic purpura, defisiensi glucose-6-phosphat dehidrogenase, pemakaian beberbagai jenis obat.
3. Produksi sel darah merah yang tidak efektif: yang disebabkan oleh defisiensi nutrisi (besi, asam folat atau itamin B12)
4. Perdarahan: Perdarahan bisa terjadi pada beberapa kondisi seperti pada keganasan (seperti Kaposi sacoma dalam saluran cerna) atau perdarahan dari lesi gastrointestinal, seperti infeksi cytomegalovirus
2.13. Obat-obat myelosupresif
Beberapa jenis obat yang dapat menyebabkan supresi sumsum tulang pada pasien HIV (Volberding PA dkk., 2004).
Tabel 2.3 Jenis- Jenis obat mielosupresif yang sering digunakan oleh pasien HIV Golongan Obat Jenis Obat
Antiretrovirus: Zidovidine, Zalciabine
Obat antiviral: Ganciclovir, foscarnet, cidofovir Obat antijamur: Flucytocin, Amphotericin
Obat anti-Pneumocystis carinii: Sulfonamide, Trimethoprim, pyrimethamne, pentamidin
Obat antineoplastik:
Cyclophosphamide, doxorubicin, methotrexate, paclitaxel, vinblastine, liposomal doxorubicin, liposomal daunorubicin
Immne respons modifier
Zidovudine merupakan salah satu jenis ARV yang paling sering digunakan dalam terapi kombinasi ARV di Negara berkembang, termasuk di Indonesia.Demikian juga pemakaian trimetroprim yang dikombinasi dengan sulfamethoxazole, sering dipakai sebagai terapi profilaksis primer atau sekunder untuk PCP, toxolasmosis dan diare. Pemakaian kotrimoxazole trimetroprim sering
dipakai dalam jangka panjang sampai tercapai kadar CD4 yang protektif untuk infeksi tersebut.
Pada penelitian kohort, pemberian ARV berbasis zidovudin bersama-sama dengan trimetropin sulfamethoxazole di Africa, dijumpai neutropenia grade 3-4 sebesar 56.3/ 100 person years dan anemia grade 3-4 sebesar 9.6/100 person
years. Neutropenia grade 3-4 terjadi segera setelah pemberian zidovudine (Moh
dkk., 2005). Sedangkan pada penelitian restrospektif di VCT RS Sanglah, angka kejadian makrositosis pada pemakaian ARV berbasis zidovudine adalah 50.6%, dimana maktositosis tanpa anemia sebanyak 46.4% dan makrositosis dengan anemia sebanyak 7.9%. (Wibawa dan Merati, 2010)
2.14. Penyakit dasar pada anemia penyakit kronik
Anemia pada infeksi HIV lebih sering disebabkan oleh anemia penyakit kronik. Beberapa penyakit dasar yang juga dapat merupakan penyebab anemia penyakit kronik adalah:
2.14.1. Penyakit autoimun
Beberapa penyakit autoimum yang dapat merupakan penyebab anemia akibat penyakit kronik adalah Arthritis rheumatoid, SLE, Vasculitis, Sarcoidosis, Inflammatory bowel disease. Diperkirakan penyakit autoimum menyebabkan anemia penyakit kronik antara 8 – 73% (Weiss dan Goodnough. 2005). Pada era terapi kombinasi ARV, prevalensi penyakit arthritis terkait autoimum sangat jarang dilaporkan pada pasien HIV. Pada tinjauan kepustakaan dari januari 1981 sampai agustus 2007 dijumpai prevalensi berbagai spectrum klinis rematik pada pasien infeksi HIV adalah sebagai berikut: SLE (0.3%), psoriasis (0.2%), arthritis
rheumatoid (0.1%), polymyositis (0.1%), scleroderma (0.1%) (Yao dkk,, 2008). Sedangkan pada penelitian retrospektif selama 20 tahun di Taiwan dijumpai penyakit arthritis autoimun sebesar 0.7% ( 26 dari 3623 pasien HIV) masing masing 18 (0.49%) pasien dengan ankylosing spondylitis, 6 (0.1%) pasien dengan arthritis rheumatoid, 1(0.02%) pasien dengan arthritis psoriatis, dan 1 (0.02%) pasien dengan sindroma sjorgen. 15 pasien (57.7%) dari prevalensi tersebut terjadi setelah pemberian cARV( Yang JJ dkk., 2013).
2.14.2. Penyakit keganasan
Penyakit keganasan yang meliputi keganasan hematologi dan keganasan organ solid diperkirakan menyebabkan anemia penyakit kronik sekitar 30 – 77% (Weiss dan Goodnough, 2005). Pada infeksi HIV diketahui risiko terhadap kanker seperti sarcoma Kaposi, limfoma non hodgkin (NHL) dan kanker servik yang disebut dengan AIDS defining cancer (ADCs) adalah lebih tinggi. Pada penelitian kohort secara konsisten dilaporkan terjadi peningkatan risiko non AIDS
defining cancer (NADCs) seperti penyakit Hodgkin dan kanker anogenital. Pada
era pemakaian cARV dilaporkan telah terjadi penurunan insiden kanker sarcoma Kaposi dan NHL.
Data tentang keganasan pada pasien HIV di Asia sangat terbatas. Pada penelitian observasional 13 site di Asia Pasifik (TAHOD), dijumpai dari 215 kasus kanker 66% termasuk ADCs (16% Sarkoma Kaposi, 40% lymphoma non-Hodgkin’s dan 9% kancer cervik). Kanker yang termasuk NADCs yang paling banyak ditemukan adalah kanker Paru (6%), Payudara (5%), kanker
hepatocellular (2%), lymphoma Hodgkin’s (2%) dan leiomyosarcoma (1.4%). (Petoumenos K dkk., 2010)
2.14.3. Penyakit infeksi oportunistik
Penyakit infeksi yang meliputi infeksi virus, bakteri, jamur dan parasit diperkirakan menyebabkan anemia penyakit kronik sekitar 18 – 95% (Weiss dan Goodnough, 2005). Prevalensi infeksi oportunistik berbeda pada beberapa daerah dan Negara. Di Negara sub Sahara Afrika > 80% pasien dengan HIV meninggal karena kasus infeksi dengan penyebab yang paling sering adalah tuberculosis. Di klinik VCT Sanglah prevalensi penyakit oportunistik yang paling sering dijumpai selama 2004 sampai 2007 adalah tuberculosis paru (Wiryani dkk., 2008).
2.14.4. Penyakit ginjal kronik
Penyakit ginjal kronik diperkirakan mendasari anemia pada penyakit kronik sekitar 23 – 50% (Weiss dan Goodnough, 2005). Pada pasien HIV, penyakit ginjal dapat terjadi akibat dari infeksi HIV yang disebut dengan HIVAN (HIV associated nefropathy). Beberpa faktor yang dilaporkan terkait dengan terjadinya penyakit ginjal kronik pada HIV adalah genetic, umur, perubahan metabolic terkait pemberian cARV, paparan berbagai obat nefrotoksis, dan koinsiden dengan hepatitis C dan pemakaian obat intravenous. Pada beberapa penelitian terakhir dilaporkan prevalensi penyakit ginjal kronik pada pasien dengan infeksi HIV berkisar kurang dari 2.4% sampai sekitar 10% (Estrella dan Fine, 2010).
2.15. Patogenesis anemia penyakit kronik pada infeksi HIV
Anemia pada penyakit kronik ditandai oleh penurunan produksi sel darah merah, supresi respon retikulosit dan menurunnya respon fisiologis eritropoetin. Patogenesis anemia pada penyakit kronik melibatkan mekanisme imun, sitokin dan sel sel sistem retikuloendotelial yang menginduksi hemostasis besi, proliferasi sel progenitor eritroid, produksi eritropoetin dan masa hidup dari sel darah merah. Saat ini mekanisme patogenesis anemia pada penyakit kronik secara umum meliputi( Weiss dan Goodnough, 2005):
2.15.1. Disregulasi hemostasis besi
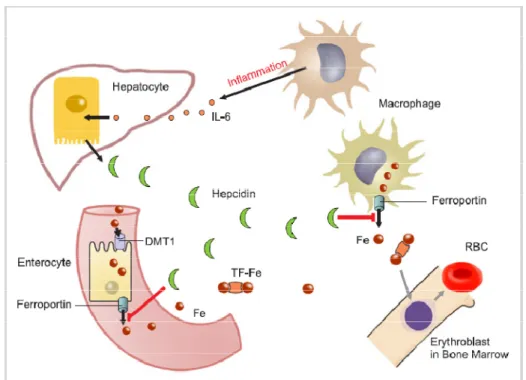
Ciri utama anemia pada penyakit kronik adalah terjadinya gangguan hemostasis besi, berupa peningkatan uptake dan retensi besi dalam sel-sel RES. Hal tersebut menyebabkan pergeseran besi dari sirkulasi kedalam tempat tempat penyimpanan besi di RES, terbatasnya ketersediaan besi untuk sel sel progenitor eritroid dan gangguan eritropoesis karena restriksi besi. Pada binatang yang diinjeksi dengan sitokin proinflamasi IL 1 dan TNF α, dapat menyebabkan hipoferemia dan anemia. Kondisi kombinasi tersebut berkaitan dengan sintesis feritin yang berperan dalam penyimpanan besi oleh makrofag dan hepatosit. Pada infeksi kronik makrofag lebih sering mendapatkan besi melalui eritrofagositosis dan import ferrous iron transmembrans melalui protein divalent metal transporter 1 (DMT1) ( Weiss dan Goodnough, 2005).
Interferon γ, lipopolisaccharida dan TNF α meningkatkan regulasi ekspresi DMT1, dengan meningkatkan uptake besi ke dalam makrofag yang sudah aktif.
Rangsangan proinflamasi tersebut juga menginduksi retensi besi dalam makrofag dengan cara menurunkan regulasi ekspresi ferroportin, kemudian menghambat pelepasan besi dari sel tersebut. Ferroportin merupakan sebuah protein eksportir besi transmembran, yang berperan dalam proses yang terkait dengan transfer besi ferrous yang diabsorpsi dari enterosit duodenum ke sirkulasi. IL 10 yang merupakan sitokin antiinflamasi dapat menginduksi anemia melalui stimulasi transferrin yang memerantarai akusisi besi oleh makrofag dan melalui translasi stimlasi ekspresi ferritin. ( Weiss dan Goodnough, 2005).
Hepsidin adalah reaktan protein fase akut terdiri dari 25 asam amino, yang berperan dalam regulasi besi. Ekspresi hepsidin diinduksi oleh lipopolisakarida dan IL 6 serta dihambat oleh TNF α. Hepsidin memegang peranan yang penting dalam diversi lalu lintas besi melalui penurunan absorpsi besi di duodenum dan menghambat pelepasan besi dari makrofag ( Weiss dan Goodnough, 2005).
2.15.2. Gangguan proliferasi sel –sel progenitor
Gangguan proliferasi dan diferensiasi prekusor eritroid ( erytroid burst
forming unit dan erytroid colony forming unit) terkait dengan efek hambatan dari
interferon α-β dan γ, TNF α dan IL 1 yang mempengaruhi pertumbuhan erytroid
burst forming unit dan erytroid colony forming unit). Interferon γ merupakan
inhibitor yang poten, yang direfleksikan melalui hubungan terbalik antara interferon γ dengan kadar hemoglobin dan hitung retikulosit. Mekanisme penyakit dasar yang melibatkan sitokin yang memicu apoptosis, yang mana tampaknya, menjadi bagian, hubungan dengan pembentukkan ceramide, menurunkan regulasi ekspresi reseptor eritropoetin pada sel sel progenitor dan menurunnya ekspresi
factor – factor pro hematopoesis, seperti faktor stemsel. Disamping itu sitokin juga memiliki efek toksik langsung pada sel progenitor dengan cara meransang pembentukkan radikal bebas labil seperti nitric oksida atau anion superoxide oleh
neighboring makcrophage-like cells ( Weiss and Goodnough, 2005).
2.15.3. Respon eritropoetin
Eritropoetin memegang peranan penting dalam regulasi proliferasi sel eritroid. Ekspresi eritropoetin berbanding terbalik dengan kadar hemoglobin dan oksigenasi jaringan, dimana terdapat hubungan semilogaritme antara respon eritropoeitin (log) dan derajat berat anemia (linier). Pada umumnya respon eritropoetin pada anemia penyakit kronik tidak adequate sesuai dengan derajat anemia. In vitro IL 1dan TNF α secara langsung menghambat ekspresi eritropoetin. Respon sel-sel progenitor eritroid tampaknya berbanding terbalik dengan derajat berat penyakit yang mendasari dan jumlah sitokin dalam sirkulasi, dimana semakin tinggi konsentrasi interferon γ atau TNF α, maka lebih tinggi jumlah eritropoetin yang diperlukan untuk merestorasi pembentukkan erythroid
colony forming unit. Setelah eritropoetin berikatan dengan receptor, eritropoetin
menstimulasi komponen dari jalur signal transduksi dan selanjutnya mengaktifkan mitogen dan phosphorylase tyrosine kinase, proses tersebut dipengaruhi oleh sitokin inflamasi dan pengaturan umpan balik negatif ( Weiss and Goodnough, 2005).
Kurangnya respon eritropoetin disebabkan oleh efek hambatan oleh sitokin proinflamasi terhadap proliferasi sel sel progenitor erytroid, down regulasi reseptor eritropoetin, dan terbatasnya persediaan besi memberikan kontribusi
terhadap berkurangnya proliferasi sel dan sintesis hemoglobin. Peningkatan eritropagositosis selama proses inflamasi menyebabkan penurunan waktu hidup eritrosit yang diperantarai oleh sitokin dan radikal bebas( Weiss and Goodnough, 2005).
2.16. Peranan Interleukin 6 pada anemia penyakit kronik pada infeksi HIV IL 6 merupakan sitokin pleiotropik yang diproduksi oleh beberapa jenis sel seperti monosit, fibroblast, sel-sel endotel dan limfosit T dan B. IL 6 tidak diekspresikan secara terus menerus, melainkan banyak diinduksi dan diproduksi sebagai respon terhadap sejumlah rangsangan keradangan seperti IL-1, TNF α, produk – produk bakteri, atau infeksi virus. IL 6 memiliki fungsi yang berbeda meliputi diferensiasi dan/atau aktivasi makrofag dan sel T, sel-sel pertumbuhan dan diferensiasi sel-sel B, stimulasi hematopoesis dan diferensiasi neural (Scheller dkk., 2011).Kemungkinan peranan dari IL 6 pada keradangan akut ke keradangan kronik adalah(Gabay, 2008):
- pada tahap 1 keradangan akut, IL 6 berikatan dengan soluble IL6 receptor. - Pada tahap 2, trans-signaling melalui gp 130 akan menyebabkan penarikan
dari monosit.
- Pada tahap 3, IL 6 memicu apoptosis neutrophil, fagositosis dan akumulasi mononuclear pada tempat injury.
Pola kadar IL-6 serum pada pasien infeksi HIV yang mendapatkan ARV masih kontroversi. Basrard dkk., (2012) melaporkan bahwa kadar IL-6 serum berkorelasi positif dengan kadar viral load (VL) HIV pada pasien yang sudah terkendali dengan terapi cARV. Nilai batas kadar VL yang bermakna dengan peningkatan IL-6 adalah 31 copi/ml. Sedangkan Shive dkk., (2012) melaporkan bahwa tidak terdapat hubungan antara kadar IL-6 dengan kadar HIV-1 RNA dan tidak terbukti bahwa replikasi HIV memicu ekspresi IL-6 secara in vivo atau in vivo. Kadar IL-6 dilaporkan berbanding terbalik dengan kadar CD4 nadir. (Borges Gambar 2.5Peran dari IL 6 pada keradangan akut ke keradangan kronik (Gabay, 2008)
AH, 2014) Pada penelitian cross sectional dijumpai bahwa kadar IL-6 serum yang tinggi terkait dengan anemia pada pasien HIV yang mendapat cARV (Borges dkk., 2014).
Pada anemia akibat penyakit kronik, IL-6 berperan melalui induksi translasi dan transkripsi feritin sehingga mengakibatkan peningkatan simpanan besi dalam RES. IL-6 juga memicu pembentukkan hepsidin, sehingga absorpsi besi di duodenum dan eksport besi dari makrofag menurun. Secara sistemik IL 6 memberikan dampak hipoferrinemia dan hiperferitinemia. ( Weiss dan Goodnough, 2005; Raj DS, 2009)
Peranan IL 6 pada bebeberapa penelitian masih kontradiksi. Pada penelitian di Bali, tidak dijumpai hubungan yang bermakna antara kadar IL 6 dengan kadar besi serum dan kadar hemoglobin pada penderita anemia penyakit kronik (Wibawa dan Bakta, 2008). Sedangkan pada penelitian potong lintang pada orang dewasa di Jepang dijumpai hubungan terbalik antara kadar IL 6 serum dengan kadar besi pada serum (Nakagawa, 2014).
2.17. Faktor -faktor yang mempengaruhi kadar IL-6 serum selama infeksi HIV
Sangat sedikit data yang tersedia tentang factor-faktor yang berkaitan dengan kadar IL 6 serum yang beredar dalam sirkulasi . Penelitian trial 3 study besar seperti INSIGT SMART. ESPRITdan SILCAAT yang melibatkan 9864 responden menemukan bahwa tingginya kadar IL-6 berkaitan peningkatan umur, ras bukan hitam, peningkatan IMT, kadar serum lipid yang lebih rendah, replikasi HIV. Hitung nadir CD4 yang rendah, pemakaian protease inhibitor, kondisi
ko-morbid, penurunan kadar estimated glomerular filtration rate (eGFR)(Borges, 2015).
2.18. Peranan hepsidin pada anemia penyakit kronik pada infeksi HIV
Hepsidin merupakan asam amino yang berperan sebagai regulator utama metabolism besi. Hepsidin disintesis terutama di hati, namun beberapa sel dan jaringan tubuh yang lain seperti jaringan adiposit, otak, sel makrofag dan neutropil yang teraktivasi akibat infeksi bakteri, juga mensintesis hepsidin dalam jumlah kecil. Hepsidin yang matang beredar dalam plasma, 89% terikat spesifik pada α2 -makroglobulin (Ganz dan Nemeth, 2009; Babitt dan Lin, 2010)
Regulasi sintesis hepsidin pada inflamasi secara umum melalui peranan IL-6 yang dilepaskan oleh makrofag Sintesishepsidinmeningkat dalam kondisi konsentrasibesi plasma yang tinggi, infeksi danatau peradangansehingga terjadi
penurunanketersediaanbesi, sedangkansintesishepsidinmenurun terjadi pada kondisi yangmemerlukanpeningkatan konsentrasizat besiserum, seperti peningkatanatau tidak efektifnya eritropoiesis, hipoksia, anemiadandefisiensi besi.
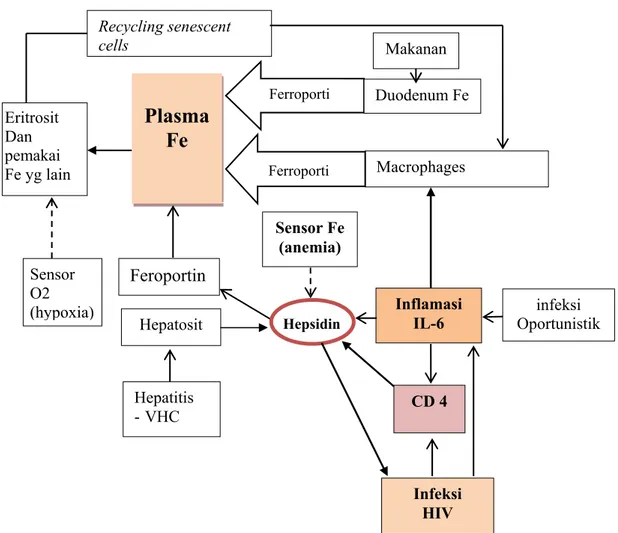
Pada infeksi HIV, selama fase akut pada saat terdeteksi viremia, terjadi peningkatan kadar hepsidin disertai kadar besi plasma. Pada saat terjadi transisi dari infeksi akut ke kronik yaitupada 60 hari pertama infeksi, hepsidin berkorelasi positif dengan kadar set poin VL plasma. Hepsidin masih tetap meningkat pada pasien HIV kronik yang tidak diterapi maupun yang mendapat terapi ARV. Hepsidin masih tetap meningkat walaupun pasien sudah mendapat cARV yang mensupresi HIV sampai kadar tidak terdeteksi. Hal tersebut disebabkan oleh masih persistennya aktivasi imun yang ditunjukkan oleh adanya peningkatan hepsidin yang disertai oleh peningkatan kadar CRP, IL-18 dan TNFα pada pasien yang mendapat terapi cARV. Kadar hepsidin pada fase akut infeksi, menurun seiring dengan tersupresinya HIV, namun hepsidin masih tetap meningkat secara bermakna (sekitar 2 kali lipat) pada fase kronik (Armitage dkk., 2014). Namun hal yang sebaliknya dilaporkan pada publikasi terakhir pada pasien HIV yang mendapat cARV, dijumpai kadar hepsidin secara bermakna lebih tinggi pada pasien dengan kadar RNA yang tinggi dibandingkan dengan kadar HIV-RNA yang tidak terdeteksi ( Malvoisin dkk.,2015). Penelitian terakhir melaporkan bahwa kadar hepsidin pada pasien HIV dengan ARV naïve lebih rendah dibandingkan kadar hepsidin partisipan seronegatif dan pasien HIV yang mendapat ARV (Cunha JD dkk., 2015). Pada HIV stadium lanjut dijumpai kadar hepsidin berbanding terbalik dengan kadar CD4 ( Wisaksana dkk., 2013). Gambaran regulasi hepsidin pada infeksi HIV dapat dilihat pada gambar berikut:
Gambar 2.7 Regulasi hepsidin pada infeksi HIV (Modifikasi dari Mupfudze TG, 2014 yang dikutip dari Nemets dan Ganz, 2006)
2.19. Gambaran klinis anemia pada pasien HIV
Tidak ada gejala atau tanda spesifik anemia yang lebih sering muncul pada kelompok pasien dengan infeksi HIV. Manifestasi klinis anemia pada pasien HIV sangat bervariasi tergantung pada penurunan dari kapasitas angkut oksigen, derajat perubahan volume total darah, kecepatan terjadinya anemia, kemampuan kompensasi dari sitem paru-paru dan kardiovaskular dan manifestasi penyakit
Ferroporti Ferroporti Eritrosit Dan pemakai Fe yg lain Sensor O2 (hypoxia) Hepatosit Feroportin Sensor Fe (anemia) Inflamasi IL-6 CD 4
Plasma
Fe
Recycling senescent cells Macrophages Duodenum Fe infeksi Oportunistik Infeksi HIV Hepatitis - VHC Hepsidin Makananyang mendasari. Pada umumnya pasien dengan anemia derajat sedang dan berat akan menunjukkan gejala-gejala. Gejala yang timbul dapat terjadi pada berbagai sistim organ.
2.20. Diagnosis anemia penyakit kronik pada infeksi HIV
Pada umumnya anemia penyakit kronik adalah berderajat ringan sampai sedang dengan gambaran morfologi normokromik normositer, namun dapat juga menjadi hipokromik-normositer, namun dengan memberatnya progresivitas penyakit, anemia yang berlangsung lama, atau yang terjadi papa populasi yang membutuhkan besi lebih banyak, maka dapat menjadi hipokromik-mikrositer (Ganz dan Nemeth, 2009; Roy, 2010). Secara biokimiawi, anemia ini ditandai oleh kadar serum iron yang rendah, menurunnya kadar total iron binding capacity, kadar saturasi transferin menurun, namun cadangan besi masih pada sumsum tulang cukup (Price dan Schirier,2010; Roy, 2010)
Diagnosis anemia penyakit kronik ditegakkan bila kadar Hb < 13 g/dl pada laki-laki atau < 12 g/dl pada perempuan, dengan morfologi normokromik-normositer atau hipokromik-mikrositer (MCV < 80 fl dan MCH < 27 pg) dengan kadar besi serum < 50 mg/dL, TIBC < 350 mg/dL dan kadar serum feritin ≥ 30 ng/ml, dengan menyingkirkan anemia pada penyakit ginjal kronik, penyakit hati kronik dan hipotiroid. (Bakta, 2006; Cullis, 2011, Poggiali dkk, 2014 )
2.21. Diagnosis Banding anemia penyakit kronik 2.21.1 Anemia Pada tumor sumsum tulang
Tumor pada sumsum tulang pada pasien dengan infeksi HIV terutama disebabkan oleh leukemia, multiple myeloma, limfoma dan tumor metastase ke sumsum tulang. Kemungkinan diagnosis tumor pada sumsum tulang perlu dipikirkan bila dijumpai anemia yang disertai splenomegali, organomegali, leukositosis, leucopenia, trombositosis atau trombositopenia. (Koury dan Rhodes, 2012)
2.21.2 Anemia akibat infeksi sumsum tulang
Infeksi sumsum tulang pada pendeita HIV dapat disebabkan oleh M. TBC, M avium complex, Histoplasmosis, Cryptococcus, cytomegalovirus, Leishmania, Pneumocystis carinii dan Parvovirus (Tripathi dkk 2005). Kemungkinan diagnosis infeksi pada sumsum tulang perlu dipikirkan bila dijumpai demam yang tidak jelas sumbernya, dijumpai anemia yang disertai leukositosis atau leucopenia (Koury dan Rhodes, 2012)
2.21.3 Anemia pada pemakaian obat-obat mielosupresif
Beberapa obat yang dapat menekan sumsum tulang. Obat ARV yang sering menyebabkan anemia adalah zidovudin. Anemia karena zidovudine memiliki gambaran morfologis makrositer. Pada pemakaian zidovudin juga sering dijumpai neutropenia.
2.22. Penatalaksanaan anemia penyakit kronik pada infeksi HIV
Sampai saat ini pendekatan terapi anemia pada HIV adalah koreksi terhadap penyakit yang mendasari.
2.22.1. Obat kombinasi antiretrovirus
Penelitian prospektif pada wanita dengan HIV dijumpai pemakaian cARV dalam 6 bulan memberikan dampakperbaikananemia (odds ratio [OR] = 1.45; P< 0.05) sedangkan pemakaian 12 bulan atau lebih berkaitan dengan efek protektif terhadap terjadinya anemia (OR = 0.71; P< 0.001) (Berhane K dkk 2004). Dilaporkan bahwa terputusnya pemakaian cARV memiliki risiko yang lebih tinggi terjadinya anemia atau perburukkan anemia. Pada penelitian tersebut dilaporkan juga bahwa anemia meningkatkan insiden terjadinya AIDS, kejadian
non-AIDS defining atau kematian (Mocroft dkk ., 2011)
2.22.2. Epoetin alfa
Epoetin alfa telah diketahui aman dan efektif untuk terapi anemia pada infeksi HIV. Dilaporkan pemberian epoetin alfa 100 – 200 U/kgBB 3 kali per minggu secara bermakna meningkatka kadar hematokrit pada pasien AIDS yang mendapat terapi zidovudine dengan kadar endogenous erythropoietin < 500 IU/L. peningkatan kadar hemoglobin > 1 g tampak setelah pemberian pada minggu 2, dengan dikuti peningkatan > 2 g pada minggu 4. Pemberian epoetin alfa juga secara bermakna berkaitan berkurangnya kebutuhan transfusi sehingga akan meningkatkan kualitas hidup (Volberding PA dkk., 2004)
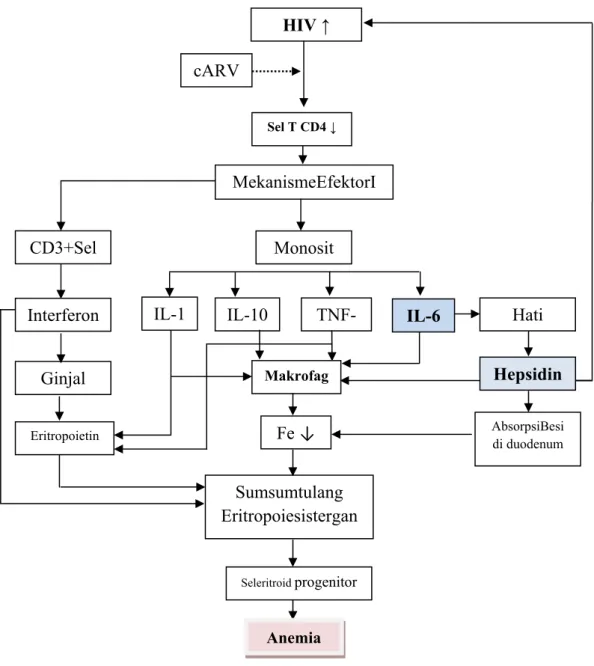
Gambar 2.8 Dugaan Mekanisme Anemia Penyakit Kronik Pada Infeksi HIV yang mendapat terapi kombinasi ARV
HIV ↑ cARV
Interferon IL-1 IL-10 TNF- IL-6
CD3+Sel Monosit MekanismeEfektorI Sel T CD4 ↓ Seleritroid progenitor Sumsumtulang Eritropoiesistergan Fe ↓ Makrofag Eritropoietin Ginjal AbsorpsiBesi di duodenum Hepsidin Hati Anemia