97
PENGARUH PEMBERIAN SIMETIDIN TERHADAP KADAR SGOT
DAN SGPT TIKUS PUTIH (
Rattus norvegicus
) YANG DIBERI
ANTI TUBERKULOSIS RIFAMPISIN DAN ISONIAZID
Eska Perdini1, Wahyu Siswandari, Fajar Wahyu Pribadi1
1
Fakultas Kedokteran dan Ilmu-Ilmu Kesehatan, Universitas Jenderal Soedirman, Purwokerto E-mail: fajar@unsoed.ac.id
ABSTRACT
Tuberkulosis (TB) has long been known as an infection diseases, and has been reported to increased. The INH dan Rifampisin are two different drugs that are known tobe the most active drugs, therefore both drugs are being used as never ending drugs in curing the TB. Utilization of both INH and rifampisin in a combination to cure the TB patients, however could increase the possibility of hepar lession risk. This research was aimed to firstly, knowing whether cimetidine could prevent increase of SGOT and SGPT levels of rats (Rattus norvegicus) given by both drugs INH and rifampisin, and secondly what was the minimum dose of cimetidine that able to prevent the increase of SGOT and SGPT levels. A Completely Random Design (CRD) was applied in this research, 24 male rats (Rattus norvegicus) of the wistar variety were divided into 4 different groups. The first group, was only given the INH and rifampisin orally at the doses of 50 mg/Kg body weight/day, the next groups groups II, III, and IV were also given those two drugs at the same dose, but the cimetidine was also given at 112,5 , 225, and 450 mg/Kg body weight/day for the 28 days. Consequently the SGOT and SGPT levels were measured twice pre and post treatments. The data obtained were analysied by the paired t test, a one way ANOVA, Post Hoc Tukey’s HSD, Kruskal-Wallis and Mann-Whitney test. This research result showed that the cimetidine that given following the INH and rifampisin could prevent the increase of SGOT and SGPT levels. The highest dose of 450 mg/Kg body weight/day that given orally showed highly significant different from other (p<0,00) in preventing the SGOT and SGPT of treated animals.
Key words: isoniazid, rifampisin, cimetidine, SGOT, SGPT
PENDAHULUAN
Penyakit infeksi merupakan salah satu
masalah kesehatan. Salah satu penyakit
infeksi
yang
masih
menjadi
masalah
kesehatan baik di Indonesia maupun di dunia
adalah Tuberkulosis (TB). Tuberkulosis
adalah
penyakit
infeksi
kronik
yang
disebabkan oleh kuman
Mycobacterium
tuberculosis
1.
Insidensi
penyakit
TB
saat
ini
meningkat di negara tertentu akibat dari
tingkat infeksi yang tinggi, penurunan daya
tahan tubuh karena kemiskinan atau penyakit
AIDS
(
Acquired
Immune
Deficiency
Syndrome
), dan peningkatan insidensi kasus
TB
resisten
2.
Lingkungan
hidup
dan
pemukiman yang padat di wilayah perkotaan
juga telah mempermudah proses penularan
TB dan berperan dalam peningkatan jumlah
kasus TB
1.
Tuberkulosis
merupakan
penyakit
infeksi pembunuh nomor satu di dunia. WHO
(
World Health Organization
) memperkirakan
sekitar 2 miliar orang menderita TB, dan 3
juta orang di dunia meninggal setiap
tahunnya karena TB
3. Di Indonesia, TB
merupakan
masalah
utama
kesehatan
masyarakat. Jumlah pasien TB di Indonesia
merupakan ke-3 terbanyak di dunia setelah
India dan Cina dengan jumlah pasien sekitar
10% dari total jumlah pasien TB di dunia.
Diperkirakan pada tahun 2004, setiap tahun
ada 539.000 kasus baru dan kematian
98
101.000 orang. Insidensi kasus TB BTA
positif sekitar 110 per 100.000 penduduk
4.
Jumlah kasus TB meningkat dan
banyak yang tidak berhasil disembuhkan,
terutama di negara yang dikelompokkan
dalam 22 negara dengan masalah TB besar
(high burden countries)
. Menyikapi hal
tersebut,
pada
tahun
1993,
WHO
mencanangkan TB sebagai kedaruratan dunia
(global emergency).
Awal tahun 1990-an
WHO dan IUATLD (
International Union
Against Tuberculosis and Lung Disease
)
telah
mengembangkan
strategi
penanggulangan TB yang dikenal sebagai
strategi DOTS
(Directly Observed Treatment
Short-course)
dan telah terbukti sebagai
strategi
penanggulangan
yang
secara
ekonomis paling efektif (
cost-efective)
4.
Pengobatan
TB
bertujuan
untuk
menyembuhkan
penyakit,
mencegah
kematian,
mencegah
kekambuhan,
memutuskan rantai penularan dan mencegah
terjadinya resistensi kuman terhadap Obat
Anti Tuberkulosis (OAT)
4. Obat lini pertama
yang digunakan untuk mengobati TB adalah
isoniazid,
rifampisin,
etambutol,
dan
pirazinamid untuk terapi awal, dengan
streptomisin
sebagai
terapi
alternatif
5.
Isoniazid (INH) dan rifampisin merupakan
dua obat yang paling aktif sehingga
digunakan sepanjang waktu pengobatan
6.
Penggunaan
kombinasi
isoniazid
dan
rifampisin pada pengobatan TB dapat
meningkatkan resiko kejadian kerusakan
hepar
7. Adapun insidensi hepatoksisitas lebih
tinggi pada penggunaan kombinasi isoniazid
dan
rifampisin
dibandingkan
dengan
penggunaan isoniazid saja
8.
Efek samping hepatotoksik pengobatan
TB dengan OAT dapat dihindari dengan
pemberian hepatoprotektor. Hepatoprotektor
adalah zat yang dapat melindungi hati dari
kerusakan akibat agen infeksius maupun zat
toksik. Zat yang bersifat hepatoprotektor
tersebut dapat berasal dari bahan kimia
maupun alamiah. Beberapa hepatoprotektor
yang telah terbukti secara eksperimental
antara lain adalah mengkudu (
Morinda
citrifolia
)
9, tanaman
Solanum trilobatum
10,
dan larva lalat rumah (
Musca domestica
)
11.
Saat ini sedang diteliti juga beberapa
obat
yang
diduga
mempunyai
sifat
hepatoprotektor, walaupun obat tersebut
penggunaanya untuk penyakit lain, misalnya
simetidin. Simetidin merupakan obat yang
tergolong antagonis reseptor H
2. Efek penting
dari
antagonis
reseptor
H
2adalah
menurunkan
sekresi
asam
lambung
12.
Simetidin juga dapat menghambat sistem
metabolisme obat oksidatif sitokrom P-450,
dan hal inilah yang memungkinkan simetidin
dapat berefek hepatoprotektor
8.
Penelitian ini dilakukan dengan tujuan
untuk membuktikan efek simetidin dalam
mencegah peningkatan kadar SGOT dan
SGPT tikus putih yang diberi obat anti
tuberkulosis rifampisin dan isoniazid. Hasil
penelitian ini diharapkan dapat menjadi
bahan masukan dan pertimbangan bagi
klinisi dalam terapi TB untuk mengurangi
efek samping obat anti tuberkulosis (OAT)
99
dan diharapkan dapat menjadi dasar untuk
penelitian lanjutan yang lebih mendalam.
METODE PENELITIAN
Penelitian ini menggunakan 24 ekor
tikus putih (
Rattus norvegicus
) jantan strain
Wistar.
Tikus
yang
digunakan
harus
memenuhi kriteria inklusi yaitu sehat, berusia
2-3 bulan dengan berat badan dalam kisaran
yang sama yaitu 150-200 gram, dan tidak
sedang mengidap suatu penyakit. Kriteria
eksklusinya yaitu tikus putih yang mati
selama penelitian berlangsung.
Metode penelitian yang digunakan
adalah metode eksperimental terhadap hewan
coba tikus putih (
Rattus norvegicus
) dengan
Rancangan Acak Lengkap (RAL) atau
Completely Randomized Design
(CRD).
Penelitian ini dilakukan selama 28 hari,
dengan menggunakan
pre test and post test
with control group design
. Penelitian ini
menggunakan 4 macam perlakuan terhadap
hewan coba. Masing-masing perlakuan
tersebut adalah sebagai berikut : Kelompok
perlakuan
I
(kontrol
negatif)
diberi
kombinasi rifampisin dosis 50 mg/KgBB/hari
dan isoniazid dosis 50 mg/KgBB/hari melalui
sonde lambung selama 28 hari; Kelompok
perlakuan II, diberi rifampisin dan isoniazid
masing-masing 50 mg/KgBB/hari, serta
simetidin dosis 112,5 mg/KgBB/hari melalui
sonde lambung selama 28 hari; Kelompok
perlakuan III, diberi rifampisin dan isoniazid
masing-masing 50 mg/KgBB/hari, serta
simetidin dosis 225 mg/KgBB/hari melalui
sonde lambung selama 28 hari; Kelompok
perlakuan IV, diberi rifampisin dan isoniazid
masing-masing 50 mg/KgBB/hari, serta
simetidin dosis 450 mg/KgBB/hari melalui
sonde lambung selama 28 hari.
Variabel bebas dalam penelitian adalah
dosis larutan simetidin, rifampisin, dan
isoniazid, sedangkan variabel terikat pada
penelitian adalah kadar SGOT dan SGPT.
Analisis univariat dilakukan terhadap
setiap variabel dari hasil penelitian yaitu
kadar SGOT dan SGPT. Analisis bivariat
dilakukan dengan uji t berpasangan untuk
data kadar SGOT dan SGPT
pre test
dan
post
test
pada kelompok I, kelompok II, kelompok
III, dan kelompok IV. Analisis multivariat
menggunakan
uji
One
way
ANOVA
dilanjutkan
post hoc
dengan
Tukey’s HSD
atau
Kruskall-Wallis
yang dilanjutkan dengan
uji
Mann-Whitney
(jika
data
tidak
terdistribusi secara normal).
HASIL DAN PEMBAHASAN
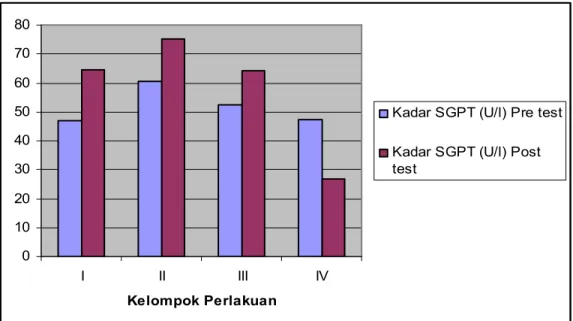
Perbandingan rerata kadar SGPT antara
pre test
dan
post test
dari tiap kelompok
perlakuan berserta hasil uji statistik tampak
pada Tabel 1 dan Gambar 1.
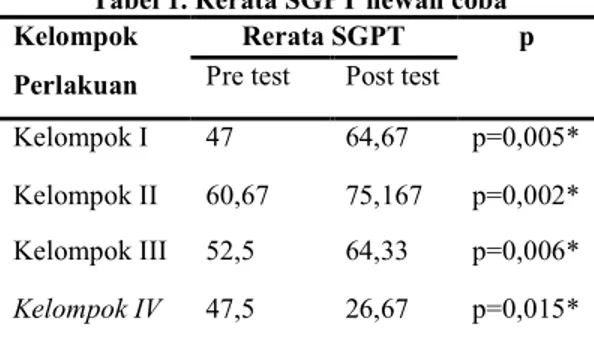
Tabel 1. Rerata SGPT hewan coba Kelompok
Perlakuan
Rerata SGPT p
Pre test Post test
Kelompok I 47 64,67 p=0,005* Kelompok II 60,67 75,167 p=0,002* Kelompok III 52,5 64,33 p=0,006* Kelompok IV 47,5 26,67 p=0,015* * hasil p pada uji t berpasangan
100
Dari data di atas dapat disimpulkan
bahwa bahwa INH dan rifampisin dengan
dosis masing-masing 50 mg/kgBB/hari dapat
menyebabkan kerusakan hepar tikus putih
(
Rattus norvegicus
) ditinjau dari peningkatan
kadar SGPT. Pemberian simetidin dengan
berbagai dosis menunjukkan hasil yang
bervariasi dalam mencegah kerusakan hepar
tikus putih (
Rattus norvegicus
) yang diberi
INH dan rifampisin 50 mg/kgBB/hari. Dosis
simetidin 112,5 mg/KgBB/hari dan 225
mg/KgBB/hari dapat mencegah kerusakan
hepar
dilihat
dari
lebih
rendahnya
peningkatan
kadar
SGPT
post
test
dibandingkan dengan kelompok kontrol
negatif (Kelompok I). Dosis simetidin 450
mg/KgBB/hari dapat mencegah kerusakan
hepar ditinjau dari penurunan kadar SGPT
post test
.
Analisis
data
dilanjutkan
untuk
mengetahui dosis simetidin yang paling
bermakna untuk mencegah kerusakan hepar
tikus putih (
Rattus norvegicus
) yang diberi
INH dan rifampisin 50 mg/kgBB/hari
ditinjau dari kadar SGPT. Uji normalitas data
untuk selisih kadar SGPT pre test dan post
test dengan uji
Shapiro-Wilk
menunjukkan
data berdistribusi normal. Uji homogenitas
varians menunjukkan nilai p = 0,039 (p<
0,05) sehingga dapat disimpulkan bahwa
paling tidak terdapat dua kelompok yang
mempunyai varians data yang berbeda secara
bermakna. Pada hasil uji
Kruskall-Wallis
diperoleh nilai p= 0,003 (p<0,05), hal ini
menunjukkan
setidaknya
terdapat
dua
kelompok yang berbeda bermakna.
Analisis data dilanjutkan dengan uji
Mann-Whitney
untuk
mengetahui
pada
kelompok manakah perbedaan bermakna
tersebut ada. Hasil menunjukkan bahwa dosis
simetidin 450 mg/kgBB/hari dapat mencegah
kerusakan hepar pada tikus putih (
Rattus
0 10 20 30 40 50 60 70 80 I II III IV Kelompok PerlakuanKadar SGPT (U/l) Pre test Kadar SGPT (U/l) Post test
101
norvegicus
) yang diberi INH dan rifampisin
50 mg/kgBB/hari ditinjau dari kadar SGPT.
Perbandingan rerata kadar SGOT
antara
pre test
dan
post test
dari tiap
kelompok perlakuan berserta hasil uji
statistik tampak pada Tabel dan Gambar 2.
Penelitian ini menunjukkan bahwa INH
dan rifampisin dengan dosis masing-masing
50
mg/kgBB/hari
dapat
menyebabkan
kerusakan
hepar
tikus
putih
(
Rattus
norvegicus
) ditinjau dari peningkatan kadar
SGOT
post test
. Pemberian simetidin dosis
112,5 mg/KgBB/hari belum dapat mencegah
kerusakan
hepar
tikus
putih
(
Rattus
norvegicus
) yang diberi INH dan rifampisin
50
mg/kgBB/hari,
ditandai
dengan
peningkatan SGOT
post test
yang lebih besar
dibandingkan kelompok I (kontrol negatif).
Pemberian simetidin dengan dosis 450
mg/KgBB/hari dapat mencegah kerusakan
hepar pada tikus putih (
Rattus novergicus
)
yang diberi INH dan rifampisin 50
mg/kgBB/hari, ditandai dengan penurunan
SGOT
post tets
secara bermakna.
Analisis data dilanjutkan dengan
One-Way ANOVA terhadap selisih kadar SGOT
pre test
dan
post test
untuk mengetahui dosis
simetidin yang paling bermakna dalam
mencegah kerusakan hepar tikus putih
(
Rattus novergicus
) yang diberi INH dan
rifampisin 50 mg/kgBB/hari ditinjau dari
kadar SGOT
.
Uji normalitas data untuk
selisih kadar SGPT
pre test
dan
post test
dengan uji
Shapiro-Wilk
menunjukkan data
Tabel 2. Rerata SGOT hewan coba Kelompok
Perlakuan
Rerata SGOT p
Pre test Post test
Kelompok I 74,67 93,83 p=0,005* Kelompok II 82,167 104,167 p=0,029* Kelompok III 65,33 62,67 p=0,660 Kelompok IV 73,5 46,83 p=0,000* * hasil p pada uji t berpasangan
0 20 40 60 80 100 120 I II III IV Kelompok Perlakuan
Kadar SGOT (U/l) Pre test Kadar SGOT (U/l) Post test
102
berdistribusi normal dan data memiliki
varians yang sama (p=0,066). Hasil uji
One-Way ANOVA menunjukkan bahwa p=0,000
dengan
demikian
setidaknya
terdapat
perbedaan selisih kadar SGOT
pre test
dan
post test
yang bermakna pada dua kelompok.
Analisis dilanjutkan dengan uji
Post
Hoc
dengan
Tukey’s
HSD
.
Hasil
menunjukkan bahwa dosis simetidin 450
mg/kgBB/hari dapat mencegah kerusakan
hepar pada tikus putih (
Rattus novergicus
)
yang diberi INH dan rifampisin 50
mg/kgBB/hari ditinjau dari kadar SGOT.
Penelitian ini menunjukkan pemberian
simetidin dengan dosis 112,5 mg/KgBB/hari
menyebabkan peningkatan kadar SGPT yang
lebih
rendah
dibandingkan
dengan
peningkatan kadar SGPT pada kelompok
kontrol negatif. Hasil ini sesuai dengan
penelitian sebelumnya yang dilakukan Kalra
et al.
8yang menyatakan bahwa simetidin
dapat mencegah kerusakan hepar yang
disebabkan INH dan rifampisin. Efek
pencegahan tersebut ditinjau dari kadar
SGPT dan SGOT. Efek pencegahan dari
simetidin ini terjadi karena simetidin dapat
menghambat sitokrom P-450
8. Sitokrom
P-450
merupakan
katalis
pada
proses
perubahan INH menjadi zat hepatotoksik,
yaitu perubahan
acetylhidrazyne
menjadi
a
cetyl radical
13. Acetyl radical ini merupakan
acylating agent
yang bersifat hepatotoksik
14.
Adanya penghambatan pada sitokrom P-450
ini menyebabkan terbentuknya acetyl radical
yang bersifat hepatotoksik juga menjadi
terhambat. Semakin banyak dosis simetidin
yang diberikan semakin besar penghambatan
yang terjadi. Hal ini terbukti dengan semakin
kecilnya peningkatan kadar SGPT pada
kelompok yang diberi simetidine dosis 225
mg/KgBB/hari, bahkan pada dosis 450
mg/KgBB/hari terjadi penurunan kadar
SGPT. Adanya penurunan kadar SGPT ini
dikarenakan
selain
efek
penghambatan
simetidin
terhadap
sitokrom
P-450,
kemungkinan terjadi perbaikan pada sel-sel
hepar yang mengalami kerusakan.
Kelompok kontrol negatif (kelompok I)
menunjukkan peningkatan kadar SGPT
paling tinggi dibandingkan kelompok lain.
Hasil
ini
sesuai
dengan
penelitian
sebelumnya yang dilakukan Rana et al.
15yang menyatakan bahwa kombinasi INH dan
rifampisin dengan dosis tersebut serta dengan
lama pemberian selama 28 hari, dapat
menimbulkan efek hepatotoksik pada tikus
putih strain Wistar. Pemberian INH dan
rifampisin dapat meningkatkan kadar SGOT
dan SGPT mencapai 3-4 kali lipat
8. INH
merupakan obat yang tergolong
metabolite
related
hepatotoxicity
,
yang
dapat
menimbulkan gangguan hepar melalui bahan
metabolitnya. Zat yang bersifat hepatotoksik
dari hasil metabolisme INH adalah acetyl
radical yang merupakan
acylating agent
14.
Pemberian kombinasi INH dan rifampisin
dapat meningkatkan toksisitas terhadap
hepar. Rifampisin meningkatkan toksisitas
INH melalui induksi sitokrom P-450 karena
acetylhidrazyne dari INH diubah menjadi
acetyl radical yang dikatalisis oleh sitokrom
P-450 menjadi zat hepatotoksik
13.
103
Hasil penelitian ini menunjukkan
bahwa simetidin dosis 112,5 mg/KgBB/hari
sudah dapat mencegah peningkatan yang
bermakna kadar SGPT, namun secara
statistik
dosis
simetidin
yang
paling
bermakna untuk mencegah kerusakan hepar
akibat pemberian INH dan rifampisin 50
mg/KgBB/hari adalah 450 mg/KgBB/hari.
Hal ini dapat dilihat dengan terjadinya
penurunan pada kadar SGPT.
Penelitian ini menunjukkan pemberian
simetidin dengan dosis 112,5 mg/KgBB/hari
menyebabkan peningkatan kadar SGOT yang
paling
tinggi
dibandingkan
kelompok
lainnya, bahkan kelompok kontrol negatif.
Penelitian sebelumnya menunjukkan bahwa
pemberian simetidin dosis 50 mg/KgBB/hari
menimbulkan peningkatan kadar SGOT yang
lebih rendah dibandingkan kelompok yang
hanya diberi INH dan Rifampisin 50
mg/KgBB/hari (kontrol negatif)
8. Hasil yang
berbeda ini dapat disebabkan karena SGOT
merupakan enzim yang banyak terdapat di sel
hati dan miokard serta dalam jumlah kecil di
muskuloskeletal, ginjal, pankreas, otak dan
eritrosit
16,17. Terdapatnya organ-organ lain
yang mengandung enzim ini menyebabkan
SGOT tidak spesifik untuk mendeteksi
adanya kerusakan hepar. Berbeda halnya
dengan SGPT yang merupakan penanda yang
lebih spesifik untuk mendeteksi adanya
kerusakan hepar
18, 19.
Hasil pemeriksaan kadar SGOT pada
kelompok yang diberi simetidin dosis 225
mg/KgBB/hari
dan
450
mg/KgBB/hari
menunjukkan adanya penurunan. Simetidin
dapat mencegah kerusakan hepar yang
disebabkan INH dan rifampisin. Semakin
tinggi dosis simetidin yang diberikan
semakin besar efek yang ditimbulkan, hal ini
ditandai dengan penurunan kadar SGOT
yang bermakna pada kelompok yang diberi
simetidin dosis 450 mg/KgBB/hari
8.
Kelompok kontrol negatif yang hanya
diberi INH dan rifampisin 50 mg/KgBB/hari
menunjukkan peningkatan kadar SGOT,
sebagaimana halnya yang terjadi pada kadar
SGPT. Hasil ini sesuai dengan penelitian
sebelumnya yang telah dilakukan Rana
et
al
.
15dan penelitian Kalra
et al
.
8INH
merupakan obat yang bersifat hepatotoksik
dikarenakan metabolitnya. Efek hepatotoksik
dari INH ini ditingkatkan oleh rifampisin
yang merupakan induksi sitokrom P-450
13.
Hasil penelitian ini menunjukkan
bahwa simetidin dosis 225 mg/KgBB/hari
sudah dapat menurunkan kadar SGOT,
namun secara statistik dosis simetidin yang
paling bermakna untuk mencegah kerusakan
hepar akibat pemberian INH dan rifampisin
50 mg/KgBB/hari adalah 450 mg/KgBB/hari.
Hal ini dapat dilihat dengan terjadinya
penurunan bermakna pada kadar SGOT.
KESIMPULAN
Pemberian simetidin dapat mencegah
peningkatan kadar SGOT dan SGPT tikus
putih (
Rattus
norvegicus
) yang diberi INH
dan
rifampisin.
Dosis
simetidin
450
mg/KgBB/hari
paling
bermakna
dalam
mencegah peningkatan kadar SGOT dan
104
SGPT tikus putih (
Rattus
norvegicus
) yang
diberi INH dan rifampisin.
DAFTAR PUSTAKA
1. Sudoyo, Aru W., Bambang S, Idrus A, Marcellus S, Siti S. 2006. Buku Ajar Ilmu Penyakit Dalam. Edisi IV. Jilid I. Departemen Ilmu Penyakit Dalam Fakultas Kedokteran Universitas Indonesia, Jakarta. 2. Dahlan, Zul. 1997. Diagnosis dan
Penatalaksanan Tuberkulosis. Cermin Dunia Kedokteran. No. 115. Hal 8.
3. Herchline, Thomas and Judith KA. 2007. Tuberculosis : Article. Emedicine. Section 2. 4. Depkes. 2007. Pedoman Nasional Penanggulangan Tuberkulosis, Edisi 2. Departemen Kesehatan Republik Indonesia, Jakarta.
5. Katzung, Bertram G. 2004. Farmakologi Dasar dan Klinik. Edisi VIII. Buku 3. Salemba Medika, Jakarta. Hal 93-98. 6. Chambers. 2001. Basic and Clinical
Pharmacology. 8thed. Lange Medical Books-McGraw-Hill, New York. pp 803-13
7. Palmer, Melissa. 2004. Medications and The Liver/Hepatitis : Article. Dr. Melissa Palmer's Guide of Hepatitis and Liver Disease.
8. Kalra, Bhupinder S, Sarita A, Nita K and Usha G. 2007. Effect of Cimetidine on Hepatotoxicity Induced by Isoniazid-Rifampicin Combination in Rabbits: Departements of Pharmacology, Biochemistry and Pathology, Maulana Azad Medical College New Delhi.
9. Sastrowardoyo, W dan SA Sudjarwo. 2004. Potensi Ekstrak Mengkudu (morinda citrifolia) Sebagai Hepatoprotektor pada Mencit yang Diberi Parasetamol. Jurnal Penelitian Medika Eksakta. Vol 5 No 2, 182-90.
10. Shahjahan, M, KE Sabitha, M Jainu, CS Devi, Syahmala. 2004. Effect of Solanum trilobatum Againts Carbon Tetrachloride Induced Hepatic Damage in Albino Rats. Indian Journal of Medical Research. 11. Wang, FR, H Ai, XM Chen, CL Lei. 2007.
Hepatoprotective Effetc of a Protein-Enriched Fraction from The Maggots (Musa domestica) Againts CCl4-Induced Hepatic Damage in Rats. Biotechnol Lett, 29 : 853-8. 12. Ganiswarna, S, Rianto S, Frans DS,
Purwantyastuti, dan Nafrialdi. 1995. Farmakologi dan Terapi, Edisi 4. Bagian Farmakologi Fakultas Kedokteran
Universitas Indonesia, Jakarta. 256-257; 599; 601 hal.
13. Chen, J dan K Raymond. 2006. Roles of Rifampicin in Drug-Drug Interaction : Underlying Molecular Mechanism Involving Nuclear Pregnane X Receptor. Annals of Clinical Microbiology and Antimicrobials. Vol 5. pp 3
14. Kasilo, OJ, and CFB Nhachi, M Dahlet, F Flesch, A Jaeger. 1992. Isoniazid : article. International Programme on Chemical Safety Poisons Information Monograph 288 Pharmaceutical
15. Rana, S, P Ravinder, V Kim, S Kartar. 2006. Effect of Different Oral Doses of Isoniazid-Rifampisin in Rats. Molecular and Cellular Biochemistry. Vol 289 : 39-47.
16. Hardjoeno, H. 2003. Interpretasi Hasil Tes Laboratorium Diagnostik Bagian dari Standar Pelayanan Medik. Lembaga Penerbitan Universitas Hasanudin, Makasar. Hal 271-273.
17. Baron, DN. 1990. Kapita Selekta Patologi Klinik. EGC, Jakarta. Hal 136; 212; 222. 18. Prihatni, D, Ida Parwati, Idaningroem Sjahid,
dan Coriejati Rita. 2005. Efek Hepatotoksik Anti Tuberkulosis Terhadap Kadar Aspartat Aminotransferase dan Alanine Aminotransferase Serum Penderita Tuberkulosis Paru. Indonesian Journal of Clinical Pathology and Medical Laboratory, Vol. 12, No. 1. Hal 2.
19. Arsyad, Zulkarnain. 1996. Evaluasi FaaI Hati pada Penderita Tuberkulosis Paru yang Mendapat Terapi Obat Anti Tuberkulosis. Cermin Dunia Kedokteran. No. 110. Hal 17.