SKRIPSI
MEMPELAJARI KARAKTERISTIK KIMIA DAN FISIK TEPUNG TAPIOKA DAN MOCAL (MODIFIED CASSAVA FLOUR) SEBAGAI
PENYALUT KACANG PADA PRODUK KACANG SALUT
Oleh:
ADIE MUHAMMAD RAHMAN F24103077
2007
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
Adie Muhammad Rahman. F24103077. Mempelajari Karakteristik Kimia Dan Fisik Tepung Tapioka Dan MOCAL (Modified Cassava Flour) Sebagai Penyalut Kacang Pada Produk Kacang Salut. Di bawah Bimbingan Ratih Dewanti-Hariyadi dan Feri Kusnandar. 2007.
Ringkasan
Tepung tapioka merupakan salah satu bahan baku dalam pembuatan penyalut pada produk kacang salut. Mutu kacang salut yang dihasilkan dapat dipengaruhi oleh sifat atau karakteritik tepung tapioka yang digunakan, namun belum ada penelitian yang memberikan informasi tentang sifat atau karakteristik tepung tapioka yang berkaitan dengan mutu kacang salut. Dalam penelitian ini, selain tepung tapioka juga digunakan MOCAL (Modified Cassava Flour). MOCAL merupakan produk turunan dari tepung singkong hasil pengembangan Laboratorium Kimia dan Biokimia Hasil Pertanian, Fakultas Teknologi Pertanian Universitas Jember (LAB KBHP-UNEJ).
Penelitian bertujuan untuk mempelajari karakteristik kimia dan fisik beberapa sampel tepung tapioka dan MOCAL, kemudian mengkorelasikan karakteritik tersebut dengan tingkat pengembangan papatan dan kerenyahan penyalut pada produk kacang salut. Kemudian menentukan karakteristik yang paling relevan terhadap kerenyahan penyalut serta menentukan sampel yang memberikan kerenyahan tertinggi terhadap penyalut pada produk kacang salut.
Penelitian ini dilakukan melalui beberapa tahapan. Tahap pertama yaitu analisis sifat kimia dan fisik, yang meliputi analisis kadar air, kadar abu, kadar pati, kadar amilosa, nilai pH, bentuk dan ukuran pati, kehalusan, derajat putih,swelling power dan kelarutan, serta sifat amilografi, kemudian juga dilakukan analisis tingkat pengembanganpapatan
tepung tapioka (tapioka A, B, C, D, E, dan F) serta MOCAL. Tahap berikutnya yaitu aplikasi tepung tapioka dan MOCAL sebagai penyalut pada produk kacang salut. Selanjutnya dilakukan analisis tekstur (kerenyahan) pada semua produk kacang salut yang dihasilkan dari tiap sampel dan mengkorelasikan sifat kimia dan fisik dari sampel yang relevan terhadap kerenyahan penyalut pada kacang salut tersebut.
Hasil analisis menunjukkan karakteristik kimia dan fisik yang berbeda antar sampel tepung tapioka, begitu pula dengan MOCAL. Berdasarkan hasil analisis korelasi, karakteristik yang paling relevan terhadap tingkat pengembangan papatan dan kerenyahan penyalut pada kacang salut adalah rasio amilosa dan amilopektin. Sementara itu, karakteristik lainnya seperti kadar air, kadar abu, kadar pati, nilai pH, bentuk dan ukuran pati, kehalusan, derajat putih,swelling power dan kelarutan, serta sifat amilografi tidak terlalu berpengaruh terhadap tingkat pengembangan papatan dan kerenyahan penyalut pada produk kacang salut.
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
MEMPELAJARI KARAKTERISTIK KIMIA DAN FISIK TEPUNG TAPIOKA DAN MOCAL (MODIFIED CASSAVA FLOUR) SEBAGAI
PENYALUT KACANG PADA PRODUK KACANG SALUT
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Ilmu dan Teknologi Pangan Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh:
ADIE MUHAMMAD RAHMAN F24103077
Dilahirkan pada tanggal 5 Desember 1985 di Jakarta
Tanggal Lulus: 30 November 2007
Menyetujui, Bogor, Januari 2008
Dr.Ir. Ratih Dewanti-Hariyadi, MSc Dr.Ir. Feri Kusnandar, Msc Rahadi Kusuma, STP
Dosen Pembimbing I Dosen Pembimbing II Pembimbing Lapang
Mengetahui,
Dr. Ir. Dahrul Syah, MSc.
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 5 Desember 1985 sebagai anak ke lima dari delapan bersaudara pasangan Salamah dan Sunaryo. Penulis mengawali masa pendidikannya pada tahun 1991 di Sekolah Dasar Negeri Karet 05 Pagi Jakarta hingga tahun 1997. Kemudian penulis melanjutkan pendidikan menengah pertama di SLTP Negeri 58 Jakarta hingga tahun 2000, dan melanjutkan pendidikan menengah atas di SMU Negeri 3 Jakarta hingga tahun 2003. Pada tahun yang sama, penulis diterima sebagai mahasiswa Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, Institut Pertanian Bogor melalui jalur USMI.
Selama masa kuliah, penulis aktif di berbagai kegiatan dan organisasi kemahasiswaan, diantaranya adalah menjadi pengurus Himpunan Mahasiswa Ilmu dan Teknologi Pangan (HIMITEPA) serta kepanitiaan lainnya seperti Masa Perkenalan Departemen Ilmu dan Teknologi Pangan (BAUR 2004), Pelatihan Web dan Graphic Design HIMITEPA, dan MC dalam acara Focus Group Discussion ”Formalin: Kebutuhan Yang Tidak Dibutuhkan” HIMITEPA. Penulis juga pernah menjadi asisten Praktikum Kimia Dasar TPB-IPB pada tahun 2005 dan 2006.
KATA PENGANTAR
Alhamdulillaahirabbil’alamin, segala puji bagi Allah SWT yang telah memberikan karunia-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul Mempelajari Karakteristik Kimia Dan Fisik Tepung Tapioka Dan Mocal (Modified Cassava Flour) Sebagai Penyalut Kacang Pada Produk Kacang Salut, sebagai tugas akhir untuk mendapatkan gelar Sarjana Teknologi Pertanian pada Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, Insitut Pertanian Bogor.
Selama melaksanakan penelitian dan penyelesaian skripsi ini penulis telah mendapatkan banyak bantuan dari berbagai pihak. Oleh karena itu penulis mengucapkan terima kasih sebesar-besarnya kepada :
1. Ayah dan Mama tercinta, Kak’Wi, Ka’Na, Bang’De, Ima, Lely, Ita dan Ois, Abank, ka’Dety, serta Adinda, Nuha, Aulia, Ayu, Delila dan Zaky, yang senantiasa memberikan kasih sayang dan cinta kepada penulis untuk terus berjuang dan bersemangat!!!
2. Dr. Ir. Ratih Dewanti-hariyadi, Msc., selaku dosen pembimbing pertama yang banyak memberikan arahan dan bimbingannya kepada penulis.
3. Dr. Ir. Feri Kusnandar, Msc., selaku dosen pembimbing kedua yang juga banyak memberikan arahan dan bimbingannya kepada penulis.
4. Ir. Betty Silalahi selaku general manager yang telah mengizinkan penulis untuk melaksanakan tugas akhir di Perusahan pengolahan kacang.
5. Mba Vivi dan Mas Rahadi selaku pembimbing lapang yang telah memberikan arahan dan bimbingan kepada penulis.You are the best!
6. Wati, Maya, dan Reza, selaku teman seperjuangan penulis selama menyelesaikan tugas akhir. Thank you so much for all the moments that we share!!!
8. Sahabat-sahabat terbaik penulis, Mitoel, Chusni, Indah, Fitri, Tylo, Arie, Pa’de, Ujo, RT, Arga, Sarwo, Ados, Yoga, Lichan, dan Oneth. You guys are like a star..Not aways seen but always there..
9. Irmawati, terima kasih untuk semangatnya!Be strong and tough girl!!!
10. Teman-teman ITP 40, Jeng’ye, Lasty, Tatan, Ade, Aca, Widhi, Iin, Vina, Nooy, Nana, Ina, Dion, Agnes, Gadink, hendy, Aan, Dhea, Rahmat, dan yang lainnya, serta teman-teman ITP 41 yang telah banyak memberikan bantuan dan semangat kepada penulis.
11. Teknisi dan laboran, pak Iyas, bu Rub, pak Koko, teh Ida, mba Ari, pak Rojak, pak Wahid, serta pak Sobirin.
12. Semua pihak yang telah membantu penulis baik secara langsung maupun tidak langsung yang tidak dapat penulis sebutkan satu per satu.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna. Oleh karena itu, pemulis mengharapkan kritik dan saran membangun untuk memperbaiki dan menyempurnakan penulisan skripsi ini selanjutnya.
Akhir kata, penulis berharap skripsi ini dapat benrmanfaat bagi semua pihak yang membutuhkan dan bagi pengembangan ilmu dan penerapan pembelajaran khususnya bagi Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Bogor, Januari 2007
DAFTAR ISI
Halaman
RINGKASAN... i
RIWAYAT HIDUP... iv
KATA PENGANTAR ... v
DAFTAR ISI ... vii
DAFTAR TABEL ... x
DAFTAR GAMBAR... xi
DAFTAR LAMPIRAN... xii
I. PENDAHULUAN A. LATAR BELAKANG ... 1
B. TUJUAN ... 2
II. TINJAUAN PUSTAKA A. TEPUNG TAPIOKA... 3
B. TEPUNG SINGKONG... 6
C. MOCAL... 7
D. PATI... 9
1. Granula Pati... 9
2. Amilosa dan Amilopektin... 10
3. Daya Kembang Pati (Swelling Power) dan Kelarutan... 12
4. Gelatinisasi Pati... 13
5. Retrogradasi Pati... 15
E. KACANG SALUT... 16
F. ANALISIS KORELASI... 17
III. BAHAN DAN METODE A. BAHAN DAN ALAT ... 19
B. METODE PENELITIAN ... 19
2. Analisis Tingkat Pengembangan Papatan... 20
3. Analisis Kerenyahan Produk Kacang Salut... 22
C. METODE ANALISIS... 23
1. Kadar Air... 23
2. Kadar Abu... 23
3. Kadar Pati... 24
4. Kadar Amilosa dan Amilopektin... 25
5. Nilai pH... 27
6. Bentuk dan Ukuran Pati... 27
7. Kehalusan... 27
8. Derajat Putih... 28
9. Daya Kembang Pati (Swelling Power) dan Kelarutan... 29
10. Pola Gelatinisasi... 30
11. Analisis Tekstur... 30
12. Uji Organoleptik... 31
13. Analisis Korelasi... 31
IV. HASIL DAN PEMBAHASAN A. SIFAT KIMIA TEPUNG TAPIOKA... 33
1. Kadar Air... 33
2. Kadar Abu... 33
3. Nilai pH... 34
4. Kadar Pati... 35
5. Kadar Amilosa dan Amilopektin... 37
B. SIFAT FISIK TEPUNG TAPIOKA... 38
1. Bentuk dan Ukuran Pati... 38
2. Kehalusan... 39
3. Derajat Putih... 40
4. Daya Kembang Pati (Swelling Power) dan Kelarutan... 41
5. Pola Gelatinisasi... 44
C. ANALISIS TINGKAT PENGEMBANGAN PAPATAN... 50
E. KARAKTERISTIK TAPIOKA F YANG MENGHASILKAN
KERENYAHAN PENYALUT TERTINGGI... 55 F. MOCAL (MODIFIED CASSAVA FLUOR)... 58
V. KESIMPULAN DAN SARAN
A. KESIMPULAN... 63 B. SARAN... 65
DAFTAR TABEL
Halaman
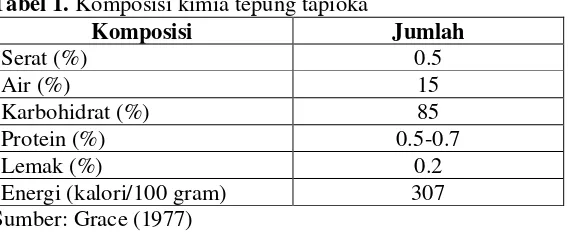
Tabel 1. Komposisi kimia tepung tapioka... 3
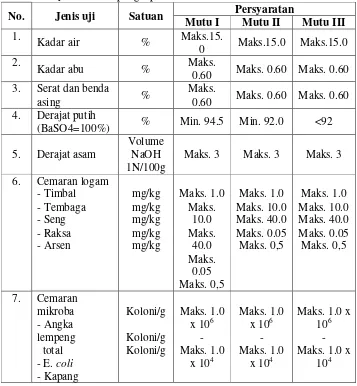
Tabel 2. Syarat mutu tepung tapioka menurut SNI 01-3451-1994... 4
Tabel 3. Standar kehalusan tepung tapioka... 4
Tabel 4. Syarat mutu tepung singkong menurut SNI 01-2997-1992... 6
Tabel 5. Spesifikasi MOCAL yang diproduksi oleh Koperasi Loh Jinawi Trenggalek... 8
Tabel 6. Syarat mutu edible cassava four dalam CODEX STAN 176-1989 (Rev.1–1995)... 9
Tabel 7. Penilaian mutu sensoris kacang salut... 31
Tabel 8. Kadar air sampel... 33
Tabel 9. Kadar abu sampel... 34
Tabel 10. Nilai pH sampel... 35
Tabel 11. Kadar pati sampel... 36
Tabel 12. Kadar amilosa dan amilopektin sampel... 37
Tabel 13. Ukuran granula sampel... 38
Tabel 14. Hasil pengukuran kehalusan sampel... 40
Tabel 15. Derajat putih sampel... 41
Tabel 16. Sifat amilografi sampel... 45
Tabel 17. Tingkat pengembanganpapatan sampel... 51
Tabel 18. Hasil pengukuran gaya (gf) dan jarak (mm), serta skor kerenyahan sampel penyalut pada produk kacang salut... 53
Tabel 19. Rekapitulasi data karakteristik kimia dan fisik tapioka F... 57
Tabel 20. Sifat kimia dan fisik MOCAL... 59
DAFTAR GAMBAR
Halaman
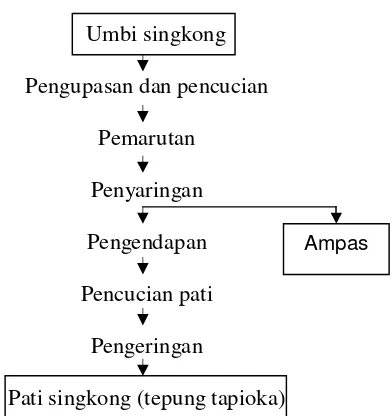
Gambar 1. Diagram alir pembuatan tepung tapioka... 5
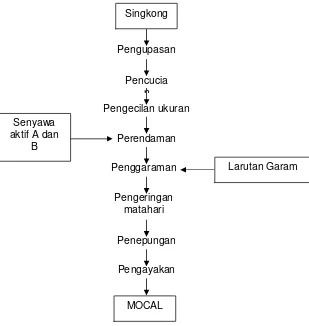
Gambar 2. Diagram alir pembuatan MOCAL... 8
Gambar 3. Struktur amilosa... 11
Gambar 4. Struktur amilopektin... 11
Gambar 5. Grafik hubungan antara gaya (force)dan jarak (distance)... 17
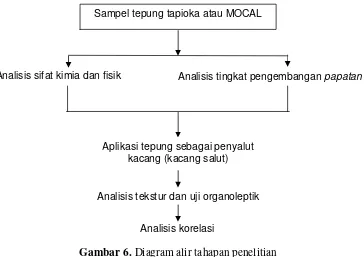
Gambar 6. Diagram alir tahapan penelitian... 20
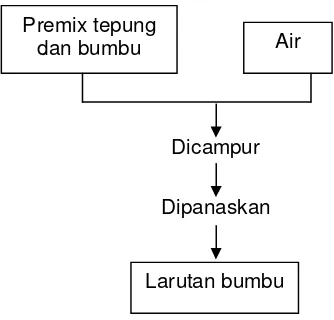
Gambar 7. Diagram alir pembuatan larutan bumbu... 21
Gambar 8. Diagram alir pembuatanpapatan... 21
Gambar 9. Diagram alir pembuatan kacang salut... 22
Gambar 10. Granula Pati Tepung Tapioka (A, B, C, D, E, dan F)... 39
Gambar 11. Polaswelling power tepung tapioka ... 42
Gambar 12. Pola kelarutan tepung tapioka... 43
Gambar 13. Grafik pola gelatinisasi tepung tapioka... 46
Gambar 14. Korelasi antara tingkat pengembanganpapatan dengan rasio amilosa dan amilopektin... 51
Gambar 15. Korelasi antara skor kerenyahan dengan rasio amilosa dan amilopektin... 54
DAFTAR LAMPIRAN
Halaman Lampiran 1. Rekapitulasi karakteristik fisikokimia sampel
tepung tapioka dan MOCAL... 69
Lampiran 2. Hasil pengukuran kadar pati... 70
Lmapiran 3. Pembuatan kurva standar amilosa dan pengukuran kadar Amilosa... 71
Lampiran 4. Hasil uji rating kerenyahan... 72
Lampiran 5a. Hasil uji Duncan : kadar air, kadar abu, pH... 73
Lampiran 5b. Hasil uji Duncan : kadar pati, kadar amilosa, dan derajat Putih... 74
Lampiran 5c. Hasil uji Duncan : kehalusan... 75
Lampiran 6a. Hasil uji Duncan terhadap kerenyahan (gf)... 76
Lampiran 6b. Hasil uji Duncan terhadap skor kerenyahan... 77
Lampiran 7a. Hasil analisis korelasi : Amilosa terhadapswelling power dan kelarutan pati... 78
Lampiran 7b. Hasil analisis korelasi : Amilosa terhadap sifat amilografi ... 78
Lampiran 7c. Hasil analisis korelasi : tingkat pengembanganpapatan terhadap rasio amilosa dan amilopektin... 79
Lampiran 7d. Hasil analisis korelasi : tingkat pengembanganpapatan terhadapswelling powerdan kelarutan... 79
Lampiran 7e. Hasil analisis korelasi : tingkat pengembanganpapatan terhadap pH... 79
Lampiran 7f. Hasil analisis korelasi : tingkat pengembanganpapatan terhadap sifat amilografi... 80
Lampiran 7g. Hasil analisis korelasi : kerenyahan terhadap rasio amilosa dan amilopektin... 80
Lampiran 7j. Hasil analisis korelasi : kerenyahan terhadap sifat
amilografi... 81 Lampiran 7k. Hasil analisis korelasi : tingkat pengembanganpapatan,
I. PENDAHULUAN
A. LATAR BELAKANG
Tepung tapioka merupakan salah satu produk hasil olahan singkong yang banyak digunakan sebagai bahan baku utama maupun bahan penolong dalam beberapa produk pangan baik di rumah tangga maupun industri. Salah satu penggunaan tepung tapioka dalam industri pangan adalah sebagai penyalut pada produk kacang salut. Penyalut pada produk tersebut diharapkan memiliki tingkat pengembangan dan kerenyahan yang baik, namun dalam aplikasinya penggunaan jenis tepung tapioka yang berbeda akan menghasilkan mutu penyalut yang berbeda pula. Perbedaan mutu produk kacang salut yang dihasilkan dapat dipengaruhi oleh sifat atau karakteritik tepung tapioka yang digunakan, namun belum ada penelitian yang memberikan informasi tentang sifat atau karakteristik tepung tapioka yang diperlukan bagi suatu penyalut kacang.
Menurut Radley (1976), fungsionalitas pati pada produk pangan ataupun nonpangan tergantung dari sifat fisik pati. Sifat fisik pati tersebut dipengaruhi oleh dua komponen utama dalam pati yaitu amilosa dan amilopektin. Menurut Matz (1992), tingkat pengembangan dan tekstur dari makanan ringan (snack) dipengaruhi oleh rasio dari amilosa dan amilopektin. Menurut Balagopalan et al. (1988), tekstur pada produk berbahan dasar pati diperoleh dari hasil perubahan pati selama dan setelah pemasakan. Beberapa faktor yang mempengaruhi tekstur produk antara lain gelatinisasi, daya kembang, viskositas, dan retrogradasi. Faktor pH pada pati juga dapat mempengaruhi mutu produk berbahan dasar pati. Menurut Taggart (2004), asam dapat mengganggu ikatan hidrogen yang terdapat dalam pati, sehingga menyebabkan granula pati lebih mudah untuk mengembang.
produk kacang salut. Berdasarkan hasil uji coba oleh Subagio (2006), MOCAL dapat digunakan sebagai bahan baku dari berbagai jenis produk pangan, mulai dari produk rerotian, biskuit, b aha n p e nsu b t it u s i p ad a mie, hingga p r o d u k pangan semi basah. MOCAL mempunyai spektrum aplikasi yang mirip dengan tepung terigu, tepung beras, dan tepung-tepung lainnya, maka MOCAL mempunyai potensi untuk digunakan dalam penelitian ini.
B. TUJUAN
Penelitian ini dilakukan dengan tujuan sebagai berikut:
1. Mempelajari karakteristik kimia dan fisik beberapa sampel tepung tapioka dan MOCAL.
2. Mempelajari korelasi antara karakteristik kimia dan fisik sampel tersebut dengan tingkat pengembangan papatan dan kerenyahan penyalut pada produk kacang salut.
3. Menentukan karakteristik yang paling relevan terhadap kerenyahan penyalut pada produk kacang salut.
II. TINJAUAN PUSTAKA
A. TEPUNG TAPIOKA
Tepung tapioka merupakan pati yang diekstrak dari singkong. Dalam memperoleh pati dari singkong (tepung tapioka) harus dipertimbangkan usia atau kematangan dari tanaman singkong. Usia optimum yang telah ditemukan dari hasil percobaan terhadap salah satu varietas singkong yang berasal dari jawa yaitu San Pedro Preto adalah sekitar 18-20 bulan (Grace, 1977). Ketika umbi singkong dibiarkan di tanah, jumlah pati akan meningkat sampai pada titik tertentu, lalu umbi akan mejadi keras dan menyerupai kayu, sehingga umbi akan sulit untuk ditangani ataupun diolah. Komposisi kimia tepung tapioka dapat dilihat pada Tabel 1.
Tabel 1. Komposisi kimia tepung tapioka
Komposisi Jumlah
Serat (%) 0.5
Air (%) 15
Karbohidrat (%) 85
Protein (%) 0.5-0.7
Lemak (%) 0.2
Energi (kalori/100 gram) 307 Sumber: Grace (1977)
Tabel 2. Syarat mutu tepung tapioka menurut SNI 01-3451-1994
Persyaratan
No. Jenis uji Satuan
Mutu I Mutu II Mutu III
1.
Kadar air % Maks.15.
0 Maks.15.0 Maks.15.0 2.
Kadar abu % Maks.
0.60 Maks. 0.60 Maks. 0.60 3. Serat dan benda
asing %
Maks.
0.60 Maks. 0.60 Maks. 0.60 4. Derajat putih
Tabel 3. Standar kehalusan tepung tapioka Grade % Lolos ayak Ukuran
ayakan
A 99 140
B 99 80
C 95 60
Sumber : Radley (1976)
Tepung tapioka dibuat dengan mengekstrak bagian umbi singkong. Proses ekstraksi umbi kayu relatif mudah, karena kandungan protein dan lemaknya yang rendah. Jika proses pembuatannya dilakukan dengan baik, pati yang dihasilkan akan berwarna putih bersih (Moorthy, 2004). Berdasarkan derajat keputihan, maka semakin putih tepung tapioka mutunya juga semakin baik. Hal ini terdapat di dalam SNI 01-3451-1994 yang membagi tepung tapioka menjadi tiga kelas berdasarkan derajat keputihan, seperti tercantum pada Tabel 2 di atas.
Pada pembuatan produk pangan juga demikian, tepung tapioka yang lebih putih biasanya lebih diharapkan sebagai bahan baku. Contohnya pada produk kacang salut, penyalut pada produk diharapkan dapat menghasilkan warna putih yang baik (tidak kusam), sehingga produk lebih dapat diterima oleh konsumen dari segi organoleptik.
Umbi singkong
Pengupasan dan pencucian
Pemarutan
Penyaringan
Pengendapan
Pencucian pati
Pengeringan
Pati singkong (tepung tapioka)
Gambar 1. Diagram alir pembuatan tepung tapioka (Holleman dan Aten, 1956)
B. TEPUNG SINGKONG
Ubi kayu atau singko ng merupakan sumber karbohidrat yang penting setelah padi, jagung, dan sagu. Singkong memiliki nama botani Manihot esculentaCrantz tapi lebih dikenal dengan namaManihot utilissima. Singkong dapat dimanfaatkan secara langsung sebagai bahan pangan pokok ataupun diolah menjadi produk setengah jadi berupa pati singkong (tepung tapioka), gaplek, dan tepung singkong.
Menurut SNI 01-2997-1992, tepung singkong adalah tepung yang dibuat dari bagian umbi singkong yang dapat dimakan, melalui penepungan singkong iris, parut, ataupun bubur kering dengan mengindahkan ketentuan-ketentuan kebersihan. Syarat mutu tepung singkong sesuai SNI dapat dilihat pada Tabel 4.
Tabel 4. Syarat mutu tepung singkong menurut SNI 01-2997-1992
No. Jenis uji Satuan Persyaratan
1. Keadaan
10. Bahan Tambahan Pangan
Sesuai SNI 01-0222-1995 11. Cemaran logam
- Timbal 12. Cemaran mikroba
- Angka lempeng
Tepung singkong telah banyak digunakan dalam pembuatan produk-produk pangan, antara lain seperti roti, biskuit, mie instan, dan lain-lain. Tepung singkong dapat dimodifikasi untuk memperoleh mutu produk yang lebih baik dan sesuai dengan keinginan. Modifikasi tepung singkong telah dilakukan oleh peneliti terdahulu seperti Muharram (1992), yang memodifikasi tepung singkong dengan pengukusan, penyangraian, dan penambahan GMS (Glyceril Mono Stearat).
C. MOCAL
MOCAL atau Modified Cassava Flour merupakan produk turunan dari tepung singkong yang menggunakan prinsip modifikasi sel singkong secara fermentasi (Subagio, 2006). Secara teknis, cara pengolahan MOCAL sangat sederhana, mirip dengan cara pengolahan tepung singkong biasa, namun disertai dengan proses fermentasi. Singkong dibuang kulitnya, dikerok lendirnya, dan dicuci sampai bersih. Kemudian dilakukan pengecilan ukuran singkong dilanjutkan dengan tahap fermentasi selama 12-72 jam. Setelah fermentasi, singkong tersebut dikeringkan kemudian ditepungkan sehingga dihasilkan produk MOCAL (Gambar 2).
Gambar 2. Diagram alir pembuatan MOCAL
Tabel 5. Spesifikasi MOCAL yang diproduksi oleh Koperasi Loh Jinawi Trenggalek
No. Parameter Satuan Hasil
1. Keadaan
MOCAL merupakan produk hasil olahan dari singkong yang dapat dimakan (edible cassava). Oleh karena itu, syarat mutu MOCAL dapat mengacu kepada CODEX STAN 176-1989 (Rev.1–1995) tentang edible cassava flour (Tabel 6)
Tabel 6. Syarat mutu edible cassava four dalam CODEX STAN 176-1989 (Rev.1–1995)
No. Jenis Uji Satuan Persyaratan Mutu
1. Kadar air % Max. 13
2. Kadar abu % Max. 3
3. Kadar Serat Kasar % Max. 2
4. Kadar HCN mg/kg Max. 10
5. Residu pestisida - Sesuai dengan aturan yang berlaku 6. Logam berat - Tidak terdeteksi
7. Bahan Tambahan - Tidak terdeteksi
MOCAL mempunyai karakteristik yang khas, sangat berbeda dengan tepung singkong dan tepung tapioka. Dibandingkan dengan tepung tapioka, viskositas MOCAL lebih rendah. Hal ini disebabkan o l e h komponen pati t e p u n g tapioka mencakup hampir seluruh bahan kering, sedangkan pada MOCAL komponen selain pati masih dalam jumlah yang signifikan. Namun demikian, dengan fermentasi s e l a m a 72 jam akan didapatkan produk MOCAL yang mempunyai viskositas mendekati t ep u n g tapioka (data tidak ditunjukkan). Hal ini dapat dipahami bahwa semakin lama waktu fermentasi maka akan semakin banyak sel singkong yang pecah, sehingga pembebasan granula pati menjadi semakin meningkat (Subagio, 2007).
D. PATI
1. Granula Pati
Granula pati mempunyai bentuk dan ukuran yang berbeda-beda tergantung dari sumbernya. Menurut Moorthy (2004), ukuran granula tapioka menunjukan variasi yang besar yaitu sekitar 5-40 µm dengan bentuk bulat dan oval. Variasi tersebut dipengaruhi oleh varietas tanaman singkong dan periode pertumbuhan pada musim yang berbeda.
2. Amilosa dan Amilopektin
Granula pati terdiri dari dua fraksi yang dapat dipisahkan dengan air panas. Fraksi terlarut disebut amilosa dan fraksi yang tidak terlarut disebut amilopektin (Winarno, 2002). Pola difraksi sinar-x granula pati adalah bukti bahwa terdapat daerah kristalinitas atau misela pada granula pati (Swinkels, 1985). Misela merupakan bagian molekul linier yang berikatan dengan rantai molekul terluar molekul cabang (Pomeranz, 1991). Ikatan ini terjadi apabila bagian-bagian linier molekul pati berada paralel satu sama lain, sehingga gaya ikatan hidrogen akan menarik rantai ini bersatu (Swinkels, 1985). Di antara misela terdapat daerah yang renggang atau amorf (Pomeranz, 1991). Daerah amorf ini kurang padat, sehingga mudah dimasuki air. Pada pati kentang dan tapioka, misela terbentuk oleh amilopektin, sedangkan daerah amorf dibentuk oleh amilosa.
Amilosa merupakan rantai lurus yang terdiri dari molekul-molekul glukosa yang berikatan -(1,4)-D-glukosa. Panjang polimer dipengaruhi oleh sumber pati dan akan mempengaruhi berat molekul amilosa. Pada umumnya amilosa dari umbi-umbian mempunyai berat molekul yang lebih besar dibandingkan dengan berat molekul amilosa serealia, dengan rantai polimer lebih panjang daripada rantai polimer amilosa serealia (Moorthy, 2004)
Gambar 3. Struktur amilosa (Chaplin, 2006)
Jumlah atau kadar amilosa pati pada singkong berada pada kisaran 20-27% mirip dengan pati tanaman lain. Pada dasarnya, struktur amilopektin sama seperti amilosa, yaitu terdiri dari rantai pendek -(1,4)-D-glukosa dalam jumlah yang besar. Perbedaannya ada pada tingkat percabangan yang tinggi dengan ikatan -(1,6)-D-glukosa dan bobot molekul yang besar. Amilopektin juga dapat membentuk kristal, tetapi tidak sereaktif amilosa. Hal ini terjadi karena adanya rantai percabangan yang menghalangi terbentuknya kristal (Taggart, 2004). Struktur amilopektin dapat dilihat pada Gambar 4.
3. Daya Kembang Pati (swelling power) dan Kelarutan
Daya kembang pati atau swelling power didefinisikan sebagai pertambahan volume dan berat maksimum yang dialami pati dalam air (Balagopalan et al., 1988). Swelling power dan kelarutan terjadi karena adanya ikatan non-kovalen antara molekul-molekul pati. Bila pati dimasukkan ke dalam air dingin, granula pati akan menyerap air dan membengkak. Namun demikian, jumlah air yang terserap dan pembengkakannya terbatas hanya mencapai 30% (Winarno, 2002). Ketika granula pati dipanaskan dalam air, granula pati mulai mengembang (swelling). Swelling terjadi pada daerah amorf granula pati. Ikatan hidrogen yang lemah antar molekul pati pada daerah amorf akan terputus saat pemanasan, sehingga terjadi hidrasi air oleh granula pati. Granula pati akan terus mengembang, sehingga viskositas meningkat hingga volume hidrasi maksimum yang dapat dicapai oleh granula pati (Swinkels, 1985). Faktor-faktor seperti rasio amilosa-amilopektin, distribusi berat molekul dan panjang rantai, serta derajat percabangan dan konformasinya menentukan swelling power dan kelarutan (Moorthy, 2004). Swelling merupakan sifat yang dipengaruhi oleh amilopektin (Li dan Yeh, 2001). Proporsi yang tinggi pada rantai cabang amilopektin memiliki kontribusi dalam peningkatan nilaiswelling.Selain itu, terdapat korelasi yang negatif antara swelling power dengan kadar amilosa, swelling power menurun seiring dengan peningkatan kadar amilosa (Sasaki dan Matsuki, 1998 dalam Li dan Yeh, 2001). Amilosa dapat membentuk kompleks dengan lipida pada pati sehingga dapat menghambat swelling (Charles et al., 2005).
membuat suspensi pati dalam botol sentrifusa lalu dipanaskan selama 30 menit pada suhu yang telah ditentukan. Kemudian bagian yang cair (supernatan) dipisahkan dari endapan. Swelling power diukur sebagai berat pati yang mengembang (endapan) per berat pati kering. Tepung tapioka memilikiswelling power yang besar (Balagopalan et al., 1988).
Ketika pati dipanaskan dalam air, sebagian molekul amilosa akan keluar dari granula pati dan larut dalam air. Persentase pati yang larut dalam air ini dapat diukur dengan mengeringkan supernatan yang dihasilkan saat pengukuranswelling power. Menurut Fleche (1985), ketika molekul pati sudah benar-benar terhidrasi, molekul-molekulnya mulai menyebar ke media yang ada di luarnya dan yang pertama keluar adalah molekul-molekul amilosa yang memiliki rantai pendek. Semakin tinggi suhu maka semakin banyak molekul pati yang akan keluar dari granula pati. Selama pemanasan akan terjadi pemecahan granula pati, sehingga pati dengan kadar amilosa lebih tinggi, granulanya akan lebih banyak mengeluarkan amilosa.
Menurut Pomeranz (1991), kelarutan pati semakin tinggi dengan meningkatnya suhu, serta kecepatan peningkatan kelarutan adalah khas untuk tiap pati. Pola kelarutan pati dapat diketahui dengan cara mengukur berat supernatan yang telah dikeringkan dari hasil pengukuran swelling power. Solubilitas atau kelarutan pati tapioka lebih besar dibandingkan pati dari umbi-umbi yang lain.
4. Gelatinisasi Pati
pati menjadi irreversible (tidak dapat kembali). Kondisi pembengkakan granula pati yang bersifat irreversible ini disebut dengan gelatinisasi, sedangkan suhu terjadinya peristiwa ini disebut dengan suhu gelatinisasi. Menurut Winarno (2002) dan Pomeranz (1991), suhu gelatinisasi tepung tapioka berada pada kisaran 52-64°C. Menurut Swinkels (1985), suhu gelatinisasi tepung tapioka berkisar antara 65-70°C.
Moorthy (2004) menyatakan bahwa gelatinisasi merupakan fenomena kompleks yang bergantung dari ukuran granula, persentase amilosa, bobot molekul, dan derajat kristalisasi dari molekul pati di dalam granula. Pada umumnya granula yang kecil membentuk gel lebih lambat sehingga mempunyai suhu gelatinisasi yang lebih tinggi daripada granula yang besar. Makin besar bobot molekul dan derajat kristalisasi dari granula pati, pembentukkan gel semakin lambat. Menurut Pomeranz (1991), tidak semua granula pati tergelatinisasi pada titik yang sama, tetapi terjadi pada suatu kisaran suhu tertentu. Menurut Olkku dan Rha (1978) dalam Pomeranz (1991), proses gelatinisasi melibatkan peristiwa-peristiwa sebagai berikut: (1) hidrasi dan swelling (pengembangan) granula; (2) hilangnya sifat birefringent; (3) peningkatan kejernihan; (4) peningkatan konsistensi dan pencapaian viskositas puncak; (5) pemutusan molekul-molekul linier dan penyebarannya dari granula yang telah pecah.
Suhu gelatinisasi tergantung pada konsentrasi dan pH larutan pati. Makin kental larutan, suhu gelatinisasi makin sulit tercapai. Bila pH terlalu tinggi, pembentukan gel semakin cepat tercapai tetapi cepat turun lagi. Pembentukan gel optimum pada pH 4-7. Selain itu, penambahan gula juga berpengaruh terhadap kekentalan gel yang terbentuk. Gula akan menurunkan kekentalan, hal ini disebabkan karena gula dapat mengikat air, sehingga pembengkakan butir-butir pati menjadi lebih lambat, akibatnya suhu gelatinisasi akan lebih tinggi. Adanya gula akan menyebabkan gel lebih tahan terhadap kerusakan mekanik (Winarno, 2002).
Menurut Pomeranz (1991), suhu gelatinisasi tapioka berkisar antara 52-64°C.
5. Retrogradasi Pati
Retrogradasi adalah proses kristalisasi kembali pati yang telah mengalami gelatinisasi. Beberapa molekul pati, khususnya amilosa yang dapat terdispersi dalam air panas, meningkatkan granula-granula yang membengkak dan masuk ke dalam cairan yang ada di sekitarnya. Oleh karena itu, pasta pati yang telah mengalami gelatinisasi terdiri dari granula-granula yang membengkak yang tersuspensi ke dalam air panas dan molekul-molekul amilosa yang terdispersi ke dalam air. Molekul-molekul amilosa tersebut akan terus terdispersi, asalkan pati tersebut dalam kondisi panas. Dalam kondisi panas, pasta masih memiliki kemampuan mengalir yang fleksibel dan tidak kaku. Bila pasta pati tersebut kemudian mendingin, energi kinetik tidak lagi cukup tinggi untuk melawan kecenderungan molekul-molekul amilosa untuk bersatu kembali. Molekul-molekul amilosa berikatan kembali satu sama lain serta berikatan dengan cabang amilopektin pada pinggir-pinggir luar granula, dengan demikian mereka menggambungkan butir-butir pati yang bengkak tersebut menjadi semcam jaring-jaring membentuk mikrokristal dan mengendap (Winarno, 2002).
Menurut Fleche (1985), ketika molekul pati sudah benar-benar terhidrasi, molekul-molekulnya mulai menyebar ke media yang ada di luarnya dan yang pertama keluar adalah molekul-molekul amilosa yang memiliki rantai pendek. Keluarnya molekul-molekul amilosa ini menyebabkan terjadinya presipitasi (jika konsentrasi pati rendah) atau membentuk gel (jika konsentrasi pati tinggi).
adalah proses yang kompleks dan dipengaruhi oleh beberapa faktor, antara lain jenis dan konsentrasi pati, prosedur pemasakan, suhu, waktu peyimpanan, prosedur pendinginan, pH, dan keberadaan komponen lain.
E. KACANG SALUT
Kacang salut adalah kacang yang disalut dengan tepung dan bumbu-bumbu kemudian digoreng hingga matang. Dalam pembuatan kacang salut, tepung yang digunakan biasanya adalah tepung tapioka ataupun tepung-tepungan lain seperti tepung terigu maupun tepung telur yang dapt memberikan tekstur sesuai dengan keinginan.
Tepung yang digunakan diharapkan akan menghasilkan penyalut yang mengembang dan memiliki kerenyahan yang baik. Oleh karena itu, untuk memperkirakan pengembangan tepung biasanya dilakukan analisis tingkat pengembangan tepung dengan membuat produk berupa papatan. Papatan merupakan adonan tepung tanpa kacang yang dibentuk bulat-bulat kecil, baik dalam keadaan sebelum digoreng maupun setelah digoreng.
Gambar 4. Grafik hubungan antara gaya (force)dan jarak (distance)
Anonim (2005) menambahkan, untuk membandingkan kerenyahan antara dua sampel yang memiliki gaya (force) dan jarak (distance) yang berbeda, dapat digunakan uji organoleptik untuk mengetahui sampel yang memiliki kerenyahan lebih tinggi.
F. ANALISIS KORELASI
Analisis korelasi mencoba mengukur kekuatan hubungan antara dua peubah (X dan Y) melalui sebuah bilangan yang disebut koefisien korelasi (r). Jadi, r mengukur sejauh mana titik-titik menggerombol di sekitar sebuah garis lurus. Bila titik-titk bergerombol mengikuti sebuah garis lurus dengan kemiringan positif, maka ada korelasi positif yang tinggi antara kedua peubah. Akan tetapi, bila titik-titik bergerombol mengikuti sebuah garis lurus dengan kemiringan negatif, maka antara kedua peubah tersebut terdapt korelasi negatif. Hubungan linier sempurna antara kedua peubah terdapat bila nilai r = 1 atau r = -1. Koefisien korelasi antara dua peubah adalah suatu ukuran hubungan linier antara kedua peubah tersebut. (Walpole, 1995).
III. METODOLOGI
A. BAHAN DAN ALAT
Bahan utama yang digunakan dalam penelitian ini adalah enam jenis tepung tapioka dengan kode tapioka A, tapioka B, tapioka C, tapioka D, tapioka E, dan tapioka F, yang diperoleh dari dua jenis pemasok (industri rumah tangga dan industri besar) serta MOCAL (Modified Cassava Fluor) yang diperoleh dari Koperasi Loh Jinawi Trenggalek. Bahan-bahan kimia yang digunakan adalah alkohol 95%, HCl 3%, H2SO4 25%, KI 20%, larutan
Luff-Schoorl, NaOH 3%, indikator fenolftalen, indikator amilum 0.5%, Na2S2O3 0.1N, amilosa kentang, NaOH 1N, asam asetat 1N, KOH 0.2N,
larutan Iod 0.01N, serta akuades.
Alat-alat yang digunakan antara lain cawan alumunium, oven, neraca analitik, desikator, ruang asap, pendingin tegak, erlenmeyer asah, buret, cawan porselen, tanur, Spectronic Instrumen 20D+ Spektrofotometer, waterbath, labu takar, kertas saring, Mettler Toledo MP220 pH-meter, kaca preparat dan gelas penutup, Olympus BH-2 Polarized Light Microscope, Kett Electric Laboratory C-100-3 Whitenessmeter, Stable Micro System TAXT2 Texture Analyzer, Brabender viscoamylograph OHG Duisburg Type 800121, sentrifusa,Digital sieve shaker, serta alat-alat gelas lainnya.
B. METODE PENELITIAN
Gambar 6.Diagram alir tahapan penelitian
1. Analisis Kimia dan Fisik Tepung Tapioka dan MOCAL
Pada tahap ini dilakukan beberapa analisis sifat kimia dan fisik dari tepung tapioka dan MOCAL. Sifat kimia dan fisik yang diuji meliputi kadar air, kadar abu, kadar pati, kadar amilosa, nilai pH, bentuk dan ukuran pati, kehalusan, derajat putih, swelling power dan kelarutan pati, serta pola amilografi. Semua analisis dilakukan sebanyak dua kali pengukuran (dulplo), kecuali pada analisis kelarutan pati dan sifat amilografi hanya dilakukan sekali pengukuran (simplo). Pembahasan sifat fisik dan kimia antara tepung tapioka dan MOCAL dibedakan karena kedua produk tersebut berbeda.
2. Analisis Tingkat PengembanganPapatan
Tingkat pengembangan papatan dipelajari dengan mengukur volumepapatan saat sebelum digoreng maupun setelah digoreng. Terlebih dahulu dibuat larutan bumbu, yang kemudian diuleni bersama sampel sampai kalis sehingga terbentuk adonan tepung. Diagram alir pembuatan
Sampel tepung tapioka atau MOCAL
Analisis sifat kimia dan fisik Analisis tingkat pengembanganpapatan
Analisis tekstur dan uji organoleptik Aplikasi tepung sebagai penyalut
kacang (kacang salut)
larutan bumbu dapat dilihat pada Gambar 7, sedangkan diagram alir pembuatanpapatan dapat dilihat pada Gambar 8.
Gambar 7. Diagram alir pembuatan larutan bumbu
Gambar 8. Diagram alir pembuatanpapatan Diukur diameternya (D2)
Larutan bumbu tapioka atau MOCALSampel tepung
Adonan Dicampur
Diuleni sampai kalis
Ditimbang 0.5 gram
Dibentuk bulat dan diukur diameternya (D1)
Digoreng
Papatan Premix tepung
dan bumbu
Larutan bumbu Dicampur
Pembuatan papatan dilakukan sebanyak 30 kali agar data yang diperoleh lebih beragam dan dapat mewakili sampel. Diameter papatan diukur menggunakan jangka sorong, baik pada saat sebelum digoreng (D1) maupun sesudah digoreng (D2). Volume papatan dihitung dengan asumsi bahwa papatan berbentuk lingkaran sempurna. Tingkat pengembangan sampel diukur dengan cara sebagai berikut:
Tingkat pengembangan (%) = V2 x 100% V1
Keterangan :
V1 = Volumepapatan sebelum digoreng (mm3) V2 = Volumepapatan setelah digoreng (mm3)
3. Analisis Kerenyahan Produk Kacang Salut
Larutan bumbu yang telah dicampur dengan tepung tapioka atau MOCAL dimasukkan ke dalam coating pan bersama kacang, kemudian kacang yang telah disalut oleh campuran larutan bumbu dan tepung tersebut digoreng. Diagram pembuatan kacang salut dapat dilihat pada Gambar 9.
Gambar 9. Diagram alir pembuatan kacang salut Larutan bumbu
dicampur tepung tapioka atau
MOCAL
Digoreng
Kacang Salut Dicampur
Coating pan Kacang
Analisis kerenyahan secara objektif terhadap kacang salut dilakukan dengan menggunakan alat Stable Micro System TAXT2 Texture Analyzer. Analisis kerenyahan secara subjektif dilakukan dengan uji organoleptik menggunakan ujirating.
C. METODE ANALISIS 1. Kadar Air (AOAC, 1995)
Cawan alumunium dikeringkan dalam oven pada suhu 105oC selama 15 menit, lalu didinginkan di dalam desikator selama 10 menit. Cawan ditimbang menggunakan neraca analitik (A). Sampel sebanyak 5 gram (W) dimasukkan ke dalam cawan, kemudian cawan serta sampel ditimbang dengan neraca analitik. Cawan berisi sampel dikeringkan dalam oven pada suhu 105oC selama 6 jam. Selanjutnya cawan berisi sampel didinginkan dalam desikator, kemudian ditimbang (Y). Setelah itu, cawan berisi sampel dikeringkan kembali dalam oven selama 15-30 menit, lalu ditimbang kembali. Pengeringan diulangi hingga diperoleh bobot konstan
(selisih bobot ≤ 0.0003 gram). Kadar air diukur dengan cara sebagai
berikut:
Kadar air = W – (Y – A ) x 100% W
Keterangan :
W = bobot sampel awal (g)
Y = bobot sampel dan cawan setelah dikeringkan (g) A = bobot cawan kosong (g)
2. Kadar Abu (AOAC, 1995)
6 jam. Cawan yang berisi sampel didinginkan dalam desikator, kemudian ditimbang dengan neraca analitik (X). Kadar abu diukur dengan cara sebagai berikut:
Kadar abu (%) = (X - A) x 100% W
Keterangan :
W = bobot sampel awal (g)
X = bobot sampel dan cawan setelah dikeringkan (g) A = bobot cawan kosong (g)
3. Kadar Pati (SNI 01-2892-1992)
• Pembuatan Larutan Luff Schrool
Sebanyak 71.9 g Na2CO3 anhidrat dilarutkan dalam 300 mL
akuades yang dipanaskan. Setelah larut,kemudian ditambahkan 25 g asam sitrat yang telah dilarutkan dengan 25 mL akuades sedikit demi sedikit. Kemudian di tambahkan 8 g CuSO4.5H2O dalam 100 mL
akuades sedikit demi sedikit. Setelah semua bercampur, kemudian penangas diturunkan suhunya dan dibiarkan selama 30 menit, setelah itu larutan ditera sampai 500 mL dan dibiarkan selama satu malam didalam tempat gelap.
• Analisis sampel
saat mulai mendidih). Setelah mendidih, kemudian didinginkan dalam boks es selama beberapa menit. Kemudian sampel yang telah dingin ditambahkan 25 mL H2SO4 25% dan 15 mL larutan KI 20% lalu segera dititrasi dengan Na2S2O3 0.1 N yang telah distandarisasi.
Penambahan indikator kanji 0.5% dilakukan pada saat titrasi berlangsung, titrasi dihentikan pada saat larutan berubah warna dari ungu menjadi putih keruh.
Penentuan blanko dilakukan dengan mencampurkan 25 mL larutan Luff Schrool dan 25 mL akuades (tanpa sampel). Kemudian direfluks selama 10 menit (dihitung pada saat mulai mendidih ), lalu didinginkan dalam boks es selama beberapa menit. Kemudian ditambahkan 25 mL H2SO4 25% dan 10 mL larutan KI 20%, dan
segera dititrasi dengan larutan Na2S2O3 0.1N yang telah distandarisasi.
Penambahan indikator kanji 0.5% di lakukan pada saat titrasi berlangsung, titrasi dilakukan pada saat larutan berubah warna dari ungu menjadi putih keruh. Kadar pati diukur dengan cara sebagai berikut:
Kadar Pati = G x Fp x 0.9 x 100% W
Keterangan :
G = mg glukosa dari tabel (Vol Na2S2O3 Blanko - Vol Na2S2O3
contoh)
Fp = faktor pengenceran W = bobot contoh (mg)
4. Kadar Amilosa (Apriyantonoet al.,1998) dan Amilopektin
• Pembuatan kurva standar
ditambahkan air suling sampai tanda tera. Setelah itu, dipipet masing-masing 1, 2, 3, 4, dan 5 ml larutan amilosa, masing-masing-masing-masing dimasukkan ke dalam labu ukur 100 ml. Larutan diasamkan dengan asam asetat 1 N masing-masing sebanyak 0.2, 0.4, 0.6, 0.8, dan 1.0 ml. Lalu ditambahkan 2.0 ml larutan iodine (0.2 gram iod dan 2 gram KI dalam 100 ml air). kemudian diencerkan dengan akuades sampai tanda tera, dikocok dan dibiarkan selama 20 menit. Larutan dianalisa dengan Spectronic Instrumen 20D+ Spektrofotometer pada panjang gelombang 610 nm. Lalu data yang diperoleh digunakan untuk membuat kurva standar hubungan antara konsentrasi amilosa dengan absorbansi.
• Analisis sampel
Sebanyak 100 mg sampel ditimbang dan dimasukkan dalam labu ukur 100 ml, kemudian 1 ml etanol 95% dan 9 ml NaOH 1 N ditambahkan ke dalam sampel. Larutan dipanaskan dalam water bath (air mendidih) selama 10 menit (sampai pati tergelatinisasi. Setelah itu, labu ukur yang berisi sampel didinginkan selama 1 jam dan ditambahkan akuades sampai tanda tera, kemudian dikocok.
Sebanyak 5 ml larutan sampel dipipet dan dimasukkan ke dalam labu ukur 100 ml yang telah diisi 40 ml akuades. Sebanyak 1 ml asam asetet 1 N dan 2 ml larutan, kemudian ditambahkan air sampai tanda tera. Larutan sampel dikocok dan dibiarkan selama 20 menit. Larutan sampel diambil untuk dianalisa dengan Spectronic Instrumen 20D+ Spektrofotometer. Selain itu, dibuat juga larutan blanko dengan cara mencampurkan semua bahan kecuali sampel. Kadar amilosa diukur dengan cara sebagai berikut:
Keterangan:
A = konsentrasi amilosa dari kurva standar (mg/ml) Fp = faktor pengenceran
V = volume awal (ml) W = bobot awal (mg)
Kadar amilopektin diperoleh dari selisih antara kadar pati dengan kadar amilosa sampel.
5. Nilai pH
Nilai pH diukur dengan menggunakanMettler Toledo MP220 pH-meter. Sebelum digunakan, pH meter dikalibrasi dengan menggunakan buffer pH 4 dan 7. Setelah dikalibrasi baru dilakukan pengukuran sampel dengan membuat suspensi sampel sebesar 10%.
6. Bentuk dan Ukuran Pati
Bentuk dan ukuran pati diamati dengan menggunakan Olympus BH-2 Polarized Light Microscope. Sejumlah sampel ditambahkan dengan aquades kemudian diteteskan dalam gelas objek dan ditutup dengan kaca penutup. Sampel diamati dibawah lensa mikroskop kemudian difoto dengan menggunakan kamera Olympus C-33AD-4 yang telah terpasang pada mikroskop.
7. Kehalusan
menit, sedangkan ayakan yang digunakan yaitu ayakan no.50 (300µm), no.100 (150µm), dan no. 140 (106µm). Nomor ayakan yang digunakan
berbeda dengan yang ditetapkan oleh TIA (The Tapioca Institute of America) karena adanya keterbatasan alat. Namun, karena nilai kehalusan mengacu pada TIA, maka perbedaan nomor ayakan ini diasumsikan sama dengan nomor ayakan yang ditetapkan oleh TIA.
Pengukuran dilakukan dengan menimbang sejumlah sampel lalu ditaburkan secara merata pada ayakan paling atas. Kemudian ayakan ditutup dan alat dihidupkan. Lalu kehalusan diketahui dengan menghitung persentase jumlah sampel yang lolos ayakan. Kehalusan diukur dengan cara sebagai berikut:
% Kehalusan = 100% - (% sampel yang tidak lolos ayakan) = 100% - ((D:W) x 100%)
Keterangan :
D = bobot sampel yang tertinggal di ayakan (g) W = bobot sampel (g)
8. Derajat Putih
DP (%) = A x 100% Nilai Standar BaSO4 (110.8)
Keterangan :
DP = derajat putih (%) A = nilai terbaca pada alat
9. Daya Kembang Pati (Swelling power) dan Kelarutan Pati (Modifikasi Swinkels, 1985, serta Li dan Yeh, 2001)
Swinkels (1985) mengatakan bahwa nilai swelling power dan kelarutan pati bisa diukur pada kisaran suhu terbentuknya pasta pada pati, yaitu sekitar 50°C-95°C dengan interval 5°C. Sementara itu, Li dan Yeh (2001) mengukur swelling dan kelarutan pati dengan interval 10°C yaitu pada suhu 55°C, 65°C, 75°C, 85°C, dan 95°C. Namun, dalam penelitian ini suhu yang digunakan yaitu 60°C-90°C dengan interval 10°C, kemudian juga dilakukan untuk suhu 95°C. Perbedaan suhu pengukuran ini dilakukan karena berkaitan dengan suhu pemasakan larutan bumbu pada produk kacang salut. Pati dengan konsentrasi 1% dipanaskan pada waterbath dengan suhu 60°C, 70°C, 80°C, 90°C, dan 95°C selama 30 menit, kemudian disentrifusi dengan kecepatan 3000 rpm selama 30 menit, lalu supernatan dipisahkan dari endapan. Nilai swelling power diukur dengan membagi berat endapan dengan berat pati kering sebelum dipanaskan (g/g).
Kelarutan diukur dengan mengeringkan supernatan hasil pemisahan sampai beratnya konstan. Kelarutan dinyatakan sebagai persen berat pati yang larut dalam air. Swelling power dan kelarutan diukur dengan cara sebagai berikut:
Keterangan : SP =swelling power W = berat sampel (g)
X = berat tabung kosong (g) Y = berat tabung dan endapan (g)
Kelarutan (%) x100%
W Y X − =
Keterangan :
W = berat sampel (g) X = berat cawan kosong (g) Y = berat cawan dan endapan (g)
10. Pola Gelatinisasi
Pola gelatinisasi tepung tapioka dan MOCAL dipelajari dengan mengukur sifat-sifat amilografi sampel dengan menggunakan alat Brabender viscoamylograph OHG Duisburg Type 800121. Sampel ditimbang sebanyak 45 gram, lalu dimasukkan ke dalam botol gelas yang volumenya 500 ml dan ditambah akuades sebanyak 450 ml. Kemudian campuran air dan pati tersebut dipindahkan ke dalam mangkuk amilograf yang telah terpasang pada alat.
11. Analisis Tekstur
Tekstur dianalisis dengan menggunakan Stable Micro System TAXT2 Texture Analyzer. Prinsipnya adalah dengan memberikan gaya tekan pada sampel, kemudian akan dihasilkan profil tekstur berupa grafik yang menghubungkan antara gaya (force) dengan jarak (distance). Pertama-tama dilakukan pemasangan probe dan kalibrasi ketinggian probe. Sebelum pengukuran dilakukan setting alat sesuai dengan sampel yang akan dianalisis.
Sampel diletakkan di atas wadah yang tersedia, kemudian pengukuran dilakukan dengan memberikan gaya tekan pada sampel. Pada layar komputer akan ditampilkan profil tekstur dari sampel yang dianalisis.
12. Uji Organoleptik
Uji organoleptik dilakukan terhadap 23 orang panelis tidak terlatih dengan menggunakan uji rating. Parameter yang diuji adalah tekstur (kerenyahan). Sampel disajikan secara acak dengan kode tertentu dan panelis diminta untuk memberikan penilaian sesuai dengan tingkat kerenyahan sampel yaitu pada skala 1 sampai 7. Kemudian data skor tekstur yang diperoleh diolah secara statistik dengan software SPSS, menggunakan uji Duncan dan uji Post Hoc. Penilaian kriteria mutu sensoris (tekstur) kacang salut mengacu pada Tabel 7.
Tabel 7. Penilaian mutu sensoris kacang salut
Skala Tekstur (kerenyahan)
1 amat sangat tidak renyah 2 sangat tidak renyah 3 tidak renyah 4 netral (biasa) 5 renyah 6 sangat renyah 7 amat sangat renyah
13. Analisis Korelasi
koefisien korelasi atau r. Analisis korelasi dilakukan baik antara sifat kimia dan fisik itu sendiri maupun dengan tingkat pengembanganpapatan dan kerenyahan. Namun, analisis korelasi hanya dilakukan antara sifat atau parameter yang diperkirakan memiliki kaitan. Analisis korelasi antara sifat kimia dan fisik dengan tingkat pengembangan papatan dan kerenyahan dilakukan hanya pada sampel tepung tapioka, tanpa MOCAL. Hal ini dilakukan agar dapat dilakukan perbandingan tingkat pengembangan papatan dan kerenyahan yang terjadi antar tepung tapioka, karena MOCAL berbeda dengan tepung tapioka.
IV. HASIL DAN PEMBAHASAN
TEPUNG TAPIOKA
A. SIFAT KIMIA TEPUNG TAPIOKA 1. Kadar Air
Kadar air tepung tapioka menunjukan nilai yang bervariasi (Tabel 8). Kadar air tertinggi dimiliki oleh tapioka B (12.94 %), sedangkan kadar air terendah dimiliki oleh tapioka C (9.51%). Kadar air untuk beberapa sampel tidak berbeda nyata (P>0.05), yaitu antara tapioka D, E, dan F (Lampiran 5a).
Tabel 8. Kadar air sampel
No. Sampel Kadar air (%)
1. Tapioka A 11.75a 2. Tapioka B 12.94b 3. Tapioka C 9.51c 4. Tapioka D 11.00d 5. Tapioka E 10.64d 6. Tapioka F 10.54d
Keterangan : Angka-angka yang diikuti dengan huruf yang sama menunjukan
nilai yang tidak berbeda nyata (P>0.05)
Perbedaan kadar air sampel dapat dipengaruhi oleh proses pengolahan, khususnya pada saat pengeringan. Pada industri rumah tangga, biasanya pengeringan dilakukan secara tradisional yaitu dengan penjemuran di bawah sinar matahari, sedangkan pada industri besar, pengeringan biasanya dilakukan dengan menggunakan alat pengering (dryer). Berdasarkan SNI 01-3451-1994 tentang Syarat Mutu Tepung Tapioka, kadar air keenam sampel tepung tapioka telah memenuhi standar yang ditetapkan yaitu maksimal 15%, baik tepung tapioka mutu I, mutu II maupun mutu III.
2. Kadar Abu
nyata, begitu pula dengan kadar abu antara tapioka D, dan E, tidak berbeda nyata (Lampiran 5a). Kadar abu sampel disajikan pada Tabel 9.
Tabel 9. Kadar abu sampel
No. Sampel Kadar abu (%)
1. Tapioka A 0.01a 2. Tapioka B 0.01a 3. Tapioka C 0.03c 4. Tapioka D 0.04d 5. Tapioka E 0.04d 6. Tapioka F 0.02a
Keterangan : Angka-angka yang diikuti dengan huruf yang sama menunjukan
nilai yang tidak berbeda nyata (P>0.05)
Salah satu proses pengolahan tepung tapioka yang dapat menyebabkan perbedaan nilai kadar abu adalah pada tahap ekstraksi pati. Pada industri besar, ekstraksi pati dilakukan dengan menggunakan alat canggih seperti ekstraktor, sedangkan pada industri rumah tangga ekstraksi dilakukan secara manual dengan menggunakan saringan bertingkat yang terbuat dari bak kayu. Mineral yang terkandung dalam umbi singkong dapat ikut terbuang bersama ampas hasil proses ekstraksi, sehingga kadar abu yang terukur menjadi lebih rendah.
3. Nilai pH
Berdasarkan hasil pengukuran, nilai pH sampel berada pada kisaran 4.0-7.0, dengan pH terendah pada tapioka C yaitu 4.12 dan tertinggi pada tapioka E yaitu 6.52. Nilai pH keenam sampel berbeda nyata pada taraf signifikansi 0.05 (P<0.05). Nilai pH keenam tepung tapioka telah sesuai dengan standar yang ditetapkan oleh The Tapioca Institute of America (TIA). Hasil pengukuran pH sampel dapat dilihat pada Tabel 10.
Tabel 10. Nilai pH sampel
No. Sampel pH
1 Tapioka A 5.18a
2 Tapioka B 5.42b
3 Tapioka C 4.12c
4 Tapioka D 5.02d
5 Tapioka E 6.52e
6 Tapioka F 4.19f
Keterangan : Angka-angka yang diikuti dengan huruf yang sama menunjukan
nilai yang tidak berbeda nyata (P>0.05)
4. Kadar Pati
Kadar pati tertinggi pada tapioka D yaitu 81.00% dan terendah pada tapioka B, yaitu 72.49%. Kadar pati tapioka A, B, E, dan F tidak berbeda nyata (Lampiran 5b), begitu pula dengan tapioka C dan D tidak berbeda nyata (P>0.05). Kadar pati tepung tapioka tidak dipersyaratkan dalam SNI. Beberapa studi melaporkan kandungan pati yang berbeda-beda pada tepung tapioka. Menurut Grace (1977), kadar pati tepung tapioka sekitar 85%. Sementara itu, Abera dan Rakshit (2003) melaporkan jumlah kadar pati dari tiga varietas singkong (CMR, KU50, dan R5) yang diolah dengan cara yang berbeda (penggilingan basah dan penggilingan kering) yaitu sekitar 96-98%. Kadar pati sampel tepung tapioka disajikan dalam Tabel 11.
Tabel 11. Kadar pati sampel
No. Sampel Kadar Pati (%)
1. Tapioka A 75.96a 2. Tapioka B 72.49a 3. Tapioka C 81.00b 4. Tapioka D 80.67b 5. Tapioka E 73.05a 6. Tapioka F 73.59a
Keterangan : Angka-angka yang diikuti dengan huruf yang sama menunjukan
nilai yang tidak berbeda nyata (P>0.05)
pada titik tertentu, lalu umbi akan mejadi keras dan menyerupai kayu, sehingga umbi akan sulit untuk ditangani ataupun diolah.
Perbedaan kadar pati juga dapat terjadi karena proses pengolahan. Abera dan Rakshit (2003) melaporkan bahwa proses penggilingan kering pada pembuatan tepung tapioka dapat menghilangkan kadar pati sebesar 13-20%. Selain itu, kadar pati juga dapat berkurang karena partikel-partikel pati yang berukuran kecil ikut terbuang bersama partikel serat halus selama proses pencucian pati. Pada proses penyaringan basah, kehilangan jumlah pati juga dapat terjadi karena adanya partikel-partikel pati yang lebih besar yang tidak lolos saringan, sehingga jumlah pati yang terukur menjadi lebih sedikit.
5. Kadar Amilosa dan Amilopektin
Hasil pengukuran kadar amilosa dikonversi berdasarkan bobot pati yang terukur. Kadar amilosa terbesar dimiliki oleh tapioka A yaitu 24.01% dan yang terendah adalah tapioka C yaitu 15.47%. Kadar amilosa antara tapioka A dan B tidak berbeda nyata (Lampiran 5b), Begitu pula antara tapioka C dan F (P>0.05). Kadar amilosa dan amilopektin tepung tapioka disajikan dalam Tabel 12.
Tabel 12. Kadar amilosa dan amilopektin sampel
No. Sampel Kadar amilosa (%) Kadar amilopektin (%)
1 Tapioka A 24.01a 75.99a
2 Tapioka B 23.87a 76.13a
3 Tapioka C 15.47c 84.53c
4 Tapioka D 21.30d 78.70d
5 Tapioka E 20.33d 79.67d
6 Tapioka F 17.39c 82.61c
Keterangan : Angka-angka yang diikuti dengan huruf yang sama menunjukan nilai yang tidak berbeda nyata (P>0.05)
melaporkan kadar amilosa tepung tapioka dari lima varietas singkong (Rayong 2, Rayong 5, KU50, Hanatee, dan YOO2) yaitu sekitar 15.9-22.4%. Menurut Moorthy (2004), kadar amilosa tepung tapioka berada pada kisaran 20-27% mirip dengan pati tanaman lain, sedangkan kadar amilosa pada singkong sekitar 18-25%. Variasi kadar amilosa tergantung dari varietas singkong. Sementara itu, menurut Pomeranz (1991), kadar amilosa tepung tapioka yaitu sekitar 17%. Kadar amilosa juga dipengaruhi oleh waktu panen singkong. Sriroth et al. (1999) menyatakan bahwa kadar amilosa singkong dan pati pada umumnya akan lebih rendah pada tanaman yang masih dalam fase pertumbuhan (belum siap panen).
B. SIFAT FISIK TEPUNG TAPIOKA 1. Bentuk dan Ukuran Granula Pati
Berdasarkan hasil pengamatan dengan menggunakan mikroskop cahaya terpolarisasi, dapat dilihat bahwa bentuk granula dari semua sampel tepung tapioka dengan ukuran granula yang tidak jauh berbeda untuk tiap sampel (Tabel 13). Hasil pengamatan bentuk granula tepung tapioka dapat dilihat pada Gambar 10.
Menurut Moorthy (2004), granula tepung tapioka menunjukan variasi yang besar yaitu sekitar 5-40 µ m dengan bentuk bulat dan oval. Febriyanti (1990) mendapati ukuran granula pati dari beberapa varietas tepung singkong berada pada kisaran 3-25 µ m.
100 µm
100 µm 100 µm
100 µm
100 µm
100 µm
Tabel 13. Ukuran granula sampel
No. Sampel Ukuran Granula (µm)
1. Tapioka A 3-40
2. Tapioka B 3-40
3. Tapioka C 3-30
4. Tapioka D 3-30
5. Tapioka E 3-30
6. Tapioka F 3-40
Gambar 10. Granula Pati Tepung Tapioka (A, B, C, D, E, dan F)
2. Kehalusan (lolos ayak)
no.50, no.100, maupun no.140 (Lampiran 5c). Hasil pengukuran kehalusan (lolos ayak) dapat dilihat pada Tabel 14.
Kehalusan sampel pada ayakan no.50 tidak berbeda nyata pada semua sampel tepung tapioka (P>0.05). Kehalusan sampel pada ayakan no.100 tidak berbeda nyata antara tapioka B, C, D, E, dan F (P>0.05). Kehalusan sampel pada ayakan no.150 tidak berbeda nyata antara tapioka B, C, D, dan F (P>0.05).
Tabel 14. Hasil pengukuran kehalusan sampel
Kehalusan sample (%)
No. Sampel
No.50 (300µm) No.100 (150µm) No. 140 (106µm)
1. Tapioka A 98.90a 91.81a 87.72a
2. Tapioka B 99.83a 96.81b 92.10b
3. Tapioka C 99.65a 98.23b 93.83b
4. Tapioka D 99.83a 98.65b 93.55b
5. Tapioka E 99.78a 98.95b 96.98c
6. Tapioka F 99.63a 95.69b 92.43b
Keterangan : Angka-angka yang diikuti dengan huruf yang sama menunjukan nilai yang
tidak berbeda nyata (P>0.05)
Kehalusan tepung tapioka tidak dipersyaratkan dalam SNI, namun mengacu pada TIA (The Tapioca Institute of America), maka kualitas tepung tapioka yang digunakan dalam penelitian ini, berdasarkan kehalusannya, termasuk ke dalam kategori grade C karena kehalusan semua sampel tepung tapioka telah memenuhi standar lolos ayak pada ayakan no.60 yaitu 95%. Sementara itu, kehalusan semua sampel tepung tapioka yang diayak dengan ayakan no.80 dan no.140 tidak memenuhi standar yang ditetapkan oleh TIA karena tidak memenuhi standar lolos ayak pada ayakan no.80 dan no.140 yaitu sebesar 99%.
3. Derajat Putih
Derajat putih terbesar dimiliki oleh tapioka D dan terendah dimiliki oleh tapioka F.
Menurut Meyer (1960) dalam Mulyandari (1992), derajat putih sangat dipengaruhi oleh proses ekstraksi pati. Semakin murni proses ekstraksi pati, maka tepung yang dihasilkan akan semakin putih. Jika proses ekstraksi pati dilakukan dengan baik maka semakin banyak komponen pengotor yang hilang bersama air pada saat pencucian pati. Secara umum, nilai derajat putih keenam sampel tepung tapioka telah memenuhi SNI 01-3451-94 baik pada kategori mutu I yaitu minimal 94.5%, maupun mutu II yaitu minimal 92%, dan mutu III yaitu kurang dari 92%. Derajat putih tepung tapioka dapat dilihat pada Tabel 15.
Tabel 15. Derajat putih sampel
No. Sampel Derajat putih (%)
1. Tapioka A 99.91a
2. Tapioka B 95.62b
3. Tapioka C 97.79c
4. Tapioka D 100.00a
5. Tapioka E 97.90c
6. Tapioka F 95.22b
Keterangan : Angka-angka yang diikuti dengan huruf yang sama menunjukan
bahwa nilainya tidak berbeda nyata (P>0.05)
4. Daya Kembang (Swelling power) dan Kelarutan
Secara umum, swelling power akan meningkat dengan bertambahnya suhu pengukuran. Namun, peningkatan swelling power berbeda untuk masing-masing sampel (Gambar 11)
0.00 melaporkan bahwa terdapat korelasi negatif antara swelling power dengan kadar amilosa. Hal ini terjadi karena amilosa dapat membentuk kompleks dengan lipida dalam pati, sehingga dapat menghambat swelling. Hasil analisis swelling power dan kelarutan disajikan dalam Lampiran 1.
Gambar 11. Polaswelling power sampel tepung tapioka
0 Secara umum, kelarutan pati tepung tapioka meningkat seiring dengan peningkatan suhu pengukuran (Gambar 12). Menurut Pomeranz (1991), kelarutan pati akan meningkat dengan meningkatnya suhu, dan kecepatan peningkatan kelarutan adalah khas untuk tiap pati.
Gambar 12. Pola kelarutan tepung tapioka
5. Pola Gelatinisasi
Pola gelatinisasi tepung tapioka dan MOCAL dipelajari dengan mengukur sifat-sifat amilografi sampel dengan menggunakan alat Brabender viscoamylograph OHG Duisburg Type 800121. Pengamatan dilakukan terhadap suhu gelatinisasi (SG), viskositas maksimum (VM), suhu saat viskositas maksimum (SVM), stabilitas pasta (breakdown), viskositas balik (setback), dan stabiltas pendinginan. Pola gelatinisasi yang berbeda antar masing-masing sampel dapat terjadi karena perbedaan kadar amilosa. Charles et al. (2005) melaporkan bahwa pati yang memiliki kandungan amilosa yang berbeda akan memiliki sifat fungsional yang berbeda, antara lain suhu gelatinisasi, dan viskositas. Oleh karena itu pada penelitian ini, pola gelatinisasi sampel tepung tapioka dikorelasikan dengan kadar amilosa yang dikandungnya. Hasil pengukuran sifat amilografi tepung tapioka disajikan pada Tabel 16, sedangkan pola gelatinisasi tepung tapioka dapat dilihat pada Gambar 13.
a. Suhu gelatinisasi (SG)
Suhu gelatinisasi terendah dimiliki oleh tapioka D yaitu 62.25ºC, sedangkan suhu gelatinisasi yang tertinggi ada pada tapioka B yaitu 67.50ºC. Suhu gelatinisasi yang lebih rendah pada tapioka D menunjukan bahwa hidrasi atau pengikatan air pada tapioka D lebih mudah terjadi, sehingga pada suhu yang lebih rendah, granula pati pada tapioka D sudah mulai tergelatinisasi. Menurut Swinkels (1985), suhu gelatinisasi tapioka berkisar antara 65-70°C. Sedangkan menurut Winarno (2002) dan Pomeranz (1991), suhu gelatinisasi tapioka berada pada kisaran 52-64°C.
0 200 400 600 800 1000 1200 1400 1600 1800 2000
62.25 65.2
5 95 95 50 50
Suhu (oC)
Viskosit
as
(BU
) Tapioka A
Tapioka B Tapioka C Tapioka D Tapioka E Tapioka F
Gambar 13. Grafik pola gelatinisasi tepung tapioka
Struktur amilosa yang sederhana ini dapat membentuk interaksi molekular yang kuat dengan air, sehingga pembentukan ikatan hidrogen ini lebih mudah terjadi pada amilosa (Taggart, 2004). Namun, berdasarkan uji korelasi diperoleh korelasi yang lemah antara suhu gelatinisasi dengan kadar amilosa (r=0.558).
b. Viskositas maksimum (VM) dan suhu pencapaiannya (SVM)
Viskositas maksimum yang dapat dicapai oleh pati disebut juga viskositas puncak. Sedangkan suhu viskositas maksimum (SVM) adalah suhu saat pati mencapai viskositas maksimum. Viskositas maksimum (VM) terbesar dimiliki oleh tapioka E yaitu 1720 BU (Tabel 16), yang berarti kemampuan granula patinya dalam menghidrasi air lebih besar dibandingkan sampel lainnya. Pemecahan granula pati pada E juga lebih cepat dibandingkan sampel lainnya. Hal ini dapat dilihat dari kisaran suhu sampel mulai tergelatinisasi (SG) sampai mencapai viskositas maksimum (SVM) yaitu 64.5-74.25°C. Sementara itu, viskositas maksimum (VM) terendah pada tapioka F yaitu 950 BU
Semakin tinggi viskositas maksimum, berarti kemampuan pati dalam menyerap air semakin besar dan daya thickening-nya (kelengketan) semakin besar. Sehingga hal ini memungkinkan penggunaan tepung dalam jumlah yang lebih sedikit untuk mencapai viskositas tertentu, dan akhirnya dapat mengurangi biaya produksi.
c. Stabilitas pasta panas (breakdown)
Stabilitas pasta panas diukur berdasarkan perubahan viskositas dari viskositas maksimum (VM) sampai viskositas selama pemanasan pada suhu konstan (95°C). Stabilitas pasta panas juga dikenal sebagai breakdown. Stabilitas pasta panas bernilai positif jika terjadi peningkatan viskositas dan bernilai negatif jika terjadi penurunan viskositas. Pada Gambar 12, viskositas tiap sampel selama penahanan terus mengalami penurunan. Hal ini berarti stabilitas pasta panas untuk semua sampel bernilai negatif.
Berdasarkan hasil pengukuran (Tabel 16), dapat dilihat bahwa pasta panas tapioka F cenderung lebih stabil dibandingkan sampel lainnya karena memiliki kemampuan yang lebih baik dalam mempertahankan viskositasnya selama pemanasan. Hal ini ditunjukan dengan rendahnya nilai breakdown sampel tersebut yaitu 390 BU. Stabilitas pasta panas terendah pada sampel E yaitu dengan nilai breakdown sebesar 1220 BU. Nilai breakdown yang besar selama pemasakan menunjukan bahwa granula pati yang telah membengkak secara keseluruhan memiliki sifat yang rapuh. Selain itu, pengadukan yang kontinu juga menyebabkan granula pati yang rapuh akan pecah sehingga viskositas turun secara tajam (Pomeranz, 1991).
pasta panas dengan pH (r=0.607), tetapi tidak berbeda nyata pada taraf signifikansi 0.05 (P>0.05). Selain pH, perbedaan stabilitas pasta panas (breakdown) antara tepung tapioka juga dapat dipengaruhi oleh kadar amilosa. Pada penelitian ini diperoleh adanya korelasi antara kadar amilosa dan breakdown (r=0.429), tetapi tidak berbeda nyata pada taraf signifikansi 0.05 (P>0.05). Semakin tinggi kadar amilosa pati maka viskositas breakdown akan semakin tinggi (Charles et al., 2005)
d. Viskositas balik (setback)
Viskositas balik (setback) merupakan selisih antara viskositas pada akhir pemasakan pada suhu konstan (95°C) dengan viskositas pada akhir pendinginan (50°C). Nilai setback ini menunjukan kecenderungan pati dalam beretrogradasi.
Semakin tinggi viskositas setback berarti semakin tinggi pula kemampuan pati dalam beretrogradasi (Li dan Yeh, 2001). Berdasarkan hasil pengukuran (Tabel 16) diperoleh bahwa tapioka E memiliki kecenderungan yang besar untuk beretrogradasi, hal ini ditunjukan dengan tingginya nilai viskositas setback tapioka E yaitu 250 BU. Hal ini menunjukan bahwa molekul-molekul amilosa dalam tapioka E memiliki kecenderungan yang besar untuk kembali berikatan satu sama lain saat proses pendinginan (cooling). Berbeda dengan tapioka E, kemampuan tapioka F dalam beretrogradasi paling kecil dibandingkan dengan sampel lainnya. Hal ini dapat dilihat dari nilai viskositassetback tapioka F yang sangat kecil yaitu 40 BU.
e. Stabilitas pasta selama fase pendinginan
Stabilitas pasta dingin diperoleh dari selisih viskositas selama pendinginan pada suhu konstan (50°C). Stabilitas pasta dingin digunakan untuk mengetahui kestabilan pasta pati terhadap proses pengadukan selama pendinginan setelah pemasakan. Viskositas yang tinggi menunjukan stabilitas pasta dingin yang lebih rendah, karena perubahan viskositasnya selama pendinginan konstan sangat besar. Tapioka F memiliki nilai stabilitas pasta dingin paling tinggi yaitu 50 BU dan 40 BU. Hal ini menunjukan kemampuan ikatan antara molekul tapioka F terhadap air cenderung tinggi selama pendinginan dan tidak terlalu terpengaruh oleh proses pengadukan, sehingga stabilitasnya selama fase pendinginan pada suhu konstan (50°C) lebih stabil. Nilai stabilitas pasta dingin yang terendah dimiliki oleh tapioka E yaitu 150 BU. Hal ini menunjukan bahwa stabilitas pasta dingin pada tapioka E cenderung kurang stabil akibat pengadukan, sehingga peningkatan viskositasnya selama pendinginan pada suhu konstan (50°C) cukup tinggi.
Berdasarkan uji korelasi, terdapat korelasi antara kadar amilosa dengan stabilitas pasta pada fase pendinginan (r=0.542), tetapi korelasi antara keduanya tidak berbeda nyata pada taraf signifikansi 0.05 (P>0.05).
C. ANALISIS TINGKAT PENGEMBANGANPAPATAN
Tabel 17. Tingkat pengembanganpapatan sampel
No. Sampel Tingkat pengembangan
(%)
Menurut Matz (1992), tingkat pengembangan dan tekstur dari makanan ringan (snack) dipengaruhi oleh rasio amilosa dan amilopektin. Pati yang memiliki kandungan amilopektin tinggi cenderung memberikan karakter produk yang fragile (mudah pecah), sedangkan amilosa akan memberikan tekstur yang lebih tahan terhadap kemudahan untuk pecah. Berdasarkan uji korelasi, diperoleh korelasi yang sangat kuat antara rasio amilosa dan amilopektin dengan tingkat pengembanganpapatan (r=-0.846), dan berbeda nyata pada taraf signifikansi 0.05 (P>0.05). Hal ini menunjukan bahwa semakin rendah rasio amilosa dan amilopektin makapapatan yang dihasilkan akan semakin mengembang (Gambar 14).
Gambar 14. Korelasi antara tingkat pengembangan papatan dengan rasio amilosa dan amilopektin
r2 = 0.7154
0.00 0.05 0.10 0.15 0.20 0.25 0.30
Berdasarkan hasil analisi uji korelasi ternyata diperoleh korelasi yang rendah antara tingkat pengembangan papatan dengan swelling power maupun kelarutan (Lampiran 7d). Hal ini ditunjukan dengan rendahnya nilai koefisien korelasi antara tingkat pengembangan papatan dengan swelling power (r=0.264) maupun dengan kelarutan (r=0.337). Hal ini dapat terjadi karena proses yang berbeda antara analisis swelling power dan kelarutan dengan analisis pengembangan papatan. Kemampuan pati dalam menyerap air (swelling power) dan kelarutannya tidak dapat menunjukan kemampuan pati untuk mengembang ketika dipanaskan dalam media minyak (penggorengan).
Menurut Fleche (1985), pati yang memiliki pH lebih rendah adalah pati
yang lebih cepat untuk terhidrolisis pada ikatan α (1,4). Asam dapat
mengganggu ikatan hidrogen yang terdapat dalam pati, sehingga menyebabkan granula pati lebih mudah untuk mengembang (Taggart, 2004). Dalam penelitian ini diperoleh korelasi yang sangat lemah antara pH dengan tingkat pengembangan dengan koefisien korelasi (r) sebesar -0.194 (Lampiran 7e). Korelasi antara tingkat pengembanganpapatan dengan sifat amilografi sampel menunjukan korelasi yang negatif. Koefisien korelasi antara tingkat pengembangan papatan dengan viskositas puncak (r=-0.597), setback (r=-0.403), breakdown (r=-0.559) dan stabilitas pasta fase pendinginan (r=-0.209) menunjukan korelasi yang negatif. Korelasi antara tingkat pengembangan papatan dengan sifat amilografi sampel cukup erat tetapi tidak berbeda nyata pada taraf signifikansi 0.05 (P>0.05). Maka dapat disimpulkan bahwa tingkat pengembangan papatan tidak secara langsung dipengaruhi swelling power dan kelarutan, pH maupun sifat amilografi sampel tepung tapioka (Lampiran 7f).
D. ANALISIS KERENYAHAN TEKSTUR KACANG SALUT