ASPEK PSIKOSOMATIK PADA GANGGUAN HATI
Wika Hanida Lubis, Habibah Hanum, Ricky Rivalino Sitepu
Divisi Psikosomatik Departemen Ilmu Penyakit Dalam
Fakultas Kedokteran Universitas Sumatera Utara
Pendahuluan
Gangguan hati telah lama diketahui memiliki dampak signifikan terhadap aspek psikosomatik. Gejala klinis psikosomatis dari gangguan hati mulai mulai diteliti pada 1950-an menyusul munculnya hepatologi sebagai spesialisasi medis. Gejala-gejala ini pada dasarnya merupakan gangguan mental organik yang merupakan konsekuen dari gangguan metabolik yang berat disertai sirkulasi kolateral portal sistemik. Sebagian besar bentuk penyakit hati kronis mengarah ke sirosis yang dapat mengakibatkan terjadinya ensefalopati hepatik dan bermanifestasi dengan gejala psikosis seperti mania, depresi, apatis, atau kebingungan sebelum akhirnya menjadi delirium. Gangguan psikosomatik juga dapat terjadi akibat pemberian terapi jangka panjang dan pada pasien yang menjalani transplantasi hati. Pendekatan psiokosomatik pada pasien dengan penyakit hati kronis sangat penting untuk meningkatkan kesehatan dan kualitas hidup dan juga memfasilitasi pengobatan terhadap gangguan hati. Tulisan ini membahasa hubungan antara aspek psikosomatik pada pasien dengan gangguan hati [1].
Definisi Gangguan Psikosomatik dan Gangguan Hati
2 Gangguan fungsi hati didefinisikan sebagai peningkatan dari enzim-enzim hati seperti serum glutamic pyruvic transferase (SGPT) dan serum glutamic ocsaloasetic transaminase (SGOT) sebanyak tiga kali lipat dari batas normal. Biasanya disertai dengan gejala-gejala penyakit hati seperti jaundice, urin yang coklat seperti teh, warna feces yang pucat, nyeri abdomen pada bagian kanan atas, dan sebagainya [3].
Prevalensi Gangguan Psikosomatis pada Gangguan Hati
Gangguan depresi dan ansietas merupakan gangguan psikosomatis yang paling banyak terjadi di masyarakat. Bahkan di antara kita sesekali dalam perjalanan hidup menempuh spesialis penyakit dalam pernah mengalami depresi sekalipun dalam derajat yang ringan atau setidaknya depresi terselubung. Berdasarkan departemen sosial pada tahun 2011 ada sebanyak 11.6% atau sekitar 24.708.000 dari jumlah penduduk Indonesia yang mengalami depresi dan sebanyak 8.3% mengalami ansietas [4, 5].
Prevalensi gangguan hati di Indonesia sebagian besar disebabkan oleh virus hepatitis B dan C yaitu sebesar 40-50% dan 30-40%, sedangkan 10-20% penyebabnya tidak diketahui. Data Riset Kesehatan Dasar (Riskesdas) 2007 melaporkan prevalensi hepatitis di Indonesia sebesar 0.2%. Berdasarkan data Profil Kesehatan Indonesia 2008, jumlah kasus baru hepatitis B di Indonesia pada tahun 2008 mencapai 1.727 pasien sedangkan hepatitis C mencapai 7.234 pasien [6, 7].
Gangguan psikosomatik pada pasien yang mengalami gangguan hati masih belum diketahui jumlahnya di Indonesia. Meski demikian, penelitian di Eropa oleh Golden et al menyatakan bahwa terdapat sekitar 30% pasien hepatitis C yang mengalami depresi dan 25% diantaranya mengalami ansietas. Sebagian besar dari pasien yang mengalami gangguan psikosomatis tersebut belum terdiagnosis sebelumnya [8].
Gejala Psikosomatis Pada Gangguan Hati
didominasi oleh tanda-tanda yang jelas dari disfungsi hati. Pasien biasanya mengalami kuning pada tubuh dengan sirkulasi hiperdinamik, demam, septisemia, dan mengalami gangguan perdarahan. Gangguan kesadaran pada pasien seperti delirium menunjukkan adanya ensefalopati hepatikum. Gejala psikologis utama pada penyakit hati kronis diantaranya adalah depresi, anxietas, insomnia, kelelahan dan gangguan kognitif yang progresif [9].
Patofisiologi Gangguan Psikosomatik pada Gagal hati
Gangguan psikosomatis seperti depresi dan anxietas biasanya disebabkan perubahan-perubahan fisiologis dan biokemis pada tubuh seseorang. Perubahan fisiologi ini berkaitan erat dengan adanya gangguan pada sistem saraf otonom vegetative, sistem endokrin dan sistem imun. Hipotesis yang paling banyak dikenal ialah adanya gangguan konduksi impuls melalui neurotransmitter. Gangguan konduksi ini disebabkan adanya kelebihan atau kekurangan neurotransmitter di presinaps atau adanya gangguan sensitivitas pada reseptor-reseptor postsinaps. Beberapa neurotransmitter yang telah diketahui berupa amin antara lain serotonin, noradrenalin, dan dopamine [10].
4
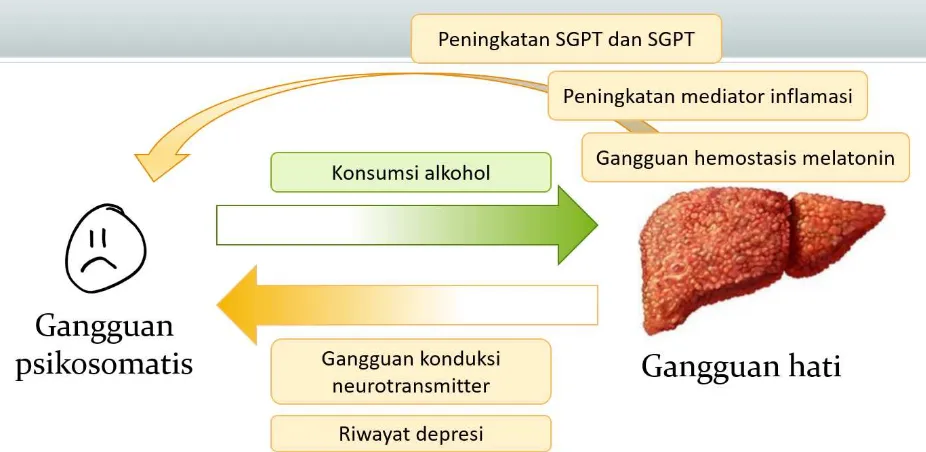
Gambar 1. Etiologi gangguan psikosomatis pada gangguan hati
Perlu diketahui bahwa kelainan depresi pada gagal hati tidak hanya disebabkan oleh perubahan-perubahan fisiologis dan biokemis dalam tubuh. Pasien dengan gangguan hati akibat alkohol biasanya memiliki riwayat gangguan psikis. Sangat sulit untuk membedakan apakah depresi pada pasien berkorelasi dengan konsumsi zat beralkohol atau tidak. Pemberian terapi interferon jangka panjang pada pasien hepatitis juga dapat menyebabkan gangguan psikosomatis. Selain itu, gejala sirosis seperti kelelahan dapat
merusak 'kualitas hidup’ dan mempengaruh persepsi pasien pada status kesehatannya,
sehingga membuat pasien lebih rentan terhadap depresi [14, 15].
Gangguan Psikosomatis Akibat Interferon
Depresi akibat IFN
Depresi yang diakibatkan oleh pemberian interferon (IFN) dilaporkan terjadi pada 10%-40% pasien. Perbedaan persentase tersebut dipengaruhi oleh desain penelitian, kriteria diagnostik, metode penilaian, dan populasi penelitian. Munculnya depresi juga dipengaruhi oleh dosis dan lamanya pemberian terapi IFN. Gejala depresi biasanya berkembang dalam 12 minggu pertama pengobatan dan sering disertai dengan lekas marah daripada dysphoria atau merasa sedih. Gejala biasanya hilang dalam waktu singkat setelah terapi IFN berakhir. Oleh karena dampaknya yang besar pada kepatuhan pengobatan, upaya telah dilakukan untuk mengidentifikasi pasien yang berada pada risiko besar untuk terjadinya depresi akibat IFN. Beberapa studi telah mengatakan bahwa pasien dengan dasar subklinis depresi memiliki risiko yang lebih tinggi dalam terjadinya depresi akibat IFN. Sebaliknya, riwayat depresi atau gangguan kejiwaan lainnya belum terbukti menjadi faktor risiko yang signifikan. Mekanisme terjadinya depresi yang diinduksi oleh IFN tidak diketahui tetapi mungkin terkait dengan kemampuannya untuk menginduksi produksi sitokin pro-inflamasi (misalnya, interleukin-6), mengubah sistem serotonergik, atau mengaktifkan sumbu hypothalamic– pituitary–adrenal axis (HPA) [17-22].
6 yang sama terhadap farmakoterapi. Pasien dengan kelelahan dan anoreksia biasanya kurang responsif terhadap terapi [23-26].
Gangguan fungsi kognitif akibat IFN
Pasien melaporkan adanya masalah kognitif selama terapi IFN, termasuk kesulitan dengan memori, konsentrasi, dan pemecahan masalah. IFN dapat mempengaruhi sistem frontal-subkortikal sehingga mengganggu memori kerja dan perhatian kompleks. Efeknya tergantung pada dosis, durasi, dan rute pemberian IFN. Mekanisme IFN dalam menyebabkan disfungsi kognitif belum diketahui, meskipun demikian pada pemeriksaan PET scans diketahui terjadi hypometabolism pada korteks prefrontal. MRI menunjukkan aktivasi korteks anterior cingulate, yang dapat menghasilkan kesulitan dalam pengenalan dan pengolahan masalah. Namun, peneliti belum mampu mengidentifikasi bukti obyektif penurunan nilai kognitif dan berhipotesis bahwa gejala hanya bersifat subjektif dan alami. Meski demikian, disfungsi kognitif tidak berkaitan dengan gejala depresi dan biasanya sembuh setelah terapi IFN dihentikan [27-30].
6.2 Kelelahan akibat IFN
Kelelahan adalah efek samping yang paling mengganggu bagi kebanyakan pasien karena mempengaruhi aktivitas sehari-hari. Kelelahan akibat IFN mungkin berhubungan dengan perubahan dalam basal ganglia, termasuk nucleus accumbens dan putamen. Beberapa pasien dapat diberikan terapi erythropoietin jika anemia atau suplemen hormon tiroid jika terdapat hipotiroid. SSRI mungkin tidak secara signifikan mengurangi kelelahan akibat IFN, tetapi stimulan seperti modafinil mungkin efektif. Meski demikian, hanya sedikit data yang ada mengenai kelelahan akibat IFN [31, 32].
Pasien dengan risiko tinggi pemberian IFN
dapat menjalani terapi IFN hingga selesai. Kekhawatiran akan ketidakmampuan untuk mematuhi pengobatan dan risiko yang berpotensi tinggi untuk terjadinya efek samping kejiwaan menyebabkan banyaknya pasien yang tidak mendapat pengobatan. Beberapa penelitian yang melibatkan populasi berisiko tinggi menunjukkan bahwa keberhasilan pengobatan adalah hal yang sangat mungkin. Namun beberapa kelompok mencatat tingkat putus obat yang lebih besar dan rendahnya penurunan tingkat penurunan virologi pada pasien dengan risiko tinggi. Saat ini, hampir semua pedoman pengobatan hepatitis merekomendasikan pasien berisiko tinggi untuk melibatkan koordinasi perawatan antara penyedia kesehatan mental dan hepatologi [3, 33, 34].
Ensefalopati Hepatikum
Semua berkontribusi dalam perubahan dalam fungsi otak. Faktor kontributor lainnya termasuk neurosteroids, endogenous benzodiazepine receptor ligands, sitokin inflamasi, manganese, mercaptans, dan asam oktanoat. Diagnosis ensefalopati hatikum merupakan hasil eksklusi penyebab lain perubahan status mental pada pasien dengan penyakit hati yang signifikan (misalnya, infeksi, penyalahgunaan zat, dan perdarahan intrakranial). Tes psikometri seperti Digit Symbol, Line Tracing, Trail-making Test dapat membantu, terutama jikat terjadi penurunan kognitif yang ringan. Temuan elektroensefalogram biasanya menunjukkan perlambatan gelombang otak secara umum dan adanya gelombang triphasic tapi tidak spesifik untuk ensefalopati. Kadar amonia dalam darah biasanya cenderung meningkat tetapi tidak pada semua pasien [35, 36].
8 juga dapat diberikan, tapi bukti tidak cukup untuk merekomendasikan penggunaannya [37, 38].
Psikofarmakologi Pada Gangguan Hati
Tidak ada obat yang benar-benar berkontraindikasi pada pasien dengan gangguan hati, tetapi beberapa obat memiliki risiko lebih besar untuk terjadinya toksisitas hati yang signifikan. Perhatian khusus perlu diberikan ketika meresepkan obat psikotropika untuk pasien dengan penyakit hati, mengingat bahwa hati memiliki kapasitas fungsional yang besar dan hanya pada kerusakan hati yang luas dimana resep harus diubah. Prinsip-prinsip berikut harus diadopsi:
1. Semakin besar tingkat kerusakan hati semakin rendah dosis awal dan dosis maksimum yang diberikan
2. Tes fungsi hati memberikan indikasi dari gangguan hati tetapi tidak selalu berkorelasi dengan baik dengan kerusakan hati yang telah terjadi
3. Beberapa obat yang memiliki first-pass clearance effect yang menyebabkan sedasi dan konstipasi sehingga dihindari pada gangguan hati yang luas
4. Selalu mulai dengan dosis rendah, meningkatkan dosis perlahan dan memantau tes fungsi hati
dengan pemberian 50% dari dosis konvensional obat psikotropika. Penderita disfungsi hati dengan skor CPS C, kegagalan hati berat atau sirosis, perlu dilakukan titrasi obat, bersama dengan pemantauan ketat untuk mencegah memburuknya status kognitif akibat pemberian obat psikotropika potensial [26, 39].
Skor merupakan hasil gabungan kelima faktor
TABEL 1. Skor Child-Pugh Scale
Faktor 1 Poin 2 Poin 3 Poin
Serum bilirubin (ilmol/L) 34 35-50 51
Serum albumin (g/dL) >3.5 3.0-3.5 <3.0
Prothrombin time (s) <4 4-6 >6
International normalized ratio (INR) <1.7 1.7-2.3 >2.3
Asites Tidak ada Ringan, medically
controlled
Moderate-severe, poorly controlled
Ensefalopati Tidak ada Stage 1-2 Stage 3-4
Skor Total 5-6 7-9 10-15
Child-Pugh Scale score A B C
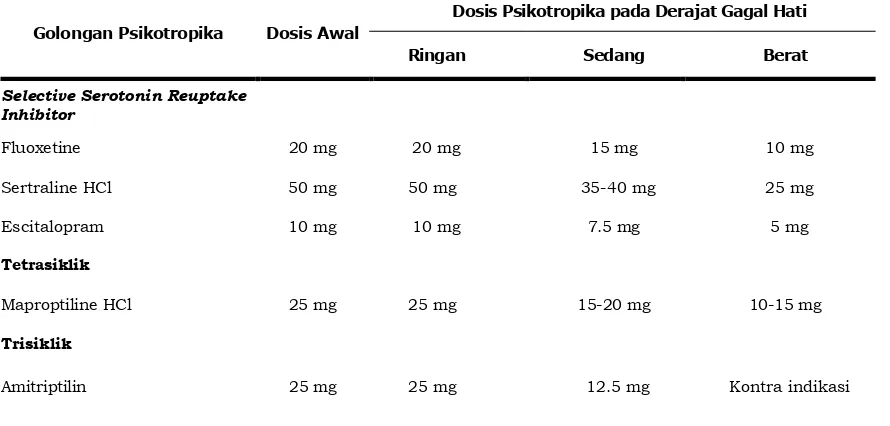
TABEL 2. Dosis Obat Psikotropika pada Gagal Hati [40]
Golongan Psikotropika Dosis Awal
Dosis Psikotropika pada Derajat Gagal Hati
Ringan Sedang Berat
Selective Serotonin Reuptake Inhibitor
Fluoxetine 20 mg 20 mg 15 mg 10 mg
Sertraline HCl 50 mg 50 mg 35-40 mg 25 mg
Escitalopram 10 mg 10 mg 7.5 mg 5 mg
Tetrasiklik
Maproptiline HCl 25 mg 25 mg 15-20 mg 10-15 mg
Trisiklik
Amitriptilin 25 mg 25 mg 12.5 mg Kontra indikasi
10
Dikutip dari MIMS Indonesia Petunjuk Konsultasi 2016
Antidepresi
Obat antidepresan memiliki sifat hepatotoksik, efek sampingnya berupa peningkatan enzim hati dan meskipun jarang dapat menyebabkan nekrosis luas dan gagal hati fulminan. Golongan monoamine oxidase inhibitor dan trisiklik memiliki kemungkinan lebih besar untuk menyebabkan kerusakan hati dibanding antidepresan baru. Kebanyakan trisiklik memiliki first-pass clearance yang dan efek samping yang tinggi, seperti mengantu, dan lebih sering terjadi pada pasien dengan gangguan hati. Selective serotonin reuptake inhibitor merupakan golongan antidepressant yang dapat lebih ditolerir pada gangguan hati dibandingkan golongan lainnya. Dosis alternatif harian fluoxetine telah direkomendasikan untuk diberikan pada pasien depresi dengan gagal hati. Sementara dosis terapeutik yang lebih rendah telah direkomendasikan untuk citalopram dan paroxetine. Sebuah studi mengatakan bahwa paroxetine adalah pilihan paling aman, tapi ini perlu diimbangi dengan risiko adanya sindroma withdrawal. Venlafaxine, mirtazapine dan reboxetine aman diberikan jika dosis awal tidak lebih dari
Phenelzine 15 mg Kontra indikasi Kontra indikasi Kontra indikasi
Tranycyclopine 10 mg Kontra indikasi Kontra indikasi Kontra indikasi
Antidepresi golongan lain
Bupropion 50 mg 50 mg 30-40 mg 25 mg
Benzodiazepine
Alprazolam 0.5-1 mg 0.5-1 mg 0.5 mg 0.25 mg
Clobazam 5 mg 2.5 mg 1.25 mg Kontra indikasi
Estazolam 1 mg 1 mg 0.5 mg 0.25 mg
Lorazepam 1-3 mg 1-3 mg 1 mg 0.5 mg
Diazepam 5-10 mg 5-10 mg 5 mg 2 mg
Hipnotik/sedatif
50% dari dosis biasa. Monoamine oxidase inhibitor memiliki sifat yang lebih hepatotoksik dibandingkan golongan antidepresan lainnya dan dapat memicu koma. Golongan ini umumnya berkontraindikasi. Jika monoamine oxidase inhibitor diperlukan atas dasar klinis maka harus diberikan dengan dosis awal dikurangi sepertiga atau setengah dan dibarengi dengan pemberian moclobemide [41-43].
Anxiolitik dan hipnotik
Gangguan hati mengganggu metabolisme diazepam dan chlordiazepoxide, dengan memperpanjang waktu paruh dari metabolism obat. Oleh karenanya dapat memicu ensefalopati dan koma. Golongan benzodiazepin yang menjadi pilihan diantaranya lorazepam, temazepam dan oxazepam dan diberikan dalam dosis rendah. Metabolisme pada obat ini tidak menunjukkan adanya perubahan. Sedangkan eliminasi dari zolpiclone berkurang pada gagal hati. Dosis 3.75 mg dapat diberikan secara hati-hati dengan dosis total tidak boleh melebihi 7,5 mg. Demikian pula zolpidem harus digunakan dalam dosis yang dikurangi. Obat ini berkontraindikasi pada gagal hati berat [44, 45].
Hepatitis Imbas Obat/Drug-Induced Liver Injury
12 elevasi yang signifikan pada serum glutamic pyruvic transferase (SGPT) bersamaan dengan alkali fosfatase. Sedangkan kerusakan hati kolestasis biasanya terjadi peningkatan yang lebih signifikan pada alkali fosfatase. Hampir semua obat psikotropika memiliki risiko terjadinya hepatotoksisitas, tapi risikonya sangat rendah. Bagi sebagian besar pasien yang sedang mengkonsumsi obat, pemantauan fungsi hati secara rutin tidak dianjurkan karena HIO masih bersifat idiosinkrasi. Karena tidak jelasnya kerusakan hati yang dapat berlanjut ke kondisi yang fulminan, pemberhentian obat disarankan pada pasien yang memiliki peningkatan SGPT hingga tiga kali diatas normal. Selain itu peningkatan bilirubin, peningkatan International normalization ratio (INR), gejala gangguan hati (misalnya, nyeri kuadran kanan atas, urin gelap, pruritus, sakit kuning, mual, anoreksia) juga merupakan indikasi untuk pemberhentian obat [43, 46-48].
Kesimpulan
Daftar Pustaka
1. De Bona, M., et al., The impact of liver disease and medical complications on quality of life and psychological distress before and after liver transplantation. Journal of hepatology, 2000. 33(4): p. 609-15.
2. Ismail, R. and K. Siste, Gangguan Depresi. Dalam Elvira, Silvia D., Hadisukanto, Gitayanti, Buku Ajar Psikiatri, Fakultas Kedokteran Universitas Indonesia, Jakarta, 2010.
3. Ghany, M.G., et al., Diagnosis, management, and treatment of hepatitis C: an update.
Hepatology, 2009. 49(4): p. 1335-74.
4. Pardede, C.M., KARAKTERISTIK PENDERITA PERCOBAAN BUNUH DIRI DENGAN RACUN DI RSUD DR. PIRNGADI KOTA MEDAN TAHUN 2006-2011. Gizi, Kesehatan Reproduksi dan Epidemiologi, 2012. 1(01).
5. Sofyani, S. and M.J. Simbolon, Hubungan Gangguan Ansietas dan Gangguan Depresi Terhadap Kejadian Sakit Perut Berulang Pada Remaja. 2012.
6. Profil Kesehatan 2008, 2009, Departemen Kesehatan.
7. Laporan Hasil Riset Kesehatan Dasar RISKESDAS Indonesia. 2007 [cited 2016 6 Maret]. 8. Golden, J., A.M. O'Dwyer, and R.M. Conroy, Depression and anxiety in patients with hepatitis
C: prevalence, detection rates and risk factors. General hospital psychiatry, 2005. 27(6): p. 431-8.
9. Loftis, J.M., A.M. Matthews, and P. Hauser, Psychiatric and substance use disorders in individuals with hepatitis C: epidemiology and management. Drugs, 2006. 66(2): p. 155-74. 10. Duman, R., Pathophysiology of depression: the concept of synaptic plasticity. European
psychiatry, 2002. 17: p. 306-310.
11. Ko, F.Y., et al., Physiologic and laboratory correlates of depression, anxiety, and poor sleep in liver cirrhosis. BMC gastroenterology, 2013. 13: p. 18.
12. Alekseeva, A.S., et al., Serotonin metabolism parameters in patients with chronic hepatitis and liver cirrhosis. Bulletin of experimental biology and medicine, 2008. 146(5): p. 577-9.
13. Culafic, D.M., et al., Plasma and platelet serotonin levels in patients with liver cirrhosis. World journal of gastroenterology, 2007. 13(43): p. 5750-3.
14. Bianchi, G., et al., Psychological status and depression in patients with liver cirrhosis. Digestive and liver disease : official journal of the Italian Society of Gastroenterology and the Italian Association for the Study of the Liver, 2005. 37(8): p. 593-600.
15. Fritz, E. and J. Hammer, Gastrointestinal symptoms in patients with liver cirrhosis are linked to impaired quality of life and psychological distress. European journal of gastroenterology & hepatology, 2009. 21(4): p. 370-5.
16. Nelligan, J.A., et al., Depression comorbidity and antidepressant use in veterans with chronic hepatitis C: results from a retrospective chart review. The Journal of clinical psychiatry, 2008. 69(5): p. 810-6.
17. Schafer, A., et al., Methodological approaches in the assessment of interferon-alfa-induced depression in patients with chronic hepatitis C - a critical review. International journal of methods in psychiatric research, 2007. 16(4): p. 186-201.
18. Capuron, L. and A. Ravaud, Prediction of the depressive effects of interferon alfa therapy by the patient's initial affective state. The New England journal of medicine, 1999. 340(17): p. 1370. 19. Raison, C.L., et al., Depression during pegylated interferon-alpha plus ribavirin therapy:
prevalence and prediction. The Journal of clinical psychiatry, 2005. 66(1): p. 41-8.
14
21. Asnis, G.M. and R. De La Garza, 2nd, Interferon-induced depression in chronic hepatitis C: a review of its prevalence, risk factors, biology, and treatment approaches. Journal of clinical gastroenterology, 2006. 40(4): p. 322-35.
22. Malek-Ahmadi, P. and R.C. Hilsabeck, Neuropsychiatric complications of interferons: classification, neurochemical bases, and management. Annals of clinical psychiatry : official journal of the American Academy of Clinical Psychiatrists, 2007. 19(2): p. 113-23.
23. Gleason, O.C., et al., Preventing relapse of major depression during interferon-alpha therapy for hepatitis C--A pilot study. Digestive diseases and sciences, 2007. 52(10): p. 2557-63.
24. Kraus, M.R., et al., Therapy of interferon-induced depression in chronic hepatitis C with citalopram: a randomised, double-blind, placebo-controlled study. Gut, 2008. 57(4): p. 531-6. 25. Morasco, B.J., et al., A randomized trial of paroxetine to prevent interferon-alpha-induced
depression in patients with hepatitis C. Journal of affective disorders, 2007. 103(1-3): p. 83-90. 26. Crone, C.C., G.M. Gabriel, and A. DiMartini, An overview of psychiatric issues in liver disease
for the consultation-liaison psychiatrist. Psychosomatics, 2006. 47(3): p. 188-205.
27. Kraus, M.R., et al., Neurocognitive changes in patients with hepatitis C receiving interferon alfa -2b and ribavirin. Clinical pharmacology and therapeutics, 2005. 77(1): p. 90-100.
28. Pawelczyk, T., et al., Pegylated interferon alpha and ribavirin therapy may induce working memory disturbances in chronic hepatitis C patients. General hospital psychiatry, 2008. 30(6): p. 501-8.
29. Juengling, F.D., et al., Prefrontal cortical hypometabolism during low-dose interferon alpha treatment. Psychopharmacology, 2000. 152(4): p. 383-9.
30. Fontana, R.J., et al., Cognitive function does not worsen during pegylated interferon and ribavirin retreatment of chronic hepatitis C. Hepatology, 2007. 45(5): p. 1154-63.
31. Capuron, L., et al., Anterior cingulate activation and error processing during interferon-alpha treatment. Biological psychiatry, 2005. 58(3): p. 190-6.
32. Martin, K.A., et al., Modafinil's use in combating interferon-induced fatigue. Digestive diseases and sciences, 2007. 52(4): p. 893-6.
33. Robaeys, G. and F. Buntinx, Treatment of hepatitis C viral infections in substance abusers. Acta gastro-enterologica Belgica, 2005. 68(1): p. 55-67.
34. Schaefer, M., et al., Hepatitis C treatment in "difficult-to-treat" psychiatric patients with pegylated interferon-alpha and ribavirin: response and psychiatric side effects. Hepatology, 2007. 46(4): p. 991-8.
35. Haussinger, D. and F. Schliess, Pathogenetic mechanisms of hepatic encephalopathy. Gut, 2008. 57(8): p. 1156-65.
36. Butterworth, R.F., Pathophysiology of hepatic encephalopathy: The concept of synergism.
Hepatology research : the official journal of the Japan Society of Hepatology, 2008. 38 Suppl 1: p. S116-21.
37. Sundaram, V. and O.S. Shaikh, Hepatic encephalopathy: pathophysiology and emerging therapies. The Medical clinics of North America, 2009. 93(4): p. 819-36, vii.
38. Als-Nielsen, B., L.L. Gluud, and C. Gluud, Benzodiazepine receptor antagonists for hepatic encephalopathy. The Cochrane database of systematic reviews, 2004(2): p. CD002798.
39. Albers, I., et al., Superiority of the Child-Pugh classification to quantitative liver function tests for assessing prognosis of liver cirrhosis. Scandinavian journal of gastroenterology, 1989. 24(3): p. 269-76.
40. Medica, C., MIMS Indonesia Petunjuk Konsultasi, 2016, Edisi.
41. Bergstrom, R., et al., The effects of renal and hepatic disease on the pharmacokinetics, renal tolerance, and risk-benefit profile of fluoxetine. International clinical psychopharmacology, 1993. 42. Livingston, M.G. and H.M. Livingston, Monoamine oxidase inhibitors. Drug safety, 1996. 14(4):
43. Lucena, M.I., et al., Antidepressant-induced hepatotoxicity. Expert opinion on drug safety, 2003. 2(3): p. 249-62.
44. Kaplan, S. and M. Jack, Pharmacokinetics and metabolism of anxiolytics, in Psychotropic Agents1981, Springer. p. 321-358.
45. Shapiro, S., et al., Clinical effects of hypnotics: II. An epidemiologic study. JAMA, 1969. 209(13): p. 2016-2020.
46. Hussaini, S.H. and E.A. Farrington, Idiosyncratic drug-induced liver injury: an overview. Expert opinion on drug safety, 2007. 6(6): p. 673-84.
47. Russo, M.W. and P.B. Watkins, Are patients with elevated liver tests at increased risk of drug-induced liver injury? Gastroenterology, 2004. 126(5): p. 1477-80.