Albertisia papuana Becc. TERHADAP
SEL KANKER PAYUDARA DAN SEL KANKER RAHIM
Elizabeth BE Kristiani, Rarastoeti Pratiwi, Ifandari, Puji F Zainal,Laurentius H Nugroho*)
Fakultas Biologi Universitas Gadjah Mada Yogyakarta
E-mail:hartantonugroho2005@yahoo.co.id
Abstract: Ethnobotanical bioprospecting approach widely applied in the discovery of new cancer drugs. Albertisia papuana Becc., an endemic plant in East Kalimantan, Indonesia has been used by Dayak people for cancer drugs. This purpose of this study was to determine the most toxic fraction of the stems and leaves Albertisia papuana Becc. on breast cancer cell lines MCF-7 and cervical cancer cell lines HeLa. Samples macerated using chloroform and methanol. The potent extract and fraction fractionated using VLC and PTLC. The cytotoxicity assay using MTT methods and determination of IC50 (ug / ml) extracts / fractions using SPSS (Probit / logit). The most toxic extract/fraction of stems on MCF-7 cell lines namely BK (181.4 ± 23.2), FB1.5 and FB1.6 (221.8 ± 15.8 and 207.8 ± 19.2) and FB2.4 (43.3 ± 19.7) while on leaves namely DK (155.4 ± 4.4), FD1.2 (525.1 ± 183.7), and FD2.2.6 (382.6 ± 145.5). The most toxic extract/fraction of stems on HeLa cell lines namely BK (63.9 ± 7.9), FB1.5 and FB1.6 (56.3 ± 4.1 and 50.6 ± 6.9), and FB2.14 (127.8 ± 39.8) while on leaves namely DK (166.0 ± 6.9), FD1.4 (394.5 ± 175.6), and FD2.4.1 (48.4 ± 3.8). The most toxic fraction of the stems (FB2.4) and leaves (FD2.4.1) were obtained from two times the potential extract fractionation.
Keywords: Albertisia papuana Becc., extraction, fractination, cytotoxicity
Abstrak: Ethnobotanical bioprospecting approach banyak diterapkan dalam pencarian obat kanker baru. Albertisia papuana Becc., tumbuhan endemik di Kalimantan Timur Indonesia telah digunakan suku Day-ak untuk obat kanker. Penelitian ini bertujuan mendapatkan frDay-aksi paling toksik dari batang dan daun Al-bertisia papuana Becc. terhadap sel kanker payudara MCF-7 dan kanker rahim HeLa. Sampel dimaserasi menggunakan kloroform dan metanol. Fraksinasi menggunakan VLC dan PTLC. Uji sitotoksisitas menggunakan metode MTT dan penentuan IC50 (µg/ml) ekstrak/fraksi menggunakan SPSS (Probit/Logit). Nilai IC50 ekstrak dan fraksi paling toksik terhadap sel MCF-7 pada batang yaitu BK (181,4±23,2), FB1.5 dan FB1.6 (221,8±15,8 dan 207,8±19,2), dan FB2.4 (43,3±19,7); pada daun yaitu DK (155,4±4,4), FD1.2 (525,1±183,7), dan FD2.2.6 (382,6±145,5). sedangkan terhadap sel HeLa pada batang yaitu BK (63,9±7,9), FB1.5 dan FB1.6 (56,3±4,1 dan 50,6±6,9), dan FB2.14 (127,8±39,8); pada daun yaitu DK (166,0±6,9), FD1.4 (394,5±175,6), dan FD2.4.1 (48,4±3,8). Fraksi paling toksik pada batang (FB2.4) dan daun (FD2.4.1) diperoleh dari 2 tahap fraksinasi ekstrak potensial.
Kata kunci: Albertisia papuana Becc, ekstraksi, fraksinasi, sitotoksisitas
Kanker merupakan salah satu penyebab uta-ma keuta-matian di dunia dan menjadi uta-masalah serius bagi masyarakat baik negara maju maupun negara berkembang (Tan dkk., 2014; Jemal dkk., 2011; Islam dkk., 2009). Salah satu usaha menemukan obat kanker adalah dengan eksplorasi tanaman obat yang telah digunakan oleh masyarakat secara tradisional dan diduga memiliki aktivitas anti kanker yang biasa dikenal dengan
ethnobo-tanical bioprospecting approach (Kashani et al., 2012; Samuelsson, 1999).
Tumbuhan mekai (Albertisia papuana Becc.) adalah salah satu tumbuhan endemik di Kalimantan yang dipercaya oleh masayarakat Suku Dayak untuk pengobatan berbagai penyakit degeneratif, hipertensi, dan kanker. Setiap organ (daun, batang, dan akar) mengandung senyawa yang tidak sama, termasuk metabolit sekundernya. Salah satu faktor penting yang mempengaruhi
2 kandungan metabolit sekunder adalah organ tumbuhan.
Studi oleh Widyasari (2012) terhadap sel kanker payudara T47D mendapatkan bahwa nilai IC50 ekstrak kloroform akar
tumbuhan mekai 4,42 μg/mL dengan senya-wa aktif berupa alkaloid. Duffy dkk. (2012) dalam ulasannya menyebutkan A. papuana merupakan tumbuhan yang memiliki ke-mampuan antimalaria dan antikanker. Angerhofer dkk. (1999) menyatakan bahwa alkaloid bisbenzyl-isoquinoline dari A. papuana toksik terhadap sel HeLa. Sejauh
ini belum ditemukan kajian tentang efektivi-tas organ lain tumbuhan mekai terhadap sel kanker payudara dari sel MCF-7 maupun sel kaker rahim HeLa belum diketahui.
Penelitian ini bertujuan untuk mendapatkan fraksi aktif dari batang dan daun tumbuhan mekai (A. pauana Becc) yang bersifat sitotoksik terhadap sel kanker payudara MCF-7 dan sel kanker rahim HeLa. Hasil penelitian ini diharapkan dapat memperkaya pengetahuan ilmiah tentang ak-tivitas antikanker tumbuhan mekai sehingga mendorong upaya penggalian lebih lanjut senyawa bioaktif antikanker utama pada tumbuhan tersebut.
METODE
Tumbuhan Mekai (A. Papuana Becc.) diambil dari daerah Mejug, Kesik, Muara Pedohon, Longsan, Jong, Sungai Pa’it Kabupaten Kutai Kartanegara Propinsi Kalimantan Timur, Indonesia pada bulan Maret 2016. Sel kanker uji (sel kanker payudara MCF-7 dan sel kanker rahim HeLa) diperoleh dari Laboratorium Parasitologi Fakultas Kedokteran Universitas Gadjah Mada Yogyakarta.
Ekstraksi serbuk kering sampel (batang dan daun) secara maserasi menggunakan dua jenia pelaut yaitu kloroform (Merck) dan metanol (Merck). Perendaman sampel selama 48 jam dan diulang 3 kali. Perbandingan sampel dengan pelarut (b/v) yaitu batang 1:4 sedangkan daun 1:14.
Uji sitotoksisitas menggunakan uji MTT (Kristiani dkk., 2016a). Senyawa
3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyl-tetrazoli- umbromide) (MTT) ultra pure (Bio Basic
Canada Inc.). Penentuan nilai IC50
menggunakan program SPSSInc/SPSS16 (Logit/Probit).
Fraksinasi ekstrak potensial menggu-nakan teknik vacuum liquid chromatography (VLC) (Kristiani dkk., 2016b). Setiap fraksi hasil VLC dianalisis dengan kromatografi Lapis Tipis (KLT) dengan fase diam pelat
silica gel GF254 dan fase gerak berupa
campuran heksana : kloroform : etil asetat : etanol (1:1:1:1).
Fraksinasi fraksi potensial menggu-nakan teknil preparative thin layer
chroma-tography (PTLC). Fase diam menggunakan
ini pelat pelat kaca Kieselgel 60F254 dengan
ketebalan 0,25 mm (Merck). Fase gerak campuran pelarut (Merck) yaitu heksana : kloroform : etil asetat : etanol dengan per-bandingan 1:60:10:5.
HASIL
Bagian organ tumbuhan mekai yang digunakan sebagai sampel adalah batang dan daun (Gambar 1).
Gambar 1. Tumbuhan Mekai (Albertisia
papuana Becc.). A. Tumbuhan
Mekai; B. Batang Mekai; C. Daun Mekai
Besarnya kemampuan sitotosisitas dapat dilihat dari nilai IC50 ekstrak terhadap sel uji.
Berdasarkan Tabel 1 tampak bahwa ekstrak dengan pelarut kloroform menunjukkan sifat
3 toksik lebih kuat dibandingkan ekstrak dengan pelarut metanol terhadap kedua sel uji. Nilai IC50 sitotoksik ekstrak tersebut
(kisaran 50-150 µg/ml) masih dibawah ke-mampuan doxorubicin (8,6 µg/ml terhadap sel MCF-7 dan 1,0 µg/ml terhadap sel HeLa). Ekstrak metanol menunjukkan nilai IC50 pada kisaran 200-750 µg/ml.
Tabel 1. Nilai IC50 ekstrak batang dan daun A. papuana Becc.
Organ Kode Nilai IC50 (µg/ml) terhadap sel MCF-7 HeLa Dx 8,6 ± 0,2 1,0 ± 0,9 Batang BK 181,3 ± 23,2 63,9 ± 7,9 BM 202,4 ± 13,3 214,2 ± 4,5 Daun DK 155,4 ± 4,4 165,5 ± 6,9 DM 383,4 ± 34,0 763,4 ± 107,9
Gambar 2. Kromatogram KLT hasil VLC ekstrak potensial batang dan daun A.
papuana Becc. A. Batang (BK); B. Daun (DK)
Ekstrak potensial BK dan DK difraksinasi menggunakan metode VLC dan diperoleh 17 fraksi. Analisis KLT pada setiap fraksi dan penggabungan fraksi yang menunjukkan po-la pemisahan mirip ditampilkan pada Gam-bar 2. Fraksi batang menjadi sembilan fraksi gabungan sedangkan daun menjadi empat fraksi gabungan (Tabel 2 dan Tabel 3).
Tabel 2. Penggabungan fraksi hasil VLC ekstrak kloroform batang A.
papuana Becc.
Fraksi gabungan Pelarut Fraksi
asal F1.B1 H:K = 9:1 1 – 2 F1.B2 H:K = 1:1 3 – 4 F1.B3 H:K = 1:4 5 F1.B4 K:EA = 3:2 6 – 7 F1.B5 K:EA = 2:3 8 – 10 F1.B6 EA = 1 11 F1.B7 EA:E = 7:3 12 – 13 F1.B8 EA:E = 1:4 14 – 16 F1.B9 A 17
Tabel 3. Penggabungan fraksi hasil VLC ekstrak kloroform daun A. papuana Becc.
Fraksi gabungan Pelarut Fraksi
asal F1.D1 H:K = 7:3 1 – 4 F1.D2 H:K:EA:E = 1:19:22:3 5 – 13 F1.D3 EA:E = 3:7 14 – 15 F1.D4 E:A = 1:1 16 – 17
Uji sitotoksisitas terhadap kedua sel uji dilakukan terhadap fraksi gabungan dari hasil VLC terhadap BK dan DK (Tabel 4 dan Tabel 5). F1.B5 dan F1.B6 menunjukkan aktivitas sitotoksik mirip yaitu nilai IC50
(µg/ml) berturut-turut 221,8 dan 207,8 terhadap sel MCF-7 sedangkan terhadap sel HeLa 56,3 dan 50,6. Fraksi lain tidak mempunyai kemampuan sitotoksik terhadap sel MCF-7 (semua sel hidup pada semua konsentrasi uji) sedangkan terhadap sel HeLa F1.B7 dan F1.B8 nilai IC50 pada
2 Tabel 4. Nilai IC50 fraksi hasil VLC
ekstrak kloroform batang A.
papuana Becc.
Fraksi Nilai IC50 (µg/ml) terhadap sel
MCF-7 HeLa F1.B1 NT NT F1.B2 NT NT F1.B3 NT NT F1.B4 NT 6.057,0 ± 7.347,8 F1.B5 221,8 ± 15,8 56,3 ± 4,1 F1.B6 207,8 ± 19,2 50,6 ± 6,9 F1.B7 NT 11,9 ± 12,7 F1.B8 NT 107,9 ± 15,1 F1.B9 NT NT
Catatan: NT (Not detected) = Tidak ada ke-matian sel uji
Tabel 5. Nilai IC50 fraksi hasil VLC ekstrak kloroform daun A. papuana Becc.
Fraksi Nilai IC50 (µg/ml) terhadap sel
MCF-7 HeLa
F1.D1 NT 464,6 ± 98,5
F1.D2 525,1 ± 183,7 3.841,0 ± 5.765,8
F1.D3 NT 394,5 ± 175,6
F1.D4 NT 166,0 ± 6,9
Catatan: NT (No toxicity) = Tidak ada kema-tian sel uji
Sitotoksisitas F1.B4 sangat lemah yaitu IC50 6.057,0 µg/ml, dan ketiga fraksi lainnya
(F1.B1-F1.B3) tidak toksik.
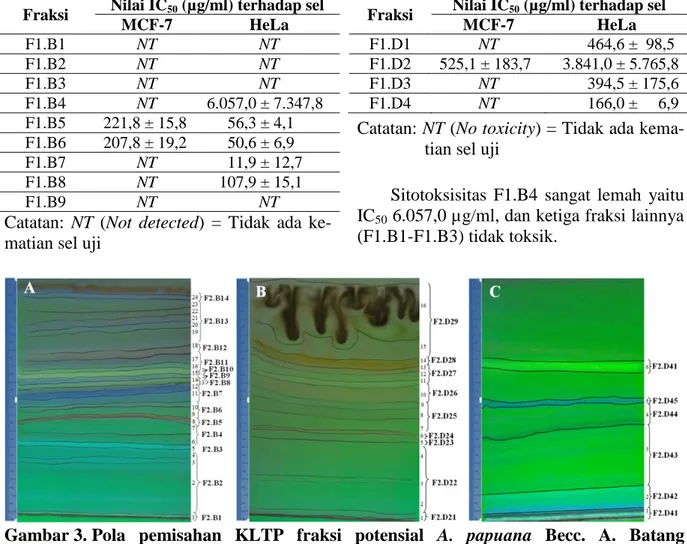
Gambar 3. Pola pemisahan KLTP fraksi potensial A. papuana Becc. A. Batang (F1.B5+F1.B6); B. Daun (F1.D2)
Pada uji terhadap sel MCF-7, hanya ada satu ekstrak yang menunjukkan sifat toksik yaitu F1.D2 (nilai IC50 525,1 µg/ml). Uji
terhadap sel HeLa, menunjukkan bahwa keempat fraksi masih bersifat toksik yaitu F1.D4 paling toksik (nilai IC50 166,0 µg/ml),
F1.D1 dan F1.D3 (nilai IC50 ± 400 µg/ml),
dan F1.D2 paling lemah toksisitasnya (nilai IC50 3.841 µg/ml).
Tahap berikutnya adalah fraksinasi II fraksi paling toksik hasil VLC yaitu gabun-gan F1.B5 dengabun-gan F1.B6 dan F1.D4 menggunakan teknik PTLC. Pita pemisahan yang mirip digabungkan, sehingga diperoleh 14 fraksi pada gabungan F1.B5 dan F1.B6, 9 fraksi pada F1.D2, dan 6 fraksi dari F1.D4 seperti yang ditampilkan pada Gambar 3.
Tabel 6. Nilai IC50 fraksi hasil PTLC batang A. papuana Becc.
Fraksi Nilai IC50 (µg/ml) MCF-7 HeLa F2.B1 133,3 ± 54,7 1.067,8 ± 372,5 F2.B2 ND 525,0 ± 64,9 F2.B3 435,4 ± 482,1 390,0 ± 59,1 F2.B4 43,3 ± 19,7 > 10.000 F2.B5 57,7 ± 30,5 2.868,9 ± 2.653,0 F2.B6 547,0 ± 720,0 654,8 ± 112,6 F2.B7 344,8 ± 229,8 454,5 ± 112,6 F2.B8 1.273,6 ± 709,3 375,4 ± 106,2 F2.B9 3.616,7 ± 1.497,8 204,1 ± 15,4 F2.B10 2.881,0 ± 2.370,4 412,1 ± 267,7 F2.B11 1.923,0 ± 505,3 239,2 ± 16,6 F2.B12 > 10.000 503,8 ± 476,0 F2.B13 5.829,4 ± 337,7 285,0 ± 89,6 F2.B14 5.312,6 ± 2.824,3 127,8 ± 39,8
2 Semua fraksi diuji sitotoksisitasnya ter-hadap sel MCF-7 dan sel HeLa (Tabel 6 dan Tabel 7). Fraksinasi II ekstrak batang A.
papuana Becc. menghasilkan fraksi dengan
toksisitas lebih kuat terhadap MCF-7 dari fraksi paling toksik hasil fraksinasi I yaitu F2.B4 dengan nilai IC50 43,3 µg/ml. Fraksi
F2.B1-F2.B7 menunjukkan nilai IC50
berkisar 100-500 µg/ml sedangkan fraksi F1.8-F1.B14 menunjukkan nilai IC50 lebih
dari 1.000 µg/ml. Pada sel Hela, sitotoksisitas semua fraksi hasil fraksinasi II lebih rendah (nilai IC50 pada kisaran 100-500
µg/ml) dibandingkan fraksi paling toksik hasil fraksinasi I.
Tabel 7. Nilai IC50 fraksi hasil PTLC daun
A. papuana Becc. Fraksi Nilai IC50 (µg/ml) MCF-7 HeLa F2.D21 709,4 ± 61,0 F2.D22 601,6 ± 88,0 F2.D23 708,2 ± 10,9 F2.D24 721,5 ± 74,3 F2.D25 641,4 ± 116,4 F2.D26 382,6 ± 145,5 F2.D27 443,0 ± 249,0 F2.D28 475,0 ± 160,9 F2.D29 414,0 ± 216,6 F2.D210 401,8 ± 211,2 F2.D41 48,4 ± 3,8 F2.D42 82,3 ± 3,0 F2.D43 89,4 ± 3,5 F2.D44 88,7 ± 0,6 F2.D45 383,6 ± 75,0 F2.D46 611,5 ± 33,3
Pada daun, proses fraksinasi II menghasilkan fraksi dengan sitotoksisitas lebih kuat dibandingkan fraksi potensial hasil fraksinasi I yaitu F2.D26 (nilai IC50 382,6 µg/ml
terhadap sel MCF-7) dan F2.D41 (nilai IC50
48,4 µg/ml terhadap sel HeLa). Sitotoksisitas F2.D26 terhadap sel MCF-7 tersebut walaupun paling toksik dalam tahap fraksinasi II tetapi lebih rendah dari ekstrak sebelum difarksinasi. Dengan demikian, ekstrak awal daun merupakan agen paling toksik terhadap sel MCF-7.
PEMBAHASAN
Saat ini banyak dilakukan upaya pencarian obat baru bersumber dari bahan alam yang dikenal Bioassay-Guided Isolation. Bioassay-Guided Isolation
merupakan serangkaian langkah pemisahan senyawa dalam campuran menggunakan metode analitik dan uji farmakologinya. Proses tersebut diulang sampai diperoleh senyawa aktif yang diharapkan (Rimando et
al., 2001; Samuelsson, 1999).
Masyarakat suku Dayak biasa menggunakan akar Mekai untuk obat kanker. Penggunaan akar akan membuat keseluruhan tumbuhan menjadi mati. Oleh karena itu pa-da penelitian ini, selain akar juga diteliti or-gan batang daun, denor-gan tujuan untuk mengetahui kemungkinan kemampuan si-totoksik dua organ tersebut. Katno dan Purnomo (2002) menyatakan bahwa se-bagian besar senyawa kimia yang di-manfaatkan dalam obat pada tumbuhan adalah metabolit sekunder. Kemungkinan pada daun dan batang juga terdapat senyawa yang memilki kemampuan sitotoksik karena metabolit sekunder tersebar terbatas dalam organisme, kelompok organisme (Dewick, 2002), atau bagian tubuh dalam satu individu (Shrikumar dan Ravi, 2007).
Pada penelitian ini, tahap awal sampel diekstraksi kemudian diuji sitotoksisitasnya. Ekstraksi merupakan proses awal dalam proses pemisahan senyawa di dalam suatu bahan (Sticher, 2008). Pada proses ekstraksi, bagian aktif di dalam tumbuhan dipisahkan menggunakan pelarut spesifik (Azwanida, 2015). Secara umum proses ekstraksi meli-puti pengeringan sampel, penggerusan sam-pel, pemilihan prosedur ekstraksi, dan pem-ilihan pelarut sesuai dengan bahan yang akan diisolasi (Samuelsson, 1999; Kashani et al., 2012, Azwanida, 2015). Metode maserasi, yang digunakan dalam penelitian memiliki kelebihan yaitu perendaman pada suhu ruang mengurangi kemungkinan proses dekompo-sisi senyawa yang terekstrak, namun metode ini juga memiliki kekurangan dalam hal waktu yang lama dan kebutuhan pelarut yang banyak. (Kashani et al., 2012; Sticher, 2008).
3 Skrining sitotoksisitas in vitro merupa-kan strategi yang cocok sebagai studi awal untuk menyeleksi adanya aktivitas anti-kanker suatu ekstrak tumbuhan (Arullappan
et al. 2013). Ekstrak dengan pelarut
kloro-form menunjukkan sitotoksisitas lebih tinggi dibandingkan dengan metanol. Kemampuan farmakologi obat herbal dipengaruhi oleh keberadaan senyawa bioaktif senyawa me-tabolit sekunder di dalamnya (Arullappan et
al., 2013; Prakash & Gupta, 2013; Almehdar et al. 2012; Kashani et al., 2012). Jenis
sen-yawa metabolit sekunder yang diperoleh ditentukan oleh pelarut yang digunakan da-lam proses ekstraksi. Penggunaan kloroform dapat mengekstrak senyawa non polar seper-ti asam lemak dan terpena (Cowan, 1999) dan sedikit tannin (Azwanida, 2015).
Crude extract masih berupa campuran
kompleks berbagai jenis senyawa yang mungkin dapat bersifat sinergis ataupun antagonis dalam peran farmakologisnya. Fraksinasi secara kromatografi merupakan salah satu pendekatan untuk memisahkan kompleksitas senyawa tersebut menjadi beberapa fraksi dengan jenis senyawa lebih terkonsentrasi sesuai dengan pelarutnya (Nwodo et al., 2010).
Sesuai dengan Bioassay-Guided
Iso-lation, ekstrak potensial difraksinasi, kemudian sitotoksisitas setiap fraksi diuji kembali. Pada batang, fraksi paling toksik adalah gabungan F1.B5 dan F1.B6 dengan nilai IC50 pada kisaran 200 µg/ml terhadap
sel MCF-7 dan 50 µg/ml terhadap sel HeLa. Proses fraksinasi I ini menurunkan sitotok-sisitas terhadap MCF-7 tetapi terhadap sel HeLa meningkat. Pada daun, kedua fraksi tidak meningkatkan sitotoksisitas terhadap kedua sel uji. Penurunan sitotoksisitas kemungkinan disebabkan ada senyawa pada fraksi tersebut yang bersifat antagonis ter-hadap sifat sel uji yang bersangkutan. Fraksi tersebut merupakan fraksi dengan pelarut kloroform : etil asetat (3:7). Hal tersebut menunjukkan bahwa senyawa bioaktif lebih cenderung merupakan senyawa dengan ke-cenderungan polar.
Fraksinasi II menggunakan teknik PTLC. Prosedur PTLC mempunyai kelebihan dalam
hal peralatan sederhana dan biaya murah tetapi memiliki kelemahan dalam hal jumlah sampel yang bisa diproses hanya sedikit se-hingga perolehan rendemen akhir sedikit (Kristanti, 2008). Sampai saat ini, prosedur ini dapat manjadi prosedur alternatif apabila jumlah sampel sedikit yang tidak memung-kinkan untuk di VLC. Berdasarkan pemisa-han pada kromatogram, tampak bahwa kan-dungan senyawa pada batang lebih beragam dibandingkan pada daun. Hasil uji sitotoksis-itas pada batang, F2.B4 sangat toksik ter-hadap sel MCF-7 (nilai IC50 43,3 µg/ml)
tetapi terhadap sel HeLa sitotoksisitas semua fraski menurun. Kondisi sebaliknya terjadi pada fraksi daun. Sitotoksisitas fraksi F2.D41 terhadap sel HeLa meingkat dengan nilai IC50 48,4 µg/ml. Dalam Syarifah dkk.
(2011), suatu bahan disebut memiliki kekuatan sitotoksik moderat jika nilai IC50 antara 10-50 µg/ml.
Studi oleh Widyasari (2012) mendapat-kan bahwa ekstrak kloroform akar tumbuhan mekai bersifat sitotoksik terhadap sel kanker payudara (T47D) dengan IC50 4,42 μg/mL.
Hasil penelitian ini menunjukkan bahwa sifat sitotoksisitas ekstrak batang dan daun lebih rendah dari akar, tetapi proses fraksinasi memungkinkan diperolehnya fraksi dengan kekuatan sitotoksisitas sepadan dengan akar.
Sampai dengan proses fraksinasi II, ak-tivitas sitotoksik ektrak atau fraksi potensial di bawah kemampuan doxorubicin (nilai IC50
8,6 µg/ml terhadap sel MCF-7 dan 1,0 µg/ml terhadap sel HeLa. Hal tersebut kemung-kinan karena ekstrak/fraksi masih merupakan campuran senyawa yang mungkin ada sifar sinergis dan antagonis didalamnya.
KESIMPULAN DAN SARAN Kesimpulan
Fraksi paling toksik terhadap sel kanker payudara MCF-7 dari tumbuhan Mekai (A.
papuana Becc.) yaitu dari batang F2.B4
(nilai IC50 43,3 µg/ml), dan dari daun (nilai
IC50 165,5 µg/ml). Fraksi paling toksik
terhadap sel kanker rahim HeLa yaitu dari batang F1.B5 (nilai IC50 56,3 µg/ml) dan
F1.B6 (nilai IC50 50,6 µg/ml), dan dari daun
4 Saran
Perlu dilakukan kajian lebih lanjut meliputi uji sitotoksisitas fraksi paling toksik terhadap sel kanker lain, sel normal, dan pendalaman mekanisme antikanker dari farski potensial
DAFTAR RUJUKAN
Angerhofer, C.K., Guinaudeau, H., Wongpanich, V., Pezzuto, J.M., Cordell, G.A. 1999. Antiplasmodial and cytotoxic activity of natural bisbenzylisoquinoline alkaloids. J. Nat.
Prod. 62 : 59-66.
Arullappan, S. et al. 2013. Cytotoxic Activity of the Leaves and Stem Extracts of Hibiscus rosa sinensis
(Malvaceae) against Leukaemic Cell
Line (K-562). Tropical Journal of
Pharmaceutical Research. 12 (5):
743-746.
Azwanida, N.N. 2015. A Review on the Extraction Methods Use in Medicinal Plants, Principle, Strength and Limit-ation. Med Aromat Plants. 4: 196.
doi:10.4172/2167-0412.1000196
Cowan M.M. 1999. Plant Products as Antimicrobial Agents. Clinical
Micro-biology Review. Vol. 12 No. 4:
564-582.
Dewick, P.M. 2002. Medicinal Natural
Products: A Biosynthetic Approach.
2th edition. John Wiley dan Sons. New York. 507 p.
Duffy, R., Wade, C., Chang, R. 2012. Discovery of anticancer drugs from antimalarial natural products: a MEDLINE literature review. Drug
Discovery Today. 17 (17/18): 942-953.
Islam, M.S., Akhtar, M.M., Rahman, M.M. 2009. Antitumor and phytotoxic activities of leaves metahanol extract of
Oldenlandia diffusa (Willd.) Roxb. Global Journal of PharmacologyI. 3
(2): 99-106.
Jemal A, Bray F, Center MM, Ferlay J, Ward E, et al. 2011. Global Cancer statistic. CA Cancer J CLin. Doi:10.3322/ caac.20107.
Katno, S. dan Pramono, S. 2002. Tingkat
Manfaat dan Keamanan Obat Tradisional. Balai Penelitian Tanaman Obat Tawanmangu. www.litbang. depkes.go.id. Akses tanggal 7 Juli 2010.
Kashani, H.H., Hoseini, E.S., Nikzad, H., Aarabi, M.H. 2012. Pharmacological properties of medicinal herbs by focus on secondary metabolites. Life Science
Journal. 9 (1) : 509-520.
Kristanti, A.N. 2008. Buku Ajar Fitokimia. Airlangga University Press, Surabaya. Kristiani, E.B.E., Nugroho, L.H.,
Moel-jopawiro, S., Widyarini, S. 2016b. Characterization of volatile compounds of Albertisia papuana Becc root extracts and cytotoxic activity in breast cancer cell line T47D. Tropical
Journal of Pharmaceutical Research.
15 (5): 959-964.
. 2016b. The Cytotoxicity of Mekai (Albertisia papuana Becc.) Root Extract on Breast Cancer Cell Lines T47D and Vero Cell Lines. AIP
Conference Proceedings. 1744, 020016: 1-8; doi: 10.1063/ 1.4953490. Nwodo, U.U., Ngene, A.A., Iroegbu, C.U.,
Obiiyeke GC. 2010. Effects of fractionation on antibacterial activity of crude extracts of Tamarindus indica.
African Journal of Biotechnology
9(42): 7108-7113.
Prakash E & Gupta D.K. 2013. In Vitro Study of Extracts of Ricinus communis Linn on Human Cancer Cell lines.
Journal of Medical Sciences and Public Health. Vol. 2, No. 1, 15-20.
Rimando, A. M., Olofsdotter, M.S.O.D., Dayan, F.E. 2001. Searching for rice allelochemicals: an example of bioassay-guided isolation. Agron. J. 93:16–20.
Samuelsson, G. 1999. Drugs of Natural
Origin: A Textbook of Pharmacognosy,
4th ed., Swedish Pharmaceutical Society, Stockholm, 551p.
Shrikumar, S., and Ravi, T.K. 2007. Approaches Towards Development and Promotion of Herbal Drugs.
Pharma-5
cognosy Reviews. 1 (1): 180-184.
Sticher, O. 2008. Natural product isolation.
Natural Product Reports. 25 : 517-554.
Syarifah, M.M.S., Nurhanan, M.Y., Haffiz, J.M., Ilham, A.M., Getha, K., Asiah, O., Norhayati, I., Sahira, H.L., Suryani, S.A. 2011. Potential Anticancer Compound from Cerbera odollam.
Journal of Tropical Forest Science. 23
(1): 89-96.
Tan, K.K., Bradshaw, T.D., Jessica C, Jin K.T., Christope W. 2014. In Vitro Anticancer Effect Of Artabotrys Crassifolius Hook.F. & Thomson Against Human Carcinoma Cell Lines.
Journal of Drug Delivery & Thera-peutics. 4(1), 1-4.
Widyasari. 2012. Efek Sitotoksik, Proliferasi, dan Apoptosis Fraksi Aktif Akar Tumbuhan Mekai (Albertisia
papuana Becc.) Terhadap Sel Kanker
Payudara (T47D). Thesis. Yogyakarta: Program Pasca Sarjana Fakultas Biologi Universitas Gadjah Mada Yogyakarta.