Dedi Ardinata
Departemen Fisiologi, Fakultas Kedokteran Universitas Sumatera Utara
Abstrak: Asma merupakan gangguan inflamasi kronik pada sistem pernafasan. Terjadi inflamasi yang khas karena disertai infiltrasi eosinofil, hal ini membedakan asma dari gangguan inflamasi jalan napas lainnya. Eosinofil merupakan mediator inflamasi utama pada asma. Eosinofil merangsang produksi mediator inflamasi, sitokin dan mediator. Pemahaman efek eosinofil menjadi dasar terapi asma, yaitu dengan menghambat sitokin, eosinofil dan menghambat interaksi
antara eosinofil dan sel endotel.Selain itu menjadi dasar pengembangan modalitas terapi asma
seperti Cyklophilin, Antibodi monoklonal antihuman IL-5, Anti Interleukin-1, Interleukin 10, Interleukin 12 dan Antihistamin. Pengetahuan ini memberi pemahaman mekanisme obat yang lazim digunakan seperti Glucocorticoid dan Anti leukotrine.
Kata kunci: Asma, eosinofil
Abstract: Asthma is chronic inflammation involving the respiratory system. This special inflammation is cause by Eosinophils infiltration, at this point asthma difference from other air tract inflammation. Eosinophils is the main inflammation mediator on asthma. Eoinophils stimulate inflammation mediator production, cytokines and lipid mediator. Understanding the effect of eosinophils become basic of asthma therapy, by inhibit cytokines, eosinophils and inhibit the interaction between eosinophils and endothelial cell. Then, its become basis of developing agent of asthma therapy like Cyklophilin, Antibodi monoklonal antihuman IL-5, Anti Interleukin-1, Interleukin 10, Interleukin 12 and Antihistamin. This knowledge lead to understanding of usual use drugs mechanisms like Glucocorticoid and Anti leukotrine.
Keywords: Asthma, eosinofil
PENDAHULUAN
Asma adalah penyakit saluran nafas kronis yang penting dan merupakan masalah kesehatan masyarakat yang serius diberbagai negara diseluruh dunia.1
Meskipun penyakit ini bukan merupakan penyebab kematian yang utama tetapi penyakit ini mempunyai dampak sosial yang cukup besar terhadap produktifitas kerja dan kehilangan angka sekolah yang tinggi serta angka kejadiannya meningkat terus dari waktu kewaktu.1.2
Asma dapat terjadi pada segala usia dengan menifestasi yang sangat bervariasi dan berbeda-beda antara satu individu dengan individu lainnya.3
Prevalensi asma pada anak-anak bervariasi antara 0-30%, sedangkan pada dewasa secara umum berdasarkan beberapa survei sekitar 6% pada beberapa negara yang berbeda.4
Di Indonesia berdasarkan Survei Kesehatan Rumah Tangga (SKRT) tahun 1992, asma, bronkhitis kronis dan emfisiema merupakan penyebab kematian ke-4 di
Indonesia atau sebesar 5.6%. Pada tahun 1995, prevalensi asma diseluruh Indonesia sebesar 13 dari 1000 penderita.1
Asma adalah gangguan inflamasi kronik saluran nafas yang melibatkan banyak sel dan elemennya. Inflamasi yang terjadi pada asma adalah inflamasi yang khas yaitu inflamasi yang disertai infiltrasi eosinofil, hal ini yang membedakan asma dari gangguan inflamasi jalan napas lainnya. Eosinofil merupakan inflamasi utama pada asma,5
terbukti setelah inhalasi dengan allergen didapatkan peningkatan eosinofil pada cairan kurasan bronkoalveolar (BAL) pada saat reaksi asma lambat yang disertai dengan inflamasi.5,6,7
Karena pentingnya peranan sel-sel inflamasi terutama sel eosinofil didalam mencetuskan simptoms asma, maka pada tulisan ini akan dibicarakan tentang peranan eosinofil pada asma dan aspek patogenesanya serta pendekatan terapi.
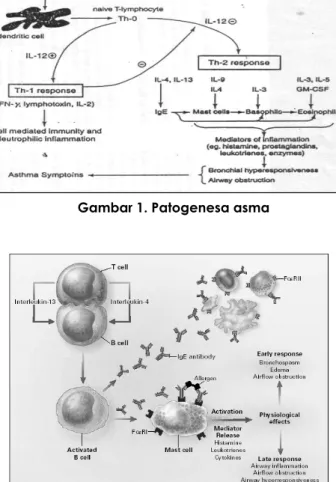
Imunitas humoral ditandai oleh produksi dan sekresi antibodi spesifik sel limfosit B. Sedangkan imunitas seluler diperankan oleh limfosit T. Sel limfosit T mengontrol fungsi Limfosit B dan meningkatkan proses inflamasi melalui aktivitas sitotoksin cluster diffrentiation 8 (CD8) dan mensekresikan berbagai sitokin. Sel limfosit T helper (CD4) dibedakan menjadi Th1 dan Th2. Sel Th1 mensekresi interleukin-2 (IL-2), IL-3,
granulocytet monocyte colony stimulating
factor (GMCSF), interferon y (IFN-y) dan
tumor necrosis factor-a (TNF-a). Sedangkan
Th2 mensekresi IL-3, IL-4, IL-5, IL-9, IL-13 dan GMCSF.4,5,9
(Gambar 1)
Gambar 1. Patogenesa asma
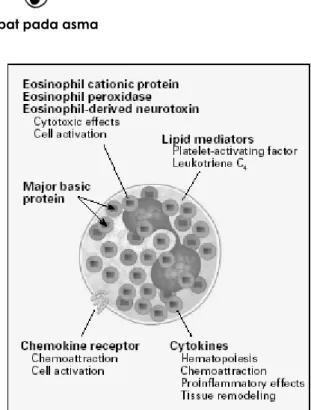
Gambar 2. Reaksi ”early onset” pada asma
profil Th2.4,5
Subtipe Th2 ini merupakan subtipe utama yang terlibat pada asma, mensekresi berbagai sitokine yang bertanggung jawab bagi berkembangnya reaksi
tipe lambat atau cell- mediated
hypersensitivity reaction.4
Rangsangan interleukin 4 dan interleukin
13 dari Th2, akan memacu sel limfosit B untuk mensintesa IgE. IgE akan dilepas limfosit B dan melekat pada high affiniting IgE reseptors (FceRI) pada permukaan sel mast. Bila alergen yang sama masuk lagi maka akan diikat oleh IgE dipermukaan sel mast. Cross Linked Reseptor IgE dengan alergen akan mengaktifkan sel mast yang menyebabkan degranulasi sel mast sehingga terjadi pelepasan perfomed mediator seperti histamin serta
newly generated modiator antara lain:
prostaglandin, leukotrin yang menyebabkan terjadinya kontraksi otot polos bronkus, sekresi mukus, vasodilitasi. Mediator inflamasi menginduksi kebocoran mikrovaskuler yang melibatkan eksudasi plasma kedalam saluran napas. Kebocoran plasma protein menginduksi penebalan dan edema dinding saluran napas yang menyebabkan penyempitan lumen saluran napas, sehingga menyebabkan kontraksi otot pernapasan dan reaksi ini berlangsung selama 1-2 jam. Reaksi ini disebut
”early onset” pada asma (Gambar 2).2
Degranulasi sel mast juga menghasilkan sejumlah sitokin a.l. IL-4,IL-5, IL-6,IL-13 dan TNF- a.4,5,9.10
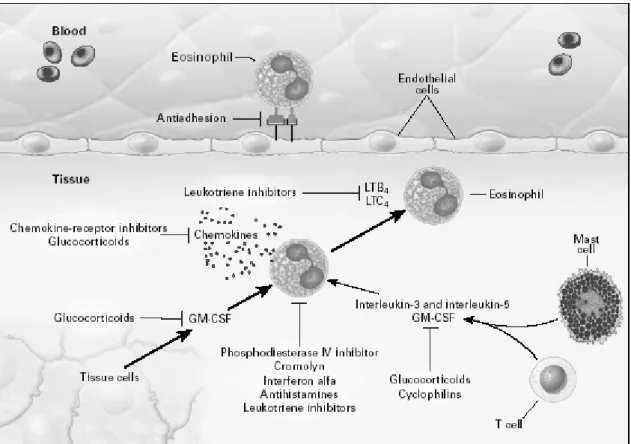
Degranulasi sel mast beserta limfosit T subtipe Th2 akan menggerakkan dan mengaktifkan sel-sel inflamasi eosinofil, basofil, neutrofil dan magrofage, melalui aktivitas sel endotel yang akan menyebabkan pembentukan molekul adhesi. Reaksi ini akan terjadi pada 4-8 jam setelah reaksi pertama dan menyebabkan kedatangan sel-sel radang sehingga meningkatkan pelepasan mediator. Reaksi ini disebut reaksi tipe lambat.4,5,9
Gambar 3. Reaksi lambat pada asma
EOSINOFIL
Pada orang normal, kadar eosinofil hanya sebagian kecil dari lekosit darah perifer dan keberadaannya di jaringan terbatas. Pada penyakit tertentu, eosinofil dapat berakumulasi pada darah tepi atau jaringan tubuh. Gangguan yang menyebabkan eosinofilia didefinisikan sebagai akumulasi abnormal eosinofil dalam darah atau jaringan sehingga menimbulkan gejala klinis.5,10,11
Normalnya kadar eosinofil hanya 1-3 % dari lekosit darah tepi, dan batas dari rentang
nilai normal adalah 350 sel/mm3
darah. Eosinofil diklasifikasikan ringan (351-1500 sel/mm3), sedang (>1500-5000 sel/mm3) atau berat (>5000 sel/mm3).11
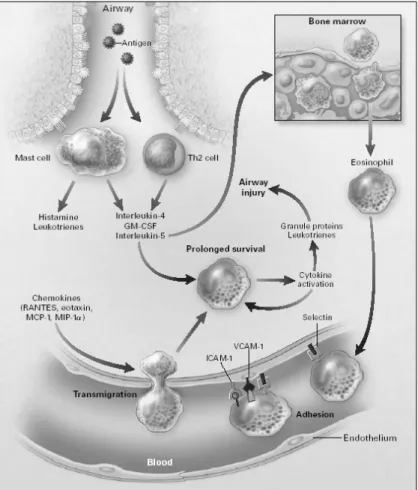
Eosinofil memproduksi mediator toksin inflamatori yang unik yang disimpan dalam granul-granul dan disintetis setelah sel ini teraktivasi, granul tersebut mengandung kristaloid yang terdiri dari Major Basic Protein
(MBP) dan matrix yang terdiri dari Eosinophil
Cationic Protein (ECP), peroxidase eosinofil
dan Eosinophil Derived Neurotoxin (EDN)
yang mengandung efek sitotoksin pada epitelium repiratori. Eosinofil juga menghasilkan berbagai sitokin yang sebagian disimpan didalam granul dan mediator lipid yang dihasikan setelah sel ini teraktivasi, antara lain rantes, eotaxin dan platelet activating faktor yang berperan mempercepat migrasi eosinofil.5,7.9,10
(Gambar 4) Eosinofil terjadi melalui 4 proses:
− diffrensiasi sel-sel progenitor dan proliferasi eosinofil pada sumsum tulang − intaraksi antara eosinofil dan sel endotel,
termasuk: rolling, adhesi dan migrasi eosinofil
− rangsangan kimia yang menarik eosinofil ke lokasi tertentu dan
− aktivasi serta destruksi eosinofil
Gambar 4. Gambaran fisiologi eosinofil
Eosinofil diproduksi oleh sel progenitor dalam sumsum tulang. Tiga sitokin yakni
interleukin-3, IL-5 dan granulocyte
macrophage colony stimulating faktor
(GH-CSF) adalah bagian penting dalam mengatur perkembangan eosinofil. IL-5 adalah spesifik untuk “eosinofil Lineage” dan bertanggung jawab terhadap diffrensiasi eosinofil, menstimulasi pelepasan eosinofil dari sumsum tulang ke dalam sirkulasi perifer.5,10,11
Eosinofil di sirkulasi akan berputar (rolling) pada endothelium yang di perantarai oleh E- Selectin. Kemudian terjadi perlengketan (adhesion) antara eosinofil dan sel endothelial yang di perantarai oleh perlengketan molekul-molekul pada sel endothelial dan ”counter –ligand” pada eosinofil. Perlengketan (adhesion) ini melalui perlengketan molekul-molekul dengan kelompok integrin dari eosinofil, yakni kelompok CD-18 (B2 Integrin) dan molekul
induksi oleh berbagai mediator inflamasi antara lain: interleukin 1 dan TNF-a sedangkan VCAM-1 di induksi oleh interleukeukin 4, kemudian esinofil bermigrasi kedalam jaringan yang diperankan oleh
molekul-molekul chemoattractant lokal
seperti leukotrin B4, mediator–mediator lipid, interleukin, dan berbagai chemokines. Dari ke semua subtansi yang relatif spesifik untuk eosinofil adalah eotaxin-1 dan eotaxin-2 dan efeknya dipertinggi oleh interleukin -5. Eosinofil dapat hidup dan bertahan di jaringan dalam jangka waktu lama (sampai berminggu-minggu) bergantung pada sitokin micro lingkungan (micro enviroment). Sitokin IL-3,
MBP, ECP, EDN sehingga terjadi kerusakan epitel saluran nafas. Major basic protein secara langsung meningkatkan reaktifasi obat polos dan merangsang degranulasi sel mast dan basofil.5,10,11
Remodeling merupakan reaksi tubuh untuk memperbaiki jaringan yang rusak akibat inflamasi dan diduga menyebabkan perubahan ireversibel pada asma. Fibroblas berperan penting dalan remodeling dan proses inflamasi. Fibroblas menghasilkan kalogen, serat elastik dan retikuler, proteoglikans dan glikoprotein dari matriks ekstraselular (ECM).5,7.9
Gambar 5. Diffrensiasi eosinofil, menstimulasi pelepasan eosinofil dari sumsum tulang ke dalam sirkulasi perifer
Gambar 6. Faktor mediator maupun sitokin yang berperan pada proses asma
PENDEKATAN TERAPI
Pengobatan asma dengan dasar mempelajari faktor mediator maupun sitokin yang berperan pada proses asma, saat ini sedang dalam tahap pengembangan yang intensip. Dalam hal peranan eosinofil pada asma, pendekatan terapi didasarkan pada penghambatan sitokin, eosinofil, dan menghambat interaksi antara eosinofil dan sel endothelial.10,11
(Gambar 6)
Glucocorticoid. Obat ini merupakan agen
paling efektif untuk mereduksi/mengurangi eosinofil, menekan trankripsi sejumlah gen mediator inflamasi, obat ini dapat menghambat produksi IL -1 sehingga menghilangkan ekpresi E-selektion dan ICAM-1 dari stimulasi endotel oleh zat tersebut. Saat ini kortikosteroid merupakan obat lini pertama dalam dalam pengobatan reaksi inflamasi pada asma.10,11,12
Cyklophilin. (Cyclosporine) Obat ini
dilaporkan dapat memblokade transkripsi dari eosinophil - active cytokines separti IL-5 dan GM-CSF. 11
Antihistamin. Cetirizine (CTR) obat anti
H1 dari generasi kedua obat antihistamin dilaporkan dapat menginhibisi ekspresi ICAM -1.11,13
Antibodi monoklonal antihuman IL-5.
Menghambat interaksi IL-5 beserta reseptor-reseptornya.
Anti leukotrine. (Zileuton, zafirlukas),
menghambat sintesa leukotrine dan menghambat pembentukan leukotrine B4 dan leukotrine C4,D4 dan E4. (11,13,14)
Interleukin 10. Pemberian IL -10 dapat
menghambat produksi TNF- a yang dapat mengaktivitas ekspresi ICAM-1 oleh endotel.13
Anti Interleukin-1. Dapat menghambat
IL-1 sehingga menghambat aktivasi endotel untuk menghasilkan ICAM-1. 13
Pemberian IL -12 dapat menghambat produksi IL-4 yang mengaktivitas endotel untuk menghasilkan VICAM. IL -12 juga menghambat produksi IL-5 yang berperan pada proses eosinophilia. 11,13
KESIMPULAN
− Asma merupakan suatu sindroma yang sangat kompleks melibatkan faktor genetik, antigen, berbagai sel inflamasi, mediator dan sitokin yang akan menyebabkan kontraksi otot jalan napas, hiperaktivitas bronkus dan inflamasi jalan napas.
− Saat ini sedang dikembangkan pendekatan terapi asma yang mempengaruhi sitokin yang berperan pada asma.
DAFTAR PUSTAKA
1. PDPI. ASMA. Dalam: Pedoman Diagnosis dan Penatalaksanaan di Indonesia, Balai Penerbit FK UI, Jakarta, 2004; 1-19. 2. Yunus F. Terapi Controller Pada Asma.
Dalam: Margono BP, Widjaja A, Amin M,dkk (editor). Pertemuan Ilmiah Paru Millenium, Surabaya,2002;1-7.
3. Barnes NC, Crompton GK. Asthma. In:Brambilla C, Costabel U,et all. Pulmonary Disease, McGraw-Hill, London, 1999; 65-82.
4. National Institutes of Health, National Heart Lung and Blood Institute. Difinition. In: Global Initiative for Asthma 2002, 2-7.
5. Rahmawati I, Yunus F, Wiyono HW. Patogenesis dan Fatofisiologi Asma. Dalam: Cermin Dunia Kedokteran No 141, Jakarta, 2003; 5-10.
COPD Basic Mechanisms and Clinical Management, London, Academic Press, 2002; 1-17.
9. Surjanto E. Patogenesis Asma. Dalam: Naskah Lengkap Pertemuan Ilmiah Khusus (PIK) X, Perhimpunan Dokter Paru Indonesia, Makasar, 2003; 35-44. 10. Busse W, Lemanske FR. Asthma, N Engl J
Med, 344, 2001: 350-62.
11. Rothenberg EM. Eosinophilia, N Engl J Med, 338, 1998: 1592-1600.
12. Saleh T. Peran Kortikosteroid Pada Serangan Asma. Dalam: Margono BP, Widjaja A, Amin M,dkk (editor). Pertemuan Ilmiah Paru Millenium, Surabaya, 2002; 1-16.
13. Patau JM, Hasbi M. Penggunaan Kortikosteroid Pada Asma Bronkial. Dalam: Naskah Lengkap Pertemuan Ilmiah Khusus (PIK) X, Perhimpunan Dokter Paru Indonesia, Makasar, 2003; 53-44.
14. Yunus F. Terapi Controller Pada Asma. Dalam: Margono BP, Widjaja A, Amin M,dkk (editor). Pertemuan Ilmiah Paru Millenium, Surabaya, 2002; 1-6.