Halaman: 20 - 27
© 2000 Jurusan Biologi FMIPA UNS Surakarta
Karyotipe Kromosom pada Allium sativum L. (Bawang Putih)
dan Pisum sativum L. (Kacang Kapri).
AHMAD DWI SETYAWAN1, SUTIKNO2 1Jurusan Biologi FMIPA UNS Surakarta
2Fakultas Biologi UGM Yogyakarta
ABSTRAK
This experiment was done rising the roots of Allium sativum L. (garlic) and Pisum sativum L. (pea). Aspects investigated in the research are the steps of mitotic division and karyotiping. Semi permanent method is used on making preparation with pre-treatment of 0.2% colchicines, fixation using 45% glacial acetic acid, hydrolysis using 1N chloride acid and dying with acetoorcein. The results suggest that pro-metaphase (c-metaphase) step is the most suitable step for cytological observations (number, shape and size of chromosome) and karyotyping. The karyotype formulae of Allium sativum is 2n = 16 = 16m, while for Pisum sativum is 2n = 14 = 14m. The size of chromosome of both species is relatively large and disperse, it thus suitable for studying mitotic division.
Key words: Allium sativum, Pisum sativum, mitosis, karyotipe
PENDAHULUAN
Kromosom merupakan unit dasar kehidupan. Di dalamnya terdapat materi genetik DNA dan RNA yang mengontrol semua aktifitas hidup, termasuk metabolisme dan penurunan sifat. DNA merupakan materi genetik utama pada sebagian besar organisme, sedang RNA umumnya terbatas pada virus (Bennett dan Leitch, 1995; DuPraw, 19 70).
Bentuk, ukuran dan jumlah kromosom setiap spesies pada dasarnya selalu tetap, sehingga sangat bernilai untuk tujuan taksonomi, mengetahui keanekaragaman, hubungan kekerabatan dan evolusi, meskipun dalam keadaan tertentu dapat pula terjadi variasi (Lewontin, 1974; Lindsey and Grell, 1967). Berdasarkan bentuk, jumlah dan ukuran kromosom dapat dibuat peta standard yang disebut karyotipe atau karyogram. Apabila pasangan kromosom digambar tunggal, maka disebut idiogram (Darnaedi, 1991; Soeryo, 1995).
Bentuk kromosom ditentukan oleh pola kontriksi primer pada sentromer. Dalam hal ini dikenal kromosom berbentuk (Soeryo, 1995; Klung dan Cummings, 1984):
1. Metasentris: sentromer tepat di tengah, kromosom berbentuk “huruf V”.
2. Sub-metasentris: sentromer agak ke ujung, kromosom berben-tuk “huruf J”.
3. Akrosentris: sentromer mendekati bagian ujung, kromosom berbentuk “huruf L” atau lurus. 4. Telosentris: sentromer di ujung, kromosom
lurus, jarang ditemukan pada tumbuhan. Levan dkk., 1964 membagi kromosom menjadi tiga kelompok berdasarkan posisi relatif sentromer, dimana bentuk metasentris memiliki indeks sentromer 50-37,5; submetasentris (sm) dengan indeks sentromer 37,5-25 dan subtelosentris dengan indeks sentromer 25-12,5.
Ukuran panjang absolut kromosom berbeda-beda antar genus dalam satu familia, meskipun jumlah dasarnya sama. Ukuran ini bervariasi antara satu hingga 20 kali. Sedang ukuran relatif berbeda-beda dalam satu spesies, terlihat dalam jajaran kromosom pada peta karyotipe. Perbedaan ukuran kromosom menunjukkan perbedaan kandungan gen dan protein (Darnaedi, 1991; Darnaedi dkk., 1989).
Perbedaan jumlah kromosom menunjukkan perbedaan susunan duplikasi gen. Pada kasus aneuploid jumlah kromosom berbeda antar spesies yang masih berkerabat dekat, disebabkan translokasi tidak seragam antara kromosom non-homolog. Aneuploid dapat menambah atau mengurangi jumlah kromosom. Pada kasus poliploid, terjadi penambahan jumlah kromosom secara berkelipatan dari jumlah dasar (Darnaedi, 1991; Darnaedi dkk., 1989; Soeryo, 1995).
Bahan yang umum digunakan dalam studi mitosis adalah ujung akar, ujung batang, primordia daun, petala muda, ovulum muda dan kalus. Namun yang paling umum digunakan adalah ujung akar karena mudah tumbuh dan seragam, sedang untuk pembelahan meiosis sering digunakan anthera atau
ujung tunas bunga (Darnaedi, 1991; Darnaedi dkk., 1989). Penelitian meiosis biasanya hanya digunakan untuk menghitung jumlah kromosom, sedang penelitian mitosis dapat digunakan untuk membuat karyotipe (Riesenberg dkk., 1987). Sifat morfologi kromosom pada pembelahan mitosis lebih stabil dari pada meiosis. Struktur penanda seperti satelit, penyempitan, letak sentromer dan panjang lengan lebih jelas (Min dkk., 1984).
Senyawa mutagen dapat menghambat pembelahan sel dan menyebabkan poliploid. Di dalam nukleus, senyawa ini berikatan dengan mikrotubuli α dan β, yang berperan dalam pembentukan, pertumbuhan, pembelahan dan sitomorfogenesis (Fosket dan Morejohn, 1992). Senyawa mutagen yang paling terkenal dan efektif adalah kolkisin. Senyawa ini berupa alkaloid dan biasanya diperoleh dari ekstrak umbi Colchicum
autumnale L. (Familia Liliaceae), tetapi dalam
kadar rendah dapat pula diperoleh dari umbi Familia Liliaceae lain, seperti Colchicum luteum dan Merendera perseca (Eigsti dan Dustin, 1957).
Perlakuan jaringan meristematik tumbuhan dengan kolkisin menghambat pembelahan sel dan menghasilkan sel poliploid, sejalan dengan pembentukan dinding sel secara normal dan depolarisasi sel-sel yang memanjang (Eleftheriou, 1994; Galatis, 1991; Murata dan Wada, 1989; Nooden, 1971). Kolkisin dapat menginduksi pembentukan parakristal sitoplasma baik pada sel hewan (Schechter dkk., 1976; Rosenbaum dan Carlson, 1969) maupun pada sel tumbuhan (Apostalakos dkk, 1990; Bennett dan Smith, 1979).
Konsentrasi efektif kolkisin berkisar antara 0,01-1,00% untuk lama perendaman 6-72 jam. Konsentrasi yang terlalu tinggi atau waktu perendaman yang terlalu lama, menyebabkan kromosom mengerut bahkan menggumpal, karena reaksi kolkisin dengan protein dan asam nukleat (Eigsti dan Dustin, 1957). Senyawa ini dapat digantikan senyawa mutagen lain seperti asenapten, kloralhidrat, 8-hidroksiquinolin, p-diklorobenzen, indolasetat dan lain-lain. Secara umum kolkisin lebih efektif karena lebih mudah larut dalam air dan tidak bersifat racun apabila kadarnya tepat. Akan tetapi pada dasarnya setiap spesies memiliki kecocokan dengan senyawa mutagen tertentu (Karangiannidou dkk., 1995; Morejohn, 1991; Grant, 1982).
BAHAN DAN METODE
Penelitian ini merupakan penelitian deskriptif kualitatif melalui tahap-tahap: penanaman sediaan, pembuatan kemikalia, pembuatan preparat, studi pedahuluan untuk mengetahui waktu optimum
pembelahan mitosis dan pembuatan peta karyotipe. Preparat dibuat dengan metode squash semi permanen (Darnaedi, 1991; Gunarsa, 1989; Okada, 1981; Radford dkk, 1974; Robert dan Short, 1979). Karyotipe dibuat mengikuti Ruas dkk. (1995), Davina dan Vernandes (1989) serta Robert dan Short (1979). Adapun bentuk kromosom merujuk pada Levan dkk. (1964).
Penanaman Sediaan
Sumber sel meristematis penelitian ini adalah ujung akar. Pada Allium sativum ujung akar diperoleh dengan merendam pangkal umbi lapis sedalam kurang lebih seperempat dari titik akar atau meletakkan umbi di atas kapas basah. Sedang pada Pisum sativum ujung akar diperoleh dengan merendam biji dalam air. Dua hari setelah perendaman, kulit biji dibuang untuk memepercepat perkecambahan.
Studi Pendahuluan
Studi pendahuluan Allium sativum dilakukan pagi hari mulai jam 08.00-13.00. Pemotongan akar dilakukan setiap 30 menit dan dibuat preparat dengan metode squash semi permanen, serta diamati. Prosedur yang sama dilakukan pula pada
Pisum sativum, namun karena tidak diperoleh
waktu pembelahan optimum, maka prosedur ini di-ulangi lagi pada malam hari mulai jam 20.00-01.30.
Pembuatan Kemikalia
Bahan kimia yang digunakan dalam penelitian ini meliputi kolkisin 0,2% untuk pra-perlakuan, asam asetat glasial 45% untuk fiksasi, asam klorida 1N untuk hidrolisis dan asetoorsein 2% untuk pewarnaan.
Kolkisin 0,2%. Kolkisin 0,2 gram dilarutkan dengan 5 ml
etanol, lalu ditambah 95 ml akuades dan diaduk hingga larut. Disimpan dalam botol tertutup rapat, berwarna gelap, dalam lemari es bersuhu 5 oC.
Asam Asetat Glasial 45%. Asam asetat glasial 45 ml dan 55
ml akuades diaduk hingga larut, lalu disimpan dalam botol tertutup pada suhu kamar.
Asam klorida 1N. Asam klorida pekat 1 bagian ditambah 11
bagian akuades, digojok hingga larut dan disimpan dalam botol tertutup pada suhu kamar.
Asetoorsein 2%. Asam asetat glasial 45 ml dipanaskan hingga
hampir mendidih (90-100oC), ditambah 2 gram orsein,
dididihkan lagi selama 10 menit sambil diaduk. Didinginkan pada suhu kamar dan ditambah 55 ml akuades, serta digojok hingga larut. Kemudian disaring dan disimpan dalam botol tertutup, berwarna gelap, pada suhu kamar. Setelah tiga hari penyimpanan biasanya terbentuk endapan, untuk itu sebelum digunakan sebaiknya digojok dan disaring lagi.
Pembuatan Preparat
Pra-perlakuan. Ujung akar dipotong 3-5 mm, dimasukkan ke
dibungkus kertas aluminium dan disimpan dalam lemari es selama 2-4 jam.
Pencucian. kolkisin dibuang dan dicuci akuades tiga kali. Fiksasi. Akuades dibuang, diganti asam asetat glasial 45% dan
disimpan dalam lemari es bersuhu 5 oC selama 15 menit.
Pencucian. asam asetat glasial 45% dibuang dan dicuci
akuades tiga kali.
Hidrolisis. Akuades dibuang, diganti asam klorida 1N dan
disimpan dalam oven bersuhu 60 oC selama ± 2 menit,
tergantung besarnya bahan.
Pencucian. Asam klorida 1N dibuang dan dicuci akuades tiga
kali.
Pewarnaan. Akuades dibuang, diganti asetoorsein 2% selama
1-3 jam, tergantung ukuran bahan dan kesegaran pewarna. Dilakukan pada suhu kamar.
Squashing. Diambil 1-2 buah ujung akar dengan kuas,
diletakkan di atas gelas benda dan dipotong hingga tersisa 1-2 mm dari ujung. Ditetesi gliserin, ditutup gelas penutup dan diketuk-ketuk, hingga hancur merata.
Penyegelan. Kelebihan gliserin di tepi gelas penutup
dibersihkan dengan kertas tisu, lalu disegel dengan cat kuku bening.
Pengamatan. Pengamatan dilakukan dengan mikroskup
cahaya, untuk memperbaiki daya pisah digunakan filter dan minyak emersi. Preparat yang baik dipotret dengan kamera mikrofotografi.
Pembuatan Karyotipe
Data sifat morfologi kromosom meliputi ukuran absolut (µm), ukuran relatif (%) dan perbandingan panjang lengan. Lalu dibuat indek asimetri karyotipe (assymetry index; AsI %) dan rasio perbandingan pasangan kromosom terpanjang dan terpendek (R). Jumlah, ukuran dan bentuk kromosom ditentukan dengan mengamati sekurangnya sepuluh sel yang sedang dalam tahap pembelahan prometafase (Ruas dkk., 1995).
Indek asimetri karyotipe dihitung dengan rumus:
AsI % = total lengan panjang pada kromosom set X 100% total panjang kromosom set
sedang rasio perbandingan pasangan kromosom dihutung dengan rumus:
R = pasangan kromosom terpanjang
pasangan kromosom terpendek
Pembuatan karyotipe dilakukan dengan memproyeksikan setidaknya dua buah preparat foto mikrofotografi pembelahan mitosis tahap prometafase ke atas kertas. Kemudian dipisah-pisahkan dan dikelompokkan berdasarkan bentuknya dengan urutan metasentris, submetasentris, akrosentris dan telosentris. Serta diurutkan berdasarkan ukuran lengan panjang, dimana lengan panjang diletakkan di bawah. Dengan demikian diperoleh karyogram. Dapat pula disajikan dalam bentuk idiogram dengan menyatukan pasangan kromosom tersebut.
HASIL DAN PEMBAHASAN
Penanaman Sediaan.
Air harus diganti setiap hari untuk mencegah tumbuhnya bakteri dan jamur. Pada Allium sativum akar akan muncul setelah 2-3 hari. Kecepatan
pertumbuhan akar tergantung umur umbi. Sedang pada Pisum sativum akar akan tumbuh setelah 4-7 hari. Sebelum digunakan biji sebaiknya dicuci untuk menghilangkan fungisida dan bakterisida yang biasa dibubuhkan pada biji/bibit. Dalam medium air senyawa ini dapat menghambat pertumbuhan akar.
Studi Pendahuluan
Setiap tumbuhan memiliki jam biologi yang mengatur waktu optimum pembelahan mitosis (Johansen, 1940). Umumnya tumbuhan melakukan pembelahan sel pada pagi hari. Dalam penelitian ini studi pendahuluan Allium sativum dilakukan pagi hari mulai jam 08.00-13.00. Pemotongan akar dilakukan setiap 30 menit dan dibuat preparat dengan metode squash semi permanen, diperoleh waktu pembelahan optimum jam 09.00. Prosedur yang sama dilakukan pula pada Pisum sativum, namun karena tidak diperoleh waktu pembelahan optimum, maka prosedur ini diulangi lagi pada malam hari mulai jam 20.00-01.30 dan diperoleh waktu pembelahan optimum jam 22.00.
Teknik Preparasi
Eksperimen mitosis dapat menggunakan sel meristem dari ujung akar, ujung batang, primordia daun, petala muda, ovulum muda dan kalus (Darnaedi, 1991; Okada, 1981). Ujung akar merupakan organ paling sering digunakan untuk mempelajari pembelahan mitosis, misalnya membuat peta karyotipe, karena merupakan organ paling meristematis. Hal ini kerkaitan dengan fungsinya sebagai alat pencari makan yang harus selalu bergerak “mengejar mangsa” serta harus permeabel untuk memungkinkan penyerapan air dan unsur-unsur hara, sehingga ujung akar selalu membelah dan dalam keadaan muda. Di samping itu ujung akar dapat diatur pertumbuhannya untuk mendapatkan bahan yang seragam umur, bentuk dan ukurannya.
Pra-perlakuan Kolkisin
Kolkisin merupakan alkaloid mutagen poliploid, bersifat permeabel terhadap dinding dan membran sel, larut dalam cairan sitoplasma, serta dapat menghambat pembelahan sel dan menyebabkan poliploid. Di dalam nukleus, kolkisin berikatan dengan mikrotubuli α dan β, yang berperan dalam pembentukan pertumbuhan, pembelahan dan sitomorfogenesis. Benang-benang spindel tidak terbentuk dan kromosom tidak dapat ditarik ke bidang ekuator maupun kutub, sehingga tahap prometafase yang dalam kondisi normal hanya berlangsung beberapa menit, dapat dihentikan dan diamati. Kolkisin menyebabkan kromosom mengerut, sehingga ukurannya memendek,
terpencar-pencar, tidak terlalu tumpang tindih dan mudah diamati. Konsentrasi efektif kolkisin berkisar antara 0,01-1,00% untuk lama perendaman 6-72 jam. Konsentrasi tinggi atau perendaman lama, menyebabkan kromosom menggumpal. Tahap prometafase akibat pemberian kolkisin disebut juga c-metafase (colchicine (c-) metaphase) (Eigsti dan Dustin, 1957; Okada, 1981).
Fiksasi dengan Asam Asetat Glasial
Sel-sel meristematis yang dipotong dari organ hidup akan segera membentuk fase metabolik (interfase). Fiksasi bertujuan menghentikan proses ini serta mematikan sel dengan jalan mendenaturasi protein dan asam nukleat. Kromosom yang terfiksasi akan mengkerut, mengeras dan mengendap sehingga tetap berada pada posisi semula seperti ketika masih hidup. Fiksasi yang terlalu lama atau terlalu asam akan menggumpalkan kromosom. Fiksasi juga menaikkan indek bias komponen-komponen sel.
Asam asetat glasial 45% dipilih karena penetrasinya cepat, cukup 15 menit. Konsentrasi 45% merupakan konsentrasi optimum. Pada konsentrasi lebih rendah daya kerjanya berkurang, sehingga butuh waktu lebih lama dan pada konsentrasi lebih tinggi dapat membengkakan kromosom. Fiksasi dengan asam asetat glasial dilakukan dalam lemari es pada suhu 5oC. Suhu rendah ini dimaksud untuk menghambat kerja enzim-enzim pengurai menghidrolisis sel, misalnya lisosom.
Pencucian dengan Akuades
Pencucian dimaksudkan untuk menghilangkan pengaruh perlakuan sebelumnya dan mengembalikan bahan pada suhu kamar sebelum diperlakukan lagi. Misalnya setelah irisan ujung akar difiksasi dengan asam asetat glasial 45% pada suhu 5oC, dicuci terlebih dahulu dengan akuades sebelum dihidrolisis pada suhu 60oC. Akuades dipilih karena larut dalam semua kemikalia yang digunakan dalam metode squash ini, sehingga daya kerjanya efektif.
Hidrolisis dengan Asam Klorida
Dasar pemikiran metode squash adalah melarutkan lamela tengah sel-sel meristimatis yang belum kuat perlekatannya. Sehingga sel dapat dipisah-pisahkan hingga ketebalannya tinggal selapis saja. Hidrolisis dapat menggunakan asam atau enzim hidrolase. Salah satu asam yang biasa digunakan adalah asam klorida. Hidrolisis yang terlalu lama dapat mengurangi affinitas pewarna terhadap kromosom dan menyebabkan kromosom terurai karena denaturasi protein dan asam nukleat.
Asam klorida memiliki kemampuan melarutkan lamela tengah sangat tinggi. Konsentrasi 1N
merupakan konsentrasi optimum. Pada konsentrasi lebih rendah daya kerjanya kurang, sehingga harus direndam lebih lama. Sedang pada konsentrasi lebih tinggi dapat menguraikan nukleus beserta kromosom di dalamnya, sehingga bentuk inti memanjang dan kromosom tidak dapat diamati dengan sempurna. Kecepatan reaksi asam klorida meningkat sejalan dengan naiknya suhu. Suhu tertinggi yang masih diperkenankan dalam prosedur ini adalah 60oC.
Pewarnaan dengan Asetoorsein
Kromosom mempunyai perbedaan mencolok dalam penyerapan warna. Hal ini sangat dipengaruhi jenis tumbuhan. Perbedaan tanggapan terhadap reaksi warna ini menunjukkan perbedaan gen dan protein yang dihasilkan. Asetoorsein sangat cocok untuk ujung akar karena penetrasinya cepat, serta tahan lama, namun dalam penyimpanan lama (misalnya setahun) penetrasinya turun, timbul lapisan film di permukaan cairan dan mengendap. Oleh karena itu dibutuhkan waktu lebih lama untuk penetrasi serta harus digojok dan disaring sebelum digunakan lagi. Endapan yang terbawa ujung akar menyebabkan terbentuknya bercak-bercak gelap yang sangat mengganggu pengamatan di bawah mikroskop.
S q u a s h
Kualitas squash sangat menentukan kualitas preparat. Squash yang baik menghasilkan preparat yang hanya terdiri dari selapis sel, terpisah-pisah, tidak tumpang-tindih, tidak terpecah-pecah dan tidak terdenaturasi. Squash dilakukan dalam media gliserin. Gliserin bersifat kental dan licin, sehingga memudahkan proses squash serta sulit menguap sehingga mampu menjaga kesegaran bahan.
P e n g a m a t a n
Kualitas mikroskop cahaya identik dengan kecilnya nilai daya pisah, yaitu jarak minimum antara dua titik yang masih dapat dibedakan dengan jelas. Nilai daya pisah sebanding dengan nilai panjang gelombang sumber cahaya. Sehingga untuk meningkatkan daya pisah digunakan filter yang meloloskan cahaya dengan panjang gelombang rendah, yaitu biru (λ=435-535) dan hijau (λ=490-535). Filter juga berguna untuk mempertinggi detail dan mengurangi kesilauan. Daya pisah berbanding terbalik dengan indek bias sehingga untuk memperkecil daya pisah, digunakan minyak emersi yang indek biasnya lebih besar dari pada udara. Nilai daya pisah juga berbanding terbalik dengan nilai “Numerical Aperture” (NA), sehingga digunakan lensa objek dengan NA tinggi.
Pembelahan Mitosis
Pembelahan mitosis terdiri dari profase, metafase, anafase dan telofase. Tahap-tahap ini
dalam kondisi alami hanya berlangsung beberapa menit. Para pakar memberi istilah prometafase untuk tahap antara profase dan metafase. Tahap ini merupakan kondisi terpenting untuk studi sitologi, karena pada prometafase bentuk, jumlah dan ukuran kromosom sangat memungkinkan untuk diteliti. Pembelahan mitosis difasilitasi terutama oleh benang-benang spindel mikrotubulin. Pada gambar-gambar mikrofotografi keberadaan benang-benang tersebut sering tidak terlihat, karena pengaruh pra-perlakuan kolkisin yang menghancurkannya. Namun keberadaan dan peran benang-benang tersebut dapat diduga berdasarkan posisi kromosom dalam pembelahan.
Ukuran sel-sel meristematis Allium sativum bervariasi. Hal ini disebabkan oleh tingkat vigoritas masing-masing sel yang berbeda-beda, tergantung umur dan posisi sel. Sel-sel muda yang terletak paling luar cenderung vigor dan besar, sedang sel yang lebih dalam cenderung lebih kecil. Pada saat pembelahan, ukuran sel dapat mempengaruhi penyebaran kromosom. Sel yang ukurannya besar cenderung memiliki cukup ruangan sehingga letak kromosom terpencar-pencar dan tidak tumpang tindih. Pada Pisum sativum vigoritas ini tidak banyak terjadi, sekalipun tetap ada beberapa sel yang higroskopis. Ukuran sel Pisum sativum jauh lebih kecil dari pada ukuran rata-rata sel Allium
sativum, sehingga Allium sativum lebih mudah
diamati biarpun jumlah kromosomnya lebih banyak.
P r o f a s e
Pada fase ini, kromatin yang larut dalam nukleus pada tahap interfase, secara bertahap terkumpul kembali membentuk kromosom yang jelas. Kemudian masing-masing mengalami duplikasi membentuk pasangan kromatid, yang memiliki urutan khas DNA di sentromer. Sentromer berperan penting pada pembelahan sel. Menjelang akhir profase, mikrotubuli yang merupakan bagian kerangka interfase dibongkar dan komponen utama mitosis, yaitu benang-benang spindel dibentuk. Benang-benang spindel membentuk dua kutub, terdiri dari mikrotubuli dan beberapa jenis protein lain.
Prometafase (C-metafase)
Prometafase dimulai secara mendadak karena gangguan pada membran inti yang merusak kerangka interfase mikrotubuli, sehingga kantung membran inti robek. Dalam keadaan normal sisa-sisa kantung membran ini terlihat di sekitar benang spindel selama mitosis. Benang-benang spindel mikrotubuli yang terletak di luar dapat memasuki daerah inti. Pada saat yang sama protein majemuk khas yang disebut kinetokor di masing-masing sentromer mencapai kematangannya dan menempel
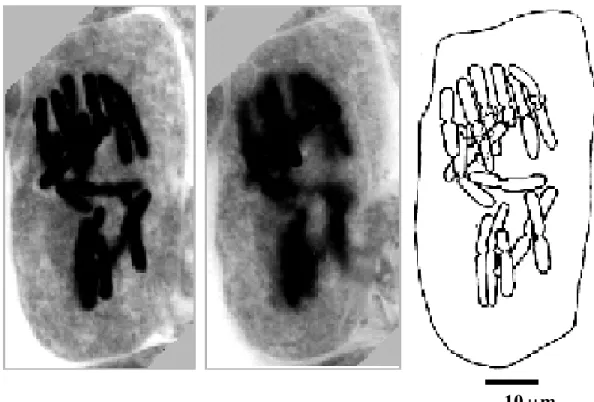
pada mikrotubuli. Pada Allium sativum letak kromosom lebih tersebar dan bentuk lekukan sentromer lebih jelas, sedang pada Pisum sativum letak kromosom agak tumpang tindih sehingga menyulitkan penghitungan jumlah, pengukuran dan pengamatan bentuknya. Tahap ini merupakan fase paling jelas untuk membuat karyotipe.
M e t a f a s e
Pada tahap ini mikrotubuli kinetokor menarik kromosom ke bidang ekuator. Posisi mikrotubuli tegak lurus dengan benang spindel sehingga letak kromosom cenderung mendatar di bidang ekuator. Tahap metafase merupakan indikator umum studi pendahuluan untuk mengetahui waktu terjadinya pembelahan sel. Metafase paling mudah ditemukan, karena pada posisi ini kromosom mengumpul, sehingga biarpun ukurannya kecil tetap dapat dilihat. Duplikasi kromosom diawali pada tahap ini.
Allium sativum memiliki ukuran kromosom lebih
panjang dari pada Pisum sativum, sehingga luasan bidang ekuator yang tertutupi kromosom Allium
sativum lebih besar dari pada Pisum sativum.
A n a f a s e
Tahap anafase berlangsung secara cepat dan tiba-tiba. Diawali terpisahnya pasangan kinetokor pada masing-masing kromosom, lalu diikuti tertariknya kromatid secara pelan-pelan ke arah kutub.
Telofase
Pada tahap telofase, dua kromatid anakan mencapai kutub. Membran inti terbentuk kembali, menyelubungi masing-masing kelompok kromosom anakan. Kromatin yang mengecil menggembung lagi. Nukleolus yang menghilang sejak profase terlihat kembali dan mitosis selesai dengan terbentuknya dua sel baru. Bentuk kromosom telofase pada Allium sativum dan Pisum sativum tidak berbeda jauh. Hanya saja ukuran kelompok kromosom Allium sativum lebih besar.
Karyotipe Kromosom
Dalam penelitian ini tata letak kromosom dalam sel Allium sativum lebih mudah diamati dari pada
Pisum sativum. Sebagian besar kromosom Allium sativum tidak mengalami pembengkokan/kontriksi
primer dan letaknya cenderung datar sejajar bidang pandang, sehingga bentuk, jumlah dan ukurannya dapat diamati dan diperkirakan dengan mudah. Sebaliknya pada Pisum sativum kontriksi primer ini sangat kuat sehingga bentuk kromosom menyerupai huruf “V”, bahkan pada beberapa kromosom lengan-lengan ini hampir bersentuhan. Di samping itu tata letak kromosom Pisum sativum sangat tidak beraturan, beberapa diantaranya terletak tegak lurus terhadap bidang pandang, sehingga sangat menyulitkan pengamatan.
10
µm
Gambar 1. Proyeksi kromosom Allium sativum.
Gambar 2. Proyeksi kromosomPisum sativum
Gambar 3. Allium sativum: A. karyogram, B. idiogram; Pisum sativum: C. karyogram, D. idiogram.
Data karyotipe Allium sativum dan Pisum sativum disajikan dalam tabel 1 dan 2. Allium sativum memiliki rumus karyotipe 2n = 16 = 16 m, sedang
Pisum sativum: 2n = 14 = 14m. Perbedaan
karyotipe menunjukkan adanya perbedaan segregasi dan rekombinasi kromosom. Bentuk kromosom kedua spesies ini didominasi tipe metasentris. Pada Allium sativum kontriksi primer cenderung dapat diabaikan, namun pada Pisum
sativum kontriksi ini sangat kuat. Pada Allium sativum terdapat sepasang kromosom berbentuk
submetasentris. Ukuran kromosom Allium sativum cenderung lebih besar dari pada Pisum sativum. Hal ini dapat dilihat dari perbedaan total panjang kromosom keduanya, masing-masing 197,2µm dan 35,53 µm.
Tabel 2. Data morfometri kromosom Allium sativum dan Pisum sativum
Pasangan kromosom Parameter 1 2 3 4 5 6 7 8 HCL Allium sativum Ukuran absolut µm 30,26 27,36 26,46 25,92 24,88 24,60 18,94 18,82 197,2 Ukuran relatif % 13,87 13,87 13,41 13,14 12,61 12,47 9,60 9,54 100 Rasio lengan L/S 1,09 1,17 1,31 1,17 1,19 1,21 0,72 1,93 Pisum sativum Ukuran absolut µm 6,58 5,92 5,53 5,26 4,74 3,82 3,68 - 35,5 Ukuran relatif % 18,52 16,66 15,56 14,80 13,34 10,75 10,35 - 100 Rasio lengan L/S 1,22 1,14 1,15 1,10 1,12 1,07 1,15 -
Halaman: 20 - 27
© 2000 Jurusan Biologi FMIPA UNS Surakarta Tabel 1. Ciri-ciri karyotipe Allium sativum dan Pisum sativum
Spesies
Rumus
karyotipe AsI% R
Allium sativum 16 m 55,3 1,56
Pisum sativum 14 m 53,35 1,70
Keterangan: AsI% = Assymetry Index (%). R = Rasio
longest pair/ shortest pair
Rasio perbandingan panjang lengan tiap-tiap pasangan kromosom Allium sativum dan Pisum
sativum berkisar pada angka 1 (satu). Hal ini
merupakan ciri khas karyotipe kromosom set yang didominasi kromosom metasentris, dimana ukuran panjang kedua lengannya hampir sama. Pasangan kromosom submetasentris pada Allium sativum memiliki rasio panjang lengan 1,93 artinya ukuran lengan panjang hampir dua kali lipat lengan pendek.
Indek asimetris (AsI %) memiliki kegunaan yang tidak jauh berbeda dengan rasio perbandingan panjang lengan, hanya saja pada indek asimetri ini dihitung untuk keseluruhan kromosom set. Indek asimetri yang besar (menuju angka 100%) menunjukkan besarnya ketidak-samaan panjang kedua lengan kromosom, dimana bentuk metasentris menjadi minoritas dalam kromosom set. Sebaliknya indek asimetri yang kecil (menuju angka 50%) menunjukkan kecilnya tingkat ketidaksamaan panjang kedua lengan kromosom, dimana bentuk metasentris dominan. Dalam pengamatan, nilai AsI% Allium sativum adalah 55,3% sedang Pisum sativum 53,35%. Hal yang tidak mengherankan karena kromosom set keduanya kebanyakan berbentuk metasentris. Nilai AsI% Allium sativum sedikit lebih besar dari pada
Pisum sativum. Hal ini mungkin disebabkan adanya
sepasang kromosom berbentuk submetasentris pada
Allium sativum, hal yang tidak terdapat pada Pisum sativum.
Nilai R (perbandingan pasangan kromosom terpanjang dengan terpendek) menunjukkan variasi ukuran kromosom dalam satu set karyotipe. Semakin besar nilai R berarti semakin besar variasi ukuran kromosom, sedang semakin kecil nilai R berarti semakin besarnya kesamaamnya. Dalam pengamatan diperoleh nilai R Allium sativum adalah 1,56, sedang Pisum sativum adalah 1,70. Angka-angka ini menunjukkan bahwa variasi
ukuran kromosom keduanya tidak terlalu jauh.
KESIMPULAN
Tahap prometafase (c-metafase) merupakan tahap paling sesuai untuk pengamatan sitologi (jumlah, bentuk, ukuran kromosom) dan pembuatan karyotipe. Rumus karyotipe Allium sativum 2n = 16: 16 m, sedang Pisum sativum: 2n = 14: 14m. Ukuran kromosom Allium sativum dan Pisum
sativum relatif besar dan terpencar-pencar sehingga
sangat cocok untuk studi eksperimental mitosis.
DAFTAR PUSTAKA
Darnaedi, D. 1991. Kromosom dalam Taksonomi. Bogor: Herbarium Bogoriense-Puslitbang Biologi-LIPI.
Davina,J.R. dan A. Vernandes. 1989. Karyotype and Meiotic Behaviour in Zephyranthes (Amaryllidaceae) from South America. Cytologia 54: 269-274.
DuPraw, E.J. 1970. DNA and Chromosomes. New York: Holt, Reinhalt and Winston.
Grant, W.F. 1982. Plant Mutagen Assay. Based upon
Chromosome Mutation. Preager Publisher. New York.
Gunarsa. W. 1989. Penuntun Praktikum Sitogenetika. Pusat Antar Universitas IPB. Bogor
Johansen. D.A. 1940. Plant Microtechnique. New Delhi: Tata McGraw-Hill Company
Karangiannidou, T.H., E.P. Elephteriou, I. Tsekos, B. Galatis dan P.Apostolakos. 1995. Colchichine induced Paracrystals in Root Cells of Weath (Triticum aestivum L.). Annals of
Botany 76 (1): 23-30.
Lewontin, R.C. 1974. The analysis of variance and and the analysis of causes. American Journal of Human Genetics 26: 400-411.
Lindsley, D.C. and E.H. Grell. 1967. Genetics variation of
Drosophilla melanogaster. Washington D.C.: Carnegie
Institute of Washington.
Morejohn, L.C. 1991. The Molecular Pharmacology of Plant
Tubulin and Microtubules. In: The Cytoskeletal Basis of
Plant Growth and Form, edited by C.W. Lloyd. London: Academic Press.
Okada. H. 1981. Report on Trainings and Investigations in
LBN-LIPI. Osaka: Departement of Biology Osaka
University. .
Radford, A.E., W.C. Dickinson. J.R. Massey dan C.R. Bell. 1974. Vascular Plant Systematics. New York: Harper & Row Publishers.
Roberts, A.V. dan K.C. Short. 1979. An Experimental Study of Mitosis. Journal of Biological Education 13 (3): 195-198. Ruas, C.F., P.M. Ruas. N.I. Matzenbacher. G. Ross. C. Bernini
dan A.L.L. Vanzela. 1995. Cytogenetic Studies of Some
Hypochoeris Spesies (Compositae) from Brazil. American Journal of Botany 82 (3): 369-375.
Suryo, 1995. Sitogenetika. Yogyakarta: Gadjah Mada University Press.