BAB I BAB I
PENDAHULUAN PENDAHULUAN
Leukemia adalah penyakit keganasan pada jaringan hematopoietik yang Leukemia adalah penyakit keganasan pada jaringan hematopoietik yang ditandai dengan penggantian elemen sumsum tulang normal oleh sel darah ditandai dengan penggantian elemen sumsum tulang normal oleh sel darah abnormal atau sel leukemik. Hal ini disebabkan oleh proliferasi tidak terkontrol abnormal atau sel leukemik. Hal ini disebabkan oleh proliferasi tidak terkontrol dari klon sel darah immatur yang berasal dari sel induk hematopoietik. Sel dari klon sel darah immatur yang berasal dari sel induk hematopoietik. Sel leukemik tersebut juga ditemukan dalam darah perifer dan sering menginvasi leukemik tersebut juga ditemukan dalam darah perifer dan sering menginvasi jaringan retikuloendotelial seperti limpa, hati dan kelenjar limfe.
jaringan retikuloendotelial seperti limpa, hati dan kelenjar limfe.11
Leukemia diklasifikasikan berdasarkan tipe sel, baik menurut maturitas sel Leukemia diklasifikasikan berdasarkan tipe sel, baik menurut maturitas sel maupun turunan sel. Berdasarkan maturitas sel, leukemia dibedakan atas akut dan maupun turunan sel. Berdasarkan maturitas sel, leukemia dibedakan atas akut dan kronik. Jika sel ganas tersebut sebagian besar immatur (blast) maka leukemia kronik. Jika sel ganas tersebut sebagian besar immatur (blast) maka leukemia diklasifikasikan akut, sedangkan jika yang dominan adalah sel matur maka diklasifikasikan akut, sedangkan jika yang dominan adalah sel matur maka diklasifikasikan sebagai leukemia kronik. Berdasarkan turunan sel, leukemia diklasifikasikan sebagai leukemia kronik. Berdasarkan turunan sel, leukemia diklasifikasikan atas leukemia mieloid dan leukemia limfoid. Kelompok leukemia diklasifikasikan atas leukemia mieloid dan leukemia limfoid. Kelompok leukemia mieloid meliputi granulositik, monositik, megakriositik dan eritrositik.
mieloid meliputi granulositik, monositik, megakriositik dan eritrositik.1,21,2 Leukemia mieloid kronik (LMK) adalah penyakit sel induk (
Leukemia mieloid kronik (LMK) adalah penyakit sel induk ( stem stem cell cell )) hematopoetik yang
hematopoetik yang ditandai oleh adanyditandai oleh adanya leukositosis yang disertai imaturitas a leukositosis yang disertai imaturitas seriseri granulosit, basofilia, anemia, trombositosis dan splenomegali. Nama lainnya granulosit, basofilia, anemia, trombositosis dan splenomegali. Nama lainnya leukimia mielogenik kronik atau leukimia myeloid kronik. Penyakit ini leukimia mielogenik kronik atau leukimia myeloid kronik. Penyakit ini merupakan salah
merupakan salah satu tipe kelainan satu tipe kelainan mieloproliferasi kronik yang mieloproliferasi kronik yang berkaitan denganberkaitan dengan translokasi kromosom resiprok lengan panjang kromosom 22 ke kromosom lain translokasi kromosom resiprok lengan panjang kromosom 22 ke kromosom lain
yaitu kromosom 9. Kromosom ini disebut sebagai kromosom Philadelphia yaitu kromosom 9. Kromosom ini disebut sebagai kromosom Philadelphia (t(9;22)(q34;q11.2).
(t(9;22)(q34;q11.2).3,4,53,4,5
LMK ini menempati kasus terbanyak kedua dari semua tipe leukemia pada LMK ini menempati kasus terbanyak kedua dari semua tipe leukemia pada orang dewasa, y
orang dewasa, yaitu sekitar 20% aitu sekitar 20% dan 3% ddan 3% dari leukimia pada ari leukimia pada anak-anak. anak-anak. InsidensiInsidensi LMK terjadi antara 1-2 per 100.000 orang. LMK dapat menyerang semua umur LMK terjadi antara 1-2 per 100.000 orang. LMK dapat menyerang semua umur tetapi sering ditemukan antara usia 40-60 tahun. Penderita LMK pada usia muda tetapi sering ditemukan antara usia 40-60 tahun. Penderita LMK pada usia muda perkembangan
perkembangan penyakitnya penyakitnya akan akan lebih lebih progresif. progresif. NCI NCI (( National National center center instituteinstitute)) menyatakan bahwa frekuensi LMK akan meningkat dengan bertambahnya umur menyatakan bahwa frekuensi LMK akan meningkat dengan bertambahnya umur dimulai dari 1 per 1000.000 orang pada usia 10 tahun pertama, 1 per 100.000 dimulai dari 1 per 1000.000 orang pada usia 10 tahun pertama, 1 per 100.000 orang pada usia 50 tahun dan
orang pada usia 50 tahun dan 1 per 10.000 orang pada usia 80 1 per 10.000 orang pada usia 80 tahun.tahun.3,43,4
Penyebab translokasi Philadelphia ini belum diketahui secara spesifik. Penyebab translokasi Philadelphia ini belum diketahui secara spesifik. Diduga penyebab dari translokasi philadelphia tersebut adalah radiasi pengion. Diduga penyebab dari translokasi philadelphia tersebut adalah radiasi pengion. Hal ini dapat dilihat dari peningkatan insidensi LMK pada individu yang selamat Hal ini dapat dilihat dari peningkatan insidensi LMK pada individu yang selamat dari serangan bom atom di Jepang. Insidensi puncak terjadinya LMK dijumpai 5 dari serangan bom atom di Jepang. Insidensi puncak terjadinya LMK dijumpai 5 sampai 12 tahun setelah pajanan radiasi.
sampai 12 tahun setelah pajanan radiasi.33
LMK dibedakan dari leukemia akut berdasarkan progresinya yang lebih LMK dibedakan dari leukemia akut berdasarkan progresinya yang lebih lambat. Sebaliknya berdasarkan pengobatannya LMK lebih sulit diobati daripada lambat. Sebaliknya berdasarkan pengobatannya LMK lebih sulit diobati daripada leukemia akut. Gambaran klinis LMK antara lain splenomegali, anemia, memar, leukemia akut. Gambaran klinis LMK antara lain splenomegali, anemia, memar, demam, epistaksis, menorhagia, gout, nyeri tulang dan gejala-gejala lain yang demam, epistaksis, menorhagia, gout, nyeri tulang dan gejala-gejala lain yang berhubungan dengan
berhubungan dengan hipermetabolisme hipermetabolisme ( ( penurunan penurunan berat berat badan, badan, anoreksia, anoreksia, atauatau keringat malam).
keringat malam).33
Sekitar 50% pasien LMK didiagnosis secara tidak sengaja dari Sekitar 50% pasien LMK didiagnosis secara tidak sengaja dari pemeriksaan
biasanya lamban dan tidak khas. Selain dari gejala-gejala diatas, untuk mendiagnosa LMK diperlukan pemeriksaan hematologi dan molekuler.3
BAB II
TINJAUAN PUSTAKA
2.1. Definisi
Chronic myelogenous leukimia (CML) atau leukimia myeloid kronik (LMK) merupakan suatu penyakit mieloproliferatif kronik untuk stem sel pluripoten hematopoeitik yang ditandai oleh adanya leukositosis yang disertai imaturitas seri granulosit, basofilia, anemia, trombositosis dan splenomegali. Nama lainnya leukimia mielogenik kronik atau leukimia myeloid kronik. Penyakit ini merupakan salah satu tipe kelainan mieloproliferasi kronik yang berkaitan dengan translokasi kromosom resiprok lengan panjang kromosom 22 ke kromosom lain 9. Kromosom ini disebut sebagai kromosom Philadelphia.3,4,6,7
2.2. Insidensi
Sebagian besar kasus LMK terjadi pada dewasa. Dari tahun 2004-2008 usia median untuk diagnosis penyakit ini adalah 66 tahun. Sedikit sekali anak yang menderita LMK ini, perjalanan penyakit ini pada dewasa dan anak-anak sama.2
Berikut di bawah ini pada dapat dilihat frekuensi peningkatan LMK seiring dengan usia, dari frekuensi 1 per 100.000 penduduk hingga usia 40 tahun, dan sekitar 2 per 100.000 penduduk pada usia hingga 55 tahun , dan sekitar 9 per 100.0000 penduduk pada mereka yang berusia 80 tahun dan lebih. Pada tahun-tahun mendatang, insidensi LMK dapat meningkat.2
Gambar 2.1. Insidensi LMK menurut umur2
Sumber: Howlader N, Noone AM, et al ., eds. SEER Cancer Statistics Review, 1975-2008, National Cancer Institute. Bethesda, MD, www.seer.cancer.gov/csr/1975_2008/, based on November 2010 SEER data submission, posted to the SEER website, 2011
(walters 2012).
Setiap tahun, sekitar 5000-7000 orang didiagnosis sebagai LMK di Amerika Serikat. LMK terhitung sekitar 15%-20% dari semua leukimia dan 7-20% untuk leukimia pada dewasa. LMK ini lebih sering mengenai pada pria dibandingkan wanita dengan ration 1,3-2,2 vs 1.8,9
2.3. Patofisiologi
Sel-sel yang normal memiliki 23 pasang kromosom yang terdiri atas 22 pasang nomor, dengan kromosom seks (XX untuk wanita dan XY untuk laki-laki) yang dihitung sebagai pasangan ke 23. LMK dibedakan dari tipe lainnya pada leukimia oleh adanya abnormalitas genetik pada kromosom 22 pada sel-sel LMK. Di tahun 1960, 2 doktor dari universitas Pensylvania fakultas kedokteran di Philadeplia mempelajari kromosom sel-sel kanker ini. Mereka menemukan bahwa kromosom 22 pada sel pasien dengan LMK lebih pendek dibandingkan dengan
kromosom 22 pada sel-sel normal. Pemendekan kromosom 22 ini dinamakan kromosom Philadelpia dan juga disebut dengan Ph kromosom.2,10
Gambar 2.2. Set kromosom dari sel sumsum tulang pada pasien wanita dengan LMK 2
Semakin tinggi nomor kromosom tampak semakin pendek kromosomnya. Panah pada bari ke 4 menunjukkan pemendekan kromosom 22, yang merupakan karakteristik pada pasien dengan LMK. Panah pada baris kedua menunjukkan kromosom 9 yang memanjang. 2 perubahan ini merefleksikan translokasi pada materi kromosom antara kromosom 9 dan 222
Gen BCR-ABL penyebab kanker. Penelitian lebih lanjut pada sel-sel leukimia fokus pada kromosom 9 dan kromosom 22 yang abnormal. Porsi kromosom-kromosom ini sesungguhnya bertukar satu sama lain. 1 porsi kromosom 9 pindah ke ujung kromosom 22; dan 1 porsi kromosom 22 pindah k ujung kromosom . pertukaran bagian kromosom ini disebut translokasi. Translokasi kromosom 9 dengan kromosom 22 hanya terlihat pada sel-sel LMK dan sebagian ditemukan pada pasien-pasien dengan ALL. Salah satu teori yang dikemukakan oleh seorang ahli bahwwa pertukaran ini terjadi ketika sel
membelah, koromosom 9 dan kromosom 22 sangat dekat satu sama lain, membuat kejadian error ini memungkinkan.2,11
Berikut di bawah ini dapat dilihat kejadian penyebab LMK-bagaimana suatu gen BCR-ABL (okogen) dibentuk.2
Gambar 2.3. Translokasi kromosom 9 dan 222
Suatu porsi gen ABL dari kromosom 9 melakukan translokasi dan bergabung dengan posi utama gen BCR pada kromosom 22. Bagian translokasi ini untuk kromosom 9 menghasilkan uatu fusi gen yang disebut BCR-ABL
Gen fusi BCR-ABL secara langsung memproduksi suatu protein abnormal (mutan), dan suatu enzim yang disebut dengan tirosin kinase bcr-abl
Protein enzim abnormal ini merupakan faktor utama yang mengubah sel-sel induk sumsum tulang dari sle-sel normal menjadi sel-sel leukimia
Gambar proses translokasi antara gen pada kromosom 9 dengan kromosom 2212 Sautu pemisahan pada kromosom 9 menyebabkan suatu mutasi gen yang disebut dengan ABL (untuk Abelson, ilmuan yang pertama kali menggambarkan gen ini). Dan pemutusan pada kromosom 22 melibatkan suatu gen yang disebut dengan BCR (untuk breakpoint cluster regio). Mutasi gen ABL berpindah ke kromosom 22 dan bergabung dengan porsi utama pada gen BCR. Hasil dari penggabungan ini merupakan fusi gen penyebab leukimia BCR-ABL. Gen-gen
ini memberikan instruksi untuk memproduksi suatu protein . gen-gen BCR-ABl menghasilkan suatu protein disfungsional yang disebut dengan “bcr -abl tirosin kinase”. Bcr -abl tirosin kinase ini menyebabkan suatu regulasi pertumbuhan dan
ketahanan sel yan abnormal, yang bertanggung jawab dalam menyebabkan LMK. Tirosin kinase bcr-abl ini juga merupakan target spesifik obat yang memblok efek-efek obat tersebut pada sebagian besar pasien dengan LMK.2,12
Gambar 2.4. Proses tejadinya leukimia pada sel induk sumsum tulang2
Gambar onkogen (gen penyebab kanker) pada batang paling atas yang menyebabkan suatu fusi gen ABL dari kromosom 9 dengen BCR dari kromosom 22. Rangkaian DNA gen ini dikopi ke dalam mRNA, ysng ditunjukkan pada batang tengah. mRNA
menyebabkan formasi protein mutan, yang merupakan suatu enzim yang disebut dengan tirosin kinase yang ditunjukkan pada batang ketiga. Enzim ini mencetuskan
sinyal yang menyebabkan sel induk susmsum tulang beraksi secara tidak teratur (leukemik), menyebabkan terjadinya pembentukan sel darah putih yang berlebihan
yang berusia terlalu lama. Hal demikian merupakan manifestasi klinik pada LMK, seperti hitung sel darah putih yang tinggi dan hitung sel darah merah yang rendah. Beberapa inhibitor bcr-abl tirosin kinase, termasuk imatinib mesylate (Gleevec®), dasatinib (Sprycel®) and nilotinib (Tasigna®), dapat berikatan dengan protein tirosin
kinase dan memblok efek protein tersebut.2
2.4. Etiologi dan faktor risiko
Penyebab LMK sebenarnya masih belum begitu jelas. Leukemogenesis merupakan suatu fenomena bertahap yang dibagi ke dalam fase inisiasi, promosi
dan progresi. Fase inisiasi melibatkan terjadinya defek genetik yang membuat sel bertahan hidup. Trigger yang menyebabkan perubuahan pada tahap inisiasi ini masih belum diketahui. Pada suatu penelitian, dimana sel-sel leukimia dipaparkan dengan irradiasi gamma, fusi-fusi gen dikarakteristikkan dengan bentuk yang berbeda-beda untuk leukimia yang terinduksi, wwalaupun defek ini juga terdeteksi pada jumlah yang rendah pada sel-sel yang tidah diapa-apakan. Perubahan gen BCR-ABL sekarang dikenal sebagai kunci molekular yang menyebabkan terjadinya LMK. Hal yang merangsang perubahan moleklular ini masih belum diketahui. Dengan menggunakan teknik sensitifitas tinggi PCR ( polymerase chain reaction), transkrip BCR-ABL dapat dideteksi pada sel-sel sumsum tulang pada 25-30% mereka yang sehat dan 5% pada bayi baru lahir, tetapi tidak pada darah di tali pusat. Diduga bahwa proses pengaturan imun berperan dalam molekuler terjadinya LMK. BCR-ABL hanya ditemukan pada sel-sel hematopoetik dan tidak ditemukan adanya peningkatan insidensi LMK pada kembar monozigotik dan keluarga yang dengan LMK.2,8
Tidak ditemukan adanya infeksi atau zat-zat kimia yang berhubungan dengan LMK. Insidensi LMK dilaporkan lebih tinggi pada mereka yang bertahan hidup setelah paparan serangan bom atom atau bom nuklir, karena ionisasi radiasi. Selain itu peningkatan risiko juga didapatkan pada mereka yang mendapatkan terapi kanker dengan radiasi seperti limfoma. Paparan diagnosis dental dan sinar-X tidak dihubungkan dengan peningkatan risiko pada LMK. Selain itu, secara umum leukimia dapat disebabkan oleh ionisasi radium, sinar X, Kobalt, Asbestos,
penggunaan permanent dyes, obat-obatan karsinogenik, defisiensi mikronutrien seperti asam folat, vitamin B12 dan B6.2,8,13
2.5. Tanda dan manifestasi klinik
Pasien dengan LMK dapat tidak memiliki gejala-gejala berikut ini pada saat didagnosis. Ini berlaku secara individual; dengan mengikuti pemeriksaan fisik untuk kondisi lainnya dan merupakan bagian pemeriksaan k esehatan.2
Tanda dan gejala LMK timbul secara bertahap. Pasien dengan LMK dapat:12,14-16
1. Merasa lelah dan nafas memendek saat melakukan aktivitas sehari-hari 2. Memiliki pembesaran lien (menyebabkan perasaan seperti tertarik pada
bagian atas sisi kiri abdomen)
3. Pucat atau anemia (menurunnya jumlah sel darah merah), merasakan keringat malam, gatal, sakit kepala, pandangan mata kabur, ketidakmampuan dalam mentolerir suhu yang hangat dan/atau kehilangan berat badan
4. Priapism (ereksi subnormal yang persisten pada penis tanpa adanya rangsangan seksual), ini merupakan gejala yang jarang terjadi namun pernah dilaporkan pada kasus pasien dengan LMK, yang mana hal ini
disebabkan oleh leukostasis
5. Hiperleukositosis, leukostasis, dan pengendapan yang dapat menimbulkan gejala neurologis (kebingungan, somnolen hingga stupor dan koma),
vaskular (DIC, infakr miokard , iskemia akut ekstremitas dan thrombosis vena renal ) dan pulmonal (dispneu, distress nafas)
2.6. Fase LMK
Fase LMK dapat dibagi atas 3 fase. Sebagian besar LMK terdiagnosis pada fase kronik, walaupun beberapa pasien terdiagnosis pada fase akselerase dan fase krisis blast. Sebagian kecil pasien yang didiagnosis dan diterapi pada fase kronik LMK namun berlanjut pada fase akselerasi. Progresi dari fase kronik, yang biasnya dapat dengan mudah di atur, untuk fase akselerasi atau blast krisis terjadi
akibat perubahan genetik pada sel-sel induk leukimia. Beberapa abnormalitas kromosom lanjutan dapat terdeteksi oleh analisis sitogenetik. Bagaimanpun, ini muncul dalam dengan perubahan genetik pada sel-sel induk LMK yang tidak dapat dideteksi dengan tes-tes laboratorium yang sekarang tersedia.2,17
Fase kronik. Pasien dengan fase kronik mungkin dapat asimtomatik, Atau gejala-gejala LMK dapat muncul selama terapi karena perubahan hitung jenis sel atau pembesaran lien. Bila ada, gejala-gejala pada fase kronik dapat hilang ketika pasien dilakukan terapi. Terapi yang efektif menurunkan jumlah sel darah putih
mendekati normal. Perbaikan jumlah sel darah putih diiringi dengan berkurangnya pembesaran limpa, perbaikan konsentrasi haemoglobin dan kondisi umum yang secraa umum membaik. Komplikasi perdarahan dan infeksi tidak biasa terjadi pada fase kronik. Ketika diterapi, umumnya pasien dengan LMK dapat berpartisipasi secara penuh dalam aktivitasnya sehari-hari.2
Tabel 2.1. Karakteristik fase kronik pada LMK 15 Darah
Granulositosis
Rentang penuh untuk precursor granulosit Predomnena mielosit & netrofil segmen
Khususnya mieloblast sekitar 1-2%; selalu <10% Basofilia
Umumnya trombositosis
Sumsum tulang
Hiperselular
Hyperplasia granulositik (meningkatnya ratio M/E) (myeloid/eritroidI Meningkatnya megakariosit; khususnya megakariosit kecil
Fibrosis ringan pada 1/3 pasien
Splenomegali
Menurunnya nilai LAP (leukosit alkalin fosfatase)
Penyusunan ulang Kromosom Philadelphia (t(9;220) dan/atau bcr/abl Meningkatnya serum kobaqlamin (vitamin B12) dan asam urik
Fase akselerasi. Anemia dapat terjadi atau berkembang menjadi fatigue, jumlah sel darah putih dapat turun atau sangat rendah atau meningkat karena akumulasi dari sel-sel blast dan hitung trombosit umumnya menurun. Jumlah sel-sel blast umumnya meningkat pada darah dan sumsum tulang pada fase akselerasi ini (dan jauh sangat meningkat pada fase krisis blast). Ginjal dapat menjadi membesar; pasien tampak aakit, dan komplikasi lainnya dapat terjadi.2
Krisis Blast. Pada fase ini, sel-sel blast meningkat pada sumsum tulang dan darah; sel darah merah, trombosit dan jumlah neutrofil dapat sangat rendah dan pasien akan mengalami episode infeksi dan perdarahan. Gejala-gejala lainnya
seperti fatigue, nafas yang memendek, nyeri tulang, dan /atau pembesaran limpa. Tidak beruntungnya, krisis blast hampei sama dengan ALL. Pada sekitar 25%
orang, transformasi krisi blast dianggap sebagai gejala ALL, sementara mayoritas dianggap sebagai AML.12
Berikut di bawah ini dapat dilihat poin-poin tanda dan laboratorium untuk fase akselerasi dan krisis blast.8
Tabel 2.2. Tanda laboratorium fase akselerasi dan krisis blast8 Fase Akselerasi LMK
A. Kriteria analisis multivariate:
Blast perifer ≥15%
Blast perifer + promielosit ≥30% Basofil perifer ≥ 20%
Trombosit < 100x109 yang tidak dihubungkan dengan terapi Evolusi klonal sitogenik
B. Kriteria yang digunakan dalam praktik umum:
Blas prefer atau sumsum tulang ≥10%
Basofil dan eosinofil perifer atau sumsum tulang ≥20%
Sering gambaran neutrofil Peger-Huet, sel-sel darah merah berinti
atau megakariosit dengan fragmen inti
Meningkatnya retikulin sumsum tulang atau fibrosis kolagen
Leukositosis (> 50x109/L), anemia (Ht<25%) dan trombositopenia
(>100x109/L) tidak responsive terhadapat terapi leukimia
Trombositosis yang jelas (>1000 x 109/L)
Splenomegali progresif yang tidak respon terhadap terapi Demam yang tidak dapat dijelaskan atau nyeri tulang Perlunya peningkatan dosis pengobatan
Fase blastik LMK
≥ 30% blast pada perifer dan sumsum tulang Hematopoeisis ektramedular dengan balst imatur
Leukapharesis. Beberapa pasien memiliki jumlah sel darah putih yang sangat tinggi saat didagnosis. Ini dapat menyebabkan masalah viskositas dan terganggunya aliran darah ke otak, paru, mata dan sisi lainnya dan juga dapat menyebabkan kerusakan pembuluh darah. Pasien dapat ditangani dengan
pembuangan sel-sel darah putih dengan menggunakan mesin yang sama dengan mesin dialisis. Proses ini disebut dengan leukaperesis.12
2.7. Diagnosis
Pada sebagian besar kasus, pemeriksaan darah dan sumsum tu;ang dapat menegakkan diagnosis LMK.
Hitung jenis sel darah (CBC). CBC ini mengukur jumlah dan tipe sel-sel dalam darah. Pada LMK konsentrasi Hb menurun dan jumlah sel darah putih meningkat, bahkan meningkat sangat tinggi. Jmulah trombosit dapat meningkat atau menurun, tergantung pada keparahan penyakit pasien dengan LMK. Pemeriksaan hapusan darah dengan mikroskop cahaya menunjukkan karakteristik/suatu pola untuk sel-sel darah putih pada pasien dengan LMK: sejumlah kecil sel-sel imatur (sel-sel blast leukemik dan promielosit) dan sejumlah besar sel-sel darah putih matur dan besar (mielosit dan neutrofil). Sel-sel blast ini, promielosit dan mielosit secara normal tidak muncul/ada pada darah perifer individu sehat.2
BMA (bone marr ow aspir ation ). Hapusan sumsum tulang pada pasien dengan LMK adalah hiperseluler dan tanpa lemak. Terdapat peningkatan kompartemen myeloid dengan mielosit yang dominan. Berikut di bawah ini dapat dilihat hapusan sumsum tulang yang menggambarkan hiperselularitas dengan hyperplasia myeloid, tidak ditemukan peningkatan blast.14,18
Gambar 2.5. Hapusan sumsum tulang pada pasien LMK 18
Analisis sitogenik . Tes ini mengukur jumlah dan struktur kromosom. Sampel di ambil dari sumsum tulang yang diperiksa untuk mengkonfirmaasi temuan pada pemeriksaan darah dan memastikan apakah terdapat abnormalitas kromosomal
seperti kromosom Philadelphia. Tes sumsum tulang disebut BMA. Sampel ini diperiksa secara mikroskopik dan sitogenetik. Adanya kromosom philadelpia (pemendekan pada kromosom 22) pada sumsum tulang, diikuti dengan tingginya hitung sel darah putih dan karakteristik temuan lainnya, mengkonfirmasi diagnosis LMK.2
F lu orescence I n Situ H ybri dizati on (FISH). 90% pasien terdiagnosis LMK dengan analisis sitogenik, tapi sebagian tidak terdiagnosis dengan analisis sitogenik tersebut tetapi memiliki nilai yang positif untuk fusi gen BCR-ABL pada kromosom 22. FISH lebih sensitif dalam mendiagnosis LMK dibandingkan analisis sitogenetik. Berikut di bawah ini dapat dilihat identifikasi gen BCR-ABL dengan menggunakan teknik FISH.2
Gambar 2.6. Teknik FISH, suatu metode dengan menggunakan florosensi molekul untuk menandai gen BCR-ABL pada LMK. Pada sel-sel normal, 2 merah dan 2 sinyal hijau mengindikasikan lokasi normal gen BCR dan ABL pada sel-sel yang abnormal, fusi BCR ABL dalam visualisasi tampak sebagai gabungan sinyal merah
dan hijau. Ini sering dideteksi sebagai flurosensi kekuningan (yang di tunjuk panah)2
Polymerase Chai n Reaction (PCR). Gen BCR-ABl juga dapat dideteksi dengan analisis molekular. Tes kuantitatif PCR merupakan metode tes molekular yang dapat dilakukan pada sel darah merah dan sel sumsum tulang. Ini merupakan tes yang paling sensitif untuk mengidentifikasi dan mengukur gen BCR-ABL. PCR ini secara esensial meningkatkan jumlah kecil bagian-bagian dari RNA atau DNA untuk membuatnya mudah dideteksi dan dihitung.2,19
Hitung jenis sel darah, pemeriksaan sumsum tulang, FISH dan PCR juga dapat digunakan untuk menilai respon terapi. Seiring dengan dilakukannya terapi, jumlah sel-sel darah merah, sel-sel darah putih , trombosit dan sel sel LMK
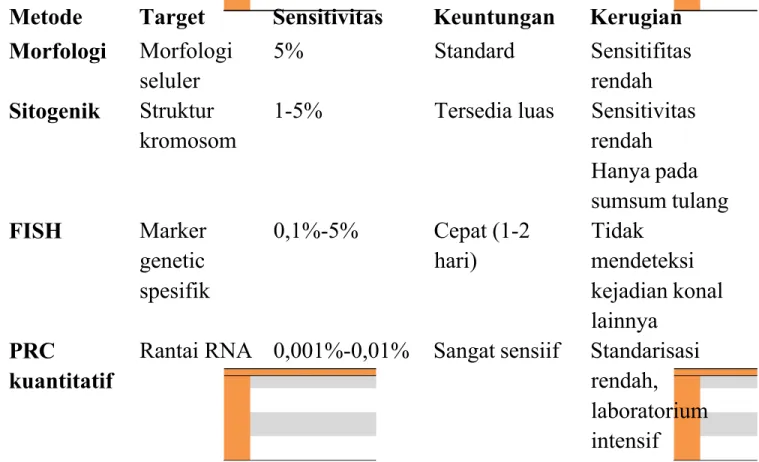
mengalami perubahan. Berikut di bawah ini dapat dilihat perbandingan berbagai metode yang dapat digunakan untuk mendiagnosis LMK.2,20
Tabel 2.3. Metode untuk mendeteksi sisa penyakit (residual) pada LMK 20 Metode Target Sensitivitas Keuntungan Kerugian Morfologi Morfologi seluler 5% Standard Sensitifitas rendah Sitogenik Struktur kromosom
1-5% Tersedia luas Sensitivitas rendah Hanya pada sumsum tulang FISH Marker genetic spesifik 0,1%-5% Cepat (1-2 hari) Tidak mendeteksi kejadian konal lainnya PRC kuantitatif
Rantai RNA 0,001%-0,01% Sangat sensiif Standarisasi rendah, laboratorium intensif
2.8. Terapi
LMK tidak mudah untuk disembuhkan dengan terapi yang sekarang tersedia, namun banyak terapi signifikan pada beberapa tahun terakhir ini, dan pilihan terapi yang memungkinkan terus berlanjut. Dengan terapi sekarang ini, pasien dengan LMK diharapkan memiliki kualitas hidup yang baik. Pilihan terapi yang digunakan untuk pasien LMK tergantung pada fase saat didiagnosis, hasil tes dan usia, terutama sekali jika transplantasi sumsum tulang dapat dipertimbangkan.2
4 macam modalitas terapi mayor untuk penyakit LMK ini meliputi : 1) allogenic stemm cell trasnplant (SCT); 2) interferon alfa (INF-α) berdasarkan regimen; 3) infuse donor limfosit (DLI) dan 4) inhibitor revolusioner tirosin
kinase Bcr-abl seperti STI571 (sinyal transduction inhibitor 571). Masing-masing modalitas tersebut memiliki aspek target yang berbeda-beda untuk biologi LMK, dan dihubungkan dengan risiko serta keuntungan yang berbeda-beda untuk masing-masing regimen.2,21
Berikut di bawah ini dapat dilihat pilihan agen kemoterapi yang dapat digunakan untuk terapi pada pasien LMK.2,21
Tabel 2.4. Beberapa obat yang digunakan untuk menterapi LMK 2
LMK sudah sejak 100 tahun yang lalu ditemukan, solusi Fowler ( arsenic trioxide dalam potassium bicarbonate) dan radiasi splenik merupakan satu-satunya terapi yang tersedia sebelum tahun 1950. Busulphansuatu agen alkylating , telah diperkenalkan pada tahun 1954 dan efektif dalam mengontrol leukositosis. Namun ini memiliki toksisitas yang tinggi-aplasia sumsum tulang (1-3%), hiperpigmentasi dan fibrosis pulmonal, dan ketahanan hidupnya lebih rendah dibandingkan dengan hidroksiurea. Ini hanya digunakan sebagai bagian dari kemoterapi dosis tinggi bersamaan dengan siklofosfamid dalam setting
transplantasi stem sel (SCT). Hidroksiurea diperkenalkan pada akhir tahun 1960-an, memiliki profil toksisitas yang cukup dan efektif dalam mengontrol jumlah sel darah putih. Rekombinan INF-α tersedia pada awal tahun 1990-an dan lebih superior dibandingkan busulphan dan hidroksiurea dalam remisi hmatologi komplet (CHR), respon sitogenetik komplet (CGR) dan ketahanan hidup yang lebih lama. Pada 25 tahun terakhir ini, pengalaman dengan allogenik hematopoetik SCT dari pencocokan HLA saudara atau donor bukan keluarga yang cocok di anggap sebagai satu-satunya terapi kuratif untuk kasus LMK ini. Keterbatasan akan ketersediaan donor yang cocok pada kurang dari 1/3 pasien dan morbiditas yang potensial (acute and chronic graft-versus-host disease) dan mortalitasnya (5-15%). Imatinib mesylate (STI-571 atau Gleevec), mulai dicanangkan pada Mei 2001 dan menjadi revolusioner dalam terapi LMK. Berikut di bawah ini dapat dilihat perbandingan penggunaan agen kmoterapi interferon alfa, hidroksi urea dan Imatinib mesylate.22
Tabel 2.5. Perbandingan Hidroksiurea, interferon-α, dan imatinib mesylate22 Faktor Hidroksiurea Interferon-α Imatinib mesilate
Mekanisme aksi Inhibitor ribonukleotida
rekduktase
Tidak diketahui Inhibitor selektif BCR-ABL
Respon hematologic Ya Ya Ya
Kecepatan Ya Tidak Ya
Respon sitogenik Tidak Ya Ya
Aktivitas pada fase blastik Tidak Tidak Ya Keuntungan survival Tidak Ya Ya Dampak pada allogenik transplantasi sumsum tulang
Dosis harian 0,5-2 gr 3-5 mU/m2 CP 400 mg/hari AP/BC 600mg/hari
Toksisitas mayor Tidak Ya Tidak
Administrasi per oral
Ya Tidak Ya
Biaya Rendah Mahal Sangat mahal
AP= fase akselerasi; BC= krisis balstik; CP= fase kronik
Berikut di bawah ini dapat dilihat pilihan regimen yang direkomendasikan oleh European LeukimiaNet untuk penanganan LMK 6
Tabel 2.6. Pilihan regimen untuk terapi LMK pilihan European LeukemiaNet 6
Fase kronik. Lini I Imatinib 400 mg/hari
Fase kronik, lini II
Intoleransi imatinib Dasatinib atau nilotinib
Respon imatinib suboptimal Lanjutkan imatinib dengan dosis yang sama; atau tes pemberian imatinib dosis tinggi, dasatinib, atau nilotinib
Imatinib gagal Dasatinib/nilotinib; trasplantasi stem sel allogenik pada pasine yang mengalami progresi menuju fase akselerasi atau
krisis blastik dan pada kasus dengan mutasi T315l
Fase kronik, lini III
Respon Dasatinib atau nilotinib suboptimal
Lanjutkan dasatinib atau nilotinib, dengan suatu pilihan transplantasi stem sel pada pasien dengan gambaran yang perlu diwaspadai (resistensi utama pada
imatinib, mutasi) dan pada kasus dengan EBMT skor risiko ≤2
Disatinib atau nilotinib gagal Transplantasi stem sel allogenik Fase akselerasi atau fasse blastik,
lini I (pasien dengan TKI naive)
Imatini 600 atau 800 mg, dasatinib, atau nilotinib (pada kasus mutasi dengan sensitifitas yang rendah terhadap imatinib) diikuti dengan transplantasi stem sel allogenik
Fase akselerasi ayau fase balstik, lini II (pasien dengan terapi utama
Dasatinib atau imatinib diikuti dengan transplantasi stem sel
imatinib
Selain rekomendasi obat-obatan di atas, terdapat berbagai obat-obatan baru yang masih dalam penelitian (pengembangan) diantaranya yaitu sebagai berikut.2
Ponatinib (AP24534)
Ponatinib, yang masih dalam perkembangan klinik, merupakan terapi LMK peroral yang menjanjikan aktivitas klniik melawan sejumlah mutasi yang terjadi disebabkan oleh resistensi terhadap Gleevec, Sprycel dan Tasigna, yang tercatat sebagai mutasi T315I, yang merupakan mutasi yang umum yang tampak sebagai respon terhadap imatinib mesylate (Gleevec), Sprycel atau Tasigna yang kurang atau hilang. Ponatinib tampaknya secara umum ditoleransi dengan baik; efek samping yang umum terjadi yaitu fatigue, konstipasi, ruam, nyeri kepala, nyeri sendi dan mual.
Bosutinib
Bosutinib, merupakan terapi peroral LMK, merupakan TKI yang aktif melawan sejumlah mutasi resisten dengan Gleevec, tetapi bukan untuk mutasi T315I. Obat ini telah menjalani evaluasi trial klinik pada pasien yang telah diterapi dengan satu atau lebih TKI, pada pasien yang baru di diagnosis LMK fase kronik. Bila disetujui, obat ini dapat menjadi pilihan pada pasien yang tidak dapat ditoleransi atau respon adekuat terhadap
Strategi eradikasi penyakit
Sejumlah penelitian laboratorium telah mengidentifikasi terapi potensial yang dapat membantu mengeradikasi beberapa sel-sel LMK pada sebagian besar pasien dengan TKI, dan kemudian memberikan harapa kesembuhan pada pasien sehingga dapat menghentikan terapi medis secara bersamaan. Salah satu area yang memberi ketertarikan yaitu pada suatu protein yang disebut dengan istilah “ smoothened ” (SMO) dalam kombinasi dengan Bcr-Abl TKI.
Terapi Vaksin
Berbagai macam vaksin telah diteliti. Protein pada permukaan sel LMK dapat cocok dengan suatu jenis vaksin tertentu, yang dapat menarik sel-sel imun pasien untuk menyerang sel-sel LMK tersebut.
Modifikasi transplantasi Stem Cell
Modifikasi dari transplantasi allogenik disebut “reduced intensity” atau “ nonmyeloablatif ” transplantasi stem cell allgoenik dapat menjadi suatu pilihan untuk pasien LMK yang tidak respon dengan terapi lainnya. Pasien yang dipersiapkan untuk transplantasi reduced-intensity menerima dosis obat-obatan kemoterapi yang lebih rendah dan/atau radiasi untuk persiapan tranplantasi, dibandingkan dosis obat yang diberikan pada pasien untuk menerima transplantasi allogenik. Obat-obatan immunosupresif digunakan untuk mencegah penolakan terhadap stem cell donor, dan menanamkan sel-sel imun donor dapat memungkinkan sel-sel ini menyerang sel-sel LMK pasien (sebagai hasilnya disebut sebagai
“graft -versus-tumor effect ”). Teori ini telah diuji coba dengan transplantasi reduced-intensity yang menjalani prosedur dengan toksisitas yang kurang untuk tranplantasi, tubuh lebih mudah menerima tranplantasi yang dilakukan. Bagaimanapun, penanaman penuh materi donor memerlukan tempat dan tujuan graft-versus-tumor effect masih dapat tercapai.
Obat-obatan lainnya yang dalam uji coba trial klinik untuk meningkatkan graft-versus-tumor effect pada transplantasi stem cell dan untuk mengurangi risiko penyakit graft versus host . Tambahan pula, penelitian menggunakan darah/materi tali pusat sebagai sumber stem cell untuk transplantasi pada anak-anak dan dewasa. Darah tali pusat memberikan sumber potensial lainnya yang cocok. Hasil yang didapatkan dari transplantasi stem cell darah tali pusat telah menjanjikan, dan ini mengurangi risiko penyakit akut graft versus host pada pasien yang lebih muda menjalani transplantasi darah tali pusat.
2.9. Prognosis
LMK dikarakteristikkan memiliki klinik yang bifasik. Fase kronik inisial secara relatif berjalan lambat yang dapat berlangsung selama beberapa tahun. LMK yang tidak diterapi tanpa kecuali dapat berlanjut menjadi akut mieloid atau limfoblastik leukimia (misalnya krisis blastik). Kadang-kadang fase akselerasi didahului dengant trasformasi blastik.6
Beriikut di bawah ini dapat dilihat kriteria dalam menilai respon terapi pada pasien dengan LMK.22
Tabel kriteria respon pada pasien LMK yang menjalani pengobatan22 Respon hematologi
Komplet
1. Hitung leukosit total <10.000/cmm, hitung trombosit < 450.000/cmm 2. Hitung jenis normal dengan bentukan imatur tidak ditemukan (mielosit,
metamielosit, promielosit dan sel blast)
3. Hilangnya semua gejala dan tanda klinis termasuk splenomegali 4. Tidak ada bukti penyakit ekstramedullar
Parisal
1. >50% menurun leukosit total dari sebelum terapi hingga <20000/cmm 2. Bentuk imatur atau persisten untuk hitung jenis sel
3. Splenomegali persisten
Respon sitogenik (metaphase Ph positif pada sumsum tulang)* Complete Parsial Minor Minimal Tidak 0% 1-35% 36-65% 66%-95% 100% Respon molekul Mayor komplet
≥ 3 log reduksi mRNA BCR -ABL Negative oleh RT-PCR
*Berdasarkan pada analisis sedikitnya 20 metafase
respon sitogenik mayor termasuk respon parisal dan respon komplet
Berikut di bawah ini dapat dilihat guideline umum untuk LMK respon terapi.2
Tabel Guideline umum untuk respon terapi pada LMK 2
Waktu terapi Respon
Setelah 3-6 bulan terapi Respon hematologic komplet dan beberapa perbaikan sitogenik
Setelah 6-12 bulan terapi Respon sitogenik dengan reduksi 2/3 pada jumlah kromosom Philadelphia
pada sumsum tulang
Setelah 12-18 bulan terapi Respon sitogenik komplet dan respon molecular sebagian
Tanpa terapi yang efektif, median ketahan hidup untuk fase kronik, fase akselerasi dan krisis blast berturut-turut adalah 2,5 hingga 5 tahun, tidak kurang dari 1,5 tahun dan 3-6 bulan.6
BAB III PENUTUP
Leukemia mieloid kronik (LMK) adalah penyakit sel induk ( stem cell ) hematopoetik yang ditandai oleh adanya leukositosis yang disertai imaturitas seri granulosit, basofilia, anemia, trombositosis dan splenomegali Penyakit ini merupakan salah satu tipe kelainan mieloproliferasi kronik yang berkaitan dengan translokasi kromosom resiprok lengan panjang kromosom 22 ke kromosom lain yaitu kromosom 9. Kromosom ini disebut sebagai kromosom Philadelphia (t(9;22)(q34;q11.2). Sebagian besar kasus LMK terjadi pada dewasa. Dengan usia median 66 tahun. gen-gen BCR-ABl menghasilkan suatu protein disfungsional yang disebut dengan “bcr -abl tirosin kinase”. Bcr -abl tirosin kinase ini menyebabkan suatu regulasi pertumbuhan dan ketahanan sel yan abnormal, yang bertanggung jawab dalam menyebabkan LMK. Gejala pada LMK berupa mudah lelah, pucat, splenomegali, priapism, hiperleukositosis dan leukostasis yang dapat menyebabkan gangguan vascular. Pada LMK terdapat 3 fase yaitu fase kronik, fase akselerase dan fase krisis blast dengan karakteristik yang berbeda- beda. Diagnosis ditegakka dengan pemeriksaan CBC, BMA, analisa sitogenik, FISH, dan PCR. Untuk penatalaksanaan pada kasus ini terdapat 4 macam modalitas terapi diantaranya yaitu 1) allogenic stemm cell trasnplant (SCT); 2) interferon alfa (INF-α) berdasarkan regimen; 3) infuse donor limfosit (DLI) dan 4) inhibitor revolusioner tirosin kinase Bcr-abl seperti STI571 (sinyal transduction inhibitor 571) yang mana fase saat diagnosis juga memiliki regimen dan dosis
pemberian yang dapat berbeda-beda. Prognosis penyakit ini tergantung pada saat diagnosis dan respon terhadap terapi yang dapat terjadi perubahan pada hematologic, sitogenik dan molekul. Tanpa terapi yang efektif, median ketahan hidup untuk fase kronik, fase akselerasi dan krisis blast berturut-turut adalah 2,5 hingga 5 tahun, tidak kurang dari 1,5 tahun dan 3-6 bulan