LAPORAN
PRAKTIKUM BIOKIMIA PANGAN
KARBOHIDRAT I
Uji MolischDiajukan untuk Memenuhi Salah Satu Persyaratan Praktikum Biokimia Pangan
Oleh :
Nama : Asri Nisa Sakinah
NRP : 113020056
Meja : 02 (Dua) Kelompok : C
Asisten : Anjar Gustaram Suparman Tgl Percobaan : 11 Maret 2013
LABORATORIUM BIOKIMIA PANGAN
JURUSAN TEKNOLOGI PANGAN
FAKULTAS TEKNIK
UNIVERSITAS PASUNDAN
BANDUNG
2013
LAPORAN PRAKTIKUM BIOKIMIA PANGAN
KARBOHIDRAT I
Uji Molisch
Asri Nisa Sakinah : 113020056 Cholillah Nur Aliefah : 113020057
INTISARI
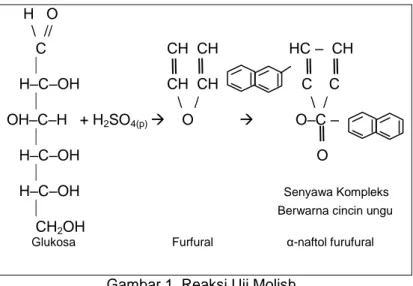
Tujuan dari percobaan uji molisch adalah untuk menguji adanya karbohidrat dalam bahan pangan. Prinsip dari percobaan uji molisch adalah berdasarkan karbohidrat oleh asam sulfat pekat akan dihidrolisa menjadi monosakarida kemudian akan mengalami dehidrasi menjadi hidroksi metil furfural yang dengan - naftol menjadi senyawa kompleks yang membentuk cincin ungu.
Berdasarkan hasil pengamatan pada uji molisch dapat disimpulkan bahwa sampel vitamin B kompleks, mayonnaise, madu dan saus sambal mengandung karbohidrat karena terdapat cincin ungu.
I PENDAHULUAN 1.1. Latar Belakang
Dalam kehidupan sehari-hari kita melakukan aktivitas. Untuk melakukan aktivitas itu kita memerlukan energi. Energi yang diperlukan ini kita peroleh dari bahan makanan yang kita makan. Pada umumnya bahan makanan itu mengandung tiga kelompok utama senyawa kimia, yaitu karbohidrat, protein, dan lemak atau lipid (Poedjiadi, 2005, Hal 8).
Karbohidrat merupakan sumber kalori utama. Walaupun jumlah kalori yang dapat dihasilkan oleh 1 gram karbohidrat hanya 4 Kal (kkal) bila dibanding protein dan lemak, karbohidrat merupakan sumber kalori yang murah. Selain itu beberapa golongan karbohidrat menghasilkan serat-serat yang berguna bagi pencernaan. Karbohidrat juga mempunyai peranan penting dalam menentukan karakteristik bahan makanan, misalnya rasa, warna, tekstur, dan lain-lain (Winarno, 1997, Hal 15).
1.2. Tujuan Percobaan
Tujuan dari percobaan uji molisch adalah untuk mengetahui adanya karbohidrat dalam bahan pangan.
1.3. Prinsip Percobaan
Prinsip percobaan uji molish berdasarkan senyawa karbohidrat dengan adanya asam pekat (H2SO4) akan membentuk senyawa hidroksi metilfurfural yang kemudian dengan adanya -naftol akan membentuk senyawa kompleks berwarna cincin ungu.
1.4. Reaksi Percobaan Uji Molish H O \ // C CH CH HC – CH H–C–OH CH CH C C \ / \ / OH–C–H + H2SO4(p) O O–C – H–C–OH O
H–C–OH Senyawa Kompleks
Berwarna cincin ungu CH2OH
Glukosa Furfural α-naftol furufural
II TINJAUAN PUSTAKA
Bab ini akan membahas mengenai : (1) Pengertian Karbohidrat, (2) Penggolongan Karbohidrat, (3) Sifat-sifat Karbohidrat
2.1. Karbohidrat
Karbohidrat merupakan sumber kalori utama bagi hampir seluruh penduduk dunia. Karbohidrat juga berguna untuk mencegah timbulnya ketosis, pemecahan protein tubuh yang berlebihan, kehilangan mineral, dan berguna untuk membantu metabolisme lemak dan protein tetapi sebagian besar karbohidrat diperoleh dari bahan makanan yang kita makan sehari-hari (Winarno, 1997, Hal 15).
Karbohidrat mempunyai gugus fungsi yang sangat penting. Berdasarkan gugus yang ada pada molekul karbohidrat, maka karbohidrat dapat didefinisikan sebagai polihidroksialdehida dan polihidroksiketon serta senyawa yang menghasilkannya pada proses hidrolisis. Senyawa yang termasuk karbohidrat terdapat gugus fungsi –OH, aldehid, dan keton (Poedjiadji, 2005, Hal 10-11).
2.2. Penggolongan Karbohidrat
Berbagai senyawa yang termasuk kelompok karbohidrat mempunyai molekul yang berbeda-beda ukuranny, yaitu dari senyawa yang sederhana yang mempunyai berat molekul 90 hingga senyawa yang mempunyai berat molekul 500.000 bahkan lebih. Berbagai senyawa itu dibagi menjadi 3 golongan yaitu golongan monosakarida, golongan oligosakarida, dan golongan polisakarida (Poedjiadi, 2005, Hal 24).
2.2.1 Monosakarida
Monosakarida ialah karbohidrat yang sederhana, dalam arti molekulnya hanya terdiri atas beberapa atom saja dan tidak dapat diuraikan dengan cara hidrolisis dalam keadaan lunak menjadi karbohidrat lain. Monosakarida yang paling sederhana ialah gliseraldehida dan dihidroksiaseton. Gliseraldehida dapat disebut aldotriosa karena terdiri atas tiga atom karbon dan mempunyai gugus aldehida. Dihidroksiaseton dinamakan ketoriosa karena terdiri atas tiga
atom karbon dan mempunyai gugus keton. Monosakarida yang terdiri atas empat atom karbon disebut tetrosa dengan rumus C4H8O4. Monosakarida terdiri atas glukosa, fruktosa, dan galaktosa (Poedjiadi. 2005, Hal 24-25).
2.2.2. Oligosakarida
Oligosakarida adalah polimer dengan derajat polimerisasi 2 sampai 10 dan biasanya bersifat larut dalam air. Oligosakarida yang terdiri dari dua molekul disebut disakarida dan bila tiga molekul disebut triosa. Sukrosa (sakarosa atau gula tebu) terdiri dari molekul glukosa dan fruktosa, sedangkan laktosa terdiri dari molekul glukosa dan galaktosa (Winarno, 1997, Hal 23).
Oligosakarida yang paling banyak di alam yaitu disakarida. Oligosakarida terdiri dari sukrosa, maltosa, laktosa, rafinosa, dan stakiosa. Sukrosa merupakan gula yang kita kenal sehari-hari, baik dari tebu maupun dari buah bit. Hidrolisis sukrosa akan terpecah dan menghasilkan glukosa dan fruktosa. Pada molekul sukrosa terdapat ikatan antara molekul glukosa dan fruktosa, yaitu antara atom karbon nomer 1 pada glukosa dengan atom karbon nomer 2 pada fruktosa melalui atom oksigen. Laktosa adalah suatu disakarida, karena hasil hidrolisis laktosa akan menghasilkan D-galaktosa dan D-glukosa. Ikatan galaktosa dan glukosa terjadi antara atom karbon nomer 1 pada galaktosa dan atom karbon nomer 4 pada glukosa. Maltose merupaka suatu disakarida yang terbentuk dari dua molekul glukosa. Ikatan yang terjadi antara atom karbon nomer 1 dan atom karbon nomer 4, oleh karena itu maltosa masih mempunyai gugus –OH glikosidik dan mempunyai sifat mereduksi. Rafinosa adalah trisakarida yang terdiri atas tiga molekul monosakarida yang berikatan, yaitu galaktosa-glukosa-fruktosa (Poedjiadi, 1994, Hal 31).
2.2.3. Polisakarida
Polisakarida mempunyai molekul besar dan lebih kompleks daripada mono dan oligosakarida. Molekul polisakarida terdiri atas banyak molekul monosakarida. polisakarida yang terdiri atas satu macam monosakarida saja disebut dengan homopolisakarida, sedangkan yang mengandung senyawa lain disebut heteropolisakarida.
Umumnya polisakarida berupa senyawa putih dan tidak berbentuk kristal. Berat molekul polisakarida bervariasi dari beberapa ribu hingga lebih dari satu juta. Polisakarida yang dapat larut dalam air akan membentuk larutan kolid. Beberapa polisakarida yang penting diantaranya amilum, glikogen, dekstrin dan selulosa (Poedjiadji, 2005, Hal 35).
Amilum atau yang biasa disebut dengan pati ini merupakan homopolimer glukosa dengan ikatan -(1,4)-D-glukosa, sedangkan amilopektin mempunyai cabang dengan ikatan -(1,4)-D-glukosa sebanyak 4-5 % dari berat total (Winarno, 1997, Hal 27).
Hidrolisis glikogen menghasilkan D-glukosa. Seperti dalam alam glikogen terdapat pada kerang dan pada alga atau rumput laut. Glokigen yang terlarut dalam air dapat diendapkan dengan menambah etanol. Glikogen dapat memutar cahaya terpolarisasi ke kanan. Struktur glikogen serupa dengan struktur amilopektin yaitu merupakan rantai glukosa dan mempunyai cabang (Poedjiadji, 2005, Hal 37). 2.3 Sifat Karbohidrat
Sifat karbohidrat berhubungan erat dengan gugus fungsi yang terdapat pada molekulnya, yaitu gugus –OH, gugus aldehida dan keton (Poedjiadji, 2005, Hal 39).
2.3.1 Sifat Mereduksi
Sifat mereduksi ini disebabkan oleh adanya gugus aldehida atau keton bebas dalam molekul karbohidrat. Sifat ini tampak pada reaksi reduksi ion-ion logam misalnya ion Cu++ dan ion Ag+ yang terdapat pada pereaksi-pereaksi tertentu (Poedjiadji, 2005, Hal 39).
2.3.2 Pembentukan Furfural
Larutan asam encer, monosakaridanya umumnya stabil walaupun dipanaskan. Apabila dipanaskan dengan asam kuat yang pekat maka monosakarida akan menghasilkan furfural. Reaksi pembentukan furfural ini adalah reaksi dehidrasi atau pelepasan molekul air dari suatu senyawa. Furfural dapat membentuk senyawa berwarna apabila direaksikan dengan -naftol karena heksosa yang terhidrasi akan menghasilkan hidroksilmetilfurfural. Dalam
pembentukan furfural digunakan pereaksi molisch. Apabila pereaksi ini ditambahkan pada larutan glukosa, kemudian ditambahkan asam sulfat pekat akan terbentuk dua lapisan zat cair. Pada batas antara kedua lapisan tersebut terdpat cincin berwarna ungu (Poedjiadji, 2005, Hal 41).
2.3.3 Pembentukan Osazon
Semua karbohidrat yang mempunyai gugus aldehida atau keton bebas akan membentuk osazon bila dipanaskan bersama fenilhidrazin berlebih. Pada reaksi antara glukosa dengan fenilhidrazine, mula-mula terbentuk D-glukosafenilhidrazon, kemudian reaksi berlanjut sehingga terbentuk D-glukosazon. Glukosa, fruktosa, dan manosa dengan fenilhidrazine menghasilkan osazon yang sama (Poedjiadji, 2005, Hal 42).
2.3.4 Isomerasi
Apabila pada larutan asam encer monosakarida dapat stabil, tidak demikian halnya apabila monosakarida dilarutkan dalam basa encer. Glukosa dalam larutan basa encer akan sebagian berubah menjadi fruktosa dan manosa sehingga tidak stabil (Poedjiadji, 2005, Hal 44).
III BAHAN DAN METODE PERCOBAAN
Bab ini akan membahas mengenai : (1) Bahan yang digunakan, (2) Alat-alat yang digunakan dan (3) Metode Percobaan.
3.1. Bahan yang digunakan
Bahan yang digunakan untu uji molisch adalah sampel vitamin B kompleks, mayonaise, madu dan saus sambal, dan air mineral. Pereaksi yang digunakan adalah larutan molisch dan H2SO4 .
3.2 Alat-alat yang digunakan
Alat-alat yang digunakan pada uji molisch antara lain tabung reaksi, rak tabung, pipet tetes, gelas kimia, tangkrus dan penangas air.
3.3 Metode Percobaan
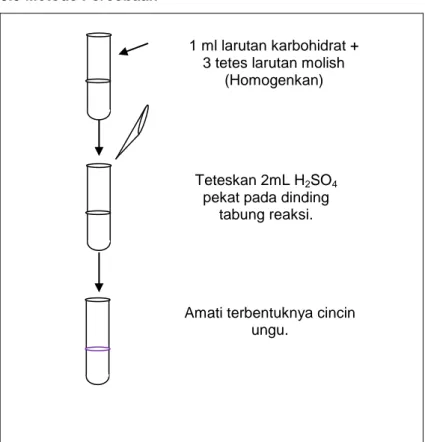
Gambar 3. Metode Percobaan Uji Molish 1 ml larutan karbohidrat +
3 tetes larutan molish (Homogenkan)
Teteskan 2mL H2SO4 pekat pada dinding
tabung reaksi.
Amati terbentuknya cincin ungu.
IV HASIL PENGAMATAN DAN PEMBAHASAN Bab ini akan membahas mengenai : (1) Hasil pengamatan dan (2) Pembahasan.
4.1. Hasil Pengamatan
Berdasarkan percobaan yang dilakukan maka didapatkan hasil pengamatn sebagai berikut :
Tabel 1. Hasil Pengamatan Uji Molish
(Sumber : Meja 2, Asri, Cholilah, 2013) Keterangan : (+) Terbentuk Cincin Ungun
(-) Tidak Terbentuk Cincin Ungu
Gambar 1. Hasil Percobaan Uji Molisch
Bahan Pereaksi Warna Hasil Keterangan Mayonnaise (B) Larutan Molish dan H2SO4 pekat Cincin ungu + Terdapat karbohidrat Vitamin B kompleks (A) Cincin ungu + Terdapat karbohidrat Saus sambal (L) Cincin ungu + Air mineral (K) Putih keruh - Tidak terdapat karbohidrat Madu (J) Cincin ungu + Terdapat karbohidrat
4.2. Pembahasan
Berdasarkan hasil pengamatan dari uji molish dapat disimpulkan bahwa sampel mayonaise (B), vitamin B kompleks (A), saus sambal (L), madu (J) mengandung karbohidrat karena terdapat cincin ungu.
Percobaan Uji Molish ini menggunakan larutan molish sebagai salah satu pereaksi yaitu larutan dari 100 gram alfanaftol dalam 100 ml alkohol.Karbohidrat oleh asam sulfat akan dihidrolisa menjadi monosakarida dan selanjutnya monosakarida akan mengalami dehidrasi oleh asam sulfat menjadi furfural atau hidroksi metil furfural. Furfural atau hidroksi metil furfural dengan alfa naftol akan berkondensasi membentuk senyawa kompleks yang berwarna ungu. Apabila pemberian asam sulfat pada larutan karbohidrat yang telah diberi alfa naftol dilakukan secara hati-hati melalui dinding gelas secara maka warna ungu yang terbentuk berupa cincin pada batas antara larutan karbohidrat dengan asam sulfat (Sudarmadji, 2007, Hal 77).
Pada uji molisch fungsi -naftol sebagai pereaksi agar terbentuknya cincin ungu sedangkan alcohol berfungsi untuk melindungi agar karbohidrat tidak rusak ketika H2SO4 dimasukkan ke dalam sampel.
H2SO4 bisa diganti dengan asam kuat yang bersifat sama dengan asam sulfat. Biasanya terdapat pada golongan IA (Shevla, 1985, Hal 450).
Pada percobaan uji molish dengan menguji kelima sampel larutan karbohidrat yang telah ditetesi dengan pereaksi molish selanjutnya dihidrolisis dengan asam sulfat pekat (H2SO4) maka terjadi pemutusan ikatan glikosidik dari rantai karbohidrat polisakarida menjadi disakarida dan monosakarida. Hal ini terlihat jelas dengan adanya perubahan warna pada keempat tabung reaksi yang berisikan larutan karbohidrat tersebut. Larutan yang bereaksi positif akan memberikan cincin yang berwarna ungu ketika direaksikan dengan alfa-naftol dan asam sulfat pekat.
Asam sulfat pekat bertindak sebagai agen dehidrasi yang bertindak pada gula untuk membentuk furfural dan turunannya yang kemudian dikombinasikan dengan alfa-naftol
untuk membentuk produk berwarna. Reaksi pembentukan furfural ini adalah reaksi dehidrasi atau pelepasan molekul air dari suatu senyawa. Dimana pereaksi molish membentuk cincin berwarna ungu pada larutan glukosa, fruktosa, laktosa, sukrosa, dekstrin dan amilum. Cincin ungu pada glukosa dan fruktosa lebih banyak karena merupakan monosakarida. Sedangkan amilum adalah polisakarida yang harus dihidrolisis menjadi monosakarida terlebih dahulu sebelum terdehidrasi menjadi furfural. Berdasarkan prinsip percobaan dengan uji molish, hasilnya (fulfural) mengalami sulfonasi dengan alfa naftol dan memberikan senyawa berwarna ungu kompleks (Herdiansyah, 2013).
Semua jenis karbohidrat baik mono, di, maupun polisakarida akan berwarna merah apabila larutannya (dalam air) dicampur dengan beberapa tetes larutan alpha-naftol (dalam alkohol) dan kemudian dialirkan pada asam sulfat pekat dengan hati-hati sehingga tidak tercampur. Warna merah akan tampak pada bidang batas antara campuran karbohidrat denganalpha-naftol dan asam sulfat pekat, sifat ini dipakai sebagai dasar uji kualitatif adanya karbohidrat dan dikenal sebagai uji molisch (Sudarmadji, 2007, Hal 73).
Penambahan H2SO4 pekat pada percobaan ini dikarenakan monosakarida umumnya stabil dalam larutan asam encer yang dipanaskan. Tetapi apabila dipanaskan dengan asam kuat yang pekat, monosakarida menghasilkan furfural atau derivatnya. Reaksi pembentukan furfural ini adalah reaksi dehidrasi atau pelepasan molekul air dari suatu senyawa (Poedjiadi,2005, Hal 41).
Percobaan uji molisch ini apabila pereaksi ini dtitambahkan pada larutan glukosa misalnya, secara hati-hati ditambahkan asam sulfat pekat akan terbentuk dua lapisan zat cair. Pada batas antara kedua lapisan itu akan terjadi warna ungu karena terjadi kondensasi antara furfural dengan alfa naftol. Ketika memasukkan H2SO4 pada tabung reaksi harus di teteskannya dengan perlahan dan hati-hati agar tidak terkena langsung pada sampel karbohidratnya karena H2SO4 akan bereaksi dengan karbohidrat. yang melindungi karbohidrat agar tidak rusak yaitu alkohol.
Konsentrasi asam sulfat pekat bertindak sebagai agen dehidrasi yang bertindak pada gula untuk membentuk furfural dan turunannya yang kemudian dikombinasikan dengan α-naftol untuk membentuk produk berwarna. Jika H2SO4 terlalu banyak ditambahkan maka hasil percobaan akan berwarna ungu semua. Apabila sampel yang sudah ditambahkan dengan asam sulfat pekat dibiarkan kontak dengan udara maka cincin berwarna ungu yang terbentuk lama-lama akan hilang. Hal ini dikarenakan asam sulfat pekat akan bereaksi dengan udara.
Pada hasil praktikum yang diperoleh seharusnya sampel vitamin B kompleks (A) tidak mengandung karbohidrat sedangkan hasil dari laboratorium menunjukkan bahwa sampel tidak mengandung karbohidrat. Kesalahan yang dilakukan kurang teliti dalam percobaan, mungkin dari cara meneteskan H2SO4 yang tidak teliti sehingga terjadi kesalahan.
V KESIMPULAN DAN SARAN
Bab ini akan membahas mengenai : (1) Kesimpulan, dan (2) Saran.
5.1 Kesimpulan
Berdasarkan hasil pengamatan dari uji molish dapat disimpulkan bahwa sampel mayonaise (B), vitamin B kompleks (A), saus sambal (L), madu (J) mengandung karbohidrat karena terdapat cincin ungu setelah larutan diberi pereaksi 3 tetes larutan molish dan 2 mL H2SO4 .
5.2 Saran
Saran yang diberikan oleh praktikan perlu ketelitian dalam uji molish ini karena jika kurang teliti akan mempengaruhi hasil yang diperoleh.
DAFTAR PUSTAKA Herdiansyah, Erick, (2013), Karbohidrat,
http://monruw.wordpress.com, Accessed : 18 Maret 2013.
Shevla, G, (1985), Analisis Anorganik Kualitatif Makro dan Semi Makro, Kalman Media Pusaka, Jakarta.
Sudarmadji, Slamet, (2007).Analisa Bahan Makanan dan Pertanian. Penerbit Liberty, Yogyakarta
Poedjiadi, Anna, (2005), Dasar-Dasar Biokimia Edisi Revisi, Jakarta : Universitas Indonesia.
Winarno, F G, (1997), Kimia Pangan dan Gizi, Jakarta : PT Gramedia Pustaka Utama