AKTIVITAS RENNET TERSEMI-PURIFIKASI Mucor pusillus
DI BERBAGAI KONSENTRASI PADA KOAGULASI
PROTEIN SUSU PASTEURISASI
(Activities of Semi-Purified Rennet Mucor pusillus in Various Concentrations
on Protein Coagulation of Pasteurised Milk)
RINI HANDAYANI danT.KHUSNIATI
Pusat Penelitian Biologi LIPI, Jl. Raya Km. 46 Cibinong, Bogor 16911
ABSTRACT
Microbial rennet is a proteolytic enzyme that coagulates protein of milk in cheese fermentation. In order to asses the activities of rennet M. pusillus in coagulating milk, the activities of semi-purified rennet M.
pusillus at various concentrations weas observed for protein coagulation of pasteurised milk.
Semi-purification of rennet were conducted by using ammonium sulphate and ethanol. The coagulation activities were measured following the method of Somkuti and Babel, and protein contents were detected by Kjeldahl method. The results showed that the concentration of 60% ammonium sulphate and 50% ethanol was better for semi-purification of rennet M. pusillus. The coagulation activities of skim milk treating with 60% NH4OH and 50% ethanol of semi-purified rennet M. pusillus were higher than whole milk. The coagulation activities of skim milk of 60% NH4OH and 50% ethanol semi-purified rennet M. pusillus were 14.0845 RU/mL and 76.923 RU/mL, respectively, while in whole milk were 9.5238RU/ml and 19.2308RU/ml. In contrast to, the protein content of skim milk were lower than that of whole milk. The protein contents of skim milk were 0.049% and 0.0372%, respectively, while the protein content of whole milk were 0.0550% and 0.0435%. It is concluded that semi-purified rennet M. pusillus was better coagulant for skim and whole milk.
Key Words: Rennet, Semi-Purification, Pasteurized Milk, Protein, Mucor pusillus
ABSTRAK
Renet mikroba mengandung enzym proteolitik yang mengkoagulasi protein susu dalam fermentasi keju. Untuk mengetahui sejauh mana aktivitas rennet M. pusillus mengkoagulasi susu, aktivitas rennet M. pusillus tersemi-purifikasi dalam berbagai konsentrasi pada koagulasi protein susu pasteurisasi diamati. Rennet tersemi-purifikasi dilakukan dengan menggunakan ammonium sulfat dan etanol, aktivitas koagulasi diukur dengan metode Somkuti dan Babel, sedangkan kandungan protein dideteksi dengan metoda Kjeldal. Hasil penelitian menunjukkan bahwa konsentrasi terbaik dari amonium sulfat untuk semi-purifikasi renet M.
pusillus adalah 60%, sedangkan konsentrasi terbaik dari etanol adalah 50%. Aktivitas koagulasi susu skim
dengan penambahan renet M. pusillus tersemi-purifikasi menggunakan amonium sulfat 60%. dan etanol 50% lebih tinggi dibandingkan pada susu berlemak dengan perlakuan yang sama. Aktivitas koagulasi susu skim dengan penambahan renet M. pusillus tersemi-purifikasi dengan amonium sulfat 60% dan etanol 50% adalah masing-masing 14.0845 RU/mL dan 76.923 RU/mL, sedangkan aktivitas koagulasi susu berlemak dengan perlakuan yang sama adalah 9.5238RU/mL dan 19.2308RU/mL. Sebaliknya, kandungan protein susu skim dengan penambhan renet M. pusillus tersemi-purifikasi dengan amonium sulfat 60% dan etanol 50% lebih rendah dibandingkan susu berlemak dengan perlakuan yang sama. Kandungan protein susu skim dengan penambahan rennet M. pusillus tersemi-purifikasi dengan amonium sulfat 60% dan etanol 50% adalah masing-masing 0,049% dan 0,0372%, sedangkan kandungan protein pada susu berlemak dengan perlakuan yang sama adalah 0,0550% dan 0,0435%. Berdasarkan koagulasi protein, disimpulkan bahwa renet M.
pusillus tersemi-purifikasi adalah baik untuk koagulasi susu skim dan susu berlemak. Kata Kunci: Renet, Semi-Purifikasi, Susu Pasteurisasi, Protein, Mucor pusillus
PENDAHULUAN
Susu adalah sumber nutrisi yang lengkap dengan nutrisi utama adalah karbohidrat, protein, lemak, vitamin dan mineral. Nutrisi ini adalah komponen-komponen penting untuk kesehatan manusia (JUDKINS dan KEENER, 1990). Susu juga sebagai media lengkap untuk pertumbuhan berbagai mikroorganisme (BROWN et al., 1984; CHANDLER et al., 1990;
DEETH et al., 2002). Pertumbuhan
mikroorganisme yang dikarenakan kontaminasi menyebabkan kerusakan (DEETH et al., 2002). Beberapa nutrisi penting, seperti: protein, vitamin B12 dan lipid terlarut pada susu berubah komposisinya pada waktu terjadi kontaminasi (GRIFFITH, 1989; HSU, 1984; JANZEN et al., 1982). Oleh karena itu, susu dapat diproses menjadi keju untuk menjaga nutrisi susu (ADAM, 1985; CHEESMAN, 1981; STENBERG, 1976). Curd dan whey dalam keju dipisahkan selama fermentasi (CHEESMAN, 1981; STENBERG, 1976), dan dengan penambahan rennet, koagulasi dalam keju dapat terjadi (CHEESMAN, 1981; STENBERG, 1976).
Rennet adalah ensim proteolitik yang mengkoagulasi susu (STENBERG, 1976; AINSWORTH et al., 1973; WISEMAN, 1977). Koagulasi susu dapat terjadi dikarenakan aktivitas proteolitik dari chimosin atau rennin dalam rennet (STENBERG, 1976; SOMKUTI dan BABEL, 1968; WISEMAN, 1977). Rennet pertama kali diekstraksi dari abomasum babi (CHEESMAN, 1981; STENBERG, 1976). Karena babi tidak dikonsumsi oleh masyarakat muslim, sehingga rennet babi diganti dengan rennet anak sapi yang diekstraksi dari abomasums anak sapi. Dikarenakan daging sapi dikonsumsi secara regular oleh manusia, anak sapi dipelihara hingga menjadi sapi untuk konsumsi daging, akibatnya, anak sapi tidak dapat digunakan sebagai sumber rennet. Oleh karena itu, untuk memecahkan masalah ini, ada sumber mikroba yang baik untuk rennet yatu rennet mikroba dari Mucor pusillus (SOMKUTI dan BABEL, 1968; STENBERG,1976).
Kelebihan rennet mikroba dibandingkan rennet abomasum anak sapi adalah karena pertumbuhan mikroorganisme lebih cepat daripada pertumbuhan anak sapi, dan mikroorganisme adalah lebih tahan terhadap
pH dibandingkan dengan anak sapi (CHEESMAN, 1981; STENBERG, 1976). Beberapa penelitian melaporkan bahwa rennet mikroba kasar mempunyai potensi yang tinggi untuk mengkoagulasi susu (CHEESMAN, 1981; STENBERG, 1976). Tujuan dari penelitian ini adalah untuk mendeteksi aktivitas rennet Mucor pusillus tersemi-purifikasi dalam berbagai konsentrasi pada koagulasi protein susu pasteurisasi.
MATERI DAN METODE Preparasi media
Sejumlah 200 g tauge dicampur dengan 2 l aquades, dan kemudian dididihkan sampai mencapai titik didih. Pendidihan kemudian dilanjutkan selama 1 jam dimulai ketika air mendidih. Ekstrak tauge disaring dan filtrat ditampung. Sejumlah 1 l tauge ekstrak dicampur dengan 20 g bakto agar dan 60 g gula. Campuran kemudian dipanaskan hingga semua bakto agar larut dalam ekstrak. Media agar tauge kemudian disterilkan dalam autoclave pada suhu 121°C selama 15 menit. Media agar tauge kemudian siap digunakan untuk pertumbuhan M. pusillus.
Pertumbuhan M. pusillus
M. pusillus diambil dari working stock jarum ose yang sudah disterilisasi. Miselia digoreskan pada media agar miring tauge dan kemudian diinkubasikan pada suhu 35°C selama 1 minggu.
Preparasi suspensi M. pusillus
Miselia M. pusillus yang tumbuh pada media agar miring "tauge" selama 1 minggu pada suhu 35°C diambil dengan jarum "ose" yang sudah disterilisasi. Miselia dicampur dengan 15 mL aquades steril dalam tabung reaksi besar, dan kemudian dibuat suspensi dengan menggunakan waring blender selama 15 menit. Suspensi diukur absorbansinya dengan menggunakan spektrophotometer λ 540 nm. Suspensi dilarutkan dengan air steril, jika nilai absorban lebih dari 0,5.
Produksi rennet
Sejumlah 17,5 g media dedak dituangkan kedalam petridish dan kemudian disterilisasi. Media yang sudah steril diinokulasi dengan suspensi sebesar 1,75 ml M. pusillus dan kemudian diinkubasi pada suhu 35°C selama 2 – 4 hari.
Ekstraksi rennet
Media yang diinokulasi jamur dipindahkan ke dalam Erlenmeyer 300 ml, dan media yang sudah dipindahkan ditambahkan aquades steril 52,5 ml dan 3 ml toluene untuk mematikan mikroorganisme lainnya. Ekstraksi rennet dilakukan dengan goyangan selama 75 menit. Ekstrak rennet disaring dan filtrat ditampung dalam erlenmeyer.
Tabel 1. Beberapa step dalam proses produksi
rennet M. pusillus
Step proses produksi Produk Preparasi media Media selektif tauge agar
untuk pertumbuhan M.
pusillus
Pertumbuhan
M. pusillus
M. pusillus dalam media
miring selektif dari tauge agar used as the source of
rennet
Preparasi suspensi
M. pusillus
Suspensi M. pusillus untuk ekstraksi rennet
Produksi rennet Produksi rennet dari suspensi
M. pusillus dalam media
dedak yang sudah disterilisasi Ekstraksi rennet Filtrat rennet untuk
semi-purifikasi dengan menggunakan
etanol/ammonium sulfat
Presipitasi dengan amonium sulfat
Larutan enzim dipresipitasi dengan amonium sulfat hingga konsentrasi 60%. Larutan dihomogenisasi dengan magnetic shaker dalam kotak es. Larutan enzim yang sudah dihomogenisasi dan amonium sulfat disimpan sepanjang malam dalam suhu dingin dan kemudian disentrifus. Presipitasi yang
diperoleh dilarutkan dalam 5 ml buffer sitrat pada pH 4 atau 5.
Presipitasi dengan etanol
Larutan enzim dipresipitasi dengan etanol hingga konsentrasi 50%. Larutan dihomogenkan dengan magnetic shaker dan dilakukan dalam kotak es. Larutan enzim yang sudah dihomogenisasi dan etanol disimpan sepanjang malam dalam ruang pendingin, dan kemudian disentrifus. Presipitasi yang diperoleh dilarutkan dalam 5 ml buffer sitrat pada pH 4 atau 5.
Aktivitas koagulasi
Deteksi aktivitas koagulasi menggunakan metode SOMKUTI dan BABEL (1976). Sejumlah 10 ml susu dituang kedalam tabung reaksi dan dikontrol suhunya hingga 35oC, dan kemudian ditambahkan 1 ml ekstrak rennet. Aktivitas koagulasi diamati, yaitu: waktu ketika presipitasi kecil muncul pada dinding tabung reaksi. Aktivitas koagulasi: T.R. RU/ml Q 10x dimana:
Q : jumlah susu yang digunakan (ml) R : jumlah enzim yang digunakan (ml)
T : waktu koagulasi (menit) RU/ml: renin unit/mililiter
Kandungan protein (APRIYANTONO et al., 1989)
Sejumlah sampel ditimbang, dan kemudian dituangkan ke dalam tabung Kjeldahl dan ditambahkan selenium dan 3 ml HC1 37%. Campuran reaksi didestruksi hingga sempurna (warna larutan adalah putih atau jernih), dan kemudian didinginkan dan dilarutkan hingga mencapai leher tabung. Campuran reaksi dipindahkan kedalam tabung yang sudah mendidih dan kemudian dilarutkan dengan air destilasi hingga mencapai 100 ml.
Peralatan destilasi disambung dengan Erlenmeyer 100 ml, dan kemudian disambung dengan peralatan destilasi. Tabung yang sudah dididihkan ditambah 20 ml NaOH 30% dan
kemudian ditutup cepat dan didestilasi hingga warna larutan yang diperoleh adalah hijau dengan volume kurang lebih 75 ml, dan kemudian dititrasi dengan HC1 37% hingga warna hijau menjadi merah dan kemudian dicatat volume titrasi. Hal ini juga dilakukan dalam kontrol.
Analisa statistik (SNEDECOR dan COHRAN, 1989)
Semua sampel yang sudah mendapat perlakuan dianalisa secara statistik dengan ANOVA menggunakan General Linear Model, tiga kali ulangan
HASIL DAN PEMBAHASAN
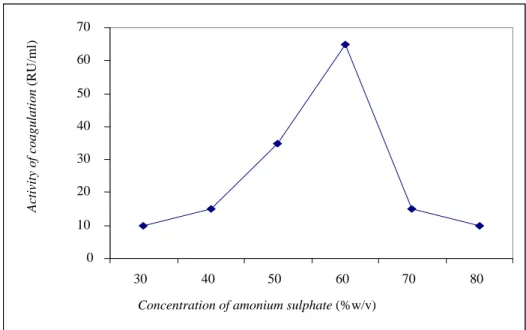
Rennet M. pusillus mempunyai aktivitas koagulasi yang paling tinggi dalam larutan enzim yang dihasilkan dari presipitasi amonium sulfat dengan konsentrasi 60% seperti diperlihatkan pada Gambar 1. Hal ini kemungkinan karena pada konsentrasi tersebut diatas, enzim ynag sudah disemi-purifikasi
(rennin) dipresipitasi secara maksimal hingga enzim tersebut mempunyai nilai aktivitas koagulasi paling tinggi dibandingkan pada konsentrasi-konsentrasi lainnya (ADAM, 1985; CHEESMAN, 1981; STENBERG, 1976).
Pada konsentrasi amonium sulfat kurang dari 60%, aktivitas koagulasi lebih rendah dibandingkan pada konsentrasi amonium sulfat yang sama dan lebih dari 60%. Hal ini kemungkinan dikarenakan pada konsentrasi ammonium sulfat yang lebih tinggi menyebabkan lebih banyak enzim yang terlarut (SOMKUTI dan BABEL, 1968; WISEMAN, 1977). Pada konsentrasi amonium sulfat yang lebih dari 60%, aktivitas koagulasi lebih tinggi dibandingkan pada konsentrasi ammonium sulfat yang sama dan kurang dari 60%. Hal ini kemungkinan karena pada konsentrasi tersebut, tidak hanya rennin yang terpresipitasi tetapi juga enzim lainnya (ADAM, 1985; CHEESMAN, 1981; STENBERG, 1976). Semakin tinggi konsentrasi amonium sulfat yang digunakan, semakin rendah konsentrasi enzim yang didapatkan (STENBERG, 1976; WISEMAN, 1977).
Gambar l. Aktivitas koagulasi dari presipitate oleh amonium sulfat 0 10 20 30 40 50 60 70 30 40 50 60 70 80
Concentration of amonium sulphate (%w/v)
Activity o
f
coagu
lation
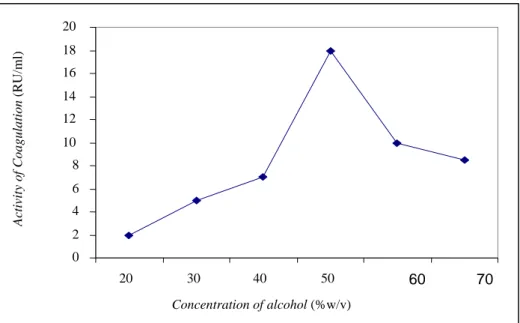
Aktivitas koagulasi yang paling tinggi dari enzim M pusillus yang terpresipitasi diantara berbagai konsentrasi alkohol adalah pada konsentrasi alkohol 50%. Hasil deteksi aktivitas koagulasi rennet yang tersemipurifikasi dari presipitasi dengan alkohol dapat dilihat pada Gambar 2.
Metode presipitasi protease dengan larutan organik dilakukan pada suhu dibawah 2°C, Hal ini bertujuan untuk menghindari denaturasi enzim. Larutan organik yang digunakan adalah larutan yang tidak diaktifkan oleh enzim yang sudah dipurifikasi.
Pada aktivitas koagulasi, ada perbedaan dalam nilai-nilai aktivitas. Perbedaan dalam nilai-nilai aktivitas koagulasi adalah dikarenakan kemampuan yang tinggi dari
koagulasi susu atau degradasi protein dan kemampuan hidrolisis dari masing-masing enzim (ADAM, 1985; CHEESMAN, 1981; STENBERG, 1976). Semi-purifikasi dari presipitasi dengan alkohol dan ammonium sulfat tidak meningkatkan aktivitas koagulasi rennet M. pusillus. Hal ini kemungkinan karena alkohol mendenaturasi rennet M. pusillus, dan ammonium sulfat menginaktivasi rennet (ADAM, 1985; CHEESMAN, 1981; STENBERG, 1976). Aktivitas rennin yang terpresipitasi dengan ammonium sulfat 60% dan alkohol 50% dalam susu skim lebih tinggi dibandingkan dalam susu berlemak (ADAM, 1985; CHEESMAN, 1981; STENBERG, 1976). Aktivitas koagulasi rennin dalam susu berlemak dan susu skim ditunjukkan dalam Tabel 2.
Gambar 2. Aktivitas koagulasi dari presipitasi dengan alkohol
Tabel 2. Aktivitas koagulasi rennin dalam susu berlemak dan susu skim
Susu berlemak Susu skim
Presipitasi Waktu koagulasi (menit) Aktivitas koagulasi (RU/ml) Waktu koagulasi (menit) Aktivitas koagulasi (RU/ml)
Amonium sulfat 60% 10.50a 9.5238c 7.10e 14.0845g
Etanol 50% 5.20b 19.2308d 1.30f 76.923Ih
Huruf-huruf yang berbeda menunjukkan perbedaan yang nyata (P <0,05) 0 2 4 6 8 10 12 14 16 18 20 20 30 40 50 60 70 Concentration of alcohol (%w/v) A ctivity o f Coag ulation (RU/ml)
Kandungan protein rennet tersemi-purifikasi dalam susu berlemak lebih tinggi dibandingkan dalam susu skim. Hal ini kemungkinan karena pada tahapan semi-purifikasi, presipitasi dengan amonium sulfat dan etanol dalam susu berlemak lebih efektif dibandingkan dalam susu skim (STENBERG, 1976; WISEMAN, 1977). Kandungan protein dalam susu berlemak dan susu skim ditunjukkan dalam Tabel 3.
Tabel 3. Kandungan protein dalam susu berlemak dan susu skim
Kandungan protein (%) Presipitasi
Susu berlemak Susu skim Amonium sulfat 60% 0.0550a 0.0497c Etanol 50% 0.0435b 0.0372d Huruf-huruf berbeda menunjukkan perbedaan yang nyata (P < 0,05)
KESIMPULAN
Konsentrasi yang paling baik dari ammonium sulfat untuk semi-purifikasi rennet M. pusillus adalah 60%, sedangkan konsentrasi yang paling baik dari etanol adalah 50%. Aktivitas koagulasi susu skim dengan penambahan rennet tersemi-purifikasi M. pusillus dengan menggunakan ammonium sulfat 60% dan etanol 50% lebih tinggi dibandingkan dari susu berlemak. Sebaliknya, kandungan protein susu skim dengan penambahan rennet tersemi-purifikasi M. pusillus dengan ammonium sulfat 60% dan etanol 50% lebih rendah dibandingkan pada susu skim. Berdasarkan koagulasi protein, dapat disimpulkan bahwa rennet tersemi-purifikasi M. pusillus adalah baik untuk koagulasi susu berlemak dan susu skim.
DAFTAR PUSTAKA
ADAM, M.R. 1985. Microbiology of fermented foods. Vol 1. WOOD,B.J.B. (Ed.). New York, NY: Elsevier.
APRIYANTONO,A.,F.DEDI,P.NI LUH,SEDARNAETI
and B. SLAMET. 1989. Food Analysis. (In Indonesian). The Inter University Center of Food and Nutrition, Bogor Agricultural University.
BROWN.J.V.,H.M.P.RANJITH and G.A.PRENTICE. 1984. Comparative shelf lives of skimmed, semi-skimmed and whole milks. J. Soc. Dairy Technol. 37: 132 – 134.
CHANDLER, R.E., S.Y. NG and R.R. HULL. 1990. Bacterial spoilage of specialty rnilk products. Food Research Quarterly. 50: 11 – 14. CHEESMAN,G.C. 1981. Rennet and Cheese Making.
In: Parker. Enzymes and Food Processing . Briek, G.G., N. Blakebrough and K.J. Appl. Sci. Publ. Ltd. London.
DEETH, H.C., T. KHUSNIATI, N. DATTA and R.B. WALLACE. 2002. Spoilage patterns of skim and whole milks at storage. J. Dairy Sci. U.K.. GRIFFITH. 1989. Effect of temperature and milk fat
on extracellular enzyme synthesis psychrotrophic bacteria during milk. Milchwissenschaft. 44: 539 – 543.
HSU, H.Y. 1984. Methods for measuring the activities of bacterial and native proteinases milk and a study of factors affecting milk protein hydrolysis. Ph.D. Thesis. Cornell University, Ithaca, USA.
JANZEN, J.L, J.R. BISHOP and A.B.BODINE. 1982. Relationship of protease activity, to shelf life, of skim and whole milk. J. Dairy Sci. 65: 1237 – 1240.
JUDKINS, H.E. and H.A. KEENER. 1990. Milk Production and Processing. John Wiley & Sons, New York.
SNEDECOR, G.W. and W.G. COHRAN. 1989. Statistical Methods, 8th Edn, Iowa State University, Ames, Iowa.
SOMKUTI and F.J.J. BABEL. 1968. Acid protease synthesis by M. pusillus in chemically define media. J. Biotechnol. 95: 1415 – 1418. STENBERG,M. 1976. Microbial rennet. In Perlman,
T. J. Appl. .Microbiol. 20: 136 – 147.
WISEMAN, A. 1977. Stabilization of enzymes. In Enzyme Technology. John Wiley and Sons. New York.