1
STABILITAS EKSTRAK PIGMEN DARI BUAH LAKUM (Cayratia trifolia (L.) Domin)
DAN APLIKASINYA SEBAGAI PEWARNA PANGAN
Hilaria Defena Panarigas1*, Nora Idiawati1
1
Program Studi Kimia, Fakultas MIPA, Universitas Tanjungpura, Jl. Prof. Dr. H. Hadari Nawawi, Pontianak, 78124
*
email: hilary.dev2@gmail.com
ABSTRAK
Pigmen dari buah lakum berpotensi untuk dimanfaatkan sebagai pewarna alami pada produk pangan. Ekstraksi pigmen buah lakum telah dilakukan menggunakan pelarut air selama 2 jam pada suhu 70oC. Uji stabilitas warna dilakukan terhadap penambahan gula sukrosa 0, 10, 20, 30, 40 dan 50%, penambahan garam NaCl 0, 2, 4, 6, 8 dan 10%, lama penyimpanan selama 18 hari pada suhu ruang dan pada suhu refrigerator serta pemanasan pada suhu air mendidih selama 0, 30, 60, 90 dan 120 menit. Analisis stabilitas warna dilakukan dengan mengukur perubahan absorbansi larutan pigmen menggunakan spektrofotometer UV-Vis pada panjang gelombang 531 nm. Kondisi dengan stabilitas terbaik diperoleh dari penambahan gula 10%, penambahan garam 4%, penyimpanan pada suhu 4oC dan lama pemanasan 30 menit, masing-masing dengan presentase perubahan absorbansi sebesar 0,10%, 2,88%, 5,58% dan 17,05%. Ekstrak pigmen kemudian diaplikasikan pada produk minuman dingin dan agar-agar. Berdasarkan uji organoleptik, diketahui bahwa penambahan ekstrak pigmen yang paling disukai untuk minuman dingin dan agar-agar adalah 7,5% V/V masing-masing dengan nilai 3,40 dan 3,20. Karakteristik dari produk yang dihasilkan adalah berbau sedikit harum khas buah lakum, berasa sedikit asam dan berwarna merah.
Kata kunci: buah lakum, pigmen, stabilitas, organoleptik
PENDAHULUAN
Antosianin merupakan salah satu kelompok zat warna alami (pigmen) yang memberikan warna merah muda, merah tua, ungu dan biru pada daun, bunga dan buah dari tumbuhan (Winarno, 1995). Beberapa tumbuhan yang kaya akan antonianin telah digunakan sebagai pewarna alami pada bahan pangan, seperti buah anggur dan stroberi. Pewarna alami telah lama digunakan sebagai pewarna pangan dan hingga saat ini penggunaannya masih dianggap lebih aman dari pada pewarna sintetik (Koswara, 2009). Sebagai contoh: daun suji digunakan untuk mewarnai serabi dan dadar gulung serta kunyit lazim digunakan untuk mewarnai nasi kuning dan tahu (Winarno, 1995). Penggunaan pigmen antosianin di Indonesia telah diizinkan
berdasarkan Permenkes RI
No.033/MENKES/PER/2012 tentang Bahan Tambahan Pangan. Di samping perannya sebagai pewarna pangan, antosianin juga memiliki beberapa manfaat bagi kesehatan. Beberapa penelitian menyatakan bahwa antosianin dapat berfungsi sebagai anti-alergi, inflamasi, virus, mutagenik, anti-mikroba, pencegah diabetes dan perlindung terhadap kerusakan jantung pada manusia (Ghosh and Konishi, 2007).
Salah satu tumbuhan di Kalimantan Barat yang berpotensi untuk digunakan sebagai sumber pigmen antosianin adalah lakum. Lakum
(Cayratia trifolia (L.) Domin) merupakan
tumbuhan perdu yang tumbuh secara liar dan banyak terdapat di Kalimantan Barat. Lakum memiliki buah yang berwarna ungu kehitaman setelah matang (Yeo, et al., 2012). Warna ungu pada buah lakum ini menunjukkan adanya pigmen dari golongan antosianin (Neliyanti dan Idiawati, 2014). Pigmen inilah yang menyebabkan lakum berpotensi digunakan sebagai pewarna alami. Pemanfaatan buah lakum sebagai pewarna alami pada bahan pangan telah dilakukan oleh Rezeki, et al. (2011), yaitu sebagai bahan baku dalam pembuatan sirup dan selai.
Widhiana, et al. (2012) telah melakukan penelitian yang menunjukkan bahwa ekstrak buah lakum ungu mengandung golongan senyawa flavonoid, saponin dan alkaloid, sehingga berpotensi sebagai antioksidan. Informasi ini menunjukkan bahwa penggunaan buah lakum sebagai pewarna alami dapat memberikan nilai tambah pada bahan pangan, yaitu sebagai antioksidan.
2 Gambar 1. Buah Lakum
Salah satu faktor yang perlu
diperhatikan pada penggunaan pewarna pada bahan pangan adalah kestabilan warna yang dihasilkan. Pewarna yang memiliki warna lebih stabil umumnya lebih disukai oleh konsumen. Dalam aplikasinya sebagai pewarna pangan, pigmen lakum biasanya dicampurkan dengan berbagai bahan lain
yang dapat meningkatkan cita rasa
makanan, seperti gula dan garam. Pewarna pangan juga diproduksi melalui beberapa proses pengolahan bahan pangan, seperti
pemanasan dan penyimpanan. Proses
pencampuran dan pengolahan bahan
pangan tersebut dapat mempengaruhi
stabilitas pigmen yang digunakan sehingga mempengaruhi kualitas dari warna yang dihasilkan.
Oleh karena itu, pada penelitian ini dilakukan uji stabilitas pigmen buah lakum terhadap penambahan gula dan garam serta
lamanya proses pemanasan dan
penyimpanan. Data stabilitas ekstrak pigmen diamati dari pengukuran absorbansi untuk menentukan kualitas warna yang dihasilkan. Pigmen alami dari buah lakum yang diperoleh juga diaplikasikan pada produk agar-agar dan minuman dingin untuk mengetahui variasi penambahan ekstrak pigmen yang paling disukai panelis serta karakteristik organoleptik dari produk pangan yang dihasilkan.
METODE PENELITIAN Alat dan Bahan
Alat-alat yang digunakan dalam
penelitian ini meliputi peralatan gelas standar, blender, bulb, hot plate, kertas saring, magnetic stirrer, neraca analitik, pH-meter, penyaring vakum, refrigerator, spektrofotometer UV-Vis (Genesys-6) dan thermometer.
Sampel yang digunakan berupa buah lakum matang dari Kecamatan Sungai Rengas, Kalimantan Barat. Bahan-bahan yang digunakan meliputi akuades, asam sitrat, gula sukrosa, natrium klorida, pewarna
sintetik, sirup komersial dan serbuk agar-agar.
Prosedur Penelitian
Ekstraksi Pigmen dari Buah Lakum
Sampel buah lakum matang ditimbang sebanyak 200 gram, Kemudian ditambahkan 200 mL akuades dan asam sitrat 2% b/v.
Buah lakum kemudian dihaluskan
menggunakan blender selama 3 menit, kemudian dipanaskan pada suhu 70oC selama 120 menit. Ekstrak kasar yang diperoleh kemudian disaring sehingga diperoleh ekstrak pigmen buah lakum (Neliyanti dan Idiawati, 2014).
Uji Stabilitas Ekstrak Pigmen dari Buah Lakum
Uji stabilitas pigmen dari buah lakum yang dilakukan meliputi uji stabilitas terhadap gula sukrosa, garam NaCl, lama pemanasan serta pengaruh suhu selama penyimpanan. Absorbansi larutan diukur pada panjang gelombang maksimum pigmen, yaitu 531 nm. Setiap pengukuran dilakukan dengan tiga kali pengulangan (triplo). Persentase
perubahan absorbansi dihitung
menggunakan persamaan berikut (Neliyanti dan Idiawati, 2014):
Keterangan:
A0 = Absorbansi mula-mula A1 = Absorbansi akhir
Pengaruh Kadar Gula Sukrosa
Prosedur ini mengacu pada penelitian Winarti, et al. (2008) dengan modifikasi pada lama penyimpanan. Sebanyak 5 mL ekstrak pigmen dituangkan ke dalam 6 buah wadah, kemudian ditambahkan 100 mL larutan gula sukrosa masing-masing dengan kadar 0, 10, 20, 30, 40 dan 50%, kemudian diaduk hingga homogen. Semua larutan disimpan di tempat gelap dan diukur absorbansinya setiap 24 jam pada panjang gelombang maksimum selama 7 hari berturut-turut.
Pengaruh Kadar Garam NaCl
Prosedur ini mengacu pada penelitian Winarti, et al. (2008) dengan modifikasi pada lama penyimpanan. Sebanyak 5 mL ekstrak pigmen dituangkan ke dalam 6 buah wadah, kemudian ditambahkan 100 mL larutan garam NaCl masing-masing dengan kadar 0,
3 2, 4, 6, 8 dan 10%, kemudian diaduk hingga homogen. Semua larutan disimpan di tempat gelap dan diukur absorbansinya setiap 24 jam pada panjang gelombang maksimum selama 7 hari berturut-turut.
Pengaruh Suhu Penyimpanan
Prosedur ini mengacu pada penelitian Saraswati dan Astutik (2011) dengan
modifikasi konsentrasi dan lama
penyimpanan. Sebanyak 10 mL ekstrak pigmen dicampurkan dengan akuades dan ditepatkan dalam labu ukur 250 mL. Dibagi larutan pigmen menjadi 2 bagian yang sama banyak, kemudian diukur absorbansi awal larutan pada panjang gelombang maksimum. Larutan pertama disimpan di tempat gelap pada suhu 28oC dan larutan kedua pada suhu 4oC. Absorbansi dari kedua larutan diukur kembali setiap 3 hari hingga hari ke-18.
Pengaruh Lama Pemanasan
Sebanyak 20 mL ekstrak pigmen dicampurkan dengan akuades dalam labu ukur 500 mL. Larutan pigmen diambil dan ditepatkan pada 5 buah labu ukur 50 mL, kemudian dituangkan ke dalam 5 buah gelas beaker. Masing-masing larutan dipanaskan selama 0, 30, 60, 90 dan 120 menit menggunakan hot-plate pada suhu air mendidih. Larutan kemudian ditepatkan kembali pada labu ukur 50 mL dan diukur absorbansinya pada panjang gelombang maksimum.
Aplikasi pada Produk Pangan
Ekstrak pigmen dari buah lakum
diaplikasikan pada 2 jenis produk pangan, yaitu minuman dingin dan agar-agar. Pada minuman dingin, ditambahkan pigmen lakum sebanyak 50 mL, 75 mL dan 100 mL serta
sirup anggur komersial pembanding
sebanyak 100 mL hingga volume larutan mencapai 1.000 mL. Pada agar-agar, ditambahkan pigmen lakum sebanyak 35 mL, 53 mL dan 70 mL serta pewarna ungu sintetik pembanding sebanyak 0,7 mL dalam larutan 700 mL.
Uji Organoleptik
Uji organoleptik dilakukan menggunakan metode angket terhadap 15 panelis semi terlatih yang terbiasa mencicipi produk pangan tersebut. Uji organoleptik yang digunakan adalah uji hedonik (kesukaan)
dan uji mutu hedonik. Uji mutu hedonik dilakukan untuk menentukan karakteristik produk yang dihasilkan. Karakteristik yang paling dominan diwakili oleh tingkat pilihan terbanyak (Setyaningsih, et al., 2010).
Uji hedonik dilakukan untuk menentukan variasi mana yang lebih disukai panelis.
Penilaian yang diberikan panelis
dikonversikan pada 5 tingkatan skala
hedonik masing-masing dengan skor
sebagai berikut: sangat suka (5), suka (4), cukup suka (3), kurang suka (2) dan tidak suka (1). Data yang diperoleh kemudian dianalisis secara statistik menggunakan analisis variansi (ANOVA) menggunakan metode Rancangan Acak Lengkap (RAL) dengan bantuan program SPSS. Produk yang paling disukai oleh responden diwakili oleh tingkat pilihan terbanyak (Setyaningsih, et al., 2010).
HASIL DAN PEMBAHASAN
Ekstraksi Pigmen dari Buah Lakum
Proses ekstraksi dilakukan selama 120 menit dengan bantuan pemanasan pada suhu 70oC. Pemilihan suhu ini didasarkan pada hasil penelitian Neliyanti dan Idiawati (2014) yang menunjukkan bahwa ekstraksi pigmen dari buah Lakum optimum pada suhu 70oC. Pemanasan pada proses ekstraksi dapat meningkatkan kecepatan perpindahan
massa dari solut ke solvent karena
temperatur dapat mempengaruhi nilai koefisien transfer massa dari suatu komponen (Mardiah, 2010). Akan tetapi, pemanasan pada suhu lebih tinggi dapat menurunkan jumlah pigmen yang terekstrak. Hal ini ditandai dengan menurunnya nilai absorbansi ekstrak yang disebabkan oleh dekomposisi pigmen (Sharifi dan Hassani, 2012).
Ekstrak kasar yang diperoleh kemudian disaring, sehingga diperoleh filtrat berwarna merah lembayung sebanyak 300 mL.
Adanya warna merah lembayung ini
menunjukkan adanya pigmen yang
terkandung dalam buah lakum, salah satunya adalah antosianin.
Berdasarkan hasil analisis yang telah
dilakukan, diketahui bahwa panjang
gelombang maksimum untuk ektrak pigmen buah lakum adalah 531 nm. Absorbansi tersebut masih berada pada rentang panjang gelombang antosianin, yaitu antara 457 – 560 nm (Harbone, 1996).
4
Stabilitas Ekstrak Pigmen Buah Lakum
Pengaruh Kadar Gula Sukrosa
Penambahan gula sukrosa dapat
meningkatkan stabilitas warna pigmen dari buah lakum. Warna larutan paling stabil diperoleh dari penambahan gula 10% yang
menghasilkan rata-rata persentase
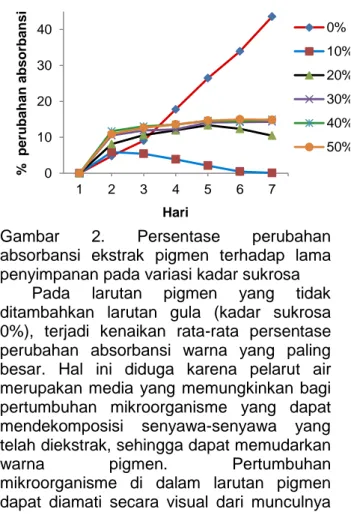
perubahan nilai absorbansi paling kecil. Penambahan gula dengan kadar 20% hingga 50% menyebabkan terjadinya penurunan stabilitas warna larutan secara signifikan yang ditandai dengan meningkatnya nilai persentase perubahan absorbansi larutan pigmen (Gambar 2). Data ini menunjukkan bahwa penambahan gula dengan kadar yang lebih tinggi dapat menyebabkan warna antosianin terdegradasi. Sudarmanto (1989)
menyatakan beberapa faktor yang
mempengaruhi laju kerusakan antosianin adalah lama penyimpanan, suhu tinggi dan peningkatan kadar gula. Hal ini diperkuat pula oleh hasil penelitian Nikkhah, et al. (2007) terhadap pigmen antosianin buah Beri menunjukkan bahwa pada kadar hingga 20%, gula dapat mempertahankan kestabilan antosianin, namun pada kadar yang tinggi dapat menyebabkan pigmen mengalami degradasi.
Gambar 2. Persentase perubahan
absorbansi ekstrak pigmen terhadap lama penyimpanan pada variasi kadar sukrosa
Pada larutan pigmen yang tidak
ditambahkan larutan gula (kadar sukrosa 0%), terjadi kenaikan rata-rata persentase perubahan absorbansi warna yang paling besar. Hal ini diduga karena pelarut air merupakan media yang memungkinkan bagi pertumbuhan mikroorganisme yang dapat mendekomposisi senyawa-senyawa yang telah diekstrak, sehingga dapat memudarkan
warna pigmen. Pertumbuhan
mikroorganisme di dalam larutan pigmen dapat diamati secara visual dari munculnya
jamur berupa benang-benang putih halus (hifa) pada dasar larutan yang mulai terlihat pada hari ketiga. Pada larutan pigmen-sukrosa 10%, pertumbuhan mikroorganisme mulai tampak sejak hari keempat, sedangkan larutan pigmen-sukrosa 20% dan 30% sejak hari kelima. Akan tetapi, pada larutan pigmen-sukrosa dengan kadar 40% dan 50% tidak terlihat adanya mikroorganisme hingga hari ke tujuh. Hal ini menunjukkan bahwa kadar gula sukrosa yang tinggi dapat
menghambat pertumbuhan mikroba,
sehingga gula sukrosa dapat digunakan sebagai bahan pengawet makanan.
Efek dari penambahan gula terhadap stabilitas antosianin bergantung pada struktur, konsentrasi dan jenis gula yang digunakan (Nikkhah, et al., 2007). Pengurangan aktifitas air (Aw) dengan penambahan gula sukrosa juga dapat mencegah kerusakan antosianin (Garzón
dan Wrolstad, 2001). Rein (2005)
menyatakan bahwa peningkatan kestabilan dan kelarutan pigmen antosianin dalam larutan gula dapat disebabkan oleh reaksi glikosilasi pada struktur antosianin. Jenis gula yang dapat mengalami reaksi glikosilasi adalah monosakarida dan disakarida. Jumlah gugus gula yang terikat juga mempengaruhi stabilitas warna antosianin. Reaksi dengan gula dapat menyebabkan
antosianin terpolimerisasi yang
menghasilkan warna coklat (Krifi, et al., 2000). Menurut Huang (1956), reaksi pencoklatan dan pembentukan polimer
pigmen kemungkinan menghasilkan
penghambat reaksi enzimatik dan mencegah reaksi hidrasi pada sisi aktif pigmen, sehingga menjadi lebih terlindung dari reaksi degradasi.
Pengaruh Kadar Garam NaCl
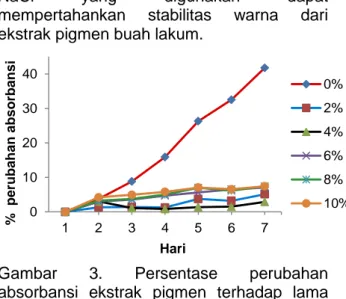
Penambahan garam NaCl juga dapat meningkatkan kestabilan warna pigmen dari buah lakum. Hal ini terlihat dari kecilnya persentase perubahan absorbansi larutan pigmen-garam. Pigmen yang ditambahkan
larutan garam mengalami penurunan
absorbansi rata-rata yang relatif kecil hingga
hari ketujuh. Persentase perubahan
absorbansi yang paling kecil terdapat pada kadar garam 4%, sedangkan kadar garam 0% memiliki persentase perubahan nilai absorbansi yang paling besar (Gambar 2). Nilai persentase perubahan absorbansi larutan sampel tidak berbeda secara nyata
0 10 20 30 40 1 2 3 4 5 6 7 % p e ruba ha n a bs orba ns i Hari 0% 10% 20% 30% 40% 50%
5 dari kadar garam 2% hingga 10%, namun berbeda nyata dengan kadar 0%. Hal ini menunjukkan bahwa variasi kadar garam
NaCl yang digunakan dapat
mempertahankan stabilitas warna dari ekstrak pigmen buah lakum.
Gambar 3. Persentase perubahan
absorbansi ekstrak pigmen terhadap lama penyimpanan pada variasi kadar NaCl
Larutan pigmen yang tidak ditambahkan garam mengalami penurunan absorbansi yang paling besar. Hal ini dikarenakan larutan pigmen mengalami degradasi oleh mikroba yang dapat berkembang dan menghasilkan enzim-enzim tertentu yang dapat mendegradasi warna larutan pigmen. Pertumbuhan mikroba ini ditunjukkan oleh munculnya hifa sejak hari ketiga yang jumlahnya terus meningkat hingga hari ketujuh.
Hasil penelitian Winarti dan Firdaus (2010) menunjukkan bahwa penambahan garam sampai 200 ppm pada sirup dan sari buah, dapat membantu mempertahankan kualitas warna yang dihasilkan. Hal ini dikarenakan garam dapat menstabilkan struktur pigmen antosianin dan mencegah
pertumbuhan mikroba yang dapat
mendegradasi warna. Hasil penelitian Goto, et al. (1976) juga menunjukkan bahwa penambahan garam dapat meningkatkan stabilitas antosianin. Beberapa mekanisme stabilisasi yang disarankan yaitu: promosi reaksi intra-molekuler antosianin (Hoshino, et al, 1981), pembentukan pasangan-ion antara ion garam dan antosianin (Goto, et al,. 1976) atau penurunan aktivitas air karena solvasi ion garam yang mengurangi hidrasi ion flavilium (Brouillard and Dangles, 1993). Akan tetapi, konsentrasi ion garam yang tinggi dapat meningkatkan kapasitas solvasi pelarut yang menyebabkan terjadinya reaksi
hidrasi dan dapat menyebabkan pemucatan warna pigmen (Hubbermann, et al., 2006).
Pengaruh Suhu terhadap Lama
Penyimpanan
Proses penyimpanan dapat menurunkan stabilitas pigmen yang terlihat dari adanya penurunan absorbansi warna yang terukur pada spektrofotometer UV-Vis. Nilai persentase perubahan absorbansi sampel selama proses penyimpanan pada suhu 4oC dan 28oC menghasilkan perbedaan yang signifikan secara statistika (Gambar 3). Larutan pigmen yang disimpan pada suhu 4oC menghasilkan warna yang lebih stabil dibandingkan pada suhu 28oC.
Gambar 4. Persentase perubahan
absorbansi ekstrak pigmen terhadap lama penyimpanan pada 4oC dan 28oC
Hasil penelitian Albarici dan Pessoa (2012) juga menunjukkan penyimpanan pada suhu yang lebih tinggi dapat menurunkan stabilitas antosianin pada minuman sari buah Acai. Penyimpanan pada suhu ruang akan
memungkinkan pertumbuhan
mikroorganisme yang dapat menguraikan (mendekomposisi) senyawa-senyawa dalam
pigmen, sehingga terjadi penurunan
absorbansi larutan. Pada suhu yang lebih rendah, enzim penyebab dekolorisasi oksidatif antosianin menjadi inaktif, sehingga
proses degradasi antosianin dapat
diperlambat. Proses penghilangan warna antosianin adalah akibat reaksi oksidasi enzim. Enzim-enzim yang menyebabkan terjadinya dekolorinasi oksidatif pigmen antosianin dikenal sebagai antosianase (Sharifi dan Hassani, 2012). Inaktifnya enzim
ini menyebabkan pigmen dapat
mempertahankan kestabilannya. 0 10 20 30 40 1 2 3 4 5 6 7 % p e rub a h a n a b s o rba n s i Hari 0% 2% 4% 6% 8% 10% 0,8 2,66 4,07 4,78 5,22 5,58 2,74 16,55 22,21 29,56 41,59 46,37 0 5 10 15 20 25 30 35 40 45 50 3 6 9 12 15 18 % p e ruba ha n a bs orba ns i hari 4oC 28oC
6 Pengaruh Lama Pemanasan
Lama pemanasan pada suhu 96oC
menyebabkan terjadinya perubahan
absorbansi sampel setiap selang waktu 30 menit yang berbeda nyata secara statistika.
Hal ini menunjukkan bahwa lama
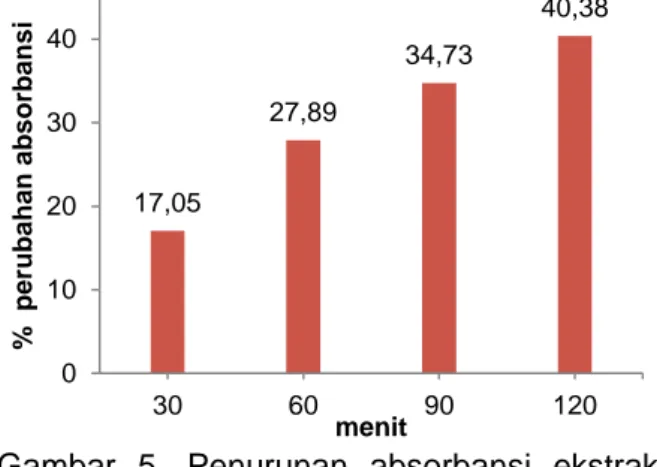
pemanasan dapat menurunkan kestabilan warna dari larutan pigmen. Semakin lama pemanasan yang dilakukan, maka nilai persentase perubahan absorbansi pigmen yang dihasilkan semakin besar. Perubahan nilai absorbansi yang terkecil adalah pada
pemanasan 30 menit dan perubahan
absorbansi yang terbesar adalah pada pemanasan 120 menit (Gambar 4). Nilai ini sesuai dengan hasil penelitian Sari (2005) yang menyatakan lama pemanasan pada suhu 100oC menyebabkan penurunan retensi warna yang semakin besar.
Gambar 5. Penurunan absorbansi ekstrak pigmen pada suhu 96oC terhadap variasi waktu pemanasan
Suhu dan lama pemanasan dapat menyebabkan pigmen mengalami perubahan struktur, sehingga terjadi penghilangan warna. Penurunan stabilitas warna karena suhu yang tinggi diduga akibat terjadinya dekomposisi antosianin dari bentuk aglikon menjadi calkon. Pemanasan lebih lanjut akan menutuskan rantai calkon menghasilkan asam benzoat yang tidak berwarna (Cabrita, et al., 2014). O H OR" OR' R1 OH R2 OH O O+ O H OR" OR' R1 OH R2 Calkon (C) Kation Flavilium (Aglikon)
Gambar 6. Perubahan struktur pigmen antosianin dari aglikon menjadi calkon
Uji Organoleptik
Uji organoleptik dilakukan terhadap 3 variasi penambahan ekstrak pigmen lakum, yaitu 5%, 7,5% dan 10%. Pembanding yang dingunakan adalah sirup komersial 10% dan pewarna pangan sintetik 0,1% berperisa
anggur. Pemilihan pembanding ini
didasarkan pada kesamaan keluarga antara lakum dan anggur, yaitu Vitaceae. Tujuan dari uji ini adalah menentukan karakteristik dari masing-masing produk pangan serta mengetahui manakah variasi konsentrasi ekstrak pigmen lakum yang paling disukai.
(a) (b)
Gambar 7. Produk minuman (a) dan agar-agar (b) dengan pewarna alami buah lakum 10% v/v (II), 7,5% v/v (III), 5% v/v (IV) dan pewarna sintetik (I)
Uji kesukaan terhadap produk pangan dianalisis secara statistik menggunakan ANOVA dengan bantuan program SPSS. Rentang penilaian kesukaan terletak pada angka 1 hingga 5. Semakin tinggi tingkat penilaian menunjukkan produk pangan semakin disukai. Hasil terbaik uji kesukaan terhadap sampel minuman lakum terdapat pada sampel SL7,5 dengan nilai 3,40.
Sehingga diketahui bahwa jumlah
penambahaan sirup lakum terbaik pada produk minuman dingin adalah dengan konsentrasi 7,5% v/v. Akan tetapi, nilai ini masih lebih rendah jika dibandingkan dengan minuman sirup komersial yang memperoleh nilai 4,33. Hasil terbaik uji kesukaan terhadap sampel agar-agar terdapat pada sampel SL7,5 dengan nilai 3,20. Sehingga diketahui bahwa jumlah penambahaan sirup lakum terbaik pada produk agar-agar adalah dengan konsentrasi 7,5% v/v. 17,05 27,89 34,73 40,38 0 10 20 30 40 30 60 90 120 % p e ruba ha n a bs orba ns i menit I II III IV I II III IV
7
Tabel 1. Hasil Penilaian Panelis terhadap Produk Minuman Dingin
Kode Sampel
Kriteria
Warna Aroma Rasa
SL5 Merah muda Tidak berasa Sedikit asam SL7,5 Merah Sedikit harum Sedikit asam SL10 Merah Sedikit harum Sedikit asam SK10 Ungu tua Harum Tidak asam
Tabel 2. Hasil Penilaian Panelis terhadap Kriteria Produk Agar-agar
Kode Sampel
Kriteria
Warna Aroma Rasa
AL5 Merah muda Harum Sedikit asam AL7,5 Merah Sedikit Harum Sedikit asam AL10 Merah Sedikit Harum Sedikit asam AK0,1 Ungu Tua Harum Tidak asam Berdasarkan uji Duncan terhadap keempat variasi sampel tersebut, diketahui bahwa masing-masing nilai yang diperoleh tidak berbeda nyata secara statistika. Hal ini berarti bahwa variasi jumlah dan jenis pigmen yang digunakan tidak berpengaruh secara signifikan terhadap kesukaan panelis.
SIMPULAN
Berdasarkan hasil penelitian yang telah
dilakukan disimpulkan bahwa pada
penyimpanan selama 7 hari, hasil terbaik pada penambahan gula sukrosa 10% dan garam NaCl 4% dengan nilai persentase perubahan absorbansi terkecil masing-masing 0,10% dan 2,88%. Penyimpanan ekstrak pigmen selama 18 hari pada refrigerator (4oC) dan suhu ruang (28oC) menghasilkan perubahan nilai absorbansi masing-masing sebesar 5,58% dan 46,37%. Lama pemanasaan pada suhu 96oC dapat menurunkan stabilitas warna pigmen buah lakum. Penambahan ekstrak pigmen lakum yang paling disukai untuk minuman dingin dan agar-agar adalah 7,5% ⁄ , masing-masing dengan nilai 3,40 dan 3,20. Karakteristik dari produk yang dihasilkan adalah berbau agak harum khas buah lakum, berasa agak asam dan berwarna merah.
DAFTAR PUSTAKA
Albarici, T.R., and Pessoa, J.D.C., 2012, Effects Heat Treatment and Storage Temperature on The Use of Açaí Drink
by Nutraceutical and Beverage
Industries, J. Chientia e Tecnologia de Alimentos, 32(1): 9-14.
Brouillard, R. And Dangles, O., 1993, Flavonoids and Flowers Color. In: Flavonoids Advances In Research Since 1986 (Ed. J.B. Harborne), Chapman and Hall, London.
Cabrita, L., Petrov,V. and Pina, F., 2014, On Thermal Degradation of Anthocyanin: Cyanidin, J. RSC Advances, 4:18939-18944.
Garzón, G.A. and R.E., Wrolstad, 2001, The
Stability of Pelargonidin-Based
Anthocyanin at Varying Water Activity, J. Food Chem., 75:185.
Ghosh, D. and Konishi, T., 2007,
Anthocyanins and Anthocyanin-Rich Extract: Role in Diabetes and Eye Function, Asia Pacific J. Clin. Nutr., 16 (2): 200-208.
Goto, T., Hoshino, T. and Obha, M., 1976, Stabilization Effect of Neutral Salts on
Anthocyanins: Flavilium Salts,
Anhidrobase and Genuine
Anthocyanins, J. Agr. Biol. Chem, 40(8): 1593-1596.
Harbone, J.B., 1996, Metode Fitokimia: Penuntun Cara Modern Menganalisis Tumbuhan, Kosasih P. dan Iwang S. (Alih bahasa), ITB, Bandung.
Hoshino, T., Matsumoto, U. and Goto, T., 1981., Journal Phytochemistry, 20: 1971-1976.
Huang, H.T., 1956, The Kineticks of The Decolorization of Anthocyanin by Fugal Anthocyanse, J. Am. Chem. Soc., 57:43-46.
Hubbermann, E.M., Heins, A., Stockmann, H. and Schwarz, K., 2006, Influence of acids, salt, sugars and hydrocolloids on the colour stability of anthocyanin rich
black currant and elderberry
concentrates, J. Eur. Food Res.
Technol., 223: 83-90.
Krifi, B.F.C., J. Bondurant and M. Metche, 2000, Degradation of Anthocyanin from Blood Orange Juice, J. Food Sci., 35:275-283.
8 Koswara, S., 2009, Pewarna Alami: Produksi
dan Penggunaannya,
ebookpangan.com.
Mardiah, 2010, Ekstraksi Kelopak Bunga dan Batang Rosella (Hibiscus sabdariffa L.) sebagai Pewarna Alami, Universitas Juanda (Laporan Penelitian).
Neliyanti dan Idiawati, N., 2014, Ekstraksi dan Uji Stabilitas Zat Warna Alami dari Buah Lakum (Cayratia trifolia (L.) Domin), J. Kim. Khatulistiwa, 3(2): 86-93.
Nikkhah, E., Khayamy, M., Heidari, R., and Jamee, R., 2007, Effect of Sugar Treatment on Stability of Anthocyanin Pigments in Berries, J. of Biol. Sci., 7: 1412-1417.
Permenkes RI No.033/MENKES/PER/2012 Tentang Bahan Tambahan Pangan. Rein, M., 2005, Copigmentation Reaction
and Color Stability of Berry
Anthocyanins, University of Helsinki (Disertasi).
Rezeki, F.S., Khoetiem, M., Widyana, W., Hadi, R.P. dan Prasetyo, B., 2011, Merintis Bisnis Prospektif melalui Pengembangan Olahan Buah Lakum (Vitis diffusa) sebagai Minuman dan Makanan yang Menyehatkan Berbasis Home Industri, Universitas Tanjungpura Pontianak (Laporan Penelitian).
Saraswati, D.N. dan Astutik, S.E., 2011, Ekstraksi Zat Warna Alami dari Kulit Manggis serta Uji Stabilitasnya, Fakultas
Teknik, Universitas Diponegoro,
Semarang (Monograf).
Sari, P., Agustina, F., Komar M., Unus, Fauzi M., dan Lindriati, T., 2005, Ekstraksi dan Stabilitas Antosianin dari Kulit Buah
Duwet (Syzygium cumini). J. Tekno. dan Industri Pangan 16(2): 142-150.
Setyaningsih, D., Apriliyantoro, A. dan Sari, M.P., 2010, Analisis Sensori: Untuk Industri Pangan dan Agro, IPB Press, Bogor.
Sharifi, A. and Hassani, B., 2012, Extraction Methods and Stability of Color Extracted From Barberry Pigments, Inter. J. of Agri Sci., 2: 320-327.
Sudarmanto, 1989, Bahan Pewarna Alami
dalam Tanaman Pangan: Proyek
Peningkatan Perguruan Tinggi. UGM, Yogyakarta.
Widhiana, E.T., Fitriana, N., Neliyanti dan Anugrah, E.T., 2012, Skrining Fitokimia dan Aktivitas Antioksidan Buah Lakum (Vitis diffusa) dalam Berbagai Fraksi
Khas Kalimantan Barat, Laporan
Penelitian, Fakultas MIPA, Universitas
Tanjungpura, Pontianak (Laporan
Penelitian).
Winarno, F.G., 1995, Kimia Pangan dan Gizi, Gramedia, Jakarta.
Winarti, S. dan Firdaus, A., 2010, Stabilitas Warna Merah Ekstrak Bunga Rosela untuk Pewarna Makanan dan Minuman, J. Tekno. Pertanian, 11: 87-93.
Winarti, S., Sarofi, U. dan Anggrahini, D., 2008, Ekstraksi dan Stabilitas Warna Ubi Jalar Ungu (Ipomoea batatas L.)sebagai Pewarna Alami, J. Teknik Kimia, 3: 207-214.
Yeo, C.K., Ang, W.F., Lok, A.F.S.L., and
Ong, K.H., 2012, Cayratya Juss.
(Vitaceae) of Singapore: With A Special Note On Cayratia japonica (Thunb.) Gagnep, J.Nature In Singapore, 5: 331-338.