125
Pengembangan dan Validasi Metode Analisis Tablet Ibuprofen
Secara Kromatografi Lapis Tipis-Densitometri
(
Development and Validation of Analitycal Methods Ibuprofen Tablets by Thin
Layer Chromatographic-Densitometry
)
Widya Kardela
1; Harrizul Rivai
2; & Anita Kartanti
1 1Sekolah Tinggi Ilmu Farmasi (STIFARM) Padang
2
Fakultas Farmasi Universitas Andalas (UNAND) Padang
Corresponding email: [email protected]
ABSTRAK
Metode Kromatografi Lapis Tipis (KLT)-densitometri yang sederhana, selektif dan akurat telah dikembangkan dan divalidasi untuk analisis kadar ibuprofen dalam sediaan farmasi. Penetapan kadar
ibuprofen ini dilakukan dengan KLT-densitometri menggunakan plat silica gel 60 F254 sebagai fase diam
dan campuran pelarut kloforom:methanol (10:1) sebagai fase gerak terbaik. Larutan standar ibuprofen pada rentang 2-10 mg/mL menghasilkan persamaan regresi y= 14293,868 + 4201,72x dengan r = 0,9973. Batas deteksi ibuprofen adalah 0.81 mg/mL dan batas kuantifikasi ibuprofen adalah 2,70 mg/mL. Akurasi
pada tablet generic ibuprofen dari PT Indo Farma dan tablet ibuprofen dengan nama dagang Proris® dari
PT Pharos mempunyai % perolehan kembali memenuhi rentang yaitu karena %RSD < 5%. Hasil analisis menunjukan kadar ibuprofen pada tablet generik sebesar 99,54%±2.99% dan tablet ibuprofen dengan
nama dagang Proris® 103.75%±4.25% kadar yang didapatkan telah memenuhi syarat sesuai Farmakope
Indonesia edisi V yaitu 90-110%.
Kata Kunci: KLT-densitometri, pengembangan dan validasi, tablet Ibuprofen
PENDAHULUAN
Ibuprofen adalah turunan sederhana dari
phenylpropionic acid dengan rumus kimia (±)-2-(p-Isobutilfenil)asampropionat, rumus molekul
C13H18O2 dan bobot molekul 206,28
(Kementerian Kesehatan RI, 2014). Obat ini lebih dari 99% terikat protein, dengan mudah dibersihkan, dan mempunyai waktu paruh terminal dari satu sampai dua jam. Ibuprofen dimetabolisme secara menyeluruh di dalam hati, dan sedikit diekskresikan dalam keadaan tak berubah (Katzung, 2002).
Ibuprofen merupakan salah satu obat yang paling banyak digunakan untuk terapi encok dan radang sendi, meredakan rasa sakit, desminore, dan kondisi lainnya serta memiliki profil keamanan yang terkenal, terutama pada dosis sederhana (Kumaresan, 2010). Ibuprofen termasuk dalam golongan obat anti-inflamasi non-steroid (NSAID), yang bekerja dengan
menghalangi enzim yang disebut
siklooksigenase, yang menghasilkan
prostaglandin yaitu zat yang terlibat dalam peradangan dan nyeri (European Medicines Agency, 2014).
126 Beberapa metode yang telah dilakukan
untuk menganalisis ibuprofen adalah dengan menggunakan kromatografi cair kinerja tinggi, fase gerak yang digunakan asetonitril:dapar fosfat (60:40, v/v) pada laju alir 0,8 mL/menit dengan deteksi UV pada 260 nm. Metode ini telah memenuhi syarat validasi yaitu linearitas metode ditentukan pada tujuh tingkat
konsentrasi 10-70 mg/mL didapatkan
persamaan regresi y = 0,0061x + 0,002 dengan r2 = 0,998 (Battu & Reddy, 2009).
Metode analisis yang telah dilakukan pada analisis ibuprofen dengan menggunakan titrimetri dan spektrofotometri ultraviolet, pada metode ini menggunakan delapan merek ibuprofen sesuai dengan batas resmi 90 -110%. Saat dilakukan titrimetri visual sampel H memiliki persentase konten tertinggi 97,8%, sedangkan sampel B memiliki persentase
konten terendah 95,7%. Metode
spektrofotometri ultraviolet cocok untuk analisis tablet ibuprofen karena mengandung kromofor yang menyerap radiasi di daerah
ultraviolet dari panjang gelombang
elektromagnetik 265 nm. Metode ini dapat digunakan untuk uji obat kuantitatif. Kalibrasi kurva dilakukan pada rentang konsentrasi 0,05 sampai 0,35 mg/mL dengan persamaan garis regresi yang diperoleh Y = 1,8679x - 0,0263 ini sejalan dengan hukum Beer-Lambert. Koefisien korelasi (r2 = 0,998) menunjukkan pembacaan
yang akurat pada semua konsentrasi sampel uji (Ebeshi et al., 2009). Metode lain adalah metode kromatografi elektrokinetik miselar, linieritas yang didapatkan memenuhi syarat validasi dengan persamaan regresi y= 3,610x - 72,000 dengan koefisien korelasi 0,9998, LOD dan LOD yang didapatkan juga telah memenuhi syarat validasi yaitu 0,0082 mg/mL dan 0,02 mg/mL (El-kommos et al., 2012).
Metode lain yang digunakan pada analisis ibuprofen yaitu menggunakan spektroskopi UV-Vis, pada panjang gelombang 224 nm didapatkan persentase perolehan kembali 99,93 ± 2,93. Linearitas pada konsentrasi 4-20 μg/mL didapatkan persamaan regresi y = 0,0477x –
0,0134, r2 = 0,9958, validasi metode yang
dilakukan sesuai dengan ICH yaitu linieritas, akurasi LOD dan LOQ (Narendra et al., 2012).
Adapun metode analisis menggunakan
spektroskopi inframerah, pada area puncak
inframerah 1721,5 cm-1 dan panjang gelombang
273 dengan deteksi sinar UV, didapatkan persamaan regresi y = 0,00 + 168,38x dan koefisien korelasi (r2) 0,998 (Matkovic, 2005).
Beberapa metode di atas merupakan metode yang mahal, canggih dan membutuhkan waktu yang lama, oleh karena itu dilakukan analisis tablet ibuprofen dengan menggunakan metode yang mempunyai sensitivitas yang tinggi, cara preparasi yang mudah, waktu pengerjaan yang singkat, perawatan alat yang mudah serta biaya yang lebih murah yaitu Kromatografi Lapis Tipis (KLT)-Densitometri. Metode ini perlu dikembangkan untuk analisis tablet ibuprofen dan diharapkan menjadi solusi untuk mendapatkan metode yang baik, valid, mudah preparasinya, dan hasil yang didapatkan dapat dipertanggung jawabkan sehingga dapat bermanfaat.
METODE PENELITIAN
Alat
Alat-alat yang digunakan antara lain:
Lampu UV 254 dan 366 (Camag®), TLC Scanner
4 dengan software Wincat (Camag®), Pipet
Kapiler ukuran 5 µL (Camag®), Twin Chamber
ukuran 20 x 20 cm (Camag®), Penotol Nanomat
4 (Camag®), plat silica gel 60 F254 250 μm
127 desikator vakum, timbangan digital (type ABJ
220-4M), corong, gelas ukur (Pyrex), pipet ukur (Pyrex), pipet tetes, spatel, labu ukur (Pyrex), kertas perkamen, kertas saring (Whatman No. 41).
Bahan
Bahan yang digunakan Baku Pembanding Farmakope Indonesia Ibuprofen didapat dari PT Indo Farma, tablet generik
mengandung ibuprofen 200 mg dari PT Indo Farma (No. Batch CD3F023), tablet ibuprofen
dengan nama dagang Proris® mengandung
Ibuprofen 200 mg dari PT Pharos (No. Batch BN
C4G580B), metanol p.a (Emsure®), kloroform
p.a (Emsure®), aseton p.a (Emsure®) dan etil
asetat p.a (Emsure®) dari PT Merck.
Pengembangan Metode Analisis Fase diam: Plat Silica gel 60 F254 250 μm.
Tabel 1. Fase gerak untuk eluen Ibuprofen (Moffat et al., 2011).
Sistem Fase Gerak Perbandingan
TD Kloroform:Aseton 8:2
TF Etil Asetat 10
TAE Metanol 10
TAD Kloroform:metanol 9:1
Dari sistem TAD dengan fase gerak
kloroform:metanol (9:1) dilakukan
pengembangan yaitu kloroform:metanol (10:1). Fase gerak yang dipilih adalah fase gerak yang memenuhi kriteria rentang Rf 0,2-0,8 (Watson, 2009).
Pembuatan Larutan Baku Ibuprofen
Ditimbang 1000 mg Ibuprofen masukkan dalam labu ukur 100 mL, kemudian dilarutkan dalam metanol sambil diaduk dan dicukupkan volumenya hingga tanda batas. Larutan ibuprofen ini mengandung 10 mg/mL atau 10.000 ppm.
Penyiapan Sampel
Tablet generik ibuprofen mengandung ibuprofen 200 mg dan tablet ibuprofen dengan
nama dagang Proris® mengandung ibuprofen
200 mg, dua puluh tablet dari masing-masingnya ditimbang dan dihitung rata-rata beratnya. Tablet kemudian digerus dan jumlah yang setara dengan berat satu tablet dilarutkan
dalam 50 mL metanol. Larutan tablet generik ibuprofen dan tablet ibuprofen dengan nama
dagang Proris® masing-masingnya mengandung
4 mg/mL atau 4000 ppm. Larutan ini disonikator lalu disaring melalui kertas Whatman no. 41.
Analisis kualitatif Larutan Sampel
Siapkan plat KLT 20 x 20 cm buat masing-masing garis penotolan 1 cm dari tepi bawah dan 1 cm dari atas. Larutan standar, sampel
generik dan sampel proris® masing-masing
dengan konsentrasi 4 mg/mL atau 4000 ppm ditotolkan 5µL sebanyak 3 totolan pada garis awal dengan jarak penotolan masing-masingnya 1 cm, masukkan plat kedalam chamber yang telah dijenuhkan dengan fase gerak terpilih tutup chamber dan dibiarkan sehingga fase gerak bergerak sampai mencapai garis atas. Chamber dibuka, plat KLT diambil dan dikering anginkan kemudian ditentukan nilai Rf.
128 Dari larutan standar ibuprofen dibuat
larutan bertingkat dipipet masing-masing secara berurutan 2, 4, 6, 8, dan 10 mL dari larutan standar dalam labu ukur 10 mL sampai tanda batas sehingga diperoleh konsentrasi 2, 4, 6, 8, 10 mg/mL. Ibuprofen untuk kurva baku dibuat dengan menotolkan 5 µL setiap konsentrasi diterapkan pada plat KLT silika gel 60 F254
kemudian dielusi dengan eluen terbaik sampai tanda batas atas dan dikeringkan dengan cara dianginkan-anginkan di suhu kamar. Plat yang telah terpisah dianalisis dengan densitometer, sehingga akan didapat data Retention factor (Rf) dan Area Under Curve (AUC). Linearitas kurva baku ditentukan dengan cara mengolah data konsentrasi seri kadar (x) dan AUC diperoleh dengan persamaan regresi linier.
Batas Deteksi dan Kuantifikasi
Setelah diperoleh kurva kalibrasi,
konsentrasi kecil yang masih dapat dideteksi (LOD) dan terdeteksi secara kuantifikasi (LOQ) dihitung secara statistik melalui garis linier dari kurva standar.
Pengujian Presisi
Pengujian presisi dilakukan adalah keterulangan (repeatability) sebagai variasi dalam sehari. Kadar yang digunakan dalam pengujian presisi adalah 6, 8, 10 mg/mL ditotolkan pada plat silika gel 60 F254 dengan
volume 5 µL dan dielusi dengan eluen terbaik dan dikeringkan, bercak dalam plat silika kemudian dianalisis dengan densitometer. Data yang akan diperoleh adalah Rf dan AUC kemudian dihitung nilai rata-rata, standar deviasi (SD) dan standar deviasi relatif (RSD). Ketepatan menengah metode presisi intraday dilakukan selama satu hari pada pagi, siang dan sore, sedangkan metode presisi interday
diperiksa dengan mengulangi penelitian selama tiga hari berturut-turut. Konsentrasi standar ibuprofen dari sampel dihitung dengan persamaan regresi yang didapat dari kurva kalibrasi.
Penetapan Kadar
Larutan uji dengan konsentrasi 4 mg/mL ditotolkan masing-masing sampel sebanyak 3 totolan dengan volume 5 µL pada garis awal dengan jarak penotolan masing-masingnya 1 cm. Masukkan plat kedalam chamber yang telah dijenuhkan dengan fase gerak terpilih, tutup
chamber dan dibiarkan sehingga fase gerak
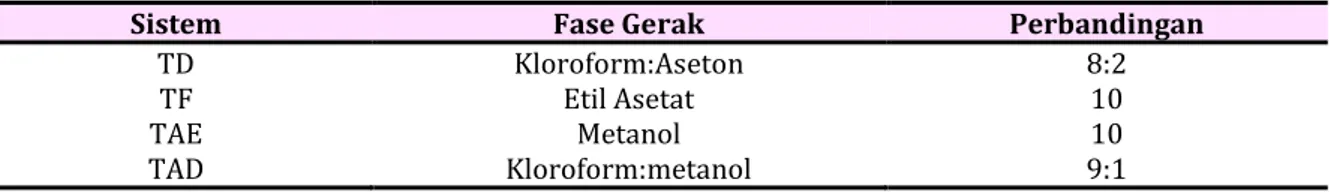
bergerak sampai mencapai garis atas. Chamber dibuka, plat KLT diambil dan dikeringanginkan. Kemudian diamati dibawah lampu UV 254 nm. Kemudian bercak discanning dengan alat Camag TLC Scanner 4 dengan panjang gelombang 222 nm dan didapat data luas histogram dari senyawa uji. Luas area dimasukkan dalam persamaan regresi yang diperoleh dari perhitungan luas area pada konsentrasi senyawa uji, maka didapatkan kadar senyawa. Akurasi
Studi recovery dilakukan untuk
memeriksa akurasi metode ini. Sampel yang dianalisis mengandung 4 mg/mL ibuprofen.
Pemulihan percobaan dilakukan dengan
menambahkan tiga jumlah yang berbeda dari ibuprofen yaitu 80, 100 dan 120 % diharapkan dapat mewakili kadar terendah dan kadar tertinggi dari kurva baku yang digunakan. Ditotolkan pada plat silika gel 60 F254
masing-masing kadar 3 kali penotolan dengan volume penotolan 5 µL dan dielusi dengan eluen terbaik. Bercak pada plat silika kemudian dianalisis dengan densitometer dan akan diperoleh data berupa nilai AUC sampel yang telah
129 ditambahkan standar kemudian dihitung %
perolehan kembali dari masing-masing kadar standar yang ditambahkan dalam sampel dengan menentukan % analit yang ditambahkan yang dapat diukur.
HASIL DAN DISKUSI
1. Pemilihan Fase Gerak.
Optimasi fase gerak dilakukan dengan mengujicobakan beberapa sistem yaitu: TD dengan perbandingan fase gerak kloroform p.a:aseton p.a (8:2) nilai Rf yang didapat adalah 0,62, sistem TF dengan fase gerak etil asetat p.a nilai Rf yang didapat adalah 0,87, Sistem TAE dengan fase gerak metanol p.a nilai Rf yang didapat adalah 0,81, sistem TAD dengan perbandingan fase gerak kloroform p.a:metanol p.a (9:1) nilai Rf yang didapat adalah 0,72, pengembangan dari sistem TAD dilakukan dengan perbandingan fase gerak kloroform p.a:metanol p.a (10:1) nilai Rf yang didapat adalah 0,48. Setelah dilakukan pengujian dengan beberapa fase gerak, kloroform p.a:metanol p.a (10:1) nilai Rf yang didapat adalah 0,48 merupakan fase gerak terbaik yang digunakan untuk analisis ibuprofen.
2. Liniearitas Kurva Baku
Linieritas suatu metode harus diuji untuk membuktikan adanya hubungan linier antara konsentrasi analit dan respon detektor. Sebagai parameter adanya hubungan linier atau tidak digunakan koefisien korelasi (r) pada garis linier y = a + bx. Pembuatan kurva kalibrasi ibuprofen pada penelitian ini dengan konsentrasi 2, 4, 6, 8, 10 mg/mL yang menghasilkan luas area 21506,90; 32174,68;
40463,73; 47528,38; dan 55847,25.
Persamaan regresi linier yang didapatkan adalah y = 14293,868 + 4201,72x dengan
koefisien korelasi kurva standar r² = 0,9946 dan didapatkan nilai r = 0,9973.
3. Batas Deteksi dan Kuantifikasi
Nilai LOD dan LOQ dari ibuprofen yang didapat adalah 0,81 mg/mL dan 2,70 mg/mL. 4. Presisi
Penentuan presisi intraday ibuprofen pada konsentrasi 6 mg/mL dengan nilai % RSD berturut-turut 4,7274%, 1,4832% dan 0,3079%; konsentrasi 8 mg/mL dengan nilai % RSD berturut-turut 1,6945%, 1,0982% dan 3,5761%; dan konsentrasi 10 mg/mL dengan nilai % RSD berturut-turut 1,8590%, 1,9117% dan 1,5002%. Penentuan presisi
interday Ibuprofen dilakukan pada
konsentrasi 6 mg/mL dengan nilai % RSD berturut-turut 3,5632%, 1,3367% dan 1,0412%; konsentrasi 8 mg/mL dengan nilai % RSD berturut-turut 3,4806%, 3,0148% dan 1,7911%; dan konsentrasi 10 mg/mL dengan nilai % RSD berturut-turut 3,5109%, 2,6597% dan 2,1407%.
5. Penetapan Kadar
Kadar ibuprofen dari masing-masing sampel generik ibuprofen dan tablet ibuprofen
dengan nama dagang Proris® adalah 99,54%
± 2,99% dan 103,75 % ± 4,25% 6. Akurasi
Penambahan larutan standar ibuprofen 80%, 100%, 120% = 3,1854 mg/mL, 3,9818 mg/mL, dan 4,7782 mg/mL, ditambahkan dalam larutan sampel generik 4 mg/mL (yang telah diketahui kadarnya) % perolehan kembali yang didapat adalah 87,90%, 100,72% dan 98,09%. Penambahan larutan standar ibuprofen 80%, 100%, 120% = 3,3200 mg/mL, 4,1500 mg/mL, dan 4,9802 mg/mL, ditambahkan dalam larutan sampel
dengan nama dagang Proris® 4 mg/mL (yang
130 kembali yang didapat adalah 107,14%,
91,79% dan 93,69%.
Penelitian ini dianalisis menjadi beberapa tahap yaitu optimasi fase gerak, validasi metode meliputi linieritas kurva baku, batas deteksi dan kuantifikasi, presisi, penetapan kadar dari sampel serta study recovery. Penelitian ini menggunakan plat KLT silica gel F254 (Merck®)
karena kedua senyawa berfluoresensi pada sinar UV terutama pada panjang gelombang 254 nm. Sinar UV yang mengeksitasi zat pada panjang gelombang 254 nm tidak dapat mencapai indikator flouresensi masing-masing zat sehingga bercak akan tampak gelap yang dikelilingi bagian yang berflouresensi. Bagian berflouresensi diakibatkan adanya senyawa sulfida yang ditambahkan pada permukaan silica gel (Watson, 1999). Sebelum melakukan elusi plat dipanaskan terlebih dahulu dalam
oven pada suhu 1000C selama 5 menit (Moffat et
al., 2011). Analisis tablet ibuprofen secara
KLT-Densitometri digunakan panjang gelombang 222 nm (Starek & Krzek, 2010).
Rf (Retardation Factor) didefinisikan sebagai laju pergerakan senyawa uji dibagi dengan laju pergerakan fase gerak. Pada kromatografi lapis tipis senyawa uji dan fase gerak bergerak dalam jangka waktu yang sama. Jarak yang ditempuh berbanding lurus dengan laju pergerakan (Bobbit et al., 1991). Nilai Rf terletak antara 0,2-0,8 untuk memaksimalkan pemisahan. Selain itu, fase gerak harus mempunyai kemurnian yang sangat tinggi karena kromatografi lapis tipis merupakan teknik yang sensitif (Rohman, 2009).
Pada penelitian ini, pengembangan dilakukan sebanyak 3 hari berturut-turut untuk memastikan fase gerak yang telah didapatkan memiliki nilai Rf yang stabil supaya
densitometri untuk senyawa tersebut terbentuk puncak yang simetris dan merata. Dari hasil percobaan didapatkan hasil fase gerak terbaik yang dapat digunakan untuk analisis ibuprofen adalah kloroform:metanol (10:1), karena setelah digunakan sebagai fase gerak selama 3 hari berturut-turut nilai Rf yang didapatkan stabil dan memasuki rentang yaitu 0,48.
Linieritas suatu metode merupakan ukuran seberapa baik kurva kalibrasi yang menghubungkan antara respon (y) dengan konsentrasi (x). Dari hasil pengukuran didapatkan persamaan garis lurus y = 14293,868 + 4201,72x dengan koefisien korelasi (r) = 0,997. Koefisien korelasi ini menunjukkan hasil yang linier, karena memenuhi kriteria penerimaan yaitu nilai koefisien korelasi (r) ≤ 1 (Gandjar & Rohman, 2013).
Penentuan LOD dan LOQ merupakan salah satu syarat untuk proses memvalidasi metode analisis (Harmita, 2004). Pengukuran ini menetapkan konsentrasi yang minimum di mana analit dapat dipercaya, dikenali dan terukur (Alsirawan et al., 2013). Nilai LOD dan LOQ dapat ditentukan dari persamaan regresi dan standar deviasi. Nilai LOD dan LOQ ibuprofen adalah 0,81 mg/mL dan 2,70 mg/mL.
Uji presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil individu, diukur melalui penyebaran hasil individual dari rata-rata jika prosedur diterapkan secara berulang pada sampel-sampel yang diambil dari campuran homogen. Kriteria seksamaan diberikan jika metode memberikan simpangan baku relatif atau koefisien variasi 2% atau kurang. Akan tetapi kriteria ini sangat fleksibel tergantung pada konsentrasi analit yang diperiksa, jumlah sampel, dan kondisi laboratorium. Dari penelitian dijumpai bahwa
131 menurunnya kadar analit yang dianalisis. Pada
kadar 1% atau lebih, standar deviasi relatif antara laboratorium adalah sekita 2,5% ada pada satu perseribu adalah 5%. Pada kadar satu per sejuta (ppm) RSDnya adalah 16% dan pada kadar part per bilion (ppb) adalah 32%. Pada metode yang sangat kritis, secara umum diterima bahwa RSD harus lebih dari 2% (Harmita, 2004).
Presisi metode intraday dilakukan dengan menotolkan standar ibuprofen murni pada pagi, siang dan sore hari, sedangkan pada presisi metode interday dilakukan dengan menotolkan standar ibuprofen murni selama 3 hari berturut-turut. Dari nilai % RSD yang didapatkan pada penelitian ini diperoleh nilai %RSD yang kurang sama dengan 16% maka dapat dikatakan bahwa metode ini mempunyai nilai keterulangan yang baik.
Dari hasil pengujian dengan motede TLC
Scanner diketahui kadar ibuprofen dalam
sampel generik ibuprofen 99,55% ± 2,99% dan
sampel tablet ibuprofen dengan nama dagang
Proris® 103,75% ± 4,25%. Dari data ini terlihat
bahwa kadar ibuprofen dalam tablet generik dan tablet ibuprofen dengan nama dagang
Proris® sesuai dengan ketentuan yang ada pada
Kementerian Kesehatan RI tahun 2014 yaitu 90-110%. Kadar yang didapatkan juga memenuhi syarat validasi yaitu diatas nilai LOD dan LOQ yang didapatkan.
Akurasi merupakan ukuran yang
menunjukkan derajat kedekatan hasil analisis dengan kadar analit yang sebenarnya.
Kecermatan dinyatakan sebagai persen
perolehan kembali (% recovery). Perolehan
kembali ibuprofen dilakukan dengan
penambahan bahan baku standar pada sampel. Dari hasil uji perolehan kembali ibuprofen berada pada rentang yang diperbolehkan (80-110%) (Harmita, 2004). Jadi ini membuktikan bahwa metode ini memberikan hasil yang akurat.
Tabel 2. Hasil pemilihan fase gerak untuk analisis ibuprofen
Sistem Fase Gerak Perbandingan Rf
TD Kloroform:Aseton 8:2 0,62
TF Etil Asetat 10 0,87
TAE Metanol 10 0,81
TAD Kloroform:Metanol 9:1 0,72
Pengembangan
Sistem TAD Kloroform:metanol 10:1 0,48
132 Gambar 2. Hasil densitogram sampel generik ibuprofen dari PT. Indo Farma volume
penotolan 5µL, fase gerak kloroform:methanol (10:1), pada panjang gelombang 222 nm
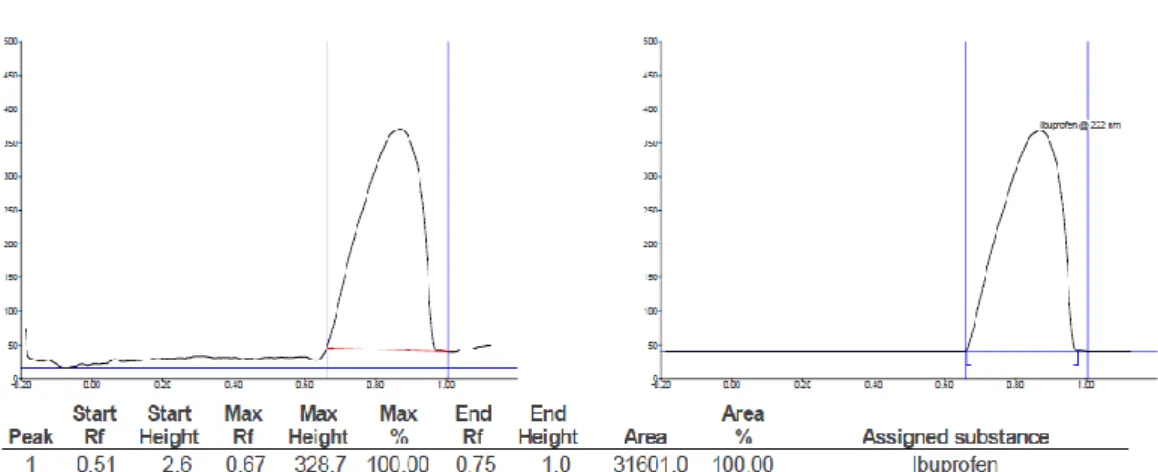
Gambar 3. Hasil densitogram sampel ibuprofen dengan nama dagang Proris® dari PT. Pharos, volume penotolan 5µL, fase gerak kloroform:methanol (10:1), pada panjang gelombang 222 nm
KESIMPULAN
Pada penelitian ini telah didapatkan fase gerak terbaik yang dapat digunakan untuk analisis ibuprofen yaitu kloroform : metanol (10:1). Validasi metode analisis ibuprofen dengan Kromatografi Lapis Tipis (KLT)-Densitometri mempunyai linieritas yang telah memenuhi syarat validasi yaitu didapatkan koefisien korelasi 0,9973, batas deteksi 0,81 mg/mL dan batas kuantifikasi 2,70 mg/mL, Akurasi pada tablet generik ibuprofen dan tablet
ibuprofen dengan nama dagang Proris®
mempunyai % perolehan kembali memenuhi rentang yaitu 80-110%. Presisi intraday dan
interday mempunyai keterulangan yang baik
karena %RSD ≤ 16%. Kadar tablet generik ibuprofen adalah 99,54% ± 2,99% dan kadar
tablet ibuprofen dengan nama dagang Proris®
adalah 103,75% ± 4,25%, kadar yang didapatkan telah memenuhi syarat sesuai Farmakope Indonesia edisi V yaitu 90-110%.
133
DAFTAR PUSTAKA
Alsirawan, M.B., Mohammad, M.A., Alkasmi, B., Alhareth, K. & El-Hammadi, M. (2013). Development and validation of a simple hplc method for the determination of ibuprofen sticking onto punch faces. International Journal of
Pharmacy and Pharmaceutical Sciences, 5(4),
227-231.
Battu, P.R. & Reddy, M.S. (2009). RP-HPLC Method for simultaneous estimation of Paracetamol and Ibuprofen in tablets. Asian J. Research Chem, 2(1), 70-72.
Bobbitt, J.M., Gritter, R.J., & Scharwarting, A.E. (1991).
Pengantar Kromatografi. (Edisi II). Penerjemah :
Kokasih Padmawinata. Bandung: Penerbit ITB. Ebeshi, B.U., Oseni, K.E., Ahmadu, A.A. & Oluwadiya,
O.O. (2009). Comparative Utilization of Visual, potentiometric titrations and UV spectophotometric methods in the determination of Ibuprofen. African
Journal of Pharmacy and Pharmacology, 3(9),
426-431.
El-kommos, M.E., Mohamed, N.A. & Hakiem, A.F.A.
(2012). Selective Micellar Electrokinetic
Chromatographic Method for Simultaneous Determination of some Pharmaceutical Binary
Mixtures Containing Non-Steroidal
Anti-Inflammatory Drugs. Journal of Pharmaceutical
Analysis, 3(1), 53-60.
European Medicines Agency. (2014). European
Medicines Agency starts review of ibuprofen medicines. London: United Kingdom.
Gandjar, I.G. & Rohman, A. (2013). Kimia Farmasi
Analisis. (Edisi XI). Yogyakarta: Pustaka Pelajar.
Harmita. (2004). Petunjuk pelaksanaan validasi metode
dan cara perhitungannya. Majalah Ilmu
Kefarmasian, 1 (3), 117-135.
Katzung, B. (2002). Farmakologi Dasar dan Klinik. (Edisi II). Penerjemah dan editor bagian farmakologi
fakultas kedokteran Universitas Erlangga.
Surabaya: Salemba Medika.
Kementerian Kesehatan Republik Indonesia. (2014).
Farmakope Indonesia. (Edisi V). Jakarta:
Kementerian Kesehatan Republik Indonesia Kumaresan, C. (2010). S+ ibuprofen (dexibuprofen): the
superior non steroidal antiinflammatory agents for development of pharmaceuticals. International
Journal of Current Pharmaceutical Research, 2(3),
1-3.
Matkovic, S.R. (2005). Quantitative analysis of Ibuprofen in pharmaceutical formulations through FTIR Spectroscopy. Latin American Applied Research, 35, 189-195.
Moffat, A.C., Osselton, M.D. & Widdop, B. (2011).
Clarke’s Analysis of Drug and Poisons. (Edisi IV).
London: Pharmaceutical Press.
Narendra, N., Jeyabalan, G.S., Mukesh, K., Naresh, K. & Gurpreet, S. (2012). Simultaneous estimation of famotidine and ibuprofen in pure and
pharmaceutical dosage form by UV-VIS
spectroscopy. International Research Journal of
Pharmacy, 3(4), 277-280.
Rohman, A. (2009). Kromatografi untuk Analisis Obat. (Edisi I). Yogyakarta: Graha Ilmu.
Starek, M. & Krzek, J. (2010). TLC Chromatographic-Densitometric assay of Ibuprofen and its impurities.
Journal of Chromatographic Science, 48, 825-829.
Watson, D.G. (2009). Analisis farmasi: buku ajar untuk
mahasiswa farmasi dan praktisi kimia farmasi.
(Edisi II). Penerjemah: Winny R. Syarief. Jakarta: EGC.