JERAMI PADI DENGAN PROSES
HIDROLISIS DAN FERMENTASI
YUDHI ANDAYANA (0631010055)
LUTFI RAMLI (0631010078)
JURUSAN TEKNIK KIMIA
FAKULTAS TEKNOLOGI INDUSTRI
UNIVERSITAS PEMBANGUNAN NASIONAL (UPN) “VETERAN” JAWA TIMUR
PEMBUATAN ETHANOL
DARI JERAMI PADI DENGAN
PROSES HIDROLISIS DAN FERMENTASI
Disusun Oleh :
LUTFI RAMLI
0631010078
Telah Dipertahankan Dihadapan dan Diterima Oleh Dosen Penguji Pada Tanggal
1 November 2010
Tim Penguji : Pembimbing :
1. 1.
Ir. Nana Dyah S, Mkes Ir. Lucky Indrati U, MT NIP. 19600422 198703 2 001 NIP. 19581005 198803 2 001 2.
Ir. Siswanto
NIP. 19541212 1983031 1 001
Mengetahui :
Dekan Fakultas Teknologi Industri
Universitas Pembangunan Nasional ” Veteran” Jawa Timur
LEMBAR PENGESAHAN
Proposal Penelitian
“Pembuatan Ethanol dari Jerami Padi dengan Proses Hidrolisis dan Fermentasi”
Disusun Oleh :
Yudhi Andayana (0631010055) Lutfi Ramli (0631010078)
Proposal ini telah dibimbing dan direvisi
Sebagai persyaratan memperoleh gelar Sarjana Teknik Jurusan Teknik Kimia Dan layak untuk diseminarkan
Menyetujui, Dosen Pembimbing
Dengan mengucapkan puji syukur ke-Hadirat Allah SWT atas segala rahmat dan hidayahnya, sehingga peneliti dapat menyelesaikan penelitian dengan judul
“PEMBUATAN ETHANOL DARI JERAMI PADI DENGAN
PROSES HIDROLISIS DAN FERMENTASI”.
Penelitian ini merupakan salah satu syarat yang harus ditempuh dalam kurikulum
program studi S1 Teknik Kimia dan untuk memperoleh gelar kesarjanaan, sarjana Teknik
Kimia di Fakultas Teknologi Industri UPN”Veteran”Jawa Timur.
Laporan penelitian ini disusun berdasarkan hasil pengamatan, analisa dan studi
literature. Dengan terselesaikannya laporan ini, penyusun menyampaikan ucapan terima kasih
kepada :
1. Ir. Sutiyono, MT, selaku Dekan Fakultas Teknologi Industri UPN”Veteran” Jawa
Timur.
2. Ir. Retno Dewati, MT, selaku Ketua Jurusan Teknik Kimia Fakultas Teknologi
Industri UPN”Veteran” Jawa Timur.
3. Ir. Lucky Indrati Utami, MT, selaku Dosen Pembimbing kami dalam
menyelesaikan peneltian ini.
4. Ir. Nana Dyah S, MKes, selaku Dosen penguji kami.
5. Ir. Siswanto, selaku Dosen penguji kami.
6. Ir. Cecilia Puji Astuti, MT, selaku Kasie Laboratorium Riset Jurusan Teknik
Kimia UPN”Veteran”Jawa Timur.
7. Bapak Solikin , selaku Laboran Riset Jurusan Teknik Kimia UPN”Veteran”Jawa
Timur.
8. Staf Fakultas Teknologi Industri UPN”Veteran”Jawa Timur.
9. Bapak, Ibu dan keluargaku yang tidak henti-hentinya mendoakan aku,
menyanyangi dan memberikan support baik materi maupun spiritual.
10.Sahabat aku Yudhi Andayana yang selalu memberikan dukungan dan
membantuku dalam segala hal baik itu materi maupun yang lainnya. Semoga
maafkan aku jika dalam setiap langkah selalu ada kerikil-kerikil yang
menghalangi. Ayo Semangat..!!!!!!!!! (Tinggal selangkah lagi perjuangan kita ).
12.Para sahabat-sahabat seperjuangan di Jurusan Teknik Kimia khususnya angkatan
2006 paralel A dan B yang tak bisa kusebut satu persatu, terima kasih atas
semuanya baik itu dukungan maupun bantuan kalian selama ini. Ayo
Semangat..!!!
Penyusun menyadari bahwa laporan penelitian ini jauh dari sempurna. Oleh
karena itu saran dan kritik yang bersifat membangun sanagt penyusun harapkan
demi kesempurnaan laporan ini. Akhir kata penyusun berharap semoga lapora
penelitian ini dapat bermanfaat dan berguna bagi kita semua.
Surabaya,…Oktober 2010
At this time Rice Straw still not get significant treatment. Because the straw is
generally left abandoned in the fields after the harvest season. Though Rice straw contains
starch, cellulose and glucose is high enough. Problems that are often faced in the chemical
industry is the use of cheap useless material into the material - material that is more useful
and valuable.
Alcohol can be produced from plants that contain lots of cellulose compounds with
the help of microbial activity. Use of Alcohol, especially ethanol as a fuel which is one of
solving the energy problem today. Because we know the use of energy (especially oil) is
increasing from year to year. While fuel sources in use are running low, so an alternative as
seek new sources of fuel.
Conditions established by 2500 ml of solution hydrolysis, hydrolysis pH 3, the
hydrolysis time of 2 days, and the fermentation pH of 4.5, whereas variables that run is the
time of fermentation (2,3,4,5,6,7 (days)), rice straw weight (40,50,60, (g)), and the volume of
stater is added (8%, 10%, 12%, times the volume of liquid fermentation).
The results showed that the best conditions on the weight of 50 grams of rice straw with a
volume of stater who added as much as 12% of the volume of fermentation liquid is
fermented for 7 days that produces ethanol concentration of 12.89%.
INTISARI
Pada saat ini Jerami Padi masih belum mendapatkan penanganan yang cukup berarti.
Karena pada umumnya jerami dibiarkan begitu saja di sawah setelah musim panen. Padahal
jerami Padi banyak mengandung Pati, Selulosa dan Glukosa yang cukup tinggi. Masalah
yang sering di hadapi pada industri kimia adalah pemanfaatan bahan tidak berguna yang
murah menjadi bahan – bahan yang lebih berguna dan bernilai tinggi.
Alkohol dapat dihasilkan dari tanaman yang banyak mengandung senyawa selulosa
dengan menggunakan bantuan aktivitas mikroba. Penggunaan Alkohol khususnya etanol
sebagai bahan bakar yang merupakan salah satu pemecahan masalah energi dewasa ini.
Karena kita ketahui pemakaian energi (terutama minyak bumi) dari tahun ketahun sangat
meningkat. Sedangkan sumber bahan bakar yang di pakai semakin menipis, sehingga
diperlukan alternatif lain dalam mencari sumber bahan bakar yang baru.
Kondisi yang ditetapkan larutan Hidrolisis sebanyak 2500 ml, pH hidrolisis 3, waktu
hidrolisis 2 hari, dan pH fermentasi sebesar 4,5 , sedangkan peubah yang dijalankan adalah
waktu fermentasi (2,3,4,5,6,7 (hari)), berat jerami padi (40,50,60, (gram)), dan volume stater
yang ditambahkan (8%,10%,12%, kali volume cairan fermentasi).
Hasil penelitian menunjukkan bahwa kondisi terbaik pada berat jerami 50 gram
dengan volume stater yang ditambahkan sebanyak 12% volume cairan fermentasi yang
DAFTAR ISI
BAB II. TINJAUAN PUSTAKA II.1. Tanaman Jerami ... 3
II.2. Selulosa ... 4
II.3. Hidrolisis ... 6
II.4. Pengertian Alkohol ... 8
II.5. Fermentasi ... 9
II.6. Mikroorganisme dalam Fermentasi II.6.1. Saccharomyces Cerevisiae ... 12
II.6.2. Pertumbuhan Mikroorganisme ... 12
II.7. Landasan Teori II.7.1. Fungsi dari HCl ... 14
II.7.1. Faktor-Faktor yang mempengaruhi Hidrolisis ... 15
II.7.2. Faktor-Faktor dalam Fermentasi ... 15
II.8. Hipotesis ... 19
BAB III. PELAKSANAAN PRAKTIKUM III.1. Bahan yang diperlukan ... 20
III.6.4. Membuat Media Cair untuk kurva pertumbuhan ... 26
III.6.5. Pembuatan Starter Saccharomyces Cerevisiae ... 27
III.6.6 Hidrolisis ... 27
III.6.7.. Fermentasi ... 28
III.7. Distilasi ... 28
III.7.1. Analisa Kadar Ethanol ... 28
III.7.2. Analisa Kadar Gulukosa ... 29
BAB IV DATA HASIL DAN PEMBAHASAN IV.1. Analisa Bahan Baku Jerami Padi ... 30
IV.3. Pembiakan Bakteri Saccharomyces Cerevisiae ... 31 IV.4. Hasil Fermentasi ... 32 BAB V KESIMPULAN DAN SARAN
V.1. Kesimpulan ... 34 V.2. Saran ... 34 DAFTAR PUSTAKA
DAFTAR GAMBAR
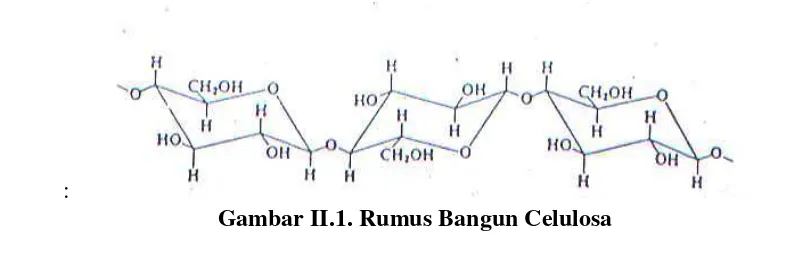
Gambar II. 1. Rumus Bangun Selulosa ... 4
Gambar II. 2. Kurva Pertumbuhan Kultur Jasad Renik ... 13
Gambar II. 3. Kurva Pertumbuhan ... 16
Gambar III. 3. 2. Proses Fermentasi ... 22
DAFTAR TABEL
Tabel II. 1. Tabel Komposisi Pada Jerami Padi ... 3
Tabel IV.1. Hasil Analisa Glukosa Awal ... 30
Tabel IV.2. Hasil Analisa Kadar Glukosa ... 30
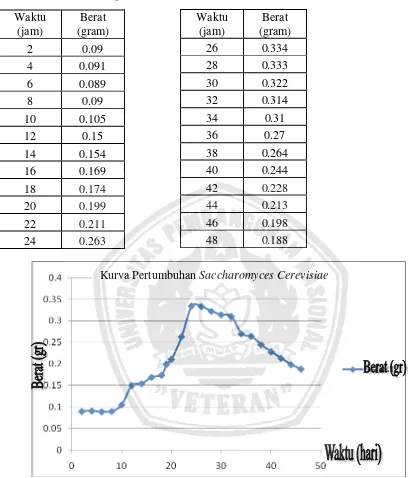
Tabel IV.3. Hasil Pengamatan Kurva Pertumbuhan ... 31
DAFTAR GRAFIK
Grafik IV.1. Hubungan biomassa Saccharomyces Cerevisiae dengan waktu ... 31 Grafik IV.2. Hubungan antara hari (lamanya fermentasi) dengan persen
BAB I
PENDAHULUAN
I.1. LATAR BELAKANG
Pada saat ini Jerami Padi masih belum mendapatkan penanganan yang cukup
berarti. Karena pada umumnya jerami dibiarkan begitu saja di sawah setelah musim
panen. Padahal jerami Padi banyak mengandung Pati, Selulosa dan Glukosa yang
cukup tinggi. Masalah yang sering di hadapi pada industri kimia adalah pemanfaatan
bahan tidak berguna yang murah menjadi bahan – bahan yang lebih berguna dan
bernilai tinggi.
Alkohol dapat dihasilkan dari tanaman yang banyak mengandung senyawa
selulosa dengan menggunakan bantuan aktivitas mikroba. Penggunaan Alkohol
khususnya etanol sebagai bahan bakar yang merupakan salah satu pemencahaan
masalah energi dewasa ini. Karena kita ketahui pemakaian energi (terutama minyak
bumi) dari tahun ketahun sangat meningkat. Sedangkan sumber bahan bakar yang di
pakai semakin menipis, sehingga diperlukan alternatif lain dalam mencari sumber
bahan bakar yang baru.
Jerami Padi merupakan limbah Petani yang mengandung Selulosa yang
banyak . Selulosa merupakan rangkaian dari Proses pembuatan glukosa, dimana tahap
awalnya dengan menghidrolisis mengunakan asam kuat (HCl) pada limbah selulosa
tersebut (jerami padi). Pada penelitian terdahulu dengan judul ” Pembuatan Bioetanol
dari Rumput Gajah dengan proses Hidrolisis dan Fermentasi” .
Pada Penelitian kali ini di pilih jerami sebagai bahan alternatif, karena
kandungan Selulosa cukup banyak. Untuk mendapat alkohol, Selulosa dari jerami
tersebut di Hidrolisis terlebih dahulu sehingga di dapat glukosa. Kemudian
difermentasi menjadi alkohol.
Pemanfaatan jerami Padi untuk bahan bakar etanol masih jarang dilakukan ,
I.2. TUJUAN
1. Untuk mengetahui berat jerami padi dan kadar glukosa yang ada
didalamnya dengan proses hidrolisis yang telah ditentukan kadar pHnya.
2. Menentukan konsentrasi stater yang terbaik untuk menghasilkan ethanol
pada saat proses fermentasi
3. Untuk mendapatkan kadar ethanol yang terbaik pada jerami Padi dengan
menggunakan proses Hidrolisis dan fermentasi.
4. Mengetahui proses pembuatan bioethanol dari jerami Padi dengan proses
Hidrolisis dan fermentasi
I.3. MANFAAT
1. Mendapatkan kadar etanol terbaik dengan proses pembuatan etanol dari
jerami Padi
2. Mengetahui proses pembuatan etanol dari jerami padi dengan Proses
Hidrolisis dan Fermentasi.
3. Menaikkan nilai tambah jerami Padi menjadi bahan kimia yang bernilai
ekonomis dan memberikan alternatif bahan baku jerami Padi sebagai
BAB II
TINJAUAN PUSTAKA
II.1. JERAMI
Bahan baku yang kita gunakan dalam penelitian kami kali ini adalah jerami
Padi, karena menurut teori bahwa jerami Padi banyak mengandung kandungan
selulosa. Ternyata kandungan selulosa selain dapat dijadikan menjadi bahan baku
kertas, selulosa juga dapat dijadikan menjadi ethanol dengan proses hidrolisis dan
fermentasi terlebih dahulu. Adapun bahan baku yang kami dapatkan berasal dari kota
Bojonegoro, karena pada saat pengambilan bahan baku jerami Padi yang ada di
daerah Surabaya dan sekitarnya telah melewati masa panen. Sehingga kami mencari
bahan baku jerami Padi ditempat lain yang belum melewati masa panen.
Hasil panen sebanyak 5 ton padi (gabah) akan menghasilkan jerami padi
sebanyak 7,5 ton yang mengandung 45 kg N,10 kg P, 125 kg K, dan 350 Si. Dengan
demikian jerami padi merupakan sumber hara makro yang baik. Di samping itu, 5 ton
padi mengandung 2 ton karbon, dan ditanah sawah secara tidak langsung merupakan
sumber N. Faktor lain yang menguntungkan dari penggunaan jerami padi sebagai
sumber pupuk organik adalah tersedia langsung di lahan usaha tani, yang bervariasi
dari 2-10 ton/ha/musim, dan sekaligus mengurangi masalah limbah.
II. 1. Tabel Komposisi pada Jerami Padi :
Komponen Jerami Padi (60 – 80 %) Presentase
Kandungan Glukosa dari jerami padi adalah:
Sellulosa pada Jerami Padi kering : 24,68% (Lab TAKI ITS)
Gulukosa pada Jerami Padi kering : 1,67%(BBLK Surabaya)
Secara tidak langsung jerami juga mengandung senyawa N dan C yang
berfungsi sebagai substrat metabolisme mikrobia tanah, termasuk gula, pati, selulose,
hemiselulose, pektin, lignin, lemak dan protein. Senyawa tersebut mengandung 40%
(sebagai C) berat kering jerami. Pembenaman jerami Padi kedalam lapisan oleh tanah
sawah akan mendorong kegiatan bakteri pengikat N yang heterotropik dan fototropik.
II.2. . SELULOSA
Selulosa adalah polimer β-glukosa dengan ikatan β-1 4 diantara satuan
glukosanya. Selulosa berfungsi sebagai bahan struktur dalam jaringan tumbuhan
dalam bentuk campuran polimer homolog dan biasanya disertai polisakarida lain dan
lignin dalam jumlah yang beragam. Molekul selulosa memanjang dan kaku, meskipun
dalam larutan. Gugus hidroksil yang menonjol dari rantai dapat membentuk ikatan
hidrogen dengan mudah, mengakibatkan kekristalan dalam batas tertentu. Derajat
kekristalan yang tinggi menyebabkan modulus kekenyalan sangat meningkat dan daya
regang serat selulosa menjadi lebih besar dan mengakibatkan makanan yang
mengangung selulosa lebih liat.(John M Deman,1997)
Selulosa yang merupakan polisakarida terbanyak di bumi dapat diubah menjadi
glukosa dengan cara hidrolisis asam.(Groggins,1985)
Selulosa juga salah satu dari jenis polisakarida yang tersusun dari kesatuan
anhidroglukosa dan mempunyai bentuk empiris C6H10O5 dan menjadi penyusun
utama dari dinding sel pada tumbuhan. Selulosa termasuk dalam polimer yang
menitik-beratkan molekul besar, serta tersusun atas unit – unit selulobiosa. Setiap
glukosa anhidrat adalah sebuah alcohol trihidrat yang mengandung dua alkohol
sekunder dalam posisi 2 dan 6, serta sebuah alkohol primer. Struktur molekul dari
selulosa dapat dilihat dalam gambar sebagai berikut:
:
Selulosa dari bahan alami yang telah dilarutkan melalui suatu reaksi akan
menghasilkan suatu selulosa murni yang disebut sebagai regenerated cellulose. Selulosa murni ini kemudian melalui sejumlah reaksi kimia akan menghasilkan
sejumlah senyawa yang merupakan turunan dari selulosa yang dapat digunakan untuk
berbagai kebutuhan. Selulosa tersebut relative higroskopis dimana pada kondisi
atmosper ( 20oC dengan kelembaban 60%) dapat menyerap 8 sampai 14% air.
Meskipun selulosa mampu menyerap air namun tidak dapat larut dalam air atau pun
asam encer. (Ullmann, 1986).
Berdasarkan derajat polimerisasi (DP) dan kelarutan dalam senyawa natrium
hidroksida (NaOH) 17,5%, selulosa dapat dibagi atas tiga jenis. Yaitu :
a. Selulosa α (Alpha Cellulose) adalah selulosa berantai panjang, tidak larut
dalam larutan NaOH 17,5% atau larutan basa kuat dengan DP (Derajat
Polimerisasi) 600 – 1500. Selulosa α dipakai sebagai penduga dan atau tingkat
kemurnian selulosa.
b. Selulosa β (Betha Cellulose) adalah selulosa berantai pendek, larut dalam
larutan NaOH 17,5% atau basa kuat dengan DP (Derajat Polimerisasi) 15 – 90,
dapat mengendap bila dinetralkan.
c. Selulosa γ (Gamma Cellulose) adalah sama dengan selulose β, tetapi DP nya
(Derajat Polimerisasi) kurang dari 15.
http://72.14.235.104/search?q=cache:omEqHMACINUJ:buletinlitbang.dephan.go.id/index.asp %3Fvnomor%3D18%26mnorutisi%3D3+pembuatan+SELULOSA&hl=id&ct=clnk&cd=1&gl=id
Semua selulosa ether dapat larut dalam pelarut organik, kecuali sulfat dan
asetat sulfat yang larut dalam air. Turunan selulosa lain yang penting adalah natrium
selulosa xantat yang dihasilkan dari reaksi antara natrium hidroksida dengan karbon
disulfida. Senyawa ini digunakan dalam pembuatan viscous rayon dan cellophane.
(Kirk & Othmer, 1952)
Selulosa menggelembung dalam air dan basa pekat. Polimer yang
tergelembung basa, dikenal sebagai selulosa alkali atau selulosa soda , dipakai untuk mempreparasi selulosa regenerasi, sebagaimana yang digambarkan pada pasal berikut.
Proses mereaksikan kapas dengan basa air, dan kemudian menghilangkan basa
kekristalannya agak sedikit rendah. Ia juga memiliki daya celup yang baik. (Malcolm P. Stevens, 2001)
II.3. HIDROLISIS
Hidrolisis merupakan proses pemecahan suatu senyawa menjadi
senyawa yang lebih sederhana dengan bantuan molekul air. (Kirck Othmer, 1967)
Jenis hidrolisis ada lima macam yaitu sebagai berikut :
1. Hidrolisis murni
Pada proses ini hanya melibatkan air saja. Proses ini tidak dapat
menghidrolisis secara efektif karena reaksi berjalan lambat. Hidrolisis
murni ini biasanya hanya untuk senyawa yang sangat reaktif dan reaksinya
dapat dipercepat dengan memakai uap air.
2. Hidrolisis dengan larutan asam
Menggunakan larutan asam sebagai katalis. Larutan asam yang digunakan
dapat encer atau pekat, seperti H2SO4 atau HCl.
3. Hidrolisis larutan basa
Menggunakan larutan basa encer maupun pekat sebagai katalis. Basa yang
digunakan pada umumnya adalah NaOH atau KOH. Selain berfungsi
sebagai katalis, larutan basa pada proses hidrolisis berfungsi untuk
mengikat asam sehingga kesetimbangan akan bergeser ke kanan.
4. Alkali fusion
Hidrolisis ini dilakukan tanpa menggunakan air pada suhu tinggi, misalnya
dengan menggunakan NaOH padat.
5. Hidrolisis dengan enzym
Hidrolisis ini dilakukan dengan mengunakan enzym sebagai katalis.
Enzym yang digunakan dan dihasilkan dari mikroba seperti enzym α
-amylase yang dipakai untuk hidrolisis pati menjadi glukosa dan maltosa.
(Groggins, 1958)
Pati merupakan komponen yang lebih kompleks daripada disakarida.
Sebelum difermentasi, pati harus dipecah dengan menggunakan enzim amilase
(banyak terdapat dalam gandum yang berkecambah) menjadi komponen
disakarida yaitu maltosa. Dengan menggunakan enzim lain yaitu maltase,
Proses hidrolisis dipengaruhi dengan beberapa faktor, antara lain
sebagai berikut :
a. Jumlah kandungan karbohidrat pada bahan baku
Jumlah kandungan karbohidrat pada bahan baku sangat
berpengaruh terhadap hasil hidrolisis asam, dimana bila kandungan
karbohidrat sedikit maka jumlah gula yang terjadi juga sedikit dan
sebaliknya bila kandungan suspensi terlalu tinggi mengakibatkan
kekentalan campuran akan meningkat, sehingga tumbukkan antara
molekul karbohidrat dan molekul air semakin berkurang dengan demikian
kecepatan reaksi pembentukan glukosa semakin berkurang pula. Bahan
yang hendak di hidrolisis diaduk dengan air panas dan jumlah bahan
kering umumnya sekitar 18 – 22 %.
b. pH operasi atau konsentrasi asam yang digunakan
pH berpengaruh terhadap jumlah produk hidrolisis, pH ini erat
hubungannya dengan konsentrasi asam, dimana pH makin rendah bila
konsentrasi asam yang digunakan lebih besar, pH yang baik sekitar 2,3.
(Soebijanto, 1986) c. Waktu hidrolisis
Semakin lama pemanasan, warna semakin keruh dan semakin besar
pula konversi pati yang dihasilkan. Waktu optimum yang diperoleh untuk
proses hidrolisis asam yaitu 60 menit.
d. Suhu Hidrolisis
Semakin besar suhunya semakin besar pula konversinya karena
konstanta kecepatan reaksi juga semakin besar. Suhu optimum yang
diperoleh adalah 60 ºC.
e. Katalisator
Katalisator yang biasa digunakan berupa asam, yaitu HCl, H2SO4,
H2SO3, HNO3, dan lain-lain. Makin banyak asam yang dipakai sebagai
katalisator, makin cepat jalannya reaksi hidrolisa. Penggunaan katalisator
dengan konsentrasi kecil (larutan encer) lebih disukai karena akan (C6H10O5)n + 1/2n H2O 1/2n C12H22O11
Enzim Amilase
memudahkan pencampuran sehingga reaksi dapat berjalan merata dan
efektif.
f. Kecepatan pengadukan
Kecepatan pengadukan yang digunakan untuk proses hidrolisis adalah
±200 rpm. (Olivia, 2004)
II.4. Pengertian Alkohol
Etil alkohol (CH3CH2OH) atau etanol dikenal dengan nama alkohol.
Merupakan suatu cairan tak berwarna dengan bau yang khas. Tata Bahasa
alkohol sendiri berasal dari bahasa arab : kuhl atau kohol, yang berarti intinya
tepung. (Soebijanto, 1986)
Ethanol dapat dibuat dari berbagai bahan hasil pertanian. Secara
umum, bahan-bahan tersebut dapat dibagi dalam tiga golongan yaitu golongan
pertama adalah bahan yang mengandung turunan gula, antara lain molase, gula
tebu, gula bit, dan sari buah-buahan. Golongan kedua adalah bahan-bahan
yang mengandung pati seperti biji-bijian (misalnya gandum), kentang, dan
tapioka. Golongan yang ketiga adalah bahan yang mengandung selulosa
seperti kayu dan beberapa limbah pertanian. Selain ketiga jenis bahan tersebut,
ethanol dapat dibuat juga dari bahan bukan asli pertanian tetapi dari bahan
yang merupakan hasil proses lain. Sebagai contohnya adalah ethylene.
(Gumbira Sa’id, 1987)
Ethanol merupakan produk fermentasi yang dapat dibuat dari
substrat yang mengandung karbohidrat (gula, pati / sukrosa). Fermentasi
ethanol terjadi pada kondisi anaerob dengan menggunakan khamir tertentu
yang dapat mengubah glukosa menjadi ethanol. (Kirck Othmer,1953)
Hasil atau produk yang diinginkan dari fermentasi glukosa adalah
ethanol. Ethanol mempunyai rumus dasar C2H5OH. Ethanol mempunyai
sifat-sifat fisik sebagai berikut:
1. Cairan tidak berwarna
2. Berbau khas, menusuk hidung
3. Mudah menguap
4. Titik didih 78,32 oC
5. Larut dalam air dan eter
7. Spesifik panas pada 20 oC adalah 0,579 cal/groC
8. Panas pembakaran pada keadaaan cair adalah 328 Kcal
9. Viskositas pada 20 oC adalah 1,17 cp
10.Flash point adalah sekitar 70 oC
Sifat-sifat kimia ethanol :
1. Berat molekul adalah 46,07 gr/mol
2. Terjadi dari reaksi fermentasi monosakarida
3. Bereaksi dengan asam asetat, asam sulfat, asam nitrit, asam ionida.
(Faith and Keyes,1957 ; Kirk Othmer vol 9 ; Soebijanto)
Didalam perdagangan dikenal tingkat-tingkat kualitas ethnol sebagai
berikut :
a. Alkohol teknis (96,5 ºGL).
Digunakan terutama untuk kepentingan industri. Sebagai pelarut organik,
bahan bakar, dan juga sebagai bahan baku ataupun antara produksi
berbagai senyawa organik lainnya.
b. Spiritus (88 ºGL).
Bahan ini biasa digunakan sebagai bahan bakar untuk alat pemanas
ruangan dan alat penerangan.
c. Alkohol absolute (99,7 - 99,8 ºGL).
Banyak digunakan dalam pembuatan sejumlah besar obat-obatan dan juga
sebagai bahan pelarut atau sebagai bahan antara didalam pembuatan
senyawa-senyawa lain skala laboratorium.
d. Alkohol murni (96,0 - 96,5 ºGL).
Alkohol jenis ini terutama digunakan untuk kepentingan farmasi dan
konsumsi (minuman keras dan lain-lain). (Soebijanto, 1986)
II.5. . FERMENTASI
Fermentasi ethanol adalah suatu proes penguraian karbohidrat menjadi
etanol dan CO2 yang dihasilkan oleh aktivitas suatu mikroba dalam keadaan
anaerob dengan menggunakan katalis enzim.
Ethanol merupakan bentuk alami yang dihasikan dari proses fermentasi
yang banyak ditemukan dalam produk bir, anggur, spiritus dan masih banyak
1. Produk hasil fermentasi yang dikonsumsi langsung.
2. Produk hasil fermentasi yang didistilasi lebih dahulu sebelum dikonsumsi.
Dalam pembentukan alkohol melalui fermentasi, peran mikrobiologi sangat
besar dan biasanya mikrobiologi yang digunakan untuk fermentasi mempunyai
beberapa syarat sebagai berikut :
1. Mempunyai kemampuan untuk memfermentasi karbohidrat yang cocok
secara cepat.
2. Bersifat membentuk flakulasi dan sedimentasi.
3. Mempunyai genetik yang stabil (tidak mudah mengalami mutasi).
4. Toleran terhadap alkohol yanng tinggi (antara 14 – 15 %).
5. Mempunyai sifat regenerasi yang cepat. (Bambang Kartika, 1993)
Minuman beralkohol yang dihasilkan tanpa distilasi (hasil fermentasi)
biasanya mempunya kadar alkohol antara 3 – 18 %. Untuk mempertinggi
kadar alkohol dalam produk sering kali hasil fermentasi di distilasi dan kadar
alkohol yang dihasilkan antara 29 – 50 %. Prinsip dasar reaksi pembentukan
ethanol dengan fermentasi sebagai berikut :
(Sri Kumalningsih, 1995)
Faktor - faktor yang mempengaruhi dalam proses fermentasi antara
lain sebagai berikut :
a. pH
pH yang baik untuk fermentasi, yaitu antara pH 4 - 5. pH ini adalah pH
yang disenangi oleh ragi dan pada pH ini dapat menahan perkembangan
banyak jenis bakteri. Untuk mengasamkan biasanya dipergunakan asam
sulfat. Yang lebih baik lagi adalah asam laktat, karena asam laktat baik
untuk pertumbuhan ragi, tetapi keburukannya dapat tumbuh bakteri asam
butirat yang dapat merugikan fermentasi dari ragi.
b. Waktu
Waktu yang diperlukan untuk fermentasi tergantung pada temperatur,
konsentrasi gula. Tetapi pada umumnya waktu yang diperlukan antara 36 -
50 jam. (D. Syamsul bahri)
c. Suhu
Pada umumnya suhu yang baik untuk proses fermentasi antara 25 – 30 ºC.
Semakin rendah suhu fermentasi akan semakin tinggi alkohol yang di
hasilkan. Hal ini dikarenakan pada suhu yang rendah fermentasi akan lebih
lengkap dan kehilangan alcohol lebih sedikit.
d. Bahan Nutrient
Kecepatan fermentasi akan dipengaruhi oleh konsentrasi garam logam
dalam perasan. Pada konsentrasi yang rendah akan menstimulur Aktivitas
dan pertumbuhan khamir, sedangkan pada konsentrasi tinggi akan
menghambat pertumbuhan khamir. Unsur yang dibutuhkan untuk aktivitas
khamir antara lain Mg, K, Zn, CO, Fe, Ca, Cu, P, S, dan N. Sebagai
sumber P dan N perlu ditambahkan ammonium phospat. Sebagai sumber
N lainnya dapat pula ditambahkan ammonium klorida dan ammonium
karbonat. Selain itu ekstrak daging merupakan medium yang sangat baik
untuk pertumbuhan mikroba. Hal ini disebabkan ekstrak daging kaya akan
zat gizi yang mengandung nitrogen, karbohidrat yang dapat difermentasi,
kaya akan mineral untuk pertumbuhan mikroba, dan memiliki pH yang
baik untuk pertumbuhan mikroba. Oleh karena itu ekstrak daging
merupakan bahan nutrient yang sangat bagus buat pertumbuhan bakteri.
http://ayamdaging.web.id/index.php/2010051167/Campuran/pengawet-daging-alami.html.
e. Konsentarsi Gula
Gula yang ditambahkan pada sari buah bertujuan untuk memperoleh kadar
alkohol yang lebih tinggi, walaupun jika kadar gula tertalu tinggi aktivitas
khamir dapat terhambat. Kadar gula yang baik untuk permulaan fermentasi
adalah 16 %. Hal ini bertujuan untuk mempercepat pertumbuhan khamir
pada awal fermentasi. Penambahan kadar gula akan mengarahkan
fermentasi lebih sempurna serta menghasilkan alkohol yang tinggi. Kadar
gula yang optimum untuk aktivitas pertumbuhan khamir adalah 10 %.
II.6. Mikroorganisme dalam Fermentasi
II.6.1. Saccharomyces Cereviceae
Jenis khamir yang paling banyak digunakan adalah Saccharomyces Cereviseae. Secara komersial khamir roti telah diproduksi pada tahun 1846 dengan ditemukan proses “wina” oleh Mautner menggunakan bahan dasar
malt dan jagung. Biakan Saccharomyces Cereviceae secara khusus digunakan dalam pembuatan khamir roti dan fermentasi alkohol. Saccharomyces Cereviseae ini bersifat fermentatif kuat. Tetapi dengan adanya oksigen,
Saccharomyces Cereviseae ini juga melakukan respirasi yaitu mengoksidasi gula menjadi karbondioksida dan air. (Srikandi Fardiaz, 1992)
Adapun sifat-sifat dari Saccharomyces Cereviseae antara lain adalah : 1. Berbentuk bulat, ellips (bulat telur).
2. Tidak berflagella.
3. Tidak mempunyai klorofil.
4. Dapat membentuk spora.
Ragi ini memerlukan bahan makanan dan keadaan lingkungan tertentu
untuk pertumbuhannya dan perkembang biakkannya. Unsur-unsur yang
diperlukan, seperti : karbon, hidrogen, oksigen, fosfor, kalium, nitrogen,
belerang, kalsium, besi, dan magnesium. Selain itu juga diperlukan
vitamin-vitamin. (D.Syamsul Bachri)
II.6.2. Pertumbuhan Mikroorganisme
Pertumbuhan sel merupakan puncak aktivitas fisiologik yang saling
mempengaruhi secara beraturan. Proses pertumbuhan ini sangat kompleks
mencakup pemasukan nutrient dasar dari lingkungan ke dalam sel, konversi
bahan-bahan nutrient menjadi energi dan berbagai konstituent sel yang vital
serta perkembang biakkan. Pertumbuhan mikroorganisme dapat ditandai
dengan peningkatan jumlah dan masa sel, sedangkan kecepatan petumbuhan
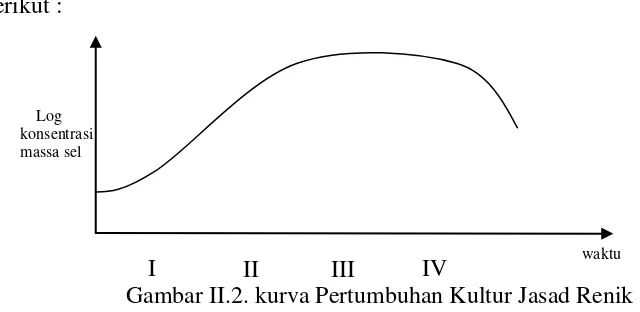
Pertumbuhan mikroorganisme dapat digambarkan sebagai kurva
berikut :
Gambar II.2. kurva Pertumbuhan Kultur Jasad Renik
Keterangan Gambar :
a.Fase Adaptasi
Fase ini adalah waktu penyesuaian suatu mikroorgnisme yang dipindahkan
ke media lain yang berbeda dari media asalnya. Lamanya fase ini
dipengaruhi oleh beberapa faktor, diantaranya :
1.Medium dan lingkungan pertumbuhan
Jika nutrient yang tersedia dan kondisi lingkungan yang baru sangat
berbeda dengan sebelumnya, diperlukan waktu penyesuaian untuk
mensintesa enzim – enzim yang dibutuhkan untuk metabolisme.
2. Jumlah inokulum
Jumlah awal sel yang semakin tinggi akan mempercepat fase adaptasi.
b.Fase Pertumbuhan Awal
Setelah mengalami fase adaptasi, sel mulai membelah dengan kecepatan
yang masih rendah karena baru selesai tahap penyesuaian diri.
c.Fase Pertumbuhan Logaritmik
Sel jasad renik membelah dengan cepat dan konstan, dimana pertumbuhan
sangat dipengaruhi oleh medium tempat tumbuhnya, seperti pH, kandungan
nutrient, suhu dan kelembabab udara. Pada fase ini sel membutuhkan energi
lebih benyak dari fase lainnya dan juga paling sensitive terhadap keadan
lingkungan.
d. Fase Pertumbuhan lambat
Pada fase ini pertumbuhan populasi jasad renik diperlambat karena beberapa
1.Zat nutrisi didalam medium sudah sangat berkurang.
2.adanya hasil – hasil metabolisme yang mungkin beracun atau dapat
menghambat pertumbuhan jasad renik.
e.Fase Pertumbuhan Statis (tetap)
Pada fase ini, jumlah populasi sel tetap, karena jumlah sel yang mati sama
dengan jumlah sel yang tumbuh. Ukuran sel menjadi lebih kecil, karena sel
terus membelah sementara nutrisi yang ada semakin berkurang. Pada fase ini
sel memjadi lebih tahan terhadap keadaan akstrim seperti panas, dingin,
radiasi, dan bahan kimi.
f.Fase Menuju Kematian dab Fase Kematian
Pada fase ini sebagian populasi jasad renik mulai mengalami kematian
karena beberapa sebab, yaitu :
1.Nutrient didalam medium sudah habis
2.energi cadangan didalam sel habis
Jumlah sel yang mati akan semakin banyak, dan kecepatan kematian
dipengaruhi oleh kondisi nutrient, lingkungan dan jenis jasad renik.
II.7. Landasan Teori
II.7.1 Fungsi dari HCl
Hidrolisis dalam larutan Asam
Asam encer atau pekat misalnya HCl, H2SO4 (Asam lain mahal). Biasanya
berfungsi sebagai katalisator. Pada Asam encer, Pada umumnya kecepatan
reaksi sebanding dengan konsentrasi H+ menjadi [H+]. Sifat ini tidak berlaku
pada Asam pekat. Pemakaian H2SO4 lebih disukai karena HCl korosif.
(C6H10O5)n + n H2O HCl C6H12O6
II.7.2. Faktor-Faktor yang mempengaruhi Hidrolisis
Selulosa dari Jerami Padi dapat diubah menjadi ethanol dengan proses
hidrolisis asam dengan kadar tertentu. Proses hidrolisis selulosa harus
dilakukan dengan asam pekat agar dapat menghasilkan glukosa.(Fieser.1963).
Proses hidrolisis ini dipengaruhi oleh beberapa faktor, diantaranya :
1. Suhu
Suhu juga mempengaruhi proses kecepatan reaksi hidrolisis. Suhu yang baik
untuk hidrolisis selulosa adalah sekitar 21 oC, selain itu pada penelitian
terdahulu oleh TEO HUDIKO dan MITHA DWIANA DEWI, 2007 dengan judul
bioetanol terhadap rumput Gajah dengan proses hidrolisis dan fermentasi suhu
terbaik ada pada suhu kamar yaitu 30oC.
2. Konsentrasi
Konsentrasi mempengaruhi laju reaksi hidrolisis. Untuk hidrolisis asam
digunakan konsentrasi HCl pekat atau H2SO4 pekat.(Groggins,1985)
Dalam proses ini selulosa dalam Jerami Padi diubah menjadi glukosa
dengan reaksi sebagai berikut:
(C6H10O5)n + n H2O C6H12O6 ...(2)
Selulosa Glukosa
3.pH (derajat keasaman)
pH mempengaruhi proses hidrolisis sehingga dapat dihasilkan hidrolisis yang
sesuai dengan yang diinginkan. pH yang baik untuk proses hidrolisis adalah
2,3.(Soebijanto,1986), selain itu pada penelitian terdahulu oleh TEO HUDIKO
dan MITHA DWIANA DEWI, 2007 dengan judul bioetanol terhadap rumput
Gajah dengan proses hidrolisis dan fermentasi yang menggunakan pH 3.
II.7.3. Faktor-Faktor dalam Fermentasi
Fermentasi pertama kalinya dilakukan perlakuan dasar terhadap bibit
fermentor / persiapan starter. Dimana starter diinokulasikan sampai
benar-benar siap menjadi fermentor, baru dimasukkan ke dalam substrat yang akan
difermentasi.(Dwijoseputro). Bibit fermentor yang biasa digunakan adalah
Saccharomyces Cerevisiae.
a. Mempunyai bentuk sel yang bulat, pendek oval, atau oval.
b. Mempunyai ukuran sel (4,2-6,6) x (5-11) mikron dalam waktu tiga hari
pada 25oC dan pada media agar.
c. Dapat bereproduksi dengan cara penyembulan atau multilateral.
d. Mampu mengubah glukosa dengan baik.
e. Dapat berkembang dengan baik pada suhu antara 20-30 oC
(Judoamidjojo,1992 dan Faith Keyes).
Khamir mempunyai kurva pertumbuhan tertentu, dengan adanya kurva
pertumbuhan ini maka dapat diketahui waktu yang tepat untuk memasukkan
khamir ke dalam substrat yang akan difermentasi.
Pada fase pertama, khamir masih dalam tahap pemindahan dan belum
mengadakan pembiakan dan disebut fase adaptasi.
Pada fase kedua, jumlah khamir mulai bertambah banyak sedikit demi
sedikit yang mana dalam fase ini sel-sel tampak lebih gemuk. Dan langsung
disusul oleh fase pembiakan cepat. Dalam fase ini disebut sebagai fase log.
Pada fase ini khamir berkembang biak dengan cepat. Fase ini merupakan fase
yang sangat baik untuk menjadikannya sebagai inokulum.
Pada fase ketiga, khamir mulai dalam fase stagnant yaitu dimana khamir
kecepatan berkembang biaknya berkurang, sehingga jumlah bakteri yang mati
sama dengan jumlah bakteri yang berkembang biak. Dengan demikian, kurva
menunjukkan garis yang horizontal.
Pada fase keempat karena berbagai faktor baik keadaan medium yang
memburuk, perubahan pH, atau pun karena bertumpuk-tumpuknya zat
kotoran, maka jumlah bakteri yang mati semakin banyak dan makin melebihi
jumlah bakteri yang membelah diri, sehingga grafiknya menunjukkan keadaan
menurun. Fase itu disebut fase kematian.
( Dwidjoseputro,1990)
4 3
Proses fermentasi dipengaruhi oleh :
1. Nutrisi
Pada proses fermentasi, mikoroorganisme sangat memerlukan
nutrisi yang baik agar dapat diperoleh hasil fermentasi yang baik.
Nutrisi yang tepat untuk menyuplai mikroorganisme adalah nitrogen
yang mana dapat diperolah dari penambahan NH3, garam amonium,
pepton, asam amino, urea. Unsur-unsur N, P, dan K yang ada pada
Jerami padi juga merupakan nutrisi makanan tambahan yang telah
ditambahkan nutrisi-nutrisi makanan sebelumnya. Penambahan
unsur-unsur N, P, dan K sendiri tidak boleh melebihi dari 8% karena jika lebih
dari itu akan menghambat pertumbuhan bakteri. (Agus Krisno, 2002)
Selain itu ekstrak daging merupakan medium yang sangat baik sebagai
pertumbuhan mikroba. Hal ini disebabkan ekstark daging kaya akan zat
gizi yang mengandung nitrogen, karbohidrat dan asam amino yang bagus
untuk proses fermentasi, ektrak daging juga kaya akan mineral serta
memiliki pH yang baik untuk pertumbuhan mikroba pada saat
pembuatan media agar.
http://ayamdaging.web.id/index.php/2010051167/Campuran/pengawet-daging-alami.htm.l
2. pH
pH yang baik untuk pertumbuhan bakteri adalah 4,5 – 5. Tetapi
pada pH 3,5 fermentasi masih dapat berjalan dengan baik dan bakteri
pembusuk akan terhambat. Untuk mengatur pH dapat digunakan NaOH
dan HNO3.
3. Suhu
Suhu yang baik untuk pertumbuhan bakteri adalah antara 20-30
o
C. Makin rendah suhu fermentasi, maka akan semakin tinggi ethanol
yang akan dihasilkan, karena pada suhu rendah fermentasi akan lebih
komplit dan kehilangan ethanol karena terbawa oleh gas CO2 akan lebih
sedikit.
4. Waktu
Waktu yang dibutuhkan untuk fermentasi adalah 7
hari.(Judoamidjojo.1992), karena pada penelitian terdahulu telah
hidrolisis dan fermentasi oleh TEO HUDIKO dan MITHA DWIANA
DEWI pada tahun 2007 melakukan proses fermentasi selama 8 hari.
5. Kandungan gula
Kandungan gula akan sangat menpengaruhi proses fermentasi,
kandungan gula optimum yang diberikan untuk fermentasi adalah 25%.
Untuk permulaan, kadar gula yang digunakan adalah
16%.(Sardjoko.1991).
6. Volume starter
Volume starter yang baik untuk melakukan fermentasi adalah
1/10 bagian dari volume substrat, selain itu pada penelitian terdahulu
telah dilakukan penelitian bioetanol terhadap rumput Gajah dengan
proses hidrolisis dan fermentasi oleh TEO HUDIKO dan MITHA DWIANA
DEWI menggunakan volume stater sebanyak 6%, 8%, 10%, 12%, dan
14%.
Dalam proses fermentasi ini, glukosa dari hasil fermentasi
diubah menjadi ethanol dengan reaksi sebagai berikut :
Saccharomyces
C6H12O6 2C2H5OH + 2CO2 ...(3)
Glukosa Etanol
Riset Pembanding
Pada penelitian terdahulu telah dilakukan penelitian bioetanol terhadap
rumput Gajah dengan proses hidrolisis dan fermentasi yang menggunakan
larutan HCl dengan kadar pH 3 pada suhu 300C dan waktu fermentasi selama
8 hari. Sehingga menghasilkan kadar gulukosa sisa sebanyak 8,09 %, dan
kadar etanol setelah didistilasi sebanyak 27,71% .(Penelitian TEO HUDIKO dan
MITHA DWIANA DEWI, 2007)
Pada penelitian terdahulu telah dilakukan penelitian terhadap biji kapas
dengan proses hidrolisis yang menggunakan 0,8 % H2SO4 pada suhu 120oC
selama 1 jam sehingga dihasilkan kadar glukosa tertinggi 13,848 %. Glukosa
ini mendapat perlakuan fermentasi yang optimum selama 72 jam dengan kadar
Pada penelitian terdahulu tentang buah siwalan dilakukan proses
hidrolisis dengan pH 2,3 , suhu 100oC , H2SO4 1 N. Dengan proses tersebut
dapat dihasilkan kadar glukosa optimum sebesar 21,86 % kemudian dilakukan
proses fermentasi dengan penambahan optimum (NH4)HPO4 sebesar 9 gram
sehingga didapatkan 9,92 % ethanol setelah distilasi dan kadar glukosa sisa
sebesar 8,02 % (Eri Maryudha Saputra, 2007).
II.8. HIPOTESIS
Adanya selulosa dan glukosa dalam jerami Padi, maka jerami Padi
BAB III
METODE PENELITIAN
III.1. BAHAN
III.1. BAHAN UNTUK PENELITIAN
1. Jerami Padi 5. Pepton
2. Larutan HCl 6. Agar-agar
3. Aquadest 7. KH2PO4
9. Asam sitrat 10.Saccharomyces Cerevisiae
11. Kecambah 12. Neraca Analitik
III.2. ALAT-ALAT
1. Pengaduk
2. Pemanas
3. Neraca analitik
4. Piknometer
5. Kertas pH
6. Kertas saring
7. Erlenmeyer
8. Pipet
9. Autoclave
10.Exicator
11.Perangkat fermentasi
12.Perangkat distilasi
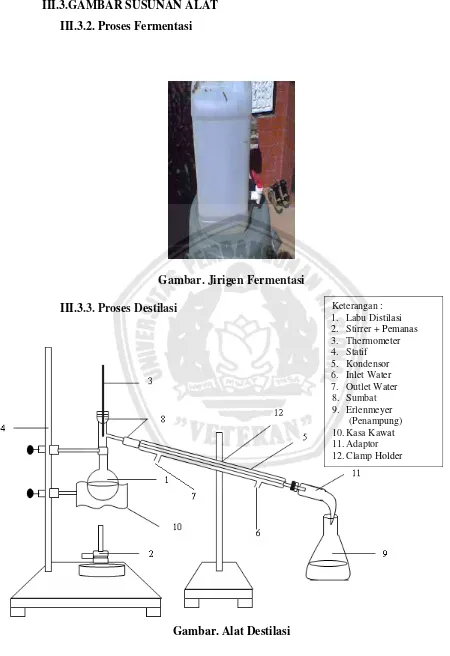
III.3.GAMBAR SUSUNAN ALAT
III.3.2. Proses Fermentasi
Gambar. Jirigen Fermentasi
III.3.3. Proses Destilasi
Gambar. Alat Destilasi
Keterangan : 1. Labu Distilasi 2. Stirrer + Pemanas 3. Thermometer 4. Statif 5. Kondensor 6. Inlet Water 7. Outlet Water 8. Sumbat 9. Erlenmeyer
III..4. KONDISI YANG DIGUNAKAN
1. Proses Hidrolisis
Kondisi tetap : suhu : 30 oC
: volume larurtan HCl : 2500 mL
: waktu : 2 hari
: pH larutan HCl :3
Kondisi berubah : berat jerami Padi : 40,50,60, (gram)
2. Proses fermentasi
Kondisi tetap : suhu : 30 oC
: pH filtrat hidrolisis : 4,5
: volume fermentasi : 2500 mL
Kondisi berubah : waktu : 2,3,4,5,6,7 (hari)
: starter : 8% (200ml), 10% (250ml),
III.6. PROSEDUR PENELITIAN
III.6.1. Persiapan Alat
Alat-alat yang akan digunakan seperti beaker glass, erlenmeyer,
pengaduk, dan botol-botol untuk proses hidrolis harus dibersihkan
terlebih dahulu baik dengan cara pemanasan atau pencucian.
III.6.2. Persiapan Bahan Baku
Jerami Padi terlebih dahulu dipotong kecil-kecil kemudian dikeringkan.
Setelah itu di tumbuk sampai berbentuk pipih atau gepeng. Ini bertujuan
untuk memudahkan proses hidrolisis lebih baik, karena dengan ditumbuk
di harapkan selulosa terhidrolisa dengan sempurna.
III.6.3. Membuat Nutrient agar
Bahan :
Ekstrak Daging = 0,6 gram
Pepton = 1 gram
Agar – agar = 3,8 gram
Aquadest = 200 ml
Cara :
1. Bahan tersebut dicampur dalam erlenmeyer / beker gelas,
dipanaskan sampai larut semua.
2. Sterilkan dalam autoclave selama 15 menit.
3. Dinginkan sampai kira – kira 70 oC, lalu pindahkan ke tabung
reaksi yang steril, lalu tabung dimiringkan. Kerjakan dalam
ruangan gelas steril.
4. Media padat dalam tabung siap ditanami.
III.6.4. Membuat Media Cair untuk kurva pertumbuhan
Bahan :
Kecambah pendek = 15 gram
Gula = 25 gram
Aquadest = 500 ml
KH2PO4 = 5 gram
Cara :
1. 15 gram kecambah (tauge) pendek yang baru tumbuh.
Tumbuklah kasar – kasar, kemudian rebuslah dengan aquadest
sebanyak 500 ml.
2. Tambahkan gula sebanyak 25 gram dan KH2PO4 sebanyak 5 gr
3. Didihkan selama 30 menit, lalu disaring.
4. Filtrat dibuat pH = 4,5, dengan penambahan asam sitrat.
5. Lalu disterilkan.
6. Filtratnya setelah dingin ditambahkan biakan Saccharomyces Cerevisiae.
7. Lalu diinkubasi selama 48 jam, setiap 2 jam sekali diambil
sampel (contoh) untuk dianalisa sel keringnya (sebentar –
sebentar dikocok / dishaker).
8. Analisa sel keringnya :
Setiap 2 jam sekali contoh diambil 10 ml, lalu disaring,
kemudian dioven pada suhu 105 oC – 110 oC. Selama 30 menit,
lalu dimasukkan ke Exikator. Setelah dingin ditimbang,
kemudian dioven lagi dan seterusnya sampai beratnya konstan.
III.6.5. Pembuatan Starter Saccharomyces Cerevisiae.
1. 150 gram kecambah (tauge) pendek yang baru tumbuh.
Tumbuklah kasar – kasar, kemudian rebuslah dengan aquadest
sebanyak 5 liter.
2. Tambahkan gula sebanyak 250 gram dan tambahkan KH2PO4
50 gram
3. Didihkan selama 30 menit, lalu disaring.
4. Filtrat dibuat pH = 4,5, dengan penambahan asam sitrat.
5. Lalu disterilkan.
6. Filtratnya setelah dingin ditambahkan biakan Saccharomyces Cerevisiae .
III.6.6 Hidrolisis
1. Menimbang jerami padi seberat variabel yang telah dijalankan
(40,50,60 gram).
2. Merendam jerami padi ke dalam 2500 ml larutan HCl yang telah
diencerkan dengan aquadest hingga mencapai kadar pH menunjukkan
angka pH 3 yang telah sesuai dengan kondisi operasi dan pada suhu
30oC selama 2 hari.
3. Menyaring larutan tersebut dan mengambil filtratnya.
4. Menganalisa kadar glukosa pada filtrat hasil hidrolisa. Kadar gulukosa
yang diketahui ini dijadikan sebagai kadar gulukosa awal atau kadar
gulukosa yang belum difermentasi.
5. Menambahkan Asam Sitrat ke dalam filtrat hasil hidrolisa yang akan
difermentasi hingga mencapai pH fermentasi yang telah ditetapkan
III.6.7 Fermentasi
1. Hasil glukosa terbaik yang diperoleh dari proses hidrolisis, yaitu glukosa
yang diperoleh dari hidrolisis jerami padi seberat (40,50,60) gr dengan
pH 3 untuk larutan HCl sebanyak dari hasil proses hidrolisis 2500 ml.
2. Menambahkan Asam Sitrat ke dalam filtrat hasil hidrolisa yang akan
difermentasi hingga mencapai pH fermentasi yang telah ditetapkan
(4,5).
3. Memasukkan starter ke dalam larutan tersebut dalam kondisi anaerobik.
4. Menutup rapat botol dan mengamati selama 2-7 hari.
5. Kemudian menganalisa kadar ethanol.
III.7. Distilasi
Hasil dari fermentasi yang didapat dimasukkan kedalam labu distilasi
untuk mendapatkan alkohol dari glukosa. Proses distilasi ini dijalankan pada
suhu 70 - 80oC selama kurang lebih 5 jam.
III.7.1. Analisa Kadar Ethanol
1. Hasil fermentasi diambil sebanyak 500 mL kemudian dimasukkan ke
dalam labu distilasi.
2. Lalu didistilasi dan hasil distilasi ditampung dengan erlenmeyer
3. Hasil distilasi tersebut dimasukkan ke dalam piknometer dan ukurlah
berart jenisnya.
Perhitungan :
-Timbang piknometer kosong : a gram
-Timbang piknometer yang berisi hasil distilat : b gram
-volume piknometer : v ml
Dari hasil berat jenis tersebut, kemudian dilihat kadar ethanol pada tabel 3.110
III.7.2. Analisa Kadar Gula
• Pipet 10 ml larutan hasil penyaringan dan masukkan ke dalam Erlenmeyer, encerkan dengan air suling 50 ml, kocok hingga homogen.
• Pipet 50 ml larutan tersebut ke dalam Erlenmeyer, tambahkan batu didih, Erlenmeyer tersebut disambung dengan pendingin tegak dan panaskan
sampai mendidih selama 10 menit.
• Kemudian segera didinginkan dalam air yang mengalir atau dalam air es dan jangan digoyang.
• Setelah dingin tambahkan 10 ml larutan KI 5 % dan 12,5 ml larutan H2SO4 (hati-hati).
• Titrasi dengan 0,1 N larutan thio (Na2S2O3) dengan amilum sebagai indikator.
Perhitungan
Misalkan volume titrasi untuk contoh = a ml
Volume titrasi untuk blanko =b ml
(b-a) x N thio = X
Harga X dihitung berdasarkan daftar Luff Schaart.
Rumus = harga X pengenceran x 100 %
BAB IV
HASIL DAN PEMBAHASAN
IV.1. Analisa Bahan Baku ( Jerami Padi )
Jerami Padi kering dianalisa terlebih dahulu kadar glukosa sebelum dilakukan
proses hidrolisis. Hasil analisa kadar glukosa dalam jerami padi kering adalah sebagai
berikut :
Tabel IV.1. Hasil Analisa Kadar Glukosa Awal
IV.2. Proses Hidrolisis
Setelah didapat hasil analisa kadar glukosa awal, selanjutnya dilakukan proses
hidrolisis untuk memecah selulosa yang terkandung dalam jerami padi menjadi
glukosa. Hasil analisa yang didapat untuk kadar glukosa setelah hidrolisis adalah
sebagai berikut :
Tabel IV.2. Hasil Analisa Kadar Glukosa
NO PARAMETER SATUAN HASIL UJI JERAMI PADI (gr) ACUAN METODE
1 Glukosa % 40,33 40 HPLC
2 Glukosa % 38,89 50 HPLC
3 Glukosa % 32,40 60 HPLC
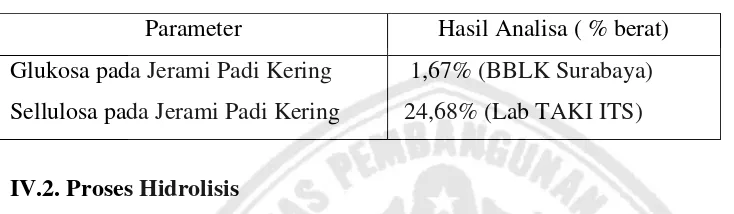
Parameter Hasil Analisa ( % berat)
Glukosa pada Jerami Padi Kering
Sellulosa pada Jerami Padi Kering
1,67% (BBLK Surabaya)
IV.3. Pembiakan Bakteri Saccharomyces Cerevisiae
Tabel IV.3. Hasil Pengamatan Kurva Pertumbuhan
Gambar IV.1. Hubungan biomassa Saccharomyces Cerevisiae dengan waktu
Pada Gambar IV.2. menunjukkan bahwa kurva pertumbuhan bakteri mengalami
empat fase yaitu fase lag yang mana Saccharomyces Cerevisiae mulai beradaptasi untuk tumbuh, ditunjukkan pada waktu 0 sampai 10 jam. Kemudian dilanjutkan
dengan fase log pada waktu 14 sampai 26 jam. Setelah itu pada waktu 26 – 28 jam
terjadi fase stasioner. Dan waktu selanjutnya merupakan fase kematian. Sehingga
berdasarkan data, waktu yang terbaik untuk memasukkan starter ke dalam filtrat
hidrolisis adalah pada waktu 10 jam. Hal ini dikarenakan pada waktu tersebut Waktu
Saccharomyces Cerevisiae mulai tumbuh menjadi gemuk dan siap untuk mengkonversi gukosa menjadi ethanol.
IV.4. Hasil Fermentasi
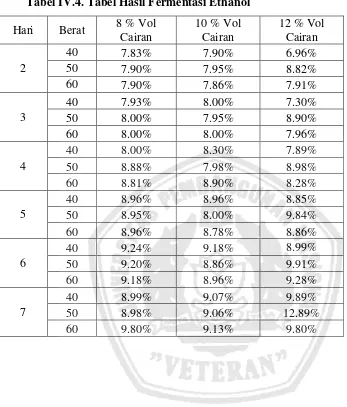
Tabel IV.4. Tabel Hasil Fermentasi Ethanol
Gamabar IV.2 Hubungan antara hari (lamanya fermentasi) dengan persen alkohol yang terbentuk.
Dari gambar grafik IV.2 diatas dapat dinyatakan bahwa kadar alkohol yang
terbaik setelah mengalami proses distilasi adalah dengan berat jerami padi kering 50
gr dengan jumlah stater 12 % volume cairan, hal ini bisa didapatkan dengan cara
distilasi yang lebih baik jika dibandingkan dengan distilasi yang lain.
Karena proses distilasi sangat sensitif terhadap suhu sehingga pada saat proses
distilasi suhu distilasi harus benar-benar diperhatikan agar didapatkan kadar alkohol
yang semurni mungkin, karena dalam praktikum menggunakan proses distilasi
manual sehingga pada saat distilasi suhu yang didapat dari maing-masing larutan
berbeda-beda antara variabel satu dengan yang lainnya.
Pengaruh kandungan mineral yang terkandung pada Jerami Padi sendiri juga
berpengaruh terhadap proses fermentasi, karena pada hidrolisis kandungan mineral
pada tumbuhan Jerami Padi ada terendapkan dan ada pula yang terikut dalam filtrat.
Sehingga kandungan mineral yang ada juga berpengaruh pada saat dilakukannya
proses fermentasi, ini dikarenakan pada saat akan melaukan proses fermentasi bakteri
BAB V
KESIMPULAN DAN SARAN
V.1. Kesimpulan
1. Pada proses fermentasi kondisi terbaik untuk menghasilkan etanol yaitu
dengan menggunakan berat Jerami Padi sebesar 50 gram dan starter
Saccharomyces Cerevisiae sebesar 12 % larutan. Proses fermentasi berlangsung selama 7 hari, yang menghasilkan ethanol sebesar 12,89 %.
2. Jerami Padi dapat digunakan sebagai bahan baku alternatif pembuatan
bio-ethanol.
V.2. Saran
Pada penelitian ini kadar glukosa yang dihasilkan sudah maksimal, tetapi
kadar ethanol yang dihasilkan tidak maksimal karena alat bioreaktor yang kurang
memadai. Diharapkan untuk penelitian serlanjutnya menggunakan alat bioreaktor
yang standart sehingga dapat dihasilkan kadar ethanol yang tinggi.
Diharapkan penelitian ini dapat dikembangkan dengan mencoba untuk
menggunakan variasi jumlah starter dan waktu fermentasi yang lebih lama guna
melihat sejauh mana kemampuan mikroorganisme dalam mengkonvesi glukosa
menjadi ethanol dengan sejumlah starter yang digunakan. Selain itu untuk
mendapatkan kadar ethanol yang jauh lebih tinggi dan murni, ada baiknya dilakukan
DAFTAR PUSTAKA
Budiyanto, Krisno Agus. H. 2002. MIKROBIOLOGI DASAR. Universitas
Muhammadiyah Malang : Malang.
Buckles, K.A, Edwards, R.A, Fleet, G.H, Wooton, M,. 1985. Ilmu Pangan. UI :
Jakarta.
Dwijoseputro. 1982 . Dasar – Dasar Mikrobiologi. Djambatan : Malang.
Fardiaz,Srikandi.1992.MIKROBIOLOGI PANGAN.Edisi 1.P.T.Gramedia Pustaka
utama : Jakarta.
Fengel,D, Wegener, G. 1995. KAYU (Kimia Ultrastruktur Reaksi-Reaksi).
UGM Press: Yogyakarta.
Fiesser dan Fisser. 1963 . Pengantar Kimia Organik. Dhiwantara : Bandung.
Hudiko Teo dan Dewi Dwiana Mitha, 2007, “Pembuatan Bio Ethanol dari Rumput
gajah dengan proses Hidrolisis dan fermentasi”, Fakultas Teknologi Industri
Jurusan Teknik Kimia UPN Veteran JATIM. Surabaya.
Judoamidjojo, Mulyono. 1992 . Teknologi Fermentasi. Rajawali Press : Jakarta.
Kirck, 0tehmer.1953.ENCYCLOPEDIA OF CHEMICAL TECHNOLOGI.2nd edition
volume 8.
Rahman, ansori.1989.PENGANTAR TEKNOLOGI FERMENTASI.Departemen
Pendidikan dan Kebudayaan Direktorat Jendral Pendidikan Tinggi Pusat
Antar Universitas Pangan dan Gizi IPB:BOGOR
Zulzaki Akbar Rois, 2005, ” Pembuatan Ethanl dari Biji Kapas dengan proses
Hidrolisis dan Fermentasi”, Fakultas Teknologi Industri Jurusan Teknik
Kimia UPN Veteran JATIM. Surabaya.
Sardjoko. 1991. Bioteknologi. Gramedia : Jakarta.
Saputra Eri Maryudha, 2007, ”Pembuatan Ethanol Dari Buah Siwalan dengan Proses
Hidrolisis dan Fermentasi”, Fakultas Teknologi Industri Jurusan Teknik
Kimia UPN Veteran JATIM. Surabaya.
Winarno. F.g, Fardiaz Srikandi, dan Fardias Dedi.1984.PENGANTAR TEKNOLOGI
PANGAN.P.T Gramedia : Jakarta.
http://72.14.235.104/search?q=cache:omEqHMACINUJ:buletinlitbang.dephan.go.id/index.asp %3Fvnomor%3D18%26mnorutisi%3D3+pembuatan+SELULOSA&hl=id&ct=clnk&cd=1&gl=id
LAMPIRAN A
APPENDIX :
Menghitung densitas Ethanol (ρ Ethanol)
Volume piknometer = 10 ml
Berat piknometer kosong = 11,4169 gr
Berat piknometer isi Distilat = 21,1959 gr
Berat piknometer isi air - Berat piknometer kosong
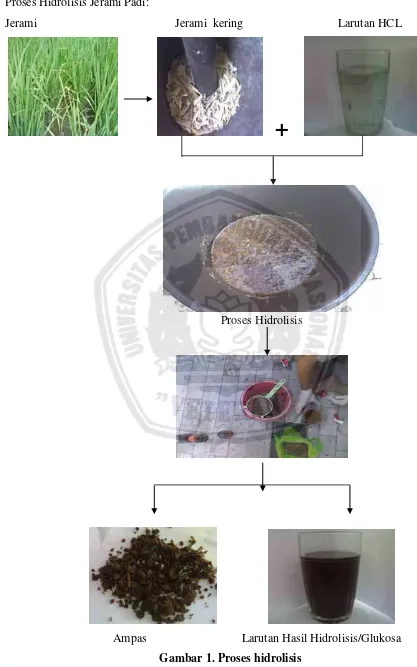
LAMPIRAN B
Proses Hidrolisis Jerami Padi:
Jerami Jerami kering Larutan HCL
+
Proses Hidrolisis
Ampas Larutan Hasil Hidrolisis/Glukosa
Saccharomyces Cerevisiae Pengenceran Saccharomyces Cerevisiae dalam larutan gula 5%
Pencampuran bahan media agar Penanaman Saccharomyces Cerevisiae
Pembiakan Saccharomyces Cerevisiae Penimbangan Bahan – Bahan
Pencampuran bahan Media Cair Pengambilan sample setiap 2 jam sekali
Penyaringan sample Pengeringan sample Saccharomyces Cerevisiae
Pembuatan Media Agar Pengambilan Untuk mengetahui
Pertumbuhan Saccharomyces Cerevisiae
tiap 2 jam sekali
Penimbangan Untuk Kurva Pertumbuhan
Kecambah Pencampuran Bahan Media Kecambah
KH2PO4 Ekstrak Daging
Aquades Saccharomyces Cerevisiae
Persiapan Botol Fermentasi Pemasukan Filtrat Glukosa
Fermentasi Awal Fermentasi setela hari yang ditentukan
Pengoyangan
Penyaringan dengan membrane
Pengujian dengan HPLC