SD SMP SMU
Ringkasan Materi
IKATAN KIMIA
KIMIA
1 SMU
Ikatan kimia : ikatan yang terjalin secara terpadu antara dua atom atau lebih dalam suatu molekul. A. Ruang Lingkup Ikatan
A. Hakikat Ikatan : setelah berikatan susunan elektron masing-masing atom mencapai kestabilan.
B. Kestabilan (Teori Oktet Lewis)
Atom menjadi stabil jika memiliki susunan elektron seperti gas mulia dengan serah terima elektron (ikatan ion) atau dengan perseketuan elektron (ikatan kovalen).
Unsur-unsur gas mulia yaitu : 2He : 2
10Ne : 2, 8
18Ar : 2, 8, 8
36Kr : 2, 8, 18, 8
54Xe : 2, 8, 18, 18, 8
86Rn : 2, 8, 18, 32, 18, 8
Unsur yang no. atomnya 5 (H, He, Li, Be, B) cenderung memiliki 2 elektron seperti Helium (duplet)
Unsur yang no. atomnya > 5 cenderung memiliki 8 elektron di kulit terluar (oktet) C. Unsur sekitar gas mulia
IA IIA IIIA VIIIA VIA VIIA
3Li 11Na
19K 37Rb 55Cs
4Be 12Mg
20Ca 38Sr 56Ba
5B 13Al
2He 10Ne 18Ar 36Kr 54Xe
8O 16S 34Se 52Te
7F 17Cl 35Br 53I
Memberikan elektron Menerima elektron
Ikatan Ion/Heteropolar/Elektrovalen
A. Pengertian :
Ikatan yang terjadi akibat perpindahan elektron
Ikatan antara atom yang melepaskan elektron (logam) dengan atom yang menangkap elektron (bukan logam)
Ikatan antara gol. IA & IIA dengan golongan VIA dan VIIA
Ikatan antara ion positif dan ion negatif
Ikatan antara atom-atom yang perbedaan keelektronegatifannya besar
Ikatan antara atom-atom yang mempunyai potensial ionisasi rendah dengan atom-atom yang mempunyai afinitas elektron tinggi
Catatan :
1. Jika atom memiliki elektron valensi 1, 2, atau 3, maka atom itu cenderung melepaskan elektron.
2. Jika atom memiliki elektron valensi
B. Pembentukan Ion Positif
Golongan Alkali
Unsur Konfigurasi elektron Elektron valensi
3Li 2, 1 1
11Na 2, 8, 1 1
19K 2, 8, 8, 1 1
37Rb 2, 8, 18, 8, 1 1 55Cs 2, 8, 18, 18, 8, 1 1 87Fr 2, 8, 18, 32, 18, 8, 1 1
Golongan Alkali Tanah
Unsur Konfigurasi elektron Elektron valensi
4Be 2, 2 2
12Mg 2, 8, 2 2
20Ca 2, 8, 8, 2 2
38Sr 2, 8, 18, 8, 2 2 56Ba 2, 8, 18, 18, 8, 2 2 88Ra 2, 8, 18, 32, 18, 8, 2 2
Ikatan antar atom
Ikatan Ion/ elektrovalen/
heteropolar
Ikatan Kovalen/ Homopolar : - Kovalen tunggal - Kovalen rangkap 2 - Kovalen rangkap 3
Polar Non polar Semipolar/ Koordinat /
SD SMP SMU
Konfigu
rasi elektron ion alkali = konfigurasi
elektron ion alkali tanah = konfigurasi elektron
gas mulia
Ion alkali Ion alkali tanah Konfigurasi Elektron
3Li+ 4Be+ 2 11Na+ 12Mg+ 2, 8
19K+ 20Ca+ 2, 8, 8 37Rb+ 38Sr+ 2, 8, 18, 8 55Cs+ 56Ba+ 2, 8, 18, 18, 8
87Fr+ 88Ra+ 2, 8, 18, 32, 18, 8 C. Pembentukan Ion Negatif
Golongan VIIA
Unsur Konfigurasi elektron Elektron valensi
9F 2, 7 7
17Cl 2, 8, 7 7
35Br 2, 8, 18, 7 7
53I 2, 8, 18, 18, 7 7 85At 2, 8, 18, 32, 18, 7 7
Golongan VIA
Unsur Konfigurasi elektron Elektron valensi
8O 2, 6 6
16S 2, 8, 6 6
34Se 2, 8, 18, 6 6
52Te 2, 8, 18, 18, 6 6
Konfigrasi elektron ion halogen = konfigurasi
elektron ion golongan oksigen = konfigurasi
elektron gas mulia
Ion halogen Ion gol. Oksigen
Konfigurasi Elektron
9F- 8O2- 2, 8 17Cl- 16S2- 2, 8, 8 35Br- 34Se2- 2, 8, 18, 8
53I- 52Te2- 2, 8, 18, 18, 8 85At- 8O2- 2, 8, 18, 32, 18, 8
D. Proses Pembentukan Ikatan Ion Contoh : Pembentukan senyawa MgF2 12Mg (2, 8, 2) → Mg2+ (2, 8) + 2e x 1 9F (2, 7) + e → F- (2, 8) x 2
Mg (2, 8, 2) + 2F (2, 7) → Mg2+ (2, 8) + 2F
-(2, 8)
Mg2+ + F- → MgF 2
Contoh senyawa Ion :
Gol. Alkali (IA) dan Gol. Halogen (VIIA)
NaF, NaBr, KI, KBr, RbI, CsF, LiF Gol. Alkali (IA) dan Gol. VIA
Na2O, Na2S, K2O, Rb2S
Gol. Alkali Tanah (IIA) dan Gol. Halogen (VIIA)
CaBr2, CaF2, MgBr2, SrCl2, CaCl2,
MgI2
Gol. Alkali Tanah (IIA) dan Gol. VIA MgO, CaO, CaS, BaO, SrO, MgS Ikatan Ion (dari ion logam dan ion
non logam )
KH, CaH2, Mg3N2, LiN, CaC2, AlCl3,
Al2O3
Ikatan Kovalen/Homopolar A. Pengertian
- Ikatan yang terjadi akibat pemakaian pasangan elektron secara bersama-sama
- Ikatan antara atom-atom yang sama-sama ingin menangkap elektron (sesama atom bukan logam) - Ikatan antara atom-atom yang perbedaan keelektronegatifan rendah
B. Pembagian
Berdasarkan penggunaan
bersama
Berdasarkan Kepolaran
Ikatan
Tunggal Rangkap 2Ikatan
Ikatan Rangkap 3
Persekutuan 2 Pihak Persekutuan Sepihak
Kovalen koordinat/ semipolar
Kovalen nonpolar
SD SMP SMU
Ikatan kovalen tunggal : penggunaan sepasang elektron bersama.
Contoh :
Rumus
Kimia H2 HCl H2O NH3 CH4
Rumus Lewis
H H
H Cl
H O H
H
N H
H
H
H C H
H
Rumus Struktur
H H
H Cl
H O H
H
N H H
H
H C H H
Ikatan kovalen rangkap 2 : penggunaan 2 pasang elektron bersama. Contoh :
Rumus Kimia
O2 CO2 C2H4
Rumus Lewis O
O O CO
H H
H C C H
Rumus Struktur
O O
O C O
H H
H C C H
Ikatan kovalen rangkap 3 : penggunaan 3 pasang elektron bersama.
Contoh :
Rumus
Kimia N2 HCN C2H2
Rumus
Lewis N
N
H C N
H C C H
Rumus Struktur
N N
H C N
H C C H
Catatan :
Pasangan elektron yang dipakai bersama-sama disebut Pasangan Elektron Ikatan (PEI) sedangkan yang tidak dipakai dalam ikatan disebut Pasangan Elektron Bebas (PEB).
Contoh :
Rumu s Kimia
O2 N2 CH4 NH3 H2O
PEI 2 3 4 3 2
PEB 4 2 - 1 2
Ikatan kovalen koordinasi = ikatan semi polar : Pasangan elektron milik bersama hanya disumbangkan oleh satu atom, sedangkan atom yang satu lagi tidak menyumbangkan elektron. Contoh : NH4Cl, NH3BH3, H2CO3,
H2SO4, HNO3, SO3, H3PO4.
- Syarat terjadinya ikatan kovalen koordinasi yaitu bila salah satu atom mempunyai PEB. - Ketika berikatan, PEB berubah status
menjadi PEI.
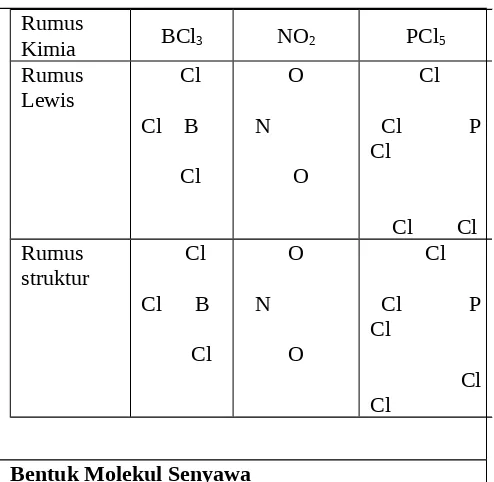
Penyimpangan Kaidah Oktet
Penyimpangan aturan oktet dibagi tiga kelompok, yaitu :
a. Senyawa yang tidak mencapai aturan oktet, yaitu senyawa yang atom pusatnya mempunyai elektron valensi kurang dari 4, sehingga setelah semua elektron valensinya dipasangkan tetap belum mencapai kaidah oktet. Contoh: BeCl2, BCl3, dan AlBr3.
b. Senyawa dengan jumlah elektron valensi ganijl, contoh : NO2.
c. Senyawa yang melampaui aturan oktet, Unsur dari periode 3 atau lebih dapat menampung lebih dari 8 elektron pada kulit terluarnya. Contoh : PCl5, SF6, ClF3,
SD SMP SMU
Untuk meramalkan bentuk molekul sederhana dapat ditempuh melalui langkah – langkah sebagai berikut:
1. Menentukan elektron valensi tiap atom 2. Menentukan jumlah elektron yang
digunakan untuk ikatan, yaitu dengan cara menjumlahkan elektron valensi atom pusat dengan elektron-elektron dari atom yang mengelilingi atom pusat.
3. Menentukan banyaknya pasangan elektron total (PE), yaitu dengan cara : banyaknya elektron yang digunakan untuk ikatan dibagi dua.
4. Menentukan banyaknya pasangan elektron terikat (PEI).
5. Menentukan banyaknya pasangan elektron bebas (PEB) dengan cara : jumlah pasangan elektron total (PE) dikurangi banyaknya pasangan elektron terikat (PEI).
Tabel berbagai kemungkinan bentuk mo
lekul
senyawa
ΣPEI Σ PEB Bentuk Molekul Contoh
4 0 Tetrahedron CH4
3 1 Piramida trigonal NH3
2 2 Planar bentuk V H2O
5 0 Bipiramida trigonal
PCl5
4 1 Bidang empat SF4
3 2 Planar bentuk T IF3
2 3 Linier XeF3
6 0 Oktahedron SF6
5 1 Piramida sisiempat IF5
4 2 Segi empat planar XeF4