ABSTRAK
Senyawa 4-asetamidofenil benzoat merupakan senyawa derivat p-aminofenol yang diduga mempunyai aksi analgetika dan anti-inflamasi, yang bekerja dengan menghambat enzim siklooksigenase-2 (COX-2). Penghambatan pada COX-2 berarti terjadi penghambatan pada interaksi enzim tersebut dengan asam arakhidonat yang memicu pembentukan prostaglandin sebagai penghasil respon inflamasi. Sintesis senyawa 4-asetamidofenil benzoat melalui reaksi substitusi nukleofilik asil (SNA) antara parasetamol (N-asetil-p-aminofenol) dan benzoil klorida dalam piridina dilakukan berdasarkan pemodelan molekul derivat p-aminofenol pada penelitian sebelumnya, yang memperoleh hasil yang menjanjikan sebagai senyawa dengan aksi yang lebih poten sebagai analgetika dan anti-inflamasi. Identifikasi senyawa hasil sintesis dilakukan melalui analisis terhadap organoleptis dan kelarutan, dilengkapi dengan uji kromatografi lapis tipis (KLT), uji titik lebur, elusidasi struktur malalui spektrofotometri inframerah, kromatografi gas, dan spektrometri massa (GC-MS), serta perhitungan rendemen. Hasil penelitian menunjukkan bahwa terjadi reaksi yang membentuk senyawa baru dengan rendemen rata-rata 26,152% b/b yang memiliki karakteristik golongan ester sesuai dengan senyawa tujuan.
ABSTRACT
4-acetamidophenyl benzoate is a p-aminophenol derivative which is believed to have actions as analgesic and anti-inflammation, that blocks cyclooxygenase-2 (COX-2) enzyme in its mechanism. Blocking in COX-2 causes the inhibition of enzyme interaction with arachidonic acid which originally produces prostaglandine, resulting in inflammation response. Synthesis of 4-acetamidophenyl benzoate through nucleophilic acyl substitution reaction between paracetamol (N-acetyl-p-aminophenol) and benzoyl chloride in pyridine was done based on the previous study in p-aminophenol derivatives molecular modelling, resulting a promising conclusion as a substance with more potent actions as analgesic and anti-inflammation. Identification of the product substance were done by organoleptic and solubility analysis, completed with thin layer chromatography (TLC), melting point test, structure elutidation by infrared spectrophotometry, gas chromatography and mass-spectrometry (GC-MS), and yield calculation. The study shows that a new substance was formed through the reaction process with average yield of 26,152% w/w which has the characteristics of ester group substances as the expected product.
SINTESIS SENYAWA 4-ASETAMIDOFENIL BENZOAT DARI PARASETAMOL DAN BENZOIL KLORIDA BERDASARKAN REAKSI
SUBSTITUSI NUKLEOFILIK ASIL
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Farmasi
Oleh:
Dolorosa Lintang Suminar
NIM : 098114047
FAKULTAS FARMASI
HALAMAN PERSEMBAHAN
Life is not something that flow like a river,
it is not something that we should follow and let go effortlessly.
Life is the stage for us actors to challenge ourselves,
it is where we have to decide, be brave, take responsibility, be committed, be
passionate, and live fully.
Dream on! For no dream is a crime. Live on! For our souls are our own.
Be who we are and who we always want to be.. And be ourselves!
I B U H E B A T, Enny Anggraini, Ph.D.; yang selalu menjadi cita-citaku, yang hampir
5 tahun terpisah benua, namun selalu kirimkan cinta.
B A P A K, Dwi Koratno, M.A.; yang selalu mengalah, yang terlalu sabar menghadapi
kerasnya tuturku, namun setia memperhatikanku.
Belahan jiwaku, mas Heronimus H E R U Adityo, suporter setiaku, generator bagi
semangatku, yang menemaniku malam hingga pagi via telpon, meskipun
dipisahkan jarak tapi kaulah yang memberiku kekuatan untuk berjuang.
Eyang-eyangku tercinta, keluarga yang terlalu besar, dan sahabat-sahabatku.
PRAKATA
Puji syukur ke hadirat Tuhan Yang Maha Esa atas berkat dan rahmat-Nya
yang melimpah sehingga penulis dapat menyelesaikan skripsi yang berjudul
“Sintesis Senyawa 4-Asetamidofenil Benzoat dari Parasetamol dan Benzoil
Klorida berdasarkan Reaksi Substitusi Nukleofilik Asil” dengan baik. Skripsi ini
disusun untuk memenuhi salah satu syarat untuk memperoleh gelar Sarjana Strata
Satu (S1) Program Studi Farmasi (S.Farm.) Fakultas Farmasi Universitas Sanata
Dharma Yogyakarta.
Penulis mengucapkan terima kasih atas segala bantuan yang diberikan
oleh berbagai pihak, yakni:
1. Aris Widayati, M.Si., Ph.D., Apt., selaku Dekan Fakultas Farmasi, Universitas
Sanata Dharma Yogyakarta.
2. Dr. Sri Hartati Yuliani, M.Si., Apt., selaku Ketua Program Studi Fakultas
Farmasi, Universitas Sanata Dharma Yogyakarta.
3. Jeffry Julianus, M.Si., selaku dosen pembimbing yang memberikan bimbingan
serta arahan dengan penuh kesabaran, sekaligus sebagai dosen penguji atas
kritik dan saran yang diberikan kepada penulis.
4. Enade Perdana Istyastono, Ph.D., Apt., selaku dosen penguji atas saran, kritik,
dan solusi yang diberikan kepada penulis.
5. F. Dika Octa Riswanto, M.Sc., selaku dosen penguji atas saran, kritik, dan
6. Pak Parlan, mas Kunto, mas Bimo, serta segenap laboran Fakultas Farmasi
yang berkenan membantu selama proses di laboratorium, dan menjadi partner
bertukar pikiran yang luar biasa.
7. Ibu, Bapak, mas Heru dan keluarga, eyang A’uk di surga, eyang Uti, bulik Ida,
budhe Ninik, Ian, Nanto, eyang Benny (alm.), tante Dien, om Norman,
keluarga besar Kusumadi, keluarga besar Bhe Yu Hie, keluarga besar Ratidjo,
serta seluruh keluarga besar penulis atas dukungan, doa, kasih sayang, dan
reminder dalam menyelesaikan tulisan ini.
8. Para sahabat: Maria Indah, Agnes Wilis, Luthfi, Sani, Neo, Aldo, Majid, atas
dukungan, semangat, kesempatan untuk bertukar pikiran, dan persahabatan
luar biasa yang diberikan kepada penulis.
9. Teman-teman seperjuangan: Dino, Ita, Gita, Meta, Ria, Ella, Albet, Calista,
teman-teman FST 2010, dan teman-teman angkatan 2009, atas bantuan,
dukungan, serta persahabatan yang diberikan.
10. Semua pihak yang tidak dapat disebutkan satu per-satu, yang berperan dalam
memberikan dukungan serta bantuan selama penyusunan skripsi ini.
Atas segala kekurangan dalam proses penelitian maupun penulisan yang
dilakukan oleh penulis, maka penulis mengharapkan kritik serta saran yang
membangun demi memperbaiki kesalahan-kesalahan tersebut. Semoga skripsi ini
dapat bermanfaat bagi pembaca dan mendukung pengembangan ilmu
DAFTAR ISI
Halaman
HALAMAN JUDUL ………i
HALAMAN PERSETUJUAN PEMBIMBING ………..ii
HALAMAN PENGESAHAN……… iii
HALAMAN PERSEMBAHAN ……….iv
HALAMAN PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH ………...v
PRAKATA………..vi
PERNYATAAN KEASLIAN KARYA ………..viii
DAFTAR ISI ………..ix
DAFTAR TABEL………..xii
DAFTAR GAMBAR ………xiii
DAFTAR LAMPIRAN ………..xv
ABSTRAK ……….………..xvi
ABSTRACT………...xvii
BAB I. PENDAHULUAN …..……….1
A. Latar Belakang ………...………1
1. Rumusan Masalah .………...3
2. Keaslian Penelitian ………...3
3. Manfaat penelitian………...4
A. Parasetamol ………5
B. Benzoil Klorida ………..6
C. Piridina ………...9
D. Reaksi Substitusi Nukleofilik Asil ………...10
E. Rekristalisasi ………12
F. Uji Kelarutan ………....12
G. Uji Titik Lebur ……….15
H. Identifikasi dan Uji Kemurnian dengan Kromatografi Lapis Tipis (KLT) …..17
I. Spektrofotometri Inframerah/Infrared (IR)…..………19
J. Kromatografi Gas ………22
K. Spektrometri Massa ……….27
L. Landasan Teori ……….31
M. Hipotesis………...33
BAB III. METODE PENELITIAN ………...34
A. Jenis Penelitian ……….34
B. Definisi Operasional Penelitian ………...34
C. Bahan Penelitian………...35
D. Alat Penelitian ……….35
E. Tata Cara Penelitian ……….35
1. Sintesis 4-Asetamidofenil Benzoat ………....35
2. Pemeriksaan Pendahuluan Senyawa Hasil Sintesis ………...36
3. Elusidasi Struktur Senyawa Hasil Sintesis ………37
1. Perhitungan Rendemen ………..38
2. Uji Pendahuluan ……….38
3. Pemeriksaan dan Uji Kemurnian Senyawa Hasil Sintesis ……….38
4. Elusidasi Struktur ………..38
BAB IV. PEMBAHASAN……….39
A. Sintesis 4-Asetamidofenil Benzoat ………..39
B. Analisis Pendahuluan ………...44
1. Pemeriksaan Organoleptis ……….44
2. Pemeriksaan Kelarutan………...44
3. Pemeriksaan Titik Lebur ………49
4. Kromatografi Lapis Tipis (KLT) ………...50
C. Elusidasi Struktur Senyawa Hasil Sintesis ………..52
1. Elusidasi Struktur dengan Spektrofotometri Inframerah (IR) …………...52
2. Elusidasi Struktur dengan Kromatografi Gas-Spektrometri Massa (GC-MS) ………55
BAB V. KESIMPULAN DAN SARAN ………...61
A. Kesimpulan ………...………...61
B. Saran ………61
DAFTAR PUSTAKA ………....62
LAMPIRAN ………...65
DAFTAR TABEL
Tabel I. Perbandingan sifat fisik senyawa produk sintesis dan starting
material ……….44
Tabel II. Perbandingan tingkat kelarutan produk sintesis dengan
parasetamol ………...45
Tabel III. Uji titik lebur terhadap produk sintesis dan starting material ……..50
Tabel IV. Perbandingan nilai Rf dan hRf produk sintesis dengan
parasetamol ………...51
DAFTAR GAMBAR
Gambar 1. Struktur parasetamol ………...…..5
Gambar 2. Struktur benzoil klorida ………..6
Gambar 3. Mekanisme reaksi antara asam klorida dengan alkohol ………….8
Gambar4. Struktur piridina ………...9
Gambar5. Reaksi substitusi nukleofilik asil ………...11
Gambar6. Interaksi dipol-dipol dan dipol-terinduksi dipol ………...23
Gambar7. Pemisahan 10 senyawa dalam (a) dimetilsiloksan (non-polar) dan
(b) etilen glikol (polar) ……….26
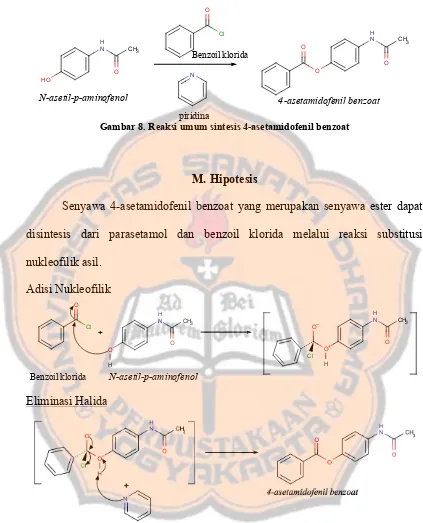
Gambar8. Reaksi umum sintesis 4-asetamidofenil benzoat ………...33
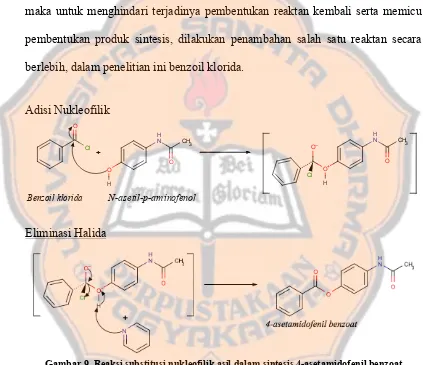
Gambar9. Reaksi substitusi nukleofilik asil dalam sintesis 4-asetamidofenil
benzoat ………...40
Gambar10. Kelarutan (a) parasetamol dan (b) 4-asetamidofenil benzoat dalam
NaOH 5% ………..………...46
Gambar11. Sisi donor dan akseptor proton pada parasetamol dan
4-asetamidofenil benzoat ……….47
Gambar12. Hasil elusi KLT terhadap parasetamol (PCT), produk orientasi (a),
dan produk sintesis replikasi I (b), II (c), dan III (d); fase
diam=silika gel GF254, fase gerak=aseton:etil asetat (2:3), deteksi
pada UV 254 nm ………...51
Gambar15. Kromatogram senyawa hasil sintesis………55
Gambar16. Spektra massa EI senyawa produk pada waktu retensi 33,683
menit ………...56
Gambar17. Spektra massa EI senyawa produk pada waktu retensi 34,183
menit ……….56
Gambar18. Spektra massa EI senyawa produk pada waktu retensi 34,942
menit ……….56
Gambar19. Usulan mekanisme fragmentasi ion molekul 4-asetamidofenil
benzoat ………...…...58
Gambar20. Spektra massa EI senyawa produk pada waktu retensi 45,392
menit ……….59
Gambar21. Spektra massa EI senyawa produk pada waktu retensi 47,092
DAFTAR LAMPIRAN
Lampiran 1. Data penimbangan starting material dan perhitungan rendemen
teoretis ……….65
Lampiran 2. Data penimbangan dan perhitungan rendemen ………...66
Lampiran 3. Spektra inframerah produk sintesis ……….67
Lampiran 4. Kondisi alat spektrometri massa ……….68
Lampiran 5. Kromatogram spektrometri massa produk sintesis ……….69
ABSTRAK
Senyawa 4-asetamidofenil benzoat merupakan senyawa derivat p-aminofenol yang diduga mempunyai aksi analgetika dan anti-inflamasi, yang bekerja dengan menghambat enzim siklooksigenase-2 (COX-2). Penghambatan pada COX-2 berarti terjadi penghambatan pada interaksi enzim tersebut dengan asam arakhidonat yang memicu pembentukan prostaglandin sebagai penghasil respon inflamasi. Sintesis senyawa 4-asetamidofenil benzoat melalui reaksi substitusi nukleofilik asil (SNA) antara parasetamol (N-asetil-p-aminofenol) dan benzoil klorida dalam piridina dilakukan berdasarkan pemodelan molekul derivat p-aminofenol pada penelitian sebelumnya, yang memperoleh hasil yang menjanjikan sebagai senyawa dengan aksi yang lebih poten sebagai analgetika dan anti-inflamasi. Identifikasi senyawa hasil sintesis dilakukan melalui analisis terhadap organoleptis dan kelarutan, dilengkapi dengan uji kromatografi lapis tipis (KLT), uji titik lebur, elusidasi struktur malalui spektrofotometri inframerah, kromatografi gas, dan spektrometri massa (GC-MS), serta perhitungan rendemen. Hasil penelitian menunjukkan bahwa terjadi reaksi yang membentuk senyawa baru dengan rendemen rata-rata 26,152% b/b yang memiliki karakteristik golongan ester sesuai dengan senyawa tujuan.
ABSTRACT
4-acetamidophenyl benzoate is a p-aminophenol derivative which is believed to have actions as analgesic and anti-inflammation, that blocks cyclooxygenase-2 (COX-2) enzyme in its mechanism. Blocking in COX-2 causes the inhibition of enzyme interaction with arachidonic acid which originally produces prostaglandine, resulting in inflammation response. Synthesis of 4-acetamidophenyl benzoate through nucleophilic acyl substitution reaction between paracetamol (N-acetyl-p-aminophenol) and benzoyl chloride in pyridine was done based on the previous study in p-aminophenol derivatives molecular modelling, resulting a promising conclusion as a substance with more potent actions as analgesic and anti-inflammation. Identification of the product substance were done by organoleptic and solubility analysis, completed with thin layer chromatography (TLC), melting point test, structure elutidation by infrared spectrophotometry, gas chromatography and mass-spectrometry (GC-MS), and yield calculation. The study shows that a new substance was formed through the reaction process with average yield of 26,152% w/w which has the characteristics of ester group substances as the expected product.
BAB I
PENDAHULUAN
A. Latar Belakang
Inflamasi adalah suatu respon sel hidup terhadap luka yang terjadi akibat
interaksi antara asam arakhidonat dan enzim siklooksigenase 2 (COX-2) yang
memicu pembentukan prostaglandin (Vane, 1996). Untuk mencegah atau
menghambat terjadinya inflamasi, maka interaksi antara asam arakhidonat dan
COX-2 harus dihambat.
Analgesik merupakan suatu agen atau senyawa yang memiliki
kemampuan untuk mengurangi rasa sakit/ nyeri dengan cara meningkatkan
ambang rasa sakit, tanpa mengganggu kesadaran maupun mempengaruhi agen
sensori lainnya (Hanson, 2000). Salah satu analgesik yang populer dan paling
sering diresepkan adalah N-asetil-p-aminofenol atau asetaminofen (parasetamol),
yang telah digunakan hampir selama 100 tahun akan tetapi belum diketahui
dengan jelas dalam hal mekanisme aksinya.
Mekanisme aksi asetaminofen/parasetamol sebagai analgesik dan
anti-inflamasi seperti mekanisme obat-obat antianti-inflamasi nonsteroid (NSAIDs). Akan
tetapi, seringkali dinyatakan bahwa parasetamol bekerja secara khusus, terpusat,
dan terbaik sebagai inhibitor lemah sintesis prostaglandin (PG) oleh enzim
siklooksigenase (COX)-1 dan COX-2. Menurut Hinz et al. (2008), penggunaan
terhadap COX-2 manusia, sementara itu hanya ditemukan inhibisi tingkat moderat
terhadap COX-1.
Penghambatan COX-1 oleh parasetamol nampak pada lemahnya aktivitas
antiplatelet serta keamanan bagi gastrointestinal yang baik. Dalam penelitian yang
dilakukan Hinz et al. (2008), fungsi platelet terhambat dengan pemberian dosis
tinggi parasetamol secara parenteral; pola yang serupa terjadi pada pengaruhnya
terhadap gastrointestinal. Dosis parasetamol yang lebih tinggi menimbulkan
peningkatan kemungkinan terjadinya gangguan gastrointestinal, seperti dispepsia,
dibandingkan dengan dalam dosis rendah. Suatu studi epidemiologi menyatakan
bahwa parasetamol yang diberikan dengan dosis harian 2 hingga 2,6 gram mampu
meningkatkan risiko efek samping yang severe/berat pada gastrointestinal,
termasuk pendarahan atau perforasi. Meskipun parasetamol masih diakui sebagai
obat yang bebas dari toksisitas gastrointestinal, sebaiknya tetap dilakukan uji coba
terhadap pasien yang menerima pengobatan dengan parasetamol dalam jangka
panjang.
Senyawa 4-asetamidofenil benzoat adalah suatu senyawa turunan
p-aminofenol yang diduga mempunyai aksi analgetika dan anti-inflamasi.
Berdasarkan pada penelitian Pudjono et al., 2011, pemodelan molekul
4-asetamidofenil benzoat berpotensi sebagai analgesik anti-inflamasi dan
merupakan salah satu senyawa yang disarankan untuk disintesis. Perhitungan
statistik menggunakan persamaan QSAR, dengan deskriptor-deskriptor yang telah
disebut sebagai senyawa nomer 10 dalam jurnal tersebut, deskriptor-deskriptor
yang diperhitungkan adalah: muatan substituen R No. 3 (qR3)= 0,035078
Coulomb; momen dwi kutub (µ)= 4,243 Debye; koefisien partisi n-oktanol–air
(Log P)= 2,08; bobot molekul (BM)= 255,273 a.m.u; luas permukaan van der
Waals (Avdw)= 274,765 Å2.
Senyawa 4-asetamidofenil benzoat merupakan senyawa golongan ester,
yang ditandai dengan adanya karbonil yang mengikat gugus –OR. Reaksi yang
secara umum digunakan sebagai dasar sintesis senyawa ester dari benzoil klorida
adalah reaksi substitusi nukleofilik asil, yaitu dengan mereaksikan benzoil klorida
dengan alkohol dalam suasana basa. Jika nukleofil mengikat karbonil, maka klor
dan gugus alkoksi berfungsi sebagai gugus pergi (leaving group). Pengikatan klor
pada karbonil akan tergantikan oleh nukleofil, yang memicu terjadinya reaksi
substitusi; sehingga pelepasan gugus pergi klorida memudahkan pembentukan
ikatan π baru (Sastrohamidjojo, 2009).
1. Rumusan masalah
Apakah 4-asetamidofenil benzoat dapat disintesis dari
N-asetil-p-aminofenol dan benzoil klorida?
2. Keaslian penelitian
Penelitian mengenai sintesis senyawa berdasarkan reaksi substitusi
nukleofilik asil telah dilakukan oleh Ramdani (2011), dalam sintesis benzoil
eugenol dari eugenol dan benzoil klorida. Ratnawati (2007) telah menggunakan
reaksi esterifikasi dalam penelitian tentang sintesis turunan benzofenon. Sejauh
N-asetil-p-aminofenol dan benzoil klorida berdasarkan reaksi substitusi nukleofilik
asil belum pernah dilakukan.
3. Manfaat penelitian
a. Manfaat teoretis. Penelitian ini diharapkan mampu memperkaya pengetahuan
khususnya di bidang sintesis organik senyawa 4-asetamidofenil benzoat dari
N-asetil-p-aminofenol dan benzoil klorida berdasarkan reaksi substitusi
nukleofilik asil.
b. Manfaat metodologis. Penelitian ini diharapkan dapat memberikan manfaat
dalam pengembangan metode sintesis senyawa 4-asetamidofenil benzoat
turunan p-aminofenol melalui reaksi substitusi nukleofilik asil.
c. Manfaat praktis. Penelitian ini diharapkan dapat menghasilkan senyawa
4-asetamidofenil benzoat yang berpotensi dalam penelitian aktivitas
farmakologis sebagai analgesik anti-inflamasi yang lebih poten daripada
senyawa turunan p-aminofenol yang telah tersedia di pasaran.
B. Tujuan Penelitian
Penelitian ini bertujuan untuk:
Melakukan sintesis 4-asetamidofenil benzoat dari N-asetil-p-aminofenol
BAB II
TINJAUAN PUSTAKA
A. Parasetamol
Parasetamol atau dikenal dengan N-asetil-p-aminofenol merupakan suatu
serbuk granular putih yang mudah mengalir serta tidak berbau dan berasa pahit.
Mempunyai bobot molekul 151,16 g/mol, serta titik lebur 169-172oC.
kelarutaannya adalah larut dalam 70 bagian air, 7 bagian etanol p (95%), 13
bagian aseton p, dalam 40 bagian gliserol p dan dalam 9 bagian propilenglikol p;
serta larut dalam larutan alkali hidroksida (Dirjen POM, 1979).
Gambar 1. Struktur Parasetamol
Parasetamol merupakan salah satu pilihan umum yang digunakan secara
luas dalam penanganan nyeri serta demam. Akan tetapi, ditemukan bahwa efek
analgesik parasetamol disebabkan karena adanya aktivasi secara tidak langsung
dari reseptor kanabinoid CB1. Pada otak dan spinal cord, parasetamol, diikuti
dengan deasetilasi menjadi amina primernya (p-aminofenol), terkonjugasi dengan
asam arakhidonat untuk membentuk N-arakhi-donoilfenolamin, suatu senyawa
yang telah diketahui sebagai kanabinoid endogen. Enzim yang terlibat di
dalamnya adalah amida asam lemak hidrolase. N-arakhi-donoilfenolamin
merupakan agonis pada reseptor reseptor vaniloid subtipe 1 (TRPV1) dan
inhibitor uptake/penyerapan anandamida seluler, yang mengakibatkan terjadinya
HO
H
N CH
3
peningkatan jumlah kanabinoid endogen; terlebih lagi, menghambat
siklooksigenase dalam otak, akan tetapi dalam konsentrasi yang tidak sebesar
dosis analgesik yang diperlukan dalam penggunaan parasetamol (Bertolini et al.,
2006).
Profil farmakologi parasetamol sangat mirip dengan inhibitor selektif
COX-2 (coxibs). Sebagai coxib, parasetamol diberikan secara per-oral dalam
dosis tunggal yang disarankan sehingga tidak menimbulkan efek toksik dalam
jalur gastrointestinal, tidak menghalangi fungsi platelet, dan memiliki
kemungkinan kecil menyebabkan terjadinya bronkokonstriksi dalam asma
aspirin-sensitif (Hinz et al., 2008).
B. Benzoil Klorida
Merupakan suatu cairan transparan atau tidak berwarna yang mudah
terbakar, memiliki bau menusuk, serta uap yang juga iritatif terhadap mukosa.
Benzoil klorida memiliki bobot molekul sebesar 140,57 g/mol serta titik didih
197,2oC. Senyawa ini mengandung tidak kurang dari 97% C7H5ClO.
Kelarutannya praktis tidak larut dalam air, namun larut dalam kebanyakan pelarut
organik; selain itu larut secara perlahan dan hampir sempurna dalam larutan
NaOH p (Dirjen POM, 1979).
Gambar 2. Struktur benzoil klorida
Benzoil klorida termasuk ke dalam derivat asam karboksilat, berupa
suatu asam halida atau asil halida, yang merupakan derivat teraktivasi dalam
sintesis senyawa asil lainnya seperti ester, amida, serta asilbenzena. Adapun asil
klorida didapatkan melalui reaksi antara asam karboksilat dengan tionil klorida
(SOCl2) atau oksalil klorida [(COCl)2], karena menghasilkan by-products berupa
gas yang tidak mengkontaminasi produk sintesis (Wade, 2013).
Ion-ion halida merupakan gugus pergi yang sangat baik untuk reaksi
substitusi nukleofilik asil; karena itulah asil halida merupakan intermediet yang
berguna dalam membuat derivat asam. Asil klorida dibuat dengan mudah dan
banyak digunakan sebagai bentuk aktif suatu asam karboksilat. Oksigen karbonil
dan atom klorin sama-sama menarik densitas elektron dari atom karbon asil,
membuatnya menjadi elektrofil yang kuat (Wade, 2013).
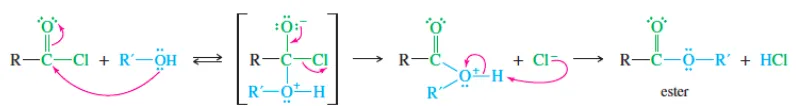
Asam klorida bereaksi dengan alkohol untuk menghasilkan suatu ester
melalui substitusi nukleofilik asil dengan mekanisme adisi-eliminasi.
Penyerangan gugus karbonil yang elektrofilik oleh alkohol memberikan
intermediet tatrahedral, kemudian hilangnya klorida dan terjadinya deprotonasi
memberikan produk ester. Reaksi tersebut merupakan reaksi yang efisien untuk
menghasilkan ester dari asam karboksilat. Piridina atau basa lainnya seringkali
ditambahkan untuk menetralkan HCl yang terbentuk, karena apabila dibiarkan,
alkohol—terutama alkohol tersier—dapat terdehidrasi di bawa kondisi asam kuat
Gambar 3. Mekanisme reaksi antara asam klorida dengan alkohol(Wade, 2013)
Benzoil klorida yang termasuk asam klorida merupakan derivat asam
karboksilat yang paling reaktif dibandingkan dengan derivat-derivat yang lainnya
(asam klorida > anhidrida > ester > amida > karboksilat), berbanding terbalik
terhadap kebasaan gugus perginya (Cl < OCOR < OR < NH2 < O). Basa-basa
kuat bukanlah gugus pergi yang baik, dan reaktivitas derivatnya menurun seiring
dengan peningkatan kebasaan gugus perginya (Wade, 2013).
Reaktivitas derivat asam karboksilat juga dipengaruhi oleh stabilisasi
resonansinya. Resonansi yang terjadi pada asam klorida sangat kecil, sehingga
membuatnya lebih reaktif dibandingkan dengan anhidrida, ester dan amida.
Pasalnya pada anhidrida, stabilisasi terjadi antara dua gugus karbonil, sehingga
masing-masing gugus karbonil terstabilkan lebih rendah daripada karbonil pada
ester. Sementara itu suatu senyawa ester beresonansi dengan lemah namun terjadi
hanya pada satu gugus karbonil. Resonansi yang cukup kuat dibandingkan dengan
derivat-derivat yang disebutkan sebelumnya terjadi pada amida. Meskipun
demikian, pada derivat-derivat tersebut resonansi akan terhenti ketika terjadi
penyerangan atom C karbonil oleh nukleofil. Sehingga, asam klorida yang kurang
stabil di antara yang lainnya merupakan senyawa paling reaktif dan mudah
mengadakan reaksi dengan nukleofil (Wade, 2013).
menggunakan piridin sebagai katalis. Katalisis piridin melibatkan pembentukan
ion asilpiridinium, yang kemudian bereaksi dengan alkohol. Piridin merupakan
nukleofil yang lebih baik daripada alkohol netral, tetapi ion asilpiridinium
bereaksi lebih cepat dengan alkohol daripada dengan asil klorida. Efek katalisis
lebih kuat dihasilkan ketika 4-dimetilaminopiridin (DMAP) digunakan sebagai
katalis nukleofilik. Gugus dimetilamino berlaku sebagai substituen donor
elektron, meningkatkan nukleofilisitas dan kebasaan nitrogen piridin (Carey and
Richard, 2001).
C. Piridina
Piridina (C5H5N) merupakan suatu cairan jernih tidak berwarna, memiliki
bau tidak sedap yang khas, serta higroskopis. Kelarutannya dapat campur dengan
air, etanol (95%) p, serta dengan kloroform p. Memiliki jarak didih tidak kurang
dari 95% tersuling pada suhu 114o dan 117oC, bobot per mL sebesar 0,981 g
hingga 0,983 g (Dirjen POM, 1979).
Gambar 4. Struktur piridina
Senyawa piridina merupakan suatu senyawa nukleofilik pada atom
nitrogennya, dikarenakan pasangan elektron bebas pada atom tersebut tidak dapat
terdelokalisasi di sekitar cincinnya. Pasangan elektron bebas itu terdapat pada
orbital ortogonal sp2 terhadap orbital p dalam cincin senyawa yang
mengakibatkan tidak adanya interaksi antara orbital-orbital ortogonal. Orbital p
dalam sistem aromatis piridina sebenarnya serupa dengan benzena, akan tetapi
peningkatan elektronegativitas atom nitrogen berperan dalam menurunkan energi
seluruh orbital. Orbital-orbital berenergi rendah berarti nukleofil tersebut kurang
reaktif, namun LUMO (lowest unoccupied molecular orbital/orbital molekul
kosong berenergi rendah) dengan energi lebih rendah berarti elektrofil yang lebih
reaktif. Maka dari itu, senyawa piridina kurang reaktif daripada benzena dalam
reaksi substitusi elektrofilik aromatik, tetapi sebaliknya dalam reaksi substitusi
nukleofilik lebih mudah bagi piridina dibandingkan dengan benzena (Szolcsànyi,
2016).
D. Reaksi Substitusi Nukleofilik Asil
Substitusi nukleofilik asil disebut juga reaksi transfer asil dikarenakan
reaksi tersebut melepaskan gugus asil dari gugus perginya menuju nukleofil yang
menyerang. Mekanisme reaksi substitusi nukleofilik asil bermula dari adisi
nukleofil pada atom C gugus karbonil (C=O) yang mendorong terbentuknya
intermediet tetrahedral. Kemudian terjadi stabilisasi pasangan elektron bebas pada
atom oksigen kembali membentuk ikatan ganda karbonil dan melepaskan gugus
pergi sehingga terbentuklah produk dan satu atom gugus pergi (Wade, 2013).
Adisi nukleofil pada ikatan C=O polar merupakan kunci dari reaksi gugus
karbonil. Saat suatu nukleofil ditambahkan ke dalam suatu derivat asam
karboksilat, akan mengalami pembentukan intermediet tetrahedral; karenanya
Asam klorida atau halida dapat bereaksi secara cepat pada suhu ruangan
dengan senyawa alkohol baik primer, sekunder, maupun tersier; dan juga dengan
fenol. Produk yang dihasilkan berupa ester, suatu derivat asam karboksilat, di
mana gugus hidroksi (–OH) pada asam karboksilat telah digantikan oleh –OR atau
–OAr (Johnson, 1999). Konversi asil halida menjadi ester disebut juga dengan
istilah alkoholisis yang berlangsung dengan adanya piridina tau NaOH untuk
bereaksi dengan asam klorida (HCl) yang terbentuk dari reaksi tersebut.
Perlu diperhatikan bahwa asam klorida selain bereaksi cepat dengan
alkohol juga merupakan reaksi yang eksotermis sehingga perlu dipastikan bahwa
reaksi berlangsung dalam suhu rendah untuk menghindari dehidrasi alkohol,
dikarenakan asam klorida merupakan agen dehidrasi yang kuat. Maka dari itu
piridin (atau basa lainnya) seringkali ditambahkan dalam reaksi untuk
menetralisasi hasil reaksi samping (by-product) berupa HCl (Wade, 2013).
Suatu kelebihan dari reaksi ini adalah pembentukan ester dari alkohol
enansiomer di mana gugus –OH berada pada bagian tengah molekul tidak
menimbulkan rasemisasi dikarenakan berdasarkan mekanisme reaksinya, ikatan
[image:30.595.86.514.223.649.2]antara karbon dan oksigen tidak pernah terputus selama reaksi berlangsung:
E. Rekristalisasi
Presipitasi yang diatur sedemikian rupa dengan cara memanipulasi
kelarutan menjadi teknik yang sering dilakukan dalam pemurnian produk hasil
reaksi dalam sintesis kimia. Reaksi samping yang tidak diharapkan dapat
menghasilkan sejumlah pengotor dalam produk; pengotor yang lainnya
didapatkan dari starting material atau senyawa lain yang digunakan misalnya
sebagai katalis reaksi.
Rekristalisasi yang merupakan salah satu metode paling ampuh dalam
pemurnian senyawa, menerapkan teknik seperti yang telah disebutkan, yakni
bergantung pada perbedaan kelarutan antara senyawa tujuan dengan
pengotor-pengotor lainnya. Produk hasil sintesis tadi dilarutkan dan diendapkan/
dipresipitasi, bila diperlukan berulang kali, dengan memperhatikan faktor-faktor
yang mempengaruhi kelarutannya, serta dilakukan kontrol terhadap faktor-faktor
tersebut. Namun bagaimanapun juga, dalam melakukan manipulasi terhadap
kelarutan diperlukan pemahaman terhadap kesetimbangan yang terdapat antara
senyawa yang tidak larut dengan larutannya (Oxtoby et al., 2008).
F. Uji Kelarutan
Gaya inter-molekuler berperan dalam menentukan sifat kelarutan senyawa
organik, atau disebut dengan istilah like dissolves like. Senyawa-senyawa polar
akan larut dalam solven polar, sebaliknya senyawa-senyawa non-polar akan larut
1. Solut polar dalam solven polar,
Kelarutan NaCl dalam air contohnya, memerlukan energi yang besar untuk
memisahkan ion-ion berlawanan muatan dalam NaCl. Solven polar seperti
air mampu mensolvatasinya, maka dengan solven air peristiwa ini disebut
hidrasi. Larutnya garam terjadi karena molekul-molekul air menyelubungi
masing ion dengan ujung momen dipol yang sesuai bagi
masing-masing muatannya. Atom oksigen dalam molekul air akan menyelubungi
ion natrium yang bermuatan positif, sementara atom hidrogennya
menyelubungi ion klorida yang bermuatan negatif.
2. Solut polar dengan solven non-polar,
Solut NaCl dalam solven non-polar seperti terpentin atau gasoline tidak
menyebabkan larutnya NaCl. Molekul non-polar solven tidak
mensolvatasi ion-ion secara kuat, dan tidak mampu mengatasi energi
lattice dari kristal garam. Ini merupakan peristiwa di mana interaksi
ion-ion dalam solut lebih besar daripada interaksinya dengan solven.
3. Solut non-polar dengan solven non-polar,
Parafin larut dalam gasoline, keduanya merupakan campuran hidrokarbon
non-polar. Molekul-molekul parafin sebagai senyawa non-polar menarik
satu sama lain secara lemah, dan interaksi van der Waals tersebut sangat
mudah diputuskan dengan interaksi van der Waals solven.
4. Solut non-polar dengan solven polar,
Parafin tidak larut dalam solven air yang polar, dikarenakan
hanya memerlukan sedikit energi untuk memisahkannya.
Permasalahannya adalah molekul air berinteraksi dengan kuat satu sama
lain karena adanya interaksi hidrogen. Saat solut parafin dilarutkan dalam
air, molekul-molekul air di sekitarnya akan membentuk rongga.
Molekul-molekul air pada tepi rongga memiliki lebih sedikit atom untuk mengalami
interaksi hidrogen, sehingga menghasilkan struktur yang lebih mampat
dan kaku di sekitar rongga tersebut. Struktur seperti ini menghasilkan
penurunan entropi sistem: ∆� = ∆�−�∆�, dan ∆� seringkali bernilai
kecil. Karenanya nilai negatif ∆� membuat ∆� positif (tidak diinginkan),
sehingga senyawa non-polar tidak dapat larut (Wade, 2013).
Suatu senyawa organik yang belum diketahui dapat ditentukan strukturnya
melalui pengujian kelarutan dalam air, larutan NaOH 5%, larutan NaHCO3 5%,
larutan HCl 5%, dan H2SO4 pekat. Keberadaan gugus fungsional menjadi hal
pertama yang diuji, misalnya senyawa hidrokarbon tidak larut dalam air, sehingga
bila sampel senyawa sebagian larut dalam air, menunjukkan bahwa terdapat gugus
fungsi bersifat polar dalam senyawa tersebut. Kedua, kelarutan dalam solven
tertentu seringkali memberikan informasi spesifik mengenai gugus fungsi,
misalnya asam benzoat yang tidak larut dalam solven polar (air), tetapi diubah
oleh larutan NaOH 5% ke dalam bentuk garam dan dapat larut dalam air;
sehingga dapat disimpulkan bahwa adanya indikasi keberadaan gugus fungsi
bersifat asam. Dugaan tentang ukuran molekul dan komposisinya terkadang
larut air, sementara lebih dari itu berarti tidak larut air. Dalam hal kelarutannya
dalam air, suatu senyawa dikatakan larut dalam air apabila memenuhi 3,3 g/100
mL solven (AJM, 2010).
G. Uji Titik Lebur
Suhu di mana terjadi peleburan suatu zat padat menjadi zat cair disebut
dengan titik lebur. Karena perubahan wujud zat tersebut memerlukan pemutusan
gaya inter-molekuler yang mengikat zat padat, maka suhu peleburan menjadi
bergantung pada struktur molekul bersangkutan; hal ini merupakan hubungan
nyata antara struktur dengan sifat senyawa. Maka dari itu, senyawa satu memiliki
titik lebur yang berbeda dengan senyawa lainnya (Calgary, 2010).
Suatu senyawa organik kristalin, non-ionik, dan murni, biasanya
mempunyai titik lebur tertentu yang tajam (pada umumnya antara 0,5-1,0o C).
Adanya campuran senyawa pengotor dapat menyebabkan penurunan titik lebur
serta peningkatan rentang titik leburnya. Akibatnya, titik lebur suatu senyawa
menjadi kriteria kemurnian selain digunakan dalam identifikasi (Calgalry, 2010).
Observasi visual dilakukan dalam uji titik lebur karena dalam prosesnya
akan nampak perubahan fisik serbuk sampel dalam pipa kapiler, baik secara fisika
maupun kimiawi. Terdapat beberapa hal yang sebaiknya diperhatikan dalam
pengujian ini:
1. Tanda-tanda perubahan sampel, meliputi: dehidrasi, perubahan fase
kristalisasi, permulaan dekomposisi atau perubahan warna (misalnya
kapiler, serta dimulainya peleburan kristal tanpa diikuti kemunculan fase cair
dalam fase kohesif (sintering point).
2. Onset point, atau permulaan peleburan, di mana fase cair mulai nampak
dengan jelas sebagai fase yang terpisah dari kristal; berbeda dengan sintering
point yang hanya merupakan beberapa titik pada permukaan kristal yang
mulai melebur.
3. Meniscus point, yakni nampaknya meniskus fase cair dalam proses peleburan;
terdapat fase padat pada dasarnya serta fase cair yang nampak jelas dengan
meniskusnya.
4. Clear/liquefaction point, tahap saat fase dalam pipa kapiler telah seluruhnya
berubah menjadi fase cair tanpa keberadaan fase padat sama sekali, atau
kristal terakhir yang melebur.
5. Tanda-tanda akhir peleburan yang meliputi: sublimasi (munculnya kristal
pada dasar pipa kapiler) serta dekomposisi (munculnya gelembung atau
perubahan warna selama dan setelah peleburan) (Stanford, 2010).
Titik lebur suatu padatan merupakan temperatur saat cairan dan padatan
berada pada titik ekuilibrium pada tekanan 1 atmosfer. Berlawanan dengan
terjadinya perubahan volume karena adanya penguapan cairan, perubahan volume
saat peleburan padatan sangatlah kecil. Hal ini membuat titik lebur padatan tidak
H. Identifikasi dan Uji Kemurnian dengan Kromatografi Lapis Lipis (KLT)
Kromatografi Lapis Tipis (KLT) merupakan cara pemisahan berdasarkan
pembagian 2 senyawa dalam fase diam yang berupa bidang datar. Campuran yang
akan dipisah berupa larutan, ditotolkan dalam bentuk pita atau bercak. Setelah plat
ditaruh dalam bejana tertutup rapat yang berisi larutan pengembang yang cocok
(fase gerak), pemisahan terjadi selama perambatan kapiler (Stahl, 1985).
Plat atau fase diam yang digunakan dalam KLT merupakan penjerap
berukuran kecil dengan diameter partikel antara 10-30 �m. Semakin kecil ukuran
rata-rata partikel dan semakin sempit kisaran ukurannya, maka kinerja KLT dalam
hal efisiensi serta resolusinya semakin meningkat. Penjerap yang paling sering
digunakan berupa silika dan serbuk selulosa; sementara mekanisme sorpsi yang
utama pada KLT adalah partisi dan adsorbsi. Terdapat fase diam berupa Silika
Gel 60 F254 yang berarti fase diam tersebut berupa silika gel (dari E. Merck) yang
mempunyai ukuran pori 60 A0 (10 A0 = 1 nm), dengan adanya penambahan bahan
yang berfluoresensi seperti seng silikat teraktivasi mangan yang akan mengalami
eksitasi dan berfosforesensi pada panjang gelombang 254 nm. Dengan demikian
berarti terdapat pula fase diam dengan beberapa ukuran pori lain, bahan penambah
lain, maupun panjang gelombang eksitasi dengan nilai berbeda; pemilihannya
tergantung pada kebutuhan analisis senyawa yang bersangkutan (Gandjar dan
Abdul, 2007).
Fase gerak yang bergerak di sepanjang plat fase diam untuk membawa
sampel yang telah ditotolkan dan terjerembab dalam fase diam tersebut merambat
akibat adanya gaya gravitasi dalam pengembangan menurun (descending).
Pemilihan fase gerak KLT dapat dilakukan melalui studi pustaka untuk
menentukan kombinasi yang umum digunakan untuk suatu senyawa tertentu.
Atau dapat juga dengan tabel yang menunjukkan misibilitas atau mampu tidaknya
lebih dari satu macam fase gerak untuk saling campur, dengan dilengkapi angka
polaritas dari literatur. Hal ini dapat dilakukan ketika telah diketahui nilai
polaritas fase gerak yang dibutuhkan. Hal ini dilakukan tidak lain agar pemisahan
dapat terjadi secara optimal (Gandjar dan Abdul, 2007).
Penentuan nilai polaritas serta perbandingan campuran lebih dari satu fase
gerak dapat dilakukan melalui kalkulasi sebagai berikut:
�! = !�!′�!′ ,
dengan �!′ = indeks polaritas solven i
�!′ = fraksi volume solven i (Cazes, 2005).
Adapun pemilihan dan optimalisasi fase gerak menurut (Gandjar dan
Abdul, 2007) dapat dilakukan melalui petunjuk-petunjuk berikut ini:
1. Fase gerak harus mempunyai kemurnian sangat tinggi karena KLT merupakan
teknik yang sensitif.
2. Daya elusi fase gerak harus diatur sehingga nilai Rf terletak antara 0,2-0,8
dengan tujuan memaksimalkan pemisahan.
3. Untuk pemisahan menggunakan fase diam polar seperti silika gel, polaritas
fase gerak akan menentukan kecepatan migrasi solut yang berarti juga
dietil eter ke dalam pelarut non polar seperti metil benzena akan
meningkatkan harga Rf secara signifikan.
4. Analisis solut-solut ionik dan solut-solut polar lebih baik menggunakan
campuran pelarut sebagai fase geraknya, seperti campuran air dan metanol
dengan perbandingan tertentu. Penambahan sedikit asam etanoat atau amonia
masing-masing akan meningkatkan solut-solut bersifat basa dan asam.
Pengamatan bercak pemisahan dalam KLT seringkali dilakukan melalui
cara khusus secara kimia, fisika, maupun biologi, dikarenakan sebagian besar
bercak merupakan bercak tidak berwarna. Cara kimia dilakukan dengan cara
penyemprotan bercak menggunakan pereaksi kimia, sementara itu cara fisika
dilakukan dengan pencacahan radioaktif dan fluoresensi sinar ultraviolet.
Pengamatan plat di bawah lampu ultraviolet dengan emisi panjang gelombang
254 atau 366 untuk menampakkan solut sebagai bercak gelap atau bercak yang
berfluoresensi terang pada dasar yang berfluoresensi seragam (Gandjar dan
Abdul, 2007).
Jarak pengembangan senyawa pada kromatogram biasanya dinyatakan
dengan angka Rf atau hRf. Harga Rf didefinisikan sebagai perbandingan antara
jarak senyawa dari titik awal dan jarak tepi muka pelarut dari awal (Stahl, 1985).
I. Spektrofotometri Inframerah/Infrared (IR)
Radiasi inframerah yang berkisar antara 10.000-100 cm-1 diabsorbsi untuk
kemudian dikonversikan oleh suatu senyawa organik menjadi energi vibrasi
muncul akibat dari energi vibrasi dari suatu senyawa organik selalu diiringi
dengan beberapa perubahan energi rotasi. Adapun besarnya frekuensi atau
panjang gelombang absorbsi bergantung pada massa relatif atom, gaya konstan
ikatan, serta struktur atom yang terlibat atau menyusun suatu senyawa
(Silverstein, 2005).
Vibrasi molekuler terdiri dari dua macam, yakni stretching dan bending.
Vibrasi stretching/ulur merupakan pergerakan ritmis dalam sepanjang ikatan aksis
yang menyebabkan perubahan jarak/panjang antar-atom. Vibrasi bending/tekuk
adalah perubahan pada besar sudut ikatan, antara ikatan-ikatan dengan atom yang
umum atau pergerakan dari sekumpulan atom terhadap sisa suatu molekul tanpa
gerakan atom dalam grup antara satu sama lain; misalnya twisting, rocking, serta
vibrasi torsional. Meskipun demikian, hanya vibrasi yang menghasilkan
perubahan pada momen dipol molekul saja yang dapat terbaca dalam inframerah
(Silverstein, 2005).
Sebuah molekul organik memiliki lebih dari satu derajat kebebasan
sebagai hasil dari derajat kebebasan masing-masing atom yang menyusunnya.
Setiap atom memiliki tiga derajat kebebasan berdasarkan pada koordinat
Cartesian (x, y, z), yakni menentukan posisinya secara relatif terhadap atom-atom
lain dalam molekul tersebut. Sebuah molekul suatu atom berjumlah n memiliki 3n
derajat kebebasan, namun aturan tersebut berlaku berbeda pada molekul
a. Molekul non-linear,
tiga buah derajat kebebasan menunjukkan rotasi dan tiga yang lainnya
menunjukkan translasi, sehingga 3n-6 derajat kebebasan merupakan
derajat kebebasan vibrasi/vibrasi fundamental.
b. Molekul linear,
Memiliki 3n-5 derajat kebebasan vibrasi, dengan hanya dua derajat
kebebasan yang diperlukan untuk menyatakan terjadinya rotasi
(Silverstein, 2005).
Vibrasi fundamental tidak melibatkan perubahan pada pusat gravitasi
molekul. Untuk membedakan keduanya, dapat dibandingkan antara vibrasi
fundamental dari molekul air serta molekul karbon dioksida. Molekul air memiliki
tiga vibrasi dasar, yaitu vibrasi ulur simetris (vs OH, 3652 cm-1), vibrasi ulur
asimetris (vas OH, 3756 cm-1), dan scissoring (�! OH, 1596 cm -1
). Molekul CO2
adalah molekul linear dan terdiri dari tiga buah atom, sehingga membuat molekul
ini memiliki empat vibrasi dasar. Vibrasi ulur simetris bersifat inaktif pada IR
dikarenakan tidak menghasilkan perubahan apapun terhadap momen dipol
molekulnya. Kedua macam vibrasi tekuk pada molekul CO2 adalah setara, serta
merupakan komponen-komponen yang dipisahkan antara gerakan tekuk yang
berpusat pada sudut manapun terhadap aksis antar-inti; memiliki frekuensi yang
sama, atau ganda. Sementara itu untuk gugus-gugus AX2 yang menjadi suatu
bagian dari molekul seperti gugus CH2 suatu molekul hidrokarbon tidak dapat
diberlakukan aturan 3n-6. Hal tersebut dikarenakan gugus CH2 hanya sebagai satu
J. Kromatografi Gas
Kromatografi gas merupakan teknik pemisahan solut-solut volatil yang
stabil terhadap suhu tinggi, bermigrasi melalui kolom yang mengandung fase
diam dengan kecepatan yang bergantung pada rasio distribusinya. Solut akan
terelusi berdasarkan peningkatan titik didihnya dikurangi dengan semua interaksi
yang mungkin terjadi antara solut dengan fase diamnya. Fase gerak berupa gas
akan mengelusi solut dari ujung kolom lalu menghantarkannya ke detektor.
Peningkatan suhu yang dilakukan dilakukan untuk dapat menguapkan solut
sehingga mampu cepat terelusi (Gandjar dan Abdul, 2009).
Jenis-jenis kromatografi gas:
1. Kromatografi gas cair
Digunakan fase diam berupa cairan yang dijerap dalam suatu pendukung
sehingga solut dapat terlarut; mekanisme sorpsinya berupa partisi.
2. Kromatografi gas padat
Digunakan fase diam berupa padatan (misalnya polimerik); mekanisme
sorpsinya berupa adsorpsi (Gandjar dan Abdul, 2009).
Sistem peralatan kromatografi gas:
1. Fase gerak
Suatu zat cair (liquid chromatography, LC) ataupun gas (gas chromatography,
GC) yang mengalami perkolasi melalui fase diam menuju ke arah tertentu.
Dalam kromatografi gas, yang disebut dengan karier gas digunakan untuk fase
2. Ruang suntik sampel
Tempat di mana sampel mengalami volatilisasi sehingga menyebabkan gas
masuk ke aliran zat pembawa dalam kolom kromatografi gas. Beberapa tipe
inlet yang ada misalnya split/splitless, Programmed Thermal Vaporizing
(PTV), serta cool-on-column (COC).
3. Kolom
Dalam kromatografi gas, retensi molekul-molekul analit timbul karena
terjadinya interaksi yang lebih kuat dengan fase diam daripada fase geraknya;
karenanya interaksi analit dengan fase diam menjadi hal yang penting.
Interaksi yang terjadi dapat berupa interaksi dispersi, dipol, maupun interaksi
[image:42.595.86.509.205.644.2]hidrogen (Crawford Scientific, 2016).
Gambar 6. Interaksi dipol-dipol dan dipol-terinduksi dipol (Crawford Scientific, 2016)
4. Detektor dan macamnya (TCD, FID, ECD, NPD, fotometri nyala,
a. Thermal Conductivity Detector (TCD)
Konduktivitas termal mengukur kemampuan senyawa untuk
memindahkan panas dari daerah panas menuju dingin. Dalam TCD, gas
mengalir dari aliran kolom kromatografi melalui filamen tungsten-rhenium
panas. Saat solut mengalir dari kolom, konduktivitas termal aliran gas
menurun, filamennya memanas, resistensi elektriknya meningkat, dan
tegangannya turun karena adanya perubahan filamen. Detektor merespon
perubahan yang terjadi dalam konduktivitas termal, sehingga
konduktivitas solut dan gas pembawa menjadi sangat berbeda. Adapun
sensitivitas TCD berbanding tebalik (inversely proportional) terhadap
kecepatan alirnya: lebih sensitif dalam kecepatan aliran lebih rendah.
b. Flame Ionization Detector (FID)
Dalam FID, eluat dibakar dalam campuran H2 dan udara. Atom karbon
(kecuali karbon karbonil dan karboksil) memproduksi radikal CH, yang
selanjutnya menghasilkan ion CHO+ dalam flame.
CH + O CHO+ + e-. Hanya sekitar 1 dalam 105 atom karbon diproduksi
suatu ion, namun produksi ion sebanding terhadap jumlah atom karbon
yang masuk ke dalam flame. FID relatif tidak sensitif terhadap O2, CO2,
H2O, dan NH3. Batas deteksi FID 100 kali lebih kecil daripada TCD dan
berkurang 50% saat tidak digunakan gas pembawa He, melainkan N2.
Untuk open tubular columns, gas N2 ditambahkan dalam eluat H2 atau He
c. Detektor lainnya, antara lain: capture detector, flame photometric
detector, alkali flame detector, sulfur chemiluminescence detector, atomic
emission detector (Harris, 1982).
5. Komputer
Sinyal yang dihasilkan dari detektor terdigitalisasi dan disimpan ke dalam
penyimpanan yang memudahkan akses data, sehingga waktu retensi, area
puncak, dan data lain yang dibutuhkan dapat dengan mudah didapatkan
kembali.
6. Derivatisasi (esterifikasi, asilasi, alkilasi, sililasi, kondensasi, siklisasi)
Derivatisasi dilakukan dengan tujuan sebagai berikut:
a. Sifat fisik solut yang tidak mendukung dalam hal volatilitas serta
stabilitasnya
b. Meningkatkan batas deteksi dan bentuk kromatogram; dalam analisis
belum tentu kromatogram yang dihasilkan sesuai dengan kriteria atau
terkadang ditemui adanya tumpang tindih, atau tidak terdeteksinya sampel
tujuan
c. Meningkatkan volatilitas seperti senyawa-senyawa gula yang tidak mudah
menguap; biasanya senyawa dengan bobot molekul yang rendah,
disebabkan keberadaan gaya tarik inter-molekuler antara gugus-gugus
polar yang dapat ditutup melalui derivatisasi sehingga meningkatkan
volatilitas senyawa secara dramatis
d. Meningkatkan deteksi, misalnya untuk kolesterol dan senyawa-senyawa
e. Meningkatkan stabilitas; biasanya dialami oleh senyawa volatil yang
mengalami dekomposisi parsial karena panas sehingga diperlukan
derivatisasi
f. Meningkatkan batas deteksi pada penggunaan electron capture detector
(ECD) (Rohman, 2009).
Penentu dasar retensi solut umumnya adalah volatilitasnya, namun
tergantung pula pada fase diam yang digunakan. Fase diam yang sangat polar
menahan solut-solut polar dengan kuat. Interaksi hidrogen pada fase diam
mungkin merupakan gaya terkuat yang berperan dalam retensi; maka dari itu tiga
alkohol adalah yang terakhir terelusi, dikuti dengan empat keton, dan empat
alkena berdasarkan contoh kromatogram pada gambar 7. Interaksi dipol pada
[image:45.595.88.512.172.648.2]keton merupakan gaya terkuat kedua (Harris, 1982).
K. Spektrometri Massa
Spektrometri massa merupakan metode spektral yang berdasar bukan dari
absorbsi energi oleh molekul senyawa organik, namun berdasarkan fragmentasi
senyawa organik yang terjadi karena adanya tumbukan antara sebuah molekul
organik dengan elektron berenergi tinggi. Tumbukan yang terjadi mengakibatkan
sebuah elektron terlepas dari molekul sehingga terbentuk ion organik.
Fragmen-fragmen yang lebih kecil dari suatu molekul organik terbentuk akibat instabilitas
ion organik yang dihasilkan dari pembombardiran elektron, yang kemudian
ditemukan dalam bentuk radikal bebas maupun ion-ion lain. Spektrum massa
merupakan alur kelimpahan (abundance) versus nisbah massa/muatan (m/e atau
m/z) dari fragmen-fragmen itu. Muatan ion dari kebanyakan partikel yang
dideteksi dalam suatu spektrometer massa adalah + 1; nilai m/e untuk suatu ion
semacam itu sama dengan massanya. Oleh karena itu, spektrum massa merupakan
suatu rekaman dari massa partikel versus kelimpahan relatif partikel tersebut
(Fessenden dan Joan, 1986).
Pada umumnya, analisis menggunakan spektrometer massa dipadukan
dengan instrumen kromatografi seperti kromatografi gas (GC-MS) maupun
kromatografi cair (LC-MS). Spektrometer massa berguna dalam analisis senyawa
organik yang belum diketahui bentuk molekulnya berdasarkan analisis terhadap
spektra massa yang nampak, sehingga dapat dikatakan merupakan suatu metode
yang bersifat luas. Dalam analisis suatu senyawa organik yang telah diketahui
atau ada sebelumnya, perangkat komputer menelusuri basis data untuk
telah tersimpan dalam sistem sehingga dapat menjawab senyawa tersebut dengan
detil. Sementara itu, dalam suatu analisis senyawa yang belum diketahui, ion
molekuler, pola fragmentasi, serta pembuktian dari analisis spektrometri lainnya
(seperti IR dan NMR) dapat membantu ditemukannya senyawa baru (Silverstein,
2005).
Pola fragmentasi suatu molekul bergantung pada kerangka karbon dan
gugus fungsional yang terikat pada molekul tersebut. Karenanya, struktur dan
massa fragmen memberikan petunjuk mengenai struktur molekul induknya; serta
seringkali untuk menentukan bobot molekul suatu senyawa dari spektrum
massanya (Fessenden dan Joan, 1986).
Suatu aturan dalam fragmentasi yang disebut dengan “aturan nitrogen”
digunakan sebagai pertimbangan dalam menentukan pola fragmentasi. Suatu
molekul dengan massa molekuler genap harus tidak mengandung nitrogen atau
mengandung atom nitrogen dalam jumlah genap; sementara molekul dengan
massa molekuler ganjil harus mengandung atom nitrogen dalam jumlah ganjil
pula. Aturan ini berlaku untuk semua senyawa yang mengandung karbon,
hidrogen, oksigen, nitrogen, sulfur, dan halogen, juga atom-atom yang tidak lazim
seperti fosfor, boron, silikon, arsen dan alkali tanah. Menurut pembuktian,
dinyatakan bahwa fragmentasi ikatan tunggal sebuah ion molekuler berjumlah
genap memberikan fragmen ion ganjil; sebaliknya ion molekuler berjumlah ganjil
memberikan fragmen ion dalam jumlah genap. Pernyataan tersebut berlaku
Intensitas puncak ion molekuler bergantung pada stabilitas ion
molekulernya. Ion molekuler yang paling stabil berasal dari sistem aromatis
murni. Apabila substituen yang memiliki jalur pemutusan yang lebih mungkin
terjadi, puncak ion molekuler akan tidak terlalu intens, sehingga puncak
fragmennya menjadi lebih intens secara relatif. Pada umumnya, gugus-gugus
senyawa berikut ini diurutkan berdasarkan penurunan kemampuannya,
menghasilkan puncak molekuler yang utama: senyawa aromatis > alkena
terkonjugasi > senyawa siklik > sulfida organik > alkana rantai pendek >
merkaptan. Ion-ion molekuler yang terdeteksi berdasarkan penurunan
kemampuan: keton > amina > ester > eter > asam karboksilat ~ aldehida ~ amida
~ halida. Ion molekuler seringkali tidak dapat dideteksi pada alkohol alifatik,
nitrit, nitrat, senyawa nitro, nitril, dan senyawa-senyawa dengan jumlah
percabangan yang banyak (Silverstein, 2005).
Dalam menentukan puncak pola fragmentasi pada spektra EI, terdapat
beberapa peraturan yang didasarkan pada konsep kimia organik fisik. Akan tetapi
perlu dipahami terlebih dulu bahwa aturan fragmentasi ini berlaku bagi
spektrometri massa EI. Hal ini dikarenakan teknik-teknik ionisasi (CI, dan
lainnya) lainnya seringkali menghasilkan ion molekuler dengan energi lebih
rendah atau ion kuasimolekuler dengan pola fragmentasi yang sangat berbeda,
sehingga berlaku aturan yang berbeda. Berikut ini merupakan peraturan bagi
1. Tinggi relatif suatu puncak ion molekuler tertinggi pada senyawa dengan
rantai lurus dan berkurang seiring dengan peningkatan jumlah percabangan
(lihat aturan 3).
2. Tinggi relatif puncak ion molekuler biasanya berkurang dengan adanya
peningkatan massa molekuler dalam deret homolog. Lemak ester menjadi
suatu pengecualian.
3. Pemaksapisahan (cleavage) terjadi lebih pada atom karbon tersubstitusi alkil:
semakin tersubstitusi, semakin besar kemungkinan terjadinya
pemaksapisahan. Hal ini terjadi akibat peningkatan stabilitas karbokation
tersier apabila dibandingkan dengan sekunder, yang lebih stabil daripada
karbokation primer, yakni dengan urutan stabilitas sebagai berikut:
CH3+ < R2CH2+ < R3CH+ < R3C+
Pada umumnya, substituen terbesar pada suatu cabang menjadi subtituen yang
paling mudah dieliminasi dalam bentuk radikal, diduga karena radikal rantai
panjang dapat mencapai stabilitas melalui delokalisasi elektron bebas.
4. Ikatan rangkap, struktur siklik, terlebih cincin aromatis (atau heteroatomik)
menstabilkan ion molekuler sehingga meningkatkan kemungkinan
kemunculannya.
5. Dalam ikatan rangkap, pemaksapisahan alilik lebih mungkin terjadi dan
memberikan karbokation alilik terstabilisasi resonansi. Aturan ini tidak
berlaku untuk alkena sederhana karena adanya migrasi ikatan rangkap, namun
6. Cincin jenuh lebih mudah untuk kehilangan rantai samping berupa alkil pada
ikatan �. Hal ini hanya pada kasus khusus dari percabangan (aturan 3).
Muatan positif cenderung berada pada fragmen cincinnya.
7. Dalam senyawa aromatis tersubstitusi alkil, pemaksapisahan sangat mungkin
terjadi pada ikatan � dalam cincin, sehingga membentuk ion benzyl yang
terstabilisasi resonansi, atau seringkali ion tropilium.
8. Ikatan C—C yang terletak di sebelah heteroatom seringkali mengalami
pemaksapisahan yang menghasilkan muatan pada fragmen yang mengandung
heteroatom di mana elektron yang tidak berpasangan menyediakan stabilisasi
resonansi.
9. Pemaksapisahan sering dihubungkan dengan eliminasi molekul-molekul yang
kecil, stabil, netral, seperti karbon monoksida, olefin, air, amonia, hidrogen
sulfida, hydrogen sianida, merkaptan, ketena, atau alkohol, yang seringkali
muncul dengan mengalami penataan ulang (rearrangement) (Silverstein,
2005).
L. Landasan Teori
Pembentukan senyawa melalui reaksi substitusi nukleofilik asil terjadi
antara senyawa alkohol dengan derivat asam karboksilat, yang umumnya
menghasilkan sintesis suatu senyawa golongan ester. Reaksi substitusi nukleofilik
asil diawali dengan terjadinya adisi nukleofil pada atom C gugus karbonil (C=O)
yang memicu terjadi pembentukan intermediet tetrahedral yang mengikat dua
stabilisasi pasangan elektron bebas pada atom oksigen yang menyebabkan
terbentuknya ikatan ganda karbonil kembali dan berakibat pada pelepasan gugus
pergi yakni ion klorida (Cl-), sehingga terbentuk produk dan sebuah atom gugus
pergi.
Benzoil klorida termasuk ke dalam derivat asam karboksilat yang
teraktivasi dalam sintesis senyawa asil, senyawa tersebut merupakan agen asilasi
yang sangat reaktif dalam reaksi. Reaktivitas benzoil klorida berbanding terbalik
terhadap kebasaannya, maka gugus pergi Cl yang merupakan basa lemah menjadi
gugus pergi yang lebih baik daripada gugus pergi lain yang lebih tinggi
kebasaannya. Oksigen karbonil dan atom klorin sama-sama menarik densitas
elektron dari atom karbon asil, sehingga menjadikannya elektrofil yang kuat.
Sementara itu parasetamol yang berperan sebagai senyawa alkohol mampu
bertindak sebagai nukleofil karena terdapat gugus hidroksi (-OH) yang
mempunyai pasangan elektron bebas. Nukleofil tersebut akan menyerang gugus
karbonil benzoil klorida menghasilkan senyawa 4-asetamidofenil benzoat dengan
gugus pergi atom klorin (Cl-). Reaksi antara benzoil klorida dengan alkohol
merupakan reaksi eksotermis sehingga perlu diperhatikan suhu reaksi untuk
menghindari hidrolisis maupun penurunan stabilitas reaksi. Di samping itu,
piridina (atau basa non-nukleofilik lainnya) ditambahkan ke dalam reaksi untuk
menetralisasi dan mencegah pembentukan by-product terutama asam klorida
Gambar 8. Reaksi umum sintesis 4-asetamidofenil benzoat
M. Hipotesis
Senyawa 4-asetamidofenil benzoat yang merupakan senyawa ester dapat
disintesis dari parasetamol dan benzoil klorida melalui reaksi substitusi
BAB III
METODE PENELITIAN
A. Jenis Penelitian
Penelitian ini termasuk jenis penelitian non-eksperimental deskriptif
karena berupa pemaparan terhadap fenomena yang terjadi tanpa adanya perlakuan
terhadap subjek uji maupun melibatkan hubungan sebab-akibat.
B. Definisi Operasional Penelitian
1. Starting material (SM) merupakan senyawa yang digunakan dalam sintesis
yang merupakan senyawa asal, dalam penelitian ini adalah parasetamol dan
benzoil klorida.
2. Molekul target (MT) merupakan senyawa tujuan yang diharapkan terbentuk
dalam penelitian, yakni 4-asetamidofenil benzoat.
3. Katalis merupakan senyawa yang digunakan dalam reaksi untuk
meningkatkan laju reaksi kimia, yaitu piridin.
4. Rendemen merupakan jumlah molekul target yang terjadi dan dapat
diperhitungkan dari jumlah starting material yang digunakan. Rendemen
senyawa hasil sintesis yang diharapkan dalam penelitian ini adalah rendemen
C. Bahan Penelitian
Parasetamol (teknis, Brataco Chemika), benzoil klorida (p.a, Merck),
piridina (p.a, Merck), etanol 96% (teknis, General Labora), etanol absolut (p.a,
Merck), NaOH (Laboratorium Sanata Dharma), kloroform (p.a, Merck), etil asetat
(teknis, Brataco Chemika; p.a, Merck), n-heksana (p.a, Merck), aseton (p.a,
Merck), silika gel GF254 (Merck), akuades (General Labora), kertas saring, kertas
timbang, dan es batu (Laboratorium Sanata Dharma).
D. Alat Penelitian
Gelas beker, labu erlenmeyer, pipet tetes, gelas ukur, kaca pengaduk,
magnetic stirrer, mantle heater, labu hisap, corong Buchner, sendok spatel,
pompa vakum, pH indikator (E. Merck), cawan petri, waterbath (Memmert
W350), neraca analitik (Ohaus PA413), tabung reaksi, Melting Point System
(Mettler Toledo MP70), chamber KLT, micropipette, oven (Memmert Oven
Model 400), lampu UV, spektrometer inframerah (IR Shimadzu Prestige-21),
spektrometer massa EI (Shimadzu QP2010S), spektrometer massa FD
(JMS-T100GCV), spektrometer 1H-NMR, aluminium foil, dan baskom.
E. Tata Cara Penelitian
1. Sintesis 4-asetamidofenil benzoat
Parasetamol sebanyak 5 gram (0,033 mol) dimasukkan dalam
erlenmeyer 500 mL, kemudian ditambahkan piridin 12 mL dan diaduk selama
dalam larutan tersebut ditambahkan benzoil klorida sejumlah 7,7 mL (0,066
mol) sedikit demi sedikit sambil terus diaduk, hingga merata dan terjadi
perubahan konsistensi (60 menit).
Akuades dingin sebanyak ± 200 mL ditambahkan ke dalam campuran
untuk disaring dengan corong Buchner dan dicuci dengan akuades yang sama.
Padatan/filtrat yang didapatkan kemudian direkristalisasi dengan
melarutkannya dalam etanol 96% panas, disaring dengan corong Buchner,
sehingga filtrat dapat didinginkan sampai terbentuk kristal produk secara
optimal (± 60 menit). Setelah rekristalisasi selesai, kristal dikeringkan dalam
oven dengan temperatur 80o C selama ± 2 jam. Hasil pengeringan kemudian
direkristalisasi lagi dengan cara yang sama menggunakan ± 250 mL etanol
96% panas, dikeringkan dalam oven dengan temperatur 80º C selama 24 jam,
ditimbang, dan dihitung rendemennya dengan rumus:
%Rendemen=
berat senyawa hasil percobaan
berat senyawa secara teoretis x100%
2. Pemeriksaan pendahuluan senyawa hasil sintesis
a. Uji organoleptis. Dilakukan dengan pengamatan terhadap warna, bentuk,
bau, dan rasa senyawa hasil sintesis. Kemudian hasil pengamatan
dibandingkan dengan starting material yang digunakan dalam penelitian,
yaitu parasetamol dan benzoil klorida.
b. Pemeriksaan kelarutan senyawa hasil sintesis. Akuades sebanyak 2 mL
dimasukkan ke dalam tabung reaksi. Kristal hasil sintesis dalam wadah
reaksi, diamati kelarutannya hingga tepat jenuh, lalu dicatat kembali bobot
sisanya. Prosedur yang serupa dilakukan dengan larutan NaOH 10%,
etanol 96%, kloroform, dan etil asetat; kemudian dibandingkan dengan
kelarutan parasetamol dalam pelarut-pelarut yang sama.
c. Pemeriksaan senyawa hasil sintesis dengan kromatografi lapis tipis (KLT).
Senyawa hasil sintesis yang dilarutkan dalam pelarut yang sesuai
(kloroform), ditotolkan sebanyak ± 1 µL pada lempeng KLT silika gel
GF254 menggunakan micropipette 0,5-10 µL. Sebagai pembanding,
digunakan starting material dan dilakukan dengan cara serupa.
Pengembangan dilakukan dengan jarak rambat fase gerak 8 cm dalam
bejana yang berisi fase gerak aseton:etil asetat (2:3) dengan p’ = 4,680;
dan fase diam berupa silika gel 60 GF254. Pengamatan terhadap bercak
yang terbentuk dilakukan pada lampu UV 254 nm, kemudian dihitung Rf
masing-masing bercak hasil elusi.
d. Pengujian titik lebur. Kristal senyawa hasil sintesis diisikan ke dalam
electrothermal capillary tubes, kemudian dimasukkan ke dalam alat
pengukur titik lebur (Melting Point System). Amati peleburan kristalnya
dan catat suhu waktu pertama kali melebur hingga semua kristal melebur
dengan kenaikan suhu 1o C per-menit.
3. Elusidasi struktur senyawa hasil sintesis
a. Spektrofotometri inframerah (IR). Kurang lebih 1 mg kristal hasil sintesis
dan dibuat menyerupai pelet. Selanjutnya dibuat spektra inframerah
dengan spektrofotometer inframerah.
b. Spektrometri massa (MS). Kristal hasil sintesis dilarutkan dalam
pelarutnya, yakni kloroform (CHCl3), kemudian dilakukan pemeriksaan
dengan alat kromatografi gas-spektroskopi massa (GC-MS) dalam kondisi:
alat pengionan Electron Impact (EI) 70 eV, suhu injektor 310o C, jenis
kolom AGILENT