INTISARI
2-(4-isobutilfenil) propanoat merupakan suatu analgetika golongan Non Setroidal Anti Inflammatory Drugs (NSAIDs) yang penggunaannya dapat menimbulkan efek samping tukak peptik pada saluran pencernaan. Esterifikasi 2-(isobutilfenil) propanoat dengan N-(hidroksifenil) asetamida membentuk 4-asetamidofenil 2-(4-isobutilfenil) propanoat akan menurunkan efek samping dan meningkatkan efek terapi karena efek sinergis dari penggunaan secara bersamaan.
Metode yang digunakan untuk sintesis senyawa 4-asetamidofenil 2-(4-isobutilfenil) propanoat menggunakan prinsip esterifikasi Yamaguchi. Proses sintesis dilakukan dengan derivatisasi 2-(4-isobutilfenil) propanoat dengan benzoil klorida membentuk benzoil 2-(4-isobutilfenil) propanoat anhidrida yang kemudian akan direaksikan dengan N-(4-hidroksifenil) asetamida menggunakan katalis NaOH/etanol 0,1 N. Analisis senyawa hasil sintesis menggunakan uji warna dengan FeCl3, uji gas dengan NaHCO3, uji titik lebur, uji KLT dengan fase
diam silika gel GF254 dan fase gerak etil asetat, serta analisis spektroskopi IR.
Hasil analisis menunjukkan tidak ada perubahan warna menjadi ungu dengan penambahan FeCl3 dan tidak muncul gelembung gas dengan penambahan
NaHCO3. Senyawa hasil sintesis didapati tidak melebur hingga suhu 300°C. Hasil
uji KLT menunjukkan bahwa senyawa hasil sintesis telah murni. Interpretasi spektra IR menunjukkan adanya serapan gugus amida pada 1635,64 cm-1. Berdasarkan analisis tersebut maka disimpulkan bahwa senyawa hasil sintesis yang terbentuk adalah 4-asetamidofenil 2-(4-isobutilfenil) propanoat.
ABSTRACT
2-(4-isobutylphenyl) propanoic acid is a Non Steroidal Anti Inflammatory Drugs (NSAIDs) that can cause peptic ulcers in the gastrointestinal tract. Esterification of 2-(4-isobutylphenyl) propanoic acid with N-(4-hydroxyohenyl) acetamide to form 4-acetamidophenyl 2-(4-isobutylphenyl) propanoate will reduce the risk of peptic ulcers and deals synergistic effect due to its combination.
The synthesis method of 4-acetamidophenyl 2-(4-isobutylphenyl) propanoate using the principle of Yamaguchi esterification. Synthesis process carried-out by derivatization of 2-(4-isobutylphenyl) propanoic acid with benzoyl chloride to form benzoyl 2-(4-isobutylphenyl) propanoic acid anhydride that will be reacted with N-(4-hydroxyphenyl) acetamide in NaOH/ethanol 0.1 N as a catalyst. Analysis of synthesized compounds using FeCl3 color test, NaHCO3 gas
test, melting point test, TLC analysis with silica gel GF254 as stationary phase and
ethyl acetate as mobile phase, and IR spectroscopy analysis.
The result showed no color change to purple of FeCl3 test and no gas
appear of NaHCO3 test. Synthesized compound was not melted until 300°C. TLC
analysis showed that the compound synthesized has already pure. IR interpretation showed absorbtion at 1635.64 cm-1 of amide functional group.
Based on the analysis, it is concluded that the synthesized compound is 4-acetamidophenyl 2-(4-isobutylphenyl) propanoate.
i
SINTESIS SENYAWA 4-ASETAMIDOFENIL 2-(4-ISOBUTILFENIL) PROPANOAT DARI 2-(4-ISOBUTILFENIL) PROPANOAT DAN
N-(4-HIDROKSIFENIL) ASETAMIDA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh: Christian Gunawan
NIM : 108114078
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
“Thousands of candles can be lighted from a single candle, and the life of the candle will not be shortened. Happiness never decreases
by being shared” – Buddha
“Nilai tertinggi dari kemuliaan adalah dapat merendahkan hati, nilai
tertinggi dari kekayaan adalah gemar beramal, kaidah dalam situasi
kesusahan adalah tau diri, kaidah dalam kemiskinan adalah tiada
keinginan yang berlebihan” – Kong Hu Cu
“Durian berduri karena sedap isinya, kulit manggis pahit karena manis dalamnya. Dibalik
kesulitan, pasti ada kesenangan dan kebahagiaan” - Lao Tzu
Bersama ini, saya persembahakan karya ini kepada:
Buddha, Dhamma, Sangha
Keluargaku tercinta
Bapak/Ibu dosen Fakultas Farmasi Universitas Sanata Dharma
Sahabat dan teman-teman seperjuangan
vii
ix
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS ... v
PRAKATA... vi
PERNYATAAN KEASLIAN KARYA ... viii
x
B. Tujuan Penelitian ... 6
BAB II. PENELAAHAN PUSTAKA ... 7
A. 2-(4-isobutilfenil) propanoat ... 7
B. N-(4-hidroksifenil) asetamida ... 8
C. Esterifikasi Yamaguchi ... 11
D. Analisis Pendahuluan ... 14
1. Pemeriksaan Organoleptis... 14
2. Pemeriksaan Warna dengan FeCl3... 14
3. Pemeriksaan Gas dengan Natrium Bikarbonat (NaHCO3) ... 15
E. Pemurnian dan Pemeriksaan Kemurnian Senyawa Hasil Sintesis.. 16
1. Rekristalisasi ... 16
2. Pemeriksaan Titik Lebur ... 17
3. Kromatografi Lapis Tipis (KLT) ... 17
F. Elusidasi Struktur ... 19
1. Spektrofotometri Inframerah (IR) ... 19
G. Landasan Teori ... 21
H. Hipotesis ... 21
BAB III. METODOLOGI PENELITIAN ... 22
A. Jenis dan Rancangan Penelitian ... 22
B. Definisi Operasional ... 22
C. Bahan Penelitian ... 23
xi
E. Prosedur Penelitian ... 24
1. Rekristalisasi 2-(4-isobutilfenil) propanoat ... 24
2. Rekritalisasi N-(4-hidroksifenil) asetamida ... 24
3. Sintesis 4-asetamidofenil 2-(4-isobutilfenil) propanoat ... 24
4. Analisis Senyawa Hasil Sintesis ... 26
5. Elusidasi Struktur Senyawa Hasil Sintesis ... 27
F. Analisis Hasil ... 27
1. Perhitungan Rendemen ... 27
2. Analisis Pendahuluan ... 28
3. Pemeriksaan Kemurnian Senyawa Hasil Sintesis... 28
4. Elusidasi Struktur... 28
BAB IV. HASIL DAN PEMBAHASAN ... 29
BAB V. KESIMPULAN DAN SARAN ... 49
A. Kesimpulan... 49
B. Saran ... 49
DAFTAR PUSTAKA ... 50
LAMPIRAN ... 54
xii
DAFTAR TABEL
Halaman
Tabel I. Frekuensi inframerah gugus karbonil ... 20
Tabel II. Data organoleptis senyawa hasil sintesis dan starting material .... 35
Tabel III. Data uji warna dengan FeCl3 ... 36
Tabel IV. Data uji gas dengan natrium bikarbonat (NaHCO3) ... 37
Tabel V. Data titik lebur senyawa hasil sintesis dan starting material... 38
Tabel VI. Nilai Rf analisis KLT senyawa hasil sintesis ... 39
Tabel VII. Interpretasi spektra IR derivat 2-(4-isobutilfenil) propanoat ... 42
xiii
DAFTAR GAMBAR
Halaman
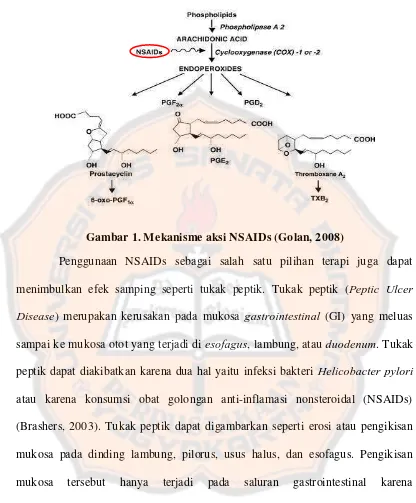
Gambar 1. Mekanisme aksi NSAIDs ... 2
Gambar 2. Sturktur kimia ibuprofen ... 4
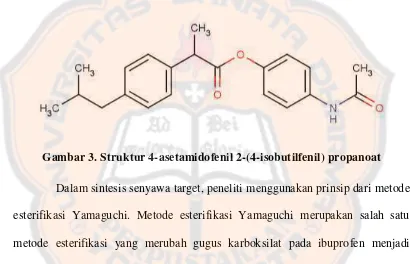
Gambar 3. Struktur 4-asetamidofenil 2-(4-isobutilfenil) propanoat ... 5
Gambar 4. Potensial elektrostatik asam karboksilat ... 8
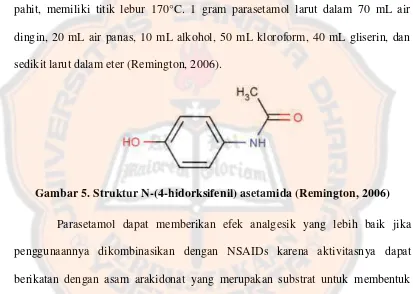
Gambar 5. Struktur N-(4-hidroksifenil) asetamida ... 9
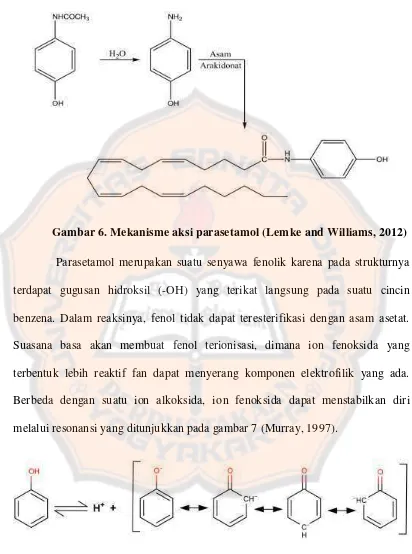
Gambar 6. Mekanisme aksi parasetamol ... 10
Gambar 7. Stabilisasi resonansi fenol... 10
Gambar 8. Skema esterifikasi Yamaguchi ... 11
Gambar 9. Derivatisasi asam karboksilat menjadi ahidrida ... 12
Gambar 10. Frekuensi streching IR asam karboksilat dan derivatnya ... 12
Gambar 11. Reaktivitas relatif derivat asam karboksilat... 13
Gambar 12. Reaksi fenol dengan FeCl3... 15
Gambar 13. Reaksi asam karboksilat dengan NaHCO3 ... 15
Gambar 14. Reaksi umum sintesis senyawa 4-asetamidofenil 2-(4-isobutilfenil) propanoat ... 21
Gambar 15. Aktivasi gugus karboksilat 2-(4-isobutilfenil) propanoat ... 29
Gambar 16. Analisis muatan 2-(4-isobutilfenil) propanoat... 30
Gambar 17. Analisis muatan 2-(4-isobutilfenil) propanoat terderivatisasi ... 30
xiv
Gambar 19. Analisis muatan 4-asetamidofenil 2-(4-isobutilfenil) propanoat. 32
Gambar 20. Analisis muatan etil 2-(4-isobutilfenil) propanoat ... 33
Gambar 21. Mekanisme reaksi derivatisasi 2-(4-isobutilfenil) propanoat ... 34
Gambar 22. Mekanisme reaksi sintesis senyawa 4-asetamidofenil 2-(4-isobutilfenil) propanoat ... 34
Gambar 23. KLT senyawa hasil sintesis pada fase gerak etil asetat... 39
Gambar 24. Spektra IR 2-(4-isobutilfenil) propanoat terderivatisasi ... 40
Gambar 25. Identifikasi gugus fungsi derivat 2-(4-isobutilfenil) propanoat .. 41
Gambar 26. Identifikasi gugus fungsi senyawa target ... 42
Gambar 27. Spektra IR senyawa hasil sintesis... 43
Gambar 28. Resonansi 2-(4-isobutilfenil) propanoat terderivatisasi ... 43
Gambar 29. Resonansi senyawa hasil sintesis ... 43
Gambar 30. Muatan atom karbon alkena rantai samping derivat 2-(4-isobutilfenil propanoat ... 45
Gambar 31. Muatan atom karbon alkena rantai samping senyawa target ... 45
Gambar 32. Ilustrasi vibrasi trans-bending out of plane ... 46
Gambar 33. Ilustrasi vibrasi cis-bending out of plane ... 46
xv
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Perhitungan rendemen senyawa hasil sintesis ... 54
Lampiran 2. Pembuatan larutan natrium nikarbonat (NaHCO3) 10% b/v... 58
Lampiran 3. Spektra IR 2-(4-isobutilfenil) propanoat... 59
Lampiran 4. Spektra IR N-(4-hidroksifenil) asetamida ... 60
Lampiran 5. Spektra IR derivat 2-(4-isobutilfenil) propanoat ... 61
xvi
INTISARI
2-(4-isobutilfenil) propanoat merupakan suatu analgetika golongan Non Setroidal Anti Inflammatory Drugs (NSAIDs) yang penggunaannya dapat menimbulkan efek samping tukak peptik pada saluran pencernaan. Esterifikasi 2-(isobutilfenil) propanoat dengan N-(hidroksifenil) asetamida membentuk 4-asetamidofenil 2-(4-isobutilfenil) propanoat akan menurunkan efek samping dan meningkatkan efek terapi karena efek sinergis dari penggunaan secara bersamaan.
Metode yang digunakan untuk sintesis senyawa 4-asetamidofenil 2-(4-isobutilfenil) propanoat menggunakan prinsip esterifikasi Yamaguchi. Proses sintesis dilakukan dengan derivatisasi 2-(4-isobutilfenil) propanoat dengan benzoil klorida membentuk benzoil 2-(4-isobutilfenil) propanoat anhidrida yang kemudian akan direaksikan dengan N-(4-hidroksifenil) asetamida menggunakan katalis NaOH/etanol 0,1 N. Analisis senyawa hasil sintesis menggunakan uji warna dengan FeCl3, uji gas dengan NaHCO3, uji titik lebur, uji KLT dengan fase
diam silika gel GF254 dan fase gerak etil asetat, serta analisis spektroskopi IR.
Hasil analisis menunjukkan tidak ada perubahan warna menjadi ungu dengan penambahan FeCl3 dan tidak muncul gelembung gas dengan penambahan
NaHCO3. Senyawa hasil sintesis didapati tidak melebur hingga suhu 300°C. Hasil
uji KLT menunjukkan bahwa senyawa hasil sintesis telah murni. Interpretasi spektra IR menunjukkan adanya serapan gugus amida pada 1635,64 cm-1. Berdasarkan analisis tersebut maka disimpulkan bahwa senyawa hasil sintesis yang terbentuk adalah 4-asetamidofenil 2-(4-isobutilfenil) propanoat.
xvii ABSTRACT
2-(4-isobutylphenyl) propanoic acid is a Non Steroidal Anti Inflammatory Drugs (NSAIDs) that can cause peptic ulcers in the gastrointestinal tract. Esterification of 2-(4-isobutylphenyl) propanoic acid with N-(4-hydroxyohenyl) acetamide to form 4-acetamidophenyl 2-(4-isobutylphenyl) propanoate will reduce the risk of peptic ulcers and deals synergistic effect due to its combination.
The synthesis method of 4-acetamidophenyl 2-(4-isobutylphenyl) propanoate using the principle of Yamaguchi esterification. Synthesis process carried-out by derivatization of 2-(4-isobutylphenyl) propanoic acid with benzoyl chloride to form benzoyl 2-(4-isobutylphenyl) propanoic acid anhydride that will be reacted with N-(4-hydroxyphenyl) acetamide in NaOH/ethanol 0.1 N as a catalyst. Analysis of synthesized compounds using FeCl3 color test, NaHCO3 gas
test, melting point test, TLC analysis with silica gel GF254 as stationary phase and
ethyl acetate as mobile phase, and IR spectroscopy analysis.
The result showed no color change to purple of FeCl3 test and no gas
appear of NaHCO3 test. Synthesized compound was not melted until 300°C. TLC
analysis showed that the compound synthesized has already pure. IR interpretation showed absorbtion at 1635.64 cm-1 of amide functional group. Based on the analysis, it is concluded that the synthesized compound is 4-acetamidophenyl 2-(4-isobutylphenyl) propanoate.
1
BAB I
PENDAHULUAN
A. Latar Belakang
Non-Steroidal Anti-Inflamatory Drugs (NSAIDs) merupakan senyawa
kimia yang menghambat aktivitas enzim cyclooxigenase (COX-1 dan COX-2)
yang berperan dalam produksi prostaglandin seperti yang ditunjukkan pada
gambar 1 dibawah ini. Adanya gugus karboksilat akan membentuk interaksi
hidrogen dengan residu arginin pada posisi 120 baik pada COX-1 dan COX-2
secara irreversible, sehingga asam arakidonat tidak dapat menempati sisi aktif
enzim dan tidak dapat membentuk prostaglandin (Bhagavan, 2002).
Cyclooxigenase disebut juga prostaglandin sintase merupakan enzim yang
berperan dalam metabolisme asam arakidonat menjadi prostaglandin G2 (PGG2)
dan prostaglandin H2 (PGH2) yang merupakan prekursor prostanoid yang
memediasi timbulnya rasa nyeri (Tollison, Satterthwaite, and Tollison, 2002).
Terhambatnya sintesis prostaglandin akibat penggunaan NSAIDs akan
mengurangi distribusi sel darah putih yang memicu terjadinya peradangan. Selain
itu, NSAIDs juga dapat berperan dalam menekan rasa sakit karena dapat
menembus sawar darah otak sehingga mencegah prostaglandin dalam
memproduksi neuromodulator di sumsum tulang belakang yang dapat
2
Gambar 1. Mekanisme aksi NSAIDs (Golan, 2008)
Penggunaan NSAIDs sebagai salah satu pilihan terapi juga dapat
menimbulkan efek samping seperti tukak peptik. Tukak peptik (Peptic Ulcer
Disease) merupakan kerusakan pada mukosa gastrointestinal (GI) yang meluas
sampai ke mukosa otot yang terjadi di esofagus, lambung, atau duodenum. Tukak
peptik dapat diakibatkan karena dua hal yaitu infeksi bakteri Helicobacter pylori
atau karena konsumsi obat golongan anti-inflamasi nonsteroidal (NSAIDs)
(Brashers, 2003). Tukak peptik dapat digambarkan seperti erosi atau pengikisan
mukosa pada dinding lambung, pilorus, usus halus, dan esofagus. Pengikisan
mukosa tersebut hanya terjadi pada saluran gastrointestinal karena
ketidakseimbangan asam lambung dan pepsin. Tukak duodeni disebabkan karena
sekresi asam lambung yang berlebihan, sedangkan tukak lambung disebabkan
karena aktivitas bakteri Helicobacter pylori atau karena konsumsi NSAIDs dalam
3
Tukak peptik atau perdarahan lambung terjadi karena ketidakseimbangan
asam lambung dan pepsin dengan mekanisme pertahanan dan perbaikan mukosa.
Di Amerika Serikat, prevalensi tukak peptik mencapai angka 350.000 per tahun.
Angka kematian disebabkan tukak peptik ialah 6000 penderita per tahun dengan
3000 penderita tukak duodeni dan 3000 lagi penderita tukak lambung. Prevalensi
terjadinya tukak peptik pada Indonesia akibat penggunaan NSAIDs pada beberapa
penelitian ditemukan berkisar antara 6-15% terutama pada usia 20-50 tahun
(Suyono, 2001).
Ibuprofen merupakan suatu NSAIDs derivat asam propionat yang paling
sering digunakan sebagai analgesik terutama dalam pengobatan nyeri pada bagian
orofacial (Sharav, 2008). Penggunaan ibuprofen menjadi pilihan pertama dalam
terapi karena kemungkinan terjadinya efek samping yang paling kecil (Neal,
2010). Walaupun begitu, seperti halnya NSAIDs yang lain, ibuprofen juga dapat
menyebabkan perforasi dan perdarahan pada saluran pencernaan dengan rasio
2,9% dalam 1 milyar peresepan (Vane, Botting, and Botting, 1996). Efek samping
ibuprofen yang dapat menyebabkan tukak peptik kronis menjadi perhatian utama
bagi pasien yang memiliki riwayat penyakit pada saluran pencernaan. Selain itu,
penggunaan ibuprofen juga harus diperhatikan pada pasien yang mengkonsumsi
alkohol dan merokok yang dapat meningkatkan risiko terjadinya tukak peptik
(Aschenbrenner, 2009). NSAIDs menyebabkan kerusakan mukosa saluran cerna
melalui dua mekanisme: iritasi topikal dan inhibisi sistemik sintesis prostaglandin.
Dilaporkan lebih dari 80% pasien yang menderita tukak peptik akibat konsumsi
4
Gambar 2. Struktur kimia ibuprofen (Myers, 2007)
Gugus karboksilat (-COOH) pada ibuprofen seperti yang ditunjukkan
pada gambar 2 dapat menyebabkan perforasi atau perdarahan karena mengiritasi
topikal pada mukosa saluran gastrointestinal mengingat sifatnya yang asam. Salah
satu bentuk pengembangan untuk menekan efek samping yang ditimbulkan adalah
dengan menutup gugus karboksilat pada ibuprofen membentuk ester untuk
menekan keasaman. Bentuk ester dari ibuprofen tidak akan menghilangkan efek
farmakologisnya karena merupakan suatu prodrug yang akan terhidrolisis secara
in vivo membentuk ibuprofen kembali yang mempunyai efek terapetik
(Kankanala, Billur, Reddy, Mukkanti, and Pal, 2013). Sintesis ester ibuprofen
sebagai prodrug melibatkan reaksi dengan suatu alkohol. Komponen alkohol yang
dipilih adalah parasetamol, sehingga ketika prodrug terhidrolisis akan membentuk
parasetamol kembali yang aktif secara farmakologis dengan aktivitas sebagai
pereda rasa nyeri yang bekerja sinergis dengan ibuprofen dan tidak menimbulkan
interaksi dengan ibuprofen.
Parasetamol merupakan suatu alternatif obat analgesik turunan anilina
yang memiliki tingkat toleransi tinggi pada pasien yang memiliki gangguan
percernaan seperti maag. Akan tetapi penggunaan dalam dosis besar akan
4-5
asetamidofenil 2-(4-isobutilfenil) propanoat merupakan bentuk ester ibuprofen
dengan parasetamol akan menekan efek samping dari masing-masing komponen.
Didalam tubuh 4-asetamidofenil 2-(4-isobutilfenil) propanoat akan mengalami
hidrolisis secara in vivo oleh enzim esterase (Kwoon, 2001). Hidrolisis yang
terjadi akan membentuk kembali ibuprofen dan parasetamol yang kombinasi
keduanya akan memberikan efek yang sinergis (Torabinejad and Walton, 2009).
Gambar 3. Struktur 4-asetamidofenil 2-(4-isobutilfenil) propanoat
Dalam sintesis senyawa target, peneliti menggunakan prinsip dari metode
esterifikasi Yamaguchi. Metode esterifikasi Yamaguchi merupakan salah satu
metode esterifikasi yang merubah gugus karboksilat pada ibuprofen menjadi
gugus anhidrida yang lebih reaktif dibandingkan bentuk asamnya. Derivatisasi
ibuprofen menjadi suatu anhidrida menggunakan benzoil klorida dengan katalis
piridina. Anhidrida yang terbentuk memiliki reaktivitas yang lebih tinggi dan
dapat bereaksi dengan parasetamol menggunakan katalis NaOH/etanol
membentuk senyawa target yaitu 4-asetamidofenil 2-(4-isobutilfenil) propanoat.
1. Rumusan Masalah
Dari latar belakang tersebut, permasalahan yang dapat dirumuskan
6
Apakah senyawa 4-asetamidofenil 2-(4-isobutilfenil) propanoat dapat disintesis
dari 2-(4-isobutilfenil) propanoat dan N-(4-hidroksifenil) asetamida?
2. Keaslian Penelitian
Sejauh penelusuran yang telah dilakukan oleh peneliti, penelitian
berjudul “sintesis senyawa 4-asetamidofenil 2-(4-isobutilfenil) propanoat dari
2-(4-isobutilfenil) propanoat dan N-(4-hidroksifenil) asetamida” belum pernah
dilakukan sebelumnya. Penelitian sejenis yang pernah dilakukan adalah “Stable
ester and amide conjugates of some NSAIDs as analgesc and antiinflammatory
compounds with improved biological activity” oleh Orhan, Burcu, Asli,
Nilufer, Yagmur, dan Erden yang dipublikasikan tahun 2011.
3. Manfaat Penelitian
a. Manfaat teoretis yang dapat diperoleh yaitu memberikan informasi terkait
sintesis senyawa 4-asetamidofenil isobutilfenil) propanoat dari
2-(4-isobutilfenil) propanoat dan N-(4-hidroksifenil) asetamida.
b. Manfaat metodologis yang dapat diperoleh yaitu memberikan informasi
terkait metode dalam sintesis senyawa 4-asetamidofenil 2-(4-isobutilfenil)
propanoat dari 2-(4-isobutilfenil) propanoat dan N-(4-hidroksifenil)
asetamida.
B. Tujuan Penelitian
Penelitian yang dilakukan ini bertujuan untuk mensintesis
4-asetamidofenil 2-(4-isobutilfenil) propanoat dari 2-(4-isobutilfenil) propanoat dan
7
BAB II
PENELAAHAN PUSTAKA
A. 2-(4-isobutilfenil) propanoat
Senyawa 2-(4-isobutilfenil) propanoat yang juga dikenal dengan
ibuprofen, merupakan NSAIDs turunan asam propionat yang dapat disintesis
dengan berbagai macam metode dari iso-butilbenzena dengan asetil klorida, lalu
iso-butilbenzofenon yang dihasilkan akan direaksikan dengan natrium sianida
yang selanjutnya akan mengalami proses dehidrasi, reduksi, dan hidrolisis
membentuk ibuprofen (Vardanyan and Hruby, 2006). NSAIDs turunan asam
propionat ini dapat menghambat sintesis prostaglandin karena aktivitasnya
sebagai inhibitor enzim siklooksigenase pada bagian periferal enzim. Terjadinya
tukak peptik dalam penggunaan NSAIDs turunan asam propionat tidak sebanyak
pengunaan NSAIDs golongan lainnya. Penggunaan NSAIDs turunan asam
propionat secara oral sangat cepat mengalami absorbsi dalam tubuh. Setelah
mengalami absorbsi, 99% dari turunan asam propionat akan terikat lama oleh
protein plasma yaitu albumin (Delisa and Walsh, 2005).
Senyawa 2-(4-isobutilfenil) propanoat memiliki rumus molekul C13H18O2
dengan bobot molekul 206,3 g/
mol. Ibuprofen memiliki titik lebur 77°C. Ibuprofen
sukar larut dalam air, mudah larut dalam pelarut organik seperti alkohol dan
aseton (Myers, 2007). 2-(4-isobutilfenil) propanoat merupakan suatu asam
8
dengan cincin benzena. Asam karboksilat merupakan asam organik dengan
tingkat keasaman yang lemah. Berdasarkan gambar 4 dibawah ini, asam
karboksilat alifatik dalam bentuk tidak terionisasi memiliki panjang ikatan C-O
yang lebih panjang yaitu 0,123 Å dibandingkan C=O dengan panjang ikatan 0,133
Å. Berbeda dalam keadaan terionisasi, panjang ikatan C-O akan ekivalen dengan
C=O yaitu 0,128 Å, hal tersebut diakibatkan karena adanya delokalisasi elektron
pada gugus karboksilat (Clungston and Rosalind, 2000).
Gambar 4. Potensial elektrostatik asam karboksilat (Clungston and Rosalind, 2000)
B. N-(4-hidroksifenil) asetamida
Senyawa N-(4-hidroksifenil) asetamida yang juga dikenal dengan
parasetamol atau asetaminofen, dapat digunakan sebagai analgesik ataupun
antipiretik pada pasien yang memiliki gangguan pada lambung karena sifatnya
yang tidak iritatif pada mukosa dinding lambung. Parasetamol tidak memiliki
aktivitas antiinflamasi karena afinitasnya dengan enzim siklooksigenase yang
9
dengan beberapa NSAIDs untuk suatu tujuan terapi karena kombinasi keduanya
akan memiliki onset dan efektivitas yang lebih baik daripada penggunaan
parasetamol saja (Mirzayan, 2006). Senyawa N-(4-hidroksifenil) asetamida
memiliki rumus molekul C8H9NO2 dengan bobot molekul 151,16 g/mol.
Parasetamol murni berupa serbuk kristal berwarna putih, tidak berbau, berasa
pahit, memiliki titik lebur 170°C. 1 gram parasetamol larut dalam 70 mL air
dingin, 20 mL air panas, 10 mL alkohol, 50 mL kloroform, 40 mL gliserin, dan
sedikit larut dalam eter (Remington, 2006).
Gambar 5. Struktur N-(4-hidorksifenil) asetamida (Remington, 2006)
Parasetamol dapat memberikan efek analgesik yang lebih baik jika
penggunaannya dikombinasikan dengan NSAIDs karena aktivitasnya dapat
berikatan dengan asam arakidonat yang merupakan substrat untuk membentuk
prostaglandin sehingga tidak dapat menempati sisi aktif enzim siklooksigenase
seperti ditunjukkan pada gambar 6. Disamping itu, adanya NSAIDs seperti
ibuprofen akan berikatan dengan sisi aktif enzim siklooksigenase sehingga enzim
tidak dapat merubah asam arakidonat menjadi prostaglandin yang merupakan
10
Gambar 6. Mekanisme aksi parasetamol (Lemke and Williams, 2012)
Parasetamol merupakan suatu senyawa fenolik karena pada strukturnya
terdapat gugusan hidroksil (-OH) yang terikat langsung pada suatu cincin
benzena. Dalam reaksinya, fenol tidak dapat teresterifikasi dengan asam asetat.
Suasana basa akan membuat fenol terionisasi, dimana ion fenoksida yang
terbentuk lebih reaktif fan dapat menyerang komponen elektrofilik yang ada.
Berbeda dengan suatu ion alkoksida, ion fenoksida dapat menstabilkan diri
melalui resonansi yang ditunjukkan pada gambar 7 (Murray, 1997).
11
C. Esterifikasi Yamaguchi
Metode Yamaguchi merupakan suatu metode esterifikasi yang merubah
asam karboksilat menjadi suatu anhidrida dengan suatu asil klorida. Seperti
ditunjukkan pada gambar 8, derivatisai asam karboksilat dibantu dengan
penggunaan basa amina yang akan men-deprotonasi asam karboksilat. Anhidrida
yang terbentuk akan direaksikan dengan dimethylaminopyridine (DMAP) sebagai
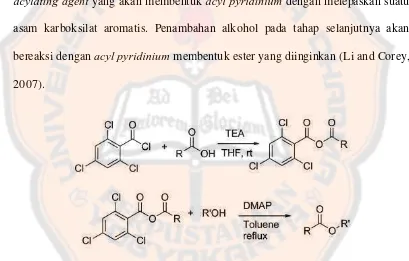
acylating agent yang akan membentuk acyl pyridinium dengan melepaskan suatu
asam karboksilat aromatis. Penambahan alkohol pada tahap selanjutnya akan
bereaksi dengan acyl pyridinium membentuk ester yang diinginkan (Li and Corey,
2007).
Gambar 8. Skema esterifikasi Yamaguchi (Dhimitruka and Lucia, 2005)
Esterifikasi Yamaguchi menggunakan reagen khas Yamaguchi yang
tidak lain adalah 2,4,6-trichlorobenzoyl chloride dengan katalis trietilamin (TEA)
dalam derivatisasi asam karboksilat menjadi suatu anhidrida (Dhimitruka and
Lucia, 2005). Reagen Yamaguchi tersebut dapat diganti dengan suatu asil klorida
lain yang lebih mudah didapat seperti benzoyl chloride. Mekanisme dari
12
nukleofil dan dilanjutkan dengan eliminasi klorida pada asil klorida yang
digunakan. Asam karboksilat akan bersifat sebagai nukleofil jika dikondisikan
dalam suasana basa (Starkey, 2012).
Gambar 9. Derivatisasi asam karboksilat menjadi anhidrida (Starkey, 2012)
Derivatisasi gugus karboksilat pada 2-(4-isobutilfenil) propanoat menjadi
suatu anhidrida akan meningkatkan reaktivitas sehingga substitusi nukleofilik oleh
N-(4-hidroksifenil) asetamida membentuk suatu ester akan lebih efektif. Tingkat
reaktivitas gugus pergi ditentukan oleh besarnya delokalisasi elektron terhadap
gugusan karbonil disebelahnya. Besarnya delokalisasi elektron yang terjadi dapat
ditentukan melalui pengukuran tingkat streching gugusan karbonil dengan
bantuan infra merah (Clayden, Greeves, and Warren, 2012).
Gambar 10. Frekuensi streching IR asam karboksilat dan derivatnya (Clayden dkk, 2012)
Kekuatan streching berdasarkan pengukuran infra merah digunakan
untuk menentukan kekuatan ikatan heteroatom terhadap suatu karbonil. Semakin
13
dengan karbonil, sehingga merupakan leaving group yang baik (Clayden dkk,
2012). Kekuatan leaving group juga dipengaruhi oleh perbedaan
elektronegatifitas, dimana semakin besar perbedaan elektronegativitas antara
heteroatom dengan karbonil maka atom C pada gugusan karbonil akan semakin
bersifat elektrofil (E+) sehingga substitusi nukleofilik oleh alkohol membentuk
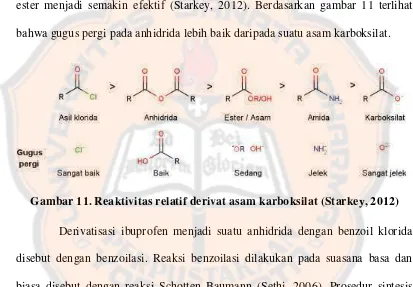
ester menjadi semakin efektif (Starkey, 2012). Berdasarkan gambar 11 terlihat
bahwa gugus pergi pada anhidrida lebih baik daripada suatu asam karboksilat.
Gambar 11. Reaktivitas relatif derivat asam karboksilat (Starkey, 2012)
Derivatisasi ibuprofen menjadi suatu anhidrida dengan benzoil klorida
disebut dengan benzoilasi. Reaksi benzoilasi dilakukan pada suasana basa dan
biasa disebut dengan reaksi Schotten Baumann (Sethi, 2006). Prosedur sintesis
dari metode Yamaguchi adalah dengan mencampurkan asam karboksilat dengan
2,4,6-trichlorobenzoyl chloride (1 equivalen) dan trietilamin (TEA) (1 equivalen)
yang diaduk pada suhu ruangan selama 20 menit. Penyaringan dan pengeringan
menggunakan gas nitrogen digunakan untuk mengisolasi anhidrida yang
terbentuk. Anhidrida yang terbentuk kemudian dilarutkan dan dicampur dengan
komponen alkohol (1-2 equivalen) dan DMAP (2-4 equivalen) untuk
14
E. Analisis Pendahuluan
Analisis pendahuluan merupakan analisis untuk mengetahui karakteristik
dari senyawa hasil reaksi. Analisis pendahuluan yang dilakukan antara lain:
1. Pemeriksaan Organoleptis
Organoleptis didefinisikan sebagai suatu hal yang dapat dirasakan oleh
satu atau lebih indra manusia. Pemeriksaan organoleptik menggunakan indra
penciuman, perasa, sentuhan, dan penglihatan (Bart, 2006). Pemeriksaan
organoleptik dapat digunakan untuk menarik kesimpulan awal menggunakan
indra manusia, dimana karakter yang dievaluasi meliputi: warna, bau, rasa,
ukuran, bentuk, dan beberapa hal khusus seperti tekstur (Kokate, Purohit, and
Gokhale, 2009).
2. Pemeriksaan Warna dengan FeCl3
Uji kualitatif berdasarkan perubahan warna padatan dapat digunakan
untuk pemeriksaan apakah molekul target sudah terbentuk dan telah bersih dari
N-(4-hidroksifenil) asetamida. Pemeriksaan warna yang dilakukan didasarkan
atas reaksi pembentukan kompleks antara N-(4-hidroksifenil) asetamida yang
merupakan senyawa fenolik dengan FeCl3. Reaksi antara senyawa fenolik yang
akan bereaksi dengan FeCl3 akan membentuk kompleks berwarna ungu sampai
biru, hijau bahkan merah tergantung dari struktur senyawa fenolik yang
15
Gambar 12. Reaksi fenol dengan FeCl3 (Sagar, 1996)
Suatu senyawa kompleks dapat berwarna karena adanya transisi elektron
dari ion pusat akibat adanya ligan. Fe3+ merupakan ion logam transisi trivalen
dengan orbital molekul paramagnetik. Bentuk orbital molekul dari Fe3+ adalah
oktahedral yang kompleks ikatannya melibatkan ikatan sigma atau ikatan pi
dengan ligan (Sahoo, Nayak, Samantarai, and Pujapanda, 2012).
3. Pemeriksaan Gas dengan Natrium Bikarbonat (NaHCO3)
Uji kualitatif menggunakan NaHCO3 digunakan untuk identifikasi
apakah molekul target sudah terbentuk dan telah bersih dari 2-(4-isobutilfenil)
propanoat. Gas yang terbentuk didasarkan atas reaksi effervesen antara
NaHCO3 dengan 2-(4-isobutilfenil) propanoat yang merupakan suatu asam
karboksilat seperti ditunjukkan pada gambar 13. Pengujian ini spesifik untuk
2-(4-isobutilfenil) propanoat, NaHCO3 tidak bereaksi dengan N-(4-hidroksifenil)
asetamida karena tetapan disosiasi senyawa fenolik lebih rendah sekitar 10-10
dibandingkan dengan asam karboksilat sekitar 10-6 sampai 10-5 (Sethi, 2006).
Gambar 13. Reaksi asam karboksilat dengan NaHCO3 (Ahluwalia and
16
Pengujian asam karboksilat dilakukan pada kondisi bebas alkohol, jika
alkohol digunakan sebagai pelarut maka perlu dilakukan uji pelarut sebagai
kontrol (Ahluwalia and Dhingra, 2004). Dalam pengujian penyusun tidak
melarutkan 2-(4-isobutifenil) propanoat. Pengujian dilakukan langsung pada
serbuk kristal 2-(4-isobutilfenil) propanoat dibandingkan dengan senyawa hasil
sintesis.
F. Pemurnian dan Pemeriksaan Kemurnian Senyawa Hasil Sintesis
1. Rekristalisasi
Rekristalisasi merupakan salah satu metode pemurnian yang sangat
efektif. Metode ini digunakan untuk memisahkan suatu senyawa yang terlarut
dalam sistem yang tidak murni dengan cara didinginkan pada suhu ruangan.
Ketika pendinginan, senyawa tersebut akan mengkristal keluar dari sistem
larutan dimana pengotor lainnya terlarut dalam sistem. Rekristalisasi harus
menggunakan pelarut yang tepat karena proses ini didasarkan atas tingkat
keterlarutan senyawa pada suhu pelarut yang digunakan (Bansal, 2003).
Rekristalisasi suatu padatan merupakan teknik yang umum dilakukan
dalam pemurnian. Padatan dilarutkan dengan pelarut yang sesuai pada suhu
dimana zat yang diinginkan terlarut didalam sistem, dan dengan adanya
pendinginan maka zat terlarut akan kembali mengkristal. Proses rekristalisasi
tidak dapat menjamin kemurnian terhadap suatu senyawa, sehingga perlu
17
pengotor berwarna (jika perlu) dan filtrasi untuk menghilangkan pengotor yang
tidak terlarut didalam sistem (Gilbert and Martin, 2010).
2. Pemeriksaan Titik Lebur
Titik lebur suatu senyawa didefinisikan sebagai temperatur dimana
padatan dan cairan berada pada titik kesetimbangan. Pada kondisi
kesetimbangan, temperatur pada sistem tidak berubah tetapi terjadi penyerapan
kalor (Ramanathan, 2006). Pemeriksaan titik lebur sangatlah penting dalam
identifikasi senyawa organik. Titik lebur suatu padatan ditentukan pada saat
pertama padatan tersebut mulai meleleh. Titik lebur juga menunjukkan
kemurnian suatu senyawa. Titik lebur senyawa yang akurat dapat ditentukan
dengan menggunakan termometer terkalibrasi (Ahluwalia and Dhingra, 2004).
Rentang titik lebur menjadi kriteria dalam penentuan kemurnian suatu
senyawa. Umumnya, suatu senyawa dikatakan murni apabila mempunyai
rentang titik lebur yang tidak melebihi 2°C (MacKenzie, 1967). Rentang titik
lebur dihitung dari temperatur awal ketika padatan mulai meleleh hingga
semua sampel padatan meleleh semua. Tingkat kemurnian senyawa dilihat dari
rentang titik leburnya, jika memiliki rentang titik lebur yang sangat tajam yaitu
tidak lebih dari 2°C maka senyawa tersebut murni (Ramanathan, 2006).
3. Kromatografi Lapis Tipis (KLT)
Kromatografi Lapis Tipis (KLT) adalah suatu metode analisis dimana
komponen fase gerak akan melewati fase diam sehingga campuran substansi
18
(KLT) mulai diperkenalkan pada tahun 1956 oleh E.Stahl, arti dari KLT itu
sendiri adalah pemisahan kromatografi yang terjadi pada suatu layer tipis yang
terdapat komponen padatan dan material pendukung yang disebut dengan fase
diam (Leach, 2007). Kromatografi Lapis Tipis (KLT) merupakan suatu teknik
pemisahan campuran senyawa yang mudah dan tidak mahal. Teknik
kromatografi ini biasa digunakan untuk memisahkan campuran senyawa
analgesik dengan menggunakan fase diam silika berfluoresensi dengan
menggunakan deteksi sinar UV (Pavia, Lampman, Kriz, and Engel, 2010).
Posisi atau bercak substrat (spot) pada lapisan Kromatografi Lapis Tipis
(KLT) dapat dideskripsikan sebagai retardation factor (Rf). Nilai retardation
factor (Rf) dihitung dari jarak titik tengah bercak dari titik awal, dengan nilai
retardation factor (Rf) selalu < 1 (Leach, 2007). Komponen fase diam yang
digunakan dalam penelitian ini adalah silika gel. Silika gel disiapkan melalui
presipitasi larutan sodium silicate (Na2SiO3). Lempeng KLT dengan silika gel
sebagai fase diam memiliki rata-rata ukuran pori antara 4-12 nm, dengan
konsentrasi gugus hidroksi (-OH) pada permukaan sekitar 8 µmol/m2, atau
sama dengan 5 gugus hidroksi (-OH) setiap mm2. Gypsum, pati, dan bahan
pengikat organik biasa digunakan sebagai campuuran silika gel sebagai
material pendukung (Spangenberg, Poole, and Weins, 2011).
Fase gerak yang digunakan dalam penelitian ini adalah etil asetat.
Penggunaan etil asetat didasarkan karena dapat memberikan resolusi
pemisahan yang bagus dalam memisahkan 2-(4-isobutilfenil) propanoat dan
19
diam silika gel GF 254 untuk 2-(4-isobutilfenil) propanoat yaitu 0,57 dan untuk
N-(4-hidroksifenil) asetamida yaitu 0,32 (Moffat, David, and Brian, 2011).
F. Elusidasi Struktur
Elusidasi stuktur merupakan teknik analisis suatu struktur senyawa.
Tahapan ini digunakan untuk identifikasi struktur senyawa hasil sintesis. Data
yang diperoleh dari elusidasi yang ditambah dengan berbagai macam uji kualitatif
yang dilakukan peneliti akan dapat menentukan struktur senyawa tersebut.
1. Spektrofotometri Inframerah (IR)
Spektrofotometri inframerah adalah teknik analisis spektrofotometri
tercepat dan termurah yang digunakan dalam kimia organik. Sampel dapat
berupa padatan, cairan, atau gas, dan dapat diukur dalam larutan dengan KBr
atau minyak mineral, kemudian spektra diperoleh dalam beberapa menit.
Identifikasi spektra inframerah menunjukkan gugus fungsi dari senyawa yang
dianalisis (Pavia dkk, 2010). Sampel yang akan dianalisis menggunakan
spektroskopi inframerah diletakkan pada material pendukung. Material standar
yang biasa digunakan sebagai material pendukung adalah kalium bromida
(KBr) dan barium fluorida (BaF2). Banyak material lain yang dapat digunakan
sebagai material pendukung, kalium bromida (KBr) merupakan material
pendukung yang biasa digunakan karena harganya yang relatif murah dan
dapat menyerap radiasi inframerah daerah tengah. Penggunaan kalium bromida
(KBr) sebagai material pendukung dapat memberikan informasi transmisi
20
Gugus karbonil dapat diidentifikasi berdasarkan spektra inframerah yang
diperoleh, dimana serapan pada frekuensi yang berbeda menunjukan gugus
fungsi yang berbeda pula:
Tabel I. Frekuensi Inframerah Gugus Karbonil (Cotes, 2000)
Frekuensi (cm-1) Gugus fungsional
1610-1550 Garam asam karboksilat
1680-1630 Amida
1690-1675 Kuinon atau keton terkonjugasi
1725-1700 Asam karboksilat
1725-1705 Keton
1740-1725 Adehida
1750-1725 Ester
1735 Lakton cincin segi enam
1760-1740 Alkil karbonat
1815-1770 Asil halida
1820-1775 Aril karbonat
1850-1800 / 1790-1740 Anhidrida asam rantai terbuka 1870-1820 / 1800-1775 Anhidrida cincin segi lima
2100-1800 Metal karbonil
Pada penelitian ini dilakukan derivatisasi 2-(4-isobutilfenil) propanoat
menjadi anhidrida dengan benzoil klorida. Sehingga interpretasi pita absorbsi
spesifik untuk indetifikasi terletak pada ester benzoat dengan daerah absorbsi
1730 – 1715 cm-1, spesifikasi untuk anhidrida asiklik terkonjugasi terletak pada
daerah 1775 – 1720 cm-1. Sementara untuk senyawa target, interpretasi pita
absorbsi untuk identifikasi terletak pada adanya gugusan amida pada
N-(4-hidroksifenil) asetamida. Pita absorbsi gugusan amida tumpang tindih dengan
gugusan karbonil yaitu pada daerah sekitar 1640 cm-1 (Silverstein, Francis,
21
G. Landasan Teori
Esterifikasi merupakan reaksi antara suatu alkohol dengan asam
karboksilat. Metode esterifikasi yang digunakan berdasarkan prinsip esterifikasi
Yamaguchi yaitu dengan derivatisasi asam karboksilat menjadi anhidrida.
Derivatisasi 2-(4-isobutilfenil) propanoat menggunakan benzoil klorida dengan
katalis piridina akan membentuk benzoil 2-(4-isobutilfenil) propanoat anhidrat
yang bertujuan untuk meningkatkan elektrofilisitas gugusan karbonil. benzoil
2-(4-isobutilfenil) propanoat anhidrat yang terbentuk akan direaksikan dengan
N-(4-hidroksifenil) asetamida yang merupakan senyawa golongan alkohol. Reaksi
antara N-(4-hidroksifenil) asetamida dengan derivat 2-(4-isobutilfenil) propanoat
berlangsung dalam suasana basa menggunakan katalis natrium hidroksida (NaOH)
dalam etanol membentuk 4-asetamidofenil 2-(4-isobutilfenil) propanoat.
Gambar 14. Reaksi umum sintesis senyawa 4-asetamidofenil 2-(4-isobutilfenil) propanoat
H. Hipotesis
Senyawa 4-asetamidofenil 2-(4-isobutilfenil) propanoat dapat disintesis
22
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian yang berjudul “Sintesis senyawa 4-asetamidofenil
2-(4-isobutilfenil) propanoat dari 2-(4-2-(4-isobutilfenil) propanoat dan
N-(4-hidroksifenil) asetamida” merupakan penelitian non-eksperimental deskriptif
non analitik karena pada penelitian ini tidak diberikan perlakuan pada subjek uji
dan hanya dipaparkan peristiwa yang terjadi sehingga tidak terdapat hubungan
sebab akibat didalamnya.
B. Definisi Operasional
1. Starting Material merupakan bahan awal yang digunakan dalam proses sintesis
4-asetamidofenil 2-(4-isobutilfenil) propanoat. Starting material yang
digunakan dalam penelitian yaitu 2-(4-isobutilfenil) propanoat dan
N-(4-hidroksifenil) asetamida.
2. Katalis adalah suatu senyawa yang digunakan dalam reaksi kimia yang
berfungsi mempercepat suatu reaksi dengan menurunkan energi aktivasinya.
3. Molekul target adalah molekul yang menjadi target dan diharapkan terbentuk
dari suatu proses sintesis. Senyawa yang diharapkan terbentuk adalah senyawa
23
4. Penimbangan hingga bobot tetap adalah berat pada penimbangan setelah zat
dikeringkan selama satu jam tidak berbeda lebih dari 0,5 mg/gram dari berat
zat pada penimbangan sebelumnya.
5. Rendemen senyawa hasil sintesis merupakan perbandingan antara jumlah
senyawa yang diperoleh dari hasil sintesis (aktual) dibandingkan dengan
jumlah senyawa yang didapatkan secara teoritis.
C. Bahan Penelitian
Bahan-bahan yang digunakan antara lain: N-(4-hidroksifenil) asetamida
(pharmaceutical grade, Bratachem), 2-(4-isobutilfenil) propanoat (technical
grade, Bratachem), piridin (p.a., Merck), benzoil klorida (p.a., Merck), natrium
hidroksida (p.a., Merck), etanol absolut (p.a., Merck), tetrahidrofuran (p.a.,
Merck), toluena (p.a., Merck), aquadest (Laboratorium Kimia Organik
Universitas Sanata Dharma), etil asetat (p.a., Merck), aseton (p.a., Merck).
D. Alat Penelitian
Alat-alat yang digunakan meliputi: Neraca analitik (Mextler PM 100),
oven (Memmert Oven Model 400), pendingin alihn, alat-alat gelas, alat pengukur
titik lebur/melting point tester (MP70, Mettler Tolledo), sendok, galssfirn, kertas
saring, mikropipet, chamber kaca, lampu UV254, oven, lempeng KLT, baskom,
24
E. Prosedur Penelitian
1.Rekritalisasi 2-(4-isobutilfenil) propanoat
2-(4-isobutilfenil) propanoat ditimbang 10 gram menggunakan alas
kertas timbang. Dilarutkan dengan 80 mL etanol 96% dan diaduk menggunakan
magnetic stirer pada suhu ± 60°C selama 15 menit. Kemudian disaring
menggunakan corong Buchner dan pompa vakum yang telah dihangatkan. Filtrat
didinginkan dalam kulkas selama 24 jam. Kristal yang terbentuk disaring
kemudian dikeringkan dalam oven pada suhu ± 40°C selama 24 jam.
2. Rekristalisasi N-(4-hidroksifenil) asetamida
N-(4-hidroksifenil) asetamida dilarutkan hingga jenuh dalam etanol 96%
sebanyak 80 mL. Kemudian disaring menggunakan corong Buchner dan pompa
vakum. Filtrat didinginkan dalam kulkas selama 24 jam. Kristal yang terbentuk
disaring kemudian dikeringkan dalam oven pada suhu ± 40°C selama 24 jam.
3. Sintesis 4-asetamidofenil 2-(4-isobutilfenil) propanoat
a. Pembuatan larutan NaOH/etanol 0,1 N
Pelet NaOH ditimbang 800,0 mg menggunakan alas gelas arloji
kemudian dilarutkan dengan sedikit etanol absolut. Dituang kedalam labu
ukur 200 mL, ditambahkan etanol absolut hingga tanda lalu dilakukan
25
b. Derivatisasi 2-(4-isobutilfenil) propanoat
Kristal 2-(4-isobutilfenil) propanoat ditimbang lebih kurang 825,12
mg (4 mmol) menggunakan alas kertas timbang. Dituang ke dalam labu
alas datar lalu dilarutkan dalam 10 mL tetrahidrofuran (THF) dengan
bantuan 420 µL piridin. Diaduk menggunakan magnetic stirer selama 10
menit pada suhu ruangan. Ditambahkan 512 µL benzoil klorida, kemudian
dilanjutkan pengadukan selama 20 menit pada suhu ruangan.
c. Sintesis senyawa target
Endapan yang terbentuk hasil derivatisasi 2-(4-isobutilfenil)
propanoat dipisahkan dari sistem cairan dengan cara didekantir. Pada
tempat lain, kristal N-(4-hidrosifenil) asetamida sebanyak 604,64 mg (4
mmol) dilarutkan menggunakan 40 mL NaOH/etanol 0,1 N. Larutan
dimasukkan ke dalam labu alas datar tersebut, lalu dilanjutkan pengadukan
selama 24 jam pada suhu ruangan. Padatan yang terbentuk disaring
menggunakan kertas saring yang telah dijenuhkan dengan etanol. Padatan
kemudian dicuci dengan etanol dan dilakukan analisis KLT pada etanol
pencuci untuk mengetahui kemurnian senyawa hasil sintesis. Pencucian
dengan etanol dilakukan kembali jika senyawa hasil sintesis belum murni
dari starting material. Padatan yang telah murni kemudian dikeringkan
dalam oven pada suhu ± 40°C hingga bobot tetap dan dihitung
rendemennya, dilakukan replikasi sebanyak tiga kali dan dihitung
26
4. Analisis Senyawa Hasil Sintesis
a. Uji organoleptis
Dilakukan pengamatan bentuk, warna, dan bau dari senyawa hasil
dan dibandingkan dengan starting material yang digunakan.
b. Uji warna dengan FeCl3
Sejumlah kecil senyawa hasil sintesis ditempatkan dalam cawan
arloji, lalu diteteskan FeCl3 dan diamati ada tidaknya perubahan warna
yang terjadi. Hasil pengujian dibandingkan dengan pengujian pada
N-(4-hidrosifenil) asetamida.
c. Uji gas dengan natrium bikarbonat (NaHCO3)
Sejumlah kecil senyawa hasil sintesis ditempatkan dalam tabung
reaksi, lalu ditambahkan ± 5 mL larutan natrium bikarbonat 10 % b/v dan
diamati ada tidaknya gelembung gas yang muncul. Hasil pengujian
dibandingkan dengan pengujian pada 2-(4-isobutilfenil) propanoat.
d. Uji titik lebur
Sejumlah kecil senyawa hasil sintesis diisikan kedalam
electrothermal capillary tubes, dimasukkan dalam alat pengukur titik
lebur, diamati peleburan kristalnya dan dicatat suhu waktu pertama kali
melebur hingga kristal melebur semua. Hasil pengukuran kemudian
dibandingkan dengan hasil pengukuran titik lebur pada starting material
27
e. Uji Kromatografi Lapis Tipis (KLT)
Senyawa hasil sintesis dan starting material dilarutkan dalam
etanol. Masing-masing larutan tersebut ditotolkan pada lempeng silika gel
GF254 sebanyak 3 µL menggunakan pipa kapiler. Lempeng silika yang
akan digunakan diaktifkan terlebih dahulu pada suhu 110°C selama 30
menit. Elusi dilakukan dengan fase gerak etil asetat (100%) dengan jarak
elusi 10 cm. Bercak diamati dibawah sinar UV 254 nm, lalu dihitung nilai
Rf untuk masing-masing bercak.
5. Elusidasi Struktur Senyawa Hasil Sintesis
a. Spektrofotometri IR
Senyawa hasil sintesis sebanyak ± 0,5-1 mg dicampur dengan ± 10
mg KBr hingga homogen. Campuran tersebut kemudian dikempa menjadi
tablet. Cahaya inframerah kemudian dilewatkan pada cuplikan. Cahaya
tersebut akan dipecah menjadi frekuensi individunya oleh monokromator.
Intensitas relatif dari individu tersebut terukur pada detektor hingga
didapat spektra inframerah senyawa yang bersangkutan.
F. Analisis Hasil
1. Perhitungan Rendemen
Perhitungan rendemen senyawa hasil sintesis yang telah dimurnikan
dengan membandingkan bobot tetap senyawa hasil sintesis dengan bobot
28
% rendemen =
x 100%
2. Analisis Pendahuluan
Analisis pendahuluan senyawa hasil sintesis didasarkan pada data
organoleptis, uji warna dengan FeCl3, dan uji gas dengan natrium bikarbonat
(NaHCO3).
3. Pemeriksaan Kemurnian Senyawa Hasil Sintesis
Analisis kemurnian senyawa dilakukan didasarkan pada data uji titik
leleh dan uji kromatografi lapis tipis (KLT).
4. Elusidasi Struktur
Elusidasi struktur dari senyawa hasil sintesis didasarkan pada data
29
BAB IV
HASIL DAN PEMBAHASAN
A. Sintesis 4-asetamidofenil 2-(4-isobutilfenil) propanoat
Sintesis 4-asetamidofenil isobutilfenil) propanoat dari
2-(4-isobutilfenil) propanoat dan N-(4-hidroksifenil) asetamida didasarkan atas prinsip
reaksi esterifikasi Yamaguchi, yaitu dengan melakukan derivatisasi
2-(4-isobutilfenil) propanoat yang merupakan suatu asam karboksilat menjadi
anhidrida untuk meningkatkan reaktivitas atom C karbonil (C=O). Peneliti
melakukan derivatisasi karena N-(4-hidroksifenil) asetamida sulit untuk bereaksi
dengan 2-(4-isobutilfenil) propanoat mengingat reaktivitas 2-(4-isobutilfenil)
propanoat yang lemah.
Gambar 15. Aktivasi gugus karboksilat 2-(4-isobutilfenil) propanoat
Suatu anhidrida lebih reaktif dibandingkan asam karboksilat karena
elektrofilisitas atom C pada C karbonil (C=O) yang lebih besar pada anhidrida
dibandingkan asam karboksilat. Berdasarkan analisis muatan (charge)
menggunakan MarvinSketch 5.2.5.1, didapatkan bahwa muatan atom C pada C
30
karboksilat sebesar 0,15. Elektrofilisitas yang semakin besar akan memudahkan
esterifikasi oleh N-(4-hidroksifenil) asetamida membentuk senyawa target.
Gambar 16. Analisis muatan 2-(4-isobutilfenil) propanoat
Gambar 17. Analisis muatan 2-(4-isobutilfenil) propanoat terderivatiasi
Anhidrida yang terbentuk akan segera mengendap didalam pelarut yang
digunakan (THF). Tetrahidrofuran (THF) digunakan sebagai pelarut karena
sifatnya yang inert atau tidak menimbulkan reaksi samping dengan benzoil
klorida dan 2-(4-isobutilfenil) propanoat yang digunakan. Endapan yang terbentuk
kemudian dipisahkan dari sistem dengan cara dekantasi. Pemisahan endapan tidak
menggunakan teknik filtrasi karena sifat anhidrida yang higroskopis, sehingga
tidak adanya tetrahidrofuran (THF) yang melapisi padatan akan menyebabkan
padatan kontak dengan udara lembab yang akan membuat endapan melebur dan
31
Proses sintesis dilanjutkan dengan menambahkan N-(4-hidroksifenil)
asetamida yang dilarutkan dalan NaOH/etanol 0,1 M. Larutan tersebut kemudian
dicampurkan dengan derivat 2-(4-isobutilfenil) propanoat yang telah bebas dari
pelarut (THF). Penggunaan katalis basa (NaOH) dalam proses sintesis akan
mengionisasi gugus fenolik pada N-(4-hidroksifenil) asetamida menjadi ion
fenoksida sehingga lebih reaktif karena adanya kelebihan pasangan elektron
bebas.
Gambar 18. Aktivasi N-(4-hidroksifenil) asetamida
Pemilihan NaOH sebagai katalis reaksi juga disebabkan karena
esterifikasi dalam suasana basa akan memberikan banyak keuntungan
dibandingkan esterifikasi dalam suasana asam, diantaranya waktu reaksi yang
lebih singkat dan dapat berlangsung pada temperatur dan tekanan yang rendah.
Mengingat senyawa target berupa ester yang rentan mengalami hidrolisis karena
adanya air, pelarut yang digunakan untuk melarutkan NaOH adalah etanol. Etanol
digunakan karena dapat melarutkan derivat 2-(4-isobutilfenil) propanoat dan
N-(4-hidroksifenil) asetamida. Pemilihan etanol sebagai pelarut juga disebabkan
karena kemampuan solvolytic yang lebih kecil dibandingkan air. Berdasarkan
32
konstanta laju solvolisis dari air lebih besar dibandingkan etanol pada temperatur
yang sama.
Proses sintesis dilakukan selama 24 jam pada suhu ruangan dan disimpan
didalam kulkas selama 24 jam untuk mengoptimalkan endapan yang didapat
karena pada dasarnya kelarutan suatu senyawa akan berkurang pada suhu rendah.
Endapan yang terbentuk kemudian disaring dan dicuci menggunakan etanol untuk
memurnikan senyawa hasil sintesis dari N-(4-hidroksifenil) asetamida. Rata-rata
rendemen hasil sintesis yang didapatkan sedikit, yaitu sekitar 15,8 %. Hal tersebut
disebabkan karena perbedaan muatan C karbonil (C=O) dengan substituen pada
anhidrida lebih kecil dibandingkan dengan senyawa target.
Gambar 19. Analisis muatan 4-asetamidofenil 2-(4-isobutilfenil) propanoat
Perbedaan muatan pada senyawa target menunjukkan 0,43 (gambar 19),
sedangkan perbedaan muatan pada derivat 2-(4-isobutilfenil) propanoat
menunjukkan 0,38 (gambar 17). Semakin besar perbedaan muatan maka senyawa
tersebut akan semakin tidak stabil karena kemampuan leaving group yang
semakin besar. Oleh karena itu, substitusi oleh N-(4-hidroksifenil) asetamida
menjadi sulit berlangsung karena perbedaan muatan yang lebih besar pada
33
Sedikitnya rendemen yang didapatkan juga diakibatkan adanya stabiliasi
resonansi ion fenoksida pada N-(4-hidroksifenil) asetamida. Suatu anhidrida dapat
bereaksi dengan senyawa fenolik membentuk suatu ester walaupun reaktifitas
fenolik yang sangat lemah. Adanya stabilisasi resonansi elektron bebas pada atom
O yang disebarkan pada cincin benzena akan menurunkan nukleofilisitas
N-(4-hidroksifenil) asetamida.
Gambar 20. Analisis muatan etil 2-(4-isobutilfenil) propanoat
Penggunaan etanol sebagai pelarut tidak berpengaruh terhadap
banyaknya rendemen yang didapat walaupun etanol juga memungkinkan untuk
bereaksi dengan anhidrida membentuk ester yang lain. Berdasarkan gambar 20,
perbedaan muatan antara atom C karbonil (C=O) dengan substituen yang lebih
besar yaitu 0,58 dibandingkan senyawa target yaitu 0,43 sehingga etanol akan
semakin sulit untuk bereaksi dengan derivat 2-(4-isobutilfenil) propanoat
dibandingkan N-(4-hidroksifenil) asetamida. Selain itu, terjadinya reaksi samping
membentuk etil 2-(4-isobutilfenil) propanoat justru memudahkan substitusi oleh
N-(4-hidroksifenil) asetamida membentuk senyawa target mengingat perbedaan
muatan etil 2-(4-isobutilfenil) propanoat yang lebih besar dibandingkan senyawa
34
Gambar 21. Mekanisme reaksi derivatisasi 2-(4-isobutilfenil) propanoat
35
B. Analisis Senyawa Hasil Sintesis
1. Uji organoleptis
Hasil pemeriksaan organoleptis meliputi bentuk, warna, dan bau senyawa
hasil sintesis dibandingkan dengan starting material, yaitu 2-(4-isobutilfenil)
propanoat dan N-(4-hidroksifenil) asetamida ditunjukkan pada tabel II.
Tabel II. Data organoleptis senyawa hasil sintesis dan starting material
Pemerian N-(4-hidroksifenil)
Bentuk Serbuk kristal Serbuk kristal Serbuk
Warna Putih Putih Putih
Bau Tidak berbau Tidak berbau Tidak berbau
Dari hasil pemeriksaan, didapatkan bahwa senyawa hasil sintesis
memiliki profil organoleptis yang sama dengan starting material dalam hal warna
dan bau. Sehingga berdasarkan pemeriksaan organoleptis belum dapat
disimpulkan bahwa senyawa hasil sintesis telah terbentuk karena memiliki profil
organoleptis yang sama dengan starting material.
2. Uji warna dengan FeCl3
Uji warna menggunakan FeCl3 dilakukan kepada senyawa hasil sintesis
dibandingkan dengan N-(4-hidroksifenil) asetamida. Perubahan warna yang
36
yang merupakan senyawa fenolik membentuk kompleks warna berwarna ungu.
Hasil uji ditunjukkan pada tabel III.
Tabel III. Data uji warna dengan FeCl3
Keterangan N-(4-hidroksifenil)
asetamida Senyawa hasil sintesis
Sebelum penambahan FeCl3
Setelah penambahan FeCl3
Warna Ungu kehitaman Kuning
Berdasarkan hasil pengujian, dapat disimpulkan bahwa senyawa hasil
sintesis telah murni dari N-(4-hidroksifenil) asetamida karena tidak terjadi
perubahan warna menjadi ungu kehitaman seperti yang terlihat pada
N-(4-hidroksifenil) asetamida. Selain itu, tidak terjadinya perubahan warna menjadi
ungu menunjukkan bahwa senyawa hasil sintesis bukan merupakan
N-(4-hidroksifenil) asetamida dan tidak terdapat gugus fenolik.
3. Uji gas dengan natrium bikarbonat (NaHCO3)
Uji gas menggunakan NaHCO3 dilakukan kepada senyawa hasil sintesis
37
muncul didasarkan atas reaksi antara NaHCO3 dengan 2-(4-isobutilfenil)
propanoat yang merupakan suatu asam karboksilat melepaskan gas CO2. Hasil
pengujian ditunjukkan pada tabel IV.
Tabel IV. Data uji gas dengan natrium bikarbonat (NaHCO3)
Keterangan 2-(4-isobutilfenil)
propanoat Senyawa hasil sintesis
Gambar
Pengamatan Terdapat buih gas CO2 Tidak muncul gas CO2
Berdasarkan hasil pengujian, dapat disimpulkan bahwa senyawa hasil
sintesis telah murni dari 2-(4-isobutilfenil) propanoat karena tidak terjadi muncul
gelembung gas CO2 seperti yang terjadi pada 2-(4-isobutilfenil) propanoat. Selain
itu, tidak munculnya buih atau gas CO2 menunjukkan bahwa senyawa hasil
sintesis bukan merupakan 2-(4-isobutilfenil) propanoat dan tidak terdapat gugus
karboksil.
4. Uji titik lebur
Pengujian titik lebur dilakukan terhadap senyawa hasil sintesis.
Pengujian titik lebur dilakukan mulai dari suhu 40°C - 300°C untuk replikasi I, II,
dan III senyawa hasil sintesis. Berdasarkan hasil pengujian, diperoleh titik lebur
38
Tabel V. Data titik lebur senyawa hasil sintesis dan starting material
Senyawa Titik lebur
N-(4-hidroksifenil) asetamida 170°C 2-(4-isobutilfenil) propanoat 77°C Replikasi I senyawa hasil sintesis - Replikasi II senyawa hasil sintesis - Replikasi III senyawa hasil sintesis -
Dari hasil pengujian, dapat ditarik kesimpulan bahwa senyawa hasil
sintesis sudah bukan starting material yaitu N-(4-hidroksifenil) asetamida dan
2-(4-isobutilfenil) propanoat dan memiliki titik lebur lebih dari 300°C.
5. Uji kromatografi lapis tipis (KLT)
Uji dengan kromatografi lapis tipis (KLT) bertujuan untuk identifikasi
kualitatif apakah senyawa hasil sintesis telah. Senyawa hasil sintesis ditotolkan
pada plat KLT silika gel GF254 bersama dengan starting material yaitu
N-(4-hidroksifenil) asetamida dan 2-(4-isobutilfenil) propanoat lalu dielusikan
menggunakan fase gerak etil asetat. Pelarut yang digunakan adalah etanol baik
untuk starting material dan senyawa hasil sintesis. Parameter yang digunakan
adalah Rf untuk masing-masing bercak senyawa yang ditotolkan. Rf merupakan
perbandingan jarak bercak dengan jarak elusi dari titik awal penotolan. Jika hasil
elusi menunjukkan adanya perbedaan nilai Rf maka dapat dikatakan bahwa
senyawa hasil sintesis telah terbentuk. Uji Kromatografi Lapis Tipis (KLT) juga
dapat digunakan untuk identifikasi kemurnian dari senyawa hasil sintesis dengan
meliihat ada tidaknya bercak dengan Rf yang sama pada starting material. Berikut
hasil analisis Kromatografi Lapis Tipis (KLT) dan data Rf ditunjukkan dengan
39
Gambar 23. KLT senyawa hasil sintesis pada fase gerak etil asetat
Keterangan :
Fase diam : silika gel GF254 Jarak elusi : 10 cm
Fase gerak : etil asetat Deteksi : UV 254 nm
Tabel VI. Nilai Rf analisis KLT senyawa hasil sintesis
Bercak Senyawa Rf
IBU 2-(4-isobutilfenil) propanoat 0,62
PCT N-(4-hidroksifenil) asetamida 0,40
R-I Pelarut replikasi I senyawa hasil sintesis - R-II Pelarut replikasi II senyawa hasil sintesis - R-III Pelarut replikasi III senyawa hasil sintesis -
Berdasarkan hasil analisis KLT, didapatkan bahwa totolan starting
material menghasilkan bercak tunggal dibawah sinar UV 254 nm. Sementara pada
senyawa hasil sintesis tidak didapatkan bercak, sehingga dapat disimpulkan
bahwa senyawa hasil sintesis telah murni dari starting material dan bukan
40
disebabkan karena senyawa hasil sintesis tidak terlarut dalam etanol, sehingga
analisis KLT digunakan untuk mengetahui kemurnian dari senyawa hasil sintesis
mengingat 2-(4-isobutilfenil) propanoat dan N-(4-hidroksifenil) asetamida sebagai
starting material larut dalam etanol.
C. Elusidasi Struktur Senyawa Hasil Sintesis
1. Spektrofotometri infra merah 2-(4-isobutilfenil) propanoat terderivatisasi
Spektrofotometri infra merah digunakan untuk mengetahui gugus
fungsional yang terdapat dalam senyawa uji. Setiap senyawa memiliki spektra IR
yang berbeda karena transisi elektron yang terjadi akan terkait dengan perubahan
vibrasi didalam molekul. Untuk memastikan apakah derivatisasi
2-(4-isobutilfenil) propanoat telah berlangsung, maka penyusun melakukan analisis
terhadap anhidrida yang terbentuk dan ditunjukkan pada gambar dibawah ini.
41
Spektra IR yang diperoleh menunjukkan adanya pita representatif dengan
gugus-gugus fungsi yang terdapat pada struktur derivat 2-(4-isobutilfenil)
propanoat. Gugus aromatik ditunjukkan dengan adanya serapan disebelah kiri
3000 cm-1 yaitu pada 3055,24 cm-1. Gugus gem-dimetil ditunjukkan dengan
adanya serapan doublet dengan intensitas yang hampir sama pada daerah sekitar
1385-1380 cm-1 yaitu 1381,03 cm-1 dengan intensitas 30,74 dan 1319,31 cm-1
dengan intensitas 30,78. Gugus C-H alkana ditunjukkan dengan adanya serapan
pada daerah 3000-2840 cm-1 yaitu pada 2924,09 cm-1. Gugus C-H alkena
ditunjukkan dengan adanya serapan pada daerah didekat 1416 cm-1 (
scissoring
in-plane) yaitu 1458,18 cm-1, serapan pada daerah 970 cm-1 dan 650 cm-1
(trans-bending out of plane) yaitu 948,98 cm-1 dan 671,23 cm-1 serta serapan pada daerah
sekitar 700 cm-1
(cis-bending out of plane) yaitu 779,24 cm-1. Gugus ester
ditunjukkan dengan adanya serapan kuat pada daerah 1300 – 1000 cm-1 yaitu pada
1080,14 cm-1.
Gambar 25. Identifikasi gugus fungsi derivat 2-(4-isobutilfenil) propanoat
Spesifik untuk senyawa derivat 2-(4-isobutilfenil) propanoat adanya
42
yaitu adanya serapan pada daerah 1775-1720 cm-1 yang ditunjukkan pada 1720,50
cm-1. Berikut interpretasi spektra infra merah derivat 2-(4-isobutilfenil) propanoat:
Tabel VII. Interpretasi spektra IR derivat 2-(4-isobutilfenil) propanoat
Gugus fungsional Bilangan
gelombang (cm-1) Intensitas
Gugus aromatik 3055,24 Medium, melebar
Gugus C-H alkana 2924,09 Medium, tajam
Gugus anhidrida asiklik terkonjugasi 1720,50 Lemah, tajam Gugus C-H alkena (scissoring in-plane) 1458,18 Lemah, tajam
Gugus gem-dimetil 1381,03 Lemah, tajam
1319,31 Lemah, tajam
Gugus ester (C-O) 1080,14 Medium, melebar
Gugus C-H alkena (trans –bending out of plane)
2. Spektrofotometri infra merah senyawa hasil sintesis
Spektra IR yang diperoleh menunjukkan adanya pita representatif dengan
gugus-gugus fungsi yang terdapat pada struktur senyawa hasil sintesis. Gugus
fungsional spesifik yang menunjukkan apakah senyawa hasil sintesis telah
terbentuk adalah adanya gugusan amida yang tidak terdapat pada derivat
2-(4-isobutilfenil) propanoat.
43
Gambar 27. Spektra IR Senyawa Hasil Sintesis (pelet KBr)
Gugus karbonil terdapat pada daerah 1850 – 1650 cm-1 yang ditunjukkan
pada 1851,66 cm-1. Intensitas gugus karbonil dari senyawa hasil sintesis tidak kuat
seperti derivat 2-(4-isobutilfenil) propanoat disebabkan karena adanya gugus
pendonor elektron disamping gugus karbonil yang memicu terjadinya resonansi
sehingga intensitasnya berkurang.
Gambar 28. Resonansi derivat 2-(4-isobutilfenil) propanoat