BIOSORPSI ZAT PEWARNA TEKSTIL METHYL ORANGE MENGGUNAKAN AMPAS TEH
TUGAS AKHIR
Oleh:
DEVINA 140407042
Pembimbing
Prof. Dr. Ir. Muhammad Turmuzi, M. S.
PROGRAM STUDI TEKNIK LINGKUNGAN FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA MEDAN
2019
TA/TL-USU/2019/125
BIOSORPSI ZAT PEWARNA TEKSTIL METHYL ORANGE MENGGUNAKAN AMPAS TEH
TUGAS AKHIR
Oleh:
DEVINA 140407042
TUGAS AKHIR INI DIAJUKAN UNTUK MELENGKAPI SEBAGIAN PERSYARATAN MENJADI SARJANA TEKNIK
PROGRAM STUDI TEKNIK LINGKUNGAN FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA MEDAN
2019
Saya menyatakan dengan sesungguhnya bahwa tugas akhir dengan judul:
BIOSORPSIZAT
PEWARNA TEKSTTLMETI{YL
ORANGEMENGGUNAKAN
AMPASTEH
Dibuat rmtuk melengkapi sebagian persyaratan menjadi Sarjana Teknik pada Program Studi Teknik Ungkungar Fakultas Teknik Universitas Sumatera Utara. Tugas alfuir ini adalah hasil krya mya kecuali kutipan{<utipan yang telah saya sebutkan sumbernya.
Dernikian persyratan ini dibuat, apabita dikemudian hari terbukti bahwa karya ini bukan karya saya atau merupakan hasil jiplakan maka saya bersedia menerima sanksi sesuai dengan af.ran yang berlaku.
NrM. 140407042 lv{edfin, April2019
DEVINA
IIALAMAN
PENGESAHANTugas akhir dengan judul:
BIOSORPSI
ZAT
PEWARNATEKSTIL METHYL
ORANGEMENGGUNAKAN
AMPASTEH
Dibuat untuk melengkapi persyaratan menjadi Sarjana Teknik pada Program Studi Teknik Lingkungan Fakultas Teknik Universitas Sumatera Utara. Tugas Akhir ini telah diujikan pada Sidang Tugas Akhir pada 07 Febnrari 2019 dan dinyatakan telah memenuhi ryaraVsah sebagai Tugas Akhir pada Progpuu Sfudi Teknik Lingkungan Fakultas Teknik Universitas Sumatcra Uara.
April2019
Dosen Penguji I
k. Netti Herlina. M.T.
NIP. 19680425 199903 2A04
Mengotahui,
KetuaProgram Studi
oa
Dosen Penguji IIW4a
Dr. Amir Husin. S.T.. M.T.
NIP. 19690215 199512
l00l
Isa' Survati" S.T.. M.Si.
NrP. 19790622 201404 2 0A1 Menyetujui,
or Tugas Akhir
NrP. r968M2s 199903 20A4
ABSTRAK
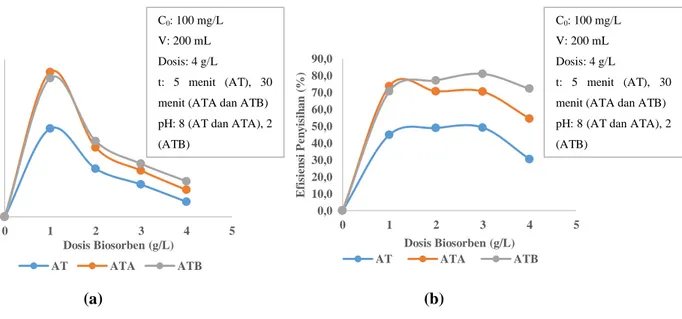
Penggunaan zat pewarna tekstil pada berbagai industri cukup meningkat selama beberapa tahun terakhir. Salah satu zat pewarna tekstil yang banyak digunakan adalah Methyl Orange. Methyl Orange berbahaya karena merupakan zat pewarna azo karsinogenik yang dapat terlarut dalam air dan merupakan zat pewarna yang paling reaktif dalam proses pencelupan bahan tekstil. Salah satu metode penyisihan zat pewarna tekstil adalah biosorpsi. Pada penelitian ini digunakan tiga jenis biosorben untuk menyisihkan zat pewarna tersebut dengan proses batch, yaitu ampas teh (AT), ampas teh dengan pencucian senyawa asam HNO3 (ATA) dan ampas teh dengan pencucian senyawa basa KOH (ATB). Biosorben dikarakterisasi dengan pengujian SEM-EDS dan daya serap iodin. Tujuan penelitian ini adalah untuk mengkaji kemampuan biosorben dalam penyisihan zat pewarna methyl orange dan kondisi optimal yang diperlukan, serta menentukan model kinetika adsorpsi dan isoterm adsorpsi yang sesuai untuk menggambarkan proses biosorpsi yang terjadi. Model kinetika adsorpsi yang digunakan adalah Orde Pertama Semu dan Orde Kedua Semu, sedangkan untuk isoterm adsorpsi dilakukan analisa menggunakan isoterm adsorpsi Langmuir dan Freundlich. Variabel penelitian terdiri dari pengaruh waktu kontak (0, 5, 30, 60 dan 90 menit), pH (2, 5, 8, 11) dan dosis biosorben (1 g/L, 2 g/L, 3 g/L dan 4 g/L). Dari ketiga biosorben, ATB merupakan biosorben terbaik untuk menyisihkan zat pewarna methyl orange dengan kondisi optimum waktu kontak selama 30 menit, pH awal limbah cair sintesis 2 dan dosis sebesar 3 g/L ATB dalam 200 mL limbah cair sintesis. Efisiensi penyisihan yang dicapai adalah sebesar 80,99%. Efisiensi penyisihan tertinggi yang dicapai oleh biosorben AT dan ATA secara berturut-turut adalah 49,20% (Waktu kontak selama 5 menit, pH awal limbah cair sintesis 8 dan dosis biosorben sebesar 3 g/L) dan 73,75% (Waktu kontak selama 30 menit, pH awal limbah cair sintesis 8 dan dosis biosorben sebesar 1 g/L). Model kinetika adsorpsi yang sesuai adalah Orde Kedua Semu dan isoterm adsorpsi yang tepat untuk menggambarkan proses yang terjadi adalah isoterm Langmuir.
Kata kunci: biosorpsi, methyl orange, ampas teh
ABSTRACT
The usage of textile dye in various industries has been increasing in recent years. One of the most widely used dye is Methyl Orange. Methyl Orange is dangerous because it is a carcinogenic azo dye which can dissolve in water and is the most reactive dye in textile material dyeing process. One of many textile dye removal methods is biosorption. In this research, three types of biosorbent were used to remove the dye by batch process, namely Tea Waste (AT), Tea Waste which was washed with acid solution of HNO3 (ATA) and Tea Waste which was washed with base solution of KOH (ATB). The biosorbents were characterized by SEM-EDS and iodine absorbance tests. The purposes of this research were to review the ability of biosorbents in the removal of methyl orange dye and the optimum condition needed, as well as to determine the suitable adsorption kinetic and isoterm models to describe the occuring biosorption process.
The adsorption kinetic models used were the Pseudo First Order and Pseudo Second Order, meanwhile for the analysis of adsorption isotherm the Langmuir and Freundlich isotherm models were used. Research variables consist of the influence of contact time (0, 5, 30, 60 and 90 minutes), pH (2, 5, 8 and 11) and biosorbent dose (1 g/L, 2 g/L, 3 g/L and 4 g/L). Of the three biosorbents, ATB was the best biosorbent to removal methyl orange dye with the optimum condition of contact time for 30 minutes, initial synthesised wastewater pH of 2 and dose of 3 g/L ATB in 200 mL of synthesised waste water. The removal efficiency reached was 80,99%.
The removal efficiency reached by AT and ATA were 49,20% (Contact time of 5 minutes, initial synthesised wastewater pH of 8 and biosorbent dose of 3 g/L) and 73,75% (Contact time of 30 minutes, initial synthesised wastewater pH of 8 and biosorbent dose of 1 g/L). The suitable adsorption kinetic‟s model was the Pseudo Second Order model and the best adsorption isoterm to describe the occuring process was Langmuir isoterm.
Keywords: biosorption, methyl orange, tea waste
KATA PENGANTAR
Puji dan syukur penulis panjatkan ke hadirat Tuhan Yang Maha Esa, karena atas berkat dan karunia-Nya penulis mampu menyelesaikan Tugas Akhir dengan judul “Biosorpsi Zat Pewarna Tekstil Methyl Orange Menggunakan Ampas Teh” sebagai syarat penyelesaian pendidikan pada Program Studi Teknik Lingkungan Universitas Sumatera Utara.
Ucapan terima kasih atas bimbingan, bantuan dan dukungan motivasi sehingga Tugas Akhir ini dapat terselesaikan dengan baik penulis tujukan kepada:
1. Bapak Prof. Dr. Ir. Muhammad Turmuzi, M.S. sebagai dosen pembimbing yang telah memberikan dorongan, arahan, moril dan materil dalam penyelesaian Tugas Akhir ini.
2. Ibu Ir. Netti Herlina, M. T. selaku Ketua Program Studi Teknik Lingkungan Fakultas Teknik Universitas Sumatera Utara dan selaku dosen penguji I, atas segala bimbingan dan bantuan yang telah diberikan.
3. Bapak Dr. Amir Husin, S.T., M.T. selaku Sekretaris Program Studi Teknik Lingkungan Fakultas Teknik Universitas Sumatera Utara dan selaku dosen penguji II, atas saran dan masukan yang telah diberikan.
4. Ibu Isra‟ Suryati, M. Si. selaku Koordinator Tugas Akhir Program Studi Teknik Lingkungan Universitas Sumatera Utara, atas saran dan masukan yang telah diberikan.
5. Mas Lutfi dan Mba Shera di PT. Labsystematic Indonesia yang telah memfasilitasi analisa karakteristik SEM-EDS.
6. Bang Juna di Laboratorium Pengembangan PTKI yang telah memfasilitasi pengujian karakteristik daya serap iodin dan konsentrasi zat warna.
Penulis menyadari bahwa laporan hasil ini masih jauh dari kesempurnaan. Segala kritik dan saran yang membangun dari semua pihak sangat diharapkan oleh penulis demi perbaikan Tugas Akhir ini agar menjadi lebih baik lagi di masa yang akan datang. Akhir kata, penulis berharap agar laporan ini dapat bermanfaat bagi berbagai pihak.
Medan, Januari 2019
Penulis
DAFTAR ISI PERNYATAAN KEASLIAN TUGAS AKHIR LEMBAR PENGESAHAN
ABSTRAK ... i
ABSTRACT ... ii
KATA PENGANTAR ... iii
DAFTAR ISI ... v
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... ix
DAFTAR PERSAMAAN ... x
DAFTAR LAMPIRAN ... xi BAB I PENDAHULUAN ... I-1 1.1 Latar Belakang ... I-1 1.2 Rumusan Masalah ... I-6 1.3 Tujuan Penelitian ... I-6 1.4 Ruang Lingkup ... I-7 1.5 Manfaat Penelitian ... I-7 BAB II TINJAUAN PUSTAKA ... II-1 2.1 Air Limbah ... II-1 2.2 Karakteristik Air Limbah ... II-1 2.2.1 Industri Zat Pewarna ... II-2 2.2.2 Methyl Orange ... II-2 2.3 Teh ... II-3 2.3.1 Metode Modifikasi Adsorben... II-3 2.3.2 Karakterisasi Adsorben ... II-4 2.4 Biosorpsi ... II-5 2.4.1 Mekanisme Biosorpsi ... II-6 2.4.2 Faktor yang Mempengaruhi Biosorpsi ... II-7 2.5 Permodelan Batch Adsorpsi ... II-9 2.5.1 Model Kinetika Adsorpsi... II-9 2.5.1.1 Orde Semu Pertama (Pseudo-First Order) ... II-9 2.5.1.2 Orde Semu Kedua (Pseudo-Second Order) ... II-10 2.5.2 Model Kesetimbangan Isoterm ... II-11 2.5.2.1 Isoterm Langmuir ... II-12 2.5.2.2 IsotermFreundlich ... II-14 BAB III METODE PENELITIAN ... III-1 3.1 Lokasi Penelitian ... III-1 3.2 Waktu Penelitian ... III-1 3.3 Jenis Penelitian ... III-1 3.4 Variabel Penelitian ... III-2 3.5 Kerangka Penelitian ... III-2 3.6 Sumber Data ... III-4 3.7 Langkah Penelitian ... III-4 3.7.1 Pembuatan Limbah Cair Sintesis ... III-4 3.7.2 Reaktor Percobaan ... III-4 3.8 Persiapan dan Pengujian ... III-5 3.8.1 Tahap Persiapan ... III-5 3.8.2 Tahap Pengujian Biosorpsi Zat Pewarna Methyl Orange ... III-6
3.8.3 Uji SEM-EDS ... III-7 3.8.4 Uji Daya Serap Iodin ... III-8 3.9 Analisa Sampel ... III-8 3.10 Analisa Data ... III-8 3.10.1 Efisiensi Penyisihan ... III-8 3.10.2 Isoterm Adsorpsi... III-9 3.10.3 Kinetika Adsorpsi ... III-9 BAB IV HASIL DAN PEMBAHASAN ... IV-1 4.1 Hasil Scanning Electron Microscope (SEM) dan Energy Dispersion Spectroscopy
(EDS) Permukaan Ampas Teh (AT), Ampas Teh Asam (ATA) dan Ampas Teh Basa (ATB)... IV-1 4.2 Uji Daya Serap Iodin ... IV-5 4.3 Pengaruh Waktu Kontak Terhadap Adsorpsi Zat Pewarna Tekstil Methyl Orange
... IV-6 4.4 Pengaruh pH Terhadap Adsorpsi Zat Pewarna Tekstil Methyl Orange . IV-8 4.5 Pengaruh Dosis Adsorben Terhadap Adsorpsi Zat Pewarna Tekstil Methyl Orange
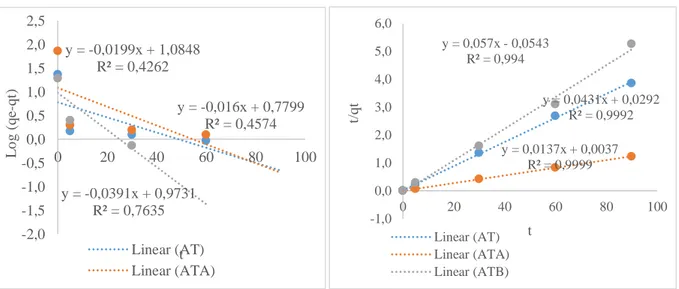
... IV-10 4.6 Kinetika Adsorpsi ... IV-12 4.7 Isoterm Adsorpsi ... IV-15 BAB V KESIMPULAN DAN SARAN ... V-1 5.1 Kesimpulan ... V-1 5.2 Saran ... V-2 DAFTAR PUSTAKA
LAMPIRAN
BIOGRAFI PENULIS
DAFTAR TABEL
Tabel 2.1 Empat Bentuk Linear dari Model Isoterm Langmuir ... II-13 Tabel 4.1 Hasil Uji Daya Serap Iodin ... IV-5 Tabel 4.2 Persamaan dan Nilai Koefisien Korelasi Model Kinetika Adsorpsi IV-13 Tabel 4.3 Parameter Model Kinetika Adsorpsi Zat Pewarna Methyl Orange . IV-15 Tabel 4.4 Persamaan dan Nilai Koefisien Korelasi Permodelan Isoterm
Adsorpsi ... IV-17 Tabel 4.5 Parameter Model Isoterm Adsorpsi Zat Pewarna Methyl Orange ... IV-18
DAFTAR GAMBAR
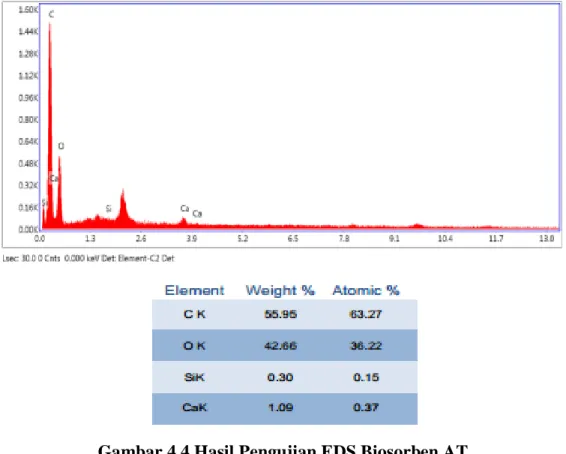
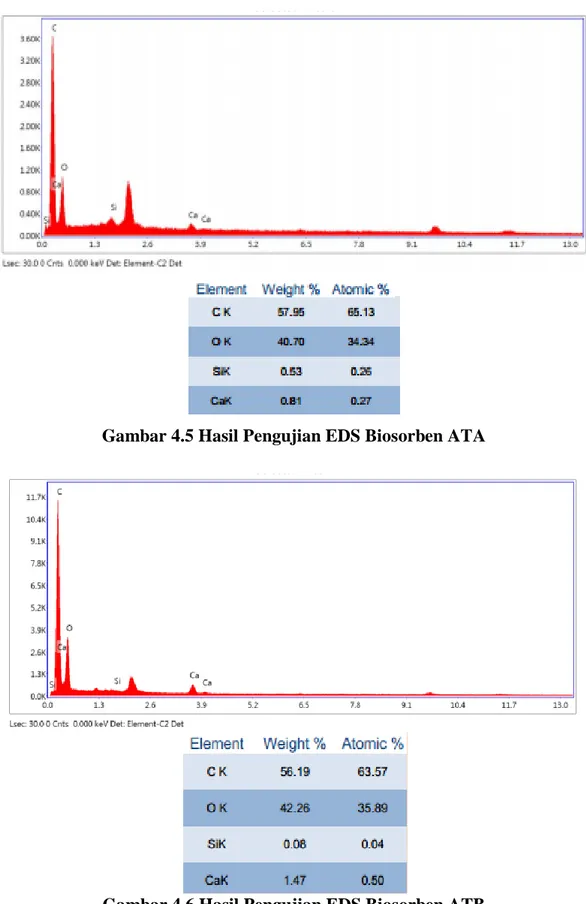
Gambar 2.1 Struktur Zat Pewarna Methyl Orange ... II-2 Gambar 3.1 Kerangka Alir Penelitian ... III-3 Gambar 3.2 Reaktor Batch ... III-5 Gambar 4.1 Hasil Pengujian SEM Biosorben AT ... IV-1 Gambar 4.2 Hasil Pengujian SEM Biosorben ATA ... IV-2 Gambar 4.3 Hasil Pengujian SEM Biosorben ATB ... IV-2 Gambar 4.4 Hasil Pengujian EDS Biosorben AT ... IV-3 Gambar 4.5 Hasil Pengujian EDS Biosorben ATA ... IV-4 Gambar 4.6 Hasil Pengujjian EDS Biosorben ATB ... IV-4 Gambar 4.7 Pengaruh Waktu Kontak Terhadap Penyisihan Zat Pewarna
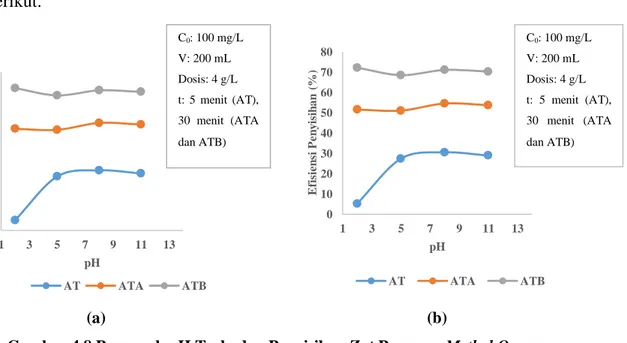
Tekstil Methyl Orange ... IV-6 Gambar 4.8 Pengaruh pH Terhadap Penyisihan Zat Pewarna Tekstil Methyl
Orange ... IV-8 Gambar 4.9 Pengaruh Dosis Terhadap Penyisihan Zat Pewarna Tekstil
Methyl Orange ... IV-11 Gambar 4.10 Grafik Kinetika Adsorpsi Zat Pewarna Methyl Orange... IV-13 Gambar 4.11 Grafik Isoterm Adsorpsi Zat Pewarna Methyl Orange ... IV-16
DAFTAR PERSAMAAN
Persamaan 2.1 Daya Serap Terhadap Iodin ... II-5 Persamaan 2.2 Persamaan Lagergren ... II-10 Persamaan 2.3 Persamaan Lagergren dengan Kondisi Pembatas ... II-10 Persamaan 2.4 Bentuk Linear Persamaan 2.3 ... II-10 Persamaan 2.5 Model Orde Kedua Semu ... II-10 Persamaan 2.6 Pemisahan Variabel Persamaan 2.5 ... II-10 Persamaan 2.7 Integrasi Persamaan 2.6 dengan Kondisi Pembatas t = 0 ke
t = t dan qt = 0 ke qt = qt ... II-11 Persamaan 2.8 Penyusunan Kembali Persamaan 2.7 ... II-11 Persamaan 2.9 Persamaan matematik Orde Kedua Semu ... II-11 Persamaan 2.10 Jumlah Adsorpsi pada Saat Kesetimbangan qe ... II-11 Persamaan 2.11 Kapasitas Adsorpsi pada Waktu Kontak t berbeda (qt) ... II-11 Persamaan 2.12 Persen Penyisihan ... II-12 Persamaan 2.13 Isoterm Langmuir ... II-13 Persamaan 2.14 Bentuk Linear Isoterm Langmuir I ... II-13 Persamaan 2.15 Bentuk Linear Isoterm Langmuir II ... II-13 Persamaan 2.16 Bentuk Linear Isoterm Langmuir III ... II-13 Persamaan 2.17 Bentuk Linear Isoterm Langmuir IV ... II-13 Persamaan 2.18 Parameter Kesetimbangan RL ... II-14 Persamaan 2.19 Isoterm Freundlich ... II-14 Persamaan 2.20 Bentuk Linear Isoterm Freundlich ... II-14
DAFTAR LAMPIRAN
L1 DATA HASIL PERCOBAAN
L2 DOKUMENTASI
BAB I PENDAHULUAN 1.1 Latar Belakang
Sebagai negara dengan jumlah penduduk terbanyak ke-empat di dunia (266.794.980 jiwa per 31 Desember 2017 oleh Statistik Dunia Internet), Indonesia merupakan sebuah negara berkembang dengan banyak kekayaan alam dan potensi pengembangannya.
Seiring dengan berjalannya waktu, jumlah penduduk akan meningkat sehingga kebutuhan hidup meningkat pula, terutama kebutuhan akan penyediaan air bersih. Krisis air bersih telah lama berlangsung di beberapa daerah tertentu di Indonesia. Salah satu penyebabnya adalah banyaknya jumlah industri di Indonesia untuk memenuhi berbagai kebutuhan masyarakat, baik masyarakat Indonesia ataupun masyarakat dunia. Limbah cair dari industri-industri tersebut dapat menyebabkan berbagai dampak negatif bila tidak dikelola dengan baik.
Hanya 3% dari air permukaan bumi yang merupakan air segar dan sisanya terkunci dalam glasier, puncak es dan salju abadi. Air segar lainnya terdapat pada air bawah tanah, danau dan sungai yang dimanfaatkan untuk agrikultur, industri dan sebagainya.
Tetapi cukup disesali, kegiatan-kegiatan tersebut dapat mengkontaminasi air segar dengan variasi polutan yang berpotensi berbahaya yang cukup banyak. Resiko terbesar dari keberadaan polutan-polutan ini pada air permukaan adalah dampak merusak jangka panjang terhadap berbagai ekosistem, termasuk toksisitas akut dan kronik (Gonzalez- Pleiter et al., 2013).
Salah satu polutan yang banyak terdapat pada limbah cair industri pada badan air permukaan adalah zat pewarna. Penggunaan zat pewarna sintesis pada berbagai proses industri telah cukup meningkat selama beberapa tahun terakhir. Bahan kimia tersebut sering digunakan pada produksi kertas dan pulp, plastik, pewarnaan kain, pengolahan kulit, percetakan dan sebagainya. Air limbah industri yang mengandung zat pewarna tersebut umumnya dikeluarkan sebagai efluen. Beberapa zat pewarna tersebut bersifat beracun di alam sehingga penyisihannya dari efluen industri merupakan masalah utama lingkungan. Air limbah yang sangat berwarna karena kehadiran berbagai pewarna dapat menghalangi penetrasi sinar matahari dan oksigen dimana keduanya penting untuk berbagai bentuk kehidupan akuatik (Madrakian et al., 2012).
Methyl orange merupakan zat warna azo yang banyak digunakan dalam pewarnaan kain dan berbagai bidang lainnya. Gugus azo yang dimilikinya merupakan zat warna sintesis dan paling reaktif dalam proses pencelupan bahan tekstil (Widjajanti et al., 2011).
Methyl orange merupakan zat pewarna azo karsinogenik yang dapat terlarut dalam air yang banyak digunakan pada industri tekstil, pembuatan kertas cetak, dan laboratorium penelitian. Zat pewarna ini juga dimetabolismekan menjadi amina aromatik dengan mikroorganisme usus. Methyl orangebersifat stabil, sehinggamemiliki biodegradibilitas yang rendah dan dapat terlarut dalam air sehingga sulit untuk menyisihkannya dari larutan cair dengan metode pemurnian atau pengolahan air biasa (Sejie dan Nadiye- Tabbiruka, 2016). Di antara metode-metode penyisihan zat pewarna yang telah ada, adsorpsi dianggap sebagai metode yang paling mudah dan ekonomis untuk penyisihan zat pewarna dari sistem akuatik. Aplikasi sukses dari adsorpsi menuntut ketentuan dari adsorben yang murah, mudah tersedia dan banyak dengan parameter kinetik yang diketahui dan karakteristik adsorpsi (Hossain dan Alam, 2012).
Adsorpsi merupakan proses transferfase yang banyak digunakan dalam praktik untuk menyisihkan zat dari fase cair (gas atau likuid). Ini juga dapat diobservasi sebagai proses alami dalam kompartemen lingkungan yang berbeda. Definisi paling umum menjelaskan adsorpsi sebagai peningkatan spesies kimia dari fase cair ke permukaan likuid atau padatan. Dalam pengolahan air, adsorpsi telah terbukti sebagai sebuah proses penyisihan yang efisien untuk beragam zat terlarut. Disini, molekul atau ion disisihkan dari larutan akuatik dengan adsorpsi ke atas permukaan padatan (Worch, 2012).
Belakangan ini, biosorpsi telah direkomendasikan sebagai teknik yang lebih murah dan efektif untuk pengolahan air limbah yang terkontaminasi zat pewarna. Metode bioadsorpsi khususnya dipertimbangkan selama dekade terakhir. Keuntungan utama dari teknologi adsorpsi polutan oleh biomassa adalah keefektifannya dalam mengurangi konsentrasi polutan sampai kadar yang sangat rendah dan penggunaan bahan biosorben yang tidak mahal. Karbon aktif merupakan sorben yang efektif, dan telah banyak digunakan dalam pengolahan air limbah zat pewarna. Namun, sorben ini telah terbatas dalam praktiknya karena harganya yang mahal. Hingga sekarang, berbagai sorben alami telah diteliti untuk penyisihan zat pewarna dari larutan cair. Biomassa-biomassa tersebut
termasuk bakteri, fungi, yeast, alga laut, dan sebagainya (Giahi et al., 2011 dan Deniz, 2013).
Menurut Chen et al. (2011), belakangan ini, telah terjadi peningkatan dalam pemanfaatan limbah agrikultur sebagai adsorben zat pewarna yang termasuk: sekam padi, tandan nanas, intisari ampas tebu, tongkol jagung, serbuk gergaji kayu, cangkang kacang hazel, biji pepaya, daun dan kulit buah-buahan, dan sebagainya. Keuntungan dari menggunakan bahan limbah agrikultur sebagai adsorben adalah penghematan biaya pembuangan sementara mengurangi potensi permasalahan lingkungan. Bahkan, produk limbah agrikultur biasanya tersusun dari bahan lignoselulosa, yaitu sebagian besar mengandung selulosa, hemiselulosa dan lignin, yang dianggap bermanfaat untuk adsorpsi. Ulasan kritis mengenai adsorben biaya rendah termasuk limbah agrikultur untuk pengolahan air limbah zat pewarna telah dihadirkan oleh Gupta dan Suhas (2009).
Pada literatur diatas dapat ditemukan bahwa kapasitas adsorpsi dari limbah agrikultur umumnya tinggi untuk zat pewarna kationik, sedangkan kapasitas adsorpsi relatif rendah didapatkan untuk zat pewarna anionik. Kasus ini kemungkinan disebabkan oleh fakta bahwa permukaan limbah tanaman biasanya bermuatan negatif dalam badan air alami, yang tidak menguntungkan untuk adsorpsi anion. Oleh karena itu, permukaan limbah tanaman alami harus dimodifikasi dalam perlakuan untuk meningkatkan kapasitas adsorpsinya untuk zat pewarna anionik.
Beberapa biosorben yang telah digunakan dalam penyisihan zat pewarna methyl orange sebelumnya yaitu cangkang telur dengan perlakuan thermal (Belay dan Hayelom, 2014), jerami gandum yang telah dimodifikasi dengan surfaktan kationik (Su et al., 2013),kulit buah kedondong (Rumky et al., 2013), nanopartikel Fe3O4 sintesis dan modifikasi permukaannya dari ekstrak pektin Azolla (Rakhshaee et al., 2011) dan limbah tulang burung unta (Arshadi et al., 2014).
Selain dari biosorben diatas, salah satu bahan yang berpotensi sebagai biosorben adalah ampas teh. Teh merupakan minuman yang paling banyak dikonsumsi setelah air di seluruh dunia karena keuntungan efeknya terhadap kesehatan, seperti sebagai antioksidan, antikarsinogenik, anti kegiatan mikrobial. Selama proses produksi teh, daun teh berkualitas tinggi dipilih untuk produksi teh hijau kering atau teh terfermentasi, sementara daun teh kualitas rendah digunakan untuk produksi minuman-
minuman teh dan untuk ekstraksi polifenol, kafein, polisakarida teh, dan sebagainya.
Sejumlah besar residu teh dihasilkan untuk produksi minuman teh dan ekstraksi, dan biasanya dibuang ke lingkungan tanpa pengolahan, dimana bukan hanya menyia- nyiakan sumber daya, tetapi juga menyebabkan permasalahan higienitas lingkungan selama proses degradasinya. Karena itu, diinginkan upaya penggunaan kembali dari residu teh tersebut (Yang dan Cui, 2013).
Dinding sel daun teh yang tidak dapat larut sebagian besar terdiri atas selulosa dan hemiselulosa, lignin, tannin terkondensasi dan protein struktural. Struktur polimer dari bahan berbasis selulosa menyatakan kemampuan adsorpsi kimia kation relatif kuat seperti ion logam dan basa organik sebaik adsorpsi fisika terhadap bahan-bahan seperti senyawa asam dan anionik (Madrakian et al., 2012). Pektin merupakan unsur polisakarida penting dari dinding sel tanaman, terbuat dari bagian-bagian rantai asam poligalakturonik dengan ikatan glikosidik ɑ (1 → 4), yang berinteraksi dengan ion Ca2+
dan Mg2+ atau zat pewarna kationik untuk membentuk polimer tiga dimensi. Tingkat metilasi pektin dalam dinding sel telah dinyatakan sebagai kandungan relatif dari gugus methoxyl (-COOCH3) dalam rantai, serta distribusi gugus karboksil (-COOH) dalam rantai (Giahi et al., 2011).
Auta dan Hameed (2011) melakukan penelitian menggunakan karbon aktif ampas teh yang telah diimpregnasi dengan Potasium Asetat untuk menyisihkan zat pewarna Acid Blue 25 dengan proses batch. Variabel penelitian tersebut terdiri dari pH, konsentrasi awal zat pewarna dan suhu. Hasilnya membuktikan bahwa ampas teh mampu mengadsorpsi zat pewarna Acid Blue 25 dengan kapasitas adsorpsi sebesar 203,34 mg/g dan penyisihan sebesar 97,88% dengan adsorpsi yang sesuai dengan isoterm Langmuir.
Adsorpsi zat pewarna methylene blue dan eosin yellow dengan menggunakan karbon dari ampas teh yang telah diimpregnasi dengan asam fosfat dilakukan oleh Borah dkk (2015). Dalam penelitian tersebut dilakukan analisa isoterm adsorpsi, kinetika adsorpsi dan termodinamika adsorpsi dengan variabel pH, konsentrasi awal zat pewarna, waktu kontak, dosis adsorben dan suhu. Hasil penelitian menunjukkan bahwa adsorpsi kedua zat pewarna sesuai dengan isoterm Langmuir dan kinetika Orde Kedua Semu. Kapasitas adsorpsi maksimum zat pewarna methylene blue dan eosin yellow masing-masing adalah sebesar 402,25 mg/g dan 400 mg/g pada suhu 300 °K.
Foroughi-Dahr dkk (2014) melakukan penelitian untuk mengadsorpsi zat pewarna congo red menggunakan ampas teh dengan sistem batch. Analisa yang dilakukan adalah analisa isoterm adsorpsi, kinetika adsorpsi, termodinamika adsorpsi, desorpsi dan pengaruh perlakuan fisik dengan menggunakan vibratrory mill. Variabel dalam penelitian tersebut adalah dosis adsorben, pH, suhu, konsentrasi awal zat pewarna dan waktu kontak. Hasilnya membuktikan bahwa penyisihan yang terjadi sesuai dengan isoterm Langmuir dan kinetika Orde Kedua Semu. Perlakuan fisik yang dilakukan mampu meningkatkan kapasitas adsorpsi dari 32,26 mg/g menjadi 43,48 mg/g. Analisa termodinamika menunjukkan bahwa proses adsorpsi terjadi secara spontan dan endotermik, dan dari plot intrapartikel disimpulkan bahwa terdapat lebih dari satu mekanisme adsorpsi terlibat dalam proses yang berlangsung,
Penyisihan zat pewarna rhodamine-B dengan proses batch dilakukan oleh Hossain dan Alam (2012). Penelitian dilakukan dengan pH larutan 2 dan dosis adsorben 0,1 g dengan variabel konsentrasi awal zat pewarna dan suhu. Hasil yang didapatkan menunjukkan bahwa proses adsorpsi yang terjadi sesuai dengan isoterm Langmuir dan kinetika Orde Kedua Semu. Kapasitas adsorpsi maksimum adalah sebesar 53,2 mg/g pada pH 2 dan jumlah kesetimbangan adsorpsi meningkat dengan peningkatan suhu.
Li dkk (2013) melakukan penelitian penyisihan zat pewarna methyl orange menggunakan ampas teh dengan proses batch. Penelitian dilakukan dengan variabel suhu, dosis biosorben, konsentrasi awal zat pewarna dan waktu kontak. Kondisi optimal didapatkan dengan konsentrasi awal zat pewarna 9,75 mg/L, suhu 35,3 °C, waktu kontak 63,8 menit dan dosis adsorben 3,90 g/L. Penyisihan zat pewarna mencapai 58,2%.
Berdasarkan hasil penelitian yang telah dipaparkan diatas, maka dalam studi penelitian ini penulis ingin menganalisis tentang biosorben dengan kinerja terbaik diantara ampas teh (AT), ampas teh dengan pencucian asam (Ampas Teh Asam atau ATA), dan ampas teh dengan pencucian basa (Ampas Teh Basa atau ATB) untuk penyisihan zat pewarna methyl orange (MO) untuk kemudian dikaji pengaruh waktu kontak, pH dan dosis biosorbenpada sistem batch. Objek penelitian adalah untuk menentukan kinetika adsorpsi untuk mengetahui laju adsorpsi (menggunakan Pseudo-First Order dan Pseudo-Second Order) dan isoterm adsorpsi (Langmuir dan Freundlich) yang dapat
menggambarkan proses biosorpsi yang terjadi dalam penyisihan zat pewarna methyl orange.
1.2 Rumusan Masalah
Berdasarkan uraian latar belakang permasalahan diatas, maka dapat diperoleh rumusan masalah sebagai berikut:
Methyl orange bersifat stabil, menunjukkan biodegradibilitas yang rendah dan dapat terlarut dalam air sehingga sulit untuk menyisihkannya dari larutan cair dengan metode pemurnian/pengolahan air biasa. Biosorpsi dianggap sebagai teknik yang lebih mudah dan ekonomis untuk penyisihan zat pewarna dari sistem akuatik daripada adsorpsi.
Dinding sel daun teh yang tidak dapat terlarut sebagian besar terdiri atas selulosa dan hemiselulosa, lignin, tannin terkondensasi dan protein struktural dinyatakan memiliki kemampuan adsorpsi kimia kation relatif kuat seperti ion logam dan basa organik sebaik adsorpsi fisika terhadap bahan-bahan seperti senyawa asam dan anionik. Studi penelitian ini diarahkan pada membandingkan kinerja biosorben terbaik di antara ampas teh (AT), ampas teh dengan pencucian asam (ATA) dan ampas teh dengan pencucian basa (ATB) dalam penyisihan zat pewarna methyl orange (MO) untuk kemudian dianalisis pengaruhwaktu kontak, pH dan dosis adsorben pada sistem batch.
1.3 Tujuan Penelitian
Tujuan dari penelitian ini adalah:
1. Mengkaji pengaruh waktu kontak, pH dan dosis terhadap efisiensi penyisihan zat pewarna methyl orange dalam sistem batch dengan menggunakan biosorben ampas teh (Tea Waste – AT), ampas teh dengan pencucian asam (Acid Washing – ATA) dan ampas teh dengan pencucian basa (Base Washing – ATB).
2. Memperoleh model isoterm adsorpsi dan kinetika adsorpsi yang sesuai.
1.4 Ruang Lingkup
Ruang lingkup penelitian ini dibatasi pada masalah sebagai berikut:
1. Limbah yang digunakan dalam penelitian ini adalah air limbah yang berasal dari air limbah sintetik dengan melarutkan zat pewarna methyl orange dalam akuades;
2. Parameter yang akan diuji dalam penelitian ini adalah kandungan zat pewarna methyl orange;
3. Proses pengolahan limbah cair dilakukan dengan biosorpsi menggunakan biosorbenampas teh (Tea Waste – AT), ampas teh dengan pencucian asam (Acid Washing – ATA) dan ampas teh dengan pencucian basa (Base Washing – ATB);
4. Percobaan ini dilakukan dengan berbagai variasi variabel bebas sebagai berikut:
a. Waktu Kontak : 0 menit, 5 menit, 30 menit, 60 menit, 90 menit;
b. pH : 2, 5, 8, 11;
c. Dosis Biosorben : 0 g/L, 1 g/L, 2 g/L, 3 g/L, 4 g/L;
5. Biosorben dikarakterisasi dengan melakukan uji SEM-EDS dan uji daya serap iodin.
1.5 Manfaat Penelitian
Manfaat dari penelitian ini yaitu:
1. Dapat diketahui kemampuan penyisihan zat pewarna methyl orange dengan menggunakan biosorben ampas teh dan kondisi optimal yang dibutuhkan agar penyisihan dapat berjalan dengan efektif.
2. Memberikan alternatif yang lebih efektif dan efisien untuk penyisihan zat pewarna methyl orange dari limbah cair.
3. Sebagai referensi dan bahan kajian terhadap penelitian berikutnya agar diuji berbagai variasi percobaan yang berbeda sehingga diperoleh data yang lebih lengkap mengenai kemampuan ampas teh dalam menyisihkan zat pewarna methyl orange pada sumber air limbah.
BAB II
TINJAUAN PUSTAKA
2.1 Air Limbah
Menurut Peraturan Menteri Lingkungan Hidup No. 5 Tahun 2014 Tentang Baku Mutu Limbah Cair Pasal 29, Air limbah adalah sisa dari suatu usaha dan/atau kegiatan yang berwujud cair. Said (2017) menyatakan bahwa air limbah secara garis besar dapat dibagi menjadi tiga: air limbah domestik yang berasal dari perkantoran dan pertokoan (daerah komersial), air limbah industri dan air limbah pertanian. Pengolahan air limbah industri meliputi mekanisme dan proses yang biasa digunakan untuk mengolah air yang terkontaminasi atau tercemar akibat kegiatan industri atau kegiatan komersial sebelum dibuang ke lingkungan atau sebelum digunakan kembali. Pada umumnya industri masih menghasilkan air limbah, walaupun di negara maju kecenderungan saat ini adalah meminimalkan atau menggunakan kembali (reuse) limbah di dalam proses produksinya.
2.2 Karakteristik Air Limbah Industri
Menurut Said (2017), berdasarkan karakteristiknya, air limbah industri secara garis besar dapat dibagi menjadi beberapa kelompok:
a. Air limbah industri yang mengandung konsentrasi zat organik yang relatif tinggi, misalnya industri makanan, industri kimia, industri minyak nabati atau hewani, industri obat-obatan, industri lem atau perekat gelatin, industri tekstil, industri pulp dan kertas, dan lain-lain.
b. Air limbah industri yang mengandung konsentrasi zat organik relatif rendah, misalnya industri pengemasan makanan, industri pemintalan, industri serat, industri kimia, industri minyak, industri batu bara, industri laundry, dan lain-lain.
c. Air limbah yang mengandung zat organik berbahaya beracun, misalnya industri penyamakan kulit, industri barang dengan bahan baku kulit, industri besi baja, industri kimia insektisida, herbisida, dan lain-lain.
d. Air limbah industri yang mengandung zat anorganik umum, misalnya industri kimia seperti pupuk anorganik, industri kimia anorganik, pencucian pada industri logam, industri keramik, dan lain-lain.
e. Air limbah industri yang mengandung zat anorganik berbahaya beracun, misalnya industri pelapisan logam (elektroplating), industri baterai, dan lain-lain.
2.2.1 Industri Zat Pewarna
Bahan pewarna banyak digunakan untuk pewarnaan serat alami atau serat sintetis, serta bahan pembantu pada industri tekstil. Prosesnya sangat kompleks dan kualitas air limbah yang dihasilkan juga sangat bervariasi. Umumnya konsentrasi BOD 200 – 500 mg/L dan konsentrasi SS 50 – 400 mg/L (Said, 2017).
2.2.2 Methyl Orange
Methyl orange merupakan zat warna azo yang digunakan dalam pewarnaan kain. Gugus azo yang dimilikinya merupakan zat warna sintesis dan paling reaktif dalam proses pencelupan bahan tekstil (Widjajanti et al., 2011). Methyl orange merupakan zat pewarna azo karsinogenik yang dapat terlarut dalam air yang banyak digunakan pada industri tekstil, pembuatan kertas cetak, dan laboratorium penelitian. Zat pewarna ini juga dimetabolismekan menjadi amina aromatik dengan mikroorganisme usus. Methyl orange stabil, menunjukkan biodegradibilitas yang rendah dan dapat terlarut dalam air sehingga sulit untuk menyisihkannya dari larutan cair dengan metode pemurnian/pengolahan air biasa (Sejie dan Nadiye-Tabbiruka, 2016).
Karena toksisitas dan sifat sulit terurai buangan dari industri industri tersebut dapat menyebabkan ancaman serius terhadap karakteristik fisika-kimia dari air segar dan kehidupan akuatik. Berbagai pengolahan kimiawi, biologis dan fisika telah digunakan untuk mengolah zat pewarna azo. Karena zat pewarna resistan terhadap biodegradasi aerobik, molekul organik membandel, dan stabil terhadap larutan pengoksidasi, proses adsorpsi terbukti sebagai tindakan terpercaya dan efektif untuk pengolahan ini (Cheah et al., 2012). Formula kimia dari methyl orange adalah C14H14N3NaO3S, dan strukturnya dapat dilihat pada Gambar 2.1 (Liu et al., 2009).
Gambar 2.1 Struktur Zat Pewarna Methyl Orange (Liu et al., 2009)
2.3 Teh
Teh merupakan minuman yang paling banyak dikonsumsi setelah air di seluruh dunia karena keuntungan efeknya terhadap kesehatan, seperti sebagai antioksidan, antikarsinogenik, anti kegiatan mikrobial. Selama proses produksi teh, daun teh berkualitas tinggi dipilih untuk produksi teh hijau kering atau teh terfermentasi, sementara daun teh kualitas rendah digunakan untuk produksi minuman-minuman teh dan untuk ekstraksi polifenol, kafein, polisakarida teh, dan sebagainya. Sejumlah besar residu teh dihasilkan untuk produksi minuman teh dan ekstraksi, dan biasanya dibuang ke lingkungan tanpa pengolahan, dimana bukan hanya menyia-nyiakan sumber daya, tetapi juga menyebabkan permasalahan higienitas lingkungan selama proses degradasinya. Karena itu, diinginkan upaya penggunaan kembali dari residu teh tersebut (Yang dan Cui, 2013).
Dinding sel daun teh tidak dapat terlarut sebagian besar terdiri atas selulosa dan hemiselulosa, lignin, tannin terkondensasi dan protein struktural. Struktur polimer dari bahan berbasis selulosa menyatakan kemampuan adsorpsi kimia kation relatif kuat seperti ion logam dan basa organik sebaik adsorpsi fisika terhadap bahan-bahan seperti senyawa asam dan anionik (Madrakian et al., 2012). Pektin merupakan unsur polisakarida penting dari dinding sel tanaman, terbuat dari bagian-bagian rantai asam poligalakturonik dengan ikatan glikosidik ɑ (1 → 4), yang berinteraksi dengan ion Ca2+
dan Mg2+ atau zat pewarna kationik untuk membentuk polimer tiga dimensi. Tingkat metilasi pektin dalam dinding sel telah dinyatakan sebagai kandungan relatif dari gugus methoxyl (-COOCH3) dalam rantai, serta distribusi gugus karboksil (-COOH) dalam rantai (Giahi et al., 2011). Ampas teh mengandung protein kasar 27.42% (persen dalam berat kering), lemak 3.26%, kobalt 1.14%, fosfor 0.25%, dan serat kasar 20.39%
(Fiberti 2002).
2.3.1 Metode Modifikasi Adsorben
Modifikasi kimia permukaan adsorben dianggap sebagai cara yang menjanjikan dan menarik untuk aplikasi adsorben dalam berbagai bidang. Penjelasan detail dari beberapa metode penting pada modifikasi permukaan adsorben selama beberapa dekade terakhir disajikan pada bagian berikut (Bhatnagar et al., 2013):
1. Perlakuan Asam
Perlakuan asam terhadap karbon umumnya digunakan untuk mengoksidasi permukaan berpori karbon karena meningkatkan sifat asam, menyisihkan elemen mineral dan meningkatkan sifat hidrofilik dari permukaan. Asam nitrit dan asam sulfat merupakan yang paling banyak dipelajari selain beberapa asam lainnya yang digunakan untuk tujuan tersebut. Gugus fungsi asam (misalnya gugus fungsi oksigen mengandung donor proton) pada permukaan karbon telah dipelajari untuk penyisihan logam berat dari air dan didapatkan sangat menguntungkan karena ion logam memiliki kecenderungan untuk membentuk kompleks logam dengan gugus asam bermuatan negatif.
2. Perlakuan Basa
Perlakuan basa (alkali) terhadap adsorben menghasilkan permukaan bermuatan positif yang sebaliknya membantu untuk menyerap spesies bermuatan negatif dalam jumlah yang lebih tinggi. Cara termudah untuk menghasilkan karbon berpori dengan sifat permukaan basa adalah dengan memperlakukannya pada temperatur tinggi dalam atmosfir inert, hidrogen atau ammonia. Pengolahan adsorben dengan NH3 pada 400 – 900 °C menyebabkan pembentukan fungsi nitrogen basa. Amida, amina aromatik dan amida terprotonasi dihasilkan pada 400 – 600 °C. Selanjutnya, struktur jenis piridin terjadi pada suhu yang lebih tinggi, dimana meningkatkan kebasaan permukaan karbon. Gugus yang menandung nitrogen umumnya memberikan sifat basa, yang dapat meningkatkan interaksi antara karbon berpori dan molekul asam, seperti, dipol-dipol, pengikatan H, pengikatan kovalen, dan sebagainya. Selanjutnya, dalam larutan alkali (basa), diharapkan bahwa ion OH- bereaksi dengan gugus fungsi permukaan karbon aktif.
Perlakuan alkali karbon aktif berguna dalam meningkatkan adsorpsi khususnya spesies organik (seperti phenol) dari air.
2.3.2 Karakterisasi Adsorben
Sebelum dilakukannya studi adsorpsi, dilakukan terlebih dahulu karakterisasi adsorben.
Adapun karakterisasi adsorben yang akan dilakukan pada penelitian ini meliputi uji SEM, EDS dan Daya Serap Iodin.
1. Scanning Electron Microscope (SEM): Untuk mengetahui struktur permukaan dan ukuran partikel dari masing-masing adsorben (Haura et al., 2017).
2. Energy Dispersion Spectroscopy (EDS): Untuk analisa kondisi dasar, kuantitas dan perubahan unsur komponen kimia penyusun adsorben (Haura et al., 2017 dan Khabibi et al., 2016).
3. Daya Serap Iodin: Daya serap terhadap iodin ditentukan dengan tujuan mengetahui kemampuan adsorpsi dari adsorben yang dihasilkan terhadap larutan berbau. Daya serap terhadap iodin adalah jumlah miligram iodin yang diadsorpsi oleh satu gram karbon aktif (Suhendarwati et al, 2014). Pertama-tama ke dalam erlenmeyer tutup asah ditimbang sekitar 1 gram biosorben, selanjutnya ditambahkan dengan di pipet 25 mL larutan iod monoklorida dan erlenmeyer ditutup dengan tutup yang telah dibasahi dengan KI, kemudian dikocok dengan hati-hati dan disimpan di tempat yang gelap selama 2 jam, ke dalam erlenmeyer ditambahkan 10 mL larutan Kalium Iodida (KI) 20% dan 150 mL air suling, kemudian dikocok dan seterusnya dititrasi dengan larutan tiosulfat 0,1 N. Sebagai penunjuk adalah larutan pati/kanji dan untuk perbandingan digunakan larutan blanko dengan cara yang sama (SNI 06-3730-1995).
Daya Serap Terhadap iod ⁄
(2.1)
Dimana:
b = Jumlah titar untuk contoh a = Normalitas larutan
N = Normalitas larutan Na2SO3 126,9 = Berat atom Iod
fp = Faktor pengenceran (2,5) 2.4 Biosorpsi
Biosorpsi merupakan proses fisika-kimia dan bebas metabolisme berdasarkan berbagai mekanisme termasuk absorpsi, adsorpsi, pertukaran ion, kompleksi permukaan dan presipitasi (Fomina dan Gadd, 2013). Oleh karena itu proses biosorpsi melibatkan fase solid (biosorben) dan fase cair (solven: umumnya air) yang mengandung spesies terlarut atau tersuspensi untuk diserap (sorbat). Biosorpsi merupakan salah satu sifat signifikan
dari mikroorganisme hidup dan mati (dan komponen-komponennya) relevan untuk pengolahan polutan. Namun, secara praktik semua bahan biologis termasuk macroalga (rumput laut) serta tanaman dan biomassa hewan dan produk turunan (Contoh Chitosan) mampu untuk biosorpsi. Selama beberapa tahun, biosorpsi telah diklaim sebagai bioteknologi yang menjanjikan untuk penyisihan polutan dan/atau pemulihan dari larutan, karena kemudahannya, operasi yang sejalan dengan teknologi ion exchange yang konvensional, efisiensi yang nyata dan ketersediaan biomassa dan limbah bioproduk (Fomina dan Gadd, 2013).
Keuntungan utama dari teknologi adsorpsi polutan oleh biomassa adalah keefektifannya dalam mengurangi konsentrasi polutan sampai kadar yang sangat rendah dan penggunaan bahan biosorben yang tidak mahal. Karbon aktif merupakan sorben yang efektif, dan telah banyak digunakan dalam pengolahan air limbah zat pewarna. Namun, sorben ini telah terbatas dalam praktiknya karena harganya yang mahal. Jadi, bahan alternatif yang tidak mahal dan efektif telah menjadi perhatian besar bagi ilmuwan- ilmuwan lingkungan. Hingga sekarang, berbagai sorben alami telah diteliti untuk penyisihan zat pewarna dari larutan cair. Biomassa-biomassa tersebut termasuk bakteri, fungi, yeast, alga laut, dan sebagainya (Giahi et al., 2011 dan Deniz, 2013).
2.4.1 Mekanisme Biosorpsi
Bahan biologis kompleks dan variasi komponen-komponen struktural yang terdapat dalam biomassa berarti bahwa banyak gugus fungsional yang mampu berinteraksi dengan spesies metal, misalnya karboksil, fosfat, hidroksil, amino, thiol, dan sebagainya, hingga derajat tertentu dan dipengaruhi oleh faktor fisika-kimia.
Kenyataannya, bergantung pada sistem dan kondisi tertentu biosorpsi dapat menjadi sebuah proses mekanis yang rumit. Presipitasi dan kristalisasi merupakan mekanisme- mekanisme lain yang mungkin terjadi dan menyulitkan sorpsi dan/atau desorpsi. Ini dapat menyebabkan kapasitas serapan yang tinggi tetapi hal ini dapat menghambat desorpsi.
Preferensi ligan dalam pembentukan logam kompleks sangat berkaitan untuk memahami biosorpsi. Cara-cara berbeda untuk mengklasifikasikan logam menurut sifat kimianya termasuk Prinsip Asam Basa Keras Lunak (HSAB) dengan rangkaian stabilitas logam kompleks Irving-William. Tipe A (asam keras) secara istimewa
mengikat pada ligan yang mengandung oksigen (keras), sementara tipe B (asam lunak) secara istimewa mengikat pada ligan yang mengandung S dan N (lunak). Namun, prinsip tersebut lebih deskriptif daripada penjelasan dan definisi tidak absolut. Beberapa perilaku akan dipengaruhi oleh konsentrasi logam, serta konsentrasi logam relatif dalam campuran dimana efek kompetitif mungkin terjadi. Skema keras/lunak memprediksi bahwa ikatan yang terbentuk antara asam keras dan ligan keras akan didominasi ionik sedangkan kompleks asam-ligan lunak lebih bersifat kovalen. Namun, hal ini bervariasi tergantung pada sifat biomassa dan ketersediaan ligan permukaan.
Pembentukan kation kompleks permukaan seperti Cu2+ mungkin melibatkan koordinasi ion logam dengan atom donor oksigen dan pelepasan proton dan pembentukan kompleks permukaan bidentat. Kation dapat berkaitan dengan permukaan biosorben sebagai kompleks lingkar dalam atau lingkar luar tergantung apabila ikatan kimia (yaitu sebagian besar kovalen) terbentuk antara logam tersebut dengan elektron donor ion oksigen dalam kasus ini (kompleks lingkar dalam) atau bila sebuah kation mendekati permukaan gugus negatif sampai jarak kritis tetapi kation dan basa dipisahkan oleh setidaknya satu molekul air. Mekanisme biosorpsi anion sedikit dipelajari. Hal ini tampaknya dipengaruhi oleh kondisi kimia seperti pH. Contohnya, spesies anionik seperti TcO4-
, PtCl43-
, CrO42-
, SeO42-
dan Au(CN)2- menunjukkan peningkatan biosorpsi pada nilai pH rendah (Fomina dan Gadd, 2013).
2.4.2 Faktor yang Mempengaruhi Biosorpsi
Terlepas dari jenis dan bentuk kimia dari sorbat, sejumlah faktor fisika-kimia menentukan keseluruhan performa biosorpsi. Faktor-faktor penting termasuk (Fomina dan Gadd, 2013):
1. pH larutan yang merupakan regulator terpenting dari biosorpsi yang mempengaruhi larutan kimia dari polutan itu sendiri, aktivitas gugus fungsional dalam biosorben, dan persaingan untuk keberadaan berdampingan dalam larutan.
Menaikkan ph meningkatkan penyisihan logam kationik atau zat pewarna dasar, tetapi mengurangi penyisihan logam anionik atau zat pewarna asam.
2. Kekuatan ionik larutan yang ketika dinaikkan, mengurangi penyisihan biosorptif dari polutan adsorptif dengan bersaing dengan adsorbat untuk situs pengikatan pada biosorben.
3. Konsentrasi awal polutan yang ketika dinaikkan, meningkatkan kuantitas polutan terserap per unit massa biosorben, tetapi menurunkan efisiensi penyisihan.
4. Pengaruh polutan lain termasuk persaingan untuk situs pengikatan atau gangguan lainnya. Peningkatan konsentrasi polutan yang bersaing biasanya akan mengurangi penyisihan biosorptif dari polutan target. Namun, beban kation dari biomassa mungkin meningkatkan biosorpsi kation lain karena efek buffer dari pH.
Dalam beberapa kasus, kation mungkin meningkatkan biosorpsi spesies anionik dengan meningkatkan pengikatan anion bermuatan negatif. Efek anionik pada kapasitas biosorpsi logam tergantung pada spesiasi logam, logam yang ada dan sifat biosorben.
5. Sifat biosorben dan ketersediaan situs pengikat, prasejarah pertumbuhan dan pengolahan, modifikasi fisik atau kimia, dosis dan ukuran sangat penting untuk performa.
6. Temperatur, yang biasanya meningkatkan penyisihan biosorptif dari polutan adsorptif ketika dinaikkan dengan meningkatkan aktivitas permukaan dan energi kinetik dari adsorbat, tetapi juga mungkin merusak struktur fisik dari biosorben tersebut.
7. Menaikkan kecepatan pengadukan dalam sistem cair yang sesuai meningkatkan tingkat penyisihan biosorptif dari polutan adsorptif dengan meminimalisir penentangan transfer massa, tetapi mungkin merusak struktur fisik dari biosorben tersebut.
8. Dosis adsorben merupakan parameter penting proses untuk menentukan kapasitas adsorben terhadap jumlah adsorben pada kondisi beroperasi. Secara umum persen penyisihan zat pewarna meningkat dengan meningkatnya dosis adsorben, dimana kuantitas atau jumlah dari situs sorpsi pada permukaan adsorben akan meningkat dengan meningkatnya jumlah adsorben. Pengaruh dari dosis adsorben memberikan ide untuk kemampuan adsorpsi zat pewarna unntuk di adsorpsi dengan jumlah adsorben terkecil, untuk mengetahui kemampuan zat pewarna dari sudut pandang ekonomis (Yagub et al., 2014).
9. Kontak antara adsorben dengan adsorbat meningkatkan kemungkinan adsorpsi dan peningkatannya dengan waktu kontak yang lebih lama. Pengaruh waktu kontak terhadap adsorpsi zat pewarna yaitu seiring dengan peningkatan waktu
kontak, kapasitas adsorpsi (qe, mg/g) dari adsorben juga meningkat (Wasti dan Awan, 2014).
2.5 Permodelan Batch Adsorpsi
Eksperimen batch digunakan untuk perbandingan kapasitas adsorpsi antar adsorben dengan variasi waktu dan variasi larutan pada adsorpsi (Nur et al 2014). Proses adsorpsi dikarakteristikan ke dalam dua bagian yaitu kesetimbangan adsorpsi dan kinetika adsorpsi.
Penting untuk mempelajari model isoterm untuk proses adsorpsi untuk mengetahui mekanisme dan kapasitas adsorpsi dari sebuah adsorben. Parameter isoterm dapat membantu untuk memahami interaksi antara adsorben dengan adsorbat. Dalam penelitian ini, model adsorpsi isoterm Langmuir dan Freundlich digunakan untuk studi isotermal (Habiba et al., 2018). Studi kinetik merupakan faktor bergantung waktu untuk menentukan waktu kesetimbangan terhadap adsorben spesifik, yang akan membantu dalam proses desain pengolahan air limbah industri (Islam et al., 2015).
2.5.1 Model Kinetika Adsorpsi
Menurut Shahmoradi et al. (2015), kinetika adsorpsi merupakan salah satu karakteristik paling penting dalam mengetahui efisiensi adsorpsi. Cara memperoleh kinetika adsorpsi yaitu dengan membuat grafik adsorpsi dari persamaan yang ada dan menuliskan model kinetika berdasarkan pada apakah ada atau tidaknya data yang sesuai. Adapun model persamaannya ditunjukkan pada orde semu pertama, orde semu kedua dan model difusi permukaan homogen (HSDM) (Hanafi dan Abdel, 2016). Model persamaan orde semu pertama dan orde semu kedua digunakan pada data kinetika adsorpsi pertukaran ion dalam studi batch.
2.5.1.1 Orde Semu Pertama (Pseudo-First Order)
Lagergren mengajukan model kinetika Orde Pertama Semu, yang cukup signifikan dalam menentukan konstanta tingkat biosorpsi berdasarkan kapasitas biosorpsinya (Selvasembian et al, 2018). Data kinetika adsorpsi dijelaskan dengan model Orde Semu Pertama (Pseudo-First Order) Lagergren, yang merupakan persamaan yang paling awal diketahui untuk menggambarkan laju adsorpsi berdasarkan kapasitas adsorpsi.
Persamaan Lagergren umumnya dinyatakan sebagai berikut (Khaled, 2009):
(2.2)
Dimana qe dan qt masing-masing merupakan kapasitas adsorpsi pada kesetimbangan dan pada waktu t (mg/g), k1 merupakan konstanta kecepatan dari adsorpsi orde semu pertama (min-1). Dengan menggabungkan persamaan (2.1) untuk kondisi pembatas t
= 0 ke t = t dan qt = 0 ke qt = qt menghasilkan:
( ) (2.3)
Persamaan (2.2) dapat disusun kembali untuk mencapai bentuk linear sebagai berikut:
(2.4)
Plot nilai log (qe – qt) versus t untuk mendapatkan hubungan linear dimana k1 dan qe dapat ditentukan masing-masing dari slope dan perpotongannya. Jika dosis perpotongan tidak sesuai dengan qe maka reaksinya tidak mungkin merupakan reaksi orde pertama bahkan plot ini memiliki koefisien korelasi yang tinggi dengan data eksperimen (Crini et al., 2007). Variasi laju harus proporsional dengan kekuatan konsentrasi pertama untuk adsorpsi permukaan yang tepat. Namun, hubungan antara konsentrasi awal zat terlarut dan laju adsorpsi tidak akan linear ketika difusi pori membatasi proses adsorpsi.
(Khaled, 2009).
2.5.1.2 Orde Semu Kedua (Pseudo-Second Order)
Model Orde Semu Kedua oleh Ho dan McKay (1999), dinyatakan sebagai:
(2.5)
Dimana k merupakan konstanta kecepatan sorpsi (g/mg.min), qe merupakan jumlah sorbat terlarut tersorpsi pada kesetimbangan (mg/g) dan qt adalah jumlah sorbat terlarut pada permukaan sorben pada waktu tertentu t (mg/g). Dengan memisahkan variabel di persamaan 2.5 didapatkan:
(2.6)
Integrasi dari ini dengan kondisi pembatas t = 0 ke t = t dan qt = 0 ke qt = qt, memberikan:
(2.7)
Yang merupakan hukum kecepatan terintegrasi untuk reaksi orde kedua semu.
Persamaan 2.7 dapat disusun untuk mendapatkan:
(2.8)
Konstanta dapat ditentukan dengan plot t/qt versus t.
Persamaan matematik dari Orde Kedua Semu ditunjukkan seperti berikut.
(2.9)
Untuk menentukan konstanta Orde Kedua Semu, plot linear antara t/qt versus t digambar dan nilai-nilai konstanta didapatkan dari slope dan intersep plot tersebut. Ho dan McKay mengajukan model kinetika Orde Kedua Semu, memperkirakan perilaku biosorpsi sepanjang waktu proses biosorpsi. Model Orde Kedua Semu didasarkan pada proses Chemisorption terjadi melalui gaya valensi dari pertukaran elektron antara zat pewarna dan gugus fungsi biosorben (Selvasembian et al, 2018).
2.5.2 Model Kesetimbangan Isoterm
Kapasitas adsorpsi pada saat kesetimbangan, qe (mg/g) ditentukan sebagai berikut (Islam, et al., 2015):
Jumlah adsorpsi pada saat kesetimbangan qe, diberikan pada persamaan berikut.
(2.10)
Studi kinetik juga diikuti sesuai dengan metode yang dijelaskan pada metode kesetimbangan Batch diatas. Kapasitas adsorpsi qt (mg/g) pada waktu kontak t yang berbeda (menit) ditentukan dengan menggunakan persamaan berikut:
(2.11)
Dimana C0, Ce, dan Ct (mg/L) masing-masing adalah konsentrasi awal larutan zat pewarna, konsentrasi larutan zat pewarna pada saat kesetimbangan, dan konsentrasi awal larutan zat pewarna pada waktu kontak t yang berbeda (menit). V merupakan volume dalam satuan L dan W merupakan berat adsorben dalam satuan gram.
Persen penyisihan dihitung dengan pernyataan berikut (Ghosh dan Bandyopadhyay, 2017).
(2.12)
Dimana Cf (dalam mg/L) merupakan konsentrasi akhir zat terlarut.
2.5.2.1 Isoterm Langmuir
Persamaan adsorpsi yang lain telah dirumuskan oleh Irving Langmuir yang dikembangkan secara teoritis dengan asumsi bahwa zat yang teradsorpsi oleh permukaan zat padat (solid) hanya dapat membentuk satu lapisan molekul yang menempel pada permukaan zat padat tersebut. Selanjutnya, Langmuir menyatakan bahwa pada proses adsorpsi terdapat 2 (dua) aksi yang saling berlawanan, yaitu pertama kondensasi molekul dari fase gas atau likuid ke permukaan zat padat dan yang kedua adalah pelepasan kembali molekul yang sudah teradsorpsi dari permukaan zat padat ke fase likuid atau gasnya.
Pada saat proses adsorpsi dimulai molekul-molekul adsorbate akan bertumbukan dengan permukaan solid tetapi pada proses adsorpsi selanjutnya, adsorpsi hanya terjadi pada bagian permukaan solid yang belum tertutup oleh lapisan molekul (yang masih kosong). Akibatnya, kecepatan kondensasi molekul di permukaan solid pada tahap awal besar dan makin lama makin turun karena luas permukaan solid yang belum tertutup makin kecil. Di pihak lain, molekul-molekul yang telah teradsorpsi pada permukaan solid kemungkinan akan lepas kembali ke fase likuid atau gasnya, misalnya karena aksi pengadukan yang disebabkan oleh panas (thermal agitation).
Kecepatan pelepasan molekul-molekul yang telah teradsorpsi (kecepatan desorpsi) sebanding dengan luas permukaan solid yang telah tertutup oleh lapisan molekul, dan akan bertambah besar pada saat terjadi keseimbangan (jenuh). Pada saat keseimbangan
terjadi, maka kecepatan kondensasi partikel ke permukaan solid sama dengan kecepatan pelepasan molekul dari permukaan solid ke fase likuid atau gasnya (Said, 2017).
Model ini berdasarkan asumsi bahwa proses biosorpsi terjadi pada permukaan homogen melalui pembentukan lapisan tunggal (monolayer) tanpa interaksi antara molekul terbiosorpsi. Kemudian, semua situs biosorpsi memiliki daya ikat yang sama terhadap biosorbat dan biosorpsi pada satu situs biosorben tidak akan mempengaruhi biosorpsi pada situs berdekatan lainnya (Selvasembian et al, 2018).
Persamaan dari isoterm Langmuir (Kumar et al., 2013) ditulis sebagai berikut:
(2.13)
Terdapat empat bentuk linear dari persamaan 2.12 yang dapat dilihat pada Tabel 2.1 sebagai berikut:
Tabel 2.1 Empat Bentuk Linear dari Model Isoterm Langmuir
Bentuk Persamaan Linear Plot
Garis Miring (Slope)
Perpotongan (Intercept)
Persamaan No.
Langmuir
1 vs. Ce
2.14
Langmuir
2 ( ) vs.
2.15
Langmuir
3 ( ) qe vs. Qm 2.16
Langmuir
4 . vs. qe Ka KaQm 2.17
Sumber: Khaled et al., 2009
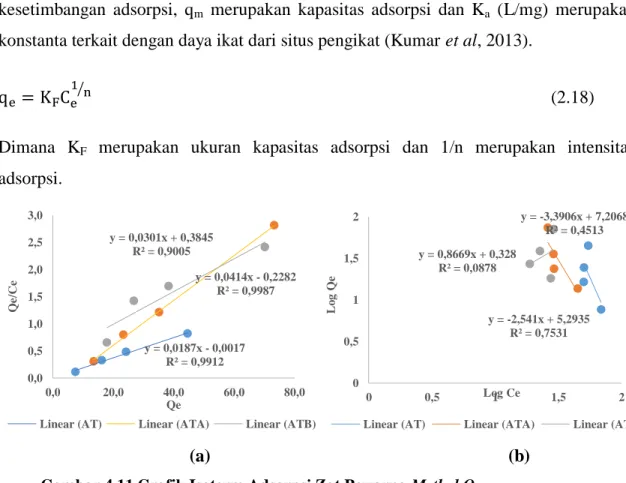
Dimana qe (mg/g) merupakan jumlah methyl orange teradsorpsi per unit massa membran, Ce (mg/L) merupakan konsentrasi larutan Methyl Orange pada kondisi kesetimbangan adsorpsi, qm merupakan kapasitas adsorpsi dan Ka (L/mg) merupakan konstanta terkait dengan daya ikat dari situs pengikat (Kumar et al, 2013).
Kesesuaian isoterm Langmuir dapat dinilai dengan intensitas adsorpsi RL (Habiba et al., 2018). Isoterm Langmuir juga dapat dinyatakan dalam istilah konstana tanpa dimensi dari faktor pemisah atau parameter kesetimbangan, RL dituliskan sebagai (Kanchi et al., 2013):
(2.18) Dimana b dan C0 adalah konstanta Langmuir dan konsentrasi awal dari molekul zat pewarna. Nilai RL mengindikasikan bentuk isoterm (Namasivayam dan Arasi, 1997 dalam Kanchi et al., 2013). Nilai RL antara 0 dan 1 mengindikasikan adsorpsi sesuai, sementara RL> 1, RL = 1, dan RL = 0 mengindikasikan ketidaksesuaian, linear dan isoterm adsorpsi irreversibel.
2.5.2.2 Isoterm Freundlich
Model Freundlich mewakili persamaan empiris, berdasarkan pada biosorpsi distribusi energetik heterogen dari situs aktif disertai dengan interaksi antara molekul terbiosorpsi.
Model isoterm Freundlich mengusulkan biosorpsi beberapa lapis (multilayer). Model ini mempertimbangkan asumsi bahwa penurunan logaritmik dalam entalpi biosorpsi dengan peningkatan dalam bagian kecil situs yang telah terisi pada permukaan biosorben (Selvasembian et al., 2018). Persamaan isoterm Freundlich dipertimbangkan untuk menggambarkan distribusi eksponensial dari pusat aktif yang merupakan karakteristik dari permukaan heterogen dan cakupan permukaan tak terbatas.
Persamaannya dituliskan sebagai (Borah et al., 2015):
⁄ (2.19)
Bentuk linear dari persamaan tersebut adalah
(2.20)
Dimana KF merupakan ukuran kapasitas adsorpsi dan 1/n merupakan intensitas adsorpsi. Nilai dari 1/n lebih kecil dari 1 mengindikasikan adsorpsi yang lebih sesuai.
Menurut Selvasembian et al. (2018), KF merupakan kapasitas biosorpsi berkaitan dengan energi pengikatan (L/g) dan n merupakan faktor heterogenitas mengindikasikan penurunan dari linearitas biosorpsi, juga diketahui sebagai koefisien model isoterm Freundlich. Dari plot log (qe) versus log (Ce), slope dan intersep memberikan nilai konstanta isoterm Freundlich 1/n dan KF.
BAB III
METODE PENELITIAN
Kajian yang dilakukan adalah penyisihan zat pewarna methyl orange menggunakan biosorben ampas teh. Ampas teh yang digunakan berasal dari pabrik pengolahan teh lokal di Sumatera Utara. Penelitian dilaksanakan berdasarkan kerangka penelitian yang merupakan gambaran umum proses penelitian dan dilakukan di tempat lokasi dan waktu penelitian yang telah ditentukan.
3.1 Lokasi Penelitian
Penelitian dilaksanakan di Laboratorium Kimia Dasar Fakultas Matematika dan Ilmu Pengetahuan Alam USU untuk pengeringan dan aktivasi biosorben. Selanjutnya, biosorben dihaluskan menggunakan ball mill di Laboratorium Operasi Teknik Kimia Fakultas Teknik USU. Biosorben kemudian dicuci dengan akuades 70 °C hingga mencapai pH netral dan dilakukan percobaan biosorpsi zat pewarna methyl orange di Laboratorium Penelitian di Fakultas Farmasi USU. Biosorben selanjutnya dikirim ke Laboratorium PT. Labsystematic Indonesia Jakarta Timur untuk menganalisa karakteristiknya dengan uji SEM-EDS, dan di Laboratorium Pengembangan PTKI Medan dilakukan analisa konsentrasi zat pewarna methyl orange dalam limbah cair sintesis dan uji daya serap iodin.
3.2 Waktu Penelitian
Penelitian dilakukan selama ± 4 bulan yaitu mulai bulan September 2018 hingga Desember 2018 yang dilanjutkan dengan pengolahan dan penyusunan data.
3.3 Jenis Penelitian
Penelitian ini termasuk dalam jenis penelitian yang bersifat eksperimental yang dilaksanakan dalam skala laboratorium dengan metode penelitian secara kuantitatif.
3.4 Variabel Penelitian
Variabel penelitian yang digunakan dalam penelitian ini meliputi:
1. Variabel Bebas (Independent Variable) meliputi:
a. Waktu Kontak : 0 menit, 5 menit, 30 menit, 60 menit, 90 menit
b. pH : 2, 5, 8, 11
c. Dosis Biosorben : 0 g, 1 g/L, 2 g/L, 3 g/L, 4 g/L 2. Variabel Terikat (Dependent Variable) meliputi:
Kandungan zat pewarna methyl orange.
3.5 Kerangka Penelitian
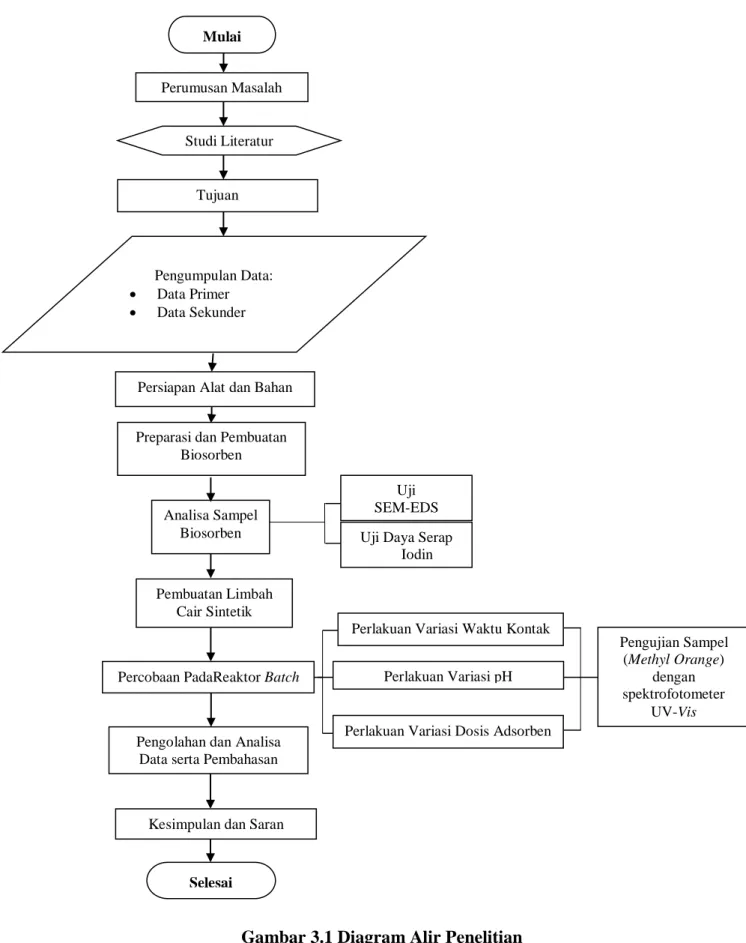
Penelitian diawali dengan perumusan masalah yang didukung dengan studi literatur untuk menentukan tujuan penelitian. Dalam penyusunan laporan penelitian, dikumpulkan data dari sumber primer dan data sekunder. Pengumpulan data primer dilakukan melalui percobaan dan data sekunder melalui studi literatur. Untuk lebih jelasnya, kerangka penelitian untuk tugas akhir ini dapat dilihat dalam bentuk diagram alir penelitian pada Gambar 3.1.
Gambar 3.1 Diagram Alir Penelitian
Percobaan PadaReaktor Batch
Pengolahan dan Analisa Data serta Pembahasan
Kesimpulan dan Saran
Selesai Perumusan Masalah
Tujuan
Pengumpulan Data:
Data Primer
Data Sekunder Studi Literatur
Pembuatan Limbah Cair Sintetik Analisa Sampel
Biosorben
Uji SEM-EDS
Perlakuan Variasi Waktu Kontak
Perlakuan Variasi pH Mulai
Persiapan Alat dan Bahan
Preparasi dan Pembuatan Biosorben
Perlakuan Variasi Dosis Adsorben
Pengujian Sampel (Methyl Orange)
dengan spektrofotometer
UV-Vis Uji Daya Serap
Iodin
3.6 Sumber Data
Data yang dikumpulkan meliputi:
a. Data Primer
Data primer merupakan data yang diperoleh dari hasil analisa penelitian di laboratorium ataupun penelitian di lapangan secara langsung mulai dari pengujian awal sampai pengujian akhir.
b. Data Sekunder
Data sekunder merupakan data yang diperoleh dari studi literatur pustaka.
3.7 Langkah Penelitian
3.7.1 Pembuatan Limbah Cair Sintesis
Tahap awal persiapan dari penelitian ini adalah pembuatan sampel dari air limbah sintetik berupa campuran akuades dengan zat pewarna methyl orange sampai volume ± 1000 mL. Untuk membuat larutan stok methyl orange (100 mg/L) dilarutkan 0,1 g zat pewarna methyl orange ke dalam 1000 mL akuades.
3.7.2 Reaktor Percobaan
Penelitian ini menggunakan erlenmeyer sebagai reaktor batch yang ditempatkan di dalam waterbath shaker yang berfungsi sebagai pengaduk. Reaktor batch (Gambar 3.2) merupakan tempat berlangsungnya proses biosorpsi antara biosorben dengan biosorbat.
Gambar 3.2 Reaktor Batch