PEMBUATAN DAN KARAKTERISASI KITOSAN – KARBON AKTIF DARI AMPAS KOPI SEBAGAI ADSORBEN UNTUK MENURUNKAN KADAR
LOGAM
KADMIUM DAN NIKEL
TESIS
FITRI PURNAMA SARI 167006008
PROGRAM PASCASARJANA ILMU KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
MEDAN 2019
PEMBUATAN DAN KARAKTERISASI KITOSAN – KARBON AKTIF DARI AMPAS KOPI SEBAGAI ADSORBEN UNTUK MENURUNKAN KADAR
LOGAM KADMIUM DAN NIKEL
TESIS
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Magister Sains
FITRI PURNAMA SARI 167006008
PROGRAM PASCASARJANA ILMU KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
MEDAN 2019
PERNYATAAN ORISINALITAS
PEMBUATAN DAN KARAKTERISASI KITOSAN – KARBON AKTIF DARI AMPAS KOPI SEBAGAI ADSORBEN UNTUK MENURUNKAN KADAR
LOGAM KADMIUM DAN NIKEL
TESIS
Saya menyatakan bahwa tesis ini adalah hasil karya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juli 2019
Fitri Purnama sari 167006008
PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Sebagai sivitas akademika Universitas Sumatera Utara, saya yang bertanda tangan dibawah ini
Nama : Fitri Purnama sari
NIM : 167006008
Program Studi : Pasca Sarjana Kimia Jenis Karya Ilmiah : Tesis
Demi pengembangan ilmu pengetahuan, menyetujui untuk memberikan kepada Universitas Sumatera Utara Hak Bebas Royalti Non-Eksklusif (Non-Exclusive Royalty Free Right) atas tesis saya yang berjudul : Pembuatan dan Karakterisasi Kitosan – Karbon Aktif Dari Ampas Kopi Sebagai Adsorben Untuk Menurunkan Kadar Logam Kadmium dan Nikel
Beserta perangkat yang ada (jika diperlukan), dengan Hak Bebas Royalti Non Eksklusif ini, Universitas Sumatera Utara berhak menyimpan, mengalih media, memformat, mengelola dalam bentuk data-base, merawat dan mempublikasikan tesis saya tanpa meminta izin dari saya selama mencantumkan nama saya sebagai penulis dan sebagai pemegang dan atau sebagai penulis dan sebagai pemilik hak cipta.
Demikian pernyataan ini dibuat dengan sebenarnya.
Medan, Juli 2019
Fitri Purnama Sari
PENGESAHAN TESIS
Judul Tesis : Pembuatan dan Karakterisasi Kitosan –
Karbon Aktif Dari Ampas Kopi Sebagai Adsorben Untuk Menurunkan Kadar Logam Kadmium dan Nikel
Kategori : Tesis
Nama : Fitri Purnama Sari Nomor Induk Mahasiswa : 167006008
Program Studi : Pasca Sarjana Kimia
Fakultas : MIPA- Universitas Sumatera Utara
Disetujui di Medan, Juli 2019
Komisi Pembimbing
Ketua Anggota
Prof.Dr.H.Harry Agusnar,MSc.M.Phill Dr.M.Taufik, M.Si
Ketua Program Studi Dekan
Prof. Dr. Tamrin, M.Sc Dr. Kerista Sebayang, MS
Telah diuji pada Tanggal:
PANITIA PENGUJI TESIS
Ketua : Prof.Dr.H.Harry Agusnar,MSc.M.Phill Anggota : 1. Dr. M.Taufik, M.Si
2. Prof. Basuki Wirjosentono, MS.Ph.D 3. Dr. Marpongahtun, M.S
4. Dr. Andriayani, M.Si
PEMBUATAN DAN KARAKTERISASI KITOSAN – KARBON AKTIF DARI AMPAS KOPI SEBAGAI ADSORBEN UNTUK MENURUNKAN KADAR
LOGAM KADMIUM DAN NIKEL
ABSTRAK
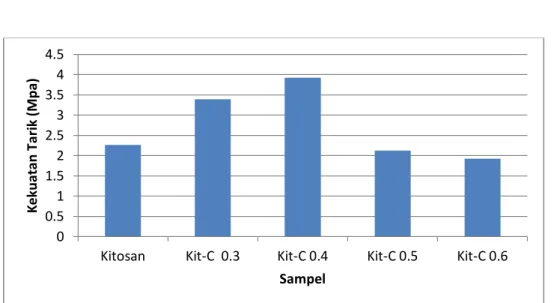
Pembuatan dan karakterisasi kitosan dengan karbon aktif dari ampas kopi sebagai adsorben telah dilakukan dengan tujuan untuk menurunkan kadar logam Kadmium (Cd) dan Nikel (Ni) dalam larutan standar. Penelitian ini terdiri dari beberapa tahap yaitu pembuatan karbon aktif dari ampas kopi, karakterisasi karbon aktif dengan PSA dan FTIR, pembuatan kitosan dengan karbon aktif dengan variasi penambahan karbon aktif adalah sebesar 0.3 g, 0.4 g, 0.5 g, 0.6 g, karakterisasi kitosan – karbon aktif dengan uji kuat tarik, FTIR, SEM, dan uji daya serap logam kadmium dan nikel dengan menggunakan instrument SSA. Adapun hasil karakterisasi ukuran partikel karbon aktif adalah sebesar 50,72 µm dan hasil FTIR karbon aktif menunjukkan gugus OH (3487.3 cm-1), gugus C-H (2924.09 cm-1, 2854.65 cm-1), gugus C=C (1604.77 cm-1), gugus C=H (1442.75 cm-1, 1381.02 cm-1), gugus C-O (1165.00 cm-1, 1118.71 cm-1) dan gugus C=C-H (771.53 cm-1). Karakterisasi kitosan kitosan - karbon aktif dari ampas kopi dengan FT-IR menunjukkan bahwa tidak terdapat perbedaan panjang gelombang: adapun gugus yang muncul yaitu gugus N-H (3448.72 cm-1), gugus C-H (2924.09 cm-1), gugus C=C (1635.64 cm-1), gugus C-N (1381 cm-1 ), dan gugus N-H (3441.01 cm-1). Karakterisasi SEM pada kitosan - karbon aktif menunjukkan bahwa permukaan kasar. Uji kuat tarik kitosan yang terbaik dengan penambahan karbon 0.4 g yaitu 3,924 Mpa. Persen penyerapan logam kadmium dan nikel pada kitosan yang terbaik yaitu dengan penambahan karbon sebesar 0.6 g yaitu 74.54% dan 73.43%.
Kata Kunci : Ampas Kopi, Kitosan, Karbon Aktif, Kadmium, Nikel.
PREPARATION AND CHARACTERIZATION OF CHITOSAN WITH ACTIVATED CARBON FROM COFFEE GROUND
AS ADSORBEN TO REDUCE LEVEL METAL CADMIUM (Cd) AND NICKEL (Ni)
ABSTRACT
Preparation and characterization of chitosan with activated carbon from coffee grounds have been made with the aim of reducing the metal content of Cadmium (Cd) and Nickel (Ni) in standard solutions. This study consisted of several stages:
manufacture of activated carbon from coffee grounds, characterization activated carbon with PSA and FTIR, manufacture chitosan with addition variations activated carbon is 0.3 g, 0.4 g, 0.5 g, 0.6 g, characterization chitosan with activated carbon by tensile strength , FTIR, SEM, and test adsorpstion by using AAS. The results characterization PSA of activated carbon were 50.72 μm and the activated carbon FTIR results showed OH group (3487.3 cm-1), CH group (2924.09 cm-1, 2854.65 cm-1), group C = C (1604.77 cm-1), group C = H (1442.75 cm-1, 1381.02 cm-1), CO group (1165.00 cm-1, 1118.71 cm-1) and group C = CH (771.53 cm-1 ).
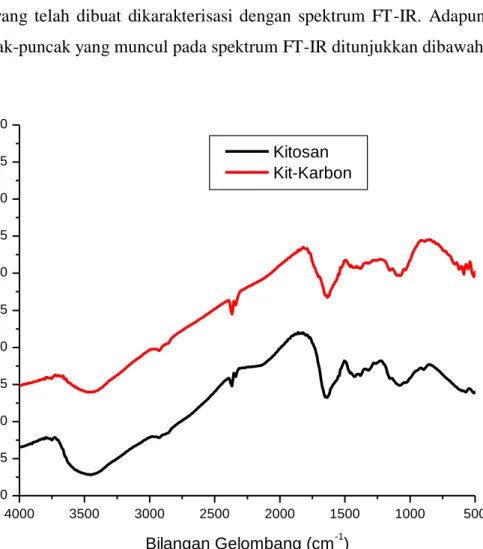
Characterization of chitosan and chitosan - activated carbon from coffee ground by FT-IR shows that there is no difference in wavelength: as for the emerging groups, NH groups (3448.72 cm-1), CH groups (2924.09 cm-1), C = C groups (1635.64 cm- 1), C-N group (1381 cm-1), and NH group (3441.01 cm-1). SEM characterization on chitosan - activated carbon shows a rude surface. The best tensile strength of chitosan with addition of carbon 0.4 g is 3.924 Mpa. Absorptions of Cd and Ni in chitosan that best with addition carbon of 0,6 g that is 74.54% and 73.43%.
Keywords: Activated Carbon, Cadmium, Chitosan, Coffee Ground, Nickel.
PRAKATA
Puji syukur penulis panjatkan kehadirat Allah SWT, dan shalawat beserta salam kepada Rasulullah SAW karena berkat rahmat dan Karunia-Nya lah sehingga tesis ini dapat diselesaikan.
Tesis dengan judul: Pembuatan dan Karakterisasi Kitosan – Karbon Aktif Ampas Kopi Sebagai Adsorben Untuk Menurunkan kadar Logam Kadmium dan Nikel merupakan salah satu syarat untuk memperoleh gelar Magister Sains pada Program Kimia FMIPA USU.
Keberhasilan dari penelitian dan penulisan tesis ini tidak terlepas dari bantuan berbagai pihak yang terlibat secara langsung maupun tidak langsung. Pada kesempatan ini penulis ingin mengucapkan terima kasih kepada :
1. Rektor Universitas Sumatera Utara, Prof. Dr. Runtung Sitepu, S.H, M.Hum atas kesempatan yang diberikan kepada penulis untuk mengikuti dan menyelesaikan pendidikan Program Magister Sains.
2. Dekan Fakultas Matematika Dan Ilmu Pengetahuan Alam Universitas Sumatera Utara, Dr. Kerista Sebayang, MS, atas kesempatan yang diberikan kepada penulis untuk menjadi mahasiswa Program Magister Sains pada Sekolah Pascasarjana Universitas Sumatera Utara.
3. Bapak Prof.Dr.H.Harry Agusnar, MSc, M.Phill dan Bapak Dr. M.Taufiq,MSi selaku Komisi Pembimbing yang memberikan arahan kepada Penulis dengan penuh hingga selesainya penelitian dan tesis ini.
4. Ketua Program Studi Magister, Prof. Dr. Tamrin, M.Sc dan Sekretaris Program Studi Magister Dr. Andriayani, MSi., serta seluruh Staf Pengajar Program Studi Magister Kimia Sekolah Pascasarjana Universitas Sumatera Utara atas kesempatan dan bantuan selama mengikuti Program Pendidikan Magister dan kak Inggih selaku staf administrasi di Pascasarjana USU.
5. Orang tua penulis, Bapak Ir.Sani Hardy dan Ibu Dian Pujawati, yang telah membesarkan dengan penuh kasih sayang, mendidik, memberikan segalanya dan mendoakan dalam keadaan apapun untuk Penulis dan abang penulis dr.Bambang Purnomo, Bambang Budiarto,S.Kom dan kakak penulis dr.Wina Adrian yang memberikan motivasi dan doa kepada Penulis untuk berjuang menyelesaikan pendidikan Magister di Sekolah Pascasarjana F-MIPA USU.
6. Rekan-Rekan Mahasiswa Magister Sekolah Pascasarjana F-MIPA USU Stambuk 2016 A : Dewi Ratih, Fetih, Vinny, Jhon Pattar, Ahmad Budiman, dan Rolly Sianturi, Stambuk 2016 B : Kak Nisa, Efbertias, Sri Rezeki Samosir dan Bang Emir Aulia yang 2 tahun sama-sama berjuang dalam menyelesaikan perkuliahan, penelitian dan penulisan tesis di Program Studi Magister Sekolah Pascasarjana F- MIPA USU.
Penulis berharap dan berdoa kepada Allah SWT agar dapat membalas segala kebaikan yang telah Bapak/Ibu berikan kepada penulis. Amin Ya Rabbal alamiinn.
Penulis menyadari bahwa tesis ini masih banyak kekurangan. Oleh karena itu, diharapkan kritik dan saran yang bersifat membangun demi kesempurnaan tesis ini.
Akhir kata, semoga tesis ini bermanfaat bagi penelitian dan kemajuan ilmu pengetahuan di masa yang akan datang.
Medan, Juli 2019
Fitri Purnama Sari
DAFTAR ISI
Halaman
PENGESAHAN TESIS i
PENETAPAN PANITIA PENGUJI ii
ABSTRAK iii
ABSTRACT iv
PRAKATA v
DAFTAR ISI vii
DAFTAR TABEL x
DAFTAR GAMBAR xi
DAFTAR LAMPIRAN xii
DAFTAR SINGKATAN xiii
BAB 1 PENDAHULUAN
1.1 Latar Belakang 1
1.2 Perumusan masalah 4
1.3 Pembatasan Masalah 4
1.4 Tujuan Penelitian 4
1.5 Manfaat Penelitian 5
1.6 Waktu dan Lokasi Penelitian 5
1.7 Metodologi Penelitian 5
BAB 2 TINJAUAN PUSTAKA
2.1 Kitosan 7
2.1.1 Sifat – Sifat Kitosan 8
2.1.2 Kegunaan Kitosan 9
2.1.3 Modifikasi Kitosan 10
2.2 Kopi 11
2.2.1 Ampas Kopi Sebagai Adsorben 12
2.3 Karbon Aktif 13
2.3.1 Jenis jenis karbon aktif 14
2.4 Proses Adsorpsi 16
2.5 Karaterisasi Adsorben 17
2.5.1 Pengujian Kekuatan Tarik 17 2.5.2 Analisis Distribusi Ukuran Partikel
menggunakan PSA 18 2.5.3 Spektroskopi FT-IR 19 2.5.4 Analisa Permukaan dengan SEM 19 2.6 Spektrofotometer Serapan Atom 21
2.6.1 Prinsip Kerja Spektroskopi Serapan Atom 21 2.6.2 Instrumentasi Spektrofotometer Serapan Atom21 2.6.3 Keuntungan Penggunaan Metode SSA 24
2.7 Logam Berat 24
2.7.1 Kadmium (Cd) 25
2.7.2 Nikel 26
BAB 3 METODE PENELITIAN
3.1 Alat-Alat Penelitian 27
3.2 Bahan-Bahan Penelitian 28
3.3 Prosedur Penelitian 28
3.3.1 Pembuatan Karbon dari Ampas Kopi 28 3.3.2 Karakterisasi Karbon arang akti dari 28 ampas kopi
3.3.2.1 Rendemen 28
3.3.2.2 Kadar Air 29
3.3.2.3 Kadar Abu 29
3.3.2.4 Kadar Zat Mudah Menguap 29
3.3.2.5 Kadar Karbon Terikat 30
3.3.3 Pembuatan Adsorben Kitosan 30 3.3.4 Pembuatan Adsorben Kitosan – Karbon 30 Aktif Ampas Kopi
3.3.5 Uji Tarik dari Adsorben Kitosan dan 31 Kitosan – Karbon Aktif dari
Ampas kopi
3.3.6 Karakterisasi Adsorben Kitosan dan 31 Kitosan-Karbn Aktif Ampas Kopi
3.3.7 Penggunaan Adsorben Kitosan dan 31 Kitosan – Karbon Aktif Ampas Kopi
sebagai adsorben untuk menurunkan Konsentrasi Ion Logam Cd dan Ni
3.4 Bagan Penelitian 32
3.4.1 Pembuatan Karbon Aktif dari Ampas Kopi 32 3.4.2 Pembuatan Adsorben Kitosan 33 3.4.3 Pembuatan Adsorben Kitosan – Karbon 34 Aktif Ampas Kopi
3.4.4 Penggunaan Kitosan dan Kitosan – 35 Karbon Aktif Ampas Kopi sebagai
Adsorben untuk menurunkan konsentrasi Ion Logam Cd dan Ni
BAB 4 HASIL DAN PEMBAHASAN
4.1 Karakterisasi Karbon 36
4.1.1 Karakterisasi Karbon dengan PSA 38 4.1.2 Karakterisasi Ampas Kopi dan Karbon
Aktif ampas kopi dengan FT-IR 38 4.2 Karakterisasi Kitosan – Karbon Aktif 41 4.2.1 Karakterisasi Kitosan-Karbon
Dengan uji FI-IR 41
4.2.2 Karakterisasi Kitosan dan Kitosan – Karbon Aktif dengan SEM 43
4.2.3 Karakterisasi Kitosan – Karbon Aktif
dengan Uji Tarik 44
4.3 Analisis Sampel dengan Instrumen SSA 46 4.3.1 Penentuan sensitifitas instrument SSA 47
4.3.2 Uji Linearitas 49
4.3.3 Analisa Pengukuran Sampel 51 4.3.3.1 Analisa Pengukuran Logam Kadmium 51 4.3.3.2 Analisis Pengukuran Logam Nikel 52 BAB 5 KESIMPULAN DAN SARAN
5.1 Kesimpulan 57
5.2 Saran 57
DAFTAR PUSTAKA 58
LAMPIRAN 63
DAFTAR TABEL
Nomor Judul Halaman
Tabel
2.1 Spesifikasi kitosan 9
2.2 Komposisi kimia ampas kopi 12
4.1 Kualitas Karbon 36
4.2 Data analisis FT-IR ampas kopi dan karbon aktif
ampas kopi 40
4.3 Data analisis kitosan dan kitosan dengan penambahan 42 karbon aktif dari ampas kopi
4.4 Data Kekuatan Tarik Kitosan dan Kitosan – Karbon Aktif 45 4.5 Kondisi Instrumen SSA Merek Shimadzu tipe 46
AA-7000 pada pengukuran konsentrasi logam Kadmium (Cd)
4.6 Kondisi Instrumen SSA Merek Shimadzu tipe 47 AA-7000 pada pengukuran konsentrasi
logam Kadmium (Ni)
4.7 Data Sensitifitas Instrumen SSA 48
4.8 Absorbansi Uji Linearitas Logam Kadimum (Cd) 49 4.9 Absorbansi Uji Linearitas Logam Nikel (Ni) 50 4.10 Hasil Pengukuran kosentrasi Cd dalam sampel dengan SSA 51 4.11 Hasil Pengukuran kosentrasi Ni dalam sampel dengan SSA 53
DAFTAR GAMBAR
Nomor Judul Halaman
Gambar
2.1 Perubahan struktur kitin 7
2.2 Struktur Kimia Karbon Aktif 14
2.3 Skema peralatan SEM 20
2.4 Komponen Instrumen SSA 22
4.1 Grafik Particle Size Analyzer (PSA) Karbon Aktif 38 4.2 Penggabungan Spektrum FT-IR dari Ampas Kopi dan 39
Karbon Aktif Ampas Kopi
4.3 Penggabungan Spektrum FT-IR dari Kitosan
Dan KItosan – Karbon Aktif 41
4.4 Hasil SEM Kitosan dengan perbesaran 43 (a) 64 kali (b) 200 kali (c) 5000 kali
4.5 Hasil SEM Kitosan – Karbon Aktif dengan
Perbesaran (a) 5.000 kali (b) 10.000 kali (c) 15.000 kali 43
4.6 Grafik Uji Kuat Tarik 45
4.7 Kurva Kalibrasi Larutan Standar Kadmium 49 4.8 Kurva Kalibrasi Larutan Standar Nikel 50
4.9 Grafik % Penyerapan Logam Cd 52
4.10 Grafik % Penyerapan Logam Ni 53 4.11 Struktrur Senyawa Kompleks Kitosan dengan Logam 55
DAFTAR LAMPIRAN
Nomor Judul Halaman
Lampiran
1 Perhitungan Kualitas Karbon 64
2 Perhitungan Uji Tarik Kitosan dan Kitosan – Karbon 65 3 Perhitungan Persentase Daya Serap Untuk Logam Cd pada 66
Kitosan-Karbon
4 PSA Karbon Aktif 72
5 SEM Kitosan 73
6 SEM Kitosan – Karbon Aktif 75
7 Spektrum FT-IR Ampas Kopi 77 8 Spektrum FT-IR Karbon Aktif Ampas Kopi 78
9 Spektrum FT-IR Kitosan 79
10 Spektrum FT-IR Kitosan- Karbon Aktif 80
11 Dokumentasi Penelitian 81
DAFTAR SINGKATAN
HCL = Hallow Cathode Lamp
PMT = Photo Multiplier Tube Detector PSA = Particle Size Analyzer
FT-IR = Fourier Transform Infrared Spectrorcopy SSA = Spektrofotometer Serapan Atom
SEM = Scanning Electron Microscopy
BAB 1 PENDAHULUAN
1.1 Latar Belakang
Kegiatan industri yang terus berkembang, mengakibatkan kontaminasi ion logam berat pada air terus meningkat. Hal ini telah menyebabkan masalah lingkungan yang serius di seluruh dunia (Manilin Li et al, 2016). Logam berat dari limbah industri seperti timbal, tembaga dan kadmium dapat mencemari sumber air, permukaan laut dan tanah. Lembaga internasional telah menetapkan kadmium sebagai racun metabolik laten karena sangat berbahaya bagi seluruh kehidupan organisme dan mempengaruhi kesehatan manusia.
Industri elektroplating memiliki risiko yang signfikan terhadap lingkungan hidup dan manusia karena air limbah yang dihasilkan mengandung ion logam berat.
Tidak seperti kontaminan organik, logam berat tidak biodegradable dan cenderung terakumulasi dalam organisme hidup yang menimbulkan efek toksik atau karsinogenik. Salah satu kandungan yang terdapat pada limbah elektroplating adalah logam nikel, logam tersebut biasanya digunakan dalam industri elektroplating karena bersifat antikorosi (Sulaiman et al, 2018). Nikel merupakan logam transisi yang beracun bagi manusia dan organisme lainnya. Pada konsentrasi yang tinggi nikel menyebabkan alergi dan penyebab kanker (Belova et al, 2014).
Kadmium bersifat bersifat non biodegradable dan dapat terakumulasi dalam kehidupan organisme. Menurut Badan Internasional untuk penelitian kanker, kadmium diketahui sebagai karsinogenik (Jeon, 2017). Kadmium yang terakumulasi di ginjal dan hati manusia dapat menyebabkan banyak penyakit seperti disfungsi ginjal, hipertensi, diare, sakit perut, kelainan tulang (Pal, 2017). Limbah yang mengandung logam kadmium berasal dari industri elektroplating, pembuatan baterai,
pestisida dan pertambangan yang dapat menyebabkan pencemaran air, udara dan tanah (Al Malack & Dauda, 2017).
Ada beberapa metode yang digunakan untuk menghilangkan logam berat dari air limbah yaitu presipitasi, membran filtrasi, pertukaran ion (Hergazi, 2013). Metode adsorpsi adalah yang paling sering digunakan karena lebih efisien, lebih ekonomis dan menggunakan adsorben alam yang murah (Manilin Li et al, 2016).
Polimer alam sering dijadikan sebagai adsorben untuk menyerap logam hal ini dikarenakan lebih ekonomis, ramah lingkungan dan aman bagi kesehatan. Salah satunya adalah kitosan. Kitosan merupakan senyawa poli-(2-amino-2-deoksi-β-(1-4)- D-glukopiranosa) dengan rumus molekul (C6H11NO4)n yang dapat diperoleh dari deasetilasi kitin (Rajasree et al, 2013). Kitosan merupakan adsorben yang sangat efektif untuk menghilangkan ion logam berat dikarenakan pada struktur kitosan memiliki gugus hidroksil yang bersifat hidrofilik dan gugus amina yang dapat mengikat logam (Mudasir, 2017), bersifat polikationik dan ketersediaannya sangat melimpah. Diantara berbagai polimer alam, kitosan merupakan biopolimer yang terbesar kedua di alam, setelah selulosa (Changyong C, 2015). Kitosan adalah polimer alam yang sangat efektif digunakan sebagai adsorben karena bersifat biodegradable (Mudasir, 2017), tidak beracun (Changyong, 2015), biokompatibilitas (Liu C, 2014), bioactivity (vakili et al, 2014).
Namun kitosan memiliki beberapa kelemahan yaitu sifat mekanik dan stabilitas termal yang rendah, porositas dan luas permukaan yang kecil .Vakili et al, 2014 memodifikasi struktur kitosan menjadi kitosan manik, membran dan film, untuk meningkatkan kemampuan adsorpsi, sifat fisik dan mekanik, sedangkan Liu &
Bai , 2014 menjelaskan bahwa memodifikasi kitosan menjadi kitosan hidrogel semi IPN (Interpenetrating Network), magnetik nano partikel, polimer grafting kitosan, dan komposit kitosan dapat meningkatkan kemampuan adsorpsi kitosan.
Kopi merupakam minuman yang paling sering di konsumsi di seluruh dunia, mencapai 400 miliar gelas per tahun dan menghasilkan sekitar 8.000 ton ampas
kopi per tahun. Ampas kopi masih dianggap limbah karena membutuhkan waktu yang lama untuk terurai dibandingkan dengan limbah lainnya (Zein et al, 2017).
Salah satu kelebihan ampas kopi dijadikan sebagai adsorben yaitu senyawa tanin terdapat pada ampas kopi yang mengandung gugus gugus polihidroksi dan polifenol yang dapat berikatan dengan kation logam membentuk khelat. (Utomo and Hunter, 2006). Selain itu ampas kopi juga mengandung karbon, nitrogen, senyawa lipofilik, etanol, lignin, alkaloid, polisakarida, dan asam chlorogenic (Pujol et al. 2013).
Bahan yang dapat dijadikan karbon seperti teh, ampas kopi dan sekam padi.
Karbon dari arang aktif dapat menyerap kontaminan anorganik (Utomo, 2015).
Karbon arang aktif adalah adsorben yang umum digunakan karena memiliki sifat fleksibilitas, lebih efektif, luas permukaan yang besar dan kapasitas yang baik untuk menurunkan logam dan senyawa beracun lainnya (Salehi , 2016, Zhang et al, 2016).
Beberapa penelitian telah dilakukan mengenai karbon aktif dari ampas kopi dijadikan sebagai adsorben diantaranya adalah adsorben untuk menyerap logam perak (Jeong, 2017), menyerap logam Ni(II) (Monica et al, 2017), dan menyerap logam timbal (Pb) (Anjali, 2018). Karbon aktif dari ampas kopi dapat digunakan sebagai substrat untuk menempelkan kitosan agar dapat menyerap logam berat. Dengan alasan tersebut, penelitian ini bertujuan memodifikasi kitosan dengan penambahan karbon aktif dari ampas kopi untuk meningkatkan daya serapnya dalam menurunkan kadar logam Cd dan Ni.
1.2 Perumusan Masalah
1. Seberapa besar kemampuan adsorben kitosan – karbon aktif ampas kopi untuk menurunkan kadar logam Cd dan Ni dalam larutan standar.
2. Bagaimana karakteristik dari adsorben kitosan – karbon aktif ampas kopi yang dihasilkan.
1.3 Pembatasan masalah
Adapun pembatasan masalah dalam penelitian ini adalah:
1. Penelitian ini dibatasi pada pembuatan adsorben kitosan yang diperoleh secara komersial.
2. Penelitian ini dibatasi pada pembuatan karbon dari ampas kopi dan dikarakterisasi dengan Particle Size Analyzer (PSA) dan Fourier Transform Infrared Spectroscopy (FTIR).
3. Penelitian ini dibatasi pada penggunaan ampas kopi dari Rumah Kupie Atjeh di jalan Raya Menteng, jenis kopi yang digunakan adalah kopi ulee kareng.
4. Penelitian ini dibatasi pada pembuatan adsorben kitosan - karbon aktif dengan variasi berat 0.3 g; 0.4 g; dan 0.5 g; dan 0,6 g kemudian dikarakterisasi dengan Uji tarik, Fourier Transform Infrared Spectroscopy (FTIR), dan Scanning Electron Microscopy (SEM).
5. Penelitian ini dibatasi pada penggunaan adsorben kitosan – karbon aktif untuk menurunkan kadar logam kadmium dan nikel dengan metode kolom.
6. Penelitian ini dibatasi pada penggunaan logam Cd dan Ni dari larutan standar.
1.4 Tujuan Penelitian
Penelitian ini bertujuan untuk adalah :
1. Untuk mengetahui kemampuan adsorben kitosan yang dimodifikasi dengan karbon aktif dari ampas kopi untuk menyerap logam Cd dan Ni pada larutan standar.
2. Untuk mengetahui persentase daya serap adsorben kitosan dengan penambahan karbon untuk penurunan kadar logam Cd dan Ni dalam larutan standar.
1.5 Manfaat Penelitian
Hasil dari penelitian ini diharapkan dapat memberikan informasi tentang pembuatan adsorben kitosan dengan penambahan karbon aktif dari ampas kopi untuk menurunkan kadar logam Cd dan Ni, dan juga memberikan informasi tentang pemanfaatan karbon aktif dari ampas kopi sebagai adsorben.
1.6 Waktu dan Lokasi Penelitian
1. Penelitian dilaksanakan dari bulan April sampai Desember 2018.
2. Pembuatan adsorben kitosan di Laboratorium Ilmu Dasar USU.
3. Penggilingan ampas kopi dengan instrumen ball mill dilakukan di laboratorium Kimia Fisika FMIPA USU.
4. Analisis ukuran partikel dengan Particle Size Analyzer (PSA) dan SEM dilakukan di PT. Laboratorium Systematic Indonesia
5. Analisis sifat mekanik menggunakan alat uji tarik dilakukan di Laboratorium Magister Tehnik Kimia USU.
6. Analisis FT-IR dilakukan di laboratorium Kimia Organik UGM.
7. Pegujian menggunakan instrumen Spektrofotometer Serapan Atom (SSA) di Balai Riset Standarisasi dan Perindustrian Medan.
1.7 Metodologi Penelitian
Penelitian ini bersifat eksperimen laboratorium, yang meliputi beberapa tahapan penelitian yang dilakukan dalam pembuatan kitosan- karbon aktif ampas kopi sebagai adsorben. Adapun langkah – langkah analisisnya adalah sebagai berikut :
1. Pembuatan karbon aktif dari ampas kopi.
2. Karakterisasi karbon aktif dengan FT-IR dan analisa PSA.
3. Pembuatan adsorben kitosan – karbon aktif ampas kopi.
4. Karakterisasi kitosan - karbon aktif ampas kopi sebagai adsorben dengan uji tarik, FT IR, dan SEM.
5. Pengukuran persentase daya serap adsorben kitosan dengan penambahan karbon untuk penurunan kadar logam Cd dan Ni dalam larutan standar.
Adapun variabel yang digunakan dalam penelitian ini adalah:
Variabel bebas yaitu berat dari karbon ampas kopi yang ditambahkan kedalam kitosan yaitu sebesar 0,3 g; 0,4 g; 0,5 g; dan 0,6 g.
Variabel tetap yaitu Suhu ( C ), Waktu (jam), putaran (rpm).
Variabel terikat yaitu karakterisasi yang dilakukan meliputi analisis morfologi, identifikasi komponen unsur, dan uji tarik.
BAB 2
TINJAUAN PUSTAKA
2.1 Kitosan
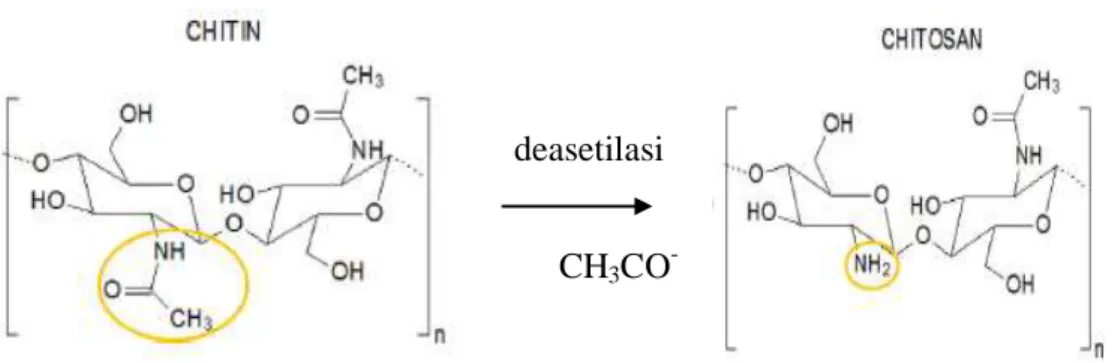
Kitosan merupakan senyawa poliaminosakarida berasal dari deasetilasi kitin, yang dibentuk dari D-glukosamina dan N-asetil-Dglukosamin terikat dengan ikatan β-1,4 glikosidik. Kitosan merupakan biopolymer yang berasal dari limbah kulit Crustacea. Kitin paling banyak diperoleh dari kulit kepiting yang mengandung protein, karotein dan kalsium karbonat. Udang, kepiting, dan lobster mengandung sumber utama kitin sebesar 15 – 20% (Mudasir, 2017). Berikut ini perubahan struktur kitin menjadi kitosan.
Gambar 2.1 Perubahan struktur kitin menjadi kitosan (Sumber: Muxika et al, 2017)
Kitosan murni mengandung gugus amino (NH2), sedangkan kitin murni mengandung gugus asetamida (NH-COCH3). Perbedaan gugus ini akan mempengaruhi sifat-sifat kimia kitin dan kitosan. Sebenarnya kitin dan kitosan yang diproduksi secara komersial memiliki kedua gugus asetamido dan gugus amino pada rantai polimernya, dengan beragam komposisi gugus tersebut (Roberts, 1992).
Kelarutan kitosan dipengaruhi oleh bobot molekul dan derajat deasetilasi (Kartini, 1997). Kitosan tidak beracun, mudah mengalami biodegradasi dan
deasetilasi
CH3CO-
polielektrolit kationik karena mempunyai gugus fungsional gugus amino. Selain gugus amino, terdapat juga gugus hidroksil primer dan sekunder. Adanya gugus fungsi tersebut mengakibatkan kitosan mempunyai kereaktifan kimia yang tinggi (Tokura, 1995). Gugus fungsi yang terdapat pada kitosan memungkinkan juga untuk modifikasi kimia yang beraneka ragam termasuk reaksi-reaksi dengan zat perantara ikatan silang.
2.1.1 Sifat - Sifat Kitosan
Kitosan adalah padatan amorf putih kekuningan yang tidak larut dalam alkali dan asam mineral kecuali pada keadaan tertentu. Kelarutan kitosan yang paling baik adalah dalam larutan asam asetat 1 %, asam format 10 % dan asam sitrat 10 %.
Kitosan tidak dapat larut dalam asam piruvat, asam laktat dan asam – asam anorganik pada pH tertentu, walaupun setelah dipanaskan dan diaduk dengan waktu yang agak lama (Hwang et al, 2001).
Kitosan hanya dapat larut dalam asam encer, seperti asam asetat,asam format, asam sitrat. Kelarutan kitosan dalam asam format ataupun asam asetat dapat membedakan kitosan dan kitin karena kitin tidak dapat melarut dalam keadaan pelarut asam tersebut. Kitosan dibedakan dari kitin oleh kelarutannya dalam larutan asam encer (Dunn et al,1997).
Kitosan dapat dikarakterisasi berdasarkan kualitas sifat fisik intrinsik yaitu kejernihan atau kemurnian, berat molekul, viskositas dan DD. Sifat dan karakteristik kitosan disajikan pada Tabel 2.2 di bawah ini.
Tabel 2.1 Spesifikasi kitosan
Parameter Ciri - ciri
Kadar Air (%) ≤ 10,0
Titik Transisi (Film) 200
Titik Dekomposisi (Film) 250
Ukuran Partikel Serpihan/Bubuk
Kelarutan pH ≤ 6
Warna Larutan Tidak Berwarna
N-Deasetilasi (%) ≥ 70,0
Kelas Viskositas (cps) :
a. Rendah < 200
b. Medium 200 - 799
c. Tinggi 800 - 2000
d. Sangat Tinggi > 2000 Sumber : Sugita et al, 2009.
2.1.2 Kegunaan Kitosan
Dewasa ini aplikasi kitosan sangat banyak dan meluas. Kitosan mudah mengalami degradasi secara biologis, tidak beracun dan baik sebagai flokulan dan koagulan serta mudah membentuk membran atau film. Kitosan merupakan suatu biopolimer alam yang reaktif yang dapat melakukan perubahan-perubahan kimia.
(Sugita et al, 2009).
Adapun kegunaan kitosan dapat dibagi beberapa bidang yaitu : 1. Bidang biomedis
Kitosan memiliki sifat biokompatibilitas, biodegradabilitas, tidak beracun, antimikrobial, sehingga kitosan dapat digunakanpada bidang medis yaitu sebagai obat obatan, obat penyembuh luka, rekayasa jaringan organ, antikoagulan, biomaterial regenerasi tulang, dan antimikroba.
2. Pengolahan air limbah
Struktur kitosan memiliki gugus amina yang efektif dalam menyerap polutan zat organik, anorganik zat pewarna dan ion logam. Kitosan sendiri memiliki sifat tidak beracun, biokompatibel, biodegradabel, biaya rendah, ramah lingkungan dan jumlah yang berlimpah, sehingga kitosan digunakan sebagai material dalam pengolahan air limbah.
3. Dibidang pertanian
Kitosan digunakan sebagai pestisida untuk tanaman pertanian.
4. Pengawet makanan
Kitosan bersifat antimikroba dan antioksidan sehingga digunakan sebagai pengawet makanan. Biasanya kitosan yang digunakan adalah dalam bentuk edible film.
5. Bidang kosmetik
Kitosan digunakan sebagai bahan dalam pembuatan sunscreen.
6. Pembuatan Kertas
7. Kitosan digunakan sebagai bahan dalam pembuatan kertas karena struktur dari kitosan hampir sama dengan selulosa (Muxika et al, 2017).
2.1.3 Modifikasi Kitosan
Kitosan dapat dimodifikasi menjadi berbagai bentuk seperti serpih, hidrogel, membran/film dan butiran. Perbedaan bentuk kitosan akan mempengaruhi pada luas permukaannya. Semakin kecil ukuran kitosan, maka luas permukaan kitosan akan semakin besar.
a. Kitosan Berbentuk Serpihan
Afinitas kitosan bentuk serpihan telah diuji coba terhadap ion , , ,, dan persentase pengikatan adalah 84 – 98, 40 – 92, dan 17 – 46%
berturut–turut.
b. Hidrogel Kitosan
Melarutkan kitosan dalam asam asetat merupakan cara sederhana untuk membentuk hidrogel kitosan. Hidrogel kitosan yang dibentuk oleh penambahan bahan senyawa pengikat silang disebut hidrogel kitosan kovalen atau ionik. Pengikat
ssilang yang digunakan merupakan molekul berbobot molekul lebih rendah daripada bobot molekul kedua rantai polimer yang akan disilangkan.
c. Kitosan Berbentuk Membran
Membran merupakan batas atau penghalang selektif antara dua fase.
Berdasarkan bahan dasarnya membran dibedakan menjadi membran organik dan anorganik. Membran dapat disiapkan dengan menggunakan beberapa metode antara lain pelelehan, pengepresan, track–etching, dan pembalikan fase. Pembalikan fase adalah proses yang mengubah polimer dari bentuk larutan menjadi bentuk padatan secara terkontrol.
d. Kitosan Berbentuk Butiran
Kitosan dapat dibuat menjadi bentuk butiran dengan melarutkan 3 gram kitosan dalam 100 ml larutan asam asetat 1% yang diteteskan pada larutan NaOH 4%
sehingga diperoleh butiran berbentuk bola. Kitosan berbentuk butiran yang terbentuk dikumpulkan dan dicuci dengan akuades (Sugita et al, 2009).
2.2 Kopi
Kopi merupakan tanaman yang berasal dari Afrika dan Asia Selaan, termasuk family Rubicaeae, dengan tinggi mencapa 5meter. Panjang daun sekitar 5-10 cm, lebar 5 cm dengan bunga kopi bewarna putih, buah berbentuk oval panjang sekitar 1,5 cm bewarna hijau kemudian kekuningan lalu hitam bila sudah disangrai.
Biasanya buah kopi terdiri dari 2 buah biji, tetapi sekitar 5 -10 % mempunyai hanya 1 biji saja yang dinamakan “peaberries”. Biji kopi siap dipetik saat berumur 7 sampai 9 bulan (Ameilia, 2016).
Faktor-faktor yang mempengaruhi komposisi minuman termasuk komposisi kopi bubuk panggang, proporsi kopi untuk air, kekerasan dan suhu air, panjang waktu kopi dalam kontak dengan air, dan bahan saringan. Jumlah padatan terlarut di kopi diseduh bervariasi dari 2 sampai 6 g/100 mL.
Secara kimiawi ampas kopi mengandung sebagian besar karbohidrat, kafein dan mineral. Komposisi kimia ampas kopi dapat dilihat pada tabel berikut :
Tabel 2.2 Komposisi kimia ampas kopi
Komponen Jumlah (%)
Kafein 1.25
Asam klorogenik 18.50
Gula 1.45
Karbohidrat 19.90
Peptida 6.0
Potasium 10.00
Mineral lain 13.60
(Wrigley, 1988)
2.2.1 Ampas Kopi Sebagai Adsorben
Ampas kopi mengandung karbon, nitrogen, senyawa lipofilik, etanol, lignin, alkaloid, senyawa polifenol, tanin, polisakarida, dan asam chlorogenic (Pujol et al.
2013). Bahan baku yang dapat dibuat menjadi karbon aktif adalah semua bahan yang mengandung karbon, baik yang berasal dari tumbuh-tumbuhan, binatang ataupun barang tambang. Bahan-bahan tersebut adalah berbagai jenis kayu, sekam padi, tulang binatang, batu-bara, tempurung kelapa, kulit biji kopi.
Ampas kopi merupakan bahan organik yang dapat dibuat menjadi arang aktif untuk digunakan sebagai adsorben atau bahan penyerap. Arang aktif dapat dihasilkan dari bahan-bahan yang mengandung karbon atau dari arang yang diperlakukan dengan cara khusus untuk mendapatkan permukaan yang lebih luas. Luas permukaan karbon aktif berkisar antara 300-3500 m2/gram dan ini berhubungan dengan struktur pori internal yang menyebabkan arang aktif mempunyai sifat sebagai daya serap yang bagus. Arang aktif dapat dibuat melalui dua tahap, yaitu tahap karbonasi dan aktivasi (Sembiring, 2003).
Kandungan hidrokarbon yang terdapat pada biji kopi cukup tinggi yaitu 19,9%. Kandungan hidrokarbon yang cukup tinggi dapat menghasilkan karbon ketika biji kopi disangrai atau dipanaskan, oleh karena itu ampas kopi bubuk yang sudah diseduh dapat dimanfaatkan sebagai arang aktif. Arang aktif dapat digunakan sebagai adsorben karena arang aktif bersifat sangat aktif terhadap partikel-partikel yang kontak dengan arang aktif tersebut (Dewi, 2013).
Karbonasi merupakan proses pengarangan dalam ruangan tanpa adanya oksigen dan bahan kimia lainnya, pada proses ini pembentukan struktur pori dimulai, sedangkan aktivasi dilakukan dengan perendaman arang, arang direndam dalam larutan pengaktif, bahan pengaktif masuk di antara sela-sela lapisan heksagonal karbon aktif dan selanjutnya membuka permukaan yang tertutup dan memperbesar pori. Aktivasi dibagi menjadi dua yaitu aktivasi fisika dan aktivasi kimia. Aktivasi fisika dapat didefinisikan sebagai proses memperluas pori dari arang aktif dengan bantuan panas, uap dan gas CO2. Sedangkan aktivasi kimia merupakan aktivasi dengan pemakaian bahan kimia yang dinamakan aktivator (Sembiring, 2003).
Pada proses pembuatan arang aktif, aktivasi adalah proses yang sangat berperanan agar diperoleh kualitas arang aktif yang baik. Proses aktivasi dapat memperluas permukaan partikel sehingga dapat meningkatkan kemampuan daya serap karbon. Aktivasi arang dapat dilakukan dengan menggunakan bahan-bahan kimia sebagai aktivator atau dengan pemanasan pada suhu yang tinggi (Dewi, 2013).
2.3 Karbon Aktif
Karbon aktif atau disebut juga sebagai arang aktif, adalah suatu jenis karbon yang memiliki luas permukaan yang sangat besar. Hal ini bisa dicapai dengan proses karbonisasi dan aktivasi. Pada proses tersebut terjadi penghilangan hidrogen, gas-gas dan air dari permukaan karbon sehingga terjadi perubahan fisik pada permukaannya.
Aktivasi ini terjadi karena terbentuknya gugus aktif akibat adanya interaksi radikal bebas pada permukaan karbon dengan atom-atom seperti oksigen dan nitrogen.
Biasanya pengaktifan hanya bertujuan untuk memperbesar luas permukaannya saja.
Karbon aktif disusun oleh atom-atom karbon yang terikat secara kovalen dalam suatu kisi yang hexagonal. Kemampuan karbon aktif mengadsorbsi ditentukan oleh struktur kimianya yaitu atom C, H, dan O yang terikat secara kimia membentuk gugus fungsional. Karbon aktif terdiri dari 87-97 % karbon dan sisanya berupa hidrogen, oksigen, sulfur dan nitrogen serta senyawa-senyawa lain yang terbentuk dari proses pembuatan. Volume pori-pori karbon aktif biasanya lebih besar dari 0,2 cm3 /gram. Sedangkan luas permukaan internal karbon aktif yang telah diteliti umumnya lebih besar dari 400 m2 /gr dan bahkan bisa mencapai di atas 1000 m2 /gr (Sudibandriyo, 2003)
Gambar 2.2 Strukur Kimia Karbon Aktif (Sumber : Sudibandriyo, 2003)
2.3.1 Jenis jenis karbon aktif
Berdasarkan bentuknya, karbon aktif dapat dibedakan menjadi tiga golongan, yaitu (Sukir, 2008):
1. Bentuk serbuk.
Karbon aktif berbentuk serbuk dengan ukuran lebih kecil dari 0,18 mm (80#).
Terutama digunakan dalam aplikasi fasa cair dan gas. Digunakan pada industri pengolahan air minum, industri farmasi, terutama untuk pemurnian monosodium glutamat, bahan tambahan makanan, penghilang warna asam furan, pengolahan pemurnian jus buah, penghalus gula, pemurnian asam sitrat, asam tartarik, pemurnian glukosa dan pengolahan zat pewarna kadar tinggi.
2. Bentuk granular.
Karbon aktif bentuk granular/tidak beraturan dengan ukuran 0,2 – 0,5 mm.
Jenis ini umumnya digunakan dalam aplikasi fasa cair dan gas. Beberapa aplikasi dari jenis ini digunakan untuk: pemurnian emas, pengolahan air, air limbah dan air tanah, pemurni pelarut dan penghilang bau busuk.
3. Bentuk pellet.
Karbon aktif berbentuk pellet dengan diameter 0,8-5 mm. Kegunaaan utamanya adalah untuk aplikasi fasa gas karena mempunyai tekanan rendah, kekuatan mekanik tinggi dan kadar abu rendah. Digunakan untuk pemurnian udara, kontrol emisi, tromol otomotif, penghilang bau kotoran, dan pengontrol emisi pada gas buang.
Berdasarkan pori-porinya, karbon aktif dapat dibedakan menjadi tiga jenis, yaitu (Sukir, 2008):
1. Makropori.
Merupakan bagian paling luar dari karbon aktif, dengan jari jari lebih besar dari 50 nm dengan volume pori-pori 0,2-0,5 cm3/gr dan luas permukaan 0,2- 2 m2/gr. Makropori dan mesopori memberikan kapasitas adsorpsi karbon aktif dan kegunaanya terbentuk selama aktivasi.
2. Mesopori.
Memiliki jari-jari 2-50 nm dengan volume pori-pori mencapai 0,02-0,01 cm3/gr dengan luas permukaan 1-100 m2/gr. Mesopori merupakan cabang setelah makropori dan berfungsi sebagai sarana transportasi.
3. Mikropori.
Merupakan pori-pori terkecil dengan jari-jari kurang dari 2 nm dengan volume pori 0,15-0,5 cm3/gr dan luas permukaan mencapai 100-1000 m2/gr.
2.4 Proses adsorpsi
Salah satu metode yang digunakan untuk menghilangkan zat pencemar dari air limbah adalah adsorpsi. Adsorpsi merupakan terserapnya suatu zat (molekul atau ion) pada permukaan adsorben. Mekanisme penyerapan tersebut dapat dibedakan
menjadi dua yaitu, serapan secara fisika (fisisorpsi) dan serapan secara kimia (kemisorpsi). Pada proses fisisorpsi gaya yang mengikat adsorbat oleh adsorben adalah gaya-gaya van derWaals. Molekul terikat sangat lemah dan energi yang dilepaskan pada adsorpsi fisika relatif rendah sekitar 20 kJ/mol. Sedangkan pada proses adsorpsi kimia, interaksi adsorbat dengan adsorben melalui pembentukan ikatan kimia. Kemisorpsi terjadi diawali dengan adsorpsi fisik, yaitu partikel-partikel adsorbat mendekat ke permukaan adsorben melalui gaya van der Waals atau melalui ikatan hidrogen. Kemudian diikuti oleh adsorpsi kimia yang terjad setelah adsorpsi fisika. Dalam adsorpsi kimia partikel melekat pada permukaan dengan membentuk ikatan kimia (biasanya ikatan kovalen), dan cenderung mencari tempat yang memaksimumkan bilangan koordinasi dengan substrat (Atkins, 1999).
Adsorpsi merupakan suatu proses penyerapan oleh padatan tertentu terhadap zat tertentu yang terjadi pada permukaan zat padat karena adanya gaya tarik atom atau molekul pada permukaan zat padat tanpa meresap ke dalam. Proses adsorpsi dapat terjadi karena adanya gaya tarik atom atau molekul pada permukaan padatan yang tidak seimbang. Adanya gaya ini, padatan cenderung menarik molekul-molekul yang lain yang bersentuhan dengan permukaan padatan, baik fasa gas atau fasa larutan ke dalam permukaannya. Akibatnya, konsentrasi molekul pada permukaan menjadi lebih besar dari pada dalam fasa gas atau zat terlarut dalam larutan. Adsorpsi dapat terjadi pada antarfasa padat-cair, padat-gas atau gas-cair. Molekul yang terikat pada bagian antarmuka disebut adsorbat, sedangkan permukaan yang menyerap molekul-molekul adsorbat disebut adsorben. Pada adsorpsi, interaksi antara adsorben dengan adsorbat hanya terjadi pada permukaan adsorben. Adapun faktor-faktor yang mempengaruhi proses adsorpsi adalah luas permukaan, jenis adsorbat, konsentrasi adsorbat, temperatur, pH, kecepatan pengadukan dan waktu kontak adsorpsi.
Isoterm adsorpsi adalah hubungan kesetimbangan antara konsentrasi dalam fase fluida dan konsentrasi di dalam partikel adsorben pada suhu tertentu.
Persamaan isoterm Freundlich ini biasanya digunakan adsorpsi gas hidrokarbon dengan karbon aktif dan isoterm Langmuir sangat cocok untuk proses adsorpsi unimolekular dan adsorpsi reversible. Berikut adalah persamaan isoterm adsorpsi Freundlich dan Langmuir.
Persamaan Isotherm Freundlich:
atau (1)
dimana: q = daya serap (g adsorbat/ g adsorben)
c = konsentrasi adsorbat dalam fluida (air) (g adsorbat/ dm3 fluida)
n dan K (dm3 fluida/ g adsorben) adalah konstanta dan didapat dari percobaan Persamaan Isotherm Langmuir:
atau
(2)
dimana: qo = daya jerap maksimum (g adsorbat/ g adsorben) q = daya serap (g adsorbat/ g adsorben)
c = konsentrasi adsorbat dalam fluida (air) (g adsorbat/ dm3 fluida) K (g adsorbat/ dm3 fluida) adalah konstanta dan didapat dari percobaan
(Tandy et al, 2012)
2.5 Karakterisasi Adsorben 2.5.1 Pengujian Kekuatan Tarik
Sifat mekanis dapat diamati pada sifat kekuatan tarik menggunakan alat pengukur tensometer, jika terhadap bahan diberi tegangan. Secara praktis kekuatan tarik diartikan sebagai besarnya beban maksimum (Fmaks) yang dibutuhkan untuk memutuskan spesimen bahan, dibagi dengan luas penampang bahan (A). Karena selama dibawah pengaruh tegangan, spesimen mengalami perubahan bentuk (deformasi) maka definisi kekuatan tarik dinyatakan dengan luas penampang. Selama deformasi, dapat diasumsikan bahwa volum spesimen tidak berubah, sehingga perbandingan luas penampang semula dengan penampang setiap saat, Aₒ/A= l/lₒ, dengan l dan lₒ masing-masing adalah panjang spesimen setiap saat dan semula.
Hasil pengamatan sifat kekuatan tarik ini dinyatakan dalam bentuk kurva tegangan, yakni nisbah beban dengan luas penampang, terhadap perpanjangan bahan (regangan), yang disebut dengan kurva tegangan-regangan. Bentuk kurva
tegangan−regangan ini merupakan karakteristik yang menunjukkan indikasi sifat mekanis bahan yang lunak, keras, kuat, lemah, rapuh atau liat (Wirjosentono, 1995).
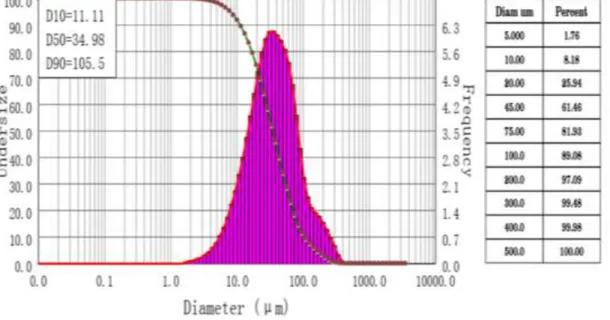
2.5.2 Analisis Distribusi Ukuran Partikel Menggunakan Particle Size Analyzer
Particle Size Analyzer (PSA) dapat menganalisis partikel suatu sampel yang bertujuan menentukan ukuran partikel dan distribusinya dari sampel yang representatif. Distribusi ukuran partikel dapat diketahui melalui gambar yang dihasilkan. Ukuran tersebut dinyatakan dalam jari-jari untuk partikel yang berbentuk bola. Penentuan ukuran dan distribusi partikel menggunakan PSA dapat dilakuan dengan (1) difraksi sinar laser untuk partikel dari ukuran submikron sampai dengan milimeter, (2) counter principle untuk mengukur dan menghitung partikel yang berukuran mikron sampai dengan milimeter, dan (3) penghamburan sinar untuk mengukur partikel yang berukuran mikron sampai dengan nanometer. PSA juga merupakan alat yang mampu mengukur partikel distribusi ukuran emulsi, suspensi dan bubuk kering. Hal ini dapat melakukan berbagai analisis dalam penggunaan operasi yang sangat ramah lingkungan (Sembiring, R.S. 2014).
2.5.3 Spektroskopi FT-IR (Fourier Transform Infrared Spectroscopy)
Penerapan cara data Fourier Transform dalam teknik spektroskopi pertama kali didemonstrasikan oleh cooley dan Turkey pada tahun 1965. Teknik ini dilakukandengan penambahan peralatan interferometer yang telah lama ditemukan oleh Michelson pada akhir abad ke 19. Mechelson telah mendapatkan infomasi diperoleh dari interferometer tersebuut. Fellget (1970) juga telah menggunakan perhitungan fourier transform dari interferogram pada spketrometer pengamatan astronomi (Wirjosentono, 1995).
Sinar Infra Merah (IR) mempunyai penjang gelombang yang lebih panjang dibandingkan dengan Uv Vis, sehingga energinya lebih rendah dengan bilangan geombang antara 600-4000 atau sekitar (1,7 x 10-3)cm sampai dengan 2,5 x 10-
4cm. Sinar infra merah hanya dapat menyebabkan vibrasi (getaran) pada ikatan baik berupa rentangan (streaching) maupun bengkokan (bending). Energy vibrasi untuk molekul adalah spesifik. Namun pada prakteknya spektroskopi IR lebih diperuntukkan untuk menentukan adanya gugus fungsional utama dalam suatu sampelyang diperoleh berdasarkan bilangan gelombang yang dibutuhkan untuk vibrasi tertentu (Marham, 2013)
Analisa FT IR telah membawa tingkat keserbagunaan yang lebih besar ke penelitian penelitian struktur polime. Karena spektrum spektrum bisa di scan, di simpan, dan di transformasikan dalam hitungan detik, teknik ini memudahkan penelitian penelitian reaksi polimer seperti degradasi dan ikat silang (Steven, 2001).
2.5.4 Analisa Permukaan dengan SEM (Scanning Electron Microscopy)
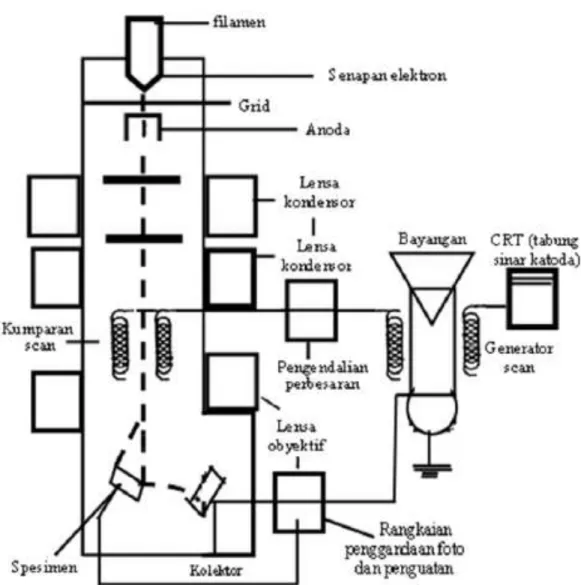
SEM (Scanning Electron Microscope) adalah sebuah mikroskop elektron yang didesain untuk mengamati permukaan objek solid secara langsung. SEM memiliki perbesaran 10-3.000.000 kali dan resolusi sebesar 1-10 nm. SEM juga dapat digunakan untuk menyimpulkan data–data kristalografi, sehingga hal ini dapat dikembangkan untuk menentukan elemen atau senyawa. Mikroskop ini pada dasarnya mampu memeriksa sediaan dengan ukuran yang besar, sehingga tidak terlalu mengalami kesulitan pada cara kerja penyediaan bahan (Soenarto, 1985).
Gambar 2.3 Skema Peralatan SEM (Smallman, 2000)
Dalam penelitian morfologi permukaan SEM terbatas pemakaiannnya, tetapi memberikan informasi yang bermanfaat mengenai topologi permukaan dengan resolusi sekitar 100A. Aplikasi aplikasi yang khas mencakup penelitian disperse disperse pigmen dalam cat, pelepuhan atau peretakan koting, batas batas fasa dalam polipaduan yang tak dapat campur, struktur sel busa – busa polimer, dan kerusakan pada bahan perekat. SEM teristimewa berharga dalam mengevaluasi betapa penanaman (implant) bedah polimerik bereaksi baik dengan lingkungan bagian tubunya (Steven, 2001).
2.6 Spektrofotometer Serapan Atom (SSA)
Peristiwa serapan atom pertama kali diamati oleh Fraunhofer, ketika mengamati garis garis hitam pada spectrum matahari. Spektroskopi serapan atom pertama kali digunakan pada tahun 1955 oleh Walsh. Sesudah itu tidak kurang dari 65 unsur diteliti dan dapat dianalisis dengan cara tersebit. Spektroskopi serapan atom digunakan untuk analisis kuantitatid unsur unsur logam dalam jumlah sekelumit (trace) dan sangat kelumit (ultratrace). Cara analisis ini memberikan kadar total unsur logam dalam suatu sampel dan tidak bergantung pada bentuk molekul dari logam dalam sampel tersebut. Cara ini cocok untuk analisa kelumit logam karena mempunyai kepekaan yang tinggi (batas deteksi kurang dari 1 ppm), pelaksanaannya relatif sederhana, dan interferensinya sedikit. Spektroskopi serapan atom didasarkan pada penyerapan energi sinar oleh atom atom netral, dan sinar yang diserap biasanya sinar tampak atau ultraviolet. Dalam garis besarnya prinsip spektroskopi serapan atom sama saja dengan spektrofotometer sinar tampak dan ultraviolet. Perbedaannya terletak pada bentuk spektrum, cara pengerjaan sampel dan peralatannya (Rohman, 2007).
2.6.1 Prinsip Kerja Spektroskopi Serapan Atom
Prinsip dasar Spektrofotometri serapan atom adalah interaksi antara radiasi elektromagnetik dengan atom. Spektrofotometri serapan atom merupakan metode yang sangat tepat untuk analisis zat pada konsentrasi rendah, teknik ini adalah teknik yang paling umum dipakai untuk analisis unsur.
Radiasi elektromagnetik dikenakan kepada suatu atom, maka akan terjadi eksitasi elektron dari tingkat dasar ke tingkat tereksitasi. Setiap panjang gelombang memiliki energi yang spesifik untuk dapat tereksitasi ke tingkat yang lebih tingggi.
Larutan sampel disemprotkan ke suatu nyala dalam bentuk aerosol dan unsur-unsur di dalam sampel diubah menjadi uap atom sehingga nyala mengandung atom unsur- unsur yang dianalisis. Beberapa diantara atom akan tereksitasi secara termal oleh
nyala, tetapi kebanyakan atom tetap tinggal sebagai atom netral dalam keadaan dasar (ground state). Atom-atom ground state ini kemudian menyerap radiasi yang diberikan oleh sumber radiasi yang terbuat oleh unsur-unsur yang bersangkutan.
Panjang gelombang yang dihasilkan oleh sumber radiasi adalah sama dengan panjang gelombang yang diabsorpsi oleh atom dalam nyala (Khopkar, 2003).
2.6.2 Intrumentasi Spektrofotometer Serapan Atom
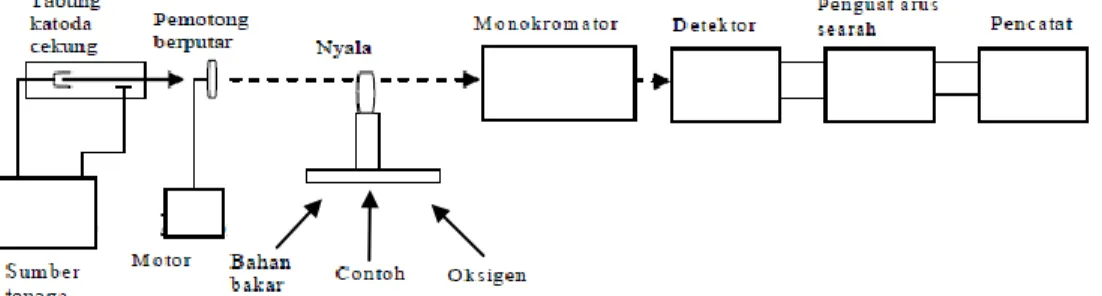
Adapun skematis peralatan spektrofotometer serapan atom dengan nyala sebagai berikut :
Gambar 2.4 Komponen Instrumen Spektrofotometer Serapan Atom
Komponen komponen alat spektrofotometer serapan atom dapat dijelaskan sebagai berikut :
1. Sumber Sinar
Sumber radiasi SSA adalah Hallow Cathode Lamp (HCL). Setiap pengukuran dengan SSA kita harus menggunakan Hallow Cathode Lamp khusus misalnya akan menentukan konsentrasi tembaga dari suatu cuplikan. Maka kita harus menggunakan Hallow Cathode Cu. Hallow Cathode Cu akan memancarkan energi radiasi yang sesuai dengan energi yang diperlukan untuk transisi electron atom. Hallow Cathode Lamp terdiri dari katoda cekung yang silindris yang terbuat dari unsur yang sama dengan yang akan dianalisis dan anoda yang terbuatdari tungsten. Dengan pemberian tegangan pada arus tertentu, logam mulai memijar dan atom-atom logam katodanya akan teruapkan dengan pemercikan. Atom akan tereksitasi kemudian mengemisikan
2. Nyala
Nyala digunakan untuk mengubah sampel yang berupa padatan atau cairan menjadi bentuk uap atomnya, dan juga berfungsi untuk atomisasi. Untuk spektroskopi nyala suatu persyaratan yang penting adalah bahwa nyala yang dipakai hendaknya menghasilkan temperatur lebih dari 20000K untuk memenuhi persyaratan ini digunakan suatu gas pembakar bersama-sama dengan suatu gas pengoksidasi / oksidator, seperti udara ataupun gas dinitrogen oksida (N2O) (Haswell,S.J.,1991).
3. Monokromator
Dalam spektroskopi serapan atom fungsi monokromator adalah untuk memisahkan garis resonansi dari semua garis yang tak diserap yang dipancarkan oleh sumber radiasi (Braun, 1982).
4. Detektor
Detektor pada spektrofotometer serapan atom berfungsi mengubah intensitas radiasi yang datang menjadi arus listrik. Pada Spektrofotometer Serapan Atom yang umum dipakai sebagai detektor adalah tabung penggandaan foton (PMT = Photo Multiplier Tube Detector) (Mulja, 1995).
5. Readout
Readout merupakan suatu alat petunjuk atau dapat juga diartikan sebagai sistem pencatat hasil. Pencatat hasil dilakukan dengan suatu alat yang telah terkalibrasi untuk pembacaan suatu transmisi atau absorbsi. Hasil pembacaan dapat berupa angka atau berupa kurva dari suatu recorder yang menggambarkan absorbansi atau intensitas emisi. Untuk keperluan analisis kuantitatif dengan SSA, maka sampel harus dalam bentuk larutan. Untuk menyiapkan larutan, sampel harus diperlakukan sedemikian rupa yang pelaksanaannya tergantung dari macam dan jenis sampel.
Yang penting untuk diingat adalah bahwa larutan yang akan dinalisis haruslah sangat encer (Rohman, 2007).
2.6.3 Keuntungan Penggunaan Metode SSA
Analisis dilakukan dengan metode Spektrofotometer Serapan Atom (SSA) dengan pertimbangan bahwa :
a. Metode analisis SSA dapat menentukan hamper keseluruhan logam
b. Metode analisis SSA dapat menentukan logam dalam skala kualitatif karena lampunya satu untuk setiap logam
c. Analisis unsur logam langsung dapat ditentukan walau sampel dalam bentuk campuran
d. Analisis unsur logam dapat didapat juga hasil kualitatif
e. Analisis dapat diulangi beberapa kali, tetapi datanya sama (Alfian, 2004).
2.7 Logam Berat
Diantara beberapa jenis logam yang telah ditemukan ternyata hanya beberapa logam yang sangat berbahaya dalam jumlah kecil yang dapat menyebabkan keracunan fatal.Menurut Gossel dan Bricker ada 5 logam yang berbahaya pada manusia yaitu : Arsen(As), cadmium (Cd), timbal (Pb), merkuri (Hg) dan besi (Fe).
Logam bersifat toksik karena logam tersebut terikat dengan ligan dari struktur biologis. Sebagian besar logam menduduki ikatan tersebut dalam beberapa jenis system enzim dalam tubuh. Ikatan tersebut mengakibatkan tidak dapat aktifnya enzim yang bersangkutan, hal inilah penyebab utama toksisitas logam tersebut.
Biasanya logam tertentu terikat dalam daerah ikatan yang spesifik untuk setiap logam dan hal ini dapat dilihat dari gejala gejala dan tanda tanda dari gangguna yang timbul. Tempat ikatan logam yang spesifik tersebut menjadi dasar perkiraan dari organ atau jaringan yang sensitif terhadap keracunan logam dosis kecil. Pada pemberian dosis yang lebih besar, jaringan lain mungkin akan terganggu juga karena logam menduduki ikatan pada jenis enzim yang lebih banyak. Dengan demikian dosis dari logam tersebut merupakan faktor yang sangat penting untuk mencari cara
pengobatan terhadap keracunan logam tersebut, selain meramalkan tentang prognosis dari pasien penderita keracunan logam tersebut (Darmono, 2001)
2.7.1 Kadmium (Cd)
Kadmium adalah logam bewarna putih perak, lunak, mengkilap, tidak larut dalam basa, mudah bereaksi, serta menghasilkan cadmium oksida bila dipanasakan.
Cd umumnya terdapat dalam kombinasi dengan klor (Cd Klorida) atau belerang (Cd Sulfit). Kadmium bisa membentuk ion Cd2+ yang bersifat tidak stabil (Widowati et al, 2008).
Unsur Cd sering ditemukan pada berbagai jenis limbah pertambangan logam seperti timah (Pb) dan seng (Zn). Dalam industri pengolahan hasil tambang, dari proses pemurnian kedua jenis logam tadi akan selalu diperoleh hasil samping limbang yang mengandung Cd yang terbuang ke lingkungan. Dalam batubara berkadar belerang tinggi biasanya terdapat logam Cd dengan kadar yang relatif kecil dibandingkan kadarnya dalam bahan bahan tambang jenis lainnya. Tanah yang berasal dari proses sedimentasi batuan biasanya lebih banyak mengandung Cd dari pada tanah jenis lainnya. Di antara pupuk yang dijual dipasaran, pupuk posfat biasanya mengandung Cd lebih tinggi. Karena itu, semakin lama pemakaian pupuk posfat disuatu area pertanian, akan menaikkan konsentrasi Cd di atas permukaan tanah. Pencemaran Cd melalui pembakaran batubara secara meluas menyebabkan ancaman kesehatan yang luas pula bagi masyarakat.
Keracunan logam Cd dapat berakibat pada timbulnya penyakit paru paru yang akut. Penyakit ini terjadi apabila penderita terpapar oleh uap Cd selama 24 jam.
Selain itu, keracunan akut yang disebabkan oleh uap Cd atau CdO dapat menimbulkan kematian bila konsentrasi Cd atau CdO berkisar dari 2500 sampai 2900 mg/m3. Cadmium lebih beracun bila terhirup melalui saluran pernapasan dari pada melalui saluran pencernaan. Kematian korban disebabkan karena terjadinya oedema paru (Mukhlis, 2014)
2.7.2 Nikel
Nikel adalah logam berwarna putih perak dengan berat jenis 8,5 dan berat atom 58,71 g/mol. Ni merupakan logam yang resistensi terhadap korosi dan oksidasi pada temperatur tinggi sehingga bisa digunakan untuk memproduksi stainless steel.
Bijih nikel lateric (nickel ore) mengandung kadar Ni tinggi, sedangkan ferronikel adalah paduan logam antara nikel dan besi. Logam nikel memiliki sifat kuat, dapat ditempa, serta tahan terhadap karat dan tahan terhadap oksidasi Untuk mengetahui adanya paparan Ni, bisa dilakukan analisis terhadap kadar Ni dalam darah, urin, feses dan rambut. Konsumsi makanan mengandung Ni 600 µg/hari sudah menunjukkan toksisitas pada manusia. Logam ini adalah salah satu penyebab kausatif yang paling biasa dari reaksi hipersensitivitas kulit di masyarakat luas. Reaksi ini biasanya muncul setelah kontak dengan barang logam yang mengandung Ni, misalnya uang logam dan barang-barang perhiasan (Widowati et al, 2008).
Pembuangan limbah yang mengandung Ni mengakibatkan pencemaran Ni pada tanah, air, dan tanaman. Total Ni dalam tanah bisa mencapai 5-500 ppm, sedangkan kadar Ni pada air tanah mencapai 0,005-0,05 ppm dan kadar Ni pada tumbuhan tidak lebih dari 1 ppm (Sukandarrumidi, 2009).
Pada kondisi pH < 9, nikel membentuk senyawa kompleks dengan hidroksida, karbonat, dan sulfat. Pada pH > 9, nikel akan membentuk senyawa kompleks dengan hidroksida dan karbonat, dan selanjutnya mengalami presipitasi.
Demikian juga pada kondisi anaerob, nikel bersifat tidak larut (Effendi, 2003).
BAB 3
METODE PENELITIAN
3.1 Alat-Alat Penelitian
Adapun alat-alat yang digunakan dalam penelitian ini adalah:
Nama Alat Spesifikasi
Alat-alat gelas Pyrex
Neraca Analitis Ohaus
Kertas saring Whatman nomor 42
Pipet Volume Pyrex
Corong Pyrex
Cawan porselen Pyrex
Indikator Universal Sartorius
Spatula
Plat akrilik 15 cm x 7 cm Ayakan 80 mesh
Desikator Magnetic Stirer Bola karet
Hot plate Cimarec
Oven Carbolite
Alumunium foil Bagus
Tanur Thermolyne
Ball mill Retsch
Seperangkat alat uji tarik Gotech AI-7000M
Seperangkat alat (SEM) JSM-35 C Shimadzu
Seperangkat alat Particle Size Analyzer (PSA) Horiba
Seperangkat alat (FTIR) Shidmazu
Seperangkat alat SSA Shimadzu AA-7000F
3.2 Bahan-Bahan Penelitian
Adapun bahan-bahan yang digunakan dalam penelitian ini adalah:
Bahan Spesifikasi
Ampas kopi Aquadest Kitosan
NaOH p.a (E.Merck)
HCl(p) p.a (E.Merck)
Asam asetat p.a (E.Merck)
Larutan 100 mg/L p.a(E.Merck)
Larutan induk 1000 mg/L p.a (E.Merck)
3.3 Prosedur Penelitian
3.3.1 Pembuatan Karbon Aktif dari Ampas Kopi
Ampas kopi dikeringkan dioven pada suhu 1000 C selama 24 jam ,dihaluskan dengan alat ball mill untuk membentuk bubuk halus, kemudian diayak ukuran 80 mesh. Kemudian 100 gram bubuk halus ampas kopi 80 mesh direndam dalam HCl 0.1 M selama 48 jam, kemudian disaring dan dicuci dengan aquadest hingga netral.
Kemudian dipanaskan pada suhu 3000C selama 2 jam, didinginkan pada suhu kamar dan disimpan dalam gelas vial, dilakukan perhitungan rendemen, kadar air, kadar abu, kadar zat mudah menguap dan kadar karbon terikat dan dikarakterisasi dengan Particle Size Analyzer (PSA) dan Transform Infrared Spectrorcopy (FT-IR).
3.3.2 Karakterisasi Karbon arang akti dari ampas kopi 3.3.2.1 Rendemen
Rendemen karbon dihitung dengan cara membandingkan antara bobot bahan baku dengan bobot karbon setelah karbonisasi.
a = bobot sampel yang dikarbonasi (g)
b = bobot karbon yang dihasilkan (g)
3.3.2.2 Kadar Air
Karbon sebanyak 2 gram dimasukkan ke dalam cawan porselin yang telah diketahui bobotnya. Cawan dimasukkan ke dalam oven pada suhu 105°C selama 3 jam kemudian didinginkan dalam desikator dan ditimbang.
a = berat karbon awal (g)
b = berat karbon kering (g)
3.3.2.3 Kadar Abu
Karbon sebanyak 2 gram dimasukkan ke dalam cawan yang telah diketahui bobotnya. Cawan dimasukkan ke dalam tanur pada suhu 600°C selama 3 jam kemudian didinginkan dalam desikator dan ditimbang
a = berat abu (g)
b = berat karbon kering awal (g)
3.3.2.4 Kadar Zat MudahMenguap
Sampel kering sebanyak 2 g dimasukkan ke dalam cawan porselen yang telah diketahui bobot keringnya. Selanjutnya sampel dipanaskan dalam tanur dengan temperatur 450°C selama 45 menit (cawan ditutup serapat mungkin), kemudian didinginkan dalam desikator selama 1 jam dan ditimbang.
a = Bobot sampel sebelum pemanasan (g)
b = Bobot sampel setelah pemanasan (g)
3.3.2.5 Kadar KarbonTerikat
Karbon dalam arang adalah zat yang terdapat pada fraksi padat pirolisis selain abu (zat organik) dan zat-zat atsiri yang masih terdapat pada pori-pori arang. Definisi ini hanya berupa pendekatan.
Kadar karbon terikat (%) = 100% - (b + c) b = zat mudah menguap (%)
c = kadar abu (%)
3.3.3 Pembuatan Adsorben Kitosan
Kitosan ditimbang sebanyak 1,2 g, kemudian dilarutkan dengan asam asetat 3% sebanyak 60 mL, distirer hingga homogen. Dituangkam ke kaca akrilik, dikeringkan di oven pada suhu 600C selama 24 jam. Hasil yang terbentuk diimmersikan dengan NaOH 1M selama 24 jam. Kemudian dilepaskan dari kaca akrilik, dan dicuci dengan akuadest hingga netral. Dikeringkan pada suhu kamar.
Disimpan dalam desikator. Adsorben yang dihasilkan dilakukan analisa FT IR, analisa SEM, dan Uji Tarik.
3.3.4 Pembuatan Adsorben Kitosan – Karbon Aktif Ampas Kopi
Kitosan ditimbang sebanyak 1,2 g, kemudian dilarutkan dengan asam asetat 3% sebanyak 60 mL, ditambahkan 0.3 g karbon ampas kopi, distirer hingga homogen. Dituangkam ke kaca akrilik, dikeringkan di oven pada suhu 600C selama 24 jam. Hasil yang terbentuk diimmersikan dengan NaOH 1M selama 24 jam.
Kemudian dilepaskan dari kaca akrilik, dan dicuci dengan akuadest hingga netral.
dilakukan analisa FT-IR, analisa SEM, dan Uji Tarik. Dilakukan hal yang sama dengan variasi berat penambahan karbon sebanyak 0.4 g; 0.5 g; 0.6 g.
3.3.5 Uji Tarik dari Adsorben Kitosan dan Adsorben Kitosan − Karbon Aktif Ampas Kopi
Uji tarik adsorben kitosan dan adsorben kitosan- karbon ampas kopi dipelajari untuk menentukan kekuatan tarik mereka dan perpanjangan putus.
Pengujian dilakukan nmenggunakan Universal Testing Machine dengan standar ASTM (American Standard Testing Method) D638 Tipe 5. Kekuatan tarik diukur dalam satuan MPa yang menunjukkan kekuatan maksimum (N) per satuan luas penampang silang (mm2) diperlukan untuk memutuskan sampel.
3.3.6 Karakterisasi Adsorben Kitosan dan Adsorben Kitosan – Karbon Aktif Ampas Kopi
Adsorben kitosan dan adsorben Kitosan – Karbon Aktif ampas kopi dikarakterisasi dengan spektroskopi FT-IR (untuk menyelidiki perubahan kimia dalam struktur film sebelum dan setelah perlakuan dengan serbuk karbon ampas kopi. Permukaan morfologi adsorben kitosan diamati dengan SEM (Scanning Electron Microscopy).
3.3.7 Penggunaan Adsorben Kitosan dan Adsorben Kitosan – Karbon Aktif Ampas Kopi sebagai adsorben untuk menurunkan Konsentrasi Ion Logam Kadmium (Cd) dan Nikel (Ni)
Adsorben kitosan dan adsorben kitosan – karbon aktif ampas kopi digunakan untuk menurunkan kadar logam Cd dan Ni pada larutan standar. Dimana adsorben kitosan dan adsorben kitosan - karbon aktif dimasukkan kedalam kolom. Kemudian larutan standar Cd dan Ni dipipet sebanyak 50 mL. Selanjutnya larutan standar Cd dan Ni dilewatkan pada kolom dengan bantuan pompa vakum dan ditampung larutan
untuk dianalisis menggunakan Spektrofotometer Serapan Atom (SSA). Perlakuan yang sama dilakukan untuk adsorben kitosan – karbon aktif ampas kopi dengan variasi berat 0,3 g, 0.4 g, 0.5 g, dan 0,6 g.
3.4 Bagan Penelitian
3.4.1 Pembutan karbon aktif dari ampas kopi