BAB 2
TINJAUAN PPUSTAKA
2.1. Schwannoma
2.1.1. Defenisi Schwannoma
Schwannoma merupakan periveral nerve sheath tumor yang tumbuh
lambat pada bagian distal dari transisi myelinisasi sel oligodendroglial-schwan.
Perkembangan patogenesis dari tumor ini telah dapat dipahami dengan adanya
evaluasi molekuler dan perubahan genetik pada neurofibromatosis 2 (NF2). Gen
NF2 terlokalisasi pada kromosom 22q12. Subsekuen genetik dan pemetaan fisik
menyebabkan ditemukannya gen NF2 pada tahun 1993. Regio DNA ini
mengkode sebuah produk asam amino yang disebut merlin
(meosin-ezrin-radixin-like protein) atau disebut juga schwanomin, dan berfungsi sebagai tumor supresor.
Mutasi dari gen NF2 telah ditemukan tidak hanya pada Schwannoma terkait NF2
tetapi juga pada kasus-kasus sporadis (Osborn AG,2004).
2.1.2. Epidemiologi
Schwannoma dijumpai sekitar 8% dari tumor primer otak, frekuensi pada
wanita 2 kali lebih sering daripada pria dan pada usia pertengahan. Schwannoma
maligna juga berasal dari nervus periver, bersifat rekuren, dan metastase dapat
terjadi secara dini. Hilangnya lengan kromosom 1p dan penambahan pada lengan
kromosom 11q dijumpai pada beberapa Schwannoma, juga dijumpai hilangnya
2.1.3. Jenis – Jenis Schwannoma
Jenis yang paling sering dijumpai ialah vestibular Schwannoma, diikuti
oleh tumor trigeminal nerve sheath. Neoplasma ini dapat tumbuh, meskipun
jarang, dari nervus cranial lainnya baik intrakranial maupun ekstrakranial. Semua
Schwannoma tumbuh sebagai proses mutasi spontan, tetapi kebanyakan tumor
nonvestibular intrakranial dan 5% dari vestibular Schwannoma berkaitan dengan
NF2 (IRSA,2006).
2.1.3.1. Vestibular Schwannoma
VestibularSchwannoma (dikenal juga sebagai acoustic neuroma, acoustic
neurilemoma, atau acoustic neurinoma) yaitu suatu tumor jinak yang
pertumbuhannya lambat pada intrakranial ekstra-aksial yang biasanya
berkembang dari sistem keseimbangan (vestibular) atau yang jarang dari saraf
pendengaran (koklea) di bagian telinga dalam. Tumor berasal dari over produksi
sel schwann, yang biasanya membungkus serat saraf untuk mendukung dan
melindungi saraf (IRSA,2006).
Vestibular Schwannoma mencapai sekitar 8% dari semua tumor di dalam
tengkorak, 1 dari setiap 100.000 orang per tahun mendapat vestibular
Schwannoma. Gejala dapat muncul pada usia berapapun tetapi biasanya terjadi
antara usia 30 dan 60 tahun. Vestibular Schwannoma yang unilateral tidak
dianggap sebagai penyakit herediter. Pria dan wanita sama-sama dapat mengalami
Studi epidemiologis telah melaporkan peningkatan kejadian acoustic
neuroma selama 30 tahun terakhir. Pada tahun 1976, kejadian adalah sekitar 5
tumor per juta penduduk per tahun sedangkan pada tahun 2001 kejadian telah
mencapai 20 tumor per juta penduduk pertahun.(Fortnum H,2009) Schwannoma
terjadi lebih sering pada wanita (59-62%). Hal ini terjadi terlepas dari etnis dan
lebih sering didiagnosis pada pria pada kelompok usia 50-60 tahun (61%).
Diperkirakan bahwa antara 2.000 dan 3.000 kasus baru neuroma vestibular
unilateral didiagnosa setiap tahun di Amerika Serikat, dengan insidens 1:100.000.
Penelitian telah menunjukkan bahwa neuroma unilateral tidak diturunkan , dan
hanya satu dari 1.000 kasus terjadi pada anak dengan ibu yang menderita
kelainan ini (Mauricio AB,2006).
Sebagian besar peningkatan kejadian ini disebabkan munculnya teknik
diagnostik noninvasif yang lebih baik, terutama MRI. Kejadian tumor raksasa
telah menurun, sedangkan tumor kecil dan menengah meningkat. Secara
keseluruhan, median usia saat didiagnosa tidak berubah (sekitar 55 tahun). Tidak
ada data tumor regional atau nasional di Inggris untuk neuroma akustik. Sebagai
tantangan pengumpulan data adalah bahwa banyak dari tumor didiagnosa dengan
imaging saja tanpa konfirmasi
2.1.3.1.1. Etiologi
histologis (Fortnum H,2009).
Vestibular Schwannoma yang unilateral dan bilateral dapat terjadi karena
kerusakan gen pada kromosom 22, yang menghasilkan protein (schwannomine /
merlin) yang mengontrol pertumbuhan sel schwann. Pada pasien
hadir dalam semua atau sebagian besar sel-sel somatik. Namun, pada individu
dengan vestibular Schwannoma yang unilateral
2.1.3.1.2. Patofisiologi
, tidak diketahui peranan gen ini
dalam pembentukan sel Schwannoma (IRSA,2006).
Vestibular dari saraf vestibulocochlear yang superior dan inferior dengan
frekuensi yang sama tampaknya merupakan saraf asal lesi. Sangat jarang
Schwannoma muncul dari bagian koklea dari saraf vestibulocochlear. Karena
vestibular Schwannoma timbul dari sel schwann, pertumbuhan tumor umumnya
menekan serat vestibular ke permukaan. Penghancuran serat vestibular lambat dan
bertahap dan fungsi vestibular berkurang dikompensasikan melalui mekanisme
sentral dari otak. Konsekuensinya banyak pasien mengalami sedikit atau ada
ketidakseimbangan. Setelah tumor tumbuh dan cukup besar untuk mengisi
internal auditory canal, tumor terus tumbuh dengan mengikis atau memperluas
tulang dan / atau dengan memperluas sampai keluar ke cerebellopontine angle
(CPA). Vestibular Schwannoma, seperti space occupying lesion lainnya,
menghasilkan gejala dengan salah satu dari empat mekanisme yang dikenal
seperti : (1) penyumbatan ruang cairan cerebrospinal, (2) displacement batang
otak, (3) kompresi pembuluh darah atau (4) kompresi saraf (IRSA,2006).
Vestibular Schwannoma dapat terus tumbuh sampai mencapai 3-4 cm di
dalam intrakranial sebelum muncul gejala efek massa yang besar. Nervus facialis
cukup tahan terhadap peregangan yang dikenakan oleh pertumbuhan tumor tanpa
kerusakan fungsi klinis yang jelas sampai tumor telah mencapai ukuran yang
dan kompresi tumor sehingga tumor kecil yang terbatas pada internal auditory
canal dapat menghasilkan gejala awal berupa gangguan pendengaran atau
gangguan vestibular. Sebagian tumor mendekati diameter 1,5 cm dalam
intrakranial, umumnya mulai berbatasan dengan permukaan lateral batang otak.
Pertumbuhan lebih lanjut dapat terjadi hanya dengan penekanan atau mendorong
batang otak menuju sisi kontralateral. Sebuah tumor dengan ukuran 2,0 cm
biasanya meluas cukup jauh ke anterior dan superior untuk menekan saraf
trigeminal dan kadang-kadang menghasilkan hipoestesia wajah . Pertumbuhan
lebih dari 4,0 cm pada umumnya menghasilkan penipisan progresif cerebral
aqueduct dan ventrikel keempat dengan perkembangan akhir menjadi hidrosefalus
2.1.3.2. Facial Nerve Schwannoma
(IRSA,2006).
Neuroma intratemporal atau Schwannoma dari saraf wajah adalah temuan
klinis yang jarang . Tergantung pada lokasi asal dan ukuran lesi. Lesi yang timbul
dalam internal auditory canal dapat hadir muncul gejala yang mirip dengan
acoustic Schwannoma. Schwannoma yang muncul dalam kanal wajah biasanya
menyebabkan kelumpuhan wajah perifer atau c. Ketika neuroma timbul dalam
bagian timpani dari saluran saraf wajah, gejala pertama mungkin tuli konduktif
karena perambahan dari tumor pada rantai tulang pendengaran . Pada neuroma
wajah, daerah yang paling umum terlibat adalah wilayah ganglion getiniculate
Awalnya, Schwannoma saraf wajah menyebabkan penebalan saraf dan
perluasan lumen saluran saraf tulang. Untuk mendeteksi perubahan awal, maka
perlu untuk membandingkan sisi yang terkena dan yang normal. Pembesaran hasil
lesi erosi dari kanal tulang dan keterlibatan struktur lain yang berdekatan seperti
petrosus,telinga tengah dan mastoid . Ketika tumor meluas ke telinga tengah, akan
muncul soft tissue mass (Valsavasori,2005).
Hasil CT menunjukkan ekspansi atau erosi kanal saraf wajah dan jika
tumor meluas ke telinga tengah sebagai massa tumor yang sebenarnya . Studi MR
adalah studi pilihan untuk penilaian ukuran dan perluasan lesi. Sebagian tumor
membesar, gambar MR menunjukkan keterlibatan baik intratemporal dan
intrakranial. Post kontras T1-WI harus diperoleh karena tumor mengalami
penyangatan homogen (Valsavasori,2005).
Sekitar 30% dari semua tumor spinal merupakan Schwannoma. Pada kasus
yang sangat jarang (0,2% dari seluruh tumor tulang primer), Schwannoma dapat
dijumpai sebagai tumor tulang primer tanpa keterlibatan kanalis spinalis (Carney
J, 1990). Usia puncak kejadian tumor ini adalah dekade keempat sampai dekade
ketujuh. Sebagaimana meningioma, insiden Schwannoma meningkat pada pasien
dengan NF-2. Salah satu variasi Schwannoma, psammomatous melanotic
Schwannoma merupakan manifestasi karakteristik dari carneycomplex (Cetinkal
A, 2009).
Secara histologi Schwannoma merupakan proliferasi neoplastik dari sel
schwann, yang dapat memiliki berbagai variasi bentuk (spindle, epithelioid,
melanotic) (Koh JS,2008). Pada Schwannoma klasik (Grade I) potongan histologi
menunjukkan Antoni A (daerah dengan selularitas padat) dan Antoni B
(selularitas rendah, kadang kistik). Pada regio Antoni A, dijumpai Verocay bodies
(sekelompok kecil fibril yang dikelilingi oleh barisan sel neoplastik pararel).
Pada Schwannoma atypia selular menunjukkan perubahan degeneratif
namun tidak memiliki signifikansi prognosis. Perubahan degeneratif lain seperti
formasi kistik, makrofag, infiltrasi limfosit, dan hemosiderin-laden cell sering
dijumpai pada regio Antoni B. Pembuluh darah pada Schwannoma sering
memiliki dinding yang tebal dan mengalami proses sklerosis (Koh JS,2008).
Schwannoma menunjukkan imunoreaktifitas yang difus terhadap protein
S-100. Schwannoma intra medula sangat jarang dijumpai oleh karena itu harus
dibedakan dengan glioma, terutama astrositoma anaplastik (Koh JS,2008).
Schwannoma selular secara keseluruhan memiliki derajat selularitas yang
lebih tinggi dibandingkan dengan Schwannoma klasik dan terdiri dari hampir
seluruhnya regio Antoni A, verocay bodies tidak dijumpai. Penemuan histologi
tipikal pada Schwannoma selular antara lain adalah aktifitas mitosis sedang,
peningkatan indeks labelling Ki-67, atypia selular, dan pola pertumbuhan
fascicular. Oleh karena tingginya selularitas pada subtipe ini dan kurangnya
tampilan histologi patognomonik untuk Schwannoma klasik maka dibutuhkan
2.1.4. Manifestasi Klinis
Schwannoma intrakranial, seperti juga Schwannoma dari spinal,
cenderung memperlihatkan gejala gangguan dari saraf-saraf divisi sensoris.
Schwannoma sring muncul dari komponen vestibular nervus VIII (>90%), divisi
sensori nervus trigeminal (0.8%-8%), nervus fasialis (1.9%), nervus yang keluar
dari foramen jugularis (2.9%-4%), nervus hipoglosus, nervus ekstra okular, dan
nervus olfaktorius. Karena letak yang sangat dekat dengan area dari nervus
kranialis, batang otak, dean cerebelum, Schwannoma sudah menampakkan gejala
bahkan ukuran tumor masih kecil. Namun, sifat pertumbuhan yang lambat dapat
mengaburkan gejala defisit neurologi yang berkembang progresif. Hal ini
menyebabkan tidak dijumpai adanya defisit neurologi yang terjadi secara akut.
2.1.5. Histopatologi
Vestibular Schwannoma adalah neoplasma dari selubung saraf / sel
schwann. Tumor ini biasanya terlihat ditutupi oleh sel spindle, sering dengan inti
palisade dan verocay bodies (Antoni A area) dan daerah yang kurang seluler
dengan pola reticular yang longgar dan degenerasi microcystic terkadang
mengandung banyak sel xanthoma(Antoni B). Tingkat selularitas neoplasma bisa
tinggi atau rendah. Sel-sel spindle seringkali cukup pleomorfik, tetapi jarang
dengan mitosis. Kehadiran pleomorfisme tidak selalu menunjukkan
kecenderungan ganas, tetapi dalam kasus yang jarang diragukan perubahan ganas
dapat muncul terkait dengan peningkatan pertumbuhan. Mungkin ada juga
Ekstensi tumor ke dalam modiolus atau vestibular sepanjang cabang
saraf koklea atau vestibular mungkin ada bahkan dalam vestibular Schwannoma
yang soliter, meskipun lebih sering terjadi pada NF-2. Butiran atau homogen
eksudat cairan biasanya terdapat dalam ruang perilymphatic dari koklea dan
vestibular . Hal ini mungkin timbul sebagai akibat dari tekanan oleh neoplasma
pada vena koklea dan vestibular di meatus auditori internal. Hydrops dari sistem
endolymphatic mungkin terjadi dan pada tumor yang lebih besar ada atrofi sel
ganglion spiral dan serabut saraf di membran basilar
2.1.6 Diagnosa Banding
(Michaels L,2005).
2.1.6.1. Kista Epidermoid
Kista Epidermoid biasanya terjadi pada cerebellopontine cistern yang
jarang terlihat dalam IAC. MRI biasanya ditunjukkan massa nonenhancing
dengan sinyal rendah di T1-WI yang menjadi terang di T2-WI. Tidak seperti kista
aracnoid, kista epidermoid muncul hyperintense pada sequences FLAIR dan
2.1.6.2. Kista Arachnoid
diffusion weighted (Valsavasori, 2005).
Kista arachnoid adalah kelainan bawaan pada arachnoid dan secara
histologis ditandai ependyma dan ruang kistik diisi dengan cairan cerebrospinal
atau cairan xanthochromic. Kejadiannya 1% dari semua lesi intrakranial dan CPA
adalah lokasi kedua yang paling umum. Dua kasus arachnoid kista di CPA telah
dilaporkan dalam literatur dan usia rata-rata pada saat diagnosis tidak diketahui,
tetapi aliran cairan serebrospinal abnormal aliran fluida, trauma, atau inflamasi
Kista menyebabkan gejala yang mirip dengan lesi di CPA lainnya. Mereka
sering sulit untuk didiagnosa karena interval waktu antara timbulnya gejala dan
diagnosis berlangsung beberapa tahun. Pada CT scan lesi muncul kistik dengan
kepadatan rendah yang sama seperti cairan serebrospinal. Dengan CT scan sulit
membedakannya dengan kista epidermoids. Pada MRI mereka juga muncul mirip
dengan cairan serebrospinal, yaitu, hypointense pada gambar T2-WI. Tidak
terlihat adanya enhanchment (Springborg J.B,2008).
2.1.6.3. Meningioma
Kista tanpa gejala tidak memerlukan pengobatan, tetapi harus diikuti
dengan MR scan serial. Microsurgery dekompresi dengan pendekatan
retrosigmoid adalah prosedur yang paling sering direkomendasikan (Springborg
J.B,2008).
Meningioma timbul dari penutup meningeal dari tulang temporal dan dari
ekstensi meningeal dalam internal auditory canal. Sesekali meningioma ektopik
dapat melibatkan rongga telinga tengah tanpa erosi keterlibatan tegmen atau
intrakranial. Keterlibatan saraf wajah dapat terjadi di wilayah ganglion geniculate.
Erosi labirin jarang terjadi. Precontrast dan postcontrast CT dan MRI
diindikasikan pada kasus yang diduga meningioma, karena teknik ini akan
menunjukkan keterlibatan dasar tengkorak dan adanya komponen tumor
intrakranial (Valsavasori, 2005).
Meningioma timbul dalam internal auditory canal dan cerebellopontine
angle dengan klinis dan radiografi mirip acoustic Schwannoma. Diagnosis
canal dan dari falciformis crista, atau jika ada kalsifikasi tersebar dalam massa
Pada MRI, meningioma memiliki penampilan yang beragam. Mayoritas
adalah isodense dengan jaringan otak di sekitarnya dalam T1 WI dan muncul
sebagai massa terang dengan intensitas sinyal tinggi dalam T2- WI. Beberapa
tumor mempertahankan sinyal rendah pada T2-WI, yang sangat sugestif dari
sebuah meningioma. Setelah injeksi bahan kontras, meningioma menjadi
menyangat kuat dan homogen. Kalsifikasi dalam tumor menghasilkan area sinyal
yang kosong. En plaque meningioma biasanya dikenali pada MR sebagai daerah
penebalan meningeal dan enhancement. Bentuk yang khas tetapi bukan temuan
diagnostik dari meningioma adalah apa yang disebutdengan dural tail yang
dihasilkan oleh en plaque ekstensi dari massa tumor atau oleh jaringan
mesothelial reaktif (Valsavasori, 2005). (Valsavasori, 2005).
2.1.6.4. Metastasis
Lesi metastatik yang paling umum pada tulang temporal adalah karsinoma
payudara, paru-paru, prostat dan ginjal. Melanoma dan tumor lain juga
bermetastasis ke tulang temporal. Setiap daerah temporal tulang mungkin terlibat
dan simptomatologi bervariasi tergantung pada lokasi lesi. Pemeriksaan CT atau
MR harus dilakukan untuk menyingkirkan ekstensi intrakranial dari lesi temporal
bone dan menetapkan tingkat keterlibatan tulang temporal. Mereka juga
membantu untuk menyingkirkan adanya metastase intrakranial lainnya
2.1.6.5. Neurofibromatosis
Vestibular Schwannoma bilateral adalah ciri dari neurofibromatosis II
merupakan kelainan genetik pada lengan panjang kromosom 22. Lesi lain yang
ditemukan padai NF II adalah meningioma, sarkoma, Schwannoma dari saraf
kranial kelima atau lainnya, ependymomas, glioma, dan juvenile posterior
subcapsular cataracts. Pada NF II harus dibedakan dari neurofibromatosis I,
kelainan genetik yang lebih umum dari lengan panjang kromosom 17 dan ditandai
dengan adanya beberapa neurofibroma dan cafe au lait spot. Fitur lain dari NF I
adalah plexiform neurofibroma, axillary atau inguinal frecling, glioma optik,
Lisch nodule (hamartoma pada iris), dan displasia tengkorak dan meningen
(Valsavasori, 2005).
Schwannoma akustik bilateral seperti yang terlihat pada NF akan
menyajikan dilema manajemen THT setelah pengangkatan kedua schwannoma
yang sangat sering menyebabkan tuli. Menindaklanjuti audiometri dan studi MR
harus diperoleh sejak dini untuk menentukan tingkat pendengaran dan tingkat
pertumbuhan tumor
2.1.6.6. Lipoma
(Valsavasori, 2005).
Dalam suatu studi pada empat kasus, lipoma itu terletak di fundus dari
IAC. Diagnosis dibuat baik dengan mendapatkan T1-WI dan T2-WI precontras
atau dengan menambahkan teknik penekanan cepat setiap kali massa terang
terlihat pada post kontras T1-WI. Lipomas mungkin juga melibatkan wilayah
2.1.6.7. Aneurysma
Sebuah aneurysma dalam IAC sangat jarang. Dari 3 pasien aneurysma
pada IAC, dipelajari dua aneurysma intrakranial kecil, satu dengan opaque
cisternography dan lainnya dengan CT pneumocystography. Pada kedua
incounces mereka muncul sebagai massa spesifik yang mewakili Schwannoma
akustik kecil. Ketiga lesi dipelajari pada pencitraan MR dan muncul di T1 dan
T2-WI sebagai massa kecil sinyal tinggi mungkin karena trombosis atau aliran
lambat. Setelah injeksi i.v bahan kontras lesi muncul sedikit lebih besar. Pada
operasi ditemukan aneurysma kecil berasal dari arteri labirinth (Valsavasori,
2005).
Aneurysma dalam cerebellopontine cistrn mungkin komponen saraf
akustik atau wajah dan mirip dengan simptomatologi schwannoma. Pada MRI
diperoleh sebelum injeksi iv bahan kontras mendapatkan massa kecil homogen
dengan intensitas tinggi yang dihasilkan oleh bekuan darah. Jika lumen
aneurysma adalah bagian yang utuh, darah yang mengalir akan muncul sebagai
daerah dengan sinyal kosong (Valsavasori, 2005).
2.2. S100
S100 merupakan protein multifungsional dengan berbagai peran dalam
proses selular. S100 bekerja dengan perantaraan ikatan kalsium, walaupun Zn2+
dan Cu2+ juga memiliki peranan dalam aktifitas biologis protein ini (Sedaghat
Anggota ‘S100 protein family’ yang paling banyak dipelajari adalah
S100B, yang memiliki aktifitas neurotropik (pada konsentrasi fisiologis) atau
neurotoksik (pada konsentrasi tinggi). Ekspresi protein ini baik pada serum
maupun pada pewarnaan imunohistokimia dijumpai pada berbagai kelainan klinis.
Ekspresi imunohistokimia protein ini telah secara umum dikenal sebagai petanda
untuk tumor Schwannoma dan melanoma.
2.2.1. Struktur Dan Fungsi S100
S100 protein family memiliki subgrup lengan EF pengikat Ca2+. Protein
ini disebut S100 dikarenakan kelarutannya dalam ammonium sulfat pada pH
normal sebesar 100%. Protein ini pertama kali diidentifikasi oleh B.W.Moore
pada 196 ( Moore BW,1965).
S100 merupakan protein asam berukuran kecil, 10-12kDa, dan memiliki
dua lengan EF yang terpisah, 4 segmen α-helix, memiliki central hinge region
dengan panjang yang bervariasi dan juga domain N- dan C- terminal. Berbeda
dengan gen S100 yang sangat banyak terdapat pada vertebrata, protein ini tidak
dijumpai pada invertebrata. Sampai sekarang ini terdapat paling sedikit 25 protein
yang telah teridentifikasi sebagai anggota S100 protein family, dimana 21
diantaranya memiliki gen pada kromosom lokus 1q21. Kelompok gen ini dikenal
sebagai kompleks diferensiasi epidermal (Marenholz I, 2004).
Keluarga S100 merupakan protein multifungsional yang diekspresikan
pada banyak jaringan. Interaksi S100 dengan berbagai dengan berbagai protein
motilitas, diferensiasi dan pertumbuhan sel, progresi siklus sel, transkripsi,
organisasi struktural membran sel, dinamika kandungan sitoskeleton, proteksi sel
terhadap kerusakan sel oksidatif, fosforilasi protein dan sekresi ( Santamaria–
Kisiel L,2006).
S100 tidak memiliki kapasitas katalis intrinsik. Protein ini secara umum
memiliki cara kerja yang mirip dengan calmodulin dan troponin C, yang
mengalami perubahan struktur dan memodulasi aktifitas biologis melalui ikatan
kalsium (Ikura M, 1996).
Berbagai variasi fungsi S100 ini nampaknya disebabkan oleh:
1. Diversifikasi yang luas pada anggota S100 (25 anggota pada manusia)
2. Perbedaan ikatan metal ion yang berbeda-beda pada setiap S100
3. Distribusi ruang pada kompartemen intraselular spesifik atau
kompartemen ekstraselular
4. Kemampuan S100 untuk membentuk homodimer dan heterodimer non
kovalen, sehingga memungkinkan pertukaran subunit S100
S100B secara spesifik terdapat dalam jumlah yang besar di otak dan
diekspresikan oleh astrosit, oligodendrosit, dan sel schwann. Protein ini diduga
berperan sebagai sinyal regulator intraselular dan ekstraselular, yang dapat
menghasilkan efek neurotropik dan neurotoksik yang tergantung pada
konsentrasinya pada sel neuron (Donato et al,2008). S100 juga mengaktifasi
microglia, dan mungkin berperan dalam patogenesis kelainan neurodegeneratif.
S100B diekspresikan berlebih pada astrositoma dan glioblastoma, Schwannoma
ekstraserebral, terutama sel lemak dan kondrosit, oleh karena itu interpretasi
peningkatan kadar serum S100B sebagai marker cedera otak harus dilakukan
secara berhati-hati (Salama et al, 2008).
2.2.2. Metode Pengukuran S100
S100 dapat dideteksi dengan berbagai metoda analisa seperti
immunoradiometric assay (IRMA), mass spectroscopy, western blot, ELISA
(enzyme linked immunosorbent assay), electrohemiluminence dan PCR
kuantitatif, dapat mendeteksi perubahan ekspresi imunohistokimia atau pada
serum dengan sensitifitas tinggi, sehingga dapat menjadi alat ukur penting pada
diagnosa klinis (Wild D,2001)
S100B (homodimer dari subunit) memiliki berat molekul sebesar 21kD
dan dikodekan dari lengan panjang kromosom 21 (21q22.3). Waktu paruh dari
S100B adalah sekitar 30 menit. Peningkatan kadar serum S100 secara persisten
mengindikasikan adanya pelepasan secara terus menerus dari jaringan yang
terlibat. S100 dieliminasi melalui ginjal( .
Wild D,2001).
RAGE (Receptor for Advanced Glycation Endproducts) merupakan
reseptor multi ligand pada keluarga imunoglobulin. RAGE diduga berinteraksi
dengan berbagai ligand dengan struktur berbeda melalui oligomerasi dari reseptor
pada permukaan sel. Walau demikian mekanisme pasti protein ini belum
protein pengikat kalsium berukuran kecil yang memiliki struktur yang homolog
(Biochimica,2009).
RAGE pertama kali dijelaskan pada tahun 1992 dan sejak itu menarik
perhatian banyak ahli karena keterlibatannya dalam berbagai penyakit termasuk
komplikasi diabetes, pertumbuhan tumor, inflamasi kronis, dan penyakit
neurodegeneratif seperti Alzheimer atau multiple sclerosis (Biochimica,2009).
Beberapa anggota keluarga S100 terbukti berinteraksi dengan RAGE baik
secara in vitro maupun in vivo. Peneliti menemukan fakta yang menarik dimana
banyak ligand RAGE nampaknya berinteraksi dengan domain yang berbeda dari
bagian ekstraselular RAGE dan memicu terjadinya berbagai efek selular
(Biochimica,2009).
RAGE banyak diekspresikan selama masa pertumbuhan terutama pada
otak, tetapi ekspresinya menurun pada jaringan manusia dewasa. RAGE
ditemukan dalam jumlah yang rendah pada neuron, sel otot polos, sel mesangial,
fagosit mononuklear, hepatosit dan miosit jantung, tetapi ditemukan dalam jumlah
besar pada jaringan paru (Brett J,1993).
Ekspresi RAGE juga diperkuat dengan peningkatan kadar ligand pada
keadaan patologis. Sinyal RAGE merupakan proses yang kompleks dan
tergantung jenis sel, tipe dan konsentrasi ligand pada kondisi patologis (R.
Donato,2007).
Proses internalisasi, degradasi, metabolisme RAGE masih kurang
diperantarai oleh membran sel setelah fusi dengan S100B yang mengandng
vesikel sekresi (L.Perrone,2008).
Penyakit yang berhubungan dengan perubahan ekspresi S100 dapat
diklasifikasikan dalam 4 kategori, yaitu:
2.2.4. Penyakit Terkait Perubahan Ekspresi protein
2.2.4.1. Kelainan Neurologis
Sebagaimana GFAP (glial fibrillary acidic protein), S100B diproduksi
oleh astrosit pada central nervous system, peningkatan ekspresi protein ini
menandakan adanya aktifitas astrosit (Steiner J, 2007).S100B lebih tidak spesifik
dibandingkan dengan GFAP, dimana protein ini terdapat pada berbagai jenis sel
neural. Efek autokrin protein ini pada astrosit (upregulation dari IL-6, ekspresi
TNF-alpha) dimediasi melalui interaksi S100 dengan RAGE (Ponath G,2007).
Sekresi S100B merupakan proses awal respon sel glia terhadap cedera
metabolik (kekurangan oksigen, serum, glukosa). Hubungan antara kondisi stress
(cedera otak, gangguan sawar darah otak, iskemik) dan kadar serum S100
nampaknya tergantung glucocorticoid (
Scaccianoce S,2004).
Pada kasus cedera otak traumatik akan mengakibatkan peningkatan kadar
S100 pada serum dan juga pada cairan serebrospinal. Setelah terjadinya cedera
otak traumatik, terjadi peningkatan konsentrasi S100B dan S100A1B pada 31%
dan 48% pasien, tanpa hubungan yang signifikan dengan tanda dan gejala
gangguan kognitif. Kenaikan kadar serum S100B tergantung pada integritas sawar
berhubungan baik dengan gangguan sawar darah otak maupun ekspresi aktif dari
jaringan otak yang terlibat pada reaksi inflamasi sistemik.
Peranan S100 pada cedera otak merupakan bidang yang sedang diteliti
secara luas, beberapa studi menunjukkan indikasi bahwa S100B dapat
menurunkan cedera neuronal dan/atau berperan dalam proses perbaikan neuron
setelah cedera otak traumatik, memicu penyembuhan luka pada trauma dan
memiliki aktifitas tropik parakrin pada jaringan disekitarnya (Sedaghat F,2008).
2.2.4.2. Kelainan Neoplastik
Terdapat berbagai tumor yang menunjukkan ekspresi S100; antara lain
S100B, S100A2, S100A4, S100A6, dan S100P. S100-RAGE signalling pathway
memainkan peranan penting dalam hubungan inflamasi dan kanker, dan progresi
tumor (Hsieh HL,2003). Tumor yang memiliki kadar RAGE rendah akan
mengalami akselerasi apoptosis, penurunan aktifasi NFκB dan secara signifikan
mengakibatkan gangguan proliferasi.
Peningkatan kadar S100A4 (metastasin) berhubungan dengan survival rate
yang rendah pada pasien dengan kanker payudara, dan pada tikus terbukti
menginduksi metastase. Peningkatan konsentrasi serum S100A4 juga ditemukan
pada tumor esofagus dan kolon, pankreas, paru, kandung kemih dan berhubungan
dengan hasil akhir yang lebih buruk dan aktifitas tumor yang lebih agresif.
Terdapat sekresi S100B yang tinggi pada melanoma maligna, yang
berhubungan dengan stadium dan prognosa tumor. Kadar serum S100B digunakan
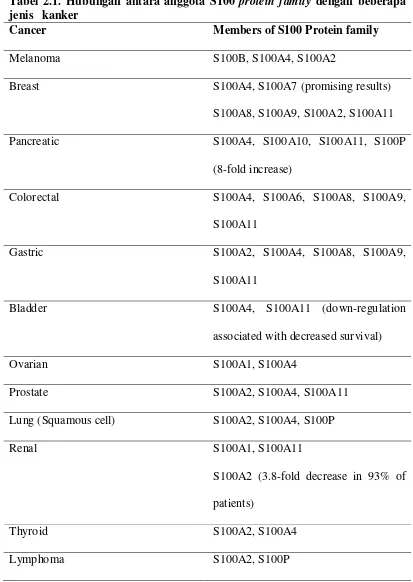
Hubungan antara anggota S100 protein family dan beberapa jenis kanker
tampak pada tabel di bawah (Von Schoultz,1996).
Tabel 2.1. Hubungan antara anggota S100 protein family dengan beberapa jenis kanker
Cancer Members of S100 Protein family
Melanoma S100B, S100A4, S100A2
Breast S100A4, S100A7 (promising results)
S100A8, S100A9, S100A2, S100A11
Pancreatic S100A4, S100A10, S100A11, S100P
(8-fold increase)
Colorectal S100A4, S100A6, S100A8, S100A9,
S100A11
Gastric S100A2, S100A4, S100A8, S100A9,
S100A11
Bladder S100A4, S100A11 (down-regulation
associated with decreased survival)
Ovarian S100A1, S100A4
Prostate S100A2, S100A4, S100A11
Lung (Squamous cell) S100A2, S100A4, S100P
Renal S100A1, S100A11
S100A2 (3.8-fold decrease in 93% of
patients)
Thyroid S100A2, S100A4
Walaupun pada kebanyakan kasus peranan S100 pada kanker masih belum
diketahui dengan jelas, pola ekspresi spesifik protein ini dapat digunakan sebagai
alat prognostik. S100A4 dan S100B berikatan dengan gen supressor tumor p53
dan menghambat fosforilasi, sehingga mengakibatkan down regulation p53 yang
tergantung kalsium.
Berbagai studi telah dilakukan untuk mengetahui peranan p53 wild type
pada neoplasma yang berhubungan dengan S100B melalui inhibisi interaksi p53
dan S100B. S100 lain menghasilkan efek berbeda terhadap aktifitas p53 (S100A2
memicu aktifitas transkripsi p53, dan sebagainya)
2.2.4.3. Kelainan Jantung
S100A1 secara spesifik diekspresikan dalam konsentrasi tinggi pada
miokardium mamalia, dimana protein ini memodulasi kontraktilitas jantung
melalui interaksi protein ini dengan filamen kontraktil dan dengan protein pada
retikulum sarkoplasma (Ehlermann P,2000).
Kombinasi Skala Koma Glasgow (<6 poin) dengan peningkatan
konsentrasi serum dari NSE (>65ng/mL) dan S100 (> 1.5μg/l) pada 48-72 jam
setelah resusitasi kardiopulmonar pada pasien yang mengalami cardiac arrest,
merupakan faktor prediktor hasil akhir neurologis dan gangguan kognitif dengan
spesifitas 100% (sensitifitas 42%) (Ekmektzoglou KA,2007). Peningkatan S100
sendiri meningkatkan risiko kematian dan persistent vegetative state sebesar 12,6
2.2.4.4. Penyakit Inflamasi
S100A8, S100A9, dan S100Al2, diekspresikan secara predominan pada
sel fagosit dan berhubungan kuat dengan fungsi proinflamasi. Protein-protein ini
disekresikan terutma pada tempat inflamasi. Konsentrasi serum dari S100
berhubungan dengan aktifitas penyakit inflamasi; seperti rheumatoid arthritis,
bronkhitis kronis, dan sistik fibrosis (
S100A9, dan S100A12 mengalami proses upregulation pada lesi psoriasis
aktif dan berbagai penyakit inflamasi epidermis lain, dermatitis atopi, mycosis
fungoides dan penyakit Darier (
Foell D,2004).
Peningkatan kadar S100B pada urin yang ditemukan pada bayi baru lahir
dengan gangguan pertumbuhan dalam rahim pada minggu pertama sesudah
kelahiran berhubungan dengan tingkat kerusakan otak. Kadar S100B berhubungan