PARAMETER KUALITAS AIR YANG DIUKUR
Kualitas air adalah karakter (sifat) air yang digambarkan oleh nilai-nilai dari berbagai macam faktor / karakteristik / komponen kualitas air baik secara fisika, kneimia dan biolgi (yang sering disebut sebagai parameter kualitas air). Berikut parameter kualitas air yang di ukur dalam praktikum pengelolaan pencemaran perairan.
A. Kekeruhan (Turbidity)
Kekeruhan (turbidity) adalah gambaran sifat optik air berdasarkan banyaknya cahaya yang diteruskan (setelah diserap oleh partikel-pertikel yang terkandung di dalamnya). Kekeruhan terutama dipengaruhi oleh bahan-bahan yang tersuspensi, seperti lumpur, pasir, bahan organik (plankton, detritus) dan anorganik lainnya. Kekeruhan dapat mengganggu insang ikan, maupun menghalangi penetrasi cahaya untuk keperluan fotosintesis (fitoplankton).
Secara langsung kekeruhan dapat mengganggu proses pernafasan organisme perairan seperti menutupi insang ikan. Kekeruhan juga dapat mengurangi penetrasi cahaya ke dalam perairan.
Prosedur Pengukuran Kekeruhan
Kekeruhan diukur dengan alat “turbidity meter”. Satuan kekeruhan adalah NTU (nephelometric turbidity unit), atau FTU (formazine turbidity unit). Bila yang digunakan adalah alat konvensional Jackson dengan menggunakan lilin, maka satuannya adalah JTU (Jackson turbidity unit)
Lampu
Tabung sampel Sensor
Gambar 1. Prinsip kerja Alat Turbidimeter Hasil dan Pembahasan
Dari hasil praktikum diperoleh hasil untuk air tawar 5,79 NTU dan air laut 9,60 NTU. Kekeruhan yang disebabkan oleh bahan organik maupun maupun anorganik tersuspensi dan terlarut dapat mempengaruhi penetrasi cahaya ke dalam kolom air perairan dan selanjutna akan menurunkan produktivitas primer fitoplankton pada perairan. Wofsy (1983) dalam Cloern (1987) menyatakan cahaya dapat menjadi faktor pembatas bagi fotosintesis ketika konsentrasi partikel tersuspensi melebihi 50 mg/l. Menurut liyold(1985) di acu dalam Effendi (2003), peningkatan nilai turbiditas pada perairan dangkal dan jernih sebesar 25 NTU dapat mengurangi 13%-50 % produktivitas primer. Peningkatan turbidiats sebesar 5 NTU di danau dan sungai dapat mengurangi produktivitas primer berturut-turut sebesar 75 % dan 3%-13%.
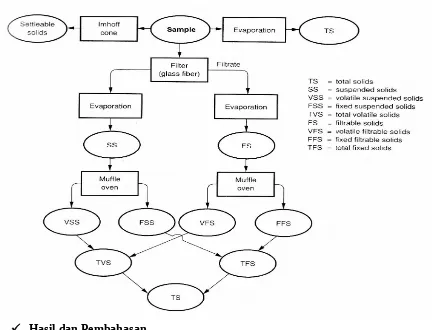
B. Padatan (TSS, TDS, TVS)
Padatan total (residu) adalah bahan yang tersisa setelah air sampel mengalami
evapoarsi dan pengeringan pada suhu tertentu (APHA, 1976). Residu dianggap sebagai
kandungan total bahan terlarut dan tersuspensi dalam air. Selama penentuan residu ini,
sebagian besar bikarbonat yang merupakan anion utama di perairan telah mengalami
tranformasi menjadi karbondioksida, sehingga karbondioksida dan gas-gas lain yang
menghilang pada saat pemanasan tidak tercakup dalm nilai padatan total (Boyd, 1988)
Padatan dalam air meliputi padatan terlarut (TDS: total dissolved solids) dan padatan
tersuspensi (TSS: total suspended solids) serta (TVS: total volatile solids) TDS.
Padatan terlarut (TDS) atau Total Dissolved Solid adalah bahan-bahan terlarut dalam
air yang tidak tersaring dengan kertas saring yang ukuran pori-porinya (porousity) 0.45 m.
Padatan tersuspensi (TSS) adalah bahan-bahan yang tercampur dalam air berupa
suspensi (tidak larut) yang dapat dipisahkan melalui pengendapan dengan cara sentrifus atau
melalui penyaringan dengan kertas filter berukuran pori 0.45 m. TSS menggambarkan
seberapa besar (mg/L) jumlah bahan-bahan yang menyebabkan kekeruhan perairan.
TDS
Padatan terlarut (Total Dissolved Solid) adalah bahan-bahan terlarut (diameter < 10 -6 mm) dan koloid (diameter 106 mm- 10-3 mm) yang berupa bahan-bahan kimia dan
bahan-bahan lain, yang tidak tersaring pada kertas saring berdiameter 0,4 m (Rao,
1992). TDS biasanya disebabkan oleh bahan anorganik yang berupa ion-ion yang biasa terdapat di perairan.
TVS
Berdasarkan sifat volatilitas (penguapan) pada suhu 6000C, padatan tersuspensi dan terlarut dibedakan menjadi volatile solids dan nonvolatile solids. Volatile solids adalah bahan organik yang teroksidasi pada pemanansan dengan suhu 600 0C, sedangkan nonvolatile solids adalah fraksi bahan anorganik yang tertinggal sebagai abu pada suhu tersebut (Rao, 1991)
Pengukuran (TSS, TDS, TVS) TDS
Untuk mendapatkan nilai TDS, sampel air disaring dengan kertas saring tersebut
(menggunakan pompa vacuum), kemudian air sampel tersaring diuapkan (dikeringkan) dalam
oven pada suhu 103-105 C selama satu jam, dan residunya ditimbang. Metode penentuan
TDS ini merupakan rangkaian kegiatan penyaringan, penguapan dan penimbangan, walaupun
Prosedur pentuan TDS:
1. Siapakan filter (milliphore dengan porousity 0,45 m atau yang setara) rendam dalam
akuades selama 24 jam dan biarkan kering.
2. Panaskan mangkuk porselen bersih pada tanur 550 0C atau oven selama 30 menit. 3. Dinginkan dalam dessikator dan timbang (D mg)
4. Pasang peralatan untuk penyaringan dengan “vacuum pump”
5. Pipet air sampel sebanyak 100 ml, aduk saring dengan peralatan filter yang telah disiapkan, tuang air tersaring kedalam mangkuk porselen
6. Uapkan air dalam mangkuk tersebut, mula-mula diatas kompor listrik atau “hot plate”sampai agak kering, kemudian masukkan kedalam oven 105 0C selama 1 jam. 7. Dinginkan mangkuk dasn residu dalam dessikator, kemudian timbang (R mg)
Perhitungan:
penguapan dan penimbangan. Dalam pelaksanaannya dapat digabungkan dengan penentuan
TDS. Filter yang telah direndam dalam akuades, dikeringkan dalam oven dan ditimbang,
digunakan untuk penyaringan 100 ml sampel dengan vacuum pump. Selanjutnya
filter+residu diuapkan dalam oven pada suhu 103-105 C selama 1 jam, lalu ditimbang.
Selisih berat filter setelah penyaringan dan berat filter awal merupakan berat residu (=TSS).
1. Siapkan filter (Milipore dengan porositas 0,45 m) dan vacuum pump. Saring 2 x 20
ml akuades, biarkan penyaringan berlanjut sampai 2-3 menit untuk menghisap
kelebihan air.
2. Keringkan kertas saring (filrter) dalam oven selama 1 jam pada temperatur 103-105 0C, dingikan dalam dissiaktor, lalu timbang (B mg)
3. Ambil 100 ml air sampel dengan gelas ukur, aduk kemudian saring dengan menggunakan kertas saring (filter) yang telah ditimbang pada prosedur no. 2
4. Keringkan filter dan residu dalam oven 103-105 0C selama paling lambat1 jam, dinginkan dalam dessikator, timbang (A mg)
Perhitungan:
TSS(mg/l)❑=(A−B) 1000 ml sampel
Dimana:
A= Berat (mg) filter dan residu B = Berat (mg) filter
TVS
Selain itu, dengan pemanasan atau penguapan lebih lanjut dari padatan total pada
suhu yang lebih tinggi (tanur, pada 550 C, 30 menit), akan diperoleh padatan volatil
total (TVS: total volatile solids) yang dapat memberikan gambaran kandungan bahan organik.
Hasil dan Pembahasan
Dari hasil pengukuran diperoleh nilai TSS air twar 11 mg/l, TSS 15 mg/l serta nilai TDS air tawar 60 mg/l dan TDS air laut 18440 mg/l. Air lautlaut memiliki nilai TDS yang tinggi karena banyak mengandung senyawa kimia, yang juga mengakibatkan tingginya nilai salinititas dan daya hantar listrik. Hubungan antara TDS dan salinitas ditunjukkan dalam Tabel 1 berikut ini:
Tabel 1. Hubungan antara Nilai TDS dan Salinitas
Nilai TDS (mg/liter) Tingkat Salinitas 0-1.0000
1.001-3.0000 3.001-10.000 10.001-100.000 > 100. 0000
Air tawar
Agak asin/ payau (slightly saline)
Keasinan sedang/ payau (moderately saline) Asin (saline)
Nilai TDS perairan sangat dipengaruhi oleh pelapukkan batuan, limpasan dari tanah dan pengaruh antropogenik (berupa limbah domsestik dan industri). Bahan-bahan tersuspensi dan terlarut pada perairan alami tidak bersifat toksik, akan tetapi jika berlebihan, terutama TSS, dapat meningkatkan nilai kekeruhan; yang selanjutnya akan menghambat penetrasi cahaya matahari ke kolom air dan akhirnya berpengaruh terhadap proses fotosintesis perairan.
Rasio antara padatan terlarut dan kedalaman rata-rata perairan merupakan salah satu cara untuk menilai produktivitas perairan. Perbandingan antara TDS dan kedalaman rata-rata nilai dikenal sebagai Morphoedaphic Indeks (MEI). Di Kanada danau-danau yang produktif menunjukkan nilai MEI sekitar 10-30 (Ryder et al., 1974 dalam Col, 1988 ). Kesesuaian perairan untuk kepentingan perikanan berdasarkan nilai padatan tersuspensi ditunjukkan dalam Tabel 2.
permukaan berasal dari air seni dan tinja; juga dari oksidasi zat organik (Ha Ob Cc Nd) secara mikrobiologis, yang berasal dari air alam atau air buangan industri dan penduduk.
Pengukuran Amoniak- Nitrogen
Dalam penentuan amoniak- nitrogen digunakan metode indophenol (metoda phenate). Metode ini memberikan hasil yang cukup baik untuk analisa air kolam atau air yang mempunyai nilai kesadahan total <400 mg/l dan konsentrasi nitrit-N < 5 mg/l. Pereaksi yangdigunakan adalah phenate (phenol), chlorox (oxidizing solution) dan mangan sulfat. Phenol dan hypoclorite (chlorox) bereaksi dalam kondisi larutan basa membentuk phenylquinone-monoimine yang selanjutnya akan bereaksi dengan amoniak membentuk indophenol yang bewarna biru. Kepekatan warna biru sebanding dengan kadar amonia dengan kadar amonia yang ada.
Penambahan Natrium-nitro-prussida dapat memperjelas warna biru indophenol yang terbentuk dapat bervariasi, sehubungan dengan umur pereaksi-pereaksi yang digunakan dan kondisi analisa. Oleh karena itu setiap set penentuan amonia, harus selalu disertai dengan penentuan standar amonia dan blanko
Prosedur Penentuan Amonia-Nitrogen Total (TAN) dalam Metoda phenate:
1. Saring 25-50 ml air sampel dengan kertas saring whatman no.42 (jangan menggunakan vacuum pum, agar tidak ada amonia yang hilang)
2. Pipet10 ml air sampel yang telah disaring, masukkan kedalam gelas piala
3. Sambil diaduk (sebaiknya dengan magnetic stirer) tambahkan 1 tetes MnSO4, 0,5 mlchlorox (oxidizing solution) dan 0,6 ml phenate. Phenate ditambahkan dengan segera dengan menggunakan pipet tetes yang sudah dikalibrasi. Diamkan selama ± 15 menit, sampai pembentukan warna stabil (warna akan tetap stabil sampai beberapa jam)
5. Buat larutan standar dari 10 ml larutan standar amonia (0,30 ppm). Lakukan prosedur 3.
6. Dengan larutan blanko pada panjang gelombang 630 nm, set spektrofotometer pada absorbance 0,000 (atau Transmittance 100%). Kemudian lakukan pengukuran sampel dan larutan standar
Konsentrasi amonia yang terukur tersebut dinyatakan dalam kadar nitrogen (N) yang terdapat dalam amonia (NH3). Untuk mengetahui konsentrasi amonia yang dinyatakan dalam mg NH3/ l (ppm NH3), nilai [TAN] di atas dikalikan dengan faktor seperti persamaan berikut:
mg NH3/L ¿ppm NH3−N
Nilai pengukuran amonia adalah 0,16 mg/l. Menurut McNeely et al., 1979 Effendi,
2003 bahwa kadar amonia pada perairan alami biasanya kuarang dari 0,1 mg/l . namun jika
kadar amonia bebas lebih dari 0,2 mg/l, perairan bersifat toksik bagi beberapa jenis ikan
(Sawyer dan Mc Carty, 1978 dalam Effendi 2003 ). Bentuk amonia tidak terionisasi (NH3
menunjukkan bahwa amonia dan amonium (NH4+) dapat beracun dari pada amonium (Maede,
1985). Namun total amonia diperlukan untuk penurunan efek racun pada pH meningkat dan
perubahan jumlah amonia ke amonium meningkat. Prosentase total amonia nitrogen (NH3 +
NH4+ N) persen sebagai sebagai amonia pada suhu dan nilai pH yang berbeda.
Menurut Schwelder et al., (1985) mekanisme utama toksisitas amonia tidak diketahui. Namun diketahui efek fisiologi pada ikan akibat dari amonia. Jika konsentrasi amonia meningkat di air, ekresi amonia oleh ikan menurun dan level amonia dalam darah dan jaringan meningkat.
D. Lemak dan Minyak
Lemak dan minyak adalah salah satu kelompok yang termasuk pada golongan lipid , yaitu senyawa organik yang terdapat di alam serta tidak larut dalam air, tetapi larut dalam pelarut organik non-polar,misalnya dietil eter (C2H5OC2H5), Kloroform(CHCl3), benzena dan hidrokarbon lainnya. Lemak dan minyak dapat larut dalam pelarut yang disebutkan di atas karena lemak dan minyak mempunyai polaritas yang sama dengan pelaut tersebut.
Bahan-bahan dan senyawa kimia akan mudah larut dalam pelarut yang sama
polaritasnya dengan zat terlarut (like dissolved like). Tetapi polaritas bahan dapat berubah
karena adanya proses kimiawi. Misalnya asam lemak dalam larutan KOH berada dalam
keadaan terionisasi dan menjadi lebih polar dari aslinya sehingga mudah larut serta dapat
diekstraksi dengan air. Ekstraksi asam lemak yang terionisasi ini dapat dinetralkan kembali
dengan menambahkan asam sulfat encer (10 N) sehingga kembali menjadi tidak terionisasi
dan kembali mudah diekstraksi dengan pelarut non-polar.
gliserida berupa trigliserida atau triasilgliserol yang ketiga gugus OH dari gliserol diesterkan
oleh asam lemak
Prosedur Pengukuran Minyak dan Lemak
Analisa lemak dan minyak yang umum dilakukan dapat dapat dibedakan menjadi tiga kelompok berdasarkan tujuan analisa, yaitu;
Penentuan kuantitatif, yaitu penentuan kadar lemak dan minyak yang terdapat dalam bahan makanan atau bahan pertanian. Penentuan kualitas minyak sebagai bahan makanan, yang berkaitan dengan proses ekstraksinya,atau ada pemurnian lanjutan , misalnya penjernihan (refining) ,penghilanganbau (deodorizing), penghilangan warna (bleaching). Penentuan tingkat kemurnian minyak ini sangat erat kaitannya dengan daya tahannya selama penyimpanan,sifat gorengnuya,baunya maupun rasanya.tolak ukur kualitas ini adalah angka asam lemak bebasnya (free fatty acid atau FFA), angka peroksida ,tingkat ketengikan dan kadar air. Penentuan sifat fisika maupun kimia yang khas ataupun mencirikan sifat minyak tertentu. data ini dapat diperoleh dari angka iodinenya,angka Reichert-Meissel,angka polenske,angka krischner,angka penyabunan, indeks refraksi titik cair,angka kekentalan,titik percik,komposisi asam-asam lemak ,dan sebagainya.
Prosedur Pengukuran Minyak dan Lemak:
Penentuan Sifat Lemak Minyak
Jenis-jenis lemak dan minyak dapat dibedakan berdasarkan sifat-sifatnya . Pengujian sifat-sifat lemak dan minyak ini meliputi:
1. penentuan angka penyabunan
mempunyai berat molekul yang besar ,mka angka penyabunan relatif kecil . angka penyabunan ini dinyatakan sebagai banyaknya (mg) NaOH yang dibutuhkan untuk menyabunkan satu gram lemak atau minyak.
Angka penyabunan =
(
Titrasiblanko−Titrasiconto h)xNHCL x BM NaoH w Sampel(gram)2. penentuan angka ester
Angka ester menunjukkan jumlah asam organik yang bersenyawa sebagai ester. Angka ester dihitung dengan selisih angka penyabuanan dengan angka asam. Angka ester = angka penyabunan –angka asam.
3. penentuan angka iodine
Penentuan iodine menunjukkan ketidakjenuhan asam lemak penyusunan lemak dan minyak. Asam lemak tidak jenuh mampu mengikat iodium dan membentuk senyawaan yang jenuh. Banyaknya iodine yang diikat menunjukkan banyaknya ikatan rangkap yang terdapat dalam asam lemaknya. Angka iodine dinyatakan sebagai banyaknya iodine dalam gram yang diikat oleh 100 gram lemak atau minyak
Angka Titrasi ¿
(
Titrasiblanko−Titrasisampel)
X N Na2S2O3x12,691W sampel(gram)
4. penentuan angka Reichert-Meissel
Angka Reichert-Meissel menunjukkan jumlah asam-asam lemak yang dapat larut
dalam air dan mudah menguap. Angka ini dinyatakan sebagai jumlah NaOH 0,1 N dalam ml
yang digunakan unutk menetralkan asam lemak yang menguap dan larut dalam air yang
diperoleh dari penyulingan 5 gram lemak atau minyak pada kondisi tertentu. asam lemak
yang mudah menguap dan mudah larut dalam air adalah yang berantai karbon 4-6.
Dimana ts = jumlah ml NaOH 0,1 N untuk titrasi sampel tb = jumlah ml NaOH 0,1 N untuk titrasi blanko
Penentuan Kualitas Lemak
Faktor penentu kualitas lemak atau minyak, antara lain:
1. penentu angka asam
Angka asam menunjukkan banyaknya asam lemak bebas yang terdapat dalam suatu lemak atau minyak . angka asam dinyatakan sebagai jumlah miligram NaOH yang dibutuhkan untuk menetralkan asam lemak bebas yang terrdapat dalam satu gram lemak atau minyak.
Penentuan angka asam ¿ml NaoH X N NaoH X BM NaoH
W sampel(gram)
2. Penentuan angka peroksida
Angka peroksida menunjukkan tingkat kerusakan dari lemak atau minyak.
Penentuan angka peroksida = ml Na2S2O3X N Na2S2O3X1000 W sampel(gram)
3. Penentuan asam thiobarbiturat(TBA)
Lemak yang tengik mengandung aldehid dan kebanyakan sebagai monoaldehid. Banyaknya monoaldehid dapat ditentukan dengan jalan destilasi lebih dahulu. Monoaldehid kemudian direaksikan dengan thiobarbiturat sehingga terbentuk senyawa kompleks berwarna merah. Intensitas warna merah sesuai dengan jumlah monoaldehid dapat ditentukan dengan spektrofotometer pada panjang gelombang 528 nm.
penentuan kadar air dalam minyak dapat dilakukan dengan cara thermogravimetrri atau cara thermovolumetri.
Kadar air = A−AF X100 %
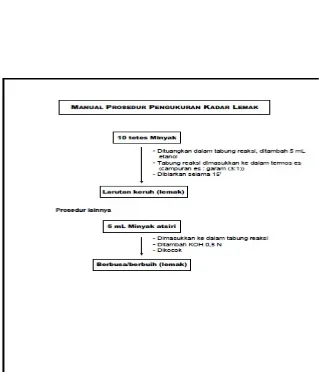
Gambar. 3 Skema Manual Prosedur Pengukuran Kadar lemak
Hasil dan Pembahasan
suatu perairan. Kasus tumpahan lemak khususnya minyak menjadi persoalan rumit yang harus segera diatasi. Sebagai contoh kasus kebocoran ladang minyak dan gas di lepas pantai
memang yang telah menjadi sesuatu yang akrab di telinga kita, terakhir terjadi di Laut Timor pada 21 Agustus 2009 pukul 04.30 WIB oleh operator kilang minyak PTTEP Australia yang berlokasi di Montara Welhead Platform (WHP), Laut Timor atau 200 km dari Pantai
Kimberley, Australia. Kejadian seperti ini merupakan yang kesekian kalinya terjadi di perairan Indonesia, tercatat sampai tahun 2001, telah terjadi 19 peristiwa tumpahan minyak di perairan Indonesia (Mukhtasor, 2007).
Tumpahan minyak tersebut telah memasuki wilayah perairan Nusa Tenggara Timur (NTT) sejauh 51 mil atau sekitar 80 km tenggara Pulau Rote. Tumpahan minyak tentu berdampak pada banyak hal, diantaranya, terhadap kondisi lingkungan laut, biota laut, dan tentu saja berdampak pada ekonomi nelayan Indonesia yang setiap harinya beraktivitas di daerah tersebut. Secara umum dampak langsung yang terjadi adalah sebanyak 400 barel atau 63,6 ribu liter minyak mentah mengalir ke Laut Timor per hari, permukaan laut tertutup 0,0001 mm minyak mentah, minyak mentah masuk ke Zona Eksklusif Ekonomi (ZEE) Indonesia pada 28 Oktober 2009, serta gas hidrokarbon terlepas ke atmosfer.
E. Bakteri Coliform
Bakteri coliform adalah golongan bakteri intestinal, yaitu hidup dalam saluran
pencernaan manusia. Bakteri coliform adalah bakteri indikator keberadaan bakteri patogenik lain. Lebih tepatnya, sebenarnya, bakteri coliform fekal adalah bakteri indikator adanya pencemaran bakteri patogen. Penentuan coliform fekal menjadi indikator pencemaran
dikarenakan jumlah koloninya pasti berkorelasi positif dengan keberadaan bakteri patogen. Selain itu, mendeteksi Coliform jauh lebih murah, cepat, dan sederhana daripada mendeteksi bakteri patogenik lain. Contoh bakteri coliform adalah, Esherichia coli dan Entereobacter
aerogenes. Jadi, coliform adalah indikator kualitas air. Makin sedikit kandungan coliform, artinya, kualitas air semakin baik. Terdapatnya bakteri coliform dalam air dapat menjadi
indikasi kemungkinan besar adanya organisme patogen lainnya. Bakteri coliform dibedakan menjadi 2 tipe, yaitu faecal coliform dan non-faecal coliform. E. coli adalah bagian dari faecal coliform. Keberadaan E. Coli dalam air dapat menjadi indikator adanya pencemaran
air oleh tinja.
fekal kurang dari 2000 colonies/100 mL, dan untuk Standar air minum kurang dari 1 koloni / 100 ml (Anonim1, 2010).
Prosedur Pengukuran Bakteri Coliform
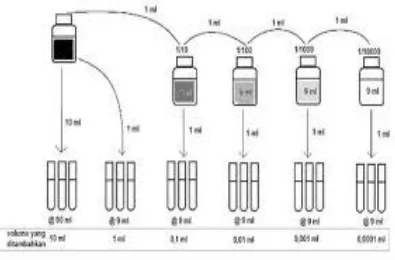
Metode perhitungan MPN Most Probable Number) untuk menghitung jumlah bakteri coliform memiliki prinsip kerja dengan menggunakan larutan sebagai media pertumbuhan atau disebut sebagai media cair (broth) yang ditempatkan dalam tabung reaksi. Hasil perhitungannya dilakukan dengan melihat jumlah tabung yang positif gas. Umumnya setiap pengenceran digunakan 3-5 buah tabung. Lebih banyak tabung yang digunakan menunjukan ketelitian yang lebih tinggi.
Pengenceran harus dilakukan sedemikian rupa sehingga beberapa tabung ditumbuhi satu sel saja sedangkan tabung lain tidak mengandung sel. Setelah inkubasi diharapkan pada beberapa tabung terjadi pertumbuhan (+) sedangkan lainnya (-). Pemilihan kombinasi yaitu berdasrkan pada pengenceran terakhir dimana semua tabung memberikan reasi positif, kemudian diambil dua pengenceran berikutnya.
Perhitungan koloni bakteri berdasarkan atas aktivitas bakteri tersebut dalam melakukan metabolisme. Metode ini disebut juga sebagai APM (Most Probable Number). Bahan uji yang akan dihitung populasi diencerkan beberapa kali, dilanjutkan dengan inokulasi hasil pengenceran tersebut dalam media tertentu yang dapat mendeteksi adanya aktifitas metabolisme bakteri uji. Hasil yang diperoleh kemudian dirujuk pada table APM atau MPN, sehingga populasi dapat diketahui dengan pendekatan tersebut.
Metode APM atau MPN sering dipakai untuk menghitung jumlah populasi bakteri E.coli dalam air limbah, karena kemampuannya dalam melakukan fermentasi dalam substrat
dalam tabung Durham yang sengaja dimasukan dalam tabung reaksinya dengan posisi terbalik.
Nilai MPN adalah perkiraan jumlah unit tumbuh (growth unit) atau unit pembentuk-koloni (colony-forming unit) dalam sampel. Namun, pada umumnya, nilai MPN juga diartikan sebagai perkiraan jumlah individu bakteri. Satuan yang digunakan, umumnya per
100 mL atau per gram. Jadi misalnya terdapat nilai MPN 10/g dalam sebuah sampel air, artinya dalam sampel air tersebut diperkirakan setidaknya mengandung 10 coliform pada setiap gramnya. Makin kecil nilai MPN, maka air tersebut makin tinggi kualitasnya, dan
makin layak minum. Metode MPN memiliki limit kepercayaan 95 persen sehingga pada setiap nilai MPN, terdapat jangkauan nilai MPN terendah dan nilai MPN tertinggi.
Metode MPN terdiri dari tiga tahap, yaitu uji pendugaan (presumtive test), uji konfirmasi (confirmed test), dan uji kelengkapan (completed test). Dalam uji tahap pertama, keberadaan coliform masih dalam tingkat probabilitas rendah; masih dalam dugaan. Uji ini mendeteksi sifat fermentatif coliform dalam sampel. Karena beberapa jenis bakteri selain coliform juga memiliki sifat fermentatif, diperlukan uji konfirmasi untuk mengetes kembali kebenaran adanya coliform dengan bantuan medium selektif diferensial. Uji kelengkapan kembali meyakinkan hasil tes uji konfirmasi dengan mendeteksi sifat fermentatif dan pengamatan mikroskop terhadap ciri-ciri coliform: berbentuk batang, Gram negatif, tidak-berspora. Adapun ragamnya yaitu:
Ada 3 ragam yang biasanya dipakai pada pemeriksaan MPN yaitu : 1. Ragam 511
- 5 tabung yang berisi LB double x 10 ml
Standar analisa air untuk mengetahui adanya bakteri coliform ada 3 melalui tahapan uji yaitu:
1. Uji duga (Presumtive Test)
Bertujuan untuk menduga adanya bakteri coli yang mempunyai sifat mampu memfermentasikan laktosa dengan menghasilkan gas. Bakteri coli yang diduga meliputi semua bakteri gram negatif tdak membentuk spora, selnya membentuk sel pendek, bersifat fakultatif anaerob, membentuk gas dalam waktu 24 jam dari laktosa pada temperatur 37 derajat Celsius. Apabila terbentuk gas dalam waktu 24 jam kedua (48 jam) uji dinyatakan meragukan. Sedangkan apabila gas tidak terbentuk dalam waktu 48 jam uji dinyatakan negatif. Apabila hasil uji duga negatif, maka uji-uji berikutnya tidak perlu dilakukan karena dalam hal ini berarti pula tidak ada bakteri coli dalam contoh.
Untuk analisis air, dalam uji penduga di gunakan lactose broth, sedangkan untuk contoh lainya yang banyak mengandung bakteri asam laktat, misalnya susu, di gunakan
brilliant green lactose bile broth (BGLBB). Bakteri asam laktat dapat memfermentasi laktosa dan membentuk gas, hingga dapat mengakibatkan pembacaan uji positif yang salah. BGLBB
tabung di nyatakan positif bila terebentuk gas sebanyak 10 % atau lebih dari volume di dalam tabung Durham.tabuung yang tidak menunjukan terbentuknya gas di perpanjang lagi
inkubasinya hingga 48 jam. Jika tetap tidak terbentuk gas, di hitung sebagai tabuung negatif. Jumlah tabuung yang positif di hitung pad masing-masing seri. MPN penduga dapat di hitung dengan melihat table MPN 7 tabung.
2. Uji Penetapan (Comfirmed Test)
Bertujuan untuk menegaskan hasil positif dari test perkiraan media yang secara umum digunakan adalah Brilliant Green Laktosa Bile Bronth (BGLBB 2%) atau bisa juga
menggunakan media selektif dan diferensial untuk bakteri coli sperti misal Endo Agar (EA). Pembacaan dilakukan dengan melihat 24-48 jam dengan melihat tabung-tabung yang positif.
Test ini merupakan test yang minimal harus dikerjakan untuk pemeriksaan bakteriologis air. Terbentuknya gas dalam lactose broth atau dalam BGLBB tidak selalu menunjukan bakteri coli karena mikroba lainya mugkin juga ada yang dapat memfermentasikan laktosa dengan
membentuk gas, misalnya bakteri asam laktat dan beberapa kahmir tertentu. Oleh karena itu perlu di lakukan uji penguat pada agar EMB.Dengan Menggunakan jaarum ose, contoh dari tabung MPN yang menunjukan uji penduga positif (terbentuk gas) masing-masing di
inokulasikan pada agar cawan EMB dengan cara goresan kuadran. Semua tabung di inkubasikan pada suhu 35oC selam 24 jam. Jumlah cawan EMB pada masing-masing
pengenceran yang menunjukan adanya pertumbhan Coliform, baik fekal maupun non fekal, dihitung, dan MPN penguat dapat di hitung dari table MPN 7.
3. Uji Lengkap ( Completed Test)
Dari pertumbuhan koloni pada agar cawan EMB, di pilih masing-masing satu koloni
yang mewakili Coliform fekal dan satu koloni yang mewakili Coliform non fekal. Uji
lengkap di lakukan untuk melihat apakah isolat yang di ambil benar merupakan bakteri
masing-masing di larutkan ke dalam 3 ml larutan pngencer steril. Dari suspensi bakteri tersebut
masing di inokulasikan menggunakan jarum ose ke dalam tabung berisi lakose broth dan
tabung Durham, dan di goreskan pada agar miring nutrien agar. Tabung di inkubasikan pada
suhu 35oC selam 24 jam, dan di amati pertumbuhan dan pembentukan gas di dalam lactose
broth. Koloni yang menunjukan reaksi pewarnaan gram negatif berbentuk batang, dan
membentuk gas di dalam lactose broth mereupakan uji lengkap adanya koloni Coliform
Bertujuan untuk mendapatkan hasil yang betul-betul lengkap dan memperkuat hasil
uji sebelumnya. Biasanya dengan membuat isolasi/ piaraan murni dengan coloni yang
tumbuh pada test penetapan. Uji ulang juga dimaksudkan untuk uji ulang apakah jasad renik
yang diduga Coliform pada uji duga memang benar. Dalam uji lengkap dapat diamati
morfologi dan fisiologi dari bakteri yang diduga coiform. Apabila semua kriteria dipenuhi
dapat ditarik kesimpulan bahwa contoh air mengandung bakteri coliform.
Hasil dan Pembahasan
Jumlah bakteri coliform yang didapatkan adalah 9200 koloni/100 ml terdapatnya bakteri coliform dalam air dapat menjadi indikasi kemungkinan besar adanya organisme patogen lainnya. Bakteri coliform dibedakan menjadi 2 tipe, yaitu faecal coliform dan non-faecal coliform. E. coli adalah bagian dari faecal coliform. Keberadaan E. Coli dalam air dapat menjadi indikator adanya pencemaran air oleh tinja. E. coli digunakan sebagai indikator pemeriksaan kualitas bakteriologis secara universal dalam analisis dengan alasan;
a) E. coli secara normal hanya ditemukan di saluran pencernaan manusia (sebagai flora normal)
atau hewan mamalia, atau bahan yang telah terkontaminasi dengan tinja manusia atau hewan; jarang sekali ditemukan dalam air dengan kualitas kebersihan yang tinggi, b) E. coli mudah diperiksa di laboratorium dan sensitivitasnya tinggi jika pemeriksaan dilakukan
dengan benar,
c) Bila dalam air tersebut ditemukan E. coli, maka air tersebut dianggap berbahaya bagi
penggunaan domestik,
d) Ada kemungkinan bakteri enterik patogen yang lain dapat ditemukan bersama-sama dengan E. coli dalam air tersebut.
Adapun keberadaan coliform umumnya diperairan ditemukan dalam konsentrasi
lebih tinggi dekat outfall dan menurunkan secara gradien sebanding dengan jarak dari
outfall dan menurunkan secara gradien sebanding dengan jarak dari outfall . Gameson (1975)
Brithish, dan menurun dengan tajam kurang dari 100 per 100 ml pada jarak 1,5 dari outfall.
Dengan mengukur intensitas cahaya yang diserap yang diteruskan (Transmitancy)
u n t u k memberikan energi sehingga unsur logam yang akan diuji, akan mudaht e r e k s i t a s i . S e l o t i p d i t a m b a h k a n , a g a r t i d a k a d a r u a n g k o s o n g u n t u k keluar masuknya gas dari luar dan keluarnya gas dari dalam, karena bilaa d a g a s y a n g k e l u a r d a r i d a l a m d a p a t m e n ye b a b k a n k e r a c u n a n p a d a lingkungan sekitar. Cara pemeliharaan lampu katoda ialah bila setelahselesai digunakan, maka lampu dilepas dari soket pada main unit AAS, dan lampu diletakkan pada tempat busanya di dalam kotaknya lagi, dand u s p e n y i m p a n a n d i t u t u p k e m b a l i . S e b a i k n y a s e t e l a h s e l e s a i penggunaan, lamanya waktu pemakaian dicatat.
b . T a b u n g G a s
Ta b u n g g a s p a d a A A S y a n g d i g u n a k a n m e r u p a k a n t a b u n g g a s yang berisi gas asetilen. Gas asetilen pada AAS memiliki kisaran suhu ±20000K, dan ada juga tabung gas yang berisi gas N2O yang lebih panasdari gas asetilen, dengan kisaran suhu ± 30000K. regulator pada tabungg a s a s e t i l e n b e r f u n g s i u n t u k p e n g a t u r a n kebocoran, jangan menggunakanminyak, karena minyak akan dapat menyebabkan saluran gas tersumbat.Gas didalam tabung dapat keluar karena disebabkan di dalam tabung pada bagian dasar tabung berisi aseton yang dapat membuat gas akanmudah keluar, selain gas juga memiliki tekanan.
u n t u k m e n ya r i n g u d a r a d a r i l u a r, a g a r b e r s i h . p o s i s i k e kanan, merupakan posisi terbuka, dan posisi ke kiri meerupakan posisitertutup. Uap air yang dikeluarkan, akan memercik kencang dan dapatmengakibatkan lantai sekitar menjadi basah, oleh karena itu sebaiknya pada saat menekan ke kanan bagian ini, sebaiknya ditampung denganlap, agar lantai tidak menjadi basah., dan uap air akan terserap ke lap.
e . B u r n e r
G a m b a r 5 . S k e m a A n a l i s a S i s t e m A A S Hasil dan Pembahasan
g o l o n g a n I A d a n I I A . U m u m n ya l a m p u y a n g d i g u n a k a n adalah lampu katoda cekung yang mana penggunaanya hanya untuk analisissatu unsur saja.Metode AAS berprinsip pada absorbsi cahaya oleh atom.Atom-at om menyerap cahaya tersebut pada panjang gelombang tertentu,tergantung pada sifat unsurnya. Metode serapan atom hanya tergantung pada perbandingan dan tidak bergantung pada temperatur.
sebagian sinar yang dipancarkan o l e h s u m b e r c a h a y a . P e n y e r a p a n e n e r g i o l e h a t o m t e r j a d i p a d a p a n j a n g g e l o m b a n g t e r t e n t u s e s u a i d e n g a n e n e r g i y a n g d i b u t u h k a n o l e h a t o m tersebut.
G Khromatografi
Kromatografi merupakan suatu cara pemisahan fisik dengan unsur-unsur yang akan dipisahkan terdistribusikan antara dua fasa, satu dari fasa-fasa ini membentuk suatu lapisan stasioner dengan luas permukaan yang besar dan yang lainnya merupakan cairan yang merembes lewat atau melalui lapisan yang stasioner. Fasa stasioner mugkin suatu zat padat atau suatu cairan, dan fasa yang bergerak mungkin suatu cairan atau suatu gas. Maka semua jenis kromatografi yang dikenal, terbagi menjadi empat golongan: padat, gas-padat, cair-cair, dan gas-cair (Underwood, 1986).
prosedur Analisa Khromatografi
Pembahasan teknik kromatografi modern baru lengkap bila disebut kromatografi
cairan penampilan tinggi (HPLC). Kromatografi cairan kolom klasik merupakan prosedur
pemisahan yang sudah mapan dalam mana fase cair yang mobil mengalir lambat-lambat
lewat kolom karena gravitasi. Umumnya metode itu dicirikan oleh efisiensi kolom yang
rendah dan waktu pemisahan yang lama. Namun sejak kira-kira tahun 1969, perhatian dalam
teknik kolom cairan hidup kembali dengan sangat menyolok karena dikembangkannya sistem
tekanan tinggi oleh Kirchland dan Huber, yang bekerja pada tekanan sampai 2,07 x 107 Nm-2
(3000 p.s.i). Dalam metode ini digunakan kolom berdiameter kecil (1-3 mm) dengan partikel
pendukung berukuran sekitar 30 ?m dan eluen dipompakan ke dalamnya dengan laju alir
yang tinggi (sekitar 1-5 cm3m-1). Pemisahan dengan metode ini dilakukan jauh lebih cepat
peralatan yang tersedia di pasar dewasa ini agak mahal. HPLC telah terbukti luas
penggunaannya dalam kimia organik. Pengembangan penerapan dalam anorganik menjadi
mungkin, misalnya dalam bidang kromatografi pertukaran ion di mana telah tersedia di pasar
dengan nama dagang ‘Zipax’ resin peliklar, yakni resin yang dihasilkan dalam bentuk saluran
tipis pada permukaan manik kaca yang blat (diameter 2050 mikrometer). Manik-manik itu
mempunyai permukaan berpori yang tebalnya 2 mikrometer yang berperan sebagai pengikat
saluran resin itu (Bassett et. all., 1994).
Umumnya metode kromatografi seperti adsorpsi, partisi, dan penukar ion adalah contoh-contoh dari kromatografi kolom. Pada metode kromatografi cair ini digunakan kolom tabung gelas dengan bermacam diameter. Partikel dengan dimensi yang bervariasi digunakan sebagai penunjang stasioner. Banyaknya cairan pada kolom jumlahnya sedemikian rupa sehingga hanya cukup menghasilkan sedikit tekanan untuk memelihara aliran fase bergerak yang seragam. Secara keseluruhan pemisahan ini memakan waktu lama. Berbagai usaha telah dilakukan untuk menambah laju aliran tanpa mengubah tinggi piringan teoritis kolom. Penurunan ukuran partikel penunjang stasioner tidak selalu menguntungkan. Kromatografi cair kinerja tinggi atau High Performance Liquid Chromatography (HPLC) berbeda dari kromatografi cair klasik. HPLC menggunakan kolom dengan diameter umumnya kecil, 2-8 mm dengan ukuran partikel penunjang 50 ?m; sedangkan laju aliran dipertinggi dengan tekanan yang tinggi (Khopkar, 2003).
Bila dibandingkan terhadap kromatografi gas-cair/gas-liquid chromatography (GLC),
maka HPLC lebih bermanfaat untuk isolasi zat tidak mudah menguap, demikian juga zat
yang secara termal tidak stabil. Tetapi ditinjau dari kecepatan dan kesederhanaan, GC lebih
hanya memerlukan sampel berjumlah sedikit serta keduanya dapat digunakan untuk analisis
kuantitatif (Khopkar, 2003).
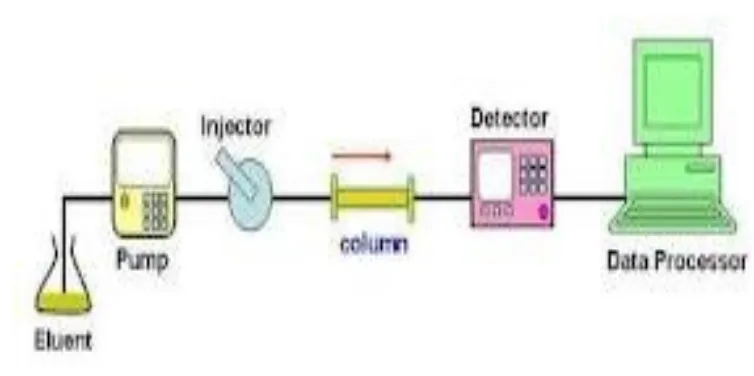
Gambar 6. Skema Analisa Khromatografi Ion Hasil dan Pembahasan
Nilai khromatografi sampel 1 adalah 24,8797 mg/l dan sampel 101,1921 mg/ l. Berdsarkan hasil pengukuran tersbut di atas maka nilai dari khromatografi logam berat yang diukur tidak sesuai dengan baku mutu dan bersifat toksik bagi kehidupan organisme air. Analisa HPLC adalah alat yang sangat bermanfaat dalam analisis. Prinsip dasar dari HPLC adalah memisahkan setiap komponen dalam sample untuk selanjutnya diidentifikasi (kualitatif) dan dihitung berapa konsentrasi dari masing-masing komponen tersebut (kuantitatif). Sebetulnya hanya ada dua hal utama yang menjadi krusial point dalam metode HPLC. Yang pertama adalah proses separasi/pemisahan dan yang kedua adalah proses identifikasi. Dua hal ini mejadi faktor yang sangat penting dalam keberhasilan proses analisa. Aplikasi analisis HPLC adalah untuk penentuan kualitatif dan penentuan kuantitatif.
HPLC digunakan untuk analisa kualitatif didasarkan pada waktu retensi untuk identifikasi. Identifikasi dapat diandalkan apabila waktu retensi sampel dibandingkan dengan larutan standar.
b. Penentuan Kuantitatif
Beberapa hal yang harus diperhatikan agar HPLC dapat dipergunakan untuk penentuan secara kuantitatif adalah:
Parameter percobaan sama antara standar dan sampel
Penentuan berdasarkan waktu retensi sampel dan standar yang sama
Penentuan kadar dilakukan berdasarkan hubungan (korelasi) dengan menggunakan larutan standar seri pada waktu retensi tertentu. kromatogram dengan banyak peak. Bahkan tak jarang antar peak saling bertumpuk (overlap). Hal ini akan menyulitkan dalam identifikasi dan perhitungan konsentrasi. Oleh karena itu biasanya untuk sample jenis ini dilakukan tahapan preparasi sample yang lebih rumit agar sample yang siap diinjeksikan ke HPLC sudah cukup bersih dari impuritis. Sample farmasi biasanya jauh lebih mudah karena sedikit mengandung komponen selain zat aktif. Sample ini umumnya hanya melalui proses pelarutan saja.
milik analat. Memang senyawa/zat yang sama akan mempunyai RT yang juga sama, dengan catatan sample dan standard dijalankan dengan kondisi dan sistem HPLC yang sama. Namun bukan berarti RT yang sama pasti merupakan zat/senyawa yang sama. Disinilah para analis biasanya terkecoh.
Jadi, melihat RT sebetulnya belumlah cukup untuk mengidentifikasi suatu zat. Hal lain yang perlu dilihat adalah spektrum 3D dari signal kromatogram. Zat yang sama akan mempunyai spektrum 3D yang juga sama. Sehingga jika spektrum 3D antara dua zat berbeda, maka kedua zat tersebut juga dipastikan adalah zat yang berlainan, meskipun memiliki RT yang sama. Beberapa parameter penting yang perlu diperhatikan di dalam analisis HPLC adalah :
1. Kolom
Sebuah kolom sederhana memiliki diameter internal 4.6 mm (dan mungkin kurang dari nilai ini) dengan panjang 150 sampai 250 mm. Kolom yang biasa digunakan untuk analisa adalah bentuk kolom fase balik. Kolom diisi dengan partikel silika yang dimodifikasi menjadi non polar melalui pelekatan rantai-rantai hidrokarbon panjang pada permukaannya secara sederhana baik berupa atom karbon 8 atau 18. Sebagai contoh, pelarut polar digunakan berupa campuran air dan alkohol seperti metanol.
Senyawa-senyawa non polar dalam campuran akan cenderung membentuk atraksi
dengan gugus hidrokarbon karena adanya dispersi gaya van der Waals. Senyawa-senyawa ini
juga akan kurang larut dalam pelarut karena membutuhkan pemutusan ikatan hydrogen
sebagaimana halnya senyawa-senyawa tersebut berada dalam molekul-molekul air atau
metanol misalnya. Oleh karenanya, senyawa-senyawa ini akan menghabiskan waktu dalam
larutan dan akan bergerak lambat dalam kolom.Ini berarti bahwa molekul-molekul polar akan
bergerak lebih cepat melalui kolom.
Ada kolom yang digunakan untuk beberapa jenis analisa, misalnya kolom C18 yang dapat digunakan untuk analisa carotenoid, protein, lovastatin, dan sebagainya. Namun ada juga kolom yang khusus dibuat untuk tujuan analisa tertentu, seperti kolom Zorbax carbohydrat (Agilent) yang khusus digunakan untuk analisa karbohidrat (mono-, di-,
polysakarida). Keberhasilan proses separasi sangat dipengaruhi oleh pemilihan jenis kolom dan juga fasa mobil.
2. Komposisi Eluen
Komposisi eluen meliputi jenis dan perbandingan eluen yang digunakan. Ada 2 macam eluen, yakni pelarut nonpolar untuk fase normal, seperti heksan, dan pelarut polar untuk fase balik, seperti campuran air dan alkohol, yakni metanol.
3. Volume Injeksi
Sampel yang akan dipisahkan dimasukkan ke dalam kolom secara otomatis atau
manual melalui injeksi. Volume injeksi sangat tepat karena mempunyai sampel loop dengan
variabel volume (misalnya 20 – 500 μL). Injeksi sampel dapat dilakukan melalui manual
4. Detektor
Detektor merupakan suatu bagian integral dari sebuah peralatan analitik kromatografi cair yang modern. HPLC mempunyai keunggulan dibanding kromatografi lain, yaitu mempunyai banyak pilihan detektor yang dapat digunakan.
Secara garis besar , detektor dalam HPLC dapat dikelompokan :
§ Berdasarkan pengukuran diferensial suatu sifat yang dimiliki baik oleh molekul sampel maupun fase gerak (bulk property detector).Detektor dapat dibedakan menjadi :
Ø Detektor Indeks Bias
Detektor indeks bias merupakan detektor yang juga luas penggunaannya setelah
detektor ultraviolet. Dasarnya ialah pengukuran perbedaan indeks bias fase gerak murni
dengan indeks bias fase gerak yang berisi komponen sampel, sehingga dapat dianggap
sebagai detektor yang universal pada HPLC. Detektor ini kurang sensitif dibanding dengan
detektor ultraviolet dan sangat peka terhadap perubahan suhu.
Detektor konduktivitas Detektor tetapan dielektrika
Berdasar pengukuran suatu sifat yang spesifik dari molekul sampel (disebut solute property
detector).Jenis yang kedua ini dibedakan lagi menjadi :
Detektor-detektor fotometer (uv-vis dan inframerah)
Pada detektor ultraviolet/visibel, deteksi komponen sample didasarkan pada absorpsi
Detektor ultraviolet merupakan detektor yang paling luas digunakan karena sensitivitas dan
reprodusibelitasnya yang tinggi serta mudah operasinya. Detektor UV terutama digunakan
untuk pendeteksian senyawa-senyawa organic. Detektor UV dilengkapi dengan pengatur
panjang gelombang sehingga panjang gelombang UV yang digunakan dapat dipilih
disesuaikan dengan jenis cuplikan yang diukur. Walaupun demikian, biasanya panjang
gelombang UV yang digunakan adalah pada 254 nm karena kebanyakan senyawa organic
menyerap sinar UV pada sekitar panjang gelombang tersebut.
Detektor fotometer inframerah juga dapat digunakan pada HPLC. Dengan detektor ini dapat dibuat pola spektrum infra merah dari komponen sampel sehingga gugus-gugus fungsionalnya dapat diketahui.
Detektor Polarografi dan radioaktif;
Kedua detector ini dipengaruhi oleh variasi laju aliran..
Chart Speed
Diagram kecepatan dapat diketahui bila sampel diinjeksikan secara manual.
DAFTAR PUSTAKA
Anonim1.2010.Bakteri Koliform Fekal(Fecal Coliform).
http://www.bangkoyoy.com/2010/10/bakteri-koliform-fekal-fecal-coliform.html. [31 Mei 2011]
Bishop, Paul L. 1983. Marine Pollution and it’s Control. New York, MC Graw-Hill Book Co.
Cole, G. A. 1988. Textbook of Limnology. Third Edition. Waveland Press, Inc., Illionis, USA. 401 p
Cloern, J. E. 1987. Turbidity as a tontrol on Phytoplankton Biomass and Produktiviity in Estuaries. Cont. Shelf Res. 7:1367-1381
Effendi, H., 2003. Telaah Kualitas Air Bagi Pengelolaan Sumberdaya dan Lingkungan Perairan. Institut Pertanian Bogor. Press. Bogor. 259 hal.
Khopkar, S.M., 2003, Konsep Dasar Kimia Analitik, UI Press, Jakarta.
McNeely et al., 1979 dalam Effendi, H., 2003. Telaah Kualitas Air Bagi Pengelolaan Sumberdaya dan Lingkungan Perairan. Institut Pertanian Bogor. Press. Bogor. 259 hal.
Mukhtasor. 2007. Pencemaran Pesisir dan Laut. Jakarta : PT Pradnya Paramita
L A M P I R A N
DAFTAR ISI
Halaman
Turbidimeter Gelas Kimia
Tabung Reaksi Coliform Kromatografi
Komatografi Cair Atom Absorbtion Spektofotometer
DAFTAR ISI... i
PARAMETER KUALITAS AIR YANG DIUKUR... 1
A. Kekeruhan ... 1
B. Padatan (TDS,TSS,TVS)... 4
C. Amoniak Nitrogen... 7
D. Lemak dan Minyak... 10
E. Bakteri Coliform... 15
F. Spetrofotometer Serapan Atom ... 22
G. Khromatografi... 29
DAFTAR PUSTAKA... 37
LAMPIRAN... 38
DAFTAR TABEL
1. Hubungan antara nilai TDS dan salinitas... 6
2. Kesesusan Perairan untuk Kepentingan Perikanan Berdasarkan TSS.... 7
DAFTAR GAMBAR Halaman 1. Prinsip kerja Turbidimeter... 1
2. Skema prinsip analisa (TDS,TSS,TVS) ... 6
3. Skema manual prosedur pengukuran kadar lemak... 17
4. Skema pengukuran bakteri coliform... 21
5. Skema analisa sistem AAS... 27
6. Skemomaa analisa Khromatografi... 31
LAPORAN
PRAKTIKUM KE 2
Disusun oleh: