Lampiran 3. Data Thiol 0 bulan
Perlakuan Ulangan Total Rataan
1 2 3
Perlakuan Ulangan Total Rataan
1 2 3
Sidik Ragam Thiol 0 bulan
Lampiran 4. Data Thiol 2 bulan
Perlakuan Ulangan Total Rataan
1 2 3
K1A0 0,785 0,945 0,819 2,549 0,850
K1A1 0,845 1,465 1,022 3,332 1,111
K1A2 0,601 0,890 0,922 2,413 0,804
K1A3 0,948 0,675 1,173 2,796 0,932
K2A0 0,634 0,743 0,542 1,919 0,640
K2A1 0,861 0,703 0,624 2,188 0,729
K2A2 0,554 0,642 0,900 2,096 0,699
K2A3 0,743 0,479 0,916 2,138 0,713
Total 5,971 6,542 6,918 19,431 6,477
Sidik Ragam Thiol 2 bulan
Sumber Db JK KT F P
Block 2 0,05 0,0283 0,86 0,53
K 1 0,31 0,3146 9,59 0,09
Error (a) 2 0,06 0,0327
A 3 0,11 0,0399 0,96 0,43
A x K 3 0,05 0,0194 0,47 0,7
Error (b) 12 0,49 0,0411
Total 23 1,07
Lampiran 5. Data Thiol 4 bulan
Perlakuan Ulangan Total Rataan
1 2 3
K1A0 0,660 0,045 0,505 1,210 0,403
K1A1 0,319 0,554 0,654 1,527 0,509
K1A2 0,470 0,464 0,578 1,511 0,504
K1A3 0,501 0,479 0,637 1,618 0,539
K2A0 0,440 0,562 0,405 1,408 0,469
K2A1 0,973 0,440 0,675 2,088 0,696
K2A2 0,649 0,561 0,619 1,829 0,610
K2A3 0,698 0,651 0,655 2,004 0,668
Total 4,709 3,756 4,729 13,195 4,398
Sidik Ragam Thiol 4 bulan
Sumber Db JK KT F P
Block 2 0,07 0,0386 1,57 0,38
K 1 0,08 0,0890 3,62 0,19
Error (a) 2 0,04 0,0245
A 3 0,11 0,0372 1,39 0,29
A x K 3 0,01 0,0038 0,14 0,93
Error (b) 12 0,32 0,0267
Total 23 0,63
Lampiran 6. Data PI 0 bulan
Perlakuan Ulangan Total Rataan
1 2 3
K1A0 13,700 14,550 15,650 43,900 14,633
K1A1 11,950 16,100 18,050 46,100 15,367
K1A2 20,900 23,650 18,300 62,850 20,950
K1A3 18,250 14,250 23,500 56,000 18,667
K2A0 10,400 1,600 11,100 23,100 7,700
K2A1 7,950 10,900 12,300 31,150 10,383
K2A2 9,750 9,200 12,200 31,150 10,383
K2A3 9,500 9,900 12,200 31,600 10,533
Total 102,400 100,150 123,300 325,850 108,617
Sidik Ragam PI 0 bulan
Sumber Db JK KT F P
Block 2 40,74 20,3707 5,4 0,15
K 1 351,51 351,5176 93,28 * 0,01
Error (a) 2 7,53 3,7682
A 3 70,29 23,4314 2,66 0,09
A x K 3 24,54 8,1826 0,92 0,45
Error (b) 12 105,67 8,8060
Total 23 600,28
Lampiran 7. Data PI 2 bulan
Perlakuan Ulangan Total Rataan
1 2 3
Perlakuan Ulangan Total Rataan
1 2 3
Sidik Ragam PI 2 bulan
Lampiran 8. Data PI 4 bulan
Perlakuan Ulangan Total Rataan
1 2 3
Perlakuan Ulangan Total Rataan
1 2 3
Sidik Ragam PI 4 bulan
Lampiran 9. Data Sukrosa 0 bulan
Perlakuan Ulangan Total Rataan
1 2 3 Lampiran 9. Transformasi √ x Data Sukrosa 0 bulan
Perlakuan Ulangan Total Rataan
1 2 3
Sidik Ragam Sukrosa 0 bulan
Lampiran 10. Data Sukroa 2 bulan
Perlakuan Ulangan Total Rataan
1 2 3 Lampiran 10. Tranformasi √ x Data Sukroa 2 bulan
Perlakuan Ulangan Total Rataan
1 2 3
Sidik Ragam Sukrosa 2 bulan
Lampiran 11. Data Sukroa 4 bulan
Perlakuan Ulangan Total Rataan
1 2 3 Lampiran 11. Transformasi √ x Data Sukroa 4 bulan
Perlakuan Ulangan Total Rataan
1 2 3
Sidik Ragam Sukrosa 4 bulan
Lampiran 12. Data aktivitas superoksida dismutase (SOD) 1
Perlakuan Ulangan Total Rataan
1 2 3
Lampiran 11 . Transformasi √ x Data aktivitas superoksida dismutase (SOD) 1
Perlakuan Ulangan Total Rataan
1 2 3
Sidik Ragam aktivitas superoksida dismutase (SOD) 1
Lampiran 13. Data aktivitas superoksida dismutase (SOD) 2
Perlakuan Ulangan Total Rataan
1 2 3 Lampiran 13. Transformasi √ x Data aktivitas superoksida dismutase (SOD) 2
Perlakuan Ulangan Total Rataan
1 2 3
Sidik Ragam aktivitas superoksida dismutase (SOD) 2
Lampiran 14 . Data Produksi 1 Lampiran . Data Produksi 1
Perlakuan Ulangan Total Rataan
1 2 3
Lampiran 14. Transformasi √ x Data Produksi 1
Perlakuan Ulangan Total Rataan
Lampiran 15. Data Produksi 2
Perlakuan Ulangan Total Rataan
1 2 3
Lampiran 15. Transformasi √ x Data Produksi 2
Perlakuan Ulangan Total Rataan
Lampiran 16. Data Produksi 3
Perlakuan Ulangan Total Rataan
1 2 3
K1A0 1,23 1,60 0,99 3,82 1,27
K1A1 7,59 9,80 6,10 23,48 7,83
K1A2 9,14 8,56 11,76 29,47 9,82
K1A3 6,03 7,76 7,21 21,00 7,00
K2A0 1,26 0,64 1,90 3,80 1,27
K2A1 3,92 5,95 5,83 15,70 5,23
K2A2 7,38 2,75 2,50 12,63 4,21
K2A3 4,92 7,16 2,41 14,49 4,83
Total 41,47 44,22 38,69 124,38 41,46
Sidik Ragam Produksi 3
Sumber Db JK KT F P
Block 2 1,91 0,9556 0,61 0,6194
K 1 40,41 40,4175 25,98 * 0,0364
Error (a) 2 3,11 1,5552
A 3 126,14 42,0491 12,85 *** 0,0005
A x K 3 23,99 7,998 2,44 0,1143
Error (b) 12 39,24 3,2705
Total 23 234,80
Lampiran 17. Data Produksi 4
Perlakuan Ulangan Total Rataan
1 2 3
Lampiran 17. Trnasformasi √ x Data Produksi 4
Perlakuan Ulangan Total Rataan
Lampiran 18. Data Produksi 5
Perlakuan Ulangan Total Rataan
1 2 3
Lampiran 18. Transformasi √ x Data Produksi 5
Perlakuan Ulangan Total Rataan
Lampiran 19. Data Produksi 6
Perlakuan Ulangan Total Rataan
1 2 3
Lampiran 19. Transformasi √ x Data Produksi 6
Perlakuan Ulangan Total Rataan
Lampiran 20. Data Produksi 7
Perlakuan Ulangan Total Rataan
1 2 3
Lampiran 20. Transformasi √ x Data Produksi 7
perlakuan Ulangan TOTAL Rataan
Lampiran 21. Data Produksi 8
Perlakuan Ulangan Total Rataan
1 2 3
Lampiran 21. Transformasi √ x Data Produksi 8
Perlakuan Ulangan Total Rataan
Lampiran 22. Data IP 1 ( 2 bulan aplikasi)
Perlakuan Ulangan Total Rataan
1 2 3
perlakuan Ulangan TOTAL Rataan
1 2 3
Sidik Ragam IP 1 ( 2 bulan aplikasi)
Lampiran 23. Data IP 2 ( 4 bulan aplikasi)
Perlakuan Ulangan Total Rataan
1 2 3
Perlakuan Ulangan Total Rataan
1 2 3
Sidik Ragam IP 2 ( 4 bulan aplikasi)
Lampiran 24 . Data total solid content (TSC) 1
Perlakuan Ulangan Total Rataan
1 2 3
Lampiran 24 . Data total solid content (TSC) 2
Perlakuan Ulangan Total Rataan
1 2 3
Lampiran 24 . Data total solid content (TSC) 3
Perlakuan Ulangan Total Rataan
Lampiran 24 . Data total solid content (TSC) 4
Perlakuan Ulangan Total Rataan
1 2 3
Lampiran 24 . Data total solid content (TSC) 6
Perlakuan Ulangan Total Rataan
1 2 3
Lampiran 24 . Data total solid content (TSC) 6
Perlakuan Ulangan Total Rataan
Lampiran 24 . Data total solid content (TSC) 7
Perlakuan Ulangan TOTAL Rataan
1 2 3
K1A0 21,90 40,74 23,46 86,10 28,70
K1A1 29,55 18,26 32,38 80,19 26,73
K1A2 27,02 20,00 34,68 81,69 27,23
K1A3 26,23 31,33 23,36 80,92 26,97
K2A0 51,44 39,43 34,40 125,27 41,76
K2A1 19,28 37,14 20,58 77,00 25,67
K2A2 21,25 59,26 36,93 117,44 39,15
K2A3 40,00 19,51 23,46 82,97 27,66
TOTAL 236,67 265,67 229,23 731,57 243,86
Lampiran 24 . Data total solid content (TSC) 8
Perlakuan Ulangan Total Rataan
1 2 3
K1A0 36,55 29,39 17,70 83,63 27,88
K1A1 40,41 25,10 22,31 87,83 29,28
K1A2 18,07 25,31 28,16 71,54 23,85
K1A3 32,66 33,06 29,10 94,82 31,61
K2A0 26,97 20,00 29,39 76,36 25,45
K2A1 41,98 20,00 32,51 94,49 31,50
K2A2 19,34 27,57 26,03 72,95 24,32
K2A3 40,65 32,93 31,30 104,88 34,96
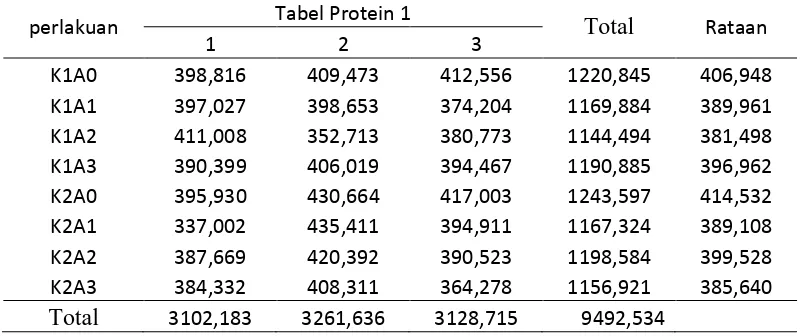
Lampiran 25 . Data Protein 1
perlakuan Tabel Protein 1 Total Rataan
1 2 3
K1A0 398,816 409,473 412,556 1220,845 406,948 K1A1 397,027 398,653 374,204 1169,884 389,961 K1A2 411,008 352,713 380,773 1144,494 381,498 K1A3 390,399 406,019 394,467 1190,885 396,962 K2A0 395,930 430,664 417,003 1243,597 414,532 K2A1 337,002 435,411 394,911 1167,324 389,108 K2A2 387,669 420,392 390,523 1198,584 399,528 K2A3 384,332 408,311 364,278 1156,921 385,640
Total 3102,183 3261,636 3128,715 9492,534
Lampiran 25 . Data Protein 2
perlakuan Tabel Protein 2 Total Rataan
1 2 3
K1A0 30,242 44,373 42,871 117,486 39,162 K1A1 6,172 93,499 63,650 163,321 54,440 K1A2 70,363 43,968 39,500 153,831 51,277 K1A3 78,245 45,973 66,706 190,924 63,641 K2A0 38,816 80,224 42,270 161,310 53,770 K2A1 60,986 69,299 75,137 205,422 68,474 K2A2 50,858 48,768 94,655 194,281 64,760 K2A3 49,219 78,428 29,080 156,727 52,242
Lampiran Gambar 1
Tanaman KAS Parsial
Lampiran Gambar 2
Produksi PB 260 ,0 ppm Produksi PB 260, 150 ppm asam askorbat asam askorbat
Lampiran Gambar 3
Produksi IRR 42, 0 ppm Produksi IRR 42, 150 PPM asam askorbat asam askorbat
Lampiran Gambar 4
DAFTAR PUSTAKA
Abraham, T., J. Mathew, P. Srinivas, an C. K. Jacob. 2006. Incidence of taping panel drynes on populer rubber clones in southren rubber clones in southern rubber growing region of india. In Jacob, J., R R. Krishnakumar and N.M Mathew. (Eds). Taping Panel Dryness Of Rubber Research Institute of India. India. 55-63.
Anwar C. 2001.Manajemen dan Teknologi Budidaya Karet.FABA Indonesia Konsultan.
Ardiansyah M., Mawarni L., Rahmawati N.2014. Respon Pertumbuhan dan Produksi Kedelai Hasil Seleksi Terhadap Pemberian Asam Askorbat dan Inokulasi Fungi Mikoriza Arbuskular di Tanah Salin. Univrsitas Sumatra Utara. Medan.
Ardianti, A., Guntarti, A., Zainab. 2014. Uji Aktivitas Antioksidan Fraksi Eter Hasil Hidrolisis Infusa Daun Binahong (Antedera Cordifolia (Ten) steenis) Dengan Metode DPPH (1.1- Diphenil-2-Picryihydrazl) . Universitas Ahmad Dahlan. Yogyakarta.
Arif, B., dan Islan, B. 2006.Penanggulangan Alur Sadap dan Penyakit Lapuk Cabang dan Batang Pada Tanaman Karet Dengan Formula Antco F-96.Balai Penelitian Sumbawa.
Arlyny F, A.2008.Program Ekspresi Gen Responsif Terhadap ReactiveOxygen
Species pada Hevea brasiliensis AkibatPelukaan dan Etilena Eksogen.
Institut Pertanian Bogor. Bogor.
Astuti S. Muchtadi D., Astawan M., Purwantara B., and Wresdiyanti T. 2009. Pengaruh Pemberian Tepung Kedelai Kaya Isoflavon Terhadap Kadar Malonaldehid (MDA), Aktivitas Superoksida Dismutase (SOD) Testis dan Profil Cu,Zn- SOD Tubuli Seminiferi Testis Tikus Jantan. Fakultas Kedokteran Hewan. Institut Pertanian Bogor. Bogor.
Bangun, M. K. 1991. Rancanagn Percobaan. Fakultas Pertanian USU. Medan.
BPS. 2014. Statistik Karet Indonesia. Badan Pusat Statistik BPS.Statistics Indonesia.
Budiman, H. 2012. Budidaya Karet Unggul. Pustaka Baru. Yogyakarta.
Dische, Z, M. 1962. Carbohydrate Chem Acad. Press, I1:488
Gebelin V., Leclercq, J., Hu, S., Tang C., and Montoro P. 2013. Regulation of MIR Genes in Response to Abiotik Stress in Hevea brasiliensis Int. J. Mol. Sci. 2013.14, 19587-19604; doi: 10.3390?ijms 141019587. International Journal of Molecular Sciences ISSN 1422-0067 www.mdp.com/journal/ijms
Gohet, J., L. Prevot, J.M. Eschbach, A. Clement,and J.L. Jacob. 1996. Clone, Growth, and Stimulation : Latex Production Factors. Plantations3(1): 30−38.
Hernofialdi, Rini, E A., Machmud R.2011.Pengaruh Pemberian Vitamin C Terhadap Kadar Inter Seluler Adhesion Molecule -1 (ICAM-1) Pada remaja laki laki dengan Obesitas di Kota Padang. Universitas Andalas. Padang.
Island,B, dan Dwi, S,A. 2013. Prospek Pengembangan Karet Diwilayah Daerah Aliran Sungai.Balai Penelitian Sumbawa.
Jacob, J. And . Krisnakumar. 2006. Tapping Panel Dryness Syndrome: What We Know And What We Do Not Know. In Jacob, J,R R. Krisnakumar and N. M. Mathew. (Eds). Tapping Panel Dryness Of Rubber Trees. Rubber Research Institute of India. India. 3-27.
Janudianto, Prahmono A, Napitupulu H, Rahayu S. 2013. Panduan budidaya karet untuk petani skala kecil.Rubber cultivation guide for small-scale farmers. Lembar Informasi AgFor 5. Bogor, Indonesia: World AgroforestryCentre (ICRAF) Southeast Asia Regional Program.
Julahir, H, S. 2009. Pengaruh Pemberian Vitamin C terhadap jumlah sel ledying dan jumlah sperma mancit dewasa yang dipapari Monosodium glutamate.Universitas Sumatra Utara. Medan.
Karintus. 2011. Pengaruh Macam Entres dan Konsentrasi BAP pada Pertumbuhan Okulasi Karet (Havea brasiliensis). Universitas Sebelas Maret. Surakarta.
Kurniawan, M., Izzati, M., Nurchayati.(2010). Kandungan Klorofil, Karonenoid dan Vitamin C pada Beberapa Spesies Tumbuhan Aquatik. Universitas Dipenogoro. Semarang.
Lacote, R. 2007. Some Considerations Concerning the Yield Potential of Some Clones HB in IRC2007. IRRDB and CRRI : Siem Reap. Cambodia
Marchino, F,Yusrizal M.Z, dan Irfan S. 2010. Pertumbuhan Stum Mata Tidur Beberapa Klon Entres Tanaman Karet (Hevea brasiliensis Muell.) Pada Batang Bawah PB 260 di Lapangan.Universitas Andalas, Padang.
Maryani. 2007. Aneka Tanaman Perkebunan, Pusat Pengembangan Universitas Riau. Pekanbaru.
Maslachah L., Sugihartuti R.,dan Kurniasanti R .2008. Hambatan Produksi Reactive Oxygen Species Radikal Superoksida (O2.-) oleh Antioksidan Vitamin E (α- tocopherol ) pada Tikus Putih (Rattus norvegicus)yang Menerima Stressor Renjatan Listrik. Universitas Erlangga. Surabaya.
Milford, G.FJ., E.C. Paarderkooper, And H.C. Yee. 1969. Latex Vessel Plugging : Its Importance To Yeild Ang Clonal Behaviour. J.Rubb. Res. Inst. Malaya 21,274282
Nugroho P, S. 2010. Karakterisasi Biologi Isolat-isolat Rigidupon Micropons Pada Tanaman Karet (Hevea brasiliensisMuell.). Universitas Sebelas Maret. Surakarta.
Peraturan Menteri Pertanian Republik Indonesia.2014. Pedoman Budidaya Karet (Hevea brasiliensis) yang Baik. Jakarta.
Rejab, I,B., Pastur V, and Mauch-Mani B. 2014.Plant Responses to Simultaneous Biotic and Abiotic Stress Molecular Mechanisms. Universal of Nechatel. Switzerland.
Sarvajeet Singh Gill, Narendra Tuteja. 2010. Plant Physiology and Biochemistry . Aruna Asaf Ali Marg, New Delhi. India.
Setiawan, D. H., danAndoko, A. 2005. Petunjuk Lengkap Budidaya Karet. Agromedia Pustaka. Jakarta.
Sianturi, H. S., 2001. Budidaya Tanaman Karet. Fakultas Pertanian USU. Medan.
Steenis, C. G. K., 2005. Flora. PT. Pradyna Paramita. Jakarta
Sulistyowati, Y. 2006. Pengaruh Pemberian Likopen Terhadap Status Antioksidan (Vitamin C dan Gluthathion Proksidase) Tikus (Rattus norvigatus galur
sprague dowly) Hiperkolesterolemik. Universitas Diponogoro. Semarang.
Suwarto, dan Yoke, O., 2010. Budidaya Tanaman Perkebunan Unggul. Penebar Swadaya. Jakarta
Syukur.2013. Kajian Okulasi Benih Karet(Hevea BrasiliensisMuell. Arg) Dengan Perbedaan Mata Tunas (Entres) dan Klon.Balai Pelatihan Pertanian Jambi
Taussky H. Hand E. Shorr. 1953. A micro colorimetric methods for the determination of inorganic phosphorus. J. Biol Chem 202: 675-685.
Tistama, R., Sumarmadji., dan Siswanto. 2006.Kejadian Kering Alur Sadap dan Teknik Pemulihannya pada Tanaman Karet.Balai Penelitian Sei Putih.
Tistama, R. 2013. Faktor Histologis dan Fisiologis Yang Berkaitan Dengan Produksi Lateks.Workshop Eksploitasi Tanaman Karet Menuju Produktivitas Tinggi dan Umur Ekonomis Optimal.Medan, 13.
BAHAN DAN METODE Tempat dan Waktu Penelitian
Penelitian dilaksanakan dikebun percobaan PB260 dan IR42 tahun
2006-2007. Balai Penelitian Sungai Putih, Kecamatan Galang,Kabupaten Deli Serdang,
tepatnya di ketinggian tempat ± 54 meter di atas permukaan laut, dari bulan Mei
sampai dengan Oktober 2015.
Bahan dan Alat
Bahan yang digunakan merupakan tegakan tanaman karet berumur 7-8 tahun
yang ditanam pada tahun 2006-2007 dengan jarak tanam 4 x 6 m dengan sistem sadap
1/2S d/3ET.2.5 (1/m 6/y), bahan kimia untuk diagnosis lateks, bahan kimia untuk
melihat histologi jaringan pembuluh lateks, asam askorbat.
Alat dan bahan yang diperlukan dalam penelitian ini adalah spidol marker,cat
minyak, pisau, sadap, spectrofometer, sentrifius microskop cahaya, alat ukur seperti
meteran dan timbangan, buku data, alat tulis, kamera beserta alat-alat lain yang
mendukung penelitian ini.
Metode Penelitian
Penelitian ini dilakukan dengan menggunakan Rancangan Petak Terbagi
(RPT/ Split Plot Design) dengan dua faktor perlakuan yaitu :
Petak utama : Klon Tanaman Karet (Main Plot)
K1 : Klon PB 260
K2 : Klon IRR 42
Anak Petak : Konsentrasi Asam Askorbit (Sub Plot)
A1 : 150 ppm
A2 : 300 ppm
A3 : 450 ppm
Sehingga diperoleh 8 kombinasi perlakuan yaitu
K1A0 K1A1 K1A2 K1A3
K2A0 K2A1 K2A2 K2A3
Jumlah ulangan : 3
Jumlah tanaman per perlakuan : 3
Jumlah kombinasi perlakuan : 8
Jumlah seluruh tanaman : 72
Adapun model liner dari sidik ragam penelitian sebagai berikut:
Yijk = µ + Bk + Ki + εik + Aj + (KA)ij+ δijk i = 1,2, j = 1,2,3,4 k= 1,2,3
Yijk = Nilai pengamatan karena pengaruh faktor K taraf ke-i dari faktor klon dan
faktor A taraf ke- J dari faktor taraf asam askorbat pada ulangan ke-k
μ = Nilai tengah umum.
Bk = Pengaruh blok atau ulangan ke-k.
Ki = Pengaruh aditif taraf ke – i dari faktor klon tanaman.
εik = Pengaruh acak dari petak utama, yang muncul pada taraf ke – i dari
faktor Klon tanaman dalam kelompok ke- K.
Aj = Pengaruh faktor A taraf ke – j dari faktor asam askorbat.
(KA)ij = Pengaruh interaksi faktor klon tanaman taraf ke – i dan interaksifaktor
δijk = Pengaruh sisa untuk anak petak atau pengaruh sisa karena pengaruh faktor
klon taraf ke-i dan faktor asam askorbat ke-j pada kelompok ke-k.
Data hasil pengamatan disusun dalam sidik ragam untuk masing masing
peubah amatan jika pengaruh perlakuan terhadap peubah yang diamati menunjukan
PELAKSANAAN PENELITIAN Plotting area Penelitian
Tahap awal dari penelitian ini adalah ploting areal penelitian dimana akan
dilakukan pengujian sampel. Tanaman akan dijadikan tanaman sampel ditandai
dengan jelas dengan cat dan diberi tali untuk menghindari kesalahan pengamatan dan
agar tanaman yang dijadikan tanaman sampel tidak disadap oleh penyadap.
Pengerokan Bidang Sadap
Setelah didapatkan sampel tanaman sampel tanaman yang mengalami
kejadian KAS maka sebelum pemberian asma askorbat terlebih dahulu bidang sadap
yang akan diberi perlakuan dikerok (bark scarpping) dengan pisau kerok untuk
mnghilangkan kulit luarnya kurang lebih 1-2 mm.
Perlakuan Pemberian Asam Askorbat
Asam askorbat yang diberikan sesuai dengan perlakuan dicampur dengan
gliserin dan dioleskan pada bidang sadap tanaman yang sudah dikerok. Interval
pemberian perlakuan adalah 1 kali dalam 1 minggu selama 4 bulan.
Pengamatan kondisi anatomis dan fisiologi
Pengamatan kondisi tersebut diamati dengan cara mengambil sampel lateks
(tanaman menunjukan gejala sembuh) dan kulit kulit untuk pengamatan
masing-masing peubah yang diamati.
Parameter Pengamatan Fisiologis lateks
Pengamatan kondisi fisiologis, yaitu kadar sukrosalateks, kadar fosfat
cara mengambil sampel lateks. Pengamatan ini dilakukan pada saat, 0, 2, 4, bulan
setelah pengaplikasian.
Peubah Amatan Thiol (R – SH) (mM)
Diukur dari serum asam Trikolro Asetat (TCA). Pengukuran dilakukan pada
sampel lateks yang sudah diambil serumnya melalui perendaman larutan trikloro –
asetat (McMullen, A, I. 1960. Berdasarkan prinsip reaksinya dengan asam dithiobis
– nitrobenzoat (DTNB) untuk membentuk TNB yang berwarna kuning yang
terabsorbsi pada λ 421 nm (nanometer) dengan spektrofotometer Beckman DU 650. Diukur pada setiap 2 bulan pengaplikasian.
Sukrosa (mM)
Diukur menggunakan metode anthrone (Dische, Z, M. 1962). Pengukuran
dilakukan pada sampel lateks yang sudah diambil serumnya melalui perendaman
larutan trikloroasetat kemudian dilarutkan pada larutan trikloro asetat sehingga
berupa serum. Dehidrasi sukrosa dalam asam sulfat pekat (H2SO4 70%) dan
pemanasan akan memberikan turunan furfural yang bereaksi dengan anthrone
mengadakan reaksi warna biru yang selanjutnya diukur absorbannya pada λ 627 nm (nanometer) dengan spektrofotometer Beckman DU 650 diukur pada setiap 2 bulan
pengaplikasian.
Fosfat Anorganik (Pi)
Diukur berdasarkan prinsip pengikatan oleh amonium molibdad
(Taussky H. H and E. Shor. 1953) . Pengukuran dilakukan pada sampel lateks yang
yang telah digerus dengan nitrogen cair kemudian dilarutkan pada larutan
trikloro-asetat sehingga berupa serum, kemudian tereduksi oleh FeSO4 yang telah
dicampurkandalam reaksi asam sehingga menjadi warna biru yang kemudian diukur
absorbannya pada λ 627 nm (nanometer) dengan spektrofotometer Beckman DU 650
diukur pada setiap 2 bulan pengaplikasian.
Produksi
Pengamatan terhadap produktivitas tanaman karet dilakukan 2 bulan setelah
perlakuan dan diamati setiap 10 hari sekali sehingga dapat dilihat apakah tanaman
yang telah mendapat perlakuan dapat menghasilkan lateks layaknya tanaman yang
sehat.
Produksi = Produksi (g/p/s) TSC x100
Pengukuran indeks penyumbatan (IP)
Indeks penyumbatan merupakan perbandingan dari laju pengaliran lateks
permenit dengan volume lateks total dikalikan 100. (Milford, et al,1969). Pengamatan
dilakukan di bulan ke 3 dan ke 4, diamati pada saat mulai penyadapan (pukul 5.30
WIB) di ukur volume lateks pada 5 menit pertama dan volume lateks pada akhir atau
total dengan gelas ukur pada setiap satuan percobaan.
Pengukuran kadar karet kering (KKK) /total solid content (TSC)
Pengukuran KKK dengan mengukur TSC (semua padatan selain patikel karet
ikut diukur) dilakukan dengan cara mengambil beberapa tetes contoh lateks segar
jam dengan suhu 65 0C hingga berat konstan. Persentase TSC diperoleh dengan
membandingkan berat basah dan berat kering dikalikan dengan 100% .
Superoksida dismutase (SOD)
Sampel lateks disentrifugasi 12 rpm selama 30 menit, jika serum belum
terpisah sampel disentrifugasi kembali 12 rpm selama 15 menit kemudian simpan
pada suhu 40C selama 15 menit. Vortex sebentar, kemudian ditambahkan aliquot
lisat. Pemeriksaan nilai aktivitas SOD dilakukan sesuai dengan metode yang
tercantum dalam kit SOD Randox. Satu unit enzim aktivitas SOD didevinisikan
sebagai aktifitas SOD/ mg protein. Kemudian di baca di spektrofotometer Beckman
DU 650. Diukur 2 kali, sebelum dan setelah 4 bulan pengaplikasian.
Analisis total protein
Lateks segar dikumpulkan dalam 1,5 ml tabung ependorf lalu sampel lateks di
sentrifugase untuk memisahkan fraksi karet dari total serum, kemudiam dikumpulkan
, eliquoted dan disimpan pada -800C lalu Kemudian di baca di spektrofotometer
Beckman DU 650 dengan absorbansi 595 nm. Dimana kadar protein ditentukan
sesuai metode Bradford (1976) diukur 2 kali, sebelum dan setelah 4 bulan
HASIL DAN PEMBAHASAN
Hasil
Fisiologi thiol lateks karet 0 bulan
Pengamatan fishiologi thiol lateks 0 bulan dari sidik ragam dapat dilihat pada
lampiran. Hasil sidik ragam diperoleh bahwa klon, konsentrasi asam askorbat dan
interaksi menunjukan tidak berbeda nyata
Rataan fisiologis thiol lateks 0 bulan dari klon dan konsentrasi asam askorbat
dapat dilihat pada tabel 1.
Tabel 1. fisiologi thiol lateks 0 bulan dengan perlakuan klon tanaman dan konsentrasi asam akorbat
Fisiologi thiol lateks karet 2 bulan
Pengamatan fishiologi thiol lateks 2 bulan dari sidik ragam dapat dilihat pada
lampiran. Hasil sidik ragam diperoleh bahwa klon , konsentrasi asam askorbat dan
interaksi menunjukan tidak berbeda nyata.
Rataan fisiologis thiol lateks 2 bulan dari klon dan konsentrasi asam askorbat
dapat dilihat pada tabel 2
Fisiologi thiol lateks karet 4 bulan
Pengamatan fishiologi thiol lateks 4 bulan dari sidik ragam dapat dilihat pada
lampiran . Hasil sidik ragam diperoleh bahwa klon , konsentrasi asam askorbat dan
interaksi menunjukan tidak berbeda nyata
Rataan fisiologis thiol lateks 4 bulan dari klon dan konsentrasi asam askorbat
dapat dilihat pada tabel 3.
Tabel 3. fisiologi thiol lateks 4 bulan dengan perlakuan klon tanaman dan konsentrasi asam askorbat
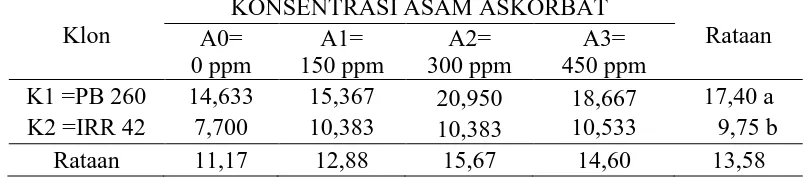
Fisiologi Fosfat Anorganik ( PI ) lateks karet 0 bulan
Pengamatan fishiologi Fosfat Anorganik ( PI ) lateks 0 bulan dari sidik ragam
dapat dilihat pada lampiran. Hasil sidik ragam diperoleh bahwa klon tanaman
menunjukan berbeda nyata pada fisiologis Fosfat Anorganik ( PI ) 0 bulan ,sedangkan
konsentrasi asam askorbat dan interaksi menunjukan tidak berbeda nyata.
Rataan fisiologis Fosfat Anorganik ( PI ) lateks 0 bulan dari klon dan
konsentrasi asam askorbat dapat dilihat pada tabel 4.
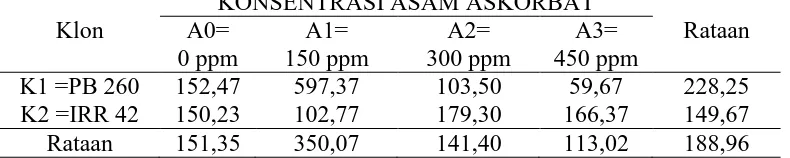
Tabel 4. fisiologi Fosfat Anorganik ( PI ) lateks 0 bulan dengan perlakuan klon tanaman dan konsentrasi asam akorbat
Keterangan : Data yang diikuti oleh huruf yang sama pada kolom yang sama tidak berbeda nyata berdasarkan Uji jarak berganda Duncan pada tara 5%
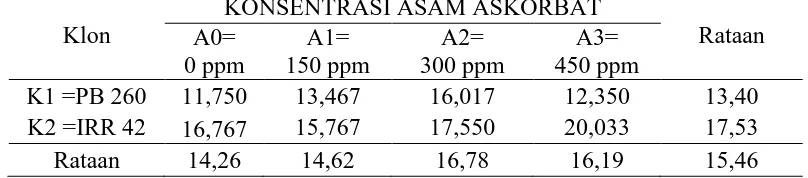
Fisiologi Fosfat Anorganik ( PI ) lateks karet 2 bulan
Pengamatan fishiologi Fosfat Anorganik ( PI ) lateks 2 bulan dari sidik ragam
dapat dilihat pada lampiran . Hasil sidik ragam diperoleh bahwa klon , konsentrasi
asam askorbat dan interaksi menunjukan tidak berbeda nyata.
Rataan fisiologis Fosfat Anorganik ( PI ) lateks 2 bulan dari klon dan
konsentrasi asam askorbat dapat dilihat pada tabel 5.
Tabel 5. fisiologi Fosfat Anorganik ( PI ) lateks 2 bulan dengan perlakuan klon tanaman dan konsentrasi asam akorbat
Klon
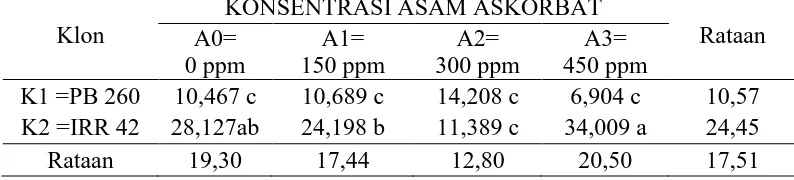
Fisiologi Fosfat Anorganik ( PI ) lateks karet 4 bulan
Pengamatan fishiologi Fosfat Anorganik ( PI ) lateks 4 bulan dari sidik ragam
dapat dilihat pada lampiran . Hasil sidik ragam diperoleh bahwa klon , konsentrasi
asam askorbat dan interaksi menunjukan tidak berbeda nyata.
Rataan fisiologis Fosfat Anorganik ( PI ) lateks 4 bulan dari klon tanam dan
konsentrasi asam askorbat dapat dilihat pada tabel 6.
Tabel 6. fisiologi Fosfat Anorganik ( PI ) lateks 4 bulan dengan perlakuan klon tanaman dan taraf asam akorbat
Fisiologi sukrosa lateks karet 0 bulan
Pengamatan fishiologi sukrosa lateks 0 bulan dari sidik ragam dapat dilihat
pada lampiran . Hasil sidik ragam diperoleh bahwa klon tanaman dan konsentrasi
asam askorbit terjadi interaksi berbedanyata.
Rataan fisiologis sukrosa lateks 0 bulan dari klon tanaman dan konsentrasi
asam askorbat dapat dilihat pada tabel 7.
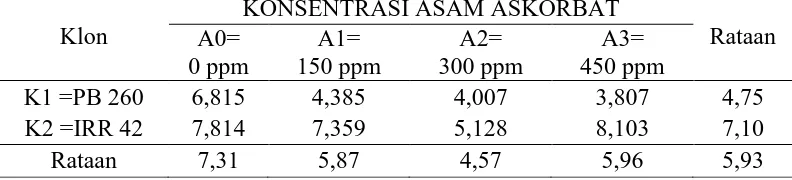
Tabel 7. fisiologi sukrosa lateks 0 bulan dengan perlakuan klon tanaman dan konsentrasi asam akorbat
Tabel 7 dapat dilihat bahwa interaksi perlakuan klon tanaman dengan
konsentrasi asam askorbat tertinggi terdapat pada K2A3 (34,10) berbeda nyata
dengan K2A2 (24,20) serta dengan K1A0 (10,47) K1A1 (10,69) K1A2 (14,21) K1A3
(6,90) K2A2 (11,39) namun K2A0 (28,13) tidak berbeda nyata dengan K2A3 (34,10)
Fisiologi sukrosa lateks karet 2 bulan
Pengamatan fishiologi sukrosa lateks 2 bulan dari sidik ragam dapat dilihat
pada lampiran . Hasil sidik ragam diperoleh bahwa klon , konsentrasi asam askorbat
dan interaksi menunjukan tidak berbeda nyata.
Rataan fisiologis sukrosa lateks 2 bulan dari klon tanam dan konsentrasi asam
Tabel 8. fisiologi sukrosa lateks 2 bulan dengan perlakuan klon tanaman dan
Fisiologi sukrosa lateks karet 4 bulan
Pengamatan fishiologi sukrosa lateks 4 bulan dari sidik ragam dapat dilihat
pada lampiran. Hasil sidik ragam diperoleh bahwa klon , konsentrasi asam askorbat
dan interaksi menunjukan tidak berbeda nyata.
Rataan fisiologis sukrosa lateks 4 bulan dari klon tanam dan konsentrasi asam
askorbat dapat dilihat pada tabel 9.
Tabel 9. fisiologi sukrosa lateks 4 bulan dengan perlakuan klon tanaman dan konsentrasi asam akorbat.
Superoksida dismutase (SOD) 0 bulan
Pengamatan Superoksida dismutase (SOD) lateks 0 bulan dari sidik ragam
dapat dilihat pada lampiran. Hasil sidik ragam di peroleh bahwa mnunjukan berbeda
nyata pada interaksi antar klon tanaman dan konsentrasi asam askorbat.
Rataan Superoksida dismutase (SOD) lateks 0 bulan dari klon tanam dan
Tabel 10. Superoksida dismutase (SOD) lateks 0 bulan dengan perlakuan klon tanaman dan konsentrasi asam akorbat.
Klon
Keterangan : Data yang diikuti oleh huruf yang sama pada kolom yang sama tidak berbeda nyata berdasarkan Uji jarak berganda Duncan pada tara 5%
Tabel 10 dapat dilihat bahwa inetraksi rataan klon tanaman dan konsentrasi
asam askorbat tertinggi terdapat pada K1A1 (67,40) berbeda nyata dengan perlakuan
K1A2 (41,93), K2A1 (20,70), K1A3 (20,07), K2A0 (15,27), K2A2 (14,87), K1A0
(12,20).
Superoksida dismutase (SOD) 4 bulan
Pengamatan Superoksida dismutase (SOD) lateks 4 bulan dari sidik ragam
dapat dilihat pada lampiran. Hasil sidik ragam diperoleh bahwa klon tanaman,
konsentrasi asam askorbat dan interaksi menunjukan tidak berbeda nyata.
Rataan Superoksida dismutase (SOD) lateks 4 bulan dari klon tanam dan
konsentrasi asam askorbat dapat dilihat pada tabel 11.
Tabel 11. Superoksida dismutase (SOD) lateks 4 bulan dengan perlakuan klon tanaman dan konsentrasi asam akorbat.
Klon
Pengamatan Produksi lateks ke 1, setelah 4 kali aplikasi di bulan ke 1 dari
sidik ragam dapat dilihat pada lampiran. Hasil sidik ragam diperoleh bahwa klon
tanaman, konsentrasi asam askorbat dan interaksi menunjukan tidak berbeda nyata.
Rataan produksi lateks ke 1, setelah 4 kali aplikasi di bulan ke 1 dari klon
tanam dan konsetrasi asam askorbat dapat dilihat pada tabel 12.
Tabel 12. produksi lateks ke 1, setelah 4 kali aplikasi di bulan ke 1 dengan perlakuan klon tanaman dan konsentrasi asam akorbat.
Klon
Produksi lateks ke 2, setelah 8 kali aplikasi di bulan ke 2
Pengamatan Produksi lateks ke 2, setelah 8 kali aplikasi di bulan ke 2 dari
sidik ragam dapat dilihat pada lampiran. Hasil sidik ragam diperoleh bahwa klon
tanaman menunjukan berbeda nyata pada produksi ke 2, setelah 8 kali aplikasi di
bulan ke 2, sedangkan konsentrasi asam askorbat tidak berbeda nyata.
Rataan produksi lateks ke 2, setelah 8 kali aplikasi di bulan ke 2 dari klon
tanam dan konsentrasi asam askorbat dapat di lihat pada tabel 13.
Tabel 13. produksi lateks ke 2, setelah 8 kali aplikasi di bulan ke 2 dengan perlakuan klon tanaman dan konsentrasi asam akorbat.
Klon
berdasarkan Uji jarak berganda Duncan pada taraf 5%
Tabel 13 dapat dilihat bahwa jenis klon tanama rataan produksi tertinggi
terdapat pada K1 (1,67 g) berbeda nyata dengan K2 (1,13 g).
Produksi lateks ke 3, 10 hari setelah aplikasi ke 9 di bulan ke 3
Pengamatan Produksi lateks ke 3, 10 hari setelah aplikasi ke 9 di bulan ke 3
dari sidik ragam dapat dilihat pada lampiran. Hasil sidik ragam diperoleh bahwa klon
tanaman dan konsentrasi asam askorbat menunjukan berbeda nyata pada produksi ke
3, 10 hari setelah aplikasi ke 9 di bulan ke 3.
Rataan produksi lateks ke 3, 10 hari setelah aplikasi ke 9 di bulan ke 3 dari
klon tanam dan konsentrasi asam askorbat dapat di lihat pada tabel 14.
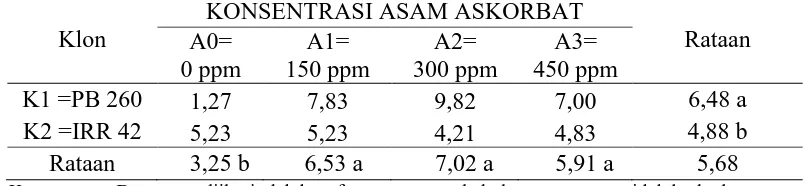
Tabel 14. produksi lateks ke 3, 10 hari setelah aplikasi ke 9 di bulan ke 3 dengan perlakuan klon tanaman dan konsentrasi asam akorbat.
Klon
Keterangan : Data yang diikuti oleh huruf yang sama pada kolom yang sama tidak berbeda nyata Berdasarkan Uji jarak berganda Duncan pada taraf 5%
Tabel 14 di ketahui bahwa rataan jenis klon tanaman tertinggi di dapat pada
K1 (6,48 g) berbeda nyata dengan K2 (4,88 g), sedangakan konsentrasi asam askorbat
A2 (7,02 g), A1 ( 6,53 g) dan A3 (5,91 g) berbeda nyata dengan A0 (3,25 g).
Produksi lateks ke 4, 10 hari setelah aplikasi ke 10 di bulan ke 3
Pengamatan Produksi lateks ke 4, 10 hari setelah aplikasi ke 10 di bulan ke 3
terdapat interkasi antara klon tanaman dan konsentrasi asam askorbat menunjukan
berbeda nyata pada produksi ke 4, 10 hari setelah aplikasi ke 10 di bulan ke 3.
Rataan produksi lateks ke 4, 10 hari setelah aplikasi ke 10 di bulan ke 3 dari
klon tanaman dan konsentrasi asam askorbat dapat di lihat pada tabel 15.
Tabel 15. produksi lateks ke 4, 10 hari setelah aplikasi ke 10 di bulan ke 3 dengan perlakuan klon tanaman dan konsentrasi asam akorbat.
Klon
Keterangan : Data yang diikuti oleh huruf yang sama pada kolom yang sama tidak berbeda nyata Berdasarkan Uji jarak berganda Duncan pada taraf 5%
Tabel 15 dapat di lihat bahwa interaksi rataan klon tanaman dan taraf asam
askorbat tertinggi terdapat pada K1A2 (10,07 G), K1A1 (8,72), K1A3 (7,87) berbeda
nyata dengan K2A1(6,15 g) K2A3 (6,03 g) K2A2 (3,38 g) K1A1 (1,41 g) K2A1
(1,08).
Produksi lateks ke 5, 10 hari setelah aplikasi ke 11 di bulan ke 3
Pengamatan Produksi lateks ke 5, 10 hari setelah aplikasi ke 11 di bulan ke 3
dari sidik ragam dapat dilihat pada lampiran. Hasil sidik ragam diperoleh bahwa
konsentrasi asam askorbat menunjukan berbeda nyata pada produksi ke 5, 10 hari
setelah aplikasi ke 11 di bulan ke 3, sedangkan jenis klon tanaman dan interaksi tidak
berbeda nyata.
Rataan produksi lateks ke 5, 10 hari setelah aplikasi ke 11 di bulan ke 3 dari
Tabel 16. produksi lateks ke 5, 10 hari setelah aplikasi ke 11 di bulan ke 3 dengan perlakuan klon tanaman dan konsentrasi asam akorbat.
Klon
Keterangan : Data yang diikuti oleh huruf yang sama pada kolom yang sama tidak berbeda nyata Berdasarkan Uji jarak berganda Duncan pada taraf 5%
Tabel 16 di ketahui bahwa rataan jenis klon tanaman tertinggi di dapat pada
konsentrasi asam askorbat A1 (5,89 g), A3 ( 4,68 g) dan A2 (4,66 g) berbeda nyata
dengan A0 (1,46 g).
Produksi lateks ke 6, 10 hari setelah aplikasi ke 12 di bulan ke 4
Pengamatan Produksi lateks ke 6, 12 hari setelah aplikasi ke 12 di bulan ke 4
dari sidik ragam dapat dilihat pada lampiran. Hasil sidik ragam diperoleh bahwa
konsentrasi asam askorbat menunjukan berbeda nyata pada produksi ke 6, 10 hari
setelah aplikasi ke 12 di bulan ke 4, sedangkan jenis klon tanaman dan interaksi tidak
berbeda nyata.
Rataan produksi lateks ke 6, 10 hari setelah aplikasi ke 12 di bulan ke 4 dari
klon tanam dan konsentrasi asam askorbat dapat di lihat pada tabel 17.
Tabel 17. Produksi lateks ke 6, 10 hari setelah aplikasi ke 12 di bulan ke 4 dengan perlakuan klon tanaman dan konsentrasi asam akorbat.
Klon
Tabel 17. di ketahui bahwa rataan konsentrasi tertinggi di dapat pada
konsentrasi asam askorbat A3 (8,23 g) A1 ( 8,20 g) dan A2 (5,97 g) berbeda nyata
dengan A0 (1,35 g).
Produksi lateks ke 7, 10 hari setelah aplikasi ke 13 di bulan ke 4
Pengamatan Produksi lateks ke 7, 10 hari setelah aplikasi ke 13 di bulan ke 4
dari sidik ragam dapat dilihat pada lampiran. Hasil sidik ragam diperoleh bahwa jenis
klon tanaman dan konsentrasi asam askorbat menunjukan berbeda nyata pada
produksi ke 7, 10 hari setelah aplikasi ke 13 di bulan ke 4, sedangkan interaksi tidak
berbeda nyata.
Rataan produksi lateks ke 7, 10 hari setelah aplikasi ke 13 di bulan ke 4 dari
klon tanam dan konsentrasi asam askorbat dapat di lihat pada tabel 18.
Tabel 18. Produksi lateks ke 7, 10 hari setelah aplikasi ke 13 di bulan ke 4 dengan perlakuan klon tanaman dan konsentrasi asam akorbat.
Klon
Keterangan : Data yang diikuti oleh huruf yang sama pada kolom yang sama tidak berbeda nyata berdasarkan Uji jarak berganda Duncan pada taraf 5%
Tabel 18 di ketahui bahwa rataan jenis klon tanaman tertinggi di dapat K1
(9,28) berbeda nyata dengan K2 (3,26 g) dan rataan konsentrasi tertinggi di dapat
pada konsentrasi asam askorbat A2 (8,67 g) A1 ( 7,48 g) serta A3 (7,17 g) berbeda
Produksi lateks ke 8, 10 hari setelah aplikasi ke 14 di bulan ke 4
Pengamatan Produksi lateks ke 8, 10 hari setelah aplikasi ke 14 di bulan ke 4
dari sidik ragam dapat dilihat pada lampiran. Hasil sidik ragam diperoleh bahwa
terdapat interkasi antara klon tanaman dan konsentrasi asam askorbat menunjukan
berbeda nyata pada produksi ke 8, 10 hari setelah aplikasi ke 14 di bulan ke 4,
sedangkan jenis klon tanaman dan konsentrasi tidak berbeda nyata.
Rataan produksi lateks ke 8, 10 hari setelah aplikasi ke 14 di bulan ke 4 dari
klon tanam dan konsentrasi asam askorbat dapat di lihat pada tabel 19.
Tabel 19. Produksi lateks ke 8, 10 hari setelah aplikasi ke 14 di bulan ke 4 dengan perlakuan klon tanaman dan konsentrasi asam akorbat.
Klon
Keterangan : Data yang diikuti oleh huruf yang sama pada kolom yang sama tidak berbeda nyata berdasarkan Uji jarak berganda Duncan pada taraf 5%
Tabel 19 dapat di lihat bahwa interaksi rataan klon tanaman dan konsentrasi
asam askorbat tertinggi terdapat pada K1A1 (13,55 g), K1A3 (10.68 g),
berbeda nyata dengan K1A2 (7,38 g), K2A2 (4,43 g), K2A3 (4,28 g), K2A1(2,57 g),
K2A0(1,15 g), K1A0 (1,03 g).
Pengamatan IP (indeks penyumbatan) 2 bulan aplikasi dari sidik ragam dapat
dilihat pada lampiran. Hasil sidik ragam diperoleh bahwa klon tanaman, konsentrasi
asam askorbat dan interaksi menunjukan tidak berbeda nyata.
Rataan IP (indeks penyumbatan) 2 bulan aplikasi dari klon tanaman dan
konsentrasi asam askorbat dapat dilihat pada tabel 20.
Tabel 20. IP (indeks penyumbatan) 2 bulan aplikasi dengan perlakuan klon tanaman dan konsentrasi asam akorbat.
IP (indeks penyumbatan) 4 bulan aplikasi
Pengamatan IP (indeks penyumbatan) 4 bulan aplikasi dari sidik ragam dapat
dilihat pada lampiran. Hasil sidik ragam diperoleh bahwa klon tanaman, konsentrasi
asam askorbat dan interaksi menunjukan tidak berbeda nyata.
Rataan IP (indeks penyumbatan) 4 bulan aplikasi dari klon tanaman dan
konsentrasi asam askorbat dapat dilihat pada tabel 21.
Pembahasaan
Respon pemberian konsentrasi asam askorbat pada klon yang berbeda terhadap status fishiologi tanaman karet yang terkena KAS parsial
Hasil pengamatan dan sidik ragam dapat dilihat bahwa jenis klon tanaman dan
konsentrasi asam askorbat tidak berbedanyata terhadap respon fisiologis thiol. Nilai
nilai fisiologis thiol yang dilakukan aplikasi selama 4 bulan mengalami peningkatan
hal ini sesuai dengan pernyataan Tistama et all ( 2006) yang menyatakan komponen
fisiologis lateks lainnya adalah thiol. Thiol (R-SH) berperan dalam mengaktifkan
beberapa enzim yang berhubungan dengan cekaman lingkungan. Status thiol
berhubungan pada saat mendapat tekanan sistem ekploitasi. Semakin tinggi intensitas
eksploitasi semakin rendah setatus thiol dalam lateks. Pada tanaman yang mengalami
KAS setatus thiolnya lebih rendah dibandingkan dengan tanaman sehat. Kemunkinan
jaringan kulit mengalami proses keletihan yang dapat diikuti dengan kematian secara
parsial sel-sel pembuluh lateks.
Hasil pengamatan dan sidik ragam dapat dilihat bahwa jenis klon tanaman dan
konsentrasi asam askorbat tidak berbedanyata terhadap respon fisiologis fosfat
anorganik (PI). Nilai nilai fisiologis fosfat anorganik (PI) yang dilakukan aplikasi
selama 4 bulan mengalami peningkatan hal ini sesuai dengan pernyataan
Krisnakumar et al (2001) yang menyatakan tanaman yang terkena KAS terjadi
hambatan perubahan mevalonat menjadi isopenteril piroposfat (IPP). Hambatan
tersebut terjadi akibat kurangnya suplai ATP sebagai sumber energi pada reaksi
perubahan mevalonat menjadi IPP . Pada tahapan tersebut merupakan proses reaksi
status fosfat anorganik yang rendah didalam lateks pada tanaman terserang KAS.
Kandungan PI memang cendrung menurun jika tanaman dieksploitasi dengan sistem
sadap yang lebih intensip.
Hasil pengamatan dan sidik ragam dapat dilihat bahwa jenis klon tanaman dan
konsentrasi asam askorbat tidak berbedanyata terhadap respon fisiologis Sukrosa.
Nilai nilai fisiologis sukrosa yang dilakukan aplikasi selama 4 bulan mengalami
penurunan hal ini sesuai dengan pernyataan tistama et al (2006) yang meyatakan dari
hasil pengamatan terhadap kandungan sukrosa pada tanaman yang sehat an tanaman
yang terkena KAS sebagian , ternyata kandungan sukrosa dari pada tanaman yang
sehat. hal ini membuktikan dua hal, pertama : adanya suplai sukrosa ynang normal
pada tanaman yang terserang KAS, kedua: adanya hamabatan biosintesis karet
sehingga sukrosa tidak dimanfaatkan dalam proses tersebut sehingga terjadi
penumpukan.
Respon pemberian konsentrasi asam askorbat pada klon yang berbeda terhadap status ROS tanaman karet yang terkena KAS parsial
Hasil pengamatan dan sidik ragam dapat dilihat bahwa jenis klon tanaman dan
konsentrasi asam askorbat tidak berbedanyata terhadap respon enzim SOD dan
Indeks Penyumbata (IP) . Hal ini dikarenakan funsi enzim yang menghadapi ROS
berbeda beda dan ketidak seimbangan aktifitas enzim SOD, APX, katalase serta
Indek Penyumbatan (IP) terganggu karna tertekan toksisitas ROS hal ini sesuai
dalam menghadapi ROS mengakibatkan tingkat ekspresi gen responsif terhadap ROS
beragam pada berbagai perlakuan. Seperti telah disebutkan sebelumnya bahwa
tingkat cekaman oksidatif dapat ditentukan dari jumlah ROS seperti superoksida,
peroksida, dan radikal hidroksil. Oleh karena itu, keseimbangan aktifitas enzim SOD,
APX, dan katalase sangat penting untuk menekan level toksisitas ROS di dalam sel.
Saat aktifitas katalase rendah di tanaman, aktifitas enzim lain, yaitu APX akan
meningkat.
Hasil penelitian yang telah dilakukan jenis klon tanaman terhadap perlakuan
yang dilakukan yaitu jenis klon tanaman dan kosentrasi asam askorbat. Jenis klon
tanaman yang kondisi labil dikarnkan kekurangan giji dan logam berat hal ini sesuai
dengan pernyataan Sarvajeet dan Narendra ( 2010 ) Dalam kondisi labil, molekul
ROS memulung berbagai mekanisme pertahanan antioksidan. Kesetimbangan antara
produksi dan pemulungan ROS mungkin terganggu oleh berbagai faktor stresbiotik
dan abiotik seperti salinitas, radiasi UV, kekeringan, logam berat, suhu ekstrim,
kekurangan gizi dan udara. Melalui berbagai reaksi, O2 mengarah pada pembentukan
H2O2, OH dan ROS lainnya. ROS terdiri O2, H2O2, 1O2, HO2, OH, ROOH, ROO, dan
RO yang sangat reaktif dan beracun dan penyebab kerusakan protein, lipid,
karbohidrat, DNA yang akhirnya menghasilkan kematian sel.
Respon pemberian konsentrasi asam askorbat pada klon yang berbeda terhadap status produksi tanaman yang terkena KAS parsial
Hasil penelitian yang telah dilakukan menunjukan bahwa jenis klon tanaman
pada tanaman yang terkena KAS parsial terhadap pemberian berbagai jenis
amatan produksi 1,3,4 dan 7 tetapi belum berpengaruh nyata terhadap peubah amatan
produksi 2,5,6 dan 8.
Adanya perbedaan respon produksi tanaman pada pengamatan produksi
bahwa antara klon tanaman karet PB 260 menunjukan berbeda nyata dalam produksi
dimana dari tabel dapat diketahui rataan tertingi produksi 1 K2 (0,46 g), produksi 3
K1 (6,48 g), produksi 4 K1 (7,02 g), produksi 7 K1 (9,28 g) dan produksi K1 (8,19 g)
namun berbeda nyata pada klon tanaman karet IRR 42 produksi 1 K1 (0,46 g),
produksi 3 K1 (4,88 g), produksi 4 K1 (4,16 g), produksi 7 K1 (3,26 g), dan
roduksi 8 K2 (8,16 g) hal ini di sebabkan klon PB 260 penghasil lateks dan klon IRR
42 penghasil lateks-kayu. Hal ini sesuai dengan pernyaatan Peraturan Menteri
Pertanian Republik Indonesia (2013) yang menyatakan untuk Rekomendasi klon-klon
karet untuk periode tahun 2010-2014 berdasarkan hasil rumusan Lokakarya Nasional
Pemuliaan Tanaman Karet Tahun 2009, yaitu sebagai berikut: Klon Anjuran
Komersial a.) klon penghasil lateks terdiri: IRR 104, IRR 112, IRR 118, IRR 220,
BPM 24, PB 260, PB 330, dan PB 340; b.) klon penghasil lateks-kayu terdiri: IRR 5,
IRR 39, IRR 42, IRR 107,dan RRIC 100.
Hasil penelitian yang telah dilakukan menunjukan bahwa jenis konsentrasi
asam askorbat pada jenis klon tanaman yang terkena KAS parsial menunjukan
pengaruh yang nyata terhadap peubah amatan produksi 3,4,5,6,7 dan 8 tetapi belum
berpengaruh nyata terhadap peubah amatan produksi 1 dan 2.
Adanya perbedaan respon produksi tanaman pada pengamatan produksi
bahwa konsentrasi asam askorbat menunjukan berbeda nyata dalam produksi dimana
(5,91 g), produksi 4 A1 (7,44 g), A2 (6,72 g), A3 (6,95 g), produksi 5 A1 (5,89 g),
A2 (4,66 g), A3 (4,68 g), produksi 6 A1 (8,20 g), A2 (5,97 g), A3 (8,23 g), produksi 7
A1 (7,48 g), A2 (8,67 g), A3 (7,17 g), produksi 8 A1 (8,06 g), A2 (5,90 g), A3
(7,48 g) namun berbeda nyata pada produksi 3 A0 (3,25 g), produksi 4 A0 (1,24 g),
produksi 5 A0 (1,46 g), produksi 6 A0 (1,35 g), produksi 7 A0 (1,75 g), produksi 8
A0 (1,09 g). Hal ini disebabkan karna asam askorbat atau vitamin c adalah
antioksidan yang dapat melawan radikal bebas. Hal ini sesuai dengan pernyataan
Ardianti et all (2014) yang menatakan Antioksidan merupakan senyawa yang mampu
menghambat laju oksidasi. Antioksidan ini memiliki banyak komponen dan
merupakan zat alami yang dihasilkan sendiri oleh tubuh atau didapat dari makanan
yang kita makan. Antioksidan bekerja dengan cara menghentikan pembentukan
radikal bebas, menetralisir serta memperbaiki kerusakan-kerusakan yang terjadi.
Radikal bebas merupakan atom atau melekul yang memiliki satu atau lebih elektron
yang tidak berpasangan. Radikal bebas dianggap pasangan elektronnya. Radikal
bebas dapat bereaksi dengan molekul sel tubuh dengan cara mengikat elektron dari
melekul sel tersebut dan dapat menyebabkan reaksi berantai yang merusak tubuh.
Hasil penelitian yang telah dilakukan, terdapat interaksi yang nyata terhadap
perlakuan yang telah di lakukan dalam peubah amatan produksi ke 4 dan ke 8, dari
tabel dapat diketahui interaksi tertinggi produksi ke 4 K1A2 (10,07 g) dan produksi
ke 8 K1A1 (13,55 g) namun berbeda nyata pada produksi ke 4 K2A0 (1,08 g) dan
produksi ke 8 K1A1 (1,03 g). Hal ini disebabkan bahwa asam askorbat sebagai
antioksidan yang mampu meningkatkan substrat enzim dan mampu mentoleransi
pendekatan untuk mendorong toleransi stres oksidatif yang akan
meningkatkansubstrat enzim pada tingkat sel adalah asamaskorbat. Asam askorbat
berfungsi sebagai antioksidan, kofaktor enzim dan sebagai modulator sel sinyal dalam
beragam proses fisiologis penting, termasuk biosintesis dinding sel, metabolit
sekunder dan fitohormon, toleransi stres, fotoproteksi, pembelahan dan pertumbuhan
sel.
KESIMPULAN DAN SARAN Kesimpulan
Hasil penelitian yang telah dilkukan di dapat kesimpulan bahwa:
1. Klon tanaman karet PB 260 memiliki produksi lebih tinggi dibandingkan
2. Tidak ada pengaruh konsentrasi asam askorbat terhadap peubah amatan
fisiologi (Thiol, sukrosa, PI), aktivitas superoksida dismutase (SOD) dan
indeks penyumbatan (IP).
3. Interaksi antara jenis klon tanaman karet dan konsentrasi asam askorbat
berpengaruh nyata terhadap peubah amatan produksi tanaman.
4. Kosentrasi asam askorbat 150 ppm sudah dapa berpengaruh nyata terhadap
peubah amatan produksi tanaman karet yang terkena KAS parsial yang
merupakan antioksidan melawan radikal bebas.
Saran
Dari hasil penelitian konsentrasi asam askorbat perlu di teliti lebih lanjut
untuk melihat analisis parameter produksi dan cekaman ROS, agar di peroleh
konsentrasi berapa untuk mendapatkan hasil produksi lateks yang tinggi serta yang
TINJAUAN PUSTAKA Botani Tanaman
Menurut Steenis et al, (2005) kedudukan tanaman karet dalam tatanama
(sistematika) sebagai berikut: Kingdom: Plantae, Divisio: Spermatophyta,
Sub-diivisio: Angiospermae, Kelas: Dicotyledoneae, Ordo: Euphorbiales, Famili:
Euphorbiaceae, Genus:Hevea, Spesies : Hevea brassiliensis Muell. Arg.
Akar tanaman karet merupakan akar tunggang yang mampu menopang batang
tanaman yang tumbuh tinggi ke atas, dengan akar seperti itu pohon karet dapat berdiri
kokoh, meskipun tingginya mencapai 25 meter (Setiawan dan Andoko, 2005).
Karet merupakan pohon yang tumbuh tinggi dan berbatang cukup besar.
Tinggi pohon dewasa mencapai 15-25 meter. Batang tanaman biasanya tumbuh lurus
dan memiliki percabangan yang tinggi. Dibeberapa kebun karet ada kecondongan
arah tumbuh tanamanya agak miring ke arah utara. Batang tanaman ini mengandung
getah yang dikenal dengan nama lateks (Nugroho, 2010).
Daun karet berselang-seling, tangkai daunnya panjang, terdiri dari 3 anak
daun yang licin berkilat. Petiola tipis, hijau, panjang 3,5-30 cm. Helaian anak daun
bertangkai pendek dan berbentuk lonjong-oblong atau oblong-obovate, pangkal
sempit dan tegang, ujung runcing; sisi atas daun hijau tua dan sisi bawah agak cerah,
panjangnya 5-35 cm dan lebar 2,5-12,5 cm (Sianturi, 2001).
Bunga karet terdiri dari bunga jantan dan betina yang terdapat dalam malai
payung tambahan yang jarang. Pangkal tenda bunga berbentuk lonceng. Pada
ujungnya terdapat lima taju yang sempit. Panjang tenda bunga 4-8 mm. Bunga betina
buah yang beruang 3. Kepala putik yang akan dibuahi dalam posisi duduk juga
berjumlah 3 buah. Bunga jantan mempunyai 10 benang sari yang tersusun menjadi
suatu tiang. Kepala sari terbagi dalam 2 karangan, tersusun 9 satu lebih tinggi dari
yang lain. Paling ujung adalah suatu bakal buah yang tidak tumbuh sempurna
(Maryani, 2007).
Karet merupakan buah berpolong (diselaputi kulit yang keras) yang sewaktu
masih muda buah berpaut erat dengan rantingnya. Buah karet dilapisi oleh kulit tipis
berwarna hijau dan didalamnya terdapat kulit yang keras dan berkotak. Tiap kotak
berisi sebuah biji yang dilapisi tempurung, setelah tua warna kulit buah berubah
menjadi keabu - abuan dan kemudian mengering. Pada waktunya pecah dan jatuh,
tiap ruas tersusun atas 2 – 4 kotak biji. Pada umumnya berisi 3 kotak biji dimana
setiap kotak terdapat 1 biji. Biji karet terdapat dalam setiap ruang buah. Jumlah biji
biasanya ada tiga kadang empat (Budiman, 2012).
Buah beruang tiga, jarang yang beruang 4 hingga 6, diameter buah 3-5 cm
dan terpisah 3,4,6. Coci berkatupdua, pericarp berbentuk endokarp berkayu. Biji
besar, bulat persegi empat, tertekan pada satu atau dua sisinya, berkilat berwarna
coklat muda, dengan noda oda coklat tua, panjang 2-3,5 dan tebal 1,5-2,5 cm
(Sianturi, 2001).
Syarat Tumbuh Iklim
Secara garis besar tanaman karet dapat tumbuh baik pada kondisi iklim
sebagai berikut: suhu rata-rata harian 280C (dengan kisaran 25–350C) dan curah hujan
pertahun. Pada daerah yang sering hujan pada pagi hari akan mempengaruhi kegiatan
penyadapan bahkan akan mengurangi hasil produktifitasnya. Keadaan daerah yang
cocok untuk tanaman karet adalah daerah-daerah Indonesia bagian barat, yaitu
Sumatera, Jawa dan Kalimatan, sebab iklimnya lebih basah (Budiman, 2012).
Tanaman karet memerlukan curah hujan optimal antara 2.500 mm sampai
4.000 mm/tahun,dengan hari hujan berkisar antara 100 sd. 150 HH/tahun. Namun
demikian, jika sering hujan pada pagi hari, produksiakan berkuran (Anwar, 2001).
Kelembaban nisbi (RH) yang sesuai untuk tanaman karet adalah rata – rata
berkisar antara 75% - 90%. Kelembapan yang terlalu tinggi tidak baik untuk
pertumuhan karet, karena dapat membuat laju aliran transpirasi tanaman karet
menjadi kecil sehingga absorbsi unsur hara dari tanah menjadi lambat. Selain itu
tanaman sering mengalami gutasi dan terjadi kelelahan lateks akibat retakan kulit.
Angin yang bertiup kencang dapat mengakibatkan patah batang, cabang atau
tumbang. Angin kencang pada musim kemarau sangat berbahaya, laju
evapotranspirasi menjadi besar (Sianturi, 2001).
Tanah
Berbagai jenis tanah dapat sesuai dengan syarat tumbuh tanaman karetbaik
tanah vulkanis muda dan tua, bahkan pada tanah gambut < 2 m. Tanah vulkanis
mempunyai sifat fisika yang cukup baik terutama struktur, tekstur, sulum, kedalaman
air tanah, aerasi dan drainasenya, tetapi sifat kimianya secara umum kurang baik
karena kandungan haranya rendah. Tanah alluvial biasanya cukup subur, tetapi sifat
fisikanya terutama drainase dan aerasenya kurang baik. Reaksi tanah berkisar antara
Tanaman karet bukanlah tanaman manja, dapat tumbuh pada tanah- tanah
yang mempunyai sifat fisik baik, atau sifat fisiknya dapat diperbaiki. Tanah yang
dikehendaki adalah bersolum dalam, kedalaman lapisan padas lebih dari 1 m,
pemukaan air tanah rendah yaitu ± 10 – 20 cm. Sangat toleran terhadap kemasaman
tanah, dapat tumbuh pada pH 3,8 hingga 8,0 , tetapi pada pH yang lebih tinggi sangat
menekan pertumbuhan (Siaturi, 2001).
Klon Tanaman Karet
Untuk meningkatkan produktivitas perkebunan karet rakyat, pemerintah telah
menempuh berbagai upaya antara lain perluasan tanaman, penyuluhan, intensifikasi,
rehabilitasi dan peremajaan serta penyebaran klon – klon unggul benih karet. Dalam
menunjang keberhasilan peningkatan produktivitas perkebunan karet, telah dilakukan
usaha khususnya terhadap benih karet (Syukur, 2013).
Rekomendasi klon-klon karet untuk periode tahun 2010-2014 berdasarkan
hasil rumusan Lokakarya Nasional Pemuliaan Tanaman Karet Tahun 2009,
yaitu sebagai berikut: Klon Anjuran Komersial a.) klon penghasil lateks
terdiri: IRR 104, IRR 112, IRR 118, IRR 220, BPM 24, PB 260, PB 330, dan PB 340;
b.) klon penghasil lateks-kayu terdiri: IRR 5, IRR 39, IRR 42, IRR 107,dan RRIC
100 (Peraturan Menteri Pertanian Republik Indonesia, 2013).
Potensi Klon PB260 Penghasil lateks Pertumbuhan jagur Resisten :
Corynespora Colletotrichum & Oidium.Produksi Lateks: 1.5-2.5 ton/ha/th. Warna :
putih kekuningan. Lateks diolah: sheet (Janudianto et al., 2013).
Klon dari jenis IRR ini terdiri dari klon penghasil lateks (IRR 104),
penghasil kayu (IRR 70, IRR 71, dan IRR 72). Klon IRR termasuk dalam klon
anjuran yang diharapkan dapat menjadi salah satu solusi untuk meningkatkan
produktivitas tanaman karet yang ada di Indonesia. Klon IRR memiliki potensi
produksi mencapai 2,9 – 3,2 ton karet kering per ha per tahun, sehingga sangat
potensial untuk dijadikan sebagai batang atas (Marchino et al., 2010).
Pada umumnya klon yang berproduksi tinggi tanpa stimulasi mempunyai
kadar Pi tinggi dan sukrosa rendah, yang menunjukkan aktifitas metabolisme yang
tinggi. Sebaliknya, kadar Pi rendah dan sukrosa tinggi pada klon berproduksi rendah,
yang menunjukkan rendahnya aktifitas metabolisme lateks (Lacote, 2007).
Thiol (R-SH) berfungsi sebagai antioksidan, sehingga stress oksidatif sebagai
akibat aktifnya metabolisme dalam sel dapat ditekan. Kadar R-SH yang rendah
menunjukkan terlalu intensifnya eksploitasi sehingga perlu dikurangi dengan
menurunkan intensitas sadapan maupun stimulasi (Gohet et al.,1996).
Kering Alur Sadap (KAS)
Penyakit kekeringan alur sadap mengakibatkan kekeringan alur sadap
sehingga tidak mengalirkan lateks, namun penyakit ini tidak mematikan tanaman.
Penyakit ini disebabkan oleh penyadapan yang terlalu sering, terlebih jika disertai
dengan penggunaan bahan perangsang lateks ethepon. Adanya kekeringan alur sadap
mula-mula ditandai dengan tidak mengalirnya lateks pada sebagian alur sadap.
Kemudian dalam beberapa minggu saja keseluruhan alur sadap ini kering tidak
mengeluarkan lateks. Bagian yang kering akan berubah warnanya menjadi cokelat
karena pada bagian ini terbentuk gum (blendok). Kekeringan kulit tersebut dapat
pulihan atau sebaliknya. Gejala lain yang ditimbulkan penyakit ini adalah terjadinya
pecah-pecah pada kulit dan pembengkakan atau tonjolan pada batang tanaman
(Anwar,2001).
Sel pembuluh lateks mngalami penyumbatan dan menjadi sel tilasoid. Sel
tilasoid ini melebar ke arah sel sel tetangga dan meluas sehingga jaringan tilasoidpun
berbentuk. Bidang sadap yang memiliki jaringan tilasoid ini bila disadap pada
awalnya akan mengalami kekeringan alur sadap sebagian (KAS parsial), kemudian
meluas dan dikenal sebagai KAS total (Tistama et al., 2006).
Kejadian KAS menurut Abraham et al, (2006). Diklasifikasikan menjadi
tanaman tidak terserang KAS (0%), rendah (0-25%), sedang (25-50%), tinggi
(50-75%), dan sangat tinggi (>75%). Klasifikasi tersebut digunakan untuk mengetahui
luas kejadian KAS dibidang panel sadapan. Persentase kejadian KAS dapat diperoleh
dari perbandingan panjang luas yang tidak mengeluarkan lateks dengan total panjang
keseluruhan bidang sadap dikalikan 100%.
Kering alur sadap dapat menyebar dengan cepat dalam angka waktu 2-4 bulan
keseluruh kulit bidang sadap. Penyebaran KAS diduga mengikuti alur pembuluh
lateks dan arah sadap. Proses penyebaran KAS pada bidang sadap BO-1 mengarah
keseluruh BO-1 dibawah irisan sadap. Penyebaran berikutnya menyebar ke bidang
panel BO-2 dibagian bawah yang dilanjutkan ke bagian atas hingga bertemu
mencapai HO-1. Pola penyebaran KAS di B1-1 hingga B1-2 kulit juga sama. Proses
penyebaran yang cepat disbabkan oleh kecepatan terbentuknya tilasoid lebih tinggi
Kejadian KAS banyak terjadi di perkebunan karet akibat penerapan sistem
eksploitasi yang tidak tepat. Fakta yang sring kali ditemukan di lapangan yaitu
praktisi kebun tidak membedakan konsentrasi dan interval aplikasi stimulan untuk
klon quick starter maupun klon slow starter, pemberian stimulan saat musim gugur
daun ,banyak terdapat luka kayu, dan konsumsi kulit yang boros
(Jacob and Krishnakumar, 2006).
Deteksi dini dampak intensitas exploitasi terhadap tanaman karet dapat
dilakukan dengan analisis fisiologi berupa ukrosa, PI (fosfat anorganik) dan thiol.
Status ketiga unsur tersebut dapat digunakan untuk menilai kondisi keletihan
fisiologis tanaman. Titik kritis status ketiga unsur tersebut sangat tergantung kepada
klon, unsur dan dinamika fisiologis tanaman atau variasi musiman. Secara umum
dapat digambarkan bahwa titik kritis untuk sukrosa < 4 mM, untuk pi >25 mM dan
untuk thiol < 0,4Mm. Dalam penilaian ini biasanya masih membutuhkan peubah
peubah yang lain (produksi g/p/s, kadar karet kering dan sebagainya. Namun cara ini
dapat secara preventif mengatsi terjadinya KAS. Beberapa perkebunan menerapkan
analisis lateks setahun sekali untuk menetapkan sistem sadap tahun berikutnya
(Tistama et al., 2006).
Gangguan fisiologis pada tanaman karet yaitu sebagian atau seluruh alur
sadapnya kering dan tidak mengalir lateks, atau bisa disebut brown bast (BB) atau
tapping dryness (TPD) atau kering alur sadap (KAS) dan sebagian petani pekebun
ada yang menyebut mati kulit, diduga disebabkan oleh terjadinya ketidak seimbangan
yakini antara lain disebabkan karena gangguan stimulan yang tidak mengikuti
anjuran. Akibatnya antara lain menurunnya kemampuan pohon untuk memproduksi
lateks (Arief dan Island, 2006).
Hasil pengamatan terhadap kandungan sukrosa pada tanaman yang sehat dan
tanaman yang terkena KAS sebagian , ternyata kandungan sukrosa dari pada
tanaman yang sehat . hal ini membuktikan dua hal, pertama : adanya suplai sukrosa
yang normal pada tanaman yang terserang KAS, kedua: adanya hamabatan biosintesis
karet sehingga sukrosa tidak dimanfaatkan dalam proses tersebut sehingga terjadi
penumpukan (Tistama et al, 2006).
Tanaman yang terkena KAS terjadi hambatan perubahan mevalonat menjadi
isopenteril piroposfat (IPP). Hambatan tersebut terjadi akibat kurangnya suplai ATP
sebagai sumber energi pada reaksi perubahan mevalonat menjadi IPP. Pada tahapan
tersebut merupakan proses reaksi yang membutuhkan banyak energi. Status ATP
yang rendah juga diiringi dengan status fosfat anorganik yang rendah didalam lateks
pada tanaman terserang KAS. Kandungan PI memang cendrung menurun jika
tanaman dieksploitasi dengan sistem sadap yang lebih intensip
(Krisnakumar et al, 2001).
Komponen fisiologis lateks lainnya adalah thiol. Thiol (R-SH) berperan dalam
mengaktifkan beberapa enzim yang berhubungan dengan cekaman lingkungan. Status
thiol berhubungan pada saat mendapat tekanan sistem ekploitasi. Semakin tinggi
mengalami KAS setatus thiolnya lebih rendah dibandingkan dengan tanaman sehat.
Kemunkinan jaringan kulit mengalami proses keletihan yang dapat diikuti dengan
kematian secara parsial sel-sel pembuluh lateks (Tistama et al, 2006).
Reactive Oxygen Species (ROS)
Radikal bebas dibentuk oleh metabolisme xenobiot atau metabolismesel aerob
secara normal. Reactive oxygen species (ROS) adalah radikal bebas yang berperan
penting pada beberapa proses fisiologis organ tubuh. Pembentukan ROS dapat
menginduksi peroksidasi lipid yang bersifat sitotoksik akibat inisiasi suatu reaksi
rantai kedalam membran, diikuti reaksi propagasi sehingga secara keseluruhan akan
mengakibatkan kerusakan sel (Astuti et al.,2009).
Dalam kondisi labil, molekul ROS memulung berbagai mekanisme
pertahanan antioksidan. Kesetimbangan antara produksi dan pemulungan ROS
mungkin terganggu oleh berbagai faktor stres biotik dana biotik seperti salinitas,
radiasi UV, kekeringan, logam berat, suhu ekstrim, kekurangan gizi dan udara.
Melalui berbagai reaksi, O2mengarah pada pembentukan H2O2, OH dan ROS lainnya.
ROS terdiri O2, H2O2, 1
O2, HO2, OH, ROOH, ROO, dan RO yang sangat reaktif dan
beracun dan penyebab kerusakan protein, lipid, karbohidrat, DNA yang akhirnya
menghasilkan kematian sel (Sarvajeet dan Narendra, 2010).
Reactive Oxygen Species (ROS) secara alami dihasilkan didalam
metabolisme tanaman. Selama stress biotik dan abiotik, ROS tersebut terakumulasi di
dalam jaringan jauh lebih cepat dibandingkan dengan reaksi yang dapat
katalase secara enzimatik maupun melalui mekanisme non enzimatik lainnya mampu
menghilangkan ROS dari jaringan tanpa menimbulkan kerusakan. Oleh karena
peroksidase dan katalase memiliki peranan utama didalam proses penghilangan
molekul H2O2 didalam jaringan biologis (Gebelin et al., 2013).
Reactive Oxygen Species (ROS) merupakan oksidan yang sangat reaktif dan
mempunyai aktivitas yang berbeda. Dampak negatif senyawa tersebut timbul karena
aktivitasnya, sehingga dapat merusak komponen sel yang sangat penting untuk
mempertahankan integritas sel. Setiap ROS yang terbentuk dapat memulai suatu
reaksi berantai yang terus berlanjut sampai ROS itu dihilangkan oleh ROS yang lain
atau sistem antioksidannya (Maslachah et al., 2008).
Fungsi enzim yang berbeda-beda dalam menghadapi ROS mengakibatkan
tingkat ekspresi gen responsif terhadap ROS beragam pada berbagai perlakuan.
Seperti telah disebutkan sebelumnya bahwa tingkat cekaman oksidatif dapat
ditentukan dari jumlah ROS seperti superoksida, peroksida, dan radikal hidroksil.
Oleh karena itu, keseimbangan aktifitas enzim SOD, APX, dan katalase sangat
penting untuk menekan level toksisitas ROS di dalam sel. Saat aktifitas katalase
rendah di tanaman, aktifitas enzim lain, yaitu APX akan meningkat
(Arlyny, 2008).
Asam Askorbat
Vitamin C dalam tubuh aktif dalam 2 bentuk yaitu asam askorbat dan
dehidroaskorbic acid (DHA). Vitamin C dalam bentuk asam askorbat berperan
radikal bebas, sedangkan dalam bentuk DHA akan menghambat secara langsung
aktifasi nuclear factorkappabeta (NF-kB) faktor transkripsi inflamasi. Beberapa
penelitian melaporkan bahwa vitamin C lebih efektif dibandingkan dengan α-
tokoferol dalam mengurangi proses patofisiologi akibat stres oksidatif seperti
aterosklerosis, karena vitamin C mempunyai kemampuan menangkap oksigen dan
nitrogen reaktif secara efektif, dan vitamin ini mempunyai kemampuan untuk
regenerasi α-tokoferol sehingga avaibilitas vitamin α-tokoferol ini dalam tubuh tetap
terjaga.Setelah bereaksi dengan radikal bebas,vitamin C pun akan menjadi produk
radikal, namun karena degradasinya sangat singkat (10-5 detik) sehingga ia tidak
reaktif, salah satu alasan vitamin C disukai sebagai antioksidan (Julahir, 2010).
Vitamin C diproduksi oleh tumbuhan dalam jumlah yang besar. Fungsi
vitamin C bagi tumbuhan dalah sebagai agen antioksidan yang dapat menetralkan
singlet oksigen yang sangat reaktif, berperan dalam pertumbuhan sel, berfungsi
seperti hormon, dan ikut berperan dalam proses fotosintesis. Vitamin C hanya dapat
dibentuk oleh tumbuhan dan terdapat pada sayuran serta buah-buahan dalam jumlah
yang besar.Hal ini disebabkan karena tumbuhan memiliki enzim mikrosomal
L-gulonolakton oksidase, sebagai komponen dalam pembentukan asam askorbat
(Kurniawan et al., 2010).
Antioksidan merupakan senyawa yang mampu menghambat laju oksidasi.
Antioksidan ini memiliki banyak komponen dan merupakan zat alami yang
dihasilkan sendiri oleh tubuh atau didapat dari makanan yang kita makan.
Antioksidan bekerja dengan cara menghentikan pembentukan radikal bebas,