SINTESIS DAN PENCIRIAN HIDROKSIAPATIT
DARI LIMBAH CANGKANG KERANG HIJAU
DENGAN METODE KERING
CHAECAR HIMAWAN SISWANTO
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER
INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan dengan skripsi berjudul Sintesis dan Pencirian Hidroksiapatit dari Limbah Cangkang Kerang Hijau dengan Metode Kering adalah karya saya dengan arahan komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, April 2013
Chaecar Himawan Siswanto
ABSTRAK
CHAECAR HIMAWAN SISWANTO. Sintesis dan Pencirian Hidroksiapatit dari Limbah Cangkang Kerang Hijau dengan Metode Kering. Dibimbing oleh CHARLENA dan AKHIRUDDIN MADDU.
Hidroksiapatit (HAp) merupakan biomaterial berbasis kalsium fosfat yang digunakan dalam dunia medis sebagai implan tulang dan penambal gigi. HAp telah disintesis dari sampel cangkang kerang hijau dengan metode kering. Kalsinasi cangkang kerang hijau pada suhu 1100 oC selama 18 jam menghasilkan CaO dengan kristalinitas 97.83%. Kontak CaO dengan udara selama 1 malam menghasilkan Ca(OH)2 dengan kristalinitas 85.45%. Pemanasan bahan awal CaO dan Ca(OH)2 tersebut pada suhu 900 dan 1100 oC selama 2 jam menghasilkan HAp sebagaimana dicirikan dengan menggunakan difraktometer sinar-X (XRD), spektrofotometer inframerah transformasi Fourier (FTIR), dan mikroskop elektron pemayaran (SEM). Hasil HAp terbaik diperoleh dari bahan awal CaO. Difraktogram XRD menunjukkan terbentuknya fase HAp dengan disertai beberapa fase kalsium fosfat lainnya pada sudut 2θ yang sesuai dengan data Joint Crystal Powder Diffraction Standard. Spektrum FTIR menunjukkan keberadaan gugus PO43– dan OH– dari HAp dan foto SEM menunjukkan ukuran butiran kristal HAp yang seragam. Dengan perlakuan tertentu ukuran pori HAp tersebut dapat disesuaikan untuk diaplikasikan sebagai implan tulang atau penambal gigi berlubang.
Kata kunci: cangkangkerang hijau, hidroksiapatit, metode kering, sintesis
ABSTRACT
CHAECAR HIMAWAN SISWANTO. Synthesis and Characterization of Hydroxyapatite from Green Mussel Waste Shell by Dry Method. Supervised by CHARLENA and AKHIRUDDIN MADDU.
Hydroxyapatite (HAp) is a calcium phosphate biomaterial utilized in medicine as bone implant and dental fillings. HAp has been synthesized from green mussel shells with dry method. Calcination of green mussel shells at 1100 o
C for 18 hours produced CaO with 97.83% crystallinity. Contact of CaO with the air for a night produced Ca(OH)2 with 85.45% crystallinity. Heating of CaO and Ca(OH)2 as the starting materials at 900 and 1100 °C for 2 hours produced HAp as characterized by using X-ray diffractometer (XRD), Fourier transform infrared (FTIR) spectrophotometer, and scanning electron microscope (SEM). The best HAp result was obtained from CaO material. The XRD diffractogram showed the formation of HAp phase accompanied by other calcium phosphate phase at 2θ angles matched with Joint Crystal Powder Diffraction Standard data. The FTIR spectra showed the presence of PO43– and OH– groups of the HAp and the SEM picture showed homogenous HAp crystal granule size. With additional treatments, the HAp pore size can be adjusted to be applied as bone implant or dental fillings.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada Departemen Kimia
SINTESIS DAN PENCIRIAN HIDROKSIAPATIT
DARI LIMBAH CANGKANG KERANG HIJAU
DENGAN METODE KERING
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2013
Judul Skripsi : Sintesis dan Pencirian Hidroksiapatit dari Limbah Cangkang Kerang Hijau dengan Metode Kering
Nama : Chaecar Himawan Siswanto NIM : G44104028
Disetujui oleh
Dr Charlena, MSi Pembimbing I
Dr Akhiruddin Maddu, SSi, MSi Pembimbing II
Diketahui oleh
Prof Dr Ir Tun Tedja Irawadi, MS Ketua Departemen Kimia
PRAKATA
Puji dan syukur penyusun panjatkan kepada Allah SWT karena dengan berkat limpahan rahmat dan hidayah-Nya penulis dapat menyelesaikan karya ilmiah dengan judul Sintesis dan Pencirian Hidroksiapatit dari Limbah Cangkang Kerang Hijau dengan Metode Kering. Karya ilmiah ini disusun berdasarkan penelitian yang dilakukan sejak bulan Maret hingga Agustus 2012 di Laboratorium Kimia Anorganik, Departemen Kimia FMIPA, Institut Pertanian Bogor.
Penyusun menyadari bahwa dalam pembuatan skripsi ini tidak lepas dari bantuan beberapa pihak. Oleh karena itu, penyusun mengucapkan terima kasih kepada Ibu Dr Charlena, MSi dan Bapak Dr Akhiruddin Maddu, SSi, MSi selaku pembimbing. Selain itu, penulis mengucapkan terima kasih kepada Tatang Hidayat selaku rekan penelitian dan seluruh staf Laboratorium Kimia Anorganik yang telah memberikan bantuan selama penelitian dilaksanakan. Taklupa apresiasi penulis ucapkan kepada Ibu dan Ayah tercinta, keluarga, sahabat, teman-teman pada Program Alih Jenis Kimia angkatan 4, serta semua pihak yang senantiasa mendukung terlaksananya penelitian ini. Semoga tulisan ini bermanfaat. Amin.
Bogor, April 2013
vi
DAFTAR ISI
DAFTAR TABEL vii
DAFTAR GAMBAR vii
DAFTAR LAMPIRAN vii
PENDAHULUAN 1
BAHAN DAN METODE 2
Alat dan Bahan 2
Metode 2
HASIL DAN PEMBAHASAN 3
Hidroksiapatit dan Hasil Pencirian dengan XRD 5 Hasil Pencirian dengan Spektrofotometer FTIR 9
Hasil Pencitraan dengan SEM 10
SIMPULAN DAN SARAN 10
Simpulan 10 Saran 11
DAFTAR PUSTAKA 11
vii
DAFTAR TABEL
1 Kristalinitas, parameter kisi, dan ukuran kristal (D) sampel hasil
sintesis hidroksiapatit 8
2 Perbandingan HAp hasil sintesis dengan HAp komersial 8
DAFTAR GAMBAR
1 Pola difraksi XRD sampel cangkang kerang hijau setelah proses kalsinasi pada 1100 oC selama 12 jam (a) dan 18 jam (b) 4 2 Pola XRD serbuk cangkang kerang hijau yang telah dikalsinasi (1100
°C, 18 jam) dan dibiarkan kontak dengan udara selama 1 malam pada suhu ruang (A). Pola XRD sampel dicerminkan dengan pola XRD
Ca(OH)2 standar JCPDS (B) 5
3 Pola difraksi hasil sintesis HAp dengan sintering CaO dan Ca(OH)2 pada 900 oC (A1 dan A2) dan 1100 oC (A3 dan A4) 7 4 Spektrum FTIR HAp hasil sintesis dari bahan awal CaO dengan
sintering pada 900 oC (A1) dan 1100 oC (A3) 9
5 Morfologi HAp hasil sintesis dari bahan awal CaO dengan sintering
pada 900 oC (A) dan 1100 oC (B) 10
DAFTAR LAMPIRAN
1 Bagan alir penelitian 12
2 Data JCPDS 13
3 Perhitungan konsentrasi kalsium cangkang kerang 18
4 Difraktogram HAp hasil sintesis 19
5 Perhitungan ukuran kristal sampel 21
6 Spektrum FTIR 22
1
PENDAHULUAN
Kerang hijau merupakan salah satu biota laut yang hidup di perairan dangkal. Umumnya kerang hijau dikonsumsi sebagai bahan pangan, dan menyisakan cangkangnya sebagai limbah. Limbah cangkang kerang hijau dapat dimanfaatkan sebagai biomaterial, bahan alam yang bersifat lembam dan dapat diimplantasikan ke dalam sistem tubuh sebagai pengganti jaringan alami yang mengalami kerusakan. Biomaterial harus bersifat biokompatibel dengan tubuh manusia. Aplikasinya terutama pada dunia kedokteran ortopedi. Salah satu biomaterial yang biokompatibel dengan tubuh manusia adalah hidroksiapatit (HAp). HAp mengandung senyawa kalsium fosfat dengan rumus molekul Ca10(PO4)6(OH)2, dan dapat berfungsi sebagai implan tulang dan gigi karena memiliki sifat bioaktif, biokompatibel, dan osteokonduktif yang sama dengan mineral tulang alami (Balumurugan et al. 2005; Kumar dan Kalainathan 2008). Senyawa HAp yang diimplankan akan memberikan sifat keras dalam jaringan tulang (Dahlan et al. 2009).
Hidroksiapatit dapat disintesis dengan berbagai cara, meliputi metode basah dan metode kering. Metode basah ada 3 jenis, yaitu metode presipitasi, hidrotermal, dan hidrolisis (Pankew et al. 2010). Metode basah lazim digunakan untuk sintesis HAp karena ekonomis dan sederhana. Selain itu, kristal HAp yang terbentuk mudah diatur komposisi dan sifat fisisnya. Keuntungan lain, hasil samping sintesisnya adalah air sehingga kemungkinan kontaminasi selama pengolahan sangat rendah (Kohoe 2008). Akan tetapi, sintesis kristal HAp dengan metode basah menghasilkan rendemen yang kurang tinggi karena terbentuk produk samping.
Sintesis HAp dengan metode kering merupakan reaksi fase padat, yakni pengubahan padatan menjadi padatan tanpa menggunakan pelarut (Muntamah 2011). Keunggulan metode kering adalah HAp terbentuk lebih banyak (Pramanik
et al. 2005) dengan butiran halus dan kristalinitas yang tinggi (Muntamah 2011). Prinsip yang digunakan dalam metode kering adalah sifat dasar atom yang bervibrasi semakin cepat pada suhu tinggi (Dahlan et al. 2009). Pramanik et al.
(2005) telah berhasil menyintesis HAp menggunakan metode kering dengan cara mereaksikan bahan awal CaO dengan pereaksi P2O5 pada suhu 1250 oC selama 1.5 jam. Selain itu, Dahlan et al. (2009) menjelaskan bahwa menggunakan suhu yang semakin tinggi pada saat sintesis akan menghasilkan HAp dengan kristalinitas yang tinggi.
BAHAN DAN METODE
Alat dan Bahan
Alat-alat yang digunakan antara lain alat-alat kaca, neraca analitik, tanur, oven, difraktometer sinar-X (XRD) Shimadzu 610, spektrofotometer inframerah transformasi Fourier (FTIR) Shimadzu Prestige-21, mikroskop elektron pemayaran (SEM) Philips 515, dan spektrofotometer serapan atom (AAS) Shimadzu AA-7000. Bahan-bahan yang digunakan dalam penelitian ini adalah sampel cangkang kerang hijau yang diperoleh dari perairan di utara Jakarta, P2O5, HNO3, standar CaCO3, dan akuabides.
Metode
Tahapan penelitian ini meliputi preparasi sampel cangkang kerang hijau hingga diperoleh sumber kalsium oksida (CaO) dan kalsium hidroksida (Ca(OH)2), penentuan kadar kalsium dengan menggunakan AAS, serta sintesis HAp dengan metode kering. Pencirian senyawa HAp hasil sintesis meliputi analisis gugus fungsi menggunakan FTIR, pengamatan ukuran partikel dengan SEM, dan penentuan pola difraksi menggunakan XRD (Lampiran 1).
Preparasi Cangkang Kerang Hijau
Cangkang kerang hijau dibersihkan (dicuci) dari kotoran dan membran cangkang, kemudian dikeringkan. Cangkang yang telah kering dikalsinasi pada suhu 1100 oC selama 12 dan 18 jam hingga diperoleh serbuk berwarna putih. Serbuk ini dihidrasi dengan cara dibiarkan kontak dengan udara (yang mengandung uap air) selama 1 malam di suhu kamar. Untuk memastikan terbentuknya Ca(OH)2, abu yang telah dibiarkan kontak dengan udara dianalisis pola difraksi sinar-X-nya.
Pengukuran Kadar Kalsium Menggunakan AAS
Sebanyak 0.1 g sampel serbuk cangkang kerang hijau dilarutkan dalam 1 mL HNO3 pekat, selanjutnya diencerkan menjadi 100 mL dengan akuabides. Sebanyak 1 mL larutan ini diambil dan diencerkan kembali menjadi 100 mL. Deret standar CaCO3 disiapkan dengan cara yang serupa dengan konsentrasi Ca2+ 0, 2, 4, 6, 8, dan 10 ppm. Sampel dan standar kemudian dianalisis menggunakan AAS.
Sintesis Hidroksiapatit dengan Metode Kering
Serbuk cangkang kerang hijau dicampurkan dengan P2O5 kemudian dilakukan proses milling selama 3 jam pada kecepatan 600 rpm dengan instrumen
3
Pencirian Senyawa Hidroksiapatit
Senyawa HAp hasil sintering terbagi menjadi 2 kelompok, kelompok kristal kalsium apatit hasil dari prekursor CaO, dan dari prekursor Ca(OH)2. Untuk membuktikan telah terbentuknya senyawa HAp, kedua kelompok tersebut dicirikan dengan menggunakan XRD, FTIR, dan SEM.
Pencirian dengan XRD
Sampel HAp disiapkan sebanyak 2 g, dimasukkan ke dalam holder yang berukuran (2x2) cm2 pada difraktometer. Analisis dilakukan dengan sumber target Cu yang memiliki panjang gelombang 1.5406 Å. Sudut awal ialah 10o dan sudut akhir 70o dengan kecepatan baca 2o per menit.
Pencirian dengan FTIR
Dua mg sampel dicampur dengan 100 mg KBr dan dibuat pelet. Pelet dianalisis pada kisaran bilangan gelombang 4000 sampai 400 cm-1.
Pencirian dengan SEM
Sampel HAp diletakkan pada pelat aluminium yang memiliki 2 sisi. Selanjutnya pengamatan dilakukan dengan tegangan 10 kV pada perbesaran 250 dan 1000 kali.
HASIL DAN PEMBAHASAN
Penelitian dimulai dengan mempersiapkan cangkang kerang hijau sebagai sumber kalsium untuk menyintesis HAp. Mula-mula kotoran yang masih melekat pada cangkang dibersihkan, kemudian cangkang dikeringudarakan. Setelah itu, cangkang dihancurkan menjadi serpihan-serpihan kecil yang selanjutnya dikalsinasi. Proses kalsinasi bertujuan menghilangkan komponen-komponen organik yang terkandung di dalam sampel. Waktu pemanasan yang digunakan adalah 12 dan 18 jam, dengan suhu 1100 oC. Pemilihan tersebut didasarkan atas hasil penelitian Muntamah (2011) yang melakukan pemanasan cangkang kerang darah selama 12 dan 24 jam pada suhu 1000 oC.
Kalsium karbonat (CaCO3) adalah salah satu penyusun utama cangkang kerang hijau. Pemanasan yang dilakukan akan mengubah CaCO3 menjadi CaO dan melepaskan karbon dioksida (CO2) ke udara, sesuai reaksi berikut:
CaCO3 → CaO + CO2
Hasil kalsinasi berupa padatan putih, kalsium oksida (CaO) yang selanjutnya dianalisis menggunakan instrumen XRD dan AAS.
4
Gambar 1 Pola difraksi XRD sampel cangkang kerang hijau setelah proses kalsinasi 1100 oC selama 12 jam (a) dan 18 jam (b)
Sampel cangkang kerang hijau yang dikalsinasi pada suhu 1100 oC selama 12 jam (Gambar 1a) menghasilkan pola difraksi dengan intensitas tinggi pada sudut 2θ 32.27o, 37.42o, 53.93o, 64.22o, dan 67.42o, sedangkan pada sampel yang dikalsinasi selama 18 jam (Gambar 1b), intensitas tinggi diperoleh pada sudut 2θ 32.35o, 37.51o, 53.99o, 64.29o, dan 67.53o. Nilai-nilai sudut 2θ ini spesifik untuk senyawa CaO sesuai dengan data JCPDS No. 37-1497. Jadi sampel yang dikalsinasi selama 12 maupun 18 jam keduanya merupakan CaO, hanya saja dengan waktu kalsinasi yang lebih lama, CaO dihasilkan dengan kristalinitas yang lebih tinggi. Kalsinasi selama 12 jam menghasilkan CaO dengan kristalinitas 91.85%, sedangkan kalsinasi selama 18 jam menghasilkan CaO dengan kristalinitas 97.83%. Menurut Firman (2006), kristalinitas juga dipengaruhi oleh suhu pemanasan yang digunakan. Cangkang kerang memiliki struktur yang lebih kuat daripada cangkang telur, sehingga hasil yang lebih baik diperoleh dari proses kalsinasi yang lebih lama (Muntamah 2011).
Karbonat merupakan zat pengganggu dalam proses kristalisasi HAp. Struktur karbonat dapat menempati 2 posisi dalam HAp. Posisi pertama, karbonat menggantikan OH– membentuk HAp tipe A, Ca10(PO4)6CO3, dan posisi kedua, karbonat menggantikan PO43– membentuk HAp tipe B, Ca10(PO4)3(CO3)3(OH)2. Untuk menghindari hal tersebut, kalsinasi dilakukan pada suhu tinggi. Menurut Helly (2008), kalsinasi dengan suhu tinggi akan mengeliminasi ion karbonat.
Kadar kalsium (Ca2+) dalam sampel hasil kalsinasi pada suhu 1100 oC selama 18 jam diukur dengan menggunakan AAS. Diperoleh 45.62% kalsium per 100 g sampel (Lampiran 3). Berdasarkan hasil ini cangkang kerang hijau dapat dijadikan bahan awal (sumber kalsium) untuk menyintesis HAp.
Pada penelitian ini digunakan 2 bahan awal untuk menyintesis HAp, yaitu CaO (hasil kalsinasi terbaik), dan Ca(OH)2. Kalsium hidroksida (Ca(OH)2) dihasilkan dari reaksi CaO dengan air, berupa kristal putih:
5
Berdasarkan hasil pengukuran XRD (Gambar 2), diperoleh pola difraksi dengan intensitas tinggi pada sudut 2θ 18.38°, 29.08°, 34.05°, 47.57°, 51.23°, dan 63.05°. Nilai sudut 2θ pada pola difraksi ini spesifik untuk senyawa Ca(OH)2 sesuai dengan data JCPDS No. 41-1475 (Lampiran 2), dan membuktikan bahwa telah terbentuk Ca(OH)2. Sampel Ca(OH)2 juga memiliki kristalinitas yang cukup baik, yaitu 85.45%.
Gambar 2 Pola XRD serbuk cangkang kerang hijau yang telah dikalsinasi (1100 °C, 18 jam) dan dibiarkan kontak dengan udara selama 1 malam pada suhu ruang (A). Pola XRD sampel dicerminkan dengan pola XRD Ca(OH)2 standar JCPDS (B)
Hidroksiapatit dan Hasil Pencirian dengan XRD
Sintesis HAp menggunakan metode kering dari serbuk garam anorganik atau oksida membutuhkan pencampuran mekanik yang ekstensif dan suhu tinggi (Beganskiene et al. 2006). Suhu tinggi dapat meningkatkan aktivitas ion sehingga menambah daya interaksi pada proses kristalisasi senyawa HAp. Bahan awal CaO atau Ca(OH)2 kemudian direaksikan dengan P2O5 melalui proses milling. Hasil yang diperoleh masing-masing dibagi menjadi 2 perlakuan sintering berbeda, yaitu dengan suhu 900 dan 1100 oC selama 2 jam. Hasil yang diperoleh berupa kristal putih yang selanjutnya diidentifikasi dengan XRD, FTIR, dan SEM.
Sintesis HAp metode kering ini merujuk penelitian Muntamah (2011) dan Pramanik et al. (2005) dengan beberapa modifikasi. Muntamah (2011) menyintesis HAp dari CaO (yang berasal dari cangkang kerang darah) melalui reaksi dengan suatu pereaksi pada suhu 1250 oC, sedangkan penelitian ini melakukan sintering pada dua variasi suhu yaitu 900 dan 1100 oC. Muntamah (2011) melakukan proses milling dengan kecepatan 300 rpm selama 6 jam, yang dimodifikasi menjadi 600 rpm selama 3 jam pada penelitian ini. Pereaksi yang digunakan sebagai sumber fosforus adalah P2O5 seperti metode yang dilakukan oleh Pramanik et al. (2005).
Sintesis HAp dengan cara ini dilakukan dengan sangat hati-hati karena senyawa P2O5 korosif, dapat menghasilkan kalor serta reaktif terhadap air dan udara. Oleh sebab itu, campuran harus terlebih dahulu didiamkan selama 24 jam dalam wadah tertutup sebelum proses sintering, agar terstabilkan (Pramanik et al.
2005) dan terhindar dari ledakan ketika kontak dengan udara.
6
terbentuk dari Ca(OH)2 tidak murni HAp (Gambar 3; A2 dan A4). Di sisi lain, apatit yang terbentuk dari CaO merupakan senyawa HAp dengan kemurnian yang tinggi (Gambar 3; A1 dan A3). Puncak-puncak yang ditunjukkan oleh sampel A1 dan A3 memiliki sudut 2θ yang spesifik untuk senyawa HAp, sedangkan puncak-puncak sampel A2 dan A4 juga menunjukkan terbentuknya β-trikalsium fosfat (β -TCP) dan apatit tipe A (AKA) (Lampiran 2).
Bahan awal CaO yang dipanaskan pada suhu 900 oC dengan pereaksi P2O5 (Gambar 3, A1) menunjukkan pola difraksi dengan intensitas yang tinggi pada sudut 2θ 25.95o, 31.86o, 32.28o, 32.99o, 39.89o, dan 46.79o. Nilai sudut 2θ ini spesifik untuk senyawa HAp sesuai dengan data JCPDS No. 09-0432 (Lampiran 2). Setiap puncak dengan intensitas sangat kecil dianggap sebagai latar belakang atau derau (noise). Hasil yang serupa juga ditunjukkan ketika bahan awal CaO dipanaskan pada suhu 1100 oC dengan pereaksi P2O5. Intensitas yang tinggi diperoleh pada sudut 2θ 25.88o, 31.76o, 32.19o, 32.90o, 39.80o, dan 46.71o. (Gambar 3, A3), yang juga spesifik mengindikasikan terbentuknya senyawa HAp.
Hasil berbeda (Gambar 3, A3), diperoleh dari bahan awal Ca(OH)2 yang dipanaskan pada suhu 900 oC dengan pereaksi P2O5 (Gambar 3, A2). Terdapat puncak dengan sudut 2θ yang spesifik untuk senyawa β-TCP (Ca3(PO4)2), yaitu pada 27.95o dan 34.50o. Selain itu, terdapat pula puncak-puncak yang dapat diidentifikasi sebagai AKA (Ca10(PO4)6CO3), yaitu pada 25.99o dan 31.24o. Demikian pula difraktogram produk pemanasan Ca(OH)2 pada suhu 1100 oC dengan pereaksi P2O5 (Gambar 3, A4), menunjukan terbentuknya β-TCP (sudut 2θ 27.79o dan 34.35o) serta AKA (sudut 2θ 25.84o dan 31.09o).
Berdasarkan hasil tersebut, bahan awal CaO dapat membentuk HAp dengan lebih baik dibandingkan dengan Ca(OH)2. Kalsium merupakan unsur logam alkali tanah yang mudah melepaskan 2 elektron valensinya untuk mencapai konfigurasi elektron yang lebih stabil. Senyawa kalsium hidroksida merupakan bentuk stabil kalsium yang telah melepaskan kedua elektron valensinya untuk berikatan dengan atom lain. Oleh karena itu, kalsium hidroksida lebih sukar bereaksi dengan P2O5. Kalsium oksida akan lebih reaktif sehingga lebih mudah membentuk HAp.
Dalam difraktogram, fase HAp menunjukkan puncak yang lebih dominan dengan intensitas lebih tinggi. Akan tetapi, masih terdapat fase kalsium fosfat lainnya pada beberapa perlakuan sampel, yakni β-TCP dan AKA. Fase HAp lebih stabil pada suhu ruang dibandingkan dengan senyawa kalsium fosfat lainnya. Akan tetapi, dengan pemanasan pada suhu tinggi (sintering), HAp dapat berubah fase menjadi kalsium fosfat yang lain. Menurut Bernache-Assolant et al. (2002), HAp mungkin terdekomposisi menjadi β-TCP setelah proses sintering. Sementara Helly (2008) menyatakan bahwa apatit yang dihasilkan dari reaksi fase padat pada suhu tinggi adalah AKA, sedangkan apatit biologis maupun hasil sintesis pada suhu rendah merupakan apatit tipe B (AKB).
Perbandingan difraktogram HAp yang terbentuk dari bahan awal CaO dan Ca(OH)2 (Lampiran 4) menunjukkan bahwa perlakuan A3 (sintering pada 1100 o
7
Gambar 3 Pola difraksi hasil sintesis HAp dengan sintering CaO dan Ca(OH)2
pada 900 oC (A1 dan A2) dan pada 1100 oC (A3 dan A4)
8
Suhu tinggi pada proses sintering menyebabkan susunan atom dalam sampel semakin teratur sehingga semakin banyak kristal yang terbentuk (Tabel 1). HAp dengan bahan awal CaO memiliki kristalinitas lebih tinggi, yakni 93.93%, sementara dengan Ca(OH)2 sebesar 92.35%.
Tabel 1 Kristalinitas, parameter kisi, dan ukuran kristal (D) sampel hasil sintesis hidroksiapatit
Bahan awal
Suhu Kristalinitas Parameter kisi D(002) (oC) (%) a (Å) c (Å) (nm)
CaO 1100 93.93 9.421 6.876 66.03
Ca(OH)2 1100 92.35 9.346 6.868 66.03
CaO 900 88.28 9.432 6.899 32.25
Ca(OH)2 900 84.09 9.377 6.884 36.49
Ukuran kristal dapat dihitung dengan menggunakan persamaan Scherrer (Lampiran 5). Ukuran kristal untuk bidang (002) diberikan pada Tabel 1. Selain informasi mengenai kristalinitas dan ukuran kristal, difraktogram XRD juga memberikan nilai parameter kisi kristal pada sampel. Menurut Aoki (1991), parameter kisi kristal merupakan jarak antarsel satuan dalam segala arah. Parameter kisi kristal untuk fase HAp adalah a = 9.432 Å dan c = 6.875 Å. Hasil yang diperoleh dari bahan awal CaO mendekati nilai tersebut, yang mengindikasikan terbentuknya fase HAp (Tabel 1).
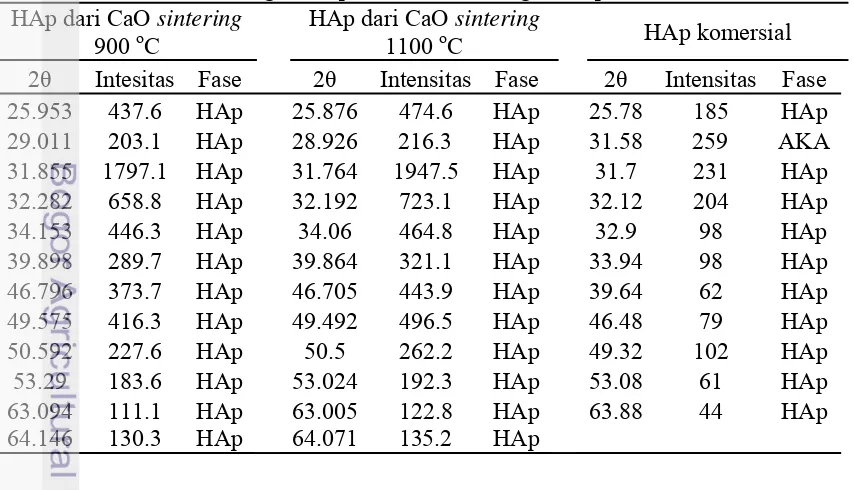
Hasil sintesis HAp yang terbaik kemudian dibandingkan dengan HAp komersial. Tabel 2 memperlihatkan bahwa HAp hasil sintesis memiliki mutu lebih baik karena tidak menunjukkan puncak AKA seperti yang terdapat pada HAp komersial. Puncak fase AKA pada HAP komersial berada pada sudut 2θ 31.580o. Hidroksiapatit hasil sintesis juga sudah tidak menunjukkan puncak fase CaO pada sudut 2θ 37.485o (Lampiran 2).
Tabel 2 Perbandingan HAp hasil sintesis dengan HAp komersial HAp dari CaO sintering
900 oC
HAp dari CaO sintering
9
Hasil Pencirian dengan Spektrofotometer FTIR
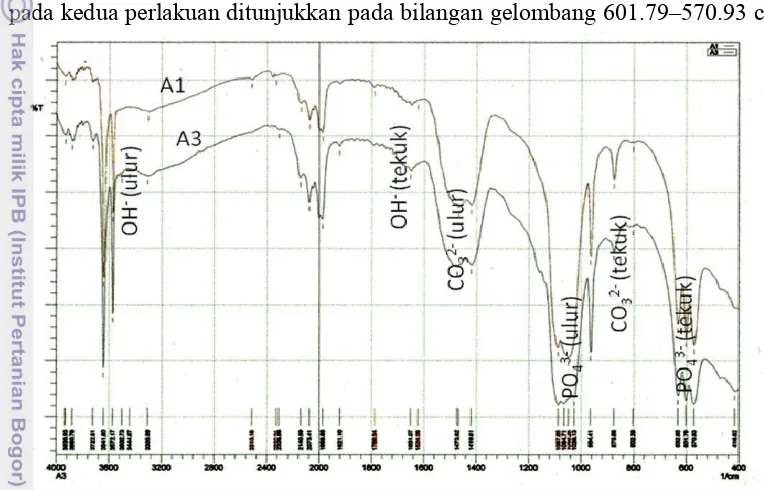
Spektrum FTIR HAp hasil sintesis dari CaO (Gambar 4), masih memiliki puncak pada bilangan gelombang 1450 dan 875 cm-1 yang menunjukkan keberadaan karbonat meskipun tidak terlalu kuat (Lampiran 6). Pita serapan pada 1024–1092 cm-1 menunjukkan vibrasi ulur asimetris dari gugus fosfat. Spektrum A3 (sintering pada 1100 oC) menunjukkan pita serapan pada 1064.71–1026.13 cm-1, sedangkan pada spektrum A1 (sintering pada 900 oC), pita serapan tersebut bergeser ke 1087.85–1049.26 cm-1. Vibrasi tekuk asimetris untuk gugus fosfat pada kedua perlakuan ditunjukkan pada bilangan gelombang 601.79–570.93 cm-1.
Gambar 4 Spektrum FTIR HAp hasil sintesis dari bahan awal CaO dengan
sintering pada 900 oC (A1) dan 1100 oC (A3)
Spektrum HAp juga memiliki pita serapan khas OH– di sekitar 3576 dan 632 cm-1. Hasil penelitian ini, spektrum A3 memperlihatkan pita serapan OH– tersebut pada 3572.17 dan 632.65 cm-1, sedangkan pada spektrum A1, pita serapan OH– berada pada 3572.17 dan 632.65 cm-1.
10
Hasil Pencitraan dengan SEM
Sampel HAp hasil kedua perlakuan kemudian juga dianalisis menggunakan SEM dengan perbesaran 1000 kali. Gambar 5 menunjukkan morfologi keduanya berupa butiran halus yang seragam. Perbedaannya terletak pada ukuran partikel. Gambar 5A (sintering CaO pada 900 oC) menghasilkan ukuran kristal HAp sebesar 32.25 nm, sedangkan sintering CaO pada 1100 oC menghasilkan ukuran partikel 2 kali lebih besar, yaitu 66.03 nm.
Gambar 5 Morfologi HAp hasil sintesis dari bahan awal CaO dengan sintering
pada 900 oC (A) dan 1100 oC (B)
SIMPULAN DAN SARAN
Simpulan
11
Saran
Sintesis HAp dengan metode kering dari limbah cangkang kerang hijau dapat dilanjutkan dengan modifikasi ukuran pori agar sesuai keperluan implan tulang atau penambal gigi berlubang. Selain itu, senyawa HAp yang terbentuk dapat dilapisi untuik meningkatkan daya ketahanan terhadap korosi.
DAFTAR PUSTAKA
Aoki H. 1991. Science and Medical Applications of Hydroxyapatite. Tokyo (JP): Tokyo Medical and Dental University.
Balmurugan A, Michel J, Farue J, Benhayoune H, Wortham L, Sockalingum G, Banchet, Bouthours S, Maquin DL, Balosseir G, 2006. Synthesis and structural analysis of solgel derived stoichiometric monophasic hydroxyapatite. Ceramics-Silikaty. 50(1):27-31.
Beganskienė A, Bogdanovičienė I, Kareiva A. 2006. Calcium acetylacetonate– a novel calcium precursor for sol-gel preparation of Ca10(PO4)6(OH)2.
Chemija. 17(2-3): 16-20.
Bernache-Assolant D, Ababou A, Champion E, Heughelaen M. 2002. Sintering of calcium phosphate hydroxyapatite Ca10(PO4)6(OH)2. Calcination and particle growth. [internet]. [diunduh 2012 Des 1]. Tersedia pada: http://www.elsevier.com.
Dahlan K, Prasetyani F, Sari YW, 2009. Sintesis hidroksiapatit dari cangkang telur menggunakan dry methode. J Biofisika. 5(2):71-78.
Firman E. 2006. Pengaruh suhu reaksi terhadap derajat kristalinitas dan komposisi dibuat dengan media air dan cairan tubuh buatan (synthetic body fluid) [skripsi]. Bogor (ID]: Institut Pertanian Bogor.
Helly Q. 2008. Sintesa Hidroksiapatit dengan memanfaatkan limbah cangkang telur: karakterisasi difraksi sinar-X dan scanning electron microscopy
(SEM) [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Kohoe S. 2008. Optimization of hydroxyapatite (HAp) for orthopedic application via the chemical precipitation technique [tesis]. Dublin (IE): Dublin City University.
Kumar AR, Kalainathan S. 2008. Growth and characterization of nanocrystalline hydroxyapatite at physiological condition. Res Technol. 43(6):640-644. Muntamah. 2011. Sintesis dan karakterisasi hidroksiapatit dari limbah cangkang
kerang darah (Anadara granosa) [tesis]. Bogor (ID): Institut Pertanian Bogor.
Pankew P, Hoonnivathana E, Limsuwan P, Naemchanthara K. 2010. Temperature effect phosphate synthesized from chicken eggshells and amonnium phosphate. Appl Sci. 10(24):3337-3342.
Pramanik S, Agarwal AK, Rai KN. 2005. Development of High Strength Hydroxyapatite for Hard Tissue Replacement. Trends Biomater Artif Organs. 19(1): 46-51.
12
Lampiran 1 Bagan alir penelitian
Sampel cangkang dibersihkan
Kalsinasi selama 12 dan 18 jam dengan pemanasan 1100 oC
CaO dibiarkan kontak dengan udara semalam
Bahan awal (CaO dan Ca(OH)2) di milling bersama P2O5 dengan kecepatan 600 rpm selama 3 jam
Proses sintering selama 2 jam dengan suhu 900 dan 1100 oC
Pencirian menggunakan XRD
dan AAS
Pencirian dengan FTIR
Pencirian dengan SEM Pencirian dengan XRD
13
Lampiran 2 Data JCPDS
Hidroksiapatit (Ca10(PO4)6(OH)2 ) JCPDS 09-0432
14
lanjutan Lampiran 2
Apatit karbonat tipe B (AKB) (Ca10(PO4)3(CO3)3(OH)2) JCPDS 19-0272
15
lanjutan Lampiran 2
Kalsium karbonat (CaCO3) JCPDS 41-1475
16
lanjutan Lampiran 2
Oktakalsium fosfat (Ca4H(PO4)3.25H2O JCPDS 44-0778
17
lanjutan Lampiran 2
18
Lampiran 3 Perhitungan konsentrasi kalsium cangkang kerang a. Absorbans standar kalsium
b. Konsentrasi kalsium pada cangkang kerang hijau Sampel Contoh perhitungan ulangan 1
Persamaan garis:
19
Lampiran 4 Difraktogram HAp hasil sintesis A1 (sintering CaO pada suhu 900 oC selama 2 jam)
20
lanjutan Lampiran 4
A3 (sintering CaO pada suhu 1100 oC selama 2 jam)
21
Lampiran 5 Perhitungan ukuran kristal sampel
D = k λ k = 0.9 dan λ = 0.15406 nm β cosθ
HAp dengan Suhu 2θ θ cos θ β β β cos θ D(002)
menggunakan (°C) (deg) (deg) (deg) (rad) (nm)
22
Lampiran 6 Spektrum FTIR
24
RIWAYAT HIDUP
Penulis dilahirkan pada tanggal 16 Desember 1989 di Mataram, sebagai putra pertama dari pasangan Bapak Agus Siswanto, SH dan Ibu Endang Tridarminingsih, SH. Pada tahun 2007, penulis lulus dari Sekolah Menengah Atas 1 Tambun Selatan dan diterima sebagai mahasiswa di Program Keahlian Analisis Kimia, Direktorat Program Diploma, Institut Pertanian Bogor melalui jalur PMDK. Penulis melanjutkan pendidikan S1 melalui program Alih Jenis Departemen Kimia, FMIPA, Inatitut Pertanian Bogor pada tahun 2010.