KAJIAN EFEKTIVITAS ASAM ASKORBAT DAN LIDAH
BUAYA UNTUK MENGHAMBAT PENCOKELATAN PADA
BUAH POTONG APEL MALANG
RIRIN NOERIANTY EFFENDI
DEPARTEMEN TEKNIK MESIN DAN BIOSISTEM FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul “Kajian Efektivitas Asam Askorbat dan Lidah Buaya untuk Menghambat Pencokelatan pada Buah Potong Apel Malang” adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan dan tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
ABSTRAK
RIRIN NOERIANTY EFFENDI. Kajian Efektivitas Asam Askorbat dan Lidah Buaya untuk Menghambat Pencokelatan pada Buah Potong Apel Malang. Dibimbing oleh Y ARIS PURWANTO.
Apel potong akan mengalami pencokelatan yang diakibatkan oleh senyawa fenolik. Penelitian ini bertujuan untuk mencegah pencokelatan pada buah potong dengan menggunakan larutan asam askorbat dan lidah buaya dengan berbagai konsentrasi, serta mengamati perubahan warna buah potong. Buah yang digunakan dalam penelitian ini adalah Apel Malang varietas Rome Beauty. Perlakuan penelitian dimulai dengan pemotongan dan pengupasan apel Malang menjadi 8 bagian. Proses pemotongan berlangsung cepat agar menghindari reaksi oksidasi. Proses selanjutnya yaitu pencelupan pada larutan asam askorbat dan larutan lidah buaya dengan konsentrasi yang berbeda. Terdapat 5 perlakuan yang digunakan yaitu pencelupan dalam asam askorbat 1 %, asam askorbat 3 %, lidah buaya 5 %, lidah buaya 10 %, dan perlakuan kontrol. Pencelupan dilakukan selama 2 menit. Hasil analisis menunjukkan bahwa pencelupan pada semua larutan yang digunakan dapat laju menghambat oksidasi enzim PPO yang dibuktikan dengan nilai Browning Index. Berdasarkan parameter-parameter yang ada, larutan yang efektif digunakan dalam mencegah pencoklatan adalah asam askorbat. Berdasarkan penelitian ini, waktu buah potong yang optimum untuk dikonsumsi dengan warna yang baik adalah selama 2 hari.
Kata kunci : asam askorbat, buah potong, lidah buaya, pencokelatan enzimatik
ABSTRACT
RIRIN NOERIANTY EFFENDI. Effectiveness Study of Ascorbic Acid and Aloe vera as Preventive Agent of Malang Apple Cut Fruits. Supervised by Y ARIS carefully prepared in this study. Fast cutting and peeling was conducted in order to minimize the oxidation occured to apple slices. Apple slices then dipped in 1% ascorbic acid solution, 3% ascorbic acid solution, 5% aloe vera solution, and 10% aloe vera solution for 2 minutes respectively. A group of apple slice did not receive any dipping treatment and used as control and used as control treatment. Several physical properties test were conducted to observe the effect of given treatments. Result showed that dipping treatments can prevent rapid PPO enzyme oxidation process. Based on the physical property parameters, ascorbic acid was the effective solution that can prevent rapid browning of apple slices and the optimum storage time was 2 days.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian
pada
Departemen Teknik Mesin dan Biosistem
KAJIAN EFEKTIVITAS ASAM ASKORBAT DAN LIDAH
BUAYA UNTUK MENGHAMBAT PENCOKELATAN PADA
BUAH POTONG APEL MALANG
RIRIN NOERIANTY EFFENDI
DEPARTEMEN TEKNIK MESIN DAN BIOSISTEM FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
Judul Skripsi : Kajian Efektivitas Asam Askorbat dan Lidah Buaya untuk Menghambat Pencokelatan pada Buah Potong Apel Malang Nama : Ririn Noerianty Effendi
NIM : F14090142
Disetujui oleh
Dr. Ir.Y. Aris Purwanto, M.Sc Pembimbing
Diketahui oleh
Dr.Ir. Desrial, M.Eng Ketua Departemen
PRAKATA
Puji syukur penulis panjatkan kehadirat Allah SWT yang telah memberikan rahmat dan karunianya sehingga penyusunan skripsi dengan judul “Kajian Efektivitas Asam Askorbat dan Lidah Buaya untuk Menghambat Pencokelatan pada Buah Potong Apel Malang” dapat diselesaikan. Penelitian ini dilaksanakan pada bulan Maret 2013 hingga Mei 2013.
Pada kesempatan ini penulis mengucapkan terimakasih kepada:
1. Dr. Ir. Y. Aris Purwanto, M.Sc selaku dosen pembimbing yang telah banyak memberikan arahan dan bimbingan kepada penulis sampai menyelesaikan skripsi ini.
2. Ayahanda Ismail Effendi, Ibunda Denden Nurtini, dan kakakku Yulliaty Erliani karena kasih sayang, dan dukungannya.
3. Bapak Suliaden, Mbak Sugih, Ibu Rubiyah, dan seluruh karyawan Teknisi Lab Teknik Pengolahan Pangan dan Hasil Pertanian yang membantu penulis saat melakukan penelitian.
4. Keluarga besar TMB 46 terimakasih atas bantuan dan kerjasamanya.
Semoga karya ilmiah ini bermanfaat dan dapat dijadikan acuan para pembaca untuk melakukan penelitian dalam bidang manajemen sumberdaya manusia.
.
DAFTAR ISI
DAFTAR TABEL vii
DAFTAR GAMBAR vii
DAFTAR LAMPIRAN viii
PENDAHULUAN 1
Latar Belakang 1
Tujuan 2
Manfaat 2
TINJAUAN PUSTAKA 3
Browning/Pencokelatan 3
Lidah Buaya 3
Asam Askorbat 4
Buah Potong 5
METODE 5
Waktu dan Tempat 5
Alat dan Bahan 5
Perlakuan Percobaan 5
Rancangan Percobaan 10
HASIL DAN PEMBAHASAN 11
Total Padatan Terlarut 11
Kekerasan 13
Susut Bobot 14
Vitamin C 15
Nilai L 17
Nilai Browning Index 19
SIMPULAN DAN SARAN 20
Simpulan 20
Saran 21
DAFTAR PUSTAKA 21
LAMPIRAN 23
DAFTAR TABEL
1 Daya larut asam askorbat 4
DAFTAR GAMBAR
1 Buah potong 1
2 Struktur senyawa asam askorbat 4
3 Diagram alir pembuatan larutan lidah buaya 6
4 Homoginezer 7
5 Diagram alir pembuatan larutan asam askorbat 7
6 Simulasi pemotongan buah apel 8
7 Proses penentuan umur simpan buah potong 8
8 Grafik warna L, a, b 10
9 Grafik perbandingan rata-rata total padatan terlarut pada apel malang potong dengan perlakuan kontrol dan penambahan asam askorbat
selama penyimpanan 6 hari di suhu 50C. 12
10 Grafik perbandingan rata-rata total padatan terlarut pada apel malang potong dengan perlakuan kontrol dan penambahan lidah buaya selama
penyimpanan 6 hari di suhu 50C. 12
11 Grafik perbandingan rata-rata kekerasan pada apel malang potong dengan perlakuan kontrol dan penambahan asam askorbat selama
penyimpanan 6 hari di suhu 50C. 13
12 Grafik perbandingan rata-rata kekerasan pada apel malang potong dengan perlakuan kontrol dan penambahan lidah buaya selama
penyimpanan 6 hari di suhu 50C 13
13 Grafik perbandingan rata-rata susut bobot pada apel malang potong dengan perlakuan kontrol dan penambahan asam askorbat selama
penyimpanan 6 hari di suhu 50C 14
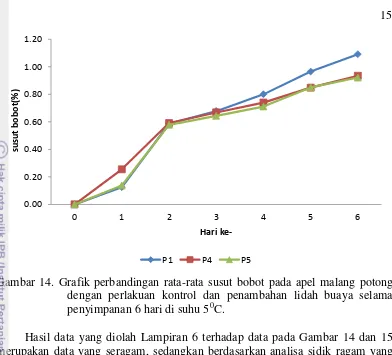
14 Grafik perbandingan rata-rata susut bobot pada apel malang potong dengan perlakuan kontrol dan penambahan lidah buaya selama
penyimpanan 6 hari di suhu 50C 15
15 Grafik perbandingan rata-rata vitamin C pada apel malang potong dengan perlakuan kontrol dan penambahan asam askorbat selama
penyimpanan 6 hari di suhu 50C 16
16 Grafik perbandingan rata-rata vitamin C pada apel malang potong dengan perlakuan kontrol dan penambahan lidah buaya selama
penyimpanan 6 hari di suhu 50C 16
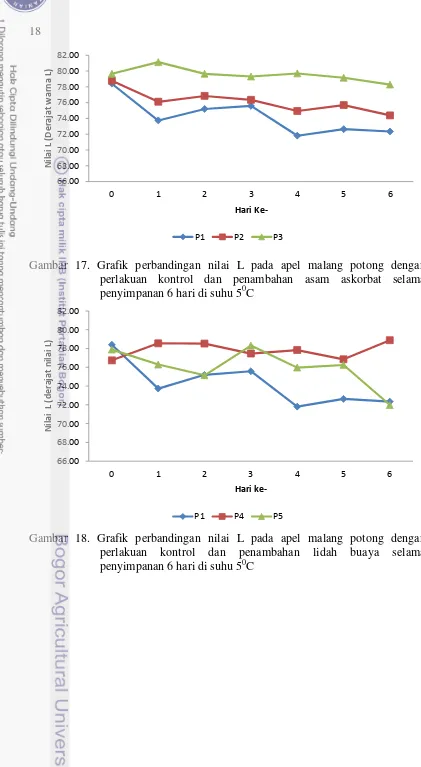
17 Grafik perbandingan rata-rata nilai L pada apel malang potong dengan perlakuan kontrol dan penambahan Asam Askorbat selama
penyimpanan 6 hari di suhu 50C 18
18 Grafik perbandingan rata-rata nilai L pada apel malang potong dengan perlakuan kontrol dan penambahan lidah buaya selama penyimpanan 6
hari di suhu 50C 18
19 Grafik perbandingan rata-rata nilai BI pada apel malang potong dengan perlakuan kontrol dan penambahan Asam askorbat selama
20 Grafik perbandingan rata-rata nilai BI pada apel malang potong dengan perlakuan kontrol dan penambahan lidah buaya selama penyimpanan 6
hari di suhu 50C 20
DAFTAR LAMPIRAN
1 Data total padatan terlarut pada suhu 50C 23
2 Hasil ANOVA untuk total padatan terlarut 24
3 Data kekerasan pada suhu 50C 25
4 Hasil ANOVA untuk kekerasan 25
5 Data susut bobot pada suhu 50C 26
6 Hasil ANOVA untuk susut bobot 26
7 Data vitamin C pada suhu 50C 27
8 Hasil ANOVA untuk vitamin C 28
9 Data warna pada parameter L pada suhu 50C 29
10 Data warna pada parameter a pada suhu 50C 29
11 Datai nilai BI 30
1
PENDAHULUAN
Latar Belakang
Buah dan sayuran merupakan bahan pangan yang diminati oleh masyarakat. Manfaat gizi yang tinggi membuat buah dan sayuran menjadi alternatif makanan yang dapat langsung dikonsumsi tanpa proses pemasakan oleh masyarakat. Pada daerah perkotaan, konsumsi dan pengeluaran rata-rata per kapita seminggu sayuran dan buah-buahan cenderung lebih tinggi apabila dibandingkan dengan masyarakat pedesaan. Contohnya, konsumsi buah apel di daerah perkotaan mencapai 0.025 kg, sedangkan untuk masyarakat pedesaan hanya mencapai 0.01 kg (BPS 2011).
Cara memakan buah bukan hanya kebutuhan melainkan menjadi bagian dari gaya hidup seseorang. Masyarakat saat ini lebih menyukai cara memakan yang siap saji. Buah potong segar merupakan salah satu cara untuk memenuhi permintaan tersebut. Internasional Fresh cut Produce Association (IFPA) pada tahun 2001 melaporkan buah potong segar adalah buah yang telah dibersihkan, dikupas dan dipotong hingga didapatkan bagian yang sepenuhnya digunakan oleh konsumen, kemudian dikemas dengan gizi yang tinggi, kenyamanan, dan rasa yang tetap segar. Penyajian buah potong seperti pada Gambar 1 sangat digemari sebagai olahan dessert atau sebagai cemilan. Konsumen dalam mengkonsumsi menginginkan buah tersedia dalam kondisi segar dan menarik pada saat disajikan dengan tingkat kematangan yang seragam dan siap konsumsi.
Gambar 1. Buah Potong
Buah potong merupakan proses penanganan pasca panen yang sederhana. Buah potong memiliki sifat mudah rusak (perishable), kemunduran kualitas disebabkan oleh aktivitas metabolisme yang masih berlangsung pada buah selama masa simpan. Aktivitas metabolisme yang melibatkan oksigen dari lingkungan akan mempercepat kematangan dan dapat menyebabkan kebusukan pada buah jika tidak dikendalikan. Pada penelitian kali ini, buah potong yang digunakan adalah apel malang, yaitu varietas Rome beauty. Apel malang merupakan komoditas apel yang dibudidayakan di Indonesia, tetapi kurang populer apabila dibandingkan dengan jenis apel impor lain.
2
cukup cepat atau disebut dengan browning/pencokelatan. Browning memiliki pengaruh yang besar bagi nilai jual suatu produk karena dapat mengurangi penampilan dan menurunkan nilai jual buah potong. Buah potong pada umumnya mengalami perlakuan seperti pengupasan, pemotongan, dan pengirisan hal tersebut dapat mengakibatkan integritas jaringan dan sel terganggu. Perlakuan tersebut mengakibatkan peningkatan produksi etilen, degradasi membran, kehilangan air, dan kerusakan akibat mikroorganisme. Dampak yang lain, sehingga mengakibatkan pencokelatan pada buah yaitu perubahan enzimatis dan penurunan umur simpan.
Diantara semua faktor penurunan kualitas pada buah potong pencokelatan enzimatis yang disebabkan oleh oksidasi senyawa fenolik adalah masalah besar. Pencokelatan dapat dicegah dengan metode kimia dan fisik, termasuk pengurangan temperatur dan oksigen, penggunaan modifikasi atmosfer kemasan, dan penerapan antibrowning yang bertindak untuk menghambat enzim (Ghidelli et al. 2013).
Pada penelitian ini, proses pencegahan pencokelatan pada buah potong digunakan dengan cara penerapan antibrowning yang bertindak untuk menghambat enzim. Dari segi kriteria permintaan konsumen yaitu kenyamanan, kesegaran, nutrisi, dan keamanan. Salah satu antibrowning yang cocok sebagai penghambat pencokelatan pada buah potong adalah lidah buaya dan asam askorbat. Asam askorbat dipilih karena bahan yang aman untuk dikonsumsi dan dapat meningkatkan kandungan vitamin yang terdapat dalam buah potong. Lidah buaya digunakan karena mengandung komponen potensial yang mampu menghambat kerusakan pascapanen. Komponen tersebut seperti glokomannan yang memiliki aktivitas antiviral, antidiabetes, antikanker, dan antimikrobial serta meningkatkan proliferasi sel-sel yang terluka. Lidah buaya mampu menjaga kelembaban dengan cara mengontrol komponen-komponen larut pada air (Reynolds 1999).
Tujuan Penelitian
Secara umum tujuan dari penelitian ini adalah menghambat pencokelatan dan memperpanjang masa simpan buah potong apel malang.
Secara khusus tujuan penelitian ini adalah:
1. Mengamati pengaruh pencelupan buah potong pada larutan lidah buaya dan larutan asam askorbat berbagai konsentrasi terhadap perubahan kualitas dan perubahan warna.
2. Mengamati perubahan warna pada buah apel potong pada suhu 50C.
Manfaat Penelitian
3
TINJAUAN PUSTAKA
Browning/Pencokelatan
Buah dan sayuran memiliki pigmen yang mempengaruhi warna dari penampakannya. Klorofil yang berada pada sayuran yang memberikan warna hijau, merah, dan ungu diakibatkan oleh antosianin; sedangkan kuning, orange, dan merah diakibatkan oleh karetonoid. Pigmen tersebut sangat penting bagi kualitas buah dan sayuran. Browning atau pencokelatan adalah suatu proses kecokelatan pada buah yang terjadi akibat proses enzimatik oleh polifenol oksidasi. Pada umumnya proses browning sering terjadi pada buah–buahan seperti pisang, pear, salak, pala, dan apel. Proses browning terbagi menjadi dua yaitu enzimatik dan non enzimatik. Reaksi pencokelatan nonenzimatik belum diketahui lebih lanjut, tetapi pada umumnya memiliki tiga macam reaksi yaitu karamelisasi, reaksi Maillard, dan pencokelatan akibat vitamin C (Winarno 1991).
Pencokelatan secara enzimatik dipicu oleh reaksi oksidasi yan dikatalisis oleh enzin fenol oksidase. Enzim tersebut dapat mengkatalisis reaksi oksidasi senyawa fenol yang menyebabkan perubahan warna menjadi cokelat. Reaksi kecokelatan enzimatis tidak diinginkan karena pembentukan warna cokelat pada buah atau sayur sering diartikan sebagai penurunan mutu (Kusnandar 2010).
Enzim yang menyebabakan reaksi pencokelatan enzimatis adalah oksidase yang disebut fenolase, fenoloksidase, tirosinase, polifenolase, atau katekolase. Dalam tanaman, enzim ini lebih sering dikenal dengan polifenol oksidase (PPO). Substrat untuk PPO dalam tanaman biasanya asam amino tirosin dan komponen polifenolik seperti katekin, asam kafeat, pirokatekol/katekol dan asam klorogenat (Garcia dan Barret 2002).
Cara untuk mengurangi pencokelatan dapat dilakukan dengan perendaman larutan sulfit, asam askorbat, asam sitrat, dan garam. Perendaman tersebut bertujuan untuk mengurangi reaksi antara enzim polifenolase, oksigen, dan senyawa polifenol yang bertanggung jawab dalam reaksi pencokelatan enzimatis (Syamsir et al. 2011).
Lidah Buaya (Aloevera)
Lidah buaya (Aloe vera) pada Gambar 2 merupakan tanaman yang banyak tumbuh pada iklim tropis ataupun subtropis dan sudah digunakan sejak dulu sebagai fungsi pengobatannya. Lidah buaya memiliki ciri-ciri morfologi pelepah daun yang runcing dan permukaan yang lebar, berdaging tebal, tidak bertulang, mengandung getah, permukaan pelepah daun dilapisi lilin, bersifat sukulen. Yaron (1991), melaporkan dalam Kismaryanti (2007) bahwa pelepah tanaman lidah buaya terdiri dari beberapa bagian utama, yakni mucilage gel dan exudate (lendir).
Asam Askorbat
4
pada tahun 1933 Haworth dan Hirst berhasil mensintesis sehingga disebut sebagai asam askorbat (Almatsier 2011).
Menurut Almatsier (2011), vitamin C adalah kristal yang mudah larut dalam air dan mudah rusak karena reaksi oksidasi terutama jika dipanaskan. Asam askorbat merupakan turunan dari heksosa diskasifikasi.
Asam askorbat dalam bentuk bubuk relatif stabil di udara. Asam askorbat tidak stabil saat larut dalam larutan alkali sehingga mudah mengalami oksidasi. Proses oksidasi dipercepat oleh cahaya, panas dan dikatalisis oleh tembaga dan besi. Derajat keasaman 5.4 merupakan kondisi stabil bagi asam askorbat. Penyimpanan asam askorbat sebaiknya dalam wadah nonlogam dan tertutup rapat, terlindung dari cahaya, serta berada ditempat kering (Rowe et al .2009). Daya larut asam askorbat dapat dilihat pada Tabel 1.
Tabel 1. Daya larut asam askorbat
Daya larut Pelarut pada 200C
Kloroform Tidak Larut
Etanol 1 dari 50
Etanol (95%) 1 dari 25
Eter Tidak larut
Minyak Tidak larut
Gliserin 1 daro 1000
Propylene glycol 1 dari 20
Air 1 dari 3.5
Sumber : (Rowe et al .2009)
Dosis besar menyebabkan diare atau gangguan pencernaan lainnya dan kerusakan gigi, tetapi tidak berbahaya apabila digunakan sebagai antibrowning dalam makanan, minuman, dan obat-obatan.
Asam askorbat merupakan senyawa turunan karbohidrat. Asam askorbat mengandung senyawa (C6H8O6) yang merupakan suatu nutrisi esensial untuk
proses metabolisme. Struktur kimia asam askorbat ditunjukkan oleh Gambar 2. (Almatsier 2011)
Gambar 2. Struktur senyawa asam askorbat
Sumber : (Rowe et al .2009)
Buah Potong/ Cut fruits
5 Komponen kualitas buah dan sayuran segar diklasifikasikan sebagai eksternal dan internal. Kualitas eksternal dapat dinilai dari penampakan buah dan sayuran potong. Kualitas internal dapat dinilai ketika produk dikonsumsi. Kualitas internal meliputi aroma, rasa, dan tekstur saat dikonsumsi. (Lamikanra 2002)
METODE
Waktu dan Tempat
Penelitian berupa penambahan dari larutan lidah buaya dan asam askorbat sebagai penghambat pencokelatan pada buah potong segar apel malang (Rome beauty). Dilaksanakan pada bulan Maret 2013 hingga Mei 2013. Tempat penelitian dan pengujian di Laboratorium Teknik Pengolahan Pangan dan Hasil Pertanian, Departemen Teknik Mesin dan Biosistem, Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Alat dan Bahan
Alat yang dipergunakan adalah:
Pisau, talenan, sendok pengaduk, sendok makan, sarung tangan, baskom, peniris, box plastic, wrapping film (dari jenis PVC) merk WITA, lemari pendingin 50 C, homoginezer, timbangan digital, kamera digital, blender, saringan, alat-alat gelas, mikroburet, chromameter Minolta CR-400, refraktometer, dan rheometer model CR-300 (ukuran diameter jarun 5mm).
Bahan yang dipergunakan adalah :
Bahan yang digunakan adalah apel malang (Rome Apple) dan daun lidah buaya yang diperoleh dari pasar swalayan Giant jalan Yasmin Bogor dan merupakan bahan yang food grade. Bahan-bahan kimia yang digunakan: asam askorbat diperoleh dari toko kimia Setia Guna, akuades, asam metafosfat(HPO3),
larutan garan 50 mg Na, diklorofenol indofenol
Perlakuan percobaan.
Pembuatan larutan dari pelepah daun lidah buaya.
6
perubahan warna, tetapi jika digunakan konsentrasi 20% akan mengakibatkan rasa buah potong menjadi pahit.
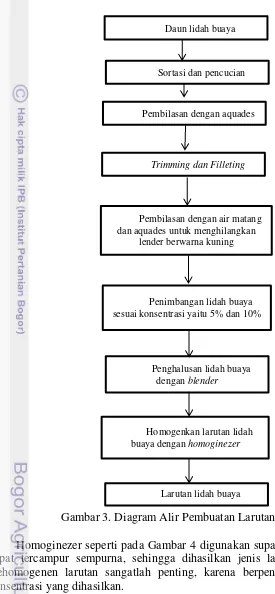
Gambar 3. Diagram Alir Pembuatan Larutan Lidah Buaya
Homoginezer seperti pada Gambar 4 digunakan supaya larutan lidah buaya dapat tercampur sempurna, sehingga dihasilkan jenis larutan yang homogen. Kehomogenen larutan sangatlah penting, karena berpengaruh dengan tingkat konsentrasi yang dihasilkan.
Daun lidah buaya
Sortasi dan pencucian
Pembilasan dengan aquades
Trimming dan Filleting
Pembilasan dengan air matang dan aquades untuk menghilangkan
lender berwarna kuning
Penimbangan lidah buaya sesuai konsentrasi yaitu 5% dan 10%
Larutan lidah buaya Penghalusan lidah buaya
dengan blender
7
Gambar 4. Homoginezer Pembuatan larutan asam askorbat.
Asam askorbat yang digunakan dalam pembuatan larutan adalah asam askorbat bubuk. Konsentrasi yang digunakan adalah 1% dan 3 proses pembutan larutan dapat dilihat pada Gambar 5. Konsentrasi yang diinginkan dapat dibuat dengan penimbangan asam askorbat bubuk, dan penambahan aquades sesuai dengan konsentrasi.
Gambar 5. Diagram Alir Pembuatan Larutan Asam askorbat
Pemotongan buah apel
Apel yang digunakan dalam penelitian adalah apel malang(Rome Beauty) berukuran sedang, dengan diameter rata-rata 22 cm. Sebelum pemotongan buah Apel dicuci dengan air matang dan disimpan terlebih dahulu pada lemari dingin 50C supaya apel dipotong dalam keadaan yang optimum. Pemotongan apel menggunakan pisau dan sarung tangan. Sarung tangan digunakan supaya mengurangi mikroorganisme yang menempel pada apel potong. Simulasi pemotongan dapat dilihat pada Gambar 6. Ukuran pemotongan dengan membagi apel kedalam 8 bagian sama besar (bentuk mendekati elips dengan ukuran 7cm x 2.5cm x2cm).
Larutan asam askorbat 1% dan 3%
Asam askorbat bubuk
Penambahan asam askorbat bubuk dengan aquades sesuai
8
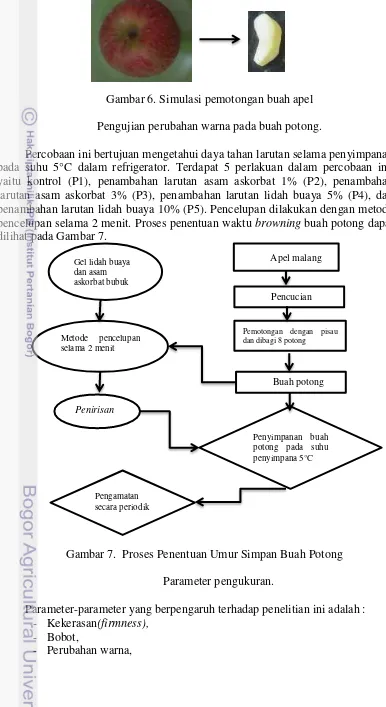
Gambar 6. Simulasi pemotongan buah apel Pengujian perubahan warna pada buah potong.
Percobaan ini bertujuan mengetahui daya tahan larutan selama penyimpanan pada suhu 5°C dalam refrigerator. Terdapat 5 perlakuan dalam percobaan ini, yaitu kontrol (P1), penambahan larutan asam askorbat 1% (P2), penambahan larutan asam askorbat 3% (P3), penambahan larutan lidah buaya 5% (P4), dan penambahan larutan lidah buaya 10% (P5). Pencelupan dilakukan dengan metode pencelupan selama 2 menit. Proses penentuan waktu browning buah potong dapat dilihat pada Gambar 7.
Gambar 7. Proses Penentuan Umur Simpan Buah Potong Parameter pengukuran.
Parameter-parameter yang berpengaruh terhadap penelitian ini adalah : - Kekerasan(firmness),
- Bobot,
- Perubahan warna,
Apel malang
Pemotongan dengan pisau dan dibagi 8 potong
Pencucian
Buah potong
Gel lidah buaya dan asam askorbat bubuk
Metode pencelupan selama 2 menit
Penirisan
Penyimpanan buah potong pada suhu penyimpana 5°C
9 - Kandungan vitamin C, dan
- Total padatanterlarut (TPT).
Analisis data. Susut Bobot
Pengukuran susut bobot dilakukan menggunakan timbangan digital. Pengukuran dilakukan sebelum buah potong disimpan (bo) dan setiap kali akhir pengamatan (bt) yaitu setiap hari. Selanjutnya susut bobot didapatkan dengan membandingkan pengurangan bobot awal pengamatan dan dinyatakan dalam persen. Rumus lengkap susut bobot adalah sebagai berikut :
Keterangan
bo = bobot awal pengamatan (g) bt = bobot akhir pengamatan (g) Kekerasan
Uji kekerasan diukur berdasarkan tingkat ketahanan buah terhadap jarum penusuk rheometer. Pengukuran kekerasan dilakukan dengan menggunakan rheometer model CR-300 yang diset dengan mode 20, beban maksimum 2 kg, kedalaman penekanan 10 mm, kecepatan penurunan beban 30 mm.menit-1 dan diameter jarum 5 mm. Pengujian dilakukan pada bagian tengah buah. Selama pengujian buah dipegang dengan tangan agar buah tidak bergeser. Pengujian kekerasan dilakukan setiap hari.
Total Padatan Terlarut (TPT)
Besar total padatan terlarut pada buah potong dapat diketahui dengan menggunakan refractrometer digital. Daging buah diambil sarinya (diperas hingga sarinya keluar), lalu hasilnya diletakan pada prisma refractrometer. Total padatan terlarut dalam sari daging buah potong yang diperas sebagian besar tersusun atas gula. Besarnya nilai padatan dinyatakan dengan derajat gula skala oBrix. Pengukuran TPT dilakukan setiap hari.
Uji Warna
Intensitas warna diukur dengan menggunakan Chromameter Minolta CR-400 . Pada Chromameter Minolta CR-400 digunakan sistem L, a, dan b. Nilai L menujukan nilai dari suatu kecerahan dari buah. Nilai –a menunjukkan warna yang mendekati hijau, sedangkan nilai +a menunjukkan warna mendekati merah. Nilai –b menunjukkan warna yang mendekati biru, sedangkan +b menunjukkan warna mendekati kuning. Nilai a dan b, dapat dikonversikan menjadi warna dengan menggunakan grafik seperti Gambar 8.
10
Berdasarkan Zhang (2008), nilai BI diperoleh menggunakan rumus sebagai berikut :
x adalah cromaticity coordinate(a) yang diperoleh dari pembacaan Chromameter.
Gambar 8. Grafik warna L, a, b Analisi vitamin C
Cara penetapan vitamin C yang paling baik adalah didasarkan atas reduksi 2.6-diklorofenol indofenol oleh asam askorbat dan didasarkan pada reaksi dehidro-asam askorbat dengan 2.4 dinitrifenil hidrasin. Indofenol dapat disebut dengan larutan dye yang berwarna biru didalam larutan basa. Titrasi perlahan dengan larutan dye sampai mencapai titik akhir, yaitu merah jambu yang bertahan 15 detik. Titer yang didapatkan merupakan titer pendahuluan yang digunakan untuk titer sebenarnya. Apabila sample yang diuji mengandung SO2, indofenol
yang terdapat dalam dye akan direduksi. (Apriyantono et al. 1989) Perhitungan:
Rancangan Percobaan
Faktor perbandingan konsentrasi asam askorbat dan lidah buaya terdiri atas lima taraf atau perlakuan, yakni P1 (kontrol), P2 (asam askorbat 1%), P3 (asam askorbat 3%), P4(lidah buaya 5%), dan P5 (lidah buaya 10%). Suhu penyimpanan yaitu dengan suhu 50C. Masing-masing faktor menggunakan rancangan acak lengkap sebagai rancangan percobaannya. Model linier yang digunakan untuk faktor perbandingan konsentrasi asam askorbat dan lidah buaya adalah sebagai berikut (Mattjik dan Sumertajaya 2002).
Yij = μ + τi + εij
I : 1,2,3,4,5,6 dan j = 1,2
Yij : Variabel penyimpanan akibat penyimpanan suhu ke-i dan ulangan ke-j
11
τi : Pengaruh perlakuan penyimpanan buah potong pada suhu 50 C
εij : Pengaruh acak pada perlakuan ke-i ulangan ke-j
Data dilakukan uji kenormalan, keaditifan, dan kehomogenan terlebih dahulu. Data yang memenuhi asumsi diolah menggunakan uji parametrik analisis keragaman (ANOVA). Uji lanjut yang dilakukan adalah uji duncan.
HASIL DAN PEMBAHASAN
Total Padatan Terlarut
Winarno dan Wirakartakusumah 1981 melaporkan dalam Hasanah (2009) buah-buahan dan sayuran menyimpan karbohidrat untuk persediaan energi. Persediaan ini digunakan untuk melaksanakan aktivitas sisa hidupnya, oleh karena itu proses pematangan kandungan gula dan karbohidrat selalu berubah.
Pada perlakuan ini terdapat 5 perlakuan yaitu P1 (perlakuan pontrol tanpa penambahan larutan), P2 (perlakuan penambahan larutan asam askorbat 1%), P3 (perlakuan penambahan larutan asam askorbat 3%), P4 (perlakuan penambahan larutan lidah buaya 5%), P5 (perlakuan penambahan larutan lidah buaya 10%).
Hasil data yang diolah Lampiran 2 merupakan data yang seragam, berdasarkan uji lanjut duncan menunjukkan bahwa perlakuan pencelupan apel potong pada larutan berpengaruh nyata terhadap P1. Nilai rataan total padatan terlarut pada P2 memiliki nilai lebih rendah jika dibandingkan dengan P1, tetapi tidak berpengaruh nyata jika dibandingkan dengan P5 dan P3. P2 menjadi berpengaruh nyata apabila dibandingkan dengan P4. Nilai rataan total padatan terlarut pada P1 lebih tinggi dan berpengaruh nyata jika dibandingakan dengan P2,P3,P4, dan P5.
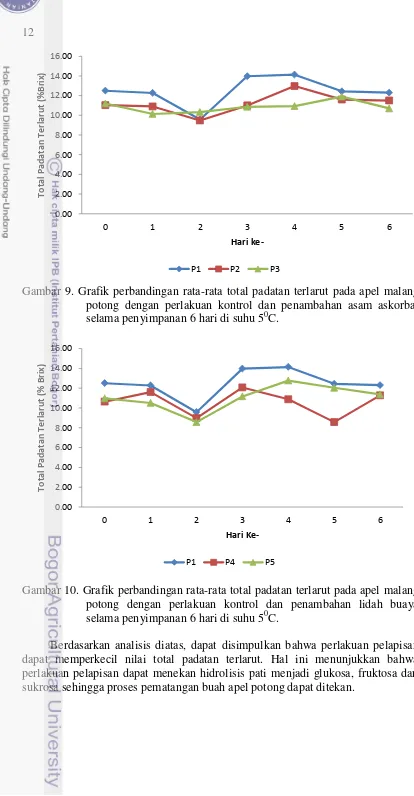
Pada Gambar 9 dan Gambar 10 total padatan terlarut cenderung meningkat dan setelah melewati titik puncak semakin menurun. Nilai total padatan terlarut pada PI lebih tinggi jika dibandingkan dengan perlakuan penambahan asam askorbat dan lidah buaya.
12
Gambar 9. Grafik perbandingan rata-rata total padatan terlarut pada apel malang potong dengan perlakuan kontrol dan penambahan asam askorbat selama penyimpanan 6 hari di suhu 50C.
Gambar 10. Grafik perbandingan rata-rata total padatan terlarut pada apel malang potong dengan perlakuan kontrol dan penambahan lidah buaya selama penyimpanan 6 hari di suhu 50C.
Berdasarkan analisis diatas, dapat disimpulkan bahwa perlakuan pelapisan dapat memperkecil nilai total padatan terlarut. Hal ini menunjukkan bahwa perlakuan pelapisan dapat menekan hidrolisis pati menjadi glukosa, fruktosa dan sukrosa sehingga proses pematangan buah apel potong dapat ditekan.
13
Kekerasan
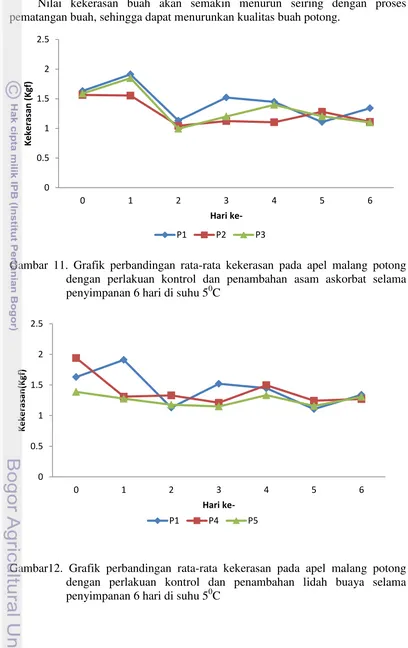
Nilai kekerasan buah akan semakin menurun seiring dengan proses pematangan buah, sehingga dapat menurunkan kualitas buah potong.
Gambar 11. Grafik perbandingan rata-rata kekerasan pada apel malang potong dengan perlakuan kontrol dan penambahan asam askorbat selama penyimpanan 6 hari di suhu 50C
14
Berdasarkan Gambar 11 dan Gambar 12 nilai kekerasan buah apel potong akan semakin menurun. Penurunan terjadi sekitar hari ke-1 setelah dilakukan perlakuan. Menurut Winarno dalam Hasanah (2009) nilai kekerasan dapat menurun dikarenakan protopektin berubah menjadi pektin yang larut dalam air, sehingga mengakibatkan penurunan daya kohesi dinding sel yang mengikat dinding sel yang lain.
Susut Bobot
Menurut Perera (2007) susut bobot terjadi karena penguapan air yang terkandung didalan buah. Potongan yang terjadi pada buah mengakibatkan jaringan dalam buah terluka dan terkena udara sehingga terjadi penguapan air.
Suhu internal buah yang tinggi menyebabkan selisih antara tekanan uap lingkungan dan buah menjadi besar. Semakin besar selisih yang terjadi maka kecepatan laju perpindahan uap air akan semakin tinggi. Sehingga berpengaruh terhadap nilai susut bobot yang besar.
Pada Gambar 13 menunjukkan perubahan nilai susut bobot pada kontrol dan penambahan asam askorbat tidak berbeda signifikan. Hal tersebut dapat terjadi karena penyimpanan buah apel potong seragam pada suhu 50C. Penyimpanan buah pada suhu rendah akan memperlambat perubahan susut bobot karena pada suhu rendah kecepatan uap air berkurang.
15
Gambar 14. Grafik perbandingan rata-rata susut bobot pada apel malang potong dengan perlakuan kontrol dan penambahan lidah buaya selama penyimpanan 6 hari di suhu 50C.
Hasil data yang diolah Lampiran 6 terhadap data pada Gambar 14 dan 15 merupakan data yang seragam, sedangkan berdasarkan analisa sidik ragam yang dilakukan pada P = 0.05 menunjukkan nilai P<0.005, yaitu nilai P= 0.658, sehingga perubahan susut bobot terhadap perlakuan tidak berpengaruh nyata. Hal ini menunjukkan bahwa penambahan larutan asam askorbat dan larutan lidah buaya tidak terlalu mempengaruhi perubahan susut bobot pada apel malang potong.
Vitamin C
Perbedaan vitamin C yang dimiliki oleh apel yang diberi perlakuan dan kontrol, menunjukkan bahwa pelapis sudah masuk ke dalam jaringan buah atau melekat permukaan potongan buah. Menurut Xuetong et al. (2005) nilai vitamin c yang lebih tinggi menunjukkan bahwa apel potong yang diberi perlakuan memiliki gizi yang lebih tinggi.
16
vitamin C menurun hingga menjelang akhir penyimpanan. Penurunan yang terjadi untuk semua perlakuan cenderung sama, dan memiliki nilai yang tidak berbeda jauh diakhir penyimpanan. Hal ini menunjukkan bahwa pengaruh pelapisan akan signifikan hingga hari ketiga.
Gambar 15. Grafik perbandingan rata-rata vitamin c pada apel malang potong dengan perlakuan kontrol dan penambahan asam askorbat selama penyimpanan 6 hari di suhu 50C
Lampiran 16. Grafik perbandingan rata-rata vitamin C pada apel malang potong dengan perlakuan kontrol dan penambahan lidah buaya selama penyimpanan 6 hari di suhu 50C
Pada Gambar 15 dan Gambar 16nilai perubahan vitamin C menurun seiring bertambahnya waktu. Pada Gambar 15 nilai P1 berada lebih rendah bila dibandingkan P2 dan P3, tetapi perubahan pada P3 menurun cukup drastis mulai hari ke-3. Hal ini terjadi karena antibrowning pada P3 mulai berkurang pada hari ke-3. Antibrowning menyebabkan reaksi oksidasi menurun sehingga vitamin C akan berkurang lebih lambat. Menurut Almatsier (2011) vitamin C akan berkurang setelah pengolahan dalam waktu yang lama.
17
Warna
Mendel melaporkan dalam Jeong (2008) bahwa perubahan warna enzimatik sangat berkorelasi dengan jumlah fenolik dan tirosi. Hasil perhitungan yang diperoleh sangat tergantung pada metode pengukuran dan keadaan permukaan dari objek diperiksa (Kuczinsky 1992). Nilai L adalah indikator yang berguna untuk mengukur kecerahan selama penyimpanan yang dihasilkan dari reaksi pencokelatan oksidatif atau dari peningkatan konsentrasi pigmen (Rocha dan Morais 2003)
Nilai BI dan L pada produk apel potong segar berhubungan dengan oksigen. Oksigen berperan penting dalam reaksi pencokelatan yaitu sebagai substrat pembantu (co-substrate),jika interaksi antara oksigen dan jaringan buah dapat ditekan, maka pencokelatan dapat diminimalisir (Latifah 2009).
Nilai L
Hasil data yang diolah Lampiran 13 merupakan data yang seragam, sedangkan berdasarkan uji lanjut Duncan perbedaan nilai L dibagi menjadi 4 bagian. Uji duncan menunjukkan bahwa perlakuan penambahan asam askorbat dan lidah buaya berpengaruh nyata terhadap P1dan berbagai perlakuan. Nilai rataan L merupakan nilai yang menunjukkan tingkat kecerahan. Pada P1 nilai rataan L paling rendah dan memiliki perbedaan yang sangat nyata jika dibandingkan dengan perlakuan yang lain. Nilai rataan L P5 berada diurutan ke-2 dan P4 pada urutan ke-3. Nilai rataan L pada P5 dan P4 tidak terlalu signifikan, karena berada pada satu kolom yang sama menurut Uji Duncan. Nilai rataan L yang paling tinggi ditunjukan oleh P3, dan memiliki perbedaan yang nyata jika dibandingan dengan perlakuan yang lain.
Pada Gambar 17 dan 18 nilai L cenderung menurun seiring bertambahnya waktu. Perubahan nilai L pada kontrol lebih rendah jika dibandingkan dengan perlakuan yang lain. Hal ini dapat terjadi karena permeabilitas perlakuan kontrol yang tinggi terhadap oksigen dan menyebabkan jaringan buah dengan mudah teroksidasi, sehingga memicu terjadinya pencokelatan lebih cepat apabila dibanding dengan perlakuan penambahan larutan.
18
Gambar 17. Grafik perbandingan nilai L pada apel malang potong dengan perlakuan kontrol dan penambahan asam askorbat selama penyimpanan 6 hari di suhu 50C
19
Nilai BI
Browning Index menunjukkan proporsi fenol teroksidasi selama penyimpanan apel. Aktivitas enzim PPO berkorelasi terhadap nilai browning index, semakin besar nilai browning index maka aktivitas PPO akan semakin tinggi. Berbeda dengan nilai BI, nilai aktivitas PPO akan menurun apabila nilai L(kecerahan) tinggi (Jeong 2008).
Hasil data yang diolah Lampiran 14 merupakan data yang seragam, sedangkan berdasarkan analisa sidik ragam yang dilakukan pada P = 0,05 dengan uji lanjut Duncan perbedaan nilai BI dibagi menjadi 4 bagian. Uji Duncan menunjukkan bahwa perlakuan penambahan asam askorbat dan lidah buaya berpengaruh nyata terhadap P1 dan berbagai perlakuan lainnya. Nilai rataan BI merupakan nilai yang menunjukkan perubahan warna dan perbandingan fenol yang teroksidasi. Pada P3 nilai rataan BI paling rendah dan memiliki perbedaan yang sangat nyata jika dibandingkan dengan perlakuan yang lain. Nilai rataan BI pada P5 dan P4 tidak terlalu signifikan, karena berada pada satu kolom yang sama menurut Uji Duncan. Nilai rataan BI pada P5 dan P4 terdapat pada satu kolom, hal ini menunjukkan bahwa kedua perlakuan tersebut tidak memiliki perbedaan yang signifikan. Nilai rataan BI yang paling tinggi ditunjukan oleh P1dan memiliki perbedaan yang nyata jika dibandingan dengan perlakuan yang lain
Berdasarkan Gambar 19 dan Gambar 20, menunjukkan nilai BI tertinggi dimiliki oleh P1. Hal ini dapat terjadi karena aktivitas enzim PPO pada perlakuan kontrol lebih tinggi sehingga menyebabkan terjadinya pencokelatan lebih cepat jika dibanding dengan perlakuan penambahan larutan.
20
Gambar 20. Grafik perbandingan rata-rata BI pada apel malang potong dengan perlakuan kontrol dan penambahan lidah buaya selama penyimpanan 6 hari di suhu 50C
Berdasarkan analisis diatas, dapat disimpulkan bahwa perlakuan pelapisan dapat menurunkan nilai BI. Hal ini menunjukkan bahwa perlakuan pelapisan dapat menurunkan aktivitas enzim PPO sebagai penyebab terjadinya pencokelatan pada buah potong. Berdasarkan nilai BI, larutan asam askorbat lebih rendah jika dibandingkan dengan larutan lidah buaya. Hal ini menunjukkan bahwa penggunaan larutan asam askorbat lebih efektif dalam mencegah pencokelatan. Berdasarkan nilai BI, larutan asam askorbat 3% memiliki nilai yang lebih rendah apabila dibanding larutan 1%. Hal ini menunjukkan bahwa larutan 3% lebih efektif menghambat pencokelatan apel potong.
SIMPULAN DAN SARAN
Simpulan
1. Berdasarkan hasil analisis menunjukkan bahwa oksidasi enzim PPO mempengaruhi total padatan terlarut, menurut uji lanjut duncan pengaruh antibrowning dan kontrol terlihat nyata. Nilai rataan kontrol mencapai 12.45 %Brix, sedangkan nilai total padatan terlarut yang paling rendah terdapat pada asam askorbat 1%. Hal ini menunjukkan bahwa perlakuan degradasi pati menjadi gula sederhana pada asam askorbat 1% lebih lama jika dibandingkan perilaku kontrol.
2. Berdasarkan hasil analisis kekerasan menunjukkan bahwa semakin lama penyimpanan mempengaruhi nilai kekerasan apel potong, tetapi menurut uji duncan analisis kekerasan tidak berpengaruh nyata terhadap setiap perlakuan. Berdasarkan hasil analisis susut bobot menunjukkan bahwa semakin lama
21 penyimpanan mempengaruhi nilai susut bobot apel potong, tetapi menurut uji duncan analisis kekerasan tidak berpengaruh nyata terhadap setiap perlakuan. 3. Nilai rataan vitamin C pada asam askorbat paling tinggi yaitu 27.43 mg vit
C/100g, jika dibandingkan dengan perilaku lainya dan akan menurun pada suatu waktu. Hal ini terjadi karena antioksida menyebabkan reaksi oksidasi menurun. Vitamin c akan berkurang setelah pengolahan dalam waktu yang lama.
4. Pada nilai L, asam askorbat 3% memiliki rataan nilai yang paling tinggi yaitu 79.55 derajat warna L, jika dibandingkan nilai kontrol yang memiliki nilai rataan 74,24 derajat nilai L . Hal ini menunjukkan bahwa perlakuan pelapisan dapat menurunkan permeabilitas buah potong terhadap oksigen. Perubahan nilai BI pada kontrol lebih tinggi yaitu 802.32 dejarat BI, jika dibandingkan dengan asam askorbat 3% yang memiliki nilai BI -2320.04 derajat BI. Hal ini dapat terjadi karena aktivitas enzim PPO pada perlakuan kontrol lebih tinggi sehingga menyebabkan terjadinya pencokelatan lebih cepat jika dibanding dengan perlakuan penambahan larutan.
5. Berdasarkan parameter-parameter yang ada, larutan yang efektif digunakan dalam mencegah pencoklatan adalah asam askorbat. Berdasarkan penelitian ini, waktu buah potong yang optimum untuk dikonsumsi dengan warna yang baik adalah selama 2 hari.
Saran
Saran penelitian selanjutnya dapat dibuat sebuah metode untuk meningkatkan nilai tambah bagi buah potong dengan menggunakan parameter analisis pada penelitian ini. Selain itu juga, penelitian selanjutnya diharapkan dapat menggunakan parameter analisis lain dalam menentukan tingkat pencokelatan buah potong, sehingga dapat diketahui indikator yang tepat bagi pengolahan buah potong.
DAFTAR PUSTAKA
Almatsier S. 2011. Prinsip Dasar Ilmu Gizi. Jakarta (ID): PT. Gramedia Pustaka Utama.
Apriyantono A, Fardiaz D, Puspitasari NL, Sedarwati, Budiyanto S. 1989. Analisis Pangan. Bogor (ID): IPB Press.
Badan Pusat Statistik. 2011.Konsumsi dan Pengeluaran rata-rata per kapita seminggu Sayuran dan Buah-buahan. Jakarta : BPS.
22
Xuetong F, Niemera BA, Mattheis J, Zhuang H, Olson DW. 2005. Quality of Fresh-cut Apple Slices as Affected by Low-dose Ionizing Radiation and Calcium Ascorbate Treatment. Journal of Food Science. 70 :143-148. Garcia E, Barret DM. 2002. Preservative Treatments for Fresh-Cut Fruits and
Vegetables. California (US): Dept. of Food Science and Technology. Ghidelli C, Mateos M, Rojas-Argudo C, Pérez-Gago MB. 2013. Antibrowning
effect of antioxidants on extract, precipitate, and fresh-cut tissue of artichokes. LWT - Food Science and Technology. 51:462-468. doi.org/10.1016/j.lwt.2012.12.009
Gonzalez-Aguilar GA, Ruiz-Cruz S, Soto-Valdez H, Vazquez-Ortiz F, Pacheco-Aguilar R, Chien YW. 2005. Biochemical changes of fresh-cut pineapple slices treated with antibrowning agents. International Journal of Food Science and Technology.40:377–383.
Hasanah U. 2009. Pemanfaatan gel lidah buaya sebagai edible coating untuk memperpanjang umur simpan [skripsi]. Bogor (ID): Institut Pertanian Bogor. Jeong HL, Jin WJ, Kwang DM, Kee JP. 2008. Effects of Anti-Browning Agents
on Polyphenoloxidase Activity and Total. ASEAN Food Journal. 79-87. Kismaryanati A. 2007. Aplikasi gel lidah buaya (aloe vera L) sebagai edible
coating pada pengawetan tomat (Lycopersicon esculentum Mill [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Kuczinsky A, Varoquaux P, Varoquaux F. 1992. Reflectometric method to Market. Florida (US): CRC Press LLC.
Latifah. 2009. Pengaruh coating pati ubi jalar putih (Ipomoea batatas L) terhadap perubahan warna apel potong segar (fresh-cut apple)[skripsi]. Bogor (ID): Institut Pertanian Bogor
Zhang M, Cui Y, Charles MT, Bondar A, DeEll J. 2008. Browning Index of New Apple Genotypes Developed for Fresh-cut and Processing. Agriculture and Agrifood Canada. 306-311.
Mattjik AA, Sumertajaya IM. 2002. Perancangan Percobaan dengan aplikasi SAS dan Minitab. Bogor (ID): Percetakan Jurursan Statistika FMIPA IPB. Perera CO. 2007. Minimal Processing of Fruits and Vegetables. New York (US):
CRC Press.
Reynolds D. 1999. "Aloe vera leaf gel." Journal of Ethnopharmacology. 3-37. Rocha, Morais. 2003. "Shelf life of minimally processed apple (cv.Jonagored)
determined by color changes." Food Control.14(1):13-20.
Rowe RC, Sheskey PJ, Quinn ME. 1986. Handbook of Pharmaceutical Excipients. London(UK): Pharmaceutical Press.
23 Lampiran 1. Data Total Padatan Terlarut pada suhu 50C
Perlakuan ulangan H0 H1 H2 H3 H4 H5 H6
P1
P11 13.70 13.20 9.60 12.60 12.00 11.80 12.30
P12 12.30 11.40 8.90 14.10 15.30 13.40 12.60
P13 11.50 12.20 10.20 15.20 15.10 12.10 12.00
Rataan 12.50 12.27 9.57 13.97 14.13 12.43 12.30
P2
P21 10.50 11.40 7.90 12.20 10.60 7.80 11.80
P22 10.40 11.50 9.90 12.90 10.10 9.30 10.90
P23 11.00 11.90 9.10 11.10 11.90 8.60 11.10
Rataan 10.63 11.60 8.97 12.07 10.87 8.57 11.27
P3
P31 10.10 9.80 8.10 12.10 12.70 11.50 11.50
P32 10.40 11.00 8.50 11.00 12.90 11.30 12.10
P33 12.40 10.70 9.10 10.40 12.70 13.30 10.50
Rataan 10.97 10.50 8.57 11.17 12.77 12.03 11.37
P4
P41 11.00 10.70 11.00 11.50 10.60 11.20 11.00
P42 11.60 11.40 7.90 10.60 14.50 11.80 11.80
P43 10.50 10.60 9.50 10.90 13.80 11.80 11.70
Rataan 11.03 10.90 9.47 11.00 12.97 11.60 11.50
P5
P51 12.40 10.30 10.30 11.30 11.20 11.50 9.60
P52 10.50 10.70 9.60 10.00 9.90 11.40 11.00
P53 10.70 9.40 11.10 11.30 11.70 12.80 11.50
24
Lampiran 2. Hasil ANOVA untuk Total Padatan Terlarut
Test of Homogeneity of Variances
Levene Statistic df1 df2 Sig.
.671 4 10 .627
ANOVA
Sum of Squares df Mean Square F Sig.
Between Groups 6.297 4 1.574 22.354 .000
Within Groups .704 10 .070
Total 7.001 14
Duncan
Perlakuan
Subset for alpha = 0.05
N 1 2 3
2 3 10.5633
5 3 10.8633 10.8633
3 3 11.0533 11.0533
4 3 11.2100
1 3 12.4500
25 Lampiran 3. Data Kekerasan pada suhu 50C
Perlakuan ulangan H0 H1 H2 H3 H4 H5 H6
P1
P11 1.6 2.05 1.09 1.43 1.34 1.08 1.3
P12 1.59 1.25 1.2 1.57 1.42 1.12 1.14
P13 1.7 2.43 1.1 1.56 1.58 1.12 1.58
Rataan 1.63 1.91 1.13 1.52 1.45 1.11 1.34
P2
P21 1.89 1.97 1.18 1.05 1.03 1.14 1.07
P22 1.1 1.06 0.93 1.19 1.12 1.3 1.08
P23 1.7 1.63 1.02 1.13 1.16 1.4 1.18
Rataan 1.56 1.55 1.04 1.12 1.10 1.28 1.11
P3
P31 1.46 1.43 0.73 1.38 1.18 0.9 1.16
P32 1.3 1.95 1.02 1.08 1.64 1.14 1.07
P33 2 2.16 1.23 1.14 1.37 1.57 1.07
Rataan 1.59 1.85 0.99 1.20 1.40 1.20 1.10
P4
P41 2.06 1.01 1.51 1.2 1.48 1.08 1.07
P42 1.86 1.6 1.21 1.14 1.45 1.46 1.47
P43 1.9 1.32 1.27 1.29 1.56 1.19 1.27
Rataan 1.94 1.31 1.33 1.21 1.50 1.24 1.27
P5
P51 1.43 1.2 1.27 1.36 1.36 1.38 1.36
P52 1.27 1.35 0.74 1.29 1.36 1.39 1.07
P53 1.46 1.28 1.52 0.8 1.28 0.7 1.49
Rataan 1.39 1.28 1.18 1.15 1.33 1.16 1.31
Lampiran 4. Hasil ANOVA untuk Kekerasan
Test of Homogeneity of Variances
Levene Statistic df1 df2 Sig.
1.110 4 10 .404
ANOVA
Sum of Squares Df Mean Square F Sig.
Between Groups .085 4 .021 1.575 .255
Within Groups .135 10 .013
26
Lampiran 5. Data Susut Bobot pada suhu 50C
Perlakuan ulangan H0 H1 H2 H3 H4 H5 H6
P1
P11 0.00 0.13 0.70 0.75 0.95 1.14 1.30
P12 0.00 0.13 0.41 0.54 0.62 0.85 0.91
P13 0.00 0.11 0.64 0.74 0.83 0.91 1.06
Rataan 0.00 0.12 0.59 0.68 0.80 0.97 1.09
P2
P21 0.00 0.09 0.55 0.53 0.69 0.77 0.86
P22 0.00 0.07 0.54 0.61 0.67 0.75 0.86
P23 0.00 0.11 0.42 0.50 0.56 0.74 0.74
Rataan 0.00 0.09 0.50 0.54 0.64 0.75 0.82
P3
P31 0.00 0.10 0.62 0.60 0.78 0.88 0.99
P32 0.00 0.08 0.53 0.60 0.68 0.78 0.89
P33 0.00 0.08 0.45 0.62 0.66 0.78 0.89
Rataan 0.00 0.09 0.53 0.61 0.71 0.81 0.92
P4
P41 0.00 0.67 0.81 0.92 0.97 1.09 1.19
P42 0.00 0.04 0.42 0.50 0.56 0.66 0.74
P43 0.00 0.05 0.54 0.59 0.69 0.79 0.87
Rataan 0.00 0.25 0.59 0.67 0.74 0.85 0.93
P5
P51 0.00 0.11 0.55 0.62 0.68 0.81 0.86
P52 0.00 0.14 0.54 0.60 0.67 0.86 0.87
P53 0.00 0.17 0.64 0.71 0.78 0.90 1.04
Rataan 0.00 0.14 0.58 0.64 0.71 0.85 0.92
Lampiran 6. Hasil ANOVA untuk Susut Bobot
Test of Homogeneity of Variances
Levene Statistic df1 df2 Sig.
4.056 4 10 .033
ANOVA
Sum of Squares Df Mean Square F Sig.
Between Groups .029 4 .007 .621 .658
Within Groups .116 10 .012
27 Lampiran 7. Data Vitamin C pada suhu 50C
Perklakuan Kode mg as askorbat/100g rata-rata Vitc
28
Lampiran 8. Hasil ANOVA untuk Vitamin C
Test of Homogeneity of Variances
Levene Statistic df1 df2 Sig.
2.245 4 10 .137
ANOVA
Sum of Squares Df Mean Square F Sig.
Between Groups 1283.691 4 320.923 35943.242 .000
Within Groups .089 10 .009
Total 1283.781 14
Duncan
Perlakuan
Subset for alpha = 0.05
N 1 2 3 4 5
1 3 3.9543
2 3 4.1780
5 3 4.3800
4 3 4.7443
3 3 27.4323
29 Lampiran 9. Data Warna pada parameter L pada suhu 50C
Perlakuan ulangan H0 H1 H2 H3 H4 H5 H6
Lampiran 10. Data Warna pada parameter a pada suhu 50C
30
Lampiran 11. Data nilai BI
Perlakuan Ulangan H0 H1 H2 H3 H4 H5 H6
P1
P11 -750 1627.907 1279.07 465.1163 1017.442 988.3721 171.5116 P12 -834.302 2284.884 476.7442 755.814 915.6977 1779.07 386.6279 P13 -938.953 1555.233 2136.628 726.7442 1174.419 569.7674 1061.047
P2 P43 -956.395 -1008.72 287.7907 11.62791 895.3488 -601.744 369.186
P5
P51 -1927.33 -927.326 -305.233 -2593.02 -822.674 -372.093 -98.8372 P52 -1023.26 61.04651 -453.488 -1127.91 -793.605 -854.651 -584.302 P53 -2017.44 -636.628 139.5349 -1433.14 46.51163 171.5116 883.7209
31 Lampiran 13. Hasil ANOVA untuk Warna parameter BI (Browning Index)
Test of Homogeneity of Variances
Levene Statistic df1 df2 Sig.
.898 4 10 .500
ANOVA
Sum of Squares df Mean Square F Sig.
Between Groups 1.514 4 3783923.397 47.084 .000
Within Groups 803649.955 10 80364.995
Total 1.594 14
Duncan
Perlakuan
Subset for alpha = 0.05
N 1 2 3 4
3 3 -2320.0443
2 3 -1108.8040
5 3 -698.5050 -698.5050
4 3 -545.1274
1 3 802.3256
Sig. 1.000 .107 .523 1.000
Lampiran 14. Penampakan warna apel pada hari ke-0 penyimpanan suhu 5°C
P1 P2 P3
32
Lampiran 15. Penampakan warna apel pada hari ke-1 penyimpanan suhu 5°C
P1 P2 P3
P4 P5
Lampiran 16. Penampakan warna apel pada hari ke-2 penyimpanan suhu 5°C
P1 P2 P3
33 Lampiran 17. Penampakan warna apel pada hari ke-3 penyimpanan suhu 5°C
P1 P2 P3
P4 P5
Lampiran 18. Penampakan warna apel pada hari ke-4 penyimpanan suhu 5°C
P1 P2 P3
34
Lampiran 19. Penampakan warna apel pada hari ke-5 penyimpanan suhu 5°C
P1 P2 P3
P4 P5
Lampiran 20. Penampakan warna apel pada hari ke-6 penyimpanan suhu 5°C
P1 P2 P3
35
RIWAYAT HIDUP
Penulis dilahirkan di Bandung pada 26 November 1989 dari Bapak Ismail Effendi dan Ibu Denden Nurtini (alm). Penulis merupakan anak kedua dari dua bersaudara (Yullyati Erliany). Penulis menyelesaikan pendidikan akademik di SD Kartika XI-10, SMPN 13 Bandung, SMAN 20 Bandung, dan diterima di IPB melalui jalur SNMPTN (Seleksi Nasional Perguruan Tinggi Negeri) 2009 pada program Studi Teknik Pertanian, Departemen Teknik Pertanian (Sekarang bernama Teknik Mesin dan Biosistem), Fakultas Teknologi Pertanian.
Selama masa perkuliahan, penulis aktif mengikuti kegiatan diberbagai organisasi intra kampus. Kegiatan tersebut diantaranya adalah Anggota Departemen Syiar di LDK Al Hurriyyah, Sekretaris DPM KM IPB, Sekretaris MPM KM IPB, dan Badan Pengawas Himpunan Mahasiswa Tekik Pertanian. Penulis mengikuti kegiatan praktik lapangan di KPBS Pangalengan, Bandung Jawa Barat pada bulan Juli-Agustus 2012.