NURMALIA MULIATI
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
BOGOR
Ekstrak Panili Komersial. Dibimbing oleh DWI SETYANINGSIH.
Panili digunakan secara luas pada industri pangan terutama sebagai flavor dan pada
industri parfum. Flavor panili ada yang alami dan ada yang sintetis. Flavor panili sintetis
hanya mengandung salah satu komponen flavor vanilla yaitu vanillin atau etil vanillin
(Boyce
et.al
, 2003), sehingga aroma yang dihasilkan tidak sekaya aroma ekstrak panili
alami. Aroma maupun rasa yang terdapat pada ekstrak panili tergantung pada varietas
tanaman, tanah, lingkungan dan proses
curing
. Ekstrak panili mengandung lebih dari 100
senyawa volatil yang terdeteksi termasuk
aromatic carbonyls, aromatic alcohol,
aromatic acids, aromatic esters, phenols
dan
phenols ethers, aliphatic alcohols,
carbonyls, acids, esters,
dan
lactones
, di mana aldehyde vanillin yang paling dominan
(Perez-Silva et al.,2005; Adedeji et al., 1992; Klimes &Lamparsky, 1976; Ranadive,
1994). Kandungan vanillin, p-hydroxybenzaldehyde,
vanillic acids
, dan
p-hydroxybenzoic dalam
cured vanilla
menentukan kualitas untuk tujuan komersial.
Sebanyak 70-80% sumber panili dunia berasal dari Madagaskar. Adapun Amerika
Serikat saat ini membeli buah panili dari Madagaskar, Indonesia, Uganda dan Tonga.
Sebagian besar panili berkualitas tinggi diperoleh dari Madagaskar. Panili
Madagaskar-Bourbon memiliki flavor
smooth, rich
dan
sweet
. Panili Mexico memiliki flavor
smooth,
strong
dan
rich.
Panili Tahiti tidak memiliki flavor yang kuat seperti yang lain, akan
tetapi sangat aromatik dengan aroma floral yang kompleks sehingga digunakan untuk
parfum.
Ekstrak panili Indonesia memiliki aroma cenderung kepada
woody
dan
phenolic
karena pemanenan yang terlalu cepat dan proses kuring yang tidak sempurna.
Usaha untuk meningkatkan nilai tambah produk pertanian terus dilakukan,
termasuk pada buah panili. Selama ini para petani menjual panili dalam bentuk segar
bahkan terkadang masih mentah. Harga rata-rata buah panili segar tahun 2001 sebesar
Rp. 301.330 / kg (Deptan Dirjen Bina Produksi Perkebunan, 2004). Pengolahan buah
panili menjadi panili kering dan ekstrak panili akan memberikan nilai tambah pada
produk panili. Penelitian ini bertujuan mengetahui karakteristik fisikokimia dan aroma
ekstrak panili yang ada di Indonesia baik produk lokal (untuk ekspor) maupun produk
impor kemudian dibandingkan dengan ekstrak panili dari buah panili lokal hasil
penelitian dengan metode terbaru.
Penelitian dilakukan dengan menganalisa sifat fisikokimia ekstrak panili sesuai
dengan standar
Food and Drug Administration (FDA)
yaitu kadar vanillin, kadar abu, abu
terlarut, alkalinitas abu terlarut, alkalinitas abu total, total asam dan
lead number
. Sifat
sensori yang dianalisa yaitu aroma. Analisa dilakukan dengan uji deskripsi kualitatif
dengan metode
in-depth interview
dan
focus group
; dan uji deskripsi kuantitatif dengan
QDA (
Quantitative Descriptive Analysis).
Uji deskripsi dilakukan oleh panelis terlatih
sebanyak 12 orang.
NURMALIA MULIATI
F34101017
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
pada DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN
FAKULTAS TEKNOLOGI PERTANIAN
KARAKTERISASI SIFAT FISIKOKIMIA DAN AROMA EKSTRAK
PANILI KOMERSIAL
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
pada DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
NURMALIA MULIATI
F34101017
Dilahirkan pada tanggal 5 Agustus 1983
Di Plaju
Tanggal lulus :
Disetujui
NURMALIA MULIATI. F34101017. Phsycochemical and Aroma Characterization
of Commercial Vanilla Extract. Under the direction of DWI SETYANINGSIH.
Vanilla is widely used as flavouring in the food and perfume industries. In
flavouring, there are natural extracts from beans harvested from vanilla orchid and
synthetics vanillin. Flavour from synthetic vanillin only consist one or two major
components usually vanillin or ethyl vanillin so that the aroma isnot as rich as natural
vanilla extract which contains complex mixture of 100-200 flavour components. The
taste and aroma of vanilla extract depend on varieties of plant, soil, environment and
curing process. Vanilla extract contains more than 100 volatil compounds detected
including aromatic carbonyls, aromatic alcohols, aromatic acids, aromatic esters, phenols
and phenols ethers, aliphatic alcohol, carbonyls, acids, esters, and lactones, of which the
aldehyde vanillin is the most abundant (Perez-Silva
et.al
., 2005; Adedeji
et a
l., 1993;
Klimes & Lamparsky, 1976; Ranadive, 1994). The level of the aldehydes vanillin,
vanillin, hydroxybenzaldehyde and their respective acids (vanillic acid and
p-hydroxybenzoic acid) in cured vanilla is used as an indicator of cured vanilla bean quality
for commercial purpose. The 70-80% sources of vanilla beans come from Madagascar.
Today, United States buys vanilla beans from Madagascar, Indonesia, Uganda and
Tonga. Most of high quality vanilla beans are achieved from Madagascar.
Madagascar-Bourbon vanilla has smooth, rich, and sweet flavour. Mexican vanilla has smooth, strong
and rich flavour. Tahitian vanilla has aromatic and complex floral aroma used in
perfume. Indonesian vanilla extracts tend to woody, and phenolic because of earliest
harvested and unperfected curing process.
The efforts to increase agricultural added value were done continuously including
vanilla. As long as we know that farmers sold fresh vanilla beans even they were still
unripe. The average prices of whole vanilla in 2001 was Rp. 301.330/kg (Deptan Dirjen
Bina Produksi Perkebunan, 2004). The curing process from cured vanilla to vanilla
extract would give added value to vanilla product. This experiment had objective to know
the phsycochemical and aroma characteristics of commercial vanilla extracts in
Indonesia from local product (to be exported) and from imported product. Then, they
were compared with vanilla extract from the new experiment.
This experiment analyzed amount of vanillin, total ash, soluble ash, alcalinity of
soluble ash, alcalinity of total ash, total acidity and lead number. Sensory characteristic
analyzed was aroma. Analysis was done by qualitative descriptive test with In-Depth
Interview and Focus Group methods, and quantitative descriptive analysis (QDA). These
tests used 12 trained panelists.
A.LATAR BELAKANG
Panili digunakan secara luas pada industri pangan terutama sebagai
flavor dan pada industri parfum. Flavor panili ada yang alami dan ada yang
sintetis. Komposisi flavor sintetis lebih sederhana yaitu terdiri dari satu atau
dua komponen mayor, biasanya vanillin atau etil vanillin (Boyce et.al, 2003),
sehingga aroma yang dihasilkan tidak sekaya aroma ekstrak panili alami.
Ekstrak panili alami mengandung 100-200 komponen flavor. Lebih dari seratus
senyawa volatil yang terdeteksi, termasuk karbonil aromatik, alkohol aromatik,
asam aromatik, ester aromatik, fenol dan fenol ester, alkohol alifatik, karbonil,
asam, ester, dan lakton, di mana aldehid vanillin adalah yang paling dominan
(Pérez-Silva et al., 2005). Setiap jenis ekstrak panili memiliki profil aroma
yang berbeda-beda tergantung tempat tumbuhnya dan spesiesnya. Beberapa
jenis ekstrak panili diantaranya Bourbon Vanilla, Mexican vanilla, Tahiti
Vanilla, Guadaloupe vanillon dan Indonesian vanilla. Vanilla Indonesia
cenderung memiliki profil aroma woody dan phenolic karena proses
pengeringan yang terlalu cepat.
Produksi panili Indonesia tahun 2001 dan 2002 sebesar 2.198 ton dan
2.731 ton. Volume ekspor panili Indonesia tahun 2001 sebesar 468 ton (US$
19.309.000) dan meningkat menjadi 3.599 ton (US$ 19.160.000) pada 2002,
sedangkan volume impor tahun 2001 dan 2002 sebesar 230 ton (US$ 868.000)
dan 1.514 ton (US$ 1.346.000). Indonesia mengekspor panili utuh (vanilla
whole) paling banyak ke USA sebesar 372 ton (US$ 15.790.000) dan Jerman 29 ton (US$ 2.351.000) pada tahun 2001, sedangkan tahun 2002, ekspor ke
USA sebesar 242 ton (US$ 11.265.000) dan Jerman 51 ton (US$ 3.373), selain
itu ekspor juga dilakukan ke Hongkong, Singapura, Malaysia, Australia,
Kanada, Inggris, Prancis, Austria, dan lainnya. Panili dalam bentuk lain (other
vanilla) diekspor ke China, Malaysia, USA, Jerman, Vietnam, Prancis, dan lainnya dengan total volume 3.278 ton (tahun 2002) senilai US$ 2.950.000.
Negara pengimpor panili utuh adalah Madagascar, Amerika, Philipina dan
Malaysia, Australia, Timor-Timur, USA, Pakistan Singapura dan lainnya
(Badan Statistik, Dirjen Bina Produksi Perkebunan, 2004).
Buah panili selama ini diekspor dalam bentuk buah panili kering, padahal
jika dilakukan pengolahan lebih lanjut dari panili kering menjadi ekstrak panili
maka nilai tambah yang diperoleh akan jauh lebih besar. Kualitas ekstrak panili
yang dihasilkan pun harus mampu bersaing dengan ekstrak panili yang selama
ini dihasilkan oleh industri-industri pengekstrak di luar negeri, oleh karena itu,
dibutuhkan informasi mengenai mutu produk ekstrak panili lokal dan mutu
ekstrak panili impor, baik sifat fisikokimia maupun karakter aroma yang
dihasilkan untuk perbaikan produk-produk berbasis panili yang akan
dikembangkan.
B.TUJUAN PENELITIAN
Penelitian ini bertujuan mengetahui sifat fisikokimia dan sensori ekstrak
panili komersial baik produk lokal (dari eksportir) maupun produk impor dan
II. TINJAUAN PUSTAKA
A.PANILI
1.Botani Panili
Panili (Vanilla planifolia, Andrews) merupakan tanaman introduksi
yang berasal dari Mexico dan Amerika Tengah, tetapi saat ini sudah banyak
dibudidayakan di daerah tropik seperti Madagascar, Reunion dan Comoro
bahkan di Indonesia (Hadipoentyanti dan Udarno, 1998).
Panili termasuk famili Orchidaceae yang merupakan famili yang
terbesar dalam tanaman berbunga, mempunyai 700 genus dan 20.000
spesies (Purseglove et al., 1981). Spesies panili yang terpenting yaitu
Vanilla planifolia ditemukan oleh Andrews pada tahun 1808 (Chalot, 1920). Panili mulai dibudidayakan di Indonesia tahun 1819 (Ridley, 1912).
Penggolongan panili adalah sebagai berikut :
Divisi : Spermatophyta
Klas : Angiospermae
Sub Klas : Monocotyledon
Ordo : Orchidules
Famili : Orchidaceae
Genus : Vanilla
Species : Vanilla planifolia Andrews.
Tanaman panili adalah tanaman tahunan memanjat. Batangnya
berbuku-buku, dari buku-buku tersebut tumbuh daun dan akar adventif,
yang berguna untuk memanjat pada tiang panjatnya. Bunga keluar dari
ketiak daun dalam bentuk tandan yang mekar satu persatu setiap hari
dimulai dari pangkal ke atas. Panili dikenal sebagai tanaman berumah satu,
dan tidak dapat melakukan penyerbukan sendiri tanpa bantuan manusia.
Setiap buah yang masak mengandung ribuan biji yang sangat kecil berwarna
www.tahiti1.com Photo by Jim Reddekopp
Gambar 1. Buah panili yang sudah matang (1) dan tanaman panili (2)
Jenis panili banyak sekali, beberapa jenis sangat berbeda baik dari
segi morfologi maupun sifat-sifat lainnya. Pada Vanilla planifolia, buah
yang belum matang, keras, berwarna hijau tua setelah matang, agak lembek
berwarna hijau kekuningan dan setelah diproses (proses kuring, red.)
berwarna coklat tua. Buah matang mempunyai aroma yang khas daripanili.
Pematangan buah tidak serempak pada satu tandan (mekar bunga tidak
serentak), karena itu pemetikan (panen) dilakukan satu persatu secara
selektif. Buah yang matang mempunyai kecenderungan berpilin dan minyak
balsem (balsam oil) yang berwarna gelap akan muncul, epidermis menjadi
lunak dan harum panili akan timbul. Biji dilapisi oleh minyak berwarna
gelap dikenal dengan balsam of vanilla (Chalot, 1920, Ridley, 1912).
Vanilla pompana Schiede memiliki buah besar-besar lebih pendek
daripada buah V. planifolia, bersudut tiga dengan panjang 12-17.5 cm, dan
lebar 16-30 mm, berwarna hijau tua. Sudut-sudut pada buah V. pompana
lebih jelas dibandingkan V. planifolia. Buah V. planifolia lurus sedangkan
buah V. pompana berpilin sejak belum matang, buah yang matang berwarna
coklat tua, berbau seperti bunga matahari.
Vanilla tahitensis J.W. Moore memiliki buah yang tidak
mengeluarkan aroma seperti buah V. planifolia (Ridley, 1912). Menurut
Heyne (1927) buah berair manis, enak dimakan dan dapat menyuburkan
rambut. Karakteristik pada jenis ini adalah tahan terhadap hujan lebat
sehingga dapat dimanfaatkan untuk mendapatkan jenis unggul baru.
Panili umumnya dapat berkembangbiak dengan cepat di daerah tropis,
sekitar 25oLU dan LS dari khatulistiwa, atau di daerah pegunungan dengan
ketinggian 400-800 meter (Kantor Pusat BRI, 1986). Namun, Panili hutan
pernah ditemukan di dataran rendah (10 m dpl) maupun di dataran tinggi
antara lain di Kalimantan Timur sampai ketinggian 1000 m dpl (Herbarium
Bogoriensis, 1994).
2.Kegunaan Panili
Kegunaan panili terutama sebagai ramuan pada minuman serta untuk
memberikan aroma pada makanan seperti coklat, kembang gula dan es krim
(Hadipoentyanti dan Udarno, 1998). Burri et al. (1989) melaporkan bahwa
vanilin dapat digunakan sebagai antioksidan pada makanan yang banyak
mengandung komponen tak jenuh. Selanjutnya Cerutti et al. (1997)
menyebutkan bahwa kombinasi vanilin dengan 500 ppm asam askorbat pada
pH 3 mampu mencegah pertumbuhan mikroba alami dan kontaminan pada
puree strawberry yang disimpan selama 60 hari pada suhu ruang. Vanillin
juga digunakan dalam sintesa obat-obatan sebagai flavouring agent, sebagai
starting material dalam pembuatan obat antihipertensi (1-3-(3,4-dihydroxyl phenyl)-2-methylalanine) dan untuk perawatan penderita Parkinson
(Chemistry Department University Of Malta, 2000).
3.Sifat Fisikokimia
Buah panili setelah mengalami fermentasi akan menghasilkan Vanilin
(C8H8O3). Kandungan vanilin pada setiap jenis panili berbeda, perbedaan
tersebut disebabkan karena perbedaan agroklimat tempat tumbuhnya.
Sebagai contoh panili berasal dari Mexico (V. planifolia), kadar vanilinnya
1.32-1.86 %, dari Reunion (V. planifolia), 1.919-2.00% dan dari Tahiti (V.
tahitensis, V. pompana) 1.55 %. Untuk panili yang berkualitas rendah, kadar vanilin minimal 1.19 % sedangkan untuk panili yang berkualitas prima
(superior), kadar vanilin ditetapkan sebesar 1.50 % (Chalot, 1920). Menurut
(Vanillons), dalam hal aromanya kurang dibandingkan V. planifolia, karena itu hanya dipergunakan untuk membuat parfum.
Buah panili segar hampir tidak mempunyai bau sehingga harus diolah
melalui proses curing untuk menghasilkan aroma khas panili. Flavor khas
panili merupakan campuran kompleks lebih dari 170 komponen volatil yang
terdapat dalam buah vanili cured. Komponen utama pembentuk flavor panili
adalah vanilin, asam vanilat, vanilil alkohol, p-hidroksibenzaldehid, asam p
-hidroksibenzoat dan p-hidroksibenzil alkohol (Rao dan Ravishankar, 2000).
Komposisi kimia buah panili dan struktur kimia komponen-komponen
pembentuk flavor vanili dapat dilihat pada Tabel 1 dan Gambar 3.
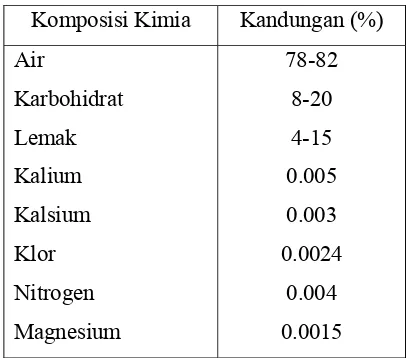
Tabel 1. Komposisi kimia Buah Panili Segar
Komposisi Kimia Kandungan (%)
Air
Karbohidrat
Lemak
Kalium
Kalsium
Klor
Nitrogen
Magnesium
78-82
8-20
4-15
0.005
0.003
0.0024
0.004
0.0015
Sumber: Purseglove et al. (1981)
Gambar 2. Buah panili cured (1) dan ekstrak panili dalam kemasan (2)
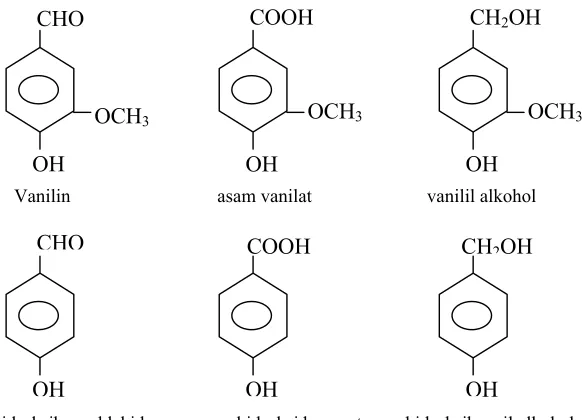
Vanilin asam vanilat vanilil alkohol
p-hidroksibenzaldehid asam p-hidroksi benzoat p-hidroksibenzil alkohol
Gambar 3. Struktur Kimia Komponen Utama Flavor Panili (Rao dan Ravishankar, 2000).
Buah panili hasil proses kuring mengandung protein, gula, serat
lignoselulosa, selulosa, asam organik, vanilin dan fenol monohidroksi,
minyak, lilin, resin, gum, pigmen, mineral, komponen aroma volatil dan
asam lemak esensial (Rao dan Ravishankar, 2000).
Tabel 2. Komponen Utama Panili Cured
Komposisi Kimia Kandungan
(g/kg berat kering)
Vanilin
Asam Vanilat
p-Hidroksibenzaldehid
p-Hidroksibenzil metil eter
Gula
Lemak
Selulosa
Mineral
Air
20
1
2
0.2
250
150
150-300
60
350
Sumber : Rao dan Ravishankar (2000) CHO
OCH3
OH
COOH
OCH3
OH
CH2OH
OCH3
OH
OH OH
CHO
OH
B.EKSTRAK PANILI
Ekstrak panili (Vanilla extract) yaitu ekstrak yang dihasilkan dari
perkolasi atau maserasi potongan-potongan buah panili dengan pelarut etil
alkohol dan air (www.vanilla.com/html/facts-extracts.html). Ekstrak panili
dapat pula dihasilkan dengan cara mencincang buah panili dan
menghaluskannya dengan gula (sebanyak setengah dari bobot buah panili)
yang akan membantu jalannya ekstraksi dan proses penuaan produk,
kemudian diperkolasi dalam ekstraktor stainless steel menggunakan ethanol
dan air kira-kira 57% volume selama 3-4 minggu. Perkolasi dikumpulkan
dan dihaluskan kemudian disimpan sampai penuaan tertentu lalu disaring
atau disentrifugasi (Cowley 1973).
FDA mengatur bahwa ekstrak panili 1 fold adalah ekstrak yang murni
mengandung 13.35 ons buah panili/gallon cairan dan mengandung 35%
alcohol. Fold adalah ukuran kekuatan ekstrak vanilla. Untuk food
processing, digunakan vanilla dua, tiga, atau empat fold. Vanilla dua fold
menggunakan 26,7 ons buah panili, mengandung dua kali lebih banyak
bahan ekstrak dan dua kali lebih kuat. Tiga fold, empat fold merupakan tiga
atau empat kali kandungan satu fold (www.nielsenmassey.com).
Aroma vanilla berkembang akibat proses enzimatik dan kimiawi
selama proses kuring. Flavor vanilla yang kaya dan lengkap mengandung
lebih dari 250 komponen senyawa volatil dan kebanyakan dari senyawa
tersebut berperan dalam sifat organoleptik secara keseluruhan (Tanudjaja,
1998; Dignum, 2002). Komposisi flavor sintetis lebih sederhana yaitu terdiri
dari satu atau dua komponen mayor, biasanya vanillin atau etil vanillin
(Boyce et.al, 2003), sehingga aroma yang dihasilkan tidak sekaya aroma
ekstrak panili alami. Pure vanilla mempunyai aroma delicate, yet rich, dan
mellow. Flavor tiruan mempunyai bau yang berat dan grassy
(Reineccius,1994).
Analisis yang menentukan banyaknya vanillin yang ada, lead
number, kandungan abu dan nilai lainnya digunakan untuk mengetahui apakah ekstrak tersebut telah mengalami pencampuran atau pemalsuan
Standar ekstrak panili berdasarkan FDA adalah kadar etanol 350 ml/l
atau lebih, mengandung gliserin, propilen glikol, gula, dan sirup sebagai
pengental dan pemanis, anti kempal pada produk akhir tidak lebih dari 20
g/kg, kekuatan two fold, kadar vanillin 1.1-3.5 g/l, abu 2.2-4.32 g/l, abu
terlarut 1.79-3.57 g/l, lead number 4.0-7.4, alkalinitas abu total 300-540 ml
0.1 N asam/l, alkalinitas abu terlarut 220-400 ml 0.1 N asam/l, total asam
300-520 ml 0.1 N basa/l, dan keasaman selain vanillin 140-420 ml 0.1 N
basa/l (Heath, 1978).
C.ANALISIS SENSORI
Analisis sensori merupakan analisis yang menggunakan manusia
sebagai instrumen, dimana kemungkinan terjadi penyimpangan sangat
besar. Dasar-dasar dari faktor fisiologi dan psikologi yang dapat
berpengaruh terhadap penilaian sensori harus dipahami untuk
meminimalisasi penyimpangan atau penilaian yang berubah-ubah,
(Meilgaard et al., 1999).
Menurut Noble (2002), analisis sensori pada analisis flavor mirip
dengan analisis menggunakan instrumen, yaitu menggunakan standar yang
baku dan dalam suatu kondisi yang terkontrol. Semua faktor eksternal yang
dapat membiaskan penilaian harus disingkirkan. Test harus difasilitasi
sebaik mungkin sehingga dapat mencegah berbagai gangguan.
Respon secara obyektif terhadap sifat makanan diperoleh dengan
penilaian organoleptik melalui penglihatan, penciuman, rasa, sentuhan, dan
pendengaran (Piggott et al., 1998). Terdapat beberapa metode dalam
mendeskripsikan sifat makanan, yaitu secara kualitatif dan secara
kuantitatif. Menurut Meilgaard et al., (1999) semua metode analisis
deskripsi menggunakan penilaian baik secara kualitatif maupun secara
kuantitatif, menuntut panelis untuk dapat mendeteksi dan menggambarkan
atribut-atribut sensori sedekat mungkin. Metode kualitatif dilakukan untuk
mendapatkan dan mengembangkan bahasa, sehingga dapat menggambarkan
sampel yang nantinya sangat penting untuk analisis secara kuantitatif,
produk dengan memberikan penilaian yang menggambarkan sampel dalam
suatu skala interval.
Metode kuantitatif yang cukup sering digunakan yaitu Quantitative
Descriptive Analysis (QDA) yaitu suatu metode yang digunakan untuk menggambarkan suatu karakteristik sensori suatu produk secara matematis
(Zook dan Pearce, 1988 dalam Aryati 2003). QDA menggunakan panelis
terlatih yang memberi penilaian terhadap intensitas atribut suatu produk
yang dibandingkan dengan standar pada skala garis sepanjang 6 inci (15
cm). Data QDA setelah mengalami transformasi data dapat ditampilkan
dalam bentuk grafik majemuk jaring laba-laba (spider web) atau
menggunakan Multivariate Analysis dengan aplikasi teknik Principal
Component Analysis (PCA).
D.PRINCIPAL COMPONENT ANALYSIS
Principal Component Analysis (PCA) merupakan metode analisis
statistika multivariate yang digunakan untuk mentransformasikan
variabel-variabel asli menjadi variabel-variabel-variabel-variabel baru yang mempunyai dimensi lebih
kecil, saling bebas dan orthogonal antara variabel satu dengan variabel
lainnya. Dimensi-dimensi yang baru ini dipilih menurut syarat khusus, yaitu
masing-masing dimensi harus memaksimalkan jumlah keragaman yang
dijelaskan (Carpenter et al., 2000). Variabel-variabel baru tersebut
merupakan kombinasi linear dari variabel aslinya (Esbensen et al., 1994)
dan dinamakan komponen utama (Principle Component/PC).
Analisis ini mampu menjelaskan sebanyak 75%-90% dari total
keragaman dalam data yang mempunyai 25 sampai 30 variabel hanya
dengan dua sampai tiga principal component (Meilgaard et al., 1999).
Menurut Esbensen et al. (1994), tahapan dasar dalam PCA adalah
mentransformasikan p variabel-variabel kuantitatif awal yang kurang saling
berkorelasi ke dalam p variabel kuantitatif baru yang disebut komponen
utama. Jadi hasil analisis tipe ini tidak berasal dari variabel-variabel awal
tetapi dari indeks sintetik yang diperoleh dari kombinasi linear
Diantara semua indeks sintetik yang mungkin terbaca, analisis ini
mencari terlebih dahulu indeks yang menunjukkan ragam individu yang
maksimum. Indeks ini disebut komponen utama-1(PC1) dan mempunyai
variasi terbesar dari variasi total individu. Selanjutnya dicari komponen
utama-2 dengan syarat berkorelasi nihil dengan yang pertama dan memiliki
variasi individu terbesar setelah komponen utama-1. Proses ini akan terus
berlanjut sampai komponen utama terakhir, dimana variasi individu yang
dijelaskan akan semakin kecil (Esbensen et al., 1994).
Setiap komponen dalam model PCA dikarakterisasi oleh tiga atribut
yang saling melengkapi, yaitu keragaman (variance) yang memberikan
berapa banyak informasi yang dapat digunakan pada komponen utama yang
dapat dinyatakan dengan residual variance dan explained variance, lalu
loading yang menyatakan gambaran hubungan (korelasi) antara
variabel-variabel dalam setiap komponen utama, dan scores yang menggambarkan
sifat-sifat subyek (sampel).
Hasil analisa merupakan gabungan dari plot loading dan scores dalam
bentuk grafik biplot. Grafik ini menggambarkan hubungan antara variabel
dan sampel secara keseluruhan. Jarak antara titik variabel menunjukkan
hubungan diantara variabel. Interpretasi untuk titik-titik sampel sama
dengan interpretasi variabel. Hubungan antara dua titik sampel dapat dilihat
dengan membandingkan jaraknya dengan titik-titik dari variabel. Titik-titik
sampel yang berdekatan menunjukkan bahwa sampel-sampel tersebut sama,
sedangkan titik-titik sampel yang berjauhan menunjukkan hal yang
sebaliknya. Titik-titik sampel yang terdapat dalam satu kelompok adalah
sama sedangkan titik-titik sampel antara kelompok adalah berbeda
III. BAHAN DAN METODE
A.BAHAN DAN ALAT
1. Bahan Baku
Kode sampel dari eksportir : Cobra (PT. Tripper Nature) dan
Djasulawangi (PT. Djasulawangi), importir: Virginia, Tahiti dan Grade II,
sedangkan dari hasil penelitian : S7 dan G11. Semua sampel diperoleh
dalam bentuk ekstrak panili kecuali Djasulawangi dalam bentuk panili
kering yang ekstraknya dibuat sendiri oleh peneliti. Ekstrak panili S7 dan
G11 merupakan hasil penelitian Melawati (2006). Metode ekstraksi
Djasulawangi, S7 dan G11 dapat dilihat pada lampiran 2, 3 dan 4. Sampel
S7 dan G11 menggunakan panili ½ kering hasil modifikasi proses kuring.
Modifikasi proses kuring adalah modifikasi pengolahan panili yang terdiri
dari tahap sortasi buah panili, penyayatan buah dengan menggunakan jarum
sedalam 1-2 mm, perendaman buah dalam aktivator butanol 0,3 M dan
sistein 1mM selama dua jam, pelayuan dalam air panas pada suhu 40oC
selama 30 menit, pemeraman selama 18 jam pada suhu 38-40oC,
pengeringan I pada suhu 40oC tiga jam/hari selama lima hari, pengeringan II
pada suhu 60oC tiga jam/hari sampai dengan kadar air 35%, dan penuaan
selama satu bulan.
Produk panili yang berasal dari konsumen tidak digunakan dalam
penelitian ini karena bukan berupa ekstrak alami akan tetapi flavor atau
essence panili sintetis.
2. Bahan Kimia
Bahan kimia yang digunakan ialah propilen glikol, Na2EDTA 0.025
N, NaOH 0.1 N, HCl 0.1 N, NaCH3COO 0.1 N, CH3COOH 0.1 N,
Pb(CH3COO)2, xylenol orange, indikator PP, indikator methyl orange,
etanol 60 %, guaiacol, ethyl butyrat, lactone, benzyl alcohol, vanillin
3. Alat
Pipet 200 µl, pipet 1000 µl, labu takar 10 ml dan 25 ml, gelas ukur,
spektrofotometer UV (Simadzu), pipet tetes, pipet 5ml dan 10 ml, cawan
porselen, hot plate, tanur, gegep, filterflask, pompa vakum, milipore 0.45
µm, buret, botol aquades, oven, labu destilasi alkohol, desikator, neraca
analitik, refrigerator, erlenmeyer, gelas piala, gelas ukur, sudip, pH meter,
botol gelap berulir 10 ml, smelling strips, dll.
B. METODE PENELITIAN
1. Analisis Sifat Fisikokimia
Analisis sifat fisikokimia ekstrak panili yaitu karakterisasi tiga
kelompok ekstrak panili yang meliputi warna, kadar vanillin, kadar abu, abu
terlarut, lead number, alkalinitas abu total, alkalinitas abu terlarut dan total
asam. Sifat fisik yang dianalisis yaitu warna yang diamati secara visual.
Sifat kimia dianalisis dengan prosedur pengujian terlampir pada lampiran 1.
Hasil analisis ini digunakan untuk menduga mutu ekstrak panili dari
eksportir, importir dan hasil percobaan dibandingkan dengan standar FDA
(Food and Drug Administration). Pendugaan ini didasarkan pada sampel ekstrak panili yang diambil. Sebaran yang diambil adalah sebaran t dengan
membandingkan dua kelompok yaitu μ karakteristik fisikokimia seluruh
ekstrak sampel dengan μ karakteristik fisikokimia standar FDA.
Hipotesis yang digunakan dalam pengujian ini adalah
Ho : μ karakteristik fisikokimia ekstrak sampel = μ karakteristik
fisikokimia standar FDA
Ht : μ karakteristik fisikokimia ekstrak sampel ≠ μ karakteristik
fisikokimia standar FDA
Nilai pembanding dalam hipotesis ini sesuai dengan spesifikasi FDA.
Syarat penerimaan adalah bila t (hitung) lebih kecil dari t (tabel) dan lebih
besar dari –t(tabel) pada taraf signifikan (α) 0.05. Nilai t (hitung) didapatkan
dengan rumus berikut:
………(1)
n s
x hitung t
/ )
Keterangan :
= nilai rata-rata contoh (sampel)
μ = nilai rata-rata populasi
s = simpangan baku sampel
n = besarnya sampel
………(2)
s2= penduga ragam
………..(3)
2. Analisis Sensori
Analisis sensori yang dilakukan adalah uji deskripsi. Untuk
melakukan uji deskripsi, diperlukan panelis yang terlatih, maka ada
beberapa tahapan yang dilakukan sebelum uji deskripsi, yaitu tahap seleksi
panelis, tahap pelatihan panelis dan tahap pengujian. Tahap pengujian terdiri
dari uji deskripsi secara kualitatif dan kuantitatif. Uji deskripsi secara
kualitatif dilakukan dengan metode In-Depth Interview dan Focus Group,
sedangkan uji deskripsi secara kuantitatif dilakukan dengan metode QDA
(Quantitative Descriptive Analysis).
a. Seleksi Panelis
Seleksi panelis dilakukan dengan menyebarkan kuesioner
(Prescreening Questionnaire) yang selanjutnya diolah dan diseleksi untuk mendapatkan calon panelis yang sesuai kriteria dan bersedia
mengikuti pelatihan panelis. Salah satu kriteria menjadi panelis adalah
kesehatan indra panelis terutama penciuman karena pengujian yang akan
dilakukan terkait dengan aroma. Setelah terpilih, maka dilanjutkan
x n x x x x x x n i i n n i
i ... ; /
dengan seleksi panelis menggunakan uji segitiga. Contoh Prescreening Questionnaire dapat dilihat pada lampiran 13.
Dalam uji segitiga, digunakan flavor standar sebagai sampel uji.
Flavor standar yang digunakan dalam uji yaitu benzyl alkohol dengan
atribut aroma sweet, vanillin dengan aroma vanilla dan eugenol dengan
aroma spicy. Ketiga flavor standar tersebut digunakan karena memiliki
atribut aroma yang ada pada ekstrak panili sebagai sampel uji pada tahap
pengujian.
Pada uji segitiga, panelis diminta menemukan satu yang beda di
antara ketiga sampel yang diuji dan apabila 60 % jawaban panelis benar
maka panelis lolos seleksi dan dapat mengikuti tahap pelatihan.
b. Pelatihan Panelis
Tahap pelatihan panelis terdiri dari pengenalan bahasa flavor,
pelatihan penskalaan, dan pelatihan intensitas skala. Pada pelatihan
pengenalan bahasa flavor, panelis diperkenalkan dengan lima flavor
standar yaitu spicy, creamy, balsamic, sweet, dan smoky.
Pada tahap pelatihan penskalaan, dilakukan uji rangking di mana
panelis diminta memberikan nomor urut terhadap sampel-sampel sesuai
dengan intensitasnya. Pelatihan ini untuk melatih kemampuan panelis
untuk membedakan intensitas aroma-aroma. Formulir isian setiap uji
dapat dilihat pada lampiran 14-19.
Tahapan terakhir dari pelatihan panelis ialah pelatihan intensitas
skala. Pelatihan ini dilakukan dengan uji skalar garis, yaitu salah satu uji
skalar yang menggunakan garis sebagai parameter penentuan suatu kesan
dari suatu rangsangan. Dengan menggunakan skalar garis dapat diketahui
besaran kesan yang diperoleh dari suatu komoditi sehingga dapat
diketahui mutu dari komoditi tersebut (Rahayu, 1998). Pelatihan uji
intensitas skala dilakukan dengan menilai intensitas aroma sampel
kemudian dibandingkan dengan flavor standar yang telah diketahui
c. Tahap Pengujian (1)Analisis Kualitatif
Analisis kualitatif dilakukan dengan teknik in-depth interview,
di mana masing-masing panelis mendeskripsikan sampel dipandu
dengan moderator, dan dengan teknik Focus Group yang berbentuk
kelompok diskusi untuk mendeskripsikan atribut-atribut yang
terdapat dalam sampel sesuai kesepakatan bersama. Teknik ini juga
dipandu oleh moderator (panel leader). Setiap panelis membaui
setiap sampel dengan bottle technique dan dilakukan simplo.
(2)QDA (Quantitative Descriptive Analysis)
QDA adalah metode analisis untuk mengukur intensitas suatu
produk (Resurreccion, 1998). Panelis menilai intensitas aroma setiap
atribut aroma pada garis sepanjang 15 cm (nilai 0 = lemah, 15 =
kuat). Kemudian nilainya ditransformasikan pada skala 1-100 dan
divalidasi keragaman datanya. Data diterima bila memenuhi:
X – SD ≤ d ≤ X + SD
di mana : X = rata-rata data intensitas atribut pada QDA
SD = simpangan baku data intensitas atribut
pada QDA
d = data intensitas atribut pada QDA
Setelah divalidasi, data QDA tersebut divisualisasikan dalam
bentuk spiderweb untuk melihat profil aromanya. Panelis
memberikan penilaian intensitas aroma dengan membandingkan
intensitas atribut aroma pada ekstrak dengan intensitas flavor standar
yang telah diberi nilai tertentu. Standar aroma yang digunakan dalam
QDA dapat dilihat pada Tabel 3.
3. Pengolahan Data
Pengolahan data dilakukan dengan PCA (Principal Component
Analysis). PCA digunakan untuk mengetahui kecenderungan hubungan pengelompokan atribut aroma pada tiap sampel dengan cara
memaksimumkan keragaman menggunakan komponen utama (PC) yang
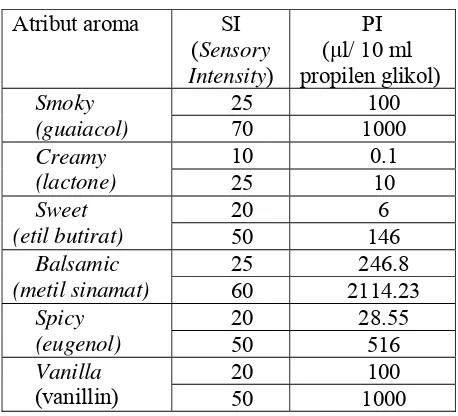
Tabel 3. Standar deskripsi aroma ekstrak panili
Atribut aroma SI
(Sensory Intensity)
PI (μl/ 10 ml propilen glikol)
Smoky (guaiacol)
25 100 70 1000
Creamy (lactone)
10 0.1 25 10
Sweet (etil butirat)
20 6 50 146
Balsamic (metil sinamat)
25 246.8 60 2114.23
Spicy (eugenol)
20 28.55 50 516
Vanilla
(vanillin)
IV. HASIL DAN PEMBAHASAN
A.SIFAT FISIKOKIMIA SAMPEL EKSTRAK PANILI 1. Warna
Sampel ekstrak panili yang digunakan dalam penelitian ini berwarna
kuning keemasan sampai coklat pekat. Berikut ini gambar sampel yang
digunakan dalam penelitian ini:
Gambar 4. Sampel ekstrak panili: (1)Tahiti, (2)Grade II, (3)Virginia, (4)Cobra, (5)S7, (6)Djasulawangi, (7)G11
Warna ekstrak panili tergantung pada beberapa faktor yaitu kualitas
buah panili, durasi (lama waktu) ekstraksi dan adanya gliserin, akan tetapi
kandungan etanol juga penting. Warna ekstrak akan lebih gelap sampai
kandungan etanol 60 persen. Di atas 70 persen warnanya lebih muda dan di
atas 95 persen sangat sedikit warna yang terekstrak (Purseglove et al., 1981;
Reineccius,1994). Apabila kandungan etanol lebih dari 70 persen, maka
sejumlah fixed oil akan ikut terekstrak dan akan mengendap, hal ini tidak
akan terjadi pada ekstrak dengan kandungan etanol 35-40% (Purseglove,
1981), sehingga kandungan etanol mempengaruhi zat yang terekstrak dan
warna ekstrak. Sampel dari eksportir dan importir memiliki warna yang
lebih gelap kecuali Djasulawangi yang diekstrak sendiri oleh peneliti, hal ini
kemungkinan disebabkan karena durasi ekstraksi Djasulawangi yang lebih
singkat (hanya 6 hari) karena pada perusahaan penghasil ekstrak panili,
dilakukan penuaan bisa lebih dari tiga minggu bahkan sampai tiga bulan
(Purseglove et al., 1981), sedangkan sampel S7 dilakukan maserasi selama
16 hari dan G11 selama 22 hari. Faktor-faktor yang lain (kualitas buah,
adanya gliserin dan kandungan etanol) juga mempengaruhi warna ekstrak
panili.
2. Kadar Vanillin
Pengukuran kadar vanillin dilakukan sebagai salah satu indikator
mutu ekstrak panili pada analisis laboratorium, akan tetapi penentuan mutu
ekstrak panili terutama dilakukan secara subyektif melalui penilaian
organoleptik terhadap aroma dan flavor karena adanya
konstituen-konstituen minor yang juga mempengaruhi aroma ekstrak panili alami
(Purseglove et al., 1981).
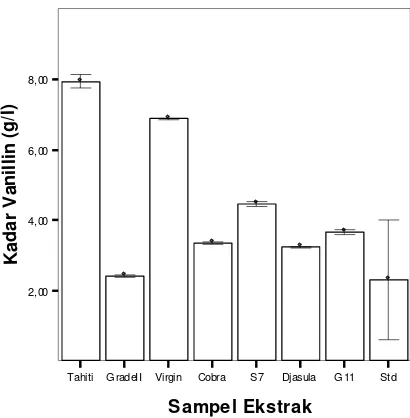
Kadar vanillin tertinggi (Gambar 6 / Lampiran 5) dimiliki oleh ekstrak
panili Tahiti (Grade I) sebesar 7,9 g/l. Ekstrak Virginia memiliki kadar
vanillin sebesar 6,9 g/l, S7 sebesar 4,5 g/l, G11 sebesar 3,8 g/l, Cobra 3,3
g/l, Djasulawangi 3,2 g/l dan yang paling rendah adalah Tahiti grade II
sebesar 2,4 g/l. Berdasarkan hasil analisis varian (ANOVA), diketahui
bahwa jenis sampel memiliki hubungan yang signifikan terhadap kadar
vanillin dengan perbedaan nyata pada setiap sampel kecuali Djasulawangi
dan Cobra.
Kadar vanillin dalam setiap sampel ekstrak panili berbeda, hal ini
disebabkan karena perbedaan agroklimat tempat tumbuhnya (Chalot, 1920).
Sampel Tahiti Grade I dan II berasal dari Tahiti, Virginia berasal dari
Madagascar, S7 dan G11 berasal dari Makassar, sedangkan Djasulawangi
dan Cobra berasal dari dalam negeri, akan tetapi tidak diketahui dari daerah
mana. Antara Tahiti Grade I dan II terdapat perbedaan kadar vanillin yang
cukup besar walaupun berasal dari daerah yang sama, hal ini terkait dengan
grade ekstrak tersebut, di mana Grade I mengandung vanillin lebih tinggi
daripada Grade II. Sampel Cobra dan Djasulawangi tidak berbeda nyata
kadar vanillinnya, sehingga mungkin menggunakan buah panili dari daerah
yang sama, sedangkan untuk sampel S7 dan G11, kemungkinan perbedaan
metode ekstraksi yang menyebabkan kadar vanillinnya berbeda karena
bahan baku buah panili yang digunakan berasal dari daerah yang sama.
ekstraksi, perbandingan air dan buah panili, serta kondisi bahan baku buah
panili segar yang digunakan. Setyaningsih (2006) menyebutkan pula bahwa
kenaikan kadar vanillin selama proses kuring disebabkan terutama oleh
hidrolisis glukovanillin dan akumulasi vanillin dari tahap-tahap sebelumnya.
Sejumlah kecil vanillin mungkin dihasilkan dari eliminasi rantai karbon dari
asam ferulat (Venturi et al, 1998), metoksi 4-hidroksi benzaldehid
(Podstolski et al, 2002 dalam Setyaningsih, 2006), serta hidroksilasi dan
metilasi asam sinamat yang terdapat sebagai prekursor lignin (Funk dan
Brodelius, 1990). Kadar vanillin juga dapat berkurang karena teroksidasi
oleh enzim peroksidase menjadi o-guaiacol atau asam vanillat (Purseglove
et al, 1981).
Tahiti G radeII Virgin Cobra S7 Djasula G 11 Std
Sampe l Ekstrak
2,00 4,00 6,00 8,00
K
a
d
a
r
V
a
n
il
li
n
(
g
/l
)
D D
D
D
D
D D
D
Gambar 5. Kadar vanillin dari ekstrak panili dan standar FDA
Berdasarkan hasil perhitungan uji hipotesis kadar vanillin disimpulkan
bahwa rata-rata kadar vanillin seluruh ekstrak yang dianalisis sama dengan
rata-rata kadar vanillin menurut standar FDA. Oleh karena itu semua sampel
ekstrak panili telah memenuhi kriteria kadar vanillin sesuai dengan standar.
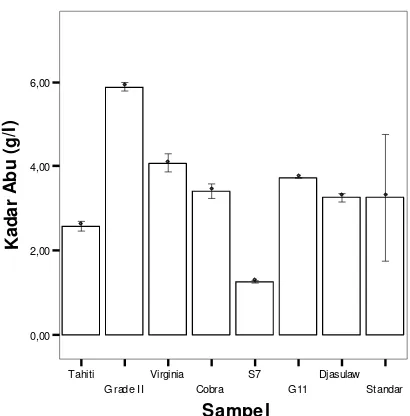
3. Kadar Abu
Kadar abu menunjukkan banyaknya zat anorganik dalam bahan
pangan, yaitu zat yang tidak terbakar saat proses pembakaran (Winarno,
1997). Kadar abu pada ekstrak panili dapat digunakan untuk mengetahui
kemurnian ekstrak panili, di mana ekstrak panili alami akan memiliki kadar
abu yang lebih besar daripada panili imitasi. Menurut standar FDA, kadar
abu ekstrak panili asli sebesar 2.2 – 4.32 g/l. Hasil pengukuran kadar abu
dari sampel ekstrak panili dibandingkan dengan standar FDA dapat dilihat
pada Lampiran 6.
Tahiti G rade II
Virginia Cobra S7 G 11 Djasulaw Standar Sampe l 0,00 2,00 4,00 6,00 K a d a r A b u ( g /l ) D D D D D D D D
Gambar 6. Kadar abu ekstrak panili
Pada Gambar 6, kadar abu tertinggi dimiliki oleh Tahiti Grade II
sebesar 5.85 g/l, nilai ini melebihi batas atas kadar abu dalam persyaratan
FDA. Penyebabnya kemungkinan terdapatnya zat anorganik dalam jumlah
yang cukup besar atau ditambahkannya alkali pada ekstrak tersebut
sehingga kadar abu melebihi standar, sedangkan kadar abu terendah dimiliki
oleh sampel S7 sebesar 1.33 g/l. Hal ini kemungkinan disebabkan karena
kandungan zat anorganiknya lebih rendah, selain itu kemungkinan penyebab
kecilnya kadar abu S7 karena dilakukan dua kali penyaringan setelah
pada filter. Hal ini dapat diketahui pula dari warna ekstrak yang lebih muda
dari sampel hasil penelitian, G11.
Dari hasil analisis varian (ANOVA), jenis sampel berpengaruh nyata
terhadap kadar abu dan masing-masing jenis sampel ekstrak panili, kecuali
Cobra dan G11. Hal ini terjadi kemungkinan karena perbedaan kandungan
mineral di dalam tiap sampel ekstrak panili. Kandungan mineral dalam buah
panili diantaranya kalium, kalsium, klor, nitrogen dan magnesium. Panili
sintetis mengandung bahan-bahan seperti vanillin, coumarin dan gula
substitusi, gliserin dan pelarut lainnya yang secara praktis bebas dari abu
(Reineccius, 1994). Oleh karena itu, pengukuran kadar abu perlu dilakukan
untuk mengetahui adanya pemalsuan atau tidak, karena industri ekstrak
panili dapat meningkatkan kadar abu dengan menggunakan alkali, tetapi
akan mengubah nilai kelarutan dan alkalinitasnya (Reineccius, 1994).
Berdasarkan hasil perhitungan uji hipotesis kadar abu total
disimpulkan bahwa rata-rata kadar abu seluruh ekstrak yang dianalisis sama
dengan rata-rata kadar abu menurut standar FDA sehingga ketujuh sampel
tersebut dapat diterima.
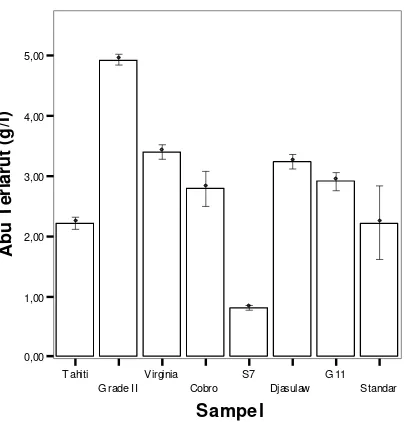
4. Abu Terlarut
Abu terlarut diperoleh dari hasil pelarutan abu total dengan air panas
yang kemudian melalui penyaringan. Menurut Reineccius (1994), lebih dari
80 persen dari total abu, terlarut dalam air.
Pada Gambar 7, nilai abu terlarut paling tinggi adalah pada ekstrak
panili Tahiti Grade II yaitu 4.93 g/l atau 83.8 % dari abu total dan yang
paling rendah adalah ekstrak panili S7 sebesar 0.80 g/l atau 64% dari abu
total. Data selengkapnya dapat dilihat pada lampiran 7. Menurut Reineccius
(1994), kadar abu berguna untuk mengetahui keaslian vanilla karena pada
vanilla imitasi yang hanya mengandung vanillin, coumarin, gula substitusi,
gliserin dan pelarut, praktis bebas dari abu. Namun, ada yang menambahkan
alkali pada pembuatan ekstrak panili sehingga meningkatkan total abu,
Tahiti G rade II
[image:31.612.211.413.103.314.2]Virginia Cobro S7 Djasulaw G 11 Standar Sampe l 0,00 1,00 2,00 3,00 4,00 5,00 A b u T e rl a ru t (g /l ) D D D D D D D D
Gambar 7. Abu terlarut antara standar dan sampel ekstrak panili
Alkali yang ditambahkan pada vanilla imitasi akan ikut terlarut dalam
analisis abu terlarut sehingga akan mempengaruhi nilai alkalinitasnya saat
uji alkalinitas abu terlarut. Hasil analisis varians menunjukkan bahwa Tahiti
Grade II berbeda nyata dari sampel yang lain. Akan tetapi Virginia, Djasula,
G11 dan Cobra memberikan nilai yang tidak berbeda nyata.
Berdasarkan hasil perhitungan uji hipotesis kadar abu terlarut
disimpulkan bahwa rata-rata kadar abu terlarut seluruh ekstrak yang
dianalisis sama dengan rata-rata kadar abu terlarut menurut standar FDA,
sehingga semua ekstrak secara keseluruhan dapat diterima mutunya sampai
pada uji abu terlarut.
5. Lead Number
Prinsip analisis lead number yaitu asam organik dari panili
diendapkan dengan Pb(CH3COO)2 netral dalam keadaan standar, garam
timbal yang tidak larut dipindahkan dan kelebihan timbal ditentukan dengan
titrasi khelometri dengan Na2EDTA. Menurut Harjadi (1993), EDTA
Bentuk sederhananya H4Y. Sebagai asam lemah, EDTA mengalami
pengionan bertahap melepaskan ion hidrogen satu persatu. EDTA mampu
membentuk kompleks dengan ion logam dan memiliki konstanta kestabilan
yang besar sehingga reaksi berjalan sempurna. Pembentukan kelat logam
dengan EDTA dapat ditulis secara umum sebagai berikut:
Mn+ + Y4-↔ MY n-4
Keterangan: M = ion logam
Y = EDTA
Pada kesetimbangan EDTA ion logam, pembentukan dari kompleks
dipengaruhi oleh pH, maka biasanya pada penitaran EDTA selalu dipakai
larutan buffer sehingga didapatkan pH yang tetap (Sumarna et al, 2000).
Lead number digunakan untuk mengetahui asam organik yang terdapat dalam ekstrak panili (AOAC, 1995). Menurut Melawati (2006),
ekstrak panili alami mengandung senyawa organik yang terbentuk dari
oksidasi senyawa vanillin selama proses kuring dan dari hasil proses
oksidasi alkohol selama proses conditioning. Kandungan asam organik yang
rendah mengindikasikan adanya pencampuran.
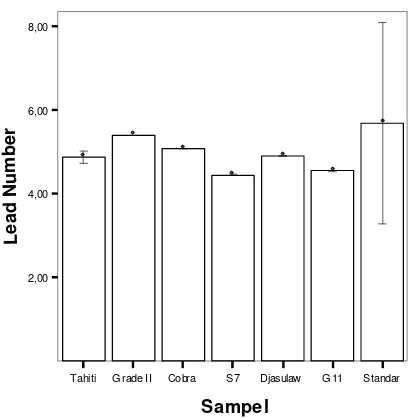
Nilai lead number (Winton) standar adalah 4.0-7.4 atau rata-rata 5.4,
sedangkan nilai lead number yang diperoleh dari pengukuran sampel
ekstrak panili dapat dilihat pada Lampiran 9. Lead number tertinggi
(Gambar 8) dimiliki oleh sampel Tahiti Grade II yaitu sebesar 5.4 sama
dengan rata-rata lead number standar. Hal ini mengindikasikan lebih banyak
terdapat asam organik di dalamnya dibandingkan dengan lainnya.
Sedangkan nilai lead number yang paling rendah dimiliki oleh S7 yang
menandakan asam organik yang dimilikinya lebih sedikit. Tahiti Grade II
memiliki lead number yang berbeda nyata dari semua jenis sampel, begitu
pula dengan Cobra. Tahiti I tidak berbeda nyata terhadap Djasulawangi,
sedangkan S7 tidak berbeda nyata dengan G11. S7 dan G11 memiliki nilai
lead number yang terendah kemungkinan disebabkan belum sempurnanya proses pembentukan asam-asam organik pada buah panili yang digunakan
Sampel Virginia tidak diuji nilai lead numbernya karena sampelnya terbatas.
Tahiti G rade II Cobra S7 Djasulaw G 11 Standar
Sampe l
2,00 4,00 6,00 8,00
L
e
a
d
N
u
m
b
e
r
D
D D D
D
D
[image:33.612.208.413.141.350.2]D
Gambar 8. Lead number antar standar dan sampel
Berdasarkan hasil perhitungan uji hipotesis lead number disimpulkan
bahwa rata-rata lead number seluruh ekstrak yang dianalisis tidak sama
dengan rata-rata lead number ekstrak menurut standar FDA. Hal ini
menunjukkan kemungkinan sedikitnya asam organik yang terkandung
dalam ekstrak sampel.
6. Alkalinitas Abu terlarut
Alkalinitas abu terlarut diukur dari filtrat hasil penyaringan larutan
abu dengan air panas. Alkalinitas menunjukkan adanya unsur logam yang
dapat membentuk basa seperti natrium, kalium, kalsium dan magnesium.
Unsur-unsur ini berasal dari unsur mineral yang ada di dalam buah panili
(Purseglove et al.,1981).
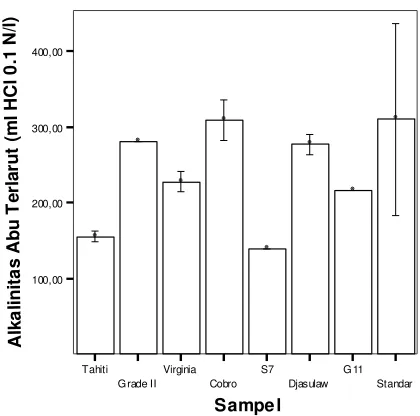
Nilai alkalinitas abu terlarut dinyatakan dalam ml 0.1N HCl/l. Nilai
alkalinitas abu terlarut digunakan untuk mengetahui kandungan alkali yang
ada pada ekstrak. Hal ini dapat pula digunakan untuk mengetahui adanya
terlarut berdasarkan FDA untuk ekstrak panili adalah 220-400 ml 0.1 N
HCl/l, sedangkan nilai alkalinitas abu terlarut yang diperoleh dari ketujuh
sampel (Gambar 9) berkisar 139-309 ml 0.1 N HCl/l. Ekstrak panili Tahiti
Grade I dan S7 tidak masuk dalam range FDA. Hal ini disebabkan kecilnya
kadar abu yang berasal dari kandungan zat anorganik dalam ekstrak panili.
Berdasarkan hasil perhitungan uji hipotesis alkalinitas abu terlarut
disimpulkan bahwa rata-rata alkalinitas abu terlarut seluruh ekstrak yang
dianalisis tidak sama dengan rata-rata alkalinitas abu terlarut ekstrak
menurut standar FDA.
Tahiti G rade II
[image:34.612.204.414.278.486.2]Virginia Cobro S7 Djasulaw G 11 Standar Sampe l 100,00 200,00 300,00 400,00 A lk a li n it a s A b u T e rl a ru t (m l H C l 0 .1 N /l ) D D D D D D D D
Gambar 9. Alkalinitas abu terlarut pada standar dan sampel.
7. Alkalinitas Abu Total
Alkalinitas abu total diperoleh dari alkalinitas abu terlarut dan tidak
terlarut. Alkalinitas abu total menurut FDA adalah 300-540 ml 0.1 N HCl/l.
Hasil pengukuran alkalinitas abu total terhadap sampel dapat diamati pada
lampiran 8.
Nilai alkalinitas abu total (Gambar 10) Tahiti Grade II dan Virginia
berbeda nyata dari sampel-sampel lainnya yaitu sebesar 721.3 dan 722.8 ml
0.1 N HCl/l. Alkalinitas abu total menjadi salah satu indikator untuk
panili yang memiliki kadar abu rendah, dapat ditambahkan alkali untuk
meningkatkan kadar abu, sehingga akan mengubah nilai kelarutan dan
alkalinitasnya. Pada ekstrak yang ditambahkan alkali, maka kadar abunya
akan tinggi, sedangkan abu terlarutnya menunjukkan banyaknya zat-zat
anorganik termasuk alkali yang larut dalam air. Alkalinitas abu total
merupakan hasil yang diperoleh dari alkalinitas abu terlarut dan alkalinitas
abu tidak terlarut sehingga dapat diketahui berapa banyak dari abu total
yang merupakan alkali.
Tahiti G rade II
Virginia Cobro S7 Djasulaw G 11 Standar Sampe l 0,00 250,00 500,00 750,00 A lk a li n it a s A b u T o ta l (m l H C l 0 .1 N /l ) D D D D D D D D
Gambar 10. Alkalinitas abu total antar standar dan sampel
Berdasarkan hasil perhitungan uji hipotesis alkalinitas abu total
disimpulkan bahwa rata-rata alkalinitas abu total seluruh ekstrak yang
dianalisis tidak sama dengan rata-rata alkalinitas abu total ekstrak menurut
standar FDA, sehingga ekstrak sampel tidak memenuhi syarat fisikokimia
dari FDA untuk alkalinitas abu total.
8. Total Asam
Keasaman air dapat disebabkan oleh adanya CO2 yang tidak terikat,
asam-asam mineral, dan garam-garam dari asam kuat dan basa lemah.
total, dan dalam hal ini termasuk asam-asam lemah, garam-garam asam dan
beberapa keasaman yang disebabkan karena hidrolisa (Jenie dan Fardiaz,
1989).
Keasaman mengindikasikan adanya asam-asam organik terlarut dalam
buah panili termasuk adanya vanillin alami (Reineccius, 1994). Total asam
yang rendah mengindikasikan adanya pencampuran. Nilai ini juga
digunakan untuk mengetahui ada atau tidaknya gula atau gliserin dalam
menstruum. Selain itu, kandungan alkohol yang lebih rendah dalam
menstruum akan meningkatkan kadar abu dan mengurangi keasaman. Nilai total asam dapat dilihat pada Gambar 11.
Total asam berdasarkan FDA adalah 300-520 ml 0.1 NaOH/l,
sedangkan pada sampel diperoleh total asam dalam kisaran 100 – 250 ml 0.1
NaOH/l. Hal ini mengindikasikan kemungkinan adanya pencampuran gula
dan gliserin ke dalam ekstrak atau sedikitnya asam-asam organik yang
terlarut dari buah ke dalam ekstrak tersebut. Asam-asam organik sebagian
besar terbentuk saat proses curing (Herman et al., 1990).
Berdasarkan hasil perhitungan uji hipotesis total asam disimpulkan
bahwa rata-rata total asam seluruh ekstrak yang dianalisis tidak sama
dengan rata-rata total asam ekstrak menurut standar FDA, sehingga tidak
memenuhi karakteristik ekstrak panili menurut FDA.
Tahiti G rade II
[image:36.612.217.405.491.677.2]Virginia Cobra S7 Djasulaw G 11 Standar Sampe l 0,00 100,00 200,00 300,00 400,00 500,00 T o ta l A s a m ( m l 0 ,1 N N a O H /L ) D D D D D D D D
B.DISKUSI KARAKTERISTIK FISIKOKIMIA
Berdasarkan analisis PCA (Gambar 12), diperoleh kesimpulan bahwa
sampel Virginia dan Tahiti grade II mempunyai karakteristik yang sama karena
berada pada kuadran yang sama, yaitu karakteristik alkalinitas abu total, abu
terlarut dan abu total. Kedua sampel ini juga memiliki karakter yang hampir
sama dengan G11, tapi dapat dibedakan dari kadar vanilinnya. Abu total dan
abu terlarut memiliki hubungan yang sangat dekat, begitu pula dengan
alkalinitas abu total. Hal ini sesuai dengan pernyataan Reineccius (1994) yang
menyebutkan apabila dilakukan penambahan alkali dalam pembuatan ekstrak
panili, maka akan berubah pula nilai kelarutan dan alkalinitasnya. Sampel
Cobra dan Djasulawangi terlihat lebih dekat kepada karakteristik Standar.
Hubungan antara total asam dan alkalinitas abu terlarut sangat erat (positif)
pada sampel djasulawangi dan menjadi pembeda dari sampel ekstrak yang lain.
Sedangkan sampel Tahiti grade I dikenali karakteristiknya dari kadar
vanilinnya. Sampel terakhir adalah S7 yang tidak memiliki karakteristik yang
khas dengan karakteristik yang ada.
PC1 P C 2 3 2 1 0 -1 -2 -3 -4 2 1 0 -1 -2 0 0 TotalAsam Alk AbuTerlar ut
Alk AbuTotal AbuTerlarut AbuTotal Vanillin Standar G11 Djasulaw angi S7
Cobro Pure Vanilla Extract
Virginia Dare
Grade I I Tahiti
[image:37.612.157.482.410.627.2]Scatterplot of PC2 vs PC1
Gambar 12. Biplot sifat fisikokimia dengan sampel ekstrak panili
Berdasarkan hasil analisis tersebut, dapat disimpulkan bahwa sampel
abu terlarut dan alkalinitas abu total yang cukup dekat dengan sampel Tahiti
grade I, tahiti Grade II dan Virginia yang termasuk sampel dari importir.
Sedangkan sampel Cobra dan Djasulawangi (dari eksportir) memiliki
karakteristik yang mengarah pada Standar walaupun tidak cukup dekat, tapi
dapat dibedakan dari sampel yang lain melalui karakteristik total asam dan
alkalinitas abu terlarut. Sedangkan sampel S7 (hasil penelitian) tidak mendekati
karakteristik ekstrak manapun.
Berdasarkan hasil analisis sifat fisikokimia, diperoleh hasil bahwa sampel
G11, Cobra dan Djasulawangi memenuhi nilai standar FDA pada kadar abu,
abu terlarut, alkalinitas abu terlarut, alkalinitas abu total, lead number dan
kadar vanilin. Hal ini menunjukkan ketiga ekstrak panili tersebut asli atau
sesuai dengan mutu yang ditetapkan FDA dan G11 memiliki karakter
fisikokimia yang mirip dengan sampel ekstrak panili eksportir.
C. ANALISIS SENSORI a. Deskripsi Kualitatif
Bagian pertama dari tahap pengujian deskripsi kuantitatif adalah
in-depth interview. Pengujian ini dilakukan oleh 12 orang panelis. Masing-masing panelis mendeskripsikan atribut-atribut yang terdapat pada sampel
ekstrak panili dengan cara membaui sampel ekstrak panili langsung dari
botol. Tiap panelis mendeskripsikan sesuai dengan aroma yang dapat
dideteksi masing-masing. Panel leader (peneliti) dapat membantu
menjelaskan apabila panelis sulit untuk mendeskripsikan. Atribut aroma
yang dideskripsikan oleh tiap panelis berbeda-beda satu sama lain. Hasil
deskripsi kualitatif in-depth interview dapat dilihat pada lampiran 11.
Bagian kedua dalam tahap ini yaitu analisis deskripsi dengan Focus Group.
Panelis mendiskusikan atribut-atribut yang mereka peroleh saat in-depth
interview (Lampiran 11) bersama panelis yang lain dan panel leader. Diskusi ini dilakukan untuk menyamakan persepsi dan menemukan
kesepakatan tentang atribut aroma yang dapat dideteksi oleh seluruh panelis.
Dari kesimpulan focus group, sampel ekstrak Tahiti grade I dan II
memiliki atribut aroma dominan yang berbeda, Tahiti I dengan aroma sweet
dan smokey, sedangkan Tahiti Grade II dikenali dengan atribut aroma spicy dan creamy. Atribut sweet terdeteksi pada sampel Cobra, Djasulawangi,
Tahiti grade I dan Virginia. Balsamic dapat dideteksi pada sampel ekstrak
Djasulawangi dan S7. Smoky dikenali pada Tahiti grade I, dan Virginia.
Creamy terdapat pada sampel Cobra, Tahiti Grade II, S7 dan G11. Sedangkan atribut aroma vanilla hanya dapat dideteksi pada sampel
[image:39.612.164.477.273.385.2]Djasulawangi.
Tabel 4. Hasil Uji Deskripsi dengan metode Focus Group
Jenis Ekstrak Atribut Aroma
Tahiti Grade I Sweet, smoky
Tahiti Grade II Spicy, creamy
Virginia Dare Sweet, smoky
Cobra Pure Vanilla Extract Creamy, sweet
S7 Balsamic, spicy, creamy
Djasulawangi Balsamic, sweet, vanilla
G11 Smokey, spicy, creamy
Perbedaan aroma yang terdeteksi dari setiap sampel ekstrak panili
terjadi karena ekstrak panili memiliki karakter kimiawi yang bervariasi.
Berikut ini kunci karakter rasa ekstrak panili:
- Madagascar Bourbon – creamy, brown, haylike, sweet, vanillin.
- Mexican – creamy, woody, spicy, sweet, vanillin.
- Tahitian – aromatic, fruity, sweet, cherry, anisic
- Indonesian whole – woody, strawy
- Indonesian cuts – woody, phenolic, smoky, bitter
- Bourbon-Indonesian blend – creamy, woody, phenolic.
(http://www.cookswares.com/discussions/vanilla2.asp, 2004)
Menurut Heath (1978), dalam ekstrak panili, terdapat senyawa selain
vanillin (4-hydroxy-3-methoxybenzaldehyde) yang juga berperan dalam
pembentukan profil aroma yaitu vanillic acid (4-hydroxy-3-methoxy
benzoic acid), p-hydroxy benzoic acid, p-coumaric acid. Sedangkan Gernot
Katzer (2003) dalam www.uni-graz.at menyatakan komponen aroma yang
-hydroxybenzyl methyl ether (1%). Selain itu ada 130 lebih senyawa yang
diidentifikasi dalam ekstrak panili (phenoles, phenol ether, alcohols,
carbonyl compounds, acids, ester, lactones, aliphatic and aromatic carbohydrates dan heterocyclic compounds). Dua stereoisomeric vitispiranes (2,10,10-trimethyl-1,6-dan methylidene-1-oxaspiro
(4,5)dec-7-ene) juga berpengaruh terhadap aroma.
b. Deskripsi Kuantitatif
Bagian terakhir dalam tahap pengujian yaitu uji deskripsi kuantitatif
dengan QDA. Panelis diminta memperkirakan intensitas aroma sesuai
dengan atribut aroma hasil focus group yang dapat dideteksi dari setiap jenis
ekstrak panili. Tiap panelis diberikan tujuh sampel ekstrak panili yang akan
diuji dan enam atribut flavor standar yang akan digunakan sebagai standar
penentuan intensitas atribut aroma pada sampel ekstrak panili. Contoh form
isian QDA dapat dilihat pada lampiran 18. Panelis membuka tutup botol
standar flavor lalu mencelupkan smelling strip ke dalamnya dan
mengibas-ngibaskannya sambil dicium aromanya dan diingat intensitasnya sesuai
dengan yang tertera pada label. Kemudian panelis mengidentifikasi aroma
ekstrak panili dengan menggunakan smelling strip lalu intensitasnya
dibandingkan dengan intensitas flavor standar. Hasil yang diperoleh
ditampilkan dalam spiderweb (Gambar 13) dan dianalisis dengan PCA
(Principal Component Analysis).
Gambar13. Spiderweb semua sampel ekstrak panili
0 20 40 60 Balsamic
Sw eet
Creamy
Spicy Smokey
vanilla
S7 VIRGINIA GRADE II
DJASULAWANGI TAHITI G11
Gambar14. Spider web ekstrak panili dari eksportir
Sampel ekstrak panili dari eksportir (Gambar 14) terdiri dari sampel
Cobra dan Djasulawangi. Sampel Cobra dicirikan oleh atribut vanilla,
creamy dan sweet karena memiliki nilai atribut aroma yang lebih besar dibandingkan sampel Djasulawangi, sedangkan sampel Djasulawangi
dicirikan oleh atribut aroma balsamic karena nilai atribut aromanya lebih
besar.
Gambar 15. Spider web atribut ekstrak panili dari importir
Sampel dari Eksportir
0 5 10 15 20 25 30 35 Balsamic
Sw eet
Creamy
Spicy Smokey
vanilla
COBRA DJASULAWANGI
Sampel dari importir
0 10 20 30 40 50 60 Balsamic
Sw eet
Creamy
Spicy Smokey
vanilla
[image:41.612.207.455.452.659.2]Pada Gambar 15 diperlihatkan sebuah pola yang hampir sama pada
sampel Virginia dan Tahiti Grade I dan pola yang berbeda bila keduanya
dibandingkan dengan Tahiti Grade II. Aroma vanilla dan sweet pada
Virginia dan Tahiti Grade I lebih dapat dideteksi daripada Tahiti grade II.
Sedangkan Tahiti grade II, aroma spicy lebih besar dibanding kedua sampel
lainnya. Ekstrak panili Tahiti memiliki fragrance yang sedikit berbeda dari
ekstrak panili yang lain karena mengandung piperonal (heliotropin,
3,4-dioxymethylenbenzaldehyde) dan diacetyl (butandione). Piperonal
memberikan atribut aroma sweet, strongly floral, bitter-sweet taste (Heath,
1978).
Spider web atribut aroma ekstrak panili hasil penelitian (Gambar 16) memperlihatkan pola yang sama pada S7 dan G11 pada hampir semua
atribut. Apabila dibandingkan dengan sampel dari importir, maka
kekurangan dari kedua ekstrak ini adalah pada aroma sweet dan creamy.
Untuk aroma vanilla sendiri sudah mendekati sampel dari importir. Adapun
sampel Cobra (dari eksportir) memiliki aroma sweet, vanilla dan creamy
seperti halnya sampel dari importir. Aroma ekstrak panili Indonesia
tergantung pada bagaimana proses kuring dan pengeringan yang dilalui,
karena pemanenan buah panili yang terlalu cepat dan proses kuring yang
singkat akan memberikan aroma woody dan phenolic, padahal seharusnya
aromanya mirip dengan ekstrak panili Bourbon
[image:42.612.164.512.282.680.2](www.vanilla.com/html/facts-extracts.html).
Gambar 16. Spider web atribut aroma ekstrak panili hasil penelitian
Sampel hasil penelitian
0 10 20 30 40 50 Balsamic
Sw eet
Creamy
Spicy Smokey
vanilla
c. Principal Component Analysis (PCA)
Untuk mengetahui atribut aroma yang berhubungan erat dengan jenis
sampel ekstrak panili digunakan PCA (Principal Component Analysis)
menggunakan software Minitab 14. Analisis menggunakan PCA
menghasilkan empat buah grafik yaitu scree plot, score plot, loading plot
dan scatter plot (biplot). Dalam analisis komponen utama, Minitab lebih
dahulu mencari susunan eigenvector ortogonal dari korelasi atau keragaman
matriks variabel-variabel. Matriks komponen utama (PC) adalah produk dari
matriks eigenvector dengan matriks variabel independen. PC1 menghitung
persentase terbesar dari total variasi data. PC2 menghitung persentase
terbesar kedua dari total variasi data. Tujuan dari PC adalah untuk
menjelaskan jumlah maksimum variasi dengan jumlah komponen tersedikit
(Minitab Inc., 2003).
Scree plot (Gambar 17) pada data ini menampilkan enam buah PC. Penentuan jumlah PC yang digunakan berdasarkan nilai eigenvalue yang
menerangkan keragaman komponen utama (PC). Eigenvalue yang diperoleh
PC1 sebesar 2,5017 yang dapat menjelaskan keragaman sebesar 41,7 % .
PC2 dengan nilai eigenvalue 1,7761 dapat menjelaskan keragaman sebesar
29,6 %. Dalam hal ini digunakan dua PC karena sesuai dengan pendapat
Everitt dan Dunn (1998) yang menyatakan bahwa jumlah Principal
Component (PC) yang digunakan harus mampu menerangkan minimal 70% total keragaman data. Jadi, total keragaman yang dapat dijelaskan oleh
analisis komponen utama ini sebesar 71,3 % (Lampiran 12).
Score plot (Gambar 18) menggambarkan grafik antara PC2 dan PC1 yang menerangkan hubungan antar sampel, di mana sampel yang
berdekatan mempunyai deskripsi yang sama, sedangkan sampel yang berada
pada lokasi berlawanan mempunyai deskripsi yang berbeda.
Loading plot (Gambar 19) menjelaskan hubungan antara variabel atribut aroma ekstrak panili. Untuk mengetahui hubungan antara sampel
ekstrak panili dan atribut aroma, maka digunakan scatterplot atau grafik
pengamatan dengan peubah dan nilai peubah pada suatu objek
(Sumertajaya, 2002).
Component Number
E ig e n v a lu e 6 5 4 3 2 1 2,5 2,0 1,5 1,0 0,5 0,0
[image:44.612.160.481.101.329.2]Scree Plot of Balsamic; ...; vanilla
Gambar 17. Scree plot komponen utama ekstrak panili
First Component
S e c o n d C o m p o n e n t 3 2 1 0 -1 -2 -3 2 1 0 -1 -2 COBRA G11 TAHI TI DJASULAW ANGI
GRADE I I
VI RGI NI A S7
Score Plot of Balsamic; ...; vanilla
Gambar 18. Score plot principal component 1 dan principal component 2
[image:44.612.155.486.368.585.2]First Component S e c o n d C o m p o n e n t 0,50 0,25 0,00 -0,25 -0,50 0,50 0,25 0,00 -0,25 -0,50 v anilla Smok ey Spicy Creamy Sw eet
Balsamic
Loading Plot of Balsamic; ...; vanilla
Gambar 19. Loading plot atribut aroma
Dari biplot (Gambar 20) dapat diinterpretasikan bahwa atribut creamy, sweet dan vanilla memiliki hubungan yang dekat dan berkorelasi positif.
Menurut Perez –Silva et al. (2006), sweet, woody, balsamic, spicy,
vanilla-like adalah atribut dari senyawa fenolik. Smoky memiliki korelasi positif
terhadap spicy, sedangkan balsamic memiliki korelasi negatif terhadap
atribut aroma lainnya. Sampel ekstrak panili yang posisinya berdekatan
berarti memiliki karakteristik yang sama. Hasil PCA menunjukkan bahwa
dalam kuadran yang sama, tidak ada sampel yang saling berdekatan kecuali
G11, Cobra dan S7 yang berdekatan akan tetapi masing-masing berada
pada kuadran yang berbeda. Hal ini dapat diinterpretasikan bahwa sampel
S7, G11 dan Cobra memiliki kesan yang cukup dekat, akan tetapi masih
dapat dibedakan dengan karakteristik khas masing-masing sampel, yaitu
Cobra dapat dibedakan dengan aroma creamy, sweet dan vanilla yang
dominan, S7 dengan aroma balsamic-nya dan G11 dapat dibedakan dengan
karakternya sendiri. Grade II dan Virginia walaupun tidak cukup dekat
tetapi berada dalam kuadran yang sama (kuadran II) sehingga dapat
dikelompokkan dengan karakteristik yang sama, yaitu smoky dan spicy.
Tahiti dan G11 berada dalam kuadran yang sama (kuadran IV) membentuk
[image:45.612.157.482.79.293.2]S7 berada dalam kuadran ketiga memiliki kecenderungan pada aroma
balsamic. Sedangkan Cobra berada pada kuadran I memiliki karakteristik
creamy, sweet dan vanilla.
PC1 P C 2 3 2 1 0 -1 -2 -3 2 1 0 -1 -2 0 0 v anilla Smok ey Spicy Creamy Sw eet
Balsamic COBRA
G11 TAHI TI
DJASULAW ANGI
GRADE I I
VI RGI NI A S7
Scatterplot of PC2 vs PC1
Gambar 20. Biplot PC2 vs PC1
Dari ketujuh sampel ekstrak panili tersebut, hanya sampel dari
importir yaitu Tahiti Grade II dan Virginia yang memiliki keragaman
karakteristik menonjol yang sama yaitu spicy dan smoky.
Perbedaan atribut aroma yang dominan pada tiap sampel diduga selain
karena perbedaan agroklimat tempat tumbuhnya tanaman panili dan
senyawa-senyawa volatil yang terbentuk saat proses kuring, tetapi juga
karena adanya bahan-bahan yang ditambahkan pada ekstrak panili.
Penambahan bahan-bahan ke dalam ekstrak panili yang diperbolehkan oleh
FDA adalah gliserin, propilen glikol, gula (termasuk gula invert), dekstrosa,
corn sirup (termasuk dried corn sirup).
Berdasarkan hasil uji deskripsi kuantitatif (QDA) diperoleh
[image:46.612.150.489.158.386.2]kecenderungan aroma masing-masing sampel yang dapat dijelaskan pada
<